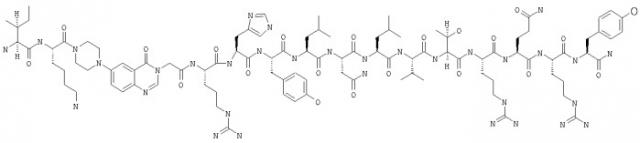
Пептиды, обладающие агонистической активностью в отношении рецептора нейропептида-2-(y2r)
Иллюстрации
Показать всеИзобретение относится к агонистам рецептора нейропептида-2 формулы (I):
а также к их фармацевтически приемлемым солям, производным и фрагментам, в которых заместители имеют значения, указанные в описании. Эти соединения и содержащие их фармацевтические композиции могут быть предназначены для лечения заболеваний, которые модулируются агонистами нейропептида-2, прежде всего ожирения. 4 н. и 9 з.п. ф-лы, 10 ил., 1 табл.
Реферат
Настоящее изобретение относится к укороченным аналогам PYY3-36 формулы (I)
,
в которой Х выбран из группы, включающей N-пиперазин-1-ил-4(3Н)-хинозолинон-3-уксусную кислоту (Pqa), N-(5-O-карбоксиметил)серотонин (Cms), 4-(2-аминометил)-6-дибензофуранпропановую кислоту, 4-(1-пиперидин-4-ил)бутановую кислоту и 4-(2-аминоэтил)-1-карбоксиметилпиперазин, Y обозначает Н, замещенный или незамещенный алкил, замещенный или незамещенный (низш.)алкил, замещенный или незамещенный арил, замещенную или незамещенную алкоксигруппу или поли(этилен)гликольную группу, R1 обозначает Ile, Ala, (D)Ile, N-метилIle, Aib, 1-1 Aic, 2-2 Aic, Ach или Аср, R2 обозначает Lys, Ala, (D)Lys, NMelys, Nie или (Lys-Gly), R3 обозначает Arg, Ala, (D)Arg, N-метилArg, Phe, 3,4,5-трифторРhе или 2,3,4,5,6-пентафторРhе, R4 обозначает His, Ala, (D)His, N-метилHis, 4-МеОАрс, 3-Pal или 4-Pal, R5 обозначает Tyr, Ala, (D)Tyr, N-метилTyr, Trp, Tic, Bip, Dip, (1)Nal, (2)Nal, 3,4,5-трифторPhe или 2,3,4,5,6-петафторPhe, R6 обозначает Leu, Ala, (D)Leu или N-метилLeu, R7 обозначает Asn, Ala или (D)Asn, R8 обозначает Leu, Ala, (D)Leu или N-метилLeu, R9 обозначает Val, Ala, (D)Val или N-метилVal, R10 обозначает Thr, Ala или N-метилТhr, R11 обозначает Arg, (D)Arg или N-метилArg, R12 обозначает Gln или Ala, R13 обозначает Arg, (D)Arg или N-метилArg и R14 обозначает Tyr, (D)Tyr или N-метилTyr, или их фармацевтически приемлемым солям.
Аналоги являются агонистами рецептора нейропептида-2 и их можно применять для лечения метаболических нарушений, таких, например, как ожирение. Все процитированные в настоящем описании документы специально включены в него в качестве ссылки.
Общепризнанно, что ожирение представляет собой серьезную проблему для здоровья в развитых странах, и оно достигло эпидемического статуса в Соединенных Штатах Америки. Согласно современным исследованиям более 50% населения США имеет избыточный вес, при этом более чем у 25% диагностировано клиническое ожирение и наличие значительного риска развития сердечного заболевания, инсулин-независимого сахарного диабета (ИНСД), гипертензии и определенных типов рака. Этот эпидемический статус в настоящее время является серьезной проблемой для системы медико-санитарной помощи, поскольку по прогнозам ежегодная стоимость лечения ожирения только в США может составлять более 70 миллиардов долларов. Стратегии лечения ожирения включают снижение потребления пищи и повышение расхода энергии индивидуумом.
Нейропептид Y (NPY), который представляет собой состоящий из 36 аминокислот пептидный нейромедиатор, является представителем панкреатических пептидов из класса нейромедиаторов/нейрогормонов, который к настоящему времени обнаружен как в периферической, так и в центральной нервной системе. NPY является одним из наиболее эффективных среди известных возбуждающих аппетит агентов, и установлено, что он играет основную роль в регуляции потребления пищи у животных, включая человека.
Было клонировано 5 рецепторов нейропептида Y (NPY), подразделяемых на подтипы Y1, Y2, Y3, Y4 и Y5 и Y6, которые принадлежат к родопсинподобным, сшитым с G-протеином, 7-трансмембранным спиралевидным рецепторам (GPCR). Рецептор NPY Y2 (Y2R) представляет собой состоящий из 381 аминокислоты белок, который ингибирует активацию аденилциклазы посредством Gi, причем он обладает низким уровнем гомологии с другими известными NPY-рецепторами. Обнаружен высокий уровень консервативности между крысиным и человеческим Y2-рецептором, характеризующийся 98%-ной идентичностью аминокислотных последовательностей.
Рецептор Y2R широко распространен в центральной нервной системе грызунов и людей. В гипоталамусе мРНК Y2 локализована в дугообразном ядре, предоптическом ядре и дорсомедиальном ядре. В головном мозге человека Y2R является доминирующим подтипом Y-рецептора. В дугообразном ядре в более чем 80% NPY-нейронов происходит совместная экспрессия мРНК Y2R. Было установлено, что применение избирательного агониста Y2 снижает высвобождение NPY из срезов гипоталамуса in vitro, в то время как не относящийся к пептидам антагонист Y2 BIIE0246 повышает высвобождение NPY. Эти данные подтверждают роль Y2R в качестве пресинаптического ауторецептора, который регулирует высвобождение NPY и поэтому может участвовать в регуляции питания (Poter Е.K. и др., Eur. J. Pharmac. 267, 1994, cc.253-262).
Пептид YY3-36 (PYY3-36) представляет собой состоящий из 33 аминокислот линейный пептид, который обладает специфической агонистической активностью в отношении рецептора нейропептида Y2 (NPY2R). Было продемонстрировано, что внутричерепная инъекция в дугу (IC) или внутрибрюшинная инъекция (IP) PYY3-36 снижала потребление корма крысами и при длительном воздействии снижала прибавление веса тела. Внутривенная инфузия (IV) PYY3-36 (0,8 пмоля/кг/мин) в течение 90 мин снижала на 33% потребление пищи у страдающих ожирением и здоровых людей в течение 24 ч. Эти данные позволяют предположить, что система PYY может являться мишенью для терапевтического воздействия при лечении ожирения (Bloom S. и др., Nature, т.418, 8 августа 2002 г., cc.650-654). Кроме того, установлено, что циклизованная версия PYY Cys2-(D)Cys27, в которой остатки 5-24 заменены на метиленовую цепь длиной 5-8 атомов углерода, активирует расположенный в кишечнике PYY-рецептор, о чем свидетельствует пониженный ток через слизистую мембрану тощей кишки крыс в препаратах с фиксацией напряжения (Krstenansky и др., в Peptides, Proceedings of the Twelfth American Peptide Symposium, под ред. J.Smith и J.Rivier, ESCOM. Leiden, cc.136-137).
Кроме того, продемонстрирована ковалентная модификация белков с помощью поли(этиленгликоля) или поли(этиленоксида) (оба обозначены как ПЭГ), таких как супероксиддисмутаза (Somack R. и др., Free Rad Res Commun 12-13, 1991, cc.553-562; US 5283317 и 5468478), и других типов белков, например, цитокинов (Saifer M.G.P. и др., Polym Preprints 38, 1997, cc.576-577; Sherman M.R. и др. в Poly(ethyleneglycol) Chemistry and Biological Applications, ACS Symposium Series 680, под ред. J.M.Harris и др., изд-во American Chemical Society, Washington, D.C., 1997, cc.155-169).
Однако существует потребность в создании новых аналогов PYY, которые имеют существенно более низкую молекулярную массу, но сохраняют при этом такую же или более высокую эффективность, фармакокинетические характеристики и фармакологические характеристики, что и существующие агонисты Y2R. Существует также необходимость в пэгилированных аналогах PYY, например, для повышения времени полужизни пептида и снижения иммуногенности для индивидуумов, которые нуждаются в применении таких агонистов.
Соединения, предлагаемые в изобретении, обладают также преимуществами, поскольку они представляют собой укороченные версии PYY3-36. Так, использование более коротких пептидов не только облегчает синтез и очистку соединений, но также улучшает и снижает количество процессов и стоимость производства. Кроме того, соединения, предлагаемые в изобретении, взаимодействуют преимущественно с PYY-рецепторами и не взаимодействуют с гомологичными рецепторами, такими как рецепторы Y1, Y4 и Y5 NPY. Тем самым минимизируются нежелательные агонистические или антагонистические побочные реакции.
На чертежах показано:
на фиг.1 - ЖХВР-хроматограмма соединения, предлагаемого в настоящем изобретении;
на фиг.2 - ЖХВР-хроматограмма соединения, предлагаемого в настоящем изобретении;
на фиг.3 - результаты MALDI-TOF-анализа соединения, предлагаемого в настоящем изобретении;
на фиг.4 - ЖХВР-хроматограмма другого соединения, предлагаемого в настоящем изобретении;
на фиг.5 - ЖХВР хроматограмма соединения, предлагаемого в настоящем изобретении;
на фиг.6 - результаты MALDI-TOF-анализа соединения, предлагаемого в настоящем изобретении;
на фиг.7 - диаграмма, характеризующая воздействия соединения, предлагаемого в настоящем изобретении, на потребление пищи после его введения;
на фиг.8 - диаграмма, характеризующая воздействия другого соединения, предлагаемого в настоящем изобретении, на потребление пищи после его введения;
на фиг.9 - диаграмма, характеризующая воздействия еще одного соединения, предлагаемого в настоящем изобретении, на потребление пищи после его введения;
на фиг.10 - диаграмма, характеризующая воздействия на потребление пищи еще одного соединения, предлагаемого в настоящем изобретении, после его введения.
Все упомянутые в настоящем описании пептидные последовательности обозначены согласно принятой конвенции, т.е. N-концевая аминокислота расположена слева, а С-концевая аминокислота расположена справа, если не указано иное. Короткая черта между двумя аминокислотными остатками обозначает пептидную связь. Если аминокислота имеет изомерные формы, то представлена L-форма аминокислоты, если специально не указано иное. Для удобства в описании настоящего изобретения используют принятые и нетрадиционные сокращения для различных применяемых аминокислот. Эти сокращения известны специалистам в данной области, но для простоты изложения перечислены ниже:
Asp=D=аспарагиновая кислота; Ala=А=аланин; Arg=R=аргинин; Asn=N=аспарагин; Gly=G=глицин; Glu=Е=глутаминовая кислота; Gln=Q=глутамин; His=Н=гистидин; Ile=I=изолейцин; Leu=L=лейцин; Lys=К=лизин; Met=М=метионин; Phe=F=фенилаланин; Pro=Р=пролин; Ser=S=серин; Thr=Т=треонин; Trp=W=триптофан; Tyr=Y=тирозин и Val=V=валин.
Также для удобства в описании настоящего изобретения использованы следующие сокращения или символы для обозначения групп, реагентов, и т.п., которые хорошо известны специалистам в данной области:
| Pqa | N-пиперазин-1-ил-4-(3Н)-хиназолинон-3-уксусная кислота; |
| Cms | N-(5-O-карбоксиметил)сератонин; |
| 3,4,5, F3-Phe | 3,4,5-трифторфенилаланин; |
| 2,3,4,5,6, F5-Phe | 2,3,4,5,6-пентафторфенилаланин; |
| 4-MeO-Apc | 4-метокси-1-амино-4-фенилциклогексанкарбоновая кислота; |
| 3-Pal | 3-пиридилаланин; |
| 4-Pal | 4-пиридилаланин; |
| Aib | аминоизомасляная кислота; |
| 1-1-Aic | 1-аминоиндан-1-карбоновая кислота; |
| 2-2-Aic | 2-аминоиндан-2-карбоновая кислота; |
| Ach | 1-аминоциклогексилкарбоновая кислота; |
| Аср | 1-аминоциклопентилкарбоновая кислота; |
| Fmoc | 9-флуоренилметилоксикарбонил; |
| Аллил | сложный аллиловый эфир; |
| Aloc | аллилоксикарбонил; |
| Mtt | 4-метилтритил; |
| 2Pip | сложный 2-фенилизопропиловый эфир; |
| Pmc | 2,2,5,7,8-пентаметилхроман-6-сульфонил; |
| CH2Cl2 | метиленхлорид; |
| А2О | уксусный ангидрид; |
| CH3CN | ацетонитрил; |
| DMAc | диметилацетамид; |
| ДМФ | диметилформамид; |
| ДИПЭА | N,N-диизопропилэтиламин; |
| ТФК | трифторуксусная кислота; |
| ГОБТ | N-гидроксибензотриазол; |
| ДИК | N,N'-диизопропилкарбодиимид; |
| БОФ | гексафторфосфат бензотриазол-1-илокситрис(диметиламино)фосфония; |
| ГБТУ | гексафторфосфат 2-(1Н-бензотриазол-1-ил)-1,1,3,3-тетраметилурония; |
| NMФ | 1-метил-2-пиролиденон; |
| Bip | бифенилаланин или 4-фенилфентилаланин; |
| Dip | дифенилаланин; |
| Tic | 1,2,3,4-тетрагидроизохинолин-3-карбоновая кислота; |
| FAB-MC | масс-спектрометрия с бомбардировкой быстрыми атомами и |
| ES-MC | масс-спектрометрия с использованием электроспрея. |
В контексте настоящего описания понятие «алкил» означает разветвленный или неразветвленный циклический или ациклический насыщенный или ненасыщенный (например, алкенил или алкинил) углеводородный радикал, который может быть замещенным или незамещенным. Если алкильная группа является циклической, то она предпочтительно представляет собой С3-С12-, более предпочтительно С5-С10-, более предпочтительно С5-С7-группу. Если алкильная группа является ациклической, то она предпочтительно представляет собой С1-С10-, более предпочтительно C1-С6-группу, более предпочтительно метил, этил, пропил (н-пропил или изопропил), бутил (н-бутил, изобутил или трет-бутил) или пентил (включая н-пентил и изопентил), более предпочтительно метил. Таким образом, должно быть очевидно, что понятие «алкил» в контексте настоящего описания включает алкил (разветвленный или неразветвленный), замещенный алкил (разветвленный или неразветвленный), алкенил (разветвленный или неразветвленный), замещенный алкенил (разветвленный или неразветвленный), алкинил (разветвленный или неразветвленный), замещенный алкинил (разветвленный или неразветвленный), циклоалкил, замещенный циклоалкил, циклоалкенил, замещенный циклоалкенил, циклоалкинил и замещенный циклоалкинил.
В контексте настоящего описания понятие «(низш.)алкил» означает разветвленный или неразветвленный циклический или ациклический насыщенный или ненасыщенный (например, алкенил или алкинил) углеводородный радикал, в котором циклическая (низш.)алкильная группа обозначает C5-, С6- или С7-группу, а ациклическая (низш.)алкильная группа обозначает C1-, С2-, С3- или С4-группу и предпочтительно обозначает метил, этил, пропил (н-пропил или изопропил) или бутил (н-бутил, изобутил или трет-бутил). Таким образом, должно быть очевидно, что понятие «(низш.)алкил» в контексте настоящего описания включает (низш.)алкил (разветвленный или неразветвленный), (низш.)алкенил (разветвленный или неразветвленный), (низш.)алкинил (разветвленный или неразветвленный), цикло(низш.)алкил, цикло(низш.)алкенил и цикло(низш.)алкинил.
В контексте настоящего описания понятие «арил» означает замещенную или незамещенную карбоциклическую ароматическую группу, такую как фенил или нафтил, или замещенную или незамещенную гетероароматическую группу, содержащую один или несколько, предпочтительно один гетероатом, такую как пиридил, пирролил, фуранил, тиенил, тиазолил, изотиазолил, оксазолил, изоксазолил, оксадиазолил, тиадиазолил, пиразолил, имидазолил, триазолил, пиримидинил, пиридазинил, пиразинил, триазинил, индолил, индазолил, хинолил, хиназолил, бензимидазолил, бензотиазолил, бензизоксазолил и бензизотиазолил.
Алкильные и арильные группы могут быть замещенными или незамещенными. Когда они являются замещенными, в них присутствуют 1-3 заместителя, предпочтительно 1 заместитель. Заместители могут представлять собой углеродсодержащие группы, такие как алкил, арил, арилалкил (например, замещенный и незамещенный фенил, замещенный и незамещенный бензил); атомы галогена и галогенсодержащие группы, такие как галоалкил (например, трифторметил); кислородсодержащие группы, такие как спирты (например, гидроксил, гидроксиалкил, арил(гидроксил)алкил), простые эфиры (например, алкоксигруппа, арилоксигруппа, алкоксиалкил, арилоксиалкил), альдегиды (например, карбоксальдегид), кетоны (например, алкилкарбонил, алкилкарбонилалкил, арилкарбонил, арилалкилкарбонил, арилкарбонилалкил), кислоты (например, карбоксигруппа, карбоксиалкил), производные кислот, такие как эфиры (например, алкоксикарбонил, алкоксикарбонилалкил, алкилкарбонилоксигруппа, алкилкарбонилоксиалкил), амиды (например, аминокарбонил, моно- или диалкиламинокарбонил, аминокарбонилалкил, моно- или диалкиламинокарбонилалкил, ариламинокарбонил), карбаматы (например, алкоксикарбониламиногруппа, арилоксикарбониламиногруппа, аминокарбонилоксигруппа, моно- или диалкиламинокарбонилоксигруппа, ариламинокарбонилоксигруппа) и мочевины (например, моно- или диалкиламинокарбониламиногруппа или ариламинокарбониламиногруппа); азотсодержащие группы, такие как амины (например, аминогруппа, моно- или диалкиламиногруппа, аминоалкил, моно- или диалкиламиноалкил), азиды, нитрилы (например, цианогруппа, цианалкил), нитрогруппы; серосодержащие группы, такие как тиолы, простые тиоэфиры, сульфоксиды и сульфоны (например, алкилтиогруппа, алкилсульфинил, алкилсульфонил, алкилтиоалкил, алкилсульфинилалкил, алкилсульфонилалкил, арилтиогруппа, арилсульфинил, арилсульфонил, арилтиоалкил, арилсульфинилалкил, арилсульфонилалкил), и гетероциклические группы, содержащие один или несколько, предпочтительно один, гетероатом (например, тиенил, фуранил, пирролил, имидазолил, пиразолил, тиазолил, изотиазолил, оксазолил, оксадиазолил, тиадиазолил, азиридинил, азетидинил, пирролидинил, пирролинил, имидазолидинил, имидазолинил, пиразолидинил, тетрагидрофуранил, пиранил, пиронил, пиридил, пиразинил, пиридазинил, пиперидил, гексагидроазепинил, пиперазинил, морфолинил, тианафтил, бензофуранил, изобензофуранил, индолил, оксииндолил, изоиндолил, индазолил, индолинил, 7-азаиндолил, бензопиранил, кумаринил, изокумаринил, хинолинил, изохинолинил, нафтридинил, циннолинил, хиназолинил, пиридопиридил, безоксазинил, хиноксалинил, хроменил, хроманил, изохроманил, фталазинил и карболинил).
(Низш.)алкильные группы могут быть замещенными или незамещенными, предпочтительно являются незамещенными. Когда они являются замещенными, то, как правило, содержат 1-3 заместителя, предпочтительно 1 заместитель. Заместителями являются перечисленные выше группы заместителей, отличные от алкила, арила и арилалкила.
В контексте настоящего описания понятие «алкоксигруппа» означает алкил-О-группу, а «алкоил» означает алкил-CO-группу. Заместители, представляющие собой алкоксигруппу, или заместители, содержащие алкоксигруппу, могут быть замещены одной или несколькими алкильными группами.
В контексте настоящего описания понятие «галоген» означает радикал фтора, хлора, брома или йода, предпочтительно радикал фтора, хлора или брома и более предпочтительно радикал фтора или хлора.
В контексте настоящего описания понятие «фармацевтически приемлемая соль» означает любую фармацевтически приемлемую соль соединения формулы (I). Соли можно получать из фармацевтически приемлемых нетоксичных кислот или оснований, включая неорганические и органические кислоты и основания. Такие кислоты представляют собой уксусную, бензолсульфоновую, бензойную, камфорсульфоновую, лимонную, этенсульфоновую, дихлоруксусную, муравьиную, фумаровую, глюконовую, глутаминовую, гиппуровую, бромистоводородную, соляную, изетионовую, молочную, малеиновую, яблочную, миндальную, метансульфоновую, слизевую, азотную, щавелевую, памовую, пантотеновую, фосфорную, янтарную, серную, винную, щавелевую, пара-толуолсульфоновую кислоту и т.п. Особенно предпочтительными являются фумаровая, соляная, бромистоводородная, фосфорная, янтарная, серная и метансульфоновая кислоты. Приемлемые соли присоединения оснований представляют собой соли щелочных металлов (например, натрия, калия), щелочно-земельных металлов (например, кальция, магния) и алюминия.
Одним из вариантов осуществления настоящего изобретения является агонист рецептора нейропептида-2 формулы (I):
,
в которой Х выбран из группы, включающей N-пиперазин-1-ил-4(3Н)-хинозолинон-3-уксусную кислоту (Pqa), N-(5-O-карбоксиметил)серотонин (Cms), 4-(2-аминометил)-6-дибензофуранпропановую кислоту, 4-(1-пиперидин-4-ил)бутановую кислоту и 4-(2-аминоэтил)-1-карбоксиметилпиперазин, Y обозначает Н, замещенный или незамещенный алкил, замещенный или незамещенный (низш.)алкил, замещенный или незамещенный арил, замещенную или незамещенную алкоксигруппу или поли(этилен)гликольную группу, R1 обозначает Ile, Ala, (D)Ile, N-метил Ile, Aib, 1-1 Aic, 2-2 Aic, Ach или Аср, R2 обозначает Lys, Ala, (D)Lys, NMelys, Nle или (Lys-Gly), R3 обозначает Arg, Ala, (D)Arg, N-метилArg, Phe, 3,4,5-трифторPhe или 2,3,4,5,6-пентафторРhe, R4 обозначает His, Ala, (D)His, N-метилHis, 4-MeOApc, 3-Pal или 4-Pal, R5 обозначает Tyr, Ala, (D)Tyr, N-метилTyr, Trp, Tic, Bip, Dip, (1)Nal, (2)Nal, 3,4,5-трифторPhe или 2,3,4,5,6-пентафторPhe, R6 обозначает Leu, Ala, (D)Leu или N-метилLeu, R7 обозначает Asn, Ala или (D)Asn, R8 обозначает Leu, Ala, (D)Leu или N-метилLeu, R9 обозначает Val, Ala, (D)Val или N-метилVal, R10 обозначает Thr, Ala или N-метилТhr, R11 обозначает Arg, (D)Arg или N-метилArg, R12 обозначает Gln или Ala, R13 обозначает Arg, (D)Arg или N-метилArg и R14 обозначает Tyr, (D)Tyr или N-метилTyr, или его фармацевтически приемлемая соль.
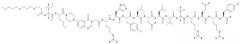
Следующим вариантом осуществления настоящего изобретения является агонист рецептора нейропептида-2 формулы (II):
(SEQ ID NO: 1),
в которой X обозначает фрагмент, выбранный из группы, включающей N-пиперазин-1-ил-4(3Н)-хинозолинон-3-уксусную кислоту (Pqa), N-(5-O-карбоксиметил)серотонин (Cms), 4-(2-аминометил)-6-дибензофуранпропановую кислоту, 4-(1-пиперидин-4-ил)бутановую кислоту и 4-(2-аминоэтил)-1-карбоксиметилпиперазин, Y обозначает Н, замещенный или незамещенный алкил, замещенный или незамещенный (низш.)алкил, замещенный или незамещенный арил, замещенную или незамещенную алкоксигруппу или поли(этилен)гликольную группу, R1 обозначает Ile, Ala, (D)Ile, N-метилIle, Aib, 1-1 Aic, 2-2 Aic, Ach или Аср и R2 обозначает Lys, Ala, (D)Lys, NMelys, Nle или (Lys-Gly), или его фармацевтически приемлемая соль.
Следующим вариантом осуществления настоящего изобретения является агонист рецептора нейропептида-2 формулы (III):
,
(SEQ ID NO: 2),
в которой X выбран из группы, включающей N-пиперазин-1-ил-4(3Н)-хинозолинон-3-уксусную кислоту (Pqa), N-(5-O-карбоксиметил)серотонин (Cms), 4-(2-аминометил)-6-дибензофуранпропановую кислоту, 4-(1-пиперидин-4-ил)бутановую кислоту и 4-(2-аминоэтил)-1-карбоксиметилпиперазин, и Y обозначает Н, замещенный или незамещенный алкил, замещенный или незамещенный (низш.)алкил, замещенный или незамещенный арил, замещенную или незамещенную алкоксигруппу или поли(этилен)гликольную группу, или его фармацевтически приемлемая соль.
Предпочтительными агонистами рецептора нейропептида-2 являются указанные выше антагонисты, в которых Х обозначает Pqa. Другими предпочтительными агонистами рецептора нейропептида-2 являются указанные выше агонисты, в которых Х обозначает Cms. Предпочтительно Y обозначает Н или C1-С6алкил, более предпочтительно Y обозначает C1-С6алкильную группу.
Предпочтительными агонистами рецептора нейропептида-2, как они определены выше, являются агонисты, выбранные из группы, включающей
IK-Pqa-RHYLNLVTRQRY,
Ac-IK-Pqa-RHYLNLVTRQRY,
IK-Pqa-RHYLNLVTRARY,
IK-Pqa-RHYLNLVARQRY,
IK-Pqa-RHYLNLATRQRY,
IK-Pqa-RHYLNAVTRQRY,
IK-Pqa-RHYLALVTRQRY,
IK-Pqa-RHYANLVTRQRY,
IK-Pqa-RHALNLVTRQRY,
IK-Pqa-RAYLNLVTRQRY,
IK-Pqa-AHYLNLVTRQRY,
IA-Pqa-RHYLNLVTRQRY,
Ac-IA-Pqa-RHYLNLVTRQRY,
AK-Pqa-RHYLNLVTRQRY,
IK-Pqa-RHYLNLVTRQR(D)Y,
IK-Pqa-RHYLNLVTRQ(D)RY,
IK-Pqa-RHYLNLVT(D)RQRY,
IK-Pqa-RHYLNL(D)VTRQRY,
IK-Pqa-RHYLN(D)LVTRQRY,
IK-Pqa-RHYL(D)NLVTRQRY,
IK-Pqa-RHY(D)LNLVTRQRY,
IK-Pqa-RH(D)YLNLVTRQRY,
IK-Pqa-R(D)HYLNLVTRQRY,
IK-Pqa-(D)RHYLNLVTRQRY,
I(D)K-Pqa-RHYLNLVTRQRY,
(D)IK-Pqa-RHYLNLVTRQRY,
IK-Pqa-RHYLNLVTRQR(N-метил)Y,
IK-Pqa-RHYLNLVTRQ(N-метил)RY,
IK-Pqa-RHYLNLVT(N-метил)RQRY,
IK-Pqa-RHYLNLV(N-метил)TRQRY,
IK-Pqa-RHYLNL(N-метил)VTRQRY,
IK-Pqa-RHYLN(N-метил)LVTRQRY,
IK-Pqa-RHY(N-метил)LNLVTRQRY,
IK-Pqa-RH(N-метил)YLNLVTRQRY,
IK-Pqa-R(N-метил)HYLNLVTRQRY,
IK-Pqa-(N-метил)RHYLNLVTRQRY,
I(N-метил)K-Pqa-RHYLNLVTRQRY,
(N-метил)IK-Pqa-RHYLNLVTRQRY,
INle-Pqa-RHYLNLVTRQRY,
Ac-INle-Pqa-RHYLNLVTRQRY,
Ac-INle-Pqa-FHYLNLVTRQRY,
IK-Pqa-RHWLNLVTRQRY,
IK-Pqa-AHWLNLVTRQRY,
Ac-INle-Pqa-RHYLNLVTRQR(D)Y,
Ac-INle-Pqa-RHYLNLVTRQR(N-метил)Y,
Ac-INle-Pqa-RHYLys(28)NLVAsp(32)RQRY(циклоLys-Asp),
IK-Cms-RHYLNLVTRQRY,
IKG-Cms-RHYLNLVTRQRY,
Ac-INle-Cms-RHYLys(28)NLVAsp(32)RQRY(циклоLys-Asp),
Ac-INle-Pqa-RHTicLNLVTRQRY,
Ac-INle-Pqa-RHBipLNLVTRQRY,
Ac-INle-Pqa-RHDipLNLVTRQRY,
Ac-INle-Pqa-RH(1)NalLNLVTRQRY,
Ac-INle-Pqa-RH(2)NalLNLVTRQRY,
Ac-INle-Pqa-RH(3,4,5-трифторPhe)LNLVTRQRY,
Ас-IМlе-Рqа-RН(2,3,4,5,6-пентафторPhe)LNLVТRQRY,
Ac-INle-Pqa-R(4-MeOApc)YLNLVTRQRY,
Ac-INle-Pqa-R(3-Pal)YLNLVTRQRY,
Ac-INle-Pqa-R(4-Pal)YLNLVTRQRY,
Ас-INlе-Рqа-(3,4,5-трифторPhe)HYLNLVTRQRY,
Ас-INlе-Рqа-(2,3,4,5,6-пентафторPhе)HYLNLVTRQRY,
Ac-Aib-Nle-Pqa-RHYLNLVTRQRT,
Ac1-1-Aic-Nle-Pqa-RHYLNLVTRQRT,
Ac1-1-Aic-Nle-Pqa-RHYLNLVTRQRT,
Ac-2-2Aic-Nle-Pqa-RHYLNLVTRQRT,
Ac-Ach-Nle-Pqa-RHYLNLVTRQRT,
Ac-Acp-Nle-Pqa-RHYLNLVTRQRT,
H-INle-Pqa-RHYLNLVTRQRY,
(ПЭГ-10000)-INle-Pqa-RHYLNLVTRQRY и
(ПЭГ-30000)-INle-Pqa-RHYLNLVTRQRY.
Более предпочтительными агонистами рецептора нейропептида-2, как они определены выше, являются агонисты, выбранные из группы, включающей
IK-Pqa-RHYLNLVTRQRY,
Ac-IK-Pqa-RHYLNLVTRQRY,
IK-Pqa-RHYLNLVTRQR(N-метил)Y,
IK-Pqa-RHYLNLVTRQ(N-метил)RY,
INle-Pqa-RHYLNLVTRQRY,
Ac-INle-Pqa-RHYLNLVTRQRY и
(ПЭГ-30000)-INle-Pqa-RHYLNLVTRQRY.
Каждый из всех перечисленных выше агонистов рецептора нейропептида-2 представляет собой индивидуальный предпочтительный вариант осуществления настоящего изобретения.
Следующим вариантом осуществления настоящего изобретения является способ лечения ожирения у пациента, который нуждается в этом, заключающийся в том, что осуществляют стадию введения пациенту в терапевтически эффективном количестве агониста рецептора нейропептида-2 формулы (I):
,
в которой Х выбран из группы, включающей N-пиперазин-1-ил-4(3Н)-хинозолинон-3-уксусную кислоту (Pqa), N-(5-O-карбоксиметил)серотонин (Cms), 4-(2-аминометил)-6-дибензофуранпропановую кислоту, 4-(1-пиперидин-4-ил)бутановую кислоту и 4-(2-аминоэтил)-1-карбоксиметилпиперазин, Y обозначает Н, замещенный или незамещенный алкил, замещенный или незамещенный (низш.)алкил, замещенный или незамещенный арил, замещенную или незамещенную алкоксигруппу или поли(этилен)гликольную группу, R1 обозначает Ile, Ala, (D)Ile, N-метилIle, Aib, 1-lAic, 2-2 Aic, Ach или Аср, R2 обозначает Lys, Ala, (D)Lys, NMelys, Nle или (Lys-Gly), R3 обозначает Arg, Ala, (D)Arg, N-метилArg, Phe, 3,4,5-трифторPhe или 2,3,4,5,6-пентафторPhe, R4 обозначает His, Ala, (D)His, N-метилHis, 4-MeOApc, 3-Pal или 4-Pal, R5 обозначает Tyr, Ala, (D)Tyr, N-метилTyr, Trp, Tic, Bip, Dip, (l)Nal, (2)Nal, 3,4,5-трифторPhe или 2,3,4,5,6-пентафторPhe, R6 обозначает Leu, Ala, (D)Leu или N-метилLeu, R7 обозначает Asn, Ala или (D)Asn, R8 обозначает Leu, Ala, (D)Leu или N-метилLeu, R9 обозначает Val, Ala, (D)Val или N-метилVal, R10 обозначает Thr, Ala или N-метилТhr, R11 обозначает Arg, (D)Arg или N-метилArg, R12 обозначает Gln или Ala, R13 обозначает Arg, (D)Arg или N-метилArg и R14 обозначает Тyr, (D)Tyr или N-метилTyr, или его фармацевтически приемлемую соль.
Предпочтительным является вариант описанного выше способа, в котором агонист рецептора нейропептида-2 вводят пациенту один раз в три дня. Предпочтительно агонист рецептора нейропептида-2 вводят пациенту один раз в неделю.
Предпочтительным является описанный выше вариант способа, в котором агонист рецептора нейропептида-2 вводят пациенту орально, интраназально, внутривенно, подкожно, парентерально, трансдермально, внутрибрюшинно или ректально. Предпочтительно агонист рецептора нейропептида-2 вводят интраназально. Предпочтительно также агонист рецептора нейропептида-2 вводят подкожно.
Предпочтительным является вариант описанного выше способа, в котором агонист рецептора нейропептида-2 вводят в дозе, составляющей от примерно 2,5 до примерно 10 мг/кг, более предпочтительно от примерно 2,5 до примерно 5 мг/кг. Предпочтительным является также вариант способа, в котором агонист рецептора нейропептида-2 вводят в дозе от примерно 5 до примерно 10 мг/кг.
В описанных выше вариантах способа предпочтительными являются агонисты рецептора нейропептида-2, в которых Х выбран из группы, включающей N-пиперазин-1-ил-4(3Н)-хинозолинон-3-уксусную кислоту (Pqa), N-(5-O-карбоксиметил)серотонин (Cms), 4-(2-аминометил)-6-дибензофуранпропановую кислоту, 4-(1-пиперидин-4-ил)бутановую кислоту и 4-(2-аминоэтил)-1-карбоксиметилпиперазин.
Следующим вариантом осуществления настоящего изобретения является агонист рецептора нейропептида-2, который содержит производное RYY3-36, в котором аминокислотные остатки 5-24 заменены группой, имеющей в длину от примерно 8 до примерно 11 ангстрем.
Ниже изобретение проиллюстрировано с помощью приведенного подробного описания и прилагаемых чертежей, в которых проиллюстрированы дополнительные варианты осуществления изобретения, признаки и преимущества изобретения.
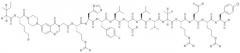
Настоящее изобретение относится к аналогам RYY3-36, в которых аминокислотные остатки 5-24 заменены группой, такой, например, как Pqa или Cms. Например, в изобретении предложены соединения формулы PYY3-4-Pqa-PYY25-36:
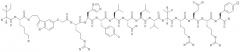
и формулы PYY3-4-Cms-PYY25-36:
В изобретении предложены также соединения формулы:
В приведенных выше структурных формулах группа -Х-СН2-СН2-О-Х- согласно общепринятой номенклатуре обозначает повторяющиеся гликольные звенья полиэтиленгликольного фрагмента, т.е. группы -(СН2-СН2-O)n-. Число «n» выбирают в зависимости от массы требуемого полиэтиленгликольного звена, составляющей предпочтительно примерно 10000 Да (n обозначает примерно 227) или примерно 30000 Да (n обозначает примерно 682). На основе полученных с помощью ЯМР данных о структуре нативного RYY3-36 получены предлагаемые в изобретении аналоги, в которых присутствует фрагмент, замещающий аминокислотные остатки 5-24 PYY3-36. Примеры таких фрагментов включают N-пиперазин-1-ил-4-(3Н)-хиназолинон-3-уксусную кислоту (Pqa) и N-(5-O-карбоксиметил)серотонин (Cms). Фрагмент, как правило, является жестким и предпочтительно может стабилизировать третичную структуру молекулы, что позволяет получать укороченные аналоги с требуемой эффективностью и фармакокинтическими и фармакологическими характеристиками. Фрагмент, как правило, имеет длину от примерно 8 до примерно 11 ангстрем, предпочтительно длину от примерно 9 до примерно 11 ангстрем, более предпочтительно длину от примерно 9 до примерно 10 ангстрем, еще более предпочтительно длину от примерно 8 до примерно 10 ангстрем и еще более предпочтительно длину от примерно 8 до примерно 9 ангстрем.
Должно быть очевидно, что изобретение не ограничено представленными в настоящем описании конкретными вариантами его осуществления, поскольку могут быть получены модификации конкретных вариантов осуществления изобретения, которые подпадают также под объем прилагаемой формулы изобретения. Должно быть очевидно также, что терминологию, применяемую для описания конкретных вариантов осуществления изобретения, не следует рассматривать как ограничивающую. Таким образом, объем настоящего изобретения определяется прилагаемой формулой изобретения.
Хотя для воплощения на практике или для оценки изобретения можно использовать любые методы, устройства и материалы, аналогичные или эквивалентные представленным в настоящем описании, ниже приведены предпочтительные методы, устройства и материалы.
Репрезентативные соединения, предлагаемые в настоящем изобретении, легко синтезировать с помощью любого общепринятого метода, пригодного для формирования пептидной связи между аминокислотами. Такие общепринятые методы включают, например, любую осуществляемую в жидкой фазе процедуру, обеспечивающую конденсацию между свободной альфа-аминогруппой аминокислоты или ее остатка, в которых защищены карбоксильная группа и другие реакционноспособные группы, со свободной первичной карбоксильной группой другой аминокислоты или ее остатка, в которых защищены аминогруппа или другие реакционноспособные группы.
Такие общепринятые методы, применяемые для синтеза новых соединений, предлагаемых в настоящем изобретении, включают, например, любой метод твердофазного пептидного синтеза. При осуществлении такого метода синтеза новых соединений можно последовательно включать требуемые аминокислотные остатки в процессе удлинения пептидной цепи согласно общим принципам методов твердофазного синтеза. Такие методы описаны, например, у Merrifield R.B., J. Amer. Chem. Soc. 85, 1963, cc.2149-2154; Barany и др., The Peptides, Analysis, Synthesis and Biology, т.2, под ред. Gross Е. и Meienhofer J., изд-во Academic Press, 1980, cc.1-284, которые включены в настоящее описание в качестве ссылки.
При химическом синтезе пептидов общая стратегия заключается в защите реакционноспособных боковых групп различных аминокислотных остатков приемлемыми защитными группами, которые должны препятствовать осуществлению в этом сайте химической реакции до тех пор, пока защитная группа не удалена. Общей стратегией является также защита альфа-аминогруппы на аминокислоте или ее фрагменте до тех пор, пока происходит взаимодействие с карбоксильной группой, с последующим избирательным удалением защитной группы альфа-аминогруппы, что позволяет в дальнейшем происходить реакции в этом сайте. Хотя в настоящем описании представлены защитные группы, которые применяют в методе твердофазного синтеза, следует отметить, что каждую аминокислоту можно защищать с помощью защитной группы, которую обычно используют для защиты соответствующей аминокислоты при синтезе в жидкой фазе.
Альфа-аминогруппы можно защищать с помощью приемлемых защитных групп, выбранных из ароматических защитных групп уретанового типа, таких как аллилоксикарбонил, бензилоксикарбонил (Z) и замещенный бензилоксикарбонил, такой как пара-хлорбензилоксикарбонил, пара-нитробензилоксикарбонил, пара-бромбензилоксикарбонил, пара-бифенилизопропилоксикарбонил, 9-флуоренилметилоксикарбонил (Fmoc) и пара-метоксибензилоксикарбонил (Moz); алифатических защитных групп уретанового типа, таких как трет-бутилоксикарбонил (Вос), диизопропилметилоксикарбонил, изопропилоксикарбонил и аллилоксикарбонил. В контексте настоящего описания наиболее предпочтительной группой для альфа-аминокислот является Fmoc.
Гуанидиногруппы можно защищать приемлемой защитной группой, выбранной из нитрогруппы, пара-толуолсульфонила (Tos), (Z), пентаметилхромансульфонила (Pmc), 4-метокси-2,3,6-триметилбензолсульфонила (Mtr), наиболее предпочтительными для аргинина (Arg) являются (Pmc) и (Mtr).
ε-Аминогруппы можно защищать приемлемой защитной группой, выбранной из 2-хлорбензилоксикарбонила (2-Cl-Z), 2-бромбензилоксикарбонила (2-Br-Z) и трет-бутилоксикарбонила (Вос). Вос является наиболее предпочтительным для (Lys).
Гидроксильные группы (ОН) можно защищать приемлемой защитной группой, выбранной из бензила (Bz1), 2,6-дихлорбензила (2,6-диСl-Вz1) и трет-бутила (t-Bu), (tBu) является наиболее предпочтительным для (Tyr), (Ser) и (Thr).
β- и γ-Амидные группы можно защищать приемлемой защитной группой, выбранной из 4-метилтритила (Mtt), 2,4,6-триметоксибензила (Tmob), 4,4-диметоксидитилбис(4-метоксифенил)метила (Dod) и тритила (Trt). Trt является наиболее предпочтительным для (Asn) и (Gln).
Индольную группу можно защищать приемлемой защитной группой, выбранной из формила (For), мезитил-2-сульфонила (Mts) и трет-бутилоксикарбонила (Воc). Вое является наиболее предпочтительным для (Тrp).
Имидазольную группу можно защищать приемлемой защитной группой, выбранной из бензила (Bzl), трет-бутилоксикарбонила (Вос) и тритила (Trt). Trt является наиболее предпочтительным для (His).
Все растворители, а именно изопропанол (iPrOH), метиленхлорид (СН2Сl2), диметилформамид (ДМФ) и N-метилпирролидон (NMП) получали от фирмы Fisher или Burdick & Jackson и применяли без дополнительной дистилляции. Трифторуксусную кислоту получали от фирмы Halocarbon или Fluka и применяли без дополнительной очистки.
Диизопропилкарбодиимид (ДИК) и диизопропилэтиламин (ДИПЭА) получали от фирмы Fluka или Aldrich и применяли без дополнительной очистки. Гидроксибензотриазол (ГОБТ), диметилсульфид (ДМС) и 1,2-этандитиол (ЭДТ) получали от фирмы Sigma Chemical Co. и применяли без дополнительной очистки. Защищенные аминокислоты, как правило, имели L-конфигурацию и их получали от фирмы Bachem или Neosystem. Чистоту этих реагентов подтверждали до их применения с помощью тонкослойной хроматографии, ЯМР и путем определения температуры плавления. Бензгидриламиносмола (ВНА) представляла собой сополимер стирола - 1% дивинилбензола (100-200 или 200-400 меш), и ее получали от фирмы Bachem или Advanced Chemtech. Общее содержание азота в этих смолах, как правило, составляло 0,3-1,2 миллиэквивалента (мэкв)/г.
Высокоэффективную жидкостную хроматогафию (ЖХВР) осуществляли на устройстве типа LDC, состоящем из насосов с постоянным напором I и III, программируемого устройства для создания градиента растворителя типа Gradient Master solvent и смесителя и снабженного спектромонитором (Spectromonitor III) УФ-детектора волн различной длины. Аналитическую ЖХВР осуществляли методом обращенной фазы, используя C18-колонки типа Vydac (0,4×30 см). Разделение с помощью препаративной ЖХВР осуществляли на колонках типа Vaydac (2×25 см).
В предпочтительных вариантах осуществления изобретения пептиды получали с помощью твердофазного синтеза с использованием метода, описанного в целом у Merrifield (J. Amer. Chem. Soc., 85, 1963, с.2149), хотя, как было отмечено выше, можно применять другие эквивалентные методы химического синтеза. Твердофазный синтез начинают с С-конца пептида путем сочетания защищенной альфа-аминокислоты с приемлемой смолой. Такой исходный продукт можно получать путем присоединения альфа-аминозащищенной аминокислоты с помощью сложноэфирной связи к пара-бензилоксибензиловому спирту (Ванг) смолы или путем создания амидной связи между Fmoc-линкером, таким как пара-((R,S)-α-(1-(9Н-флуорен-9-ил)метоксиформамидо)-2,4-диметилоксибензил)феноксиуксусная кислота (линкер Ринка), для