Пероральная композиция тедисамила с замедленным высвобождением, обладающая свойством задержки в желудке
Иллюстрации
Показать всеИзобретение относится к области фармацевтики, более конкретно к композиции тедисамила или его фармацевтически приемлемой соли с замедленным высвобождением для использования в профилактике и лечении фибрилляции предсердий, трепетания предсердий и ишемии миокарда, содержащей от 5 до 40 мас.% тедисамила или его фармацевтически приемлемой соли, от 30 до 85 мас.% набухающей в воде полимерной матрицы, содержащей гидроксипропилметилцеллюлозу (НРМС) высокой или средней вязкости и гидроксиэтилцеллюлозу (НЕС) высокой или средней вязкости в соотношении НРМС/НЕС=1/0,85-1/1,2, от 2,5 до 5 мас.% соли, способной выделять газообразный углекислый газ в желудочной среде, и от 0,5 до 10 мас.% альгиновой кислоты. Изобретение позволяет обеспечить композицию тедисамила, обладающую повышенной биодоступностью и вызывающую меньше побочных эффектов со стороны желудочно-кишечного тракта. 3 н. и 2 з.п. ф-лы, 4 табл., 2 ил.
Реферат
Область техники, к которой относится изобретение
Настоящее изобретение касается новой композиции, содержащей тедисамил или его фармацевтически приемлемую соль с замедленным высвобождением, обладающей свойством задержки в желудке, и применения этой композиции в профилактике и лечении фибрилляции предсердий, трепетания предсердий и ишемии миокарда.
Уровень техники
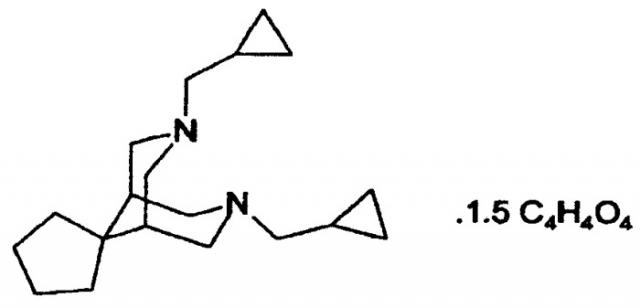
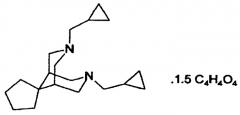
Тедисамил - соединение, разрабатываемое в виде его сесквифумаратной соли, является соединением, блокирующим калиевые каналы, которое характеризуется ограниченным терапевтическим окном и химически описывается как 3',7'-бис(циклопропилметил)-спиро[циклопентан-1,9'-[3,7]диазабицикло-[3.3.1]-нонан], (2E)-2-бутендиоат(2:3)
Было показано, что соединение эффективно в конверсии фибрилляции предсердий в обычный синусовый ритм и поддержании синусового ритма после кардиоверсии. Оно также обладает антиишемическими свойствами. Тедисамил действует как блокатор миокардиальных калиевых каналов и в более высоких концентрациях также натриевых каналов. Он не оказывает отрицательного инотропного эффекта, и он не влияет на уровень калия в сыворотке крови. Кроме того, в клинических исследованиях он успешно применялся с обычно применяемыми препаратами и варфарином. Кроме того, сердечные гликозиды, атенолол и глибенкламид не оказывали клинически значимого эффекта на фармакокинетику тедисамила.
Раскрытие изобретения
В ходе клинических исследований было выяснено, что тедисамил, применяемый в форме таблеток с немедленным высвобождением, вызывал некоторые отрицательные эффекты, в основном неблагоприятные явления со стороны желудочно-кишечного тракта в виде диареи и боли в животе, которые вероятно были вызваны высокими пиковыми концентрациями соединения в плазме при применении композиции с немедленным высвобождением. Кроме того, был сделан вывод, что низкие значения наименьших концентраций, как полагают, ответственны за ограничение эффективности, особенно в поддержании синусового ритма после кардиоверсии.
В качестве первого решения вышеупомянутых задач, с целью снижения пиковых концентраций в плазме, были разработаны композиции с модифицированным высвобождением, описанные в WO 02/26214. В WO 02/26214 раскрыты композиции, например, тедисамила с замедленным высвобождением, имеющие в основном независимое от ионной силы высвобождение при воздействии жидкостей желудочно-кишечного тракта. Однако, по-видимому, полная доступность активного соединения в этих композициях с замедленным высвобождением была недостаточна (57% по сравнению с композицией с немедленным высвобождением).
Задачей настоящего изобретения является предоставление композиции, вызывающей меньше побочных эффектов со стороны желудочно-кишечного тракта и имеющей биологическую доступность по меньшей мере 70% по сравнению с композицией с немедленным высвобождением и, предпочтительно, по меньшей мере 75%.
Было обнаружено, что вышеупомянутые задачи могут быть решены в композиции тедисамила с замедленным высвобождением, обладающей свойствами задержки в желудке. Это особенно удивительно ввиду того, что всасывание тедисамила в проксимальном отделе желудочно-кишечного тракта намного хуже, чем всасывание в дистальном отделе кишечника (подвздошная кишка).
Подробное описание изобретения
Настоящее изобретение касается композиции с замедленным высвобождением, обладающей свойствами задержки в желудке. Эти свойства задержки в желудке могут быть получены с помощью применения флотирующей системы доставки лекарства, описанной B. N. Singh и K. H. Kim (J. Controlled Release 2000, 63, 235-259), предпочтительно имеющей плотность менее 1,0 г/см3, или применения набухающей или увеличивающейся в объеме системы доставки, то есть композиции, которая набухает в желудке до такой степени, что не может пройти пилорический сфинктер (ссылка: J.Timmermans и A.J.Moes, The cut-off size for gastric emptying of dosage forms, J.Pharm. Sci. 1993, 82(8), 854).
Под замедленным высвобождением понимается (постепенное) высвобождение активной субстанции из дозированной формы за интервал времени от 2 до 8 часов или больше. Этот период начинается обычно с применения дозированной формы, или с началом теста на растворимость in vitro (момент помещения дозированной формы в среду растворения). В основе настоящего изобретения композиции с замедленным высвобождением сравниваются с композициями с немедленным высвобождением, в которых большая часть активной субстанции (то есть по меньшей мере 80%) высвобождается через 45 минут после введения дозированной формы или от начала теста на растворимость in vitro.
В одном варианте осуществления изобретения набухающая композиция набухает в желудке до такой степени, что она больше не может пройти пилорический сфинктер. Этот вариант осуществления настоящего изобретения включает от 5 до 40 мас.% (предпочтительно от 10 до 30 мас.%) тедисамила или его фармацевтически приемлемой соли, от 30 до 85 мас.% набухающего в воде полимера, и необязательно, усилитель набухания (предпочтительно от 0,5 до 10 мас.%, более предпочтительно от 1 до 4 мас.% и наиболее предпочтительно 3 мас.%). Усилитель набухания повышает скорость набухания и степень набухания. Примером усилителя набухания является альгиновая кислота.
В предпочтительном варианте осуществления изобретения вышеупомянутые системы комбинированы в системе доставки лекарства, которая и флотирует, и набухает. Самый предпочтительный вариант осуществления настоящего изобретения включает от 5 до 40 мас.% (предпочтительно от 10 до 30 мас.%) тедисамила или его фармацевтически приемлемой соли, от 30 до 85 мас.% набухающего в воде полимера и от 2,5 до 5 мас.% соли, способной выделять газообразную двуокись углерода в желудочной среде, указанная композиция обладает как свойством флотации, так и набухания, что приводит к задержке в желудке. Необязательно добавляется усилитель набухания (предпочтительно от 0,5 до 10 мас.%, более предпочтительно от 1 до 4 мас.% и более предпочтительно 3%).
Несмотря на то, что покрытие не является обязательным для достижения желательного эффекта настоящего изобретения, композиция необязательно покрыта материалом покрытия для достижения другого желательного эффекта, такого как маскирование вкуса или придание цвета.
Подходящие материалы покрытия известны в области техники, и к ним, например, относятся HPMC, акриловые полимеры, этилцеллюлоза (см. Graham Cole ed., Pharmaceutical Coating Technology, London, Taylor & Francis Ltd.; 1995).
Существует несколько набухающих в воде полимеров, которые могут применяться для получения композиции с замедленным высвобождением. К примерам набухающих в воде полимеров относятся гидроксипропилметилцеллюлоза (HPMC), гидроксипропилцеллюлоза (HPC), гидроксиэтилцеллюлоза (HEC), карбоксиметилцеллюлоза (CMC).
Эфиры целлюлозы, которые могут применяться в настоящем изобретении, известны в области техники, доступны в фармацевтических марках и имеют различные средние молекулярные массы, что приводит к различной вязкости растворов этих эфиров целлюлозы. В контексте этой заявки на патент гидрофильные полимеры могут быть охарактеризованы по их вязкости 2% мас./мас. водном растворе как имеющие низкую вязкость (менее приблизительно 1000 мПа), среднюю вязкость (от приблизительно 1000 мПа до приблизительно 10000 мПа) и высокую вязкость (более приблизительно 10000 мПа). Гидрофильные полимеры гидроксипропилметилцеллюлозы (HPMC) различной степени вязкости, которые могут применяться в настоящем изобретении, доступны от Dow Chemical Co. под торговым названием Methocel (и от Shin Etsu под торговым названием Metolose®.
К примерам полимеров низкой вязкости относятся Methocel E5®, Methocel E-15LV®, Methocel E50LV®, Methocel K100LV(и Methocel F50LV®, 2% водные растворы которых при 25°C имеют вязкость 5 мПа, 15 мПа, 50 мПа, 100 мПа и 50 мПа, соответственно).
К примерам HPMC средней вязкости относятся Methocel E4M (и Methocel K4M, 2% водные растворы которых при 25°C имеют вязкость 4000 мПа).
К примерам HPMC высокой вязкости относятся Methocel K15M (и Methocel K100M®, 2% водные растворы которых при 25°C имеют вязкость 15000 мПа и 100000 мПа).
Гидрофильные полимеры гидроксиэтилцеллюлозы (HEC) различной степени вязкости, которые могут применяться в настоящем изобретении, доступны от AQUALON под торговым названием Natrosol (и от Amerchol Corporation под торговым названием Cellosize®).
К примерам полимеров низкой вязкости относятся Natrosol L (и Natrosol J®, 2% водные растворы которых при 25°C имеют вязкость 10 мПа и 20 мПа, соответственно).
К примерам полимеров средней вязкости относятся Natrosol G (и Natrosol K®, 2% водные растворы которых при 25°C имеют вязкость 200 мПа и 1500 мПа, соответственно).
К примерам полимеров высокой вязкости относятся Natrosol M (и Natrosol HH®, 2% водные растворы которых имеют вязкость при 25°C 4000 мПа и 90000 мПа, соответственно).
В предпочтительном варианте осуществления настоящего изобретения композиция содержит смесь гидроксипропилметилцеллюлозы высокой или средней вязкости (HPMC), и гидроксиэтилцеллюлозы высокой или средней вязкости (HEC), описанную в WO 02/26214.
Соотношение HPMC высокой или средней вязкости и HEC высокой или средней вязкости составляет от 1/0,85 до 1/1,2, предпочтительно от 1/0,9 до 1/1,1, еще более предпочтительно от 1/0,95 до 1/1,05, и наиболее предпочтительно 1/1. Композиция необязательно может содержать HPMC низкой вязкости. В этом случае соотношение HPMC высокой или средней вязкости и HPMC низкой вязкости находится в диапазоне от 1/0,01 до 1/0,2 и предпочтительно от 1/0,01 до 1/0,1 и еще более предпочтительно от 1/0,02 до 1/0,05.
В качестве соли, способной выделять газообразную двуокись углерода, могут применяться карбонаты щелочных металлов, предпочтительно карбонат натрия, карбонат калия или бикарбонат натрия. Может быть добавлена кислота, например лимонная кислота и малеиновая кислота. Предпочтительным карбонатом является бикарбонат натрия, и предпочтительной кислотой является лимонная кислота.
Могут применяться другие вспомогательные материалы, такие как лубриканты (например натрия стеарилфумарат (Pruv®), глицерина бегенат (Compritol 888 ATO), глиданты (например коллоидный кремния диоксид (Aerosil®)), разрыхлители (например натрия крахмал гликолят (Primojel®)), наполнители (например маннит), красители и антиоксиданты.
Настоящее изобретение также касается способа изготовления композиции, описанной выше, отличающегося тем, что
(1) ядро спрессовано из смеси, включающей от 5 до 40 мас.% тедисамила или его фармацевтически приемлемой соли, от 30 до 85 мас.% набухающей в воде полимерной матрицы и от 2,5 до 5 мас.% соли, способной выделять газообразную двуокись углерода в желудочной среде, и необязательно от 0,5 до 10 мас.% усилителя набухания.
(2) ядро необязательно покрыто оболочкой.
В предпочтительном варианте осуществления компоненты HPMC (K4M и E5) и HEC смешиваются. Полученная смесь смешивается со смесью предварительно измельченных лимонной кислоты и бикарбоната натрия и альгиновой кислоты. Добавляется измельченный сесквифумарат тедисамила и смесь перемешивается. Просеивается и добавляется лубрикант с последующим смешиванием с наполнителем. Активная субстанция может быть добавлена в предварительно гранулированной форме к порошковой смеси, применяемой для прессования. В альтернативном варианте порошковая смесь для таблетирования может быть изготовлена с помощью процедуры смешивания с последующим процессом (влажной или сухой) грануляции. Смесь компонентов прессуется в таблетки с применением коммерчески доступного оборудования (например, Courtoy(R0) с применением регулирующих поток агентов, таких как коллоидный кремний, и смазывающих агентов, таких как тальк, натрия стеарилфумарат или магния стеарат. Содержание гидрофильной целлюлозы в готовой композиции составляет от 30% до 85%, предпочтительно от 33% до 70%, тогда как содержание тедисамила или соли тедисамила составляет от 5% до 40%, предпочтительно от 10 до 30%. Для улучшения реологических свойств порошка и предотвращения прилипания порошка к окрашивающим стенкам или перфораторам содержание регулирующего поток и смазывающего агентов является постоянным. Содержание глиданта составляет от 0 мас.% до 5 мас.%, предпочтительно от 2 до 5% и наиболее предпочтительно приблизительно 3 мас.%. Содержание лубриканта составляет от 2 мас.% до 4 мас.% и предпочтительно приблизительно 3 мас.%. Для обеспечения маскирования вкуса ядро таблетки может быть покрыто 2-4% в массовом соотношении смесью полимера с пигментами или без них. Типичные смеси покрытия коммерчески доступны, например, как Opadry(от COLORCON®.
Настоящее изобретение может применяться для введения активного соединения тедисамила млекопитающему, в особенности человеку, нуждающемуся в этом. Применение тедисамила особенно полезно в профилактике и лечении фибрилляции предсердий, трепетания предсердий и ишемии миокарда.
Таким образом, настоящее изобретение также касается применения тедисамила или его фармацевтически приемлемой соли в производстве задерживающейся в желудке дозированной формы для профилактики или лечения фибрилляции предсердий, трепетания предсердий или ишемии миокарда у млекопитающего, и особенно у человека.
Следующие примеры предназначены исключительно для дальнейшего пояснения изобретения более подробно, и следовательно, эти примеры во всяком случае не должны считаться ограничивающими объем изобретения.
Пример 1. Изготовление непокрытых композиций с модифицированным высвобождением, с 100% растворением in vitro через 4-6 часов, содержащих 150 мг тедисамила в форме его сесквифумарата.
Объем загрузки 1,5 кг, эквивалентный 4286 таблеткам, был изготовлен со следующей композицией:
| Компонент | Количество (г) |
| Сесквифумарат тедисамила | 1028 |
| HPMC (K4M) | 193 |
| HPMC (E5) | 39 |
| HEC (HX250PH) | 193 |
| Коллоидный безводный кремний | 26 |
| Натрия стеарилфумарат | 21 |
Процедура изготовления заключается в следующем:
- Просеивается необходимое количество коллоидного безводного кремния.
- Смешиваются необходимые количества тедисамила сесквифумарата, HPMC K4M, HPMC E5, HEC HX250 PH и просеянного коллоидного безводного кремния.
- Необходимое количество натрия стеарилфумарата просеивается и смешивается со смесью тедисамила.
- Результирующая порошковая смесь прессуется в таблетки (расчетный вес ядра: 350 мг).
Пример 2. Изготовление покрытых оболочкой композиций с модифицированным высвобождением со 100% растворением через 8-12 часов in vitro, содержащих 150 мг тедисамила в форме его сесквифумарата.
Объем загрузки 1,5 кг, эквивалентный 3529 таблеткам, был изготовлен со следующей композицией:
| Компонент | Количество (г) |
| Ядро таблетки | |
| Тедисамила сесквифумарат | 849 |
| HPMC (K4M) | 285 |
| HPMC (E5) | 49 |
| HEC (HX250PH) | 285 |
| Коллоидный безводный кремний | 14 |
| Натрия стеарилфумарат | 18 |
| Оболочка | |
| Дисперсия полиакрилата 30% в массовом соотношении1) | 73,5 |
| HPMC (E5) | 2,2 |
| Тальк (микротальк) | 11 |
| Дистиллированная вода | Приблизительно 417 |
| 1) например, Eudragit NE30D(от Röhm Pharma) |
Повышение массы за счет покрытия оболочкой составляет приблизительно 10 мг/таблетка.
Процедура изготовления состоит в следующем:
- Смешиваются необходимые количества тедисамила сесквифумарата, HPMC K4M, HPMC E5, HEC HX250 PH и просеянного коллоидного безводного кремния.
- Необходимое количество натрия стеарилфумарата просеивается и смешивается со смесью тедисамила.
- Результирующая порошковая смесь прессуется в таблетки (расчетная масса ядра: 425 мг).
- Таблетки покрываются оболочкой с помощью распыления на таблетки суспензии покрытия, состоящей из 30% в массовом соотношении дисперсии полиакрилата, HPMC E5 и суспензии талька в воде (расчетная масса таблетки: 435 мг).
Пример 3. Изготовление флотирующих увеличивающихся в объеме композиций, содержащих 138 мг тедисамила в форме его сесквифумарата.
Объем загрузки 1,0 кг, эквивалентный 1351 таблетке, был изготовлен со следующей композицией:
| Компонент | Количество (г) |
| Тедисамила сесквифумарат | 299,1 |
| Маннит (25) | 200 |
| HPMC (K4M) | 193 |
| HEC (HX250PH) | 193 |
| Глицерил бегенат (Compritol 888) | 40,5 |
| Альгиновая кислота | 37,8 |
| Натрия бикарбонат | 24,3 |
| Безводная лимонная кислота | 6,76 |
| HPMC (E5) | 6,08 |
Процедура изготовления состоит в следующем:
- Смешиваются необходимые количества HPMC (K4M), HPMC (E5) и HEC.
- Измельчается безводная лимонная кислота и добавляется к упомянутой выше смеси. Добавляются безводный натрия бикарбонат и альгиновая кислота, и порошки смешиваются.
- Добавляется и смешивается измельченный тедисамила сесквифумарат.
- Просеивается через сито 0,5 мм и добавляется глицерил бегенат. Добавляется маннит, и порошки смешиваются.
- Результирующая порошковая смесь прессуется в таблетки (расчетная масса таблетки: 740 мг).
Пример 4. Изготовление композиций тедисамила с немедленным высвобождением, содержащих 119,7 мг в форме его дигидрохлорида.
Объем загрузки 144,8 кг, эквивалентный 800000 таблеток, был изготовлен со следующей композицией:
| Компонент | Количество (г) |
| Тедисамила гидрохлорид | 60,00 |
| Лактозы моногидрат | 60,00 |
| стеариновая пальмитиновая кислота | 6,00 |
| Тальк | 5,40 |
| Коллоидный безводный кремний | 0,60 |
| Opadry Y-1 7000 White | 14,08 |
Процедура изготовления состоит в следующем:
- Смешиваются необходимые количества тедисамила дигидрохлорида, лактозы моногидрата, талька и коллоидного безводного кремния.
- Добавляется стеариновая пальмитиновая кислота, и порошки смешиваются.
- Результирующая порошковая смесь прессуется в таблетки (расчетная масса таблетки: 165 мг).
- Таблетки покрываются оболочкой с помощью распыления на таблетки суспензии покрытия Opadry Y-1 7000 White в воде (расчетная масса таблетки: 181 мг).
Пример 5. Частично сбалансированное перекрестное исследование однократного приема, сравнивающее две различные композиции с модифицированным высвобождением (MR) соли тедисамила, композицию с немедленным высвобождением (IR) и флотирующую увеличивающуюся в объеме (FE) композицию.
Тедисамил назначался 20 здоровым добровольцам мужского пола в возрастном диапазоне от 18 до 45 лет. Каждый субъект регулярно получал три из следующих композиций в однократной дозе:
A: композицию, описанную в примере 1 (15 субъектов имеют анализируемые данные).
B: композицию, описанную в примере 2 (14 субъектов имеют анализируемые данные).
D: композицию, описанную в примере 3 (13 субъектов имеют анализируемые данные).
E: двухкратно композицию, описанную в примере 4 (15 субъектов имеют анализируемые данные).
Были определены концентрации в плазме, и оценивалась информация о неблагоприятных реакциях, применяя ненаводящие вопросы.
Фармакокинетические данные
Представленные в Таблице 1, нормализованные относительно дозы фармакокинетические параметры показывают, что таблетка FE оказывала большее воздействие по сравнению с IR (заштриховано), и поэтому была выбрана для изучения многократного приема.
| Таблица 1 | ||||||
| Фармакокинетические данные | ||||||
| Фармакокинетика свободного основания тедисамила | ||||||
| Вариант лечения | n | Tmax ч | Cmax нг/мл | AUC0-t Нг*ч/мл | AUC Нг*ч/мл | TЅ ч |
| E 119,7 мг | 15 | 1,47 | 723 | 3700 | 3770 | 10,8 |
| A 150 мгОтношение A/E | 15 | 3,23 | 361 0,398 | 3000 0,647 | 3050 0,646 | 8,26 |
| B 150 мгОтношение B/E | 14 | 3,64 | 388 0,428 | 3080 0,664 | 3190 0,675 | 10,5 |
| D 138 мгОтношение D/E | 13 | 3,54 | 347 0,416 | 3250 0,762 | 3330 0,766 | 9,23 |
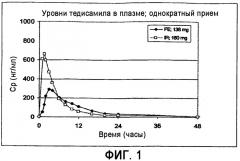
Фактические уровни свободного основания тедисамила в плазме (групповые значения), достигнутые при однократном приеме 138 мг FE (композиция D) и 119,7 мг IR (композиция E), показаны на фиг.1. Результирующее воздействие было несколько выше (AUC 113%; AUC означает участок под кривой (0→бесконечность)) для композиции IR по сравнению с FE и вдвое выше пикового уровня в плазме для композиции IR по сравнению с FE.
Толерантность
Известно, что тедисамил вызывает неблагоприятные явления со стороны желудочно-кишечного тракта, в основном жалобы типа диареи, и это было подтверждено в этом исследовании для таблетки IR. После однократного приема 119,7 мг IR шесть из 15 субъектов предъявляли жалобы на 10 неблагоприятных явлений со стороны желудочно-кишечного тракта (диарея 6-x, боль в животе 4-x). Из 10 явлений со стороны желудочно-кишечного тракта 6 были определены как средней тяжести. После однократного приема 138 мг FE три из 13 субъектов предъявляли жалобы на неблагоприятные явления стороны желудочно-кишечного тракта (нарушение функции языка 2-x, боль в животе 1-го. Нарушение функции языка было определено однократно как средней тяжести.
Неблагоприятные явления, развивающиеся при лечении, представлены в таблице 2.
| Таблица 2 | |||||||
| Неблагоприятные эффекты со стороны желудочно-кишечного тракта в исследовании однократного приема, сравнивающем композицию IR с композицией FE | |||||||
| MedDRA SOC | Предпочтительный показатель | FE 138 мг (n=13) | IR 119,7 мг (n=15) | ||||
| N | % | n | N | % | n | ||
| Расстройства желудочно-кишечноготракта | Любое | 2 | 15,4 | 3 | 6 | 40 | 10 |
| Боль в животе NOS | 1 | 7,7 | 1 | 1 | 6,7 | 2 | |
| Боль в верхнем отделе живота | 2 | 13,3 | 2 | ||||
| Диарея NOS | 5 | 33,3 | 6 | ||||
| Нарушение функции языка NOS1) | 1 | 7,7 | 2 | ||||
| N: число субъектов с явлением%: процентный показатель подвергнутых воздействию субъектов, имеющих явлениеn: число явлений 1) NOS=не уточненный иначе |
Пример 6. Исследование многократного приема, сравнивающее композицию с немедленным высвобождением (IR), флотирующую увеличивающуюся в объеме (FE) композицию соли тедисамила.
Тедисамил назначался здоровым добровольцам мужского пола в возрастном диапазоне от 18 до 45 лет. Всего 18 субъектов были разделены на 2 параллельные группы, принимающие следующие композиции в однократной дозе в течение 7 дней:
D1: два раза в день композицию, описанную в примере 3 (9 субъектов).
E1: два раза в день композицию, описанную в примере 4 (9 субъектов).
Фармакокинетические данные
В части исследования многократного приема была взята кривая уровня в плазме в стационарном состоянии после приема утренней дозы. Нормализованное по дозе воздействие (AUC) после приема композиции FE составляло приблизительно 80% от воздействия таблетки IR, и Cmax составляла приблизительно 60%, см. Таблицу 3 (из обеих групп полная кривая PK была получена у 8 субъектов).
| Таблица 3 | |||||
| Фармакокинетические данные в стационарном состоянии | |||||
| Фармакокинетика свободного основания тедисамила | |||||
| Вариант лечения | n | Tmax ч | Cmax нг/мл | AUCss нг*ч/мл | TЅ ч |
| E1 59,58 мг BID | 8 | 1,5 | 589 | 3260 | 12,3 |
| D1 138 мг BIDСоотношение FE/IR | 8 | 3 | 798 0,588 | 6250 0,832 | 11 |
| BID=дважды в деньss=стационарное состояние |
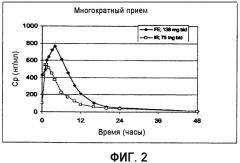
Фактические принимаемые дозы значительно различались; таблетка FE принималась дважды в день в дозе 138 мг в пересчете на свободное основание, а таблетки IR дважды в день в дозе 59,58 мг в пересчете на свободное основание. Это приводило к повышению воздействия на приблизительно 90% и повышению уровня в плазме на 35% (групповые значения) для композиции FE в отличие от IR, как показано на фиг.2.
Толерантность к многократному приему
В этом исследовании проводилось сравнение результатов толерантности к однократному приему для таблетки IR, где шесть из девяти субъектов предъявляли жалобы на 23 побочных эффекта со стороны желудочно-кишечного тракта (метеоризм 9-x, жидкий стул 4-x, диарея 4-x, водянистый стул 1-го, боль в животе 4-x, ургентная дефекация 1-го). Метеоризм и жидкий стул описывались как средней тяжести однократно, а боль в животе дважды. Напротив, в случае таблетки FE только три из девяти субъектов предъявляли жалобы на три побочных эффекта со стороны желудочно-кишечного тракта (метеоризм 1-x, жидкий стул 1-x, диарея 1-x). Все они были легкой степени тяжести. Некоторые неблагоприятные явления относились к другим классам систем органов, и они были более или менее равномерно распределены в двух группах.
Все неблагоприятные явления со стороны желудочно-кишечного тракта, возникающие при лечении, представлены в Таблице 4.
| Таблица 4 | |||||||
| Неблагоприятные эффекты со стороны желудочно-кишечного тракта в исследовании многократного приема композиции IR в сравнении с композицией FE | |||||||
| MedDRA SOC | Предпочтительный показатель | FE 276 мг (n=9) | IR 119,7 мг (n=9) | ||||
| N | % | n | N | % | n | ||
| Расстройства желудочно-кишечноготракта | Любое | 3 | 33,3 | 3 | 6 | 66,7 | 23 |
| Боль в животе NOS | 2 | 22,2 | 2 | ||||
| Боль в верхнем отделе живота | 1 | 11,1 | 2 | ||||
| Ургентная дефекация | 1 | 11,1 | 1 | ||||
| Диарея NOS | 1 | 11,1 | 1 | 2 | 22,2 | 4 | |
| Метеоризм | 1 | 11,1 | 1 | 5 | 55,6 | 9 | |
| Жидкий стул | 1 | 11,1 | 1 | 3 | 33,3 | 4 | |
| Водянистый стул | 1 | 11,1 | 1 | ||||
| N: число субъектов с явлением%: процентный показатель подвергнутых воздействию субъектов, имеющих явлениеn: число явлений |
Заключение
В отношении неблагоприятных эффектов со стороны желудочно-кишечного тракта толерантность к тедисамилу в виде соли в флотирущей увеличивающейся в объеме (FE) таблетке намного лучше, чем в композиции с немедленным высвобождением. В представленных данных различие особенно заметно в условиях многократного приема несмотря на то, что воздействие было почти в два раза выше в группе FE.
1. Композиция тедисамила или его фармацевтически приемлемой соли с замедленным высвобождением для использования в профилактике и лечении фибрилляции предсердий, трепетания предсердий и ишемии миокарда, содержащая от 5 до 40 мас.% тедисамила или его фармацевтически приемлемой соли, от 30 до 85 мас.% набухающей в воде полимерной матрицы, содержащей гидроксипропилметилцеллюлозу (НРМС) высокой или средней вязкости и гидроксиэтилцеллюлозу (НЕС) высокой или средней вязкости в соотношении НРМС/НЕС=1/0,85-1/1,2, от 2,5 до 5 мас.% соли, способной выделять газообразный углекислый газ в желудочной среде, и от 0,5 до 10 мас.% альгиновой кислоты.
2. Композиция тедисамила или его фармацевтически приемлемой соли с замедленным высвобождением по п.1, в которой указанная фармацевтически приемлемая соль является сесквифумаратной солью или дигидрохлоридом.
3. Композиция тедисамила или его фармацевтически приемлемой соли с замедленным высвобождением по п.1, характеризующаяся тем, что указанная соль, способная выделять газообразную двуокись углерода в желудочной среде, выбрана из группы, состоящей из натрия карбоната, калия карбоната и натрия бикарбоната.
4. Способ изготовления композиции по п.1, характеризующийся тем, что(1) ядро спрессовывают из смеси, включающей от 5 до 40 мас.% тедисамила или его фармацевтически приемлемой соли, от 30 до 85 мас.% набухающей в воде полимерной матрицы, содержащей гидроксипропилметилцеллюлозу (НРМС) высокой или средней вязкости и гидроксиэтилцеллюлозу (НЕС) высокой или средней вязкости в соотношении НРМС/НЕС=1/0,85-1/1,2, от 2,5 до 5 мас.% соли, способной выделять газообразную двуокись углерода в желудочной среде, и от 0,5 до 10 мас.% альгиновой кислоты.(2) ядро необязательно покрывают оболочкой.
5. Применение тедисамила или его фармацевтически приемлемой соли в изготовлении дозированной формы с задержкой в желудке по п.1 для получения лекарственного средства для профилактики и лечения фибрилляции предсердий, трепетания предсердий или ишемии миокарда.