Производные трициклического лактама в качестве ингибиторов 11- -гидроксистероидной дегидрогеназы
Иллюстрации
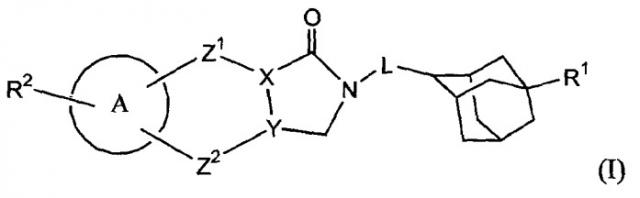
Показать всеИзобретение относится к соединениям общей формулы (I), их N-оксидным формам, фармацевтически приемлемым аддитивным солям и стереохимически изомерным формам в качестве ингибитора 11-HSD1, к их применению, фармацевтической композиции на их основе и способу ее получения. Соединения могут найти применение для лечения и профилактики заболеваний, опосредованных 11-HSD1. В общей формуле (I)
X представляет собой С или N; Y представляет собой С или N; L представляет собой метил или прямую связь; Z1 представляет собой прямую связь, С1-2алкил или радикал формулы -СН=; Z2 представляет собой прямую связь, С1-2алкил; R1 представляет собой водород, гало, гидрокси; R2 представляет собой водород, гало или С1-4алкилокси; А представляет собой фенил или моноциклический гетероцикл, выбранный из группы, состоящей из тиофенила или пирридинила. 6 н. и 3 з.п. ф-лы, 3 табл.
Реферат
Метаболический синдром представляет собой заболевание с возрастающим уровнем распространения не только на Западе, но в Азии и в развивающихся странах. Его отличает ожирение, в частности центральное или висцеральное ожирение, диабет 2 типа, гиперлипидемия, гипертензия, артериосклероз, ишемические болезни сердца и со временем хроническая почечная недостаточность (C.T. Montague et al. (2000), Diabetes, 49, 883-888).
Глюкокортикоиды и 1lβ-HSDl известны как важные факторы дифференцировки жировых стромальных клеток в зрелые адипоциты. В висцеральных стромальных клетках больных, страдающих ожирением, уровень 11β-HSD1 мРНК возрастает в сравнении с подкожной жировой тканью. Кроме того, повышенную экспрессию 11β-HSD1 в жировой ткани у трансгенных мышей связывают с возросшими уровнями кортикостерона в жировой ткани, висцеральным ожирением, инсулинчувствительностью, диабетом 2 типа, гиперлипидемией и гиперфагией (H. Masuzaki et al (2001), Science, 294, 2166-2170). Поэтому наиболее вероятно, что 11β-HSD1 вовлечен в развитие висцерального ожирения и метаболического синдрома.
Ингибирование 11β-HSD1 приводит к уменьшению дифференцировки и возрастанию, пролиферации жировых стромальных клеток. Более того, дефицит глюкокортикоидов (адреналектомия) увеличивает способность инсулина и лептина к стимуляции анорексии и потери массы; введение глюкокортикоидов обращает данный эффект в обратную сторону (P.M. Stewart et al (2002), Trends Endocrin. Metabol, 13, 94-96). Эти данные предполагают, что усиленная реактивация кортизона с помощью 11β-HSD1 может обострить ожирение и это может оказаться полезным для ингибирования этого фермента в жировой ткани больных, страдающих ожирением.
Ожирение также связано с повышенными сердечно-сосудистыми рисками. Существует ощутимая зависимость между скоростью экскреции кортизола и HDL (липопротеиды высокой плотности) холестерином как у мужчин, так и у женщин; означая, что глюкокортикоиды регулируют ключевые компоненты повышенных сердечно-сосудистых рисков. По аналогии потеря аортальной эластичности также связана с висцеральным ожирением у взрослых особей.
Влияние эффекта сниженной активности 11β-HSD1 подчеркивается тем, что мышь воздействием 11β-HSD1 приведенная в шоковое состояние имеет увеличенные плазменные уровни эндогенного активного глюкокортикоида, но несмотря на это сохраняет защищенность от инсулинрезистентности, вызываемой стрессом или ожирением. Дополнительно эти приведенные в стрессовое состояние мыши обнаруживают анти-атерогенный плазмидный липидный профиль и обладают преимуществом сниженного возрастного ослабления познавательной способности.
ГЛЮКОКОРТИКОИДЫ И ГЛАУКОМА
Глюкокортикоиды при экзогенном введении и при некоторых состояниях гиперпродуцирования, таких как синдром Кушинга, повышая внутриглазное давление, увеличивают риск заболевания глаукомой. Рост стимулируемого кортикостероидами внутриглазного давления вызывает повышенная резистентность к оттоку водянистой влаги вследствие вызванных глюкокортикоидами изменений в трабекулярной сети и ее интрацеллюлярном матриксе (Zhou et al. (Int J Mol Med (1998) 1, 339-346). Сообщалось также, что кортикостероиды увеличивают количества фибронектина, так же как и коллагена типа I и типа IV, в трабекулярный сети передних камер глаза культивируемого органа теленка.
11β-HSD1 экспрессируется в базальных клетках корнеального эпителия и непигментированных эпителиальных клетках. Глюкокортикоидную рецепторную мРНК (mRNA) определяли только в трабекулярной сети, тогда как в непигментированных эпителиальных клетках присутствовала глюкокортикоидная, минералокортикоидная рецепторная и 11β-HSD1 мРНК. Введение больным карбеноксолона приводило к значительному снижению внутриглазного давления (S. Rauz et al. (2001), Invest. Ophtalmol. Vis. Science, 42, 2037-2042). Это подчеркивает роль ингибиторов HSD1 при лечении глаукомы.
Соответственно для решения указанной проблемы с помощью настоящего изобретения было необходимо идентифицировать сильные ингибиторы 11β-HSD1, обладающие высокой селективностью по отношению к 11β-HSD1, и использовать их при лечении патологий, связанных с избыточным образованием кортизола, то есть нарушений, при которых необходим сниженный уровень активного глюкокортикоида, таких как метаболический синдром, диабет 2 типа, ослабленная толерантность к глюкозе (IGT), ослабленная утилизация глюкозы (IFG), дислипидемия, гипертензия, ожирение, диабет, сердечно-сосудистые заболевания, связанные с ожирением, артериосклероз, атеросклероз, миопатия, остеопороз, нейродегенеративные и психиатрические расстройства, расстройства, связанные со стрессом, и глаукома. Как показано в дальнейшем, было обнаружено, что 3-замещенные производные 2-пирролидинона формулы (I) оказались пригодными в качестве лекарственного средства, в частности, при получении лекарственного препарата для лечения патологий, связанных с избыточным образованием кортизола.
Blommaert A. et al. (Heterocycles (2001), 55(12), 2273-2278) предлагают получение подложки из производного (R)-фенилглицинола, закрепленной на пиперидин- и пирролидинонподобном полимере и, в частности, описывают, l-[(lR)-2-гидрокси-l-фенилэтил]-3-метил-3-(фенилметил)-2-пирролидинон и, l-[(lR)-2-гидрокси-l-фенилэтил]-3-(фенилметил)-2-пирролидинон, (3R).
Bausanne I. et al. (Tetrahedron: Assymetry (1998), 9(5), 797-804) предлагают получение 3-замещенных пирролидинонов посредством α-алкилирования хирального нерацемического γ-лактона и, в частности, описывают l-(2-гидрокси-l-фенилэтил)-3-бензилпирролидин-2-он.
US 2001/034343; US 6211199; US 6194406; WO 97/22604 и WO 97/19074 представляют собой ряд заявок на патент, поданных Aventis Pharmaceuticals Inc., в которых предлагают пригодные для лечения аллергических заболеваний 4-(lH-бензимидазол-2-ил)[l,4]диазепаны. В этих заявках описывают 3-замещенные пирролидиноны по настоящему изобретению как промежуточное соединение при синтезах указанных 4-(lH-бензимидазол-2-ил)[l,4]-диазепанов. В этих заявках, в частности, описывают 3-[(4-фторфенил)метил]-l-[(lS)-l-фенилэтил]-2-пирролидинон и 3-[(4-фторфенил)метил]-1-[(1R)-1-фенилэтил]-2-пирролидинон.
В PCT публикации WO 03065983 (Merck & Co., Inc.) и WO 2004056744 (Janssen Pharmaceutica N.V.) описывают также соединения подобные адамантилу. Если принять WO 2004056744 за наиболее близкий известный уровень техники, то соединения по настоящей заявке отличает то, что адамантиловый цикл соединен с кольцевым амидным азотом, являющимся частью трициклической кольцевой системы. Вопреки тому, что в WO 03065983 раскрывают, что адамантиловый цикл может быть непосредственно связан с трициклической кольцевой системой, следует заметить, что указанные трициклические кольцевые системы отличаются тем, что имеют 2-адамантилтриазол в качестве структурного элемента остова; и соответственно не следует ожидать, что замена триазола на имидазолидинон или пирролидинон могла бы быть выполнена без потери желаемой активности, то есть способности к сильному ингибированию 11βHSD, при селективности по отношению к 11βHSD1.
Следовательно, ни в одном из цитируемых документов терапевтическое применение производных трициклического адамантиламида по настоящему изобретению не было не описано, не предложено. Соответственно первый аспект данного изобретения касается соединения формулы (I):
его N-оксидных форм, фармацевтически приемлемых аддитивных солей и их стереохимически изомерных форм, где
X представляет собой С или N;
Y представляет собой С или N;
L представляет собой метил, прямую связь;
Z1 представляет собой направленную связь или C1-2алкил- или двухвалентный радикал формулы
-CH2-CH= (а) или -CH= (b);
Z2 представляет собой прямую связь, C1-2алкил- или двухвалентный радикал формулы
-CH2-CH= (а) или -CH= (b);
R1 представляет собой водород, гало, циано, амино, фенил, гидрокси, C1-4алкилоксикарбонил, -O-(C=O)-C1-4алкил, гидроксикарбонил, NR3R4 или C1-4алкил, где указанный C1-4алкил или -O-(C=O)-C1-4алкил являются необязательно замещенными одним или несколькими заместителями, выбранными из гало, гидроксикарбонила, фенила, C1-4алкилокси или NR5R6, или R1 представляет собой C1-4алкилокси-, необязательно замещенный одним или несколькими заместителями, выбранными из гало, гидроксикарбонила, фенила, C1-4алкилокси или NR7R8;
R2 представляет собой водород, гало, C1-4алкил или C1-4алкилокси;
R3 и R4, каждый независимо, представляют собой водород, C1-4алкил или C1-4алкилкарбонил;
R5 и R6, каждый независимо, представляют собой водород, C1-4алкил или C1-4алкилкарбонил;
R7 и R8, каждый независимо, представляют собой водород, C1-4алкил или C1-4алкилкарбонил;
A представляет собой фенил или моноциклический гетероцикл, выбранный из группы, состоящей из тиофенила, фуранила, оксазолила, тиазолила, имидазолила, изоксазолила, изотиазолила, пирридинила, пиридазинила, пиримидинила и пиперазинила.
Используемые в дальнейшем соединения формулы (I) обозначают соединения по настоящему изобретению, включающие в себя соединения формул (Ibis), (Ii), (Iii), (Iiii), (Iiv) и их фармацевтически приемлемые N-оксиды, аддитивные соли, четвертичные амины и стереохимически изомерные формы.
Используемый в предшествующих определениях и в дальнейшем термин «гало» является обобщенным обозначением для фтора, хлора, брома и йода; C1-2алкил обозначает прямые насыщенные углеводородные радикалы, содержащие от 1 до 2 атомов углерода, то есть метил или этил; C1-4алкил обозначает насыщенные углеводородные радикалы с прямой и разветвленной цепью, имеющие от 1 до 4 атомов углерода, такие как, например, метил, этил, пропил, бутил, 1-метилэтил, 2-метилпропил, 2,2-диметилэтил и тому подобное; C1-4алкилокси обозначает прямые или разветвленные насыщенные углеводородные радикалы, имеющие от 1 до 4 атомов углерода, такие как метокси, этокси, пропилокси, бутилокси, 1-метилэтилокси, 2-метилпропилокси и тому подобное.
Гетероциклы, упоминаемые в приведенных выше определениях и используемые в дальнейшем, могут быть соответствующим образом присоединены к остатку молекулы формулы (I) через любой кольцевой углеродный атом или гетероатом. Таким образом, например, если гетероциклом является имидазолил, он может представлять собой 1-имидазолил, 2-имидазолил, 3-имидазолил, 4-имидазолил и 5-имидазолил; если это тиазолил, он может представлять собой 2-тиазолил, 4-тиазолил и 5-тиазолил.
Подразумевают, что фармацевтически приемлемые аддитивные соли, упоминаемые в дальнейшем, содержат терапевтически активные нетоксичные формы аддитивной соли кислоты, которые способны образовывать соединения формулы (I). Последние могут быть получены обработкой основной формы соответствующей кислотой. Соответствующие кислоты включают в себя, например, неорганические кислоты, такие как галоидоводородные кислоты, например, хлористоводородная или бромистоводородная кислота; серная; азотная; фосфорная и подобные кислоты; или органические кислоты, такие, как, например, уксусная, пропановая, оксиуксусная, молочная, пировиноградная, щавелевая, малоновая, янтарная (т.е. бутандиовая кислота), малеиновая, фумаровая, яблочная, винная, лимонная, метансульфоновая, этансульфоновая, бензолсульфоновая, п-толуолсульфоновая, цикламовая, салициловая, п-аминосалициловая, памовая и подобные кислоты.
Подразумевают, что упомянутые выше фармацевтически приемлемые аддитивные соли включают в себя терапевтически активные нетоксичные формы основно-аддитивной соли, которые способны образовывать соединения формулы (I). Примеры таких форм основно-аддитивной соли представляют собой, например, соли натрия, калия, кальция, а также соли фармацевтически приемлемых аминов, таких как, например, аммиак, алкиламины, бензатин, N-метил-D-глюкамин, гидрабамин, аминокислоты, например, аргинин, лизин.
И обратно, указанные формы солей могут быть превращены обработкой соответствующим основанием или кислотой в форму свободной кислоты или основания.
Термин «аддитивная соль», используемый выше, также охватывает сольваты, которые соединения формулы (I) способны образовывать, как и соли. Такие сольваты представляют собой, например, гидраты, алкоголяты и тому подобное.
Термин «стереохимически изомерные формы», используемый ранее, обозначает возможные различные изомерные формы, а также конформационные формы, которыми соединения формулы (I) могут обладать. Если не оговорено или не указано иначе, химическое наименование соединений обозначает смесь всех возможных стереохимических и конформационных изомерных форм; при этом указанные смеси включают все диастереомеры, энантиомеры и/или конформеры основной молекулярной структуры. Подразумевают, что все стереохимически изомерные формы соединений формулы (I) и в беспримесном чистом виде и в виде смеси друг с другом охвачены объемом настоящего изобретения.
Подразумевают, что N-оксидные формы соединений формулы (I) включают такие соединения формулы (I), в которых один или несколько атомов азота окислены до так называемого N-оксида.
Первая группа соединений представляет собой такие соединения формулы (I), в которых приняты одно или несколько нижеследующих ограничений;
(i) X представляет собой С или N;
(ii) Y представляет собой С или N;
(iii) L представляет собой метил или прямую связь;
(iv) Z1 представляет собой прямую связь, C1-2алкил или двухвалентный радикал формулы
-CH2-CH= (а) или -CH= (b);
(v) Z2 представляет собой прямую связь, C1-2алкил или двухвалентный радикал формулы
-CH2-CH= (а) или -CH= (b);
(vi) R1 представляет собой водород, гало, циано, амино, фенил, гидрокси, C1-4алкилоксикарбонил, гидроксикарбонил, NR3R4 или C1-4алкил, необязательно замещенный одним или несколькими заместителями, выбранными из гидроксикарбонила, фенила, C1-4алкилокси или NR5R6, или R1 представляет собой C1-4алкилокси, необязательно замещенный одним или несколькими заместителями, выбранными из гидроксикарбонила, фенила, C1-4алкилокси или NR7R8;
(vii) R2 представляет собой водород, гало, C1-4алкил или C1-4алкилокси;
(viii) R3 и R4, каждый независимо, представляют собой водород, C1-4алкил или C1-4алкилкарбонил;
(ix) R5 и R6, каждый независимо, представляют собой водород, C1-4алкил или C1-4алкилкарбонил;
(x) R7 и R8, каждый независимо, представляют собой водород, C1-4алкил или C1-4алкилкарбонил;
(xi) A представляет собой фенил или моноциклический гетероцикл, выбранный из группы, состоящей из тиофенила, фуранила, оксазолила, тиазолила, имидазолила, изоксазолила, изотиазолила, пирридинила, пиридазинила, пиримидинила и пиперазинила.
Интересной группой соединений являются такие соединения формулы (I), к которым применены одно или несколько нижеследующих ограничений:
(i) X представляет собой С или N;
(ii) Y представляет собой С или N;
(iii)L представляет собой метил или прямую связь;
(iv) Z1 представляет собой прямую связь, C1-2алкил или двухвалентный радикал формулы
-CH2-CH= (а) или -CH= (b);
(v) Z2 представляет собой прямую связь, C1-2алкил или двухвалентный радикал формулы
-CH2-CH= (а) или -CH= (b);
(vi) R1 представляет собой водород, гало, циано, амино, фенил, гидрокси, C1-4алкилоксикарбонил, гидроксикарбонил, NR3R4 или C1-4алкил, необязательно замещенный одним или несколькими заместителями, выбранными из гидроксикарбонила, фенила, C1-4алкилокси или NR5R6;
(vii) R2 представляет собой водород, гало, C1-4алкил или C1-4алкилокси;
(viii) R3 и R4, каждый независимо, представляет собой водород, C1-4алкил или C1-4алкилкарбонил;
(ix) R5 и R6, каждый независимо, представляют собой водород, C1-4алкил или C1-4алкилкарбонил;
(x) A представляет собой фенил или моноциклический гетероцикл, выбранный из группы, состоящей из тиофенила, фуранила, оксазолила, тиазолила, имидазолила, изоксазолила, изотиазолила, пирридинила, пиридазинила, пиримидинила и пиперазинила.
Следующая интересная группа соединений состоит из таких соединений формулы (I), к которым применены одно или несколько нижеследующих ограничений:
(i) L представляет собой метил или прямую связь;
(ii) R1 представляет собой водород, гало или гидрокси, в частности гало или гидроксил;
(iii) R2 представляет собой водород, гало или C1-4алкилокси;
(iv) A представляет собой фенил, моноциклический гетероцикл, выбранный из группы, состоящей из пиридинила и тиофенила.
Еще одна группа соединений состоит из таких соединений формулы (I), к которым применены одно или несколько нижеследующих ограничений:
(i) L представляет собой метил или прямую связь;
(ii) R1 представляет собой водород, гало, амино или гидрокси, в частности фтор, амино или гидроксил;
(iii) R2 представляет собой водород, бром или метокси;
(iv) Z1 представляет собой прямую связь, метил, этил или двухвалентный радикал формулы
-CH2-CH= (а);
(v) Z2 представляет собой прямую связь, метил или этил;
(vi) A представляет собой фенил, моноциклический гетероцикл, выбранный из группы, состоящей из пиридинила и тиофенила.
Интерес также представляют такие соединения формулы (I), в которых:
A представляет собой фенил или пиридинил и в которых L представляет собой прямую связь; и/или
R1 представляет собой гало, циано, амино, фенил, гидрокси, C1-4алкилоксикарбонил, гидроксикарбонил, NR3R4 или C1-4алкил, необязательно замещенный одним или несколькими заместителями, выбранными из гидроксикарбонила, фенила, C1-4алкилокси или NR5R6, или R1 представляет собой C1-4алкилокси, необязательно замещенный одним или несколькими заместителями, выбранными из гидроксикарбонила, фенила, C1-4алкилокси или NR7R8; в частности R1 представляет собой гало, циано, амино, фенил, гидрокси, C1-4алкилоксикарбонил, гидроксикарбонил, NR3R4 или C1-4алкил, замещенный одним или несколькими заместителями, выбранными из гидроксикарбонила, фенила, C1-4алкилокси или NR5R6.
В предпочтительном варианте осуществления соединения формулы (I) выбирают из группы, включающей:
2-Адамантан-2-ил-2,3,3a,4,9,9a-гексагидробензо[f]изоиндол-l-он;
2-Адамантан-2-ил-2,3,10,10a-тетрагидро-5H-имидазо[l,5-b]изохинолин-l-он;
2-Адамантан-2-ил-1,5,10,10a-тетрагидро-2H-имидазо[l,5-b]изохинолин-3-он;
2-Адамантан-1-илметил-1,2,3a,4,5,9b-гексагидробензо[e]изоиндол-3-он;
7-Адамантан-2-ил-7,8,8a,9-тетрагидропирроло[3,4-g]хинолин-6-он;
2-(5-Гидроксиадамантан-2-ил)-l,5,6,10b-тетрагидро-2H-имидазо[5,l-a]изохинолин-3-он;
2-(5-Фторадамантан-2-ил)-l,2,3a,4,5,9b-гексагидробензо[e]изоиндол-3-он;
2-(5-Гидроксиадамантан-2-ил)-2,3,3a,4,9,9a-гексагидробензо[f]изоиндол-l-он.
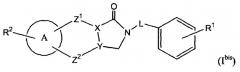
В следующем варианте осуществления в настоящем изобретении предлагают соединения формулы (Ibis)
их N-оксидные формы, фармацевтически приемлемые аддитивные соли и стереохимически изомерные формы, в которых:
X представляет собой С или N;
Y представляет собой С или N;
L представляет собой метил или прямую связь;
Z1 представляет собой прямую связь, C1-2алкил или двухвалентный радикал формулы
-CH2-CH= (а) или -CH= (b);
Z2 представляет собой прямую связь, C1-2алкил или двухвалентный радикал формулы
-CH2-CH= (а) или -CH= (b);
R1 представляет собой водород, гало, циано, амино, фенил, гидрокси, C1-4алкилоксикарбонил, -O-(C=O)-C1-4алкил, гидроксикарбонил, NR3R4 или C1-4алкил, в котором указанный C1-4алкил или -O-(C=O)-C1-4алкил являются необязательно замещенными одним или несколькими заместителями, выбранными из гало, гидроксикарбонила, фенила, C1-4алкилокси или NR5R6 или R1 представляет собой C1-4алкилокси, необязательно замещенный одним или несколькими заместителями, выбранными из гало, гидроксикарбонила, фенила, C1-4алкилокси или NR7R8;
R2 представляет собой водород, гало, C1-4алкил или C1-4алкилокси;
R3 и R4, каждый независимо, представляют собой водород, C1-4алкил или C1-4алкилкарбонил;
R5 и R6, каждый независимо, представляют собой водород, C1-4алкил или C1-4алкилкарбонил;
R7 и R8, каждый независимо, представляют собой водород, C1-4алкил или C1-4алкилкарбонил;
A представляет собой фенил или моноциклический гетероцикл, выбранный из группы, состоящей из тиофенила, фуранила, оксазолила, тиазолила, имидазолила, изоксазолила, изотиазолила, пирридинила, пиридазинила, пиримидинила и пиперазинила.
В частности, соединения формулы (Ibis), к которым применены одно или несколько нижеследующих ограничений:
(i) X представляет собой С или N;
(ii) Y представляет собой С или N;
(iii) L представляет собой метил или прямую связь;
(iv) Z1 представляет собой прямую связь, C1-2алкил или двухвалентный радикал формулы
-CH2-CH= (а) или -CH= (b);
(v) Z2 представляет собой прямую связь, C1-2алкил или двухвалентный радикал формулы
-CH2-CH= (а) или -CH= (b);
(vi) R1 представляет собой водород, гало, циано, амино, фенил, гидрокси, C1-4алкилоксикарбонил, гидроксикарбонил, NR3R4 или C1-4алкил, замещенный одним или несколькими заместителями, выбранными из гидроксикарбонила, фенила, C1-4алкилокси или NR5R6, в частности R1 представляет собой водород, гало, амино или гидрокси; даже более конкретно фтор, амино или гидроксил;
(vii) R2 представляет собой водород, гало, C1-4алкил или C1-4алкилокси; в частности R2 представляет собой водород, гало или C1-4алкилокси;
(viii) R3 и R4, каждый независимо, представляет собой водород, C1-4алкил или C1-4алкилкарбонил;
(ix) R5 и R6, каждый независимо, представляют собой водород, C1-4алкил или C1-4алкилкарбонил;
(x) A представляет собой фенил или моноциклический гетероцикл, выбранный из группы, состоящей из тиофенила, фуранила, оксазолила, тиазолила, имидазолила, изоксазолила, изотиазолила, пирридинила, пиридазинила, пиримидинила и пиперазинила; в частности, A представляет собой фенил или моноциклический гетероцикл, выбранный из группы, состоящей из пиридинила и тиофенила.
Следующий аспект настоящего изобретения касается применения любого из соединений упомянутой выше группы соединений в качестве лекарственного средства. В частности, для лечения или предупреждении патологий, связанных с избыточным образованием кортизола, таких как ожирение, диабет, сердечно-сосудистые заболевания, связанные с ожирением, стресс и глаукома.
PCT Международная заявка на патент WO 2004/089416 показывает преимущества комбинированной терапии, включающей введение ингибитора 11β-HSD1 и гипотензивного средства при лечении, например, инсулинрезистентности, дислипидемии, ожирения и гипертензии, в частности для лечения гипертензии. Соответственно целью настоящего изобретения является обеспечение любым соединением из упомянутой выше группы соединений для комбинированной терапии с гипотензивным средством, таким, как например, алпренолол, атенолол, тимолол, пиндолол, пропранолол, метопролол, бисопрололфумерат, эсмолол, ацебутелол, ацебутолол, бетаксолол, селипролол, небиволол, тертатолол, окспренолол, амузолалул, карведилол, лабеталол, S-атенолол, OPC-1085, квинаприл, лизиноприл, эналаприл, каптоприл, беназеприл, периндоприл, трандолаприл, фозиноприл, рамиприл, цилазаприл, делаприл, имидаприл, моэксиприл, спираприл, темокаприл, зофеноприл, S-5590, фазидотрил, Hoechst-Marion Roussel: 100240 (EP00481522), омапатрилат, гемопатрилат и GW-660511, нифедипин, фелодипин, никардипин, израдипин, нимодипин, дилтиазем, амлодипин, нитрендипин, верапамил, ласидипин, леракандипин, аранидипин, цилиндипин, клевидипин, азелнидипин, барнидипин, эфонодипин, иазидипин, иэмилдипин, иэркандипин, манидипин, нилвадипин, пранидипин, фурнидипин, доксазосин, урапидил, празосин, теразосин, буназосин и OPC-28326, бендрофлуметазид, хлорталидон, гидрохлортиазид и клопамид, буметанид, фуросемид, тораземид, амилорид, спиронолактон, ABT-546, амбризетан, антразентан, SB-234551, CI-1034, S-0139, YM-598, босентан, J-104133, алискирен, OPC-21268, толваптан, SR-121463, OPC-31260, Незиритид, ирбезартан, кандесартансилексетил, лозартан, валсартан, телмисартан, эпросартан, кандесартан, CL-329167, иосартан, олмесартан, пратосартан, TA-606, YM-358, фенолдопам, кетансерин, нафтопидил, N-0861, FK-352, KT2-962, экадотрил, LP-805, MYD-37, ноломирол, омакор, трепростинил, берапрост, экрапрост, PST-2238, KR-30450, PMD-3117, Индапамиды, CGRP-униген, стимуляторы гуанилатциклазы, гидралазины, метиидопа, докарпамин, моксонидин, Ко-Апровел и Мондо-Биотех-811. Указанное изобретение предоставляет собой фармацевтическую композицию, которая содержит комбинацию ингибитора 11β-HSD1 по настоящему изобретению и гипотензивного средства.
PCT Международная заявка на патент WO 2004/089415 обеспечивает преимущество комбинированной терапии, которая включает введение ингибитора 11β-HSD1 и агониста глюкокортикоидного рецептора для снижения нежелательных побочных эффектов, происходящих в процессе проведения терапии, использующей агонист глюкокортикоидного рецептора, и для лечения некоторых форм рака, заболеваний и расстройств, включающих воспалительный компонент. В частности, при снижении неблагоприятных воздействий терапии, использующей агонист глюкокортикоидного рецептора, при симптомах заболевания Кушинга, синдрома Кушинга, аллергических воспалительных заболеваний, неблагоприятных воздействий при лечении расстройств респираторной системы с помощью агониста глюкокортикоидного рецептора, неблагоприятных воздействий при лечении с помощью агониста глюкокортикоидного рецептора воспалительного заболевания пищеварительного тракта; неблагоприятных воздействий при лечении расстройства иммунной системы, соединительной ткани и суставов, используя агонист глюкокортикоидного рецептора; неблагоприятных воздействий от лечения эндокринологических заболеваний с помощью агониста глюкокортикоидного рецептора; неблагоприятных воздействий от лечения гематологических заболеваний с помощью агониста глюкокортикоидного рецептора; неблагоприятных воздействий от лечения рака с помощью агониста глюкокортикоидного рецептора, тошноты, вызванной применением химиотерапии, неблагоприятных воздействий, вызванных лечением заболеваний мышц и места нейромышечного соединения агонистом глюкокортикоидного рецептора; неблагоприятных воздействий лечения агонистом глюкокортикоидного рецептора при хирургическом вмешательстве, трансплантации; неблагоприятных воздействий, вызванных лечением агонистом глюкокортикоидного рецептора абсцесса головного мозга, тошноты/рвоты, инфекций, гиперкальцемии, гиперплазии надпочечника, аутоиммунного гепатита, заболевания спинного мозга, мешковидных аневризм.
Примерами симптомов, при которых комбинация соединения 11β-HSD1 по настоящему изобретению с агонистами глюкокортикоидного рецептора может оказаться полезной, являются нижеследующие симптомы: заболевание Кушинга, синдром Кушинга, астма, атопический дерматит, муковисцидоз, эмфизема, бронхит, гиперчувствительность, пневмонит, эозинофильная пневмония, пневмофиброз, болезнь Крона, неспецифический язвенный колит, рeактивный артрит, ревматоидный артрит, синдром Шегрена, системная красная волчанка, волчаночный нефрит, пурпура Геноха-Шенлейна, грануломатоз Вегенера, височный артерит, системный склероз, васкулит, саркоидоз, дерматомиозит-полимиозит, пузырчатка обыкновенная, гипертиреоз, гипоальдостеронизм, гипопитуитаризм, гемолитическая анемия, тромбоцитопения, пароксизмальная ночная гемоглобинурия, неопластическое сдавливание спинного мозга, опухоли головного мозга, острый лимфобластный лейкоз, болезнь Ходжинкина, тошнота, вызванная применением химиотерапии, тяжелая псевдопаралитическая миастения, наследственные миопатии, мышечная дистрофия Дюшенна, травма, послеоперационный стресс, операционный стресс, трансплантация почек, трансплантация печени, трансплантация легких, трансплантация панкреатического островка, трансплантация стволовых клеток крови, трансплантация костного мозга, трансплантация сердца, трансплантация надпочечника, трансплантация трахеи, трансплантация кишечника, трансплантация роговицы, пересадка кожи, кератопластика, имплантация хрусталика, абсцесс головного мозга, тошнота/рвота, инфекции, гиперкальцемия, гиперплазия надпочечников, аутоиммунный гепатит, заболевания спинного мозга и мешковидные аневризмы. Соответственно объектом настоящего изобретения является обеспечение любого из упомянутой выше группы соединений для комбинированной терапии с агонистом глюкокортикоидного рецептора, так же как фармацевтические препараты, содержащие указанную комбинацию соединения по настоящему изобретению с агонистом глюкокортикоидного рецептора. Агонист глюкокортикоидного рецептора, например, выбирают из группы, состоящей из: бетаметазона, дексаметазона, гидрокортизона, метилпреднизолона, преднизолона, преднизона, белкометазона, бутиксикорта, клобетазола, флунисолид, флукатизона (и аналогов), мометазона, триамцинолонацетонида, триамцинолонгексацетонида GW-685698, NXC-1015, NXC-1020, NXC-1021, NS-126, P-4112, P-4114, RU-24858 and T-25 series.
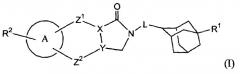
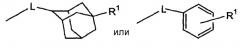
Чтобы упростить представление соединений формулы (I), группу
в дальнейшем будут обозначать как -D.
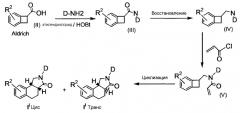
Производные "изогнутого" трициклического адамантиламида по настоящему изобретению, в дальнейшем обозначаемые как соединения формулы (Ii), обычно получают путем конденсирования на первой стадии коммерчески доступной бензоциклобутанкарбоновой кислоты (II) соответствующим амином в условиях, известных в данной области техники (схема 1). Затем полученный таким образом амид (III) восстанавливают, используя, например, алюмогидрид лития или борандиметилсульфидный комплекс, чтобы получить амин формулы (IV). В результате указанный амин ацилируют акроилхлоридом с последующей реакцией циклизации, следуя известным процедурам в данной области техники, таким, как например, нагревание амида (V) в толуоле при 190°C, для получения смеси производных цис- и транс-изомеров "изогнутого" трициклического адамантиламида по настоящему изобретению:
СХЕМА 1
где R2 обозначает то же, что и для соединений формулы (I), описанных ранее.
Для получения стереоизомеров производных "изогнутого" трициклического адамантиламида формулы (Ii), указанную ранее, коммерчески доступную бензоциклобутанкарбоновую кислоту (II) конденсируют аллил-2-адамантиламином (VI) для получения амида общей формулы (VII), который при электроциклическом замыкании цикла дает производные "изогнутого" трициклического адамантиламида формулы (Ii) (схема 2):
СХЕМА 2
где R1 и R2 обозначают то же, что и для соединений формулы (I), описанной ранее. Эти соединения формулы (I), в которых X представляет собой N, в дальнейшем обозначаемые как мочевины формулы (Iii), обычно получают по реакционным схемам 3 и 4, приведенным далее. В первом альтернативном варианте мочевины получают, исходя из коммерчески доступной BОК (бензилоксикарбонил)-защищенной тетрагидрохинолин-3-карбоновой кислоты (оба энантиомера); реакция с аминоадамантаном и восстановление амида давали диамин формулы (VIII). Последующая циклизация согласно процедурам, известным в данной области техники, дала циклические мочевины формулы (Iiii):
СХЕМА 3
Во втором альтернативном варианте производные мочевины получают по известным в данной области техники методикам, путем сочетания коммерчески доступных хинолин-2-карбоновых кислот или изохинолин-1-карбоновых кислот с соответствующим амином для получения соответствующего амида формулы (IX). Селективное гидрирование пиридинового цикла дало тетрагидро(изо)хинолинацетамиды (X), которые восстанавливали, используя, например, BH3 .DMS (борандиметилсульфидный комплекс) в толуоле для получения диаминов общей формулы (XI). Последующая циклизация, использующая, например, карбонилдиимидазол (CDI), дала циклические мочевины формулы (Iiii):
СХЕМА 4
где R2 обозначает то же, что и для соединений формулы (I), описанной ранее,
-A-A- представляет собой -N-СН2- или -CH2-N- и -A=A- представляет собой -N=CH- или -CH=N-.
В случаях, когда замещенные изохинолин-1-карбоновые кислоты не были коммерчески доступны, замещенные трициклические производные получали, исходя из фенетиламинов (XII) и этилхлорформата (схема 5). Полученный карбамат подвергали циклизации, используя способы, известные в данной области техники, такие как, например, модифицированная реакция Бишлера-Напиральского (Larsen, Robert D., et al., A модифицированный Bischler-Napieralski procedure for the synthesis of 3-aryl-3,4-dihydroisoquinolines., Journal of Organic Chemistry (1991), 56(21), 6034-8.), с получением защищенной по аминогруппе тетрагидроизохинолин-l-карбоновой кислоты формулы (X'). Следующий синтез замещенных трициклических производных осуществляют, как показано на реакционной схеме 4, приведенной выше:
СХЕМА 5
Производные "линейного" трициклического адамантиламида формулы (IiV) могут быть получены по реакционным схемам 6 и 7, приведенным далее. По первому альтернативному варианту производные "линейного" трициклического адамантиламида получают исходя из арил- или гетероарилзамещенной акриловой кислоты или хлорида кислоты (ацилхлорида) (XIII). Реакция с соответствующим амином дает амид формулы (XIV), который при электроциклическом замыкании цикла в условиях, известных в данной области техники, например в толуоле при 220°C, дает трициклическую систему формулы (IiV):
СХЕМА 6
где A и R2 обозначают то же, что и в соединениях формулы (I), приведенных ранее.
Во втором альтернативном варианте производные "линейного" трициклического адамантиламида формулы (IiV), где A представляет собой фенил, Y представляет собой N, могут быть получены путем сочетания группы D, защищенной по аминогруппе, или L-фенилаланина с соответствующим амином с получением α-аминоамида формулы (XV); см., например, реакционные условия, описанные в J.Org.Chem. 2002, 67, 8224. Снятие защиты с последующей конденсацией по Mannich бензотриазолом и формальдегидом дает промежуточное соединение формулы (XVI). Электроциклическое замыкание цикла дает производные "линейного" трициклического адамантиламида формулы (IiV):
СХЕМА 7
Следующие примеры синтеза соединений формулы (I), использующие любой из упомянутых выше методов синтеза, приведены в экспериментальной части, приведенной далее.
Если необходимо или желательно, в любом порядке могут быть осуществлены любые одна или несколько нижеследующих стадий:
(i) удаление любой остающейся защитной группы(групп);
(ii) превращение соединения формулы (I) или его защищенной формы в следующее соединение формулы (I) или его защищенную форму;
(iii) превращение соединения формулы (I) или его защищенной формы в N-оксид, соль, четвертичный амин или сольват соединения формулы (I) или его защищенной формы;
(iv) превращение N-оксида, соли, четвертичного амина или сольвата соединения формулы (I) или его защищенной формы в соединение формула (I) или его защищенную форму;
(v) превращение N-оксида, соли, четвертичного амина или сольвата соединения формулы (I) или его защищенной формы в еще один N-оксид, фармацевтически приемлемую аддитивную соль, четвертичный амин или сольват соединения формулы (I) или его защищенной формы;
(vi) в том случае, когда соединение формулы (I) получают в виде смеси (R) и (S) энантиомеров, разделение смеси с получением желательного энантиомера.
Как будет понятно специалистам в данной области техники, в способах, описанных выше, может оказаться необходимой блокировка защитными группами функциональ