Способ определения а- и в-аллелей гена каппа-казеина крупного рогатого скота методом тетрапраймерной пцр
Иллюстрации
Показать всеИзобретение относится к области молекулярной генетики и селекции крупного рогатого скота. Способ включает подготовку пробы нуклеиновой кислоты, проведение полимеразной цепной реакции с использованием двух внутренних аллельспецифичных праймеров и двух внешних праймеров. При этом внутренние праймеры характеризуются отсутствием в 3-й позиции с 3'-конца нуклеотида, негомологичного последовательностям соответствующих цепей ДНК гена каппа-казеина, кроме того, обратный внешний праймер casR обладает большей специфичностью за счет отжига его в экзоне 4 гена CSN3, а в качестве ДНК полимеразы используют KlenTaq ДНК-полимеразу, что обеспечивает амплификацию А- и В-аллельных фрагментов, размеры которых составляют соответственно 122 п.н. и 174 п.н., а также амплификацию фрагмента гена каппа-казеина размером 250 п.н., который позволяет контролировать эффективность проводимой реакции. Способ позволяет повысить специфичность ПЦР. 1 табл., 1 ил.
Реферат
Изобретение относится к области молекулярной генетики и селекции крупного рогатого скота, а именно к типированию животных по A- и B-аллелям гена каппа-казеина (CSN3) методом тетрапраймерной ПЦР с целью выявления перспективных животных в отношении качества молока для производства сыра. Определение аллельного состояния экзона 4 гена CSN3 имеет важное практическое значение, поскольку известно об ассоциации частоты B-аллеля этого гена с высоким качеством казеиновой мицеллы, образующейся при створаживании молока (Schaar et al., 1984, 1985; Robitaille 1995, Zadworny and Kuchnlein, 1990), что важно для получения сыров высокого качества. Поэтому тестирование КРС на наличие B-аллеля гена CSN3 входит в перечень генетических исследований, проводимых по MAS (marker assistant selection)-селекции и является необходимым при оценке молочного потенциала животных.
Существует ряд способов выявления А- и B-аллельного состояния гена CSN3. Все они основаны на применении полимеразной цепной реакции. В ПЦР-ПДРФ методе (1) ПЦР сочетается с рестрикционным анализом амплифицированного фрагмента соответствующими эндонуклеазами рестрикции (способ 1, Шайхаев и др., 1991; Сулимова и др., 2006, 2007; Ялуга В.Л. и др., 2008). В методе аллель-специфичной ПЦР, описанном Renaville, Robert и др. (Renaville, Robert et al., 2005) А- и B-аллели идентифицируют с помощью аллель-специфичных ДНК-зондов, меченных флюорофорами (способ 2). Оба способа являются адекватными и надежными для определения А- и B-аллельного состояния гена CSN3, но не лишены недостатков, связанных, прежде всего, с высокой стоимостью используемых реактивов и оборудования в способе 2, а в случае применения метода ПЦР-ПДРФ (1) - многостадийностью и трудоемкостью процесса анализа, токсичностью реагентов, используемых на отдельных этапах. Последнее касается применения акриламида при приготовлении полиакриламидного геля для электрофоретического разделения фрагментов, полученных в реакции амплификации соответствующего района гена каппа-казеина (экзон 4).
Существует способ (3) проведения стандартной аллельспецифичной ПЦР для выявления А и B-аллелей гена CSN3 (Вафин P.P., 2006). Типирование аллелей осуществляется путем использования двух пар специфичных праймеров: "B-F-hs" и "B-R-hs" (SEQ ID NO 1 - 5'-cccccGTGAGCCTACAAGTACACCTACCAT-3' и SEQ ID NO 2 - 5'-сСсссGАТGТСТССТТАGАGТАТТТАGАСС-3'), а также "A-F-hs" и "А-R-hs" (SEQ ID NO 3 - 5'-gggggCTGTTCACACACAAAAACAGTAAAG-3' и SEQ ID NO 4 - 5'-gggGGGTGCCTAACCTTATACAGCCTTTCG-3' (приложение 1). Все используемые аллель-специфичные праймеры имеют 5'-некомплементарные участки длиной 3-5 нуклеотидов, отмеченные в перечисленных выше последовательностях строчными буквами. Каждая пара праймеров инициирует амплификацию соответственно В- и А-аллелей гена CSN3, которым соответствуют фрагменты размером 156 п.н. и 242 п.н. Недостатком данного способа может являться не совсем удачный выбор места отжига праймеров для определения A-аллеля гена CSN3. Они гомологичны последовательности интрона 5 с 798 п.н. по 822 п.н. и с 1005 п.н. по 1034 п.н., соответственно "A-F-hs" и "A-R-hs". Учитывая более высокую скорость эволюции интронов по сравнению с экзонами, можно говорить о меньшей надежности системы анализа A-аллеля гена CSN3 по сравнению с B-аллелем. К тому же из описания изобретения не ясно, на выборке какого объема была проведена апробация предложенной системы и ДНК животных какой породы тестировали, также непонятно, осуществлялся ли параллельный контроль другими методами.
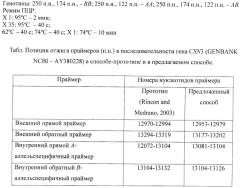
Способ (4), предложенный авторами Rincon и Medrano (Rincon G. and Medrano J.F., 2003) и рассматриваемый в качестве прототипа нашего способа, основан на проведении "tetra-primer ARMS-PCR". Его особенностью является использование четырех праймеров, двух внутренних аллель-специфичных: SEQ ID NO 5 - 5'-AGTAAGAGAGCACTGTAGCTACTCTAGAGGA-3' (для A-аллеля) и: SEQ ID NO 6 - 5'-AGGTGGGCTCTCAATAACTTCTGGAGGAG-3' (для B-аллеля), и двух внешних праймеров: прямого - SEQ ID NO 7 - 5'-ATCATTTATGGCCATTCCACCAAAG-3' и обратного - SEQ ID NO 8 - GCCCATTTCGCCTTCTCTGTAACAGA-3' (приложение 1), причем внутренние праймеры содержат в -2 позиции (3-й позиции) с 3'-конца "mismatch"-нуклеотиды, что повышает специфичность отжига праймеров. Результатом "tetra-primer ARMS-PCR" является амплификация двух аллельспецифичных фрагментов (соответственно, А- и B-аллели: 245 п.н. и 164 п.н.) и одного генспецифичного, размером 350 п.н.. Предложенная система является удобной, современной и не трудоемкой, однако и она имеет некоторые недостатки. Одним из них является последовательность обратного внешнего праймера (SEQ ID NO 8 (приложение 1)), гомологичного последовательности интрона 5 гена каппа-казеина, которая эволюционирует с большей скоростью по сравнению с последовательностью экзона 4, что может отразиться на специфичности данного праймера. К тому же метод "tetra-primer ARMS-PCR" (4) не прошел апробацию на российских породах. Учитывая отмеченное, нельзя быть полностью уверенными в универсальности и возможности его использования для тестирования российских пород.
Таким образом, задачу создания универсальной, надежной, экономически выгодной и безопасной для исследователя методики выявления А- и B-аллелей гена CSN3 нельзя считать до конца решенной.
Задача нашего изобретения - создание эффективного и универсального способа определения А- и B-аллелей гена каппа-казеина (CSN3) крупного рогатого скота для использования в животноводстве и селекции.
Сущность изобретения - определение А- и B-аллелей гена каппа-казеина (CSN3) крупного рогатого скота методом тетрапраймерной ПЦР с использованием строго гомологичных последовательностей экзона 4 гена CSN3: двух внутренних аллель-специфичных праймеров
(casFA: SEQ ID NO 9 - 5'-GAGCACTGTAGCTACTCTAGAAGA-3'-A-allele - 24 п.н.,
casRB: SEQ ID NO 10 - 5'-GCTCTCAGTAACTTCTGGAGAAG-3'-B-allele - 23 п.н.) и двух внешних праймеров
(casF: SEQ ID NO 11 - 5'-CACCCACACCCACATTTATCATTTATG-3' - 27 п.н.,
casR: SEQ ID NO 12 - 5'-CGTTGTCTTCTTTGATGTCTCCTTAG-3' - 26 п.н.) (приложение 1). Каждый внешний праймер в сочетании с соответствующим ему внутренним праймером (casFA-casR и casF-casRB) инициирует амплификацию аллельспецифичных фрагментов (А- и B-аллели соответственно, 122 п.н. и 174 п.н.). Дополнительно к этому, внешние праймеры (casF-casR) инициируют амплификацию фрагмента (250 п.н.), являющегося внутренним контролем ингибирования ПЦР, поскольку фрагмент гена CSN3 амплифицируется независимо от аллельного состояния гена. Последовательности всех праймеров являются полностью гомологичными последовательности экзона 4 гена CSN3, что определяет их высокую специфичность. Праймеры сконструированы таким образом, что фланкируемые ими фрагменты имеют достаточные размеры и могут быть легко разделены методом электрофореза в 2% агарозном геле, что исключает использование полиакриламидного геля, при приготовлении которого применяют токсическое вещество - акриламид (способ 1). Исключение из анализа стадии рестрикции значительно ускоряет типирование аллелей и удешевляет его. Наша система анализа аллельного состояния гена CSN3, как и способ 4, основана на детекции значимой нуклеотидной замены А-С в положении 13104 гена, соответствующей 416-й нуклеотидной позиции в экзоне 4 (A/N: AY380228), которая приводит к замене в белковом продукте аминокислоты Thr на Ile в 136 положении полипептидной цепи, в то время как в способе 3 A-аллель тестируют по нуклеотидной замене в положении 13510 последовательности гена (822 позиция интрона 5 гена), что может привести к неточности при выявлении A-аллеля.
От прототипа (способ 4) предложенный способ отличается: более коротким размером аллельспецифичных праймеров, отсутствием в -2 позиции (3-ей позиции) с 3'-конца "mismatch"-нуклеотида в последовательности аллельспецифичных праймеров, гомологией обратного внешнего праймера casR последовательности экзона 4 гена CSN3, а не интрона. К тому же в предложенном способе используются иные параметры ПЦР: в противоположность "touchdown"-режиму со снижением через каждые два цикла температуры отжига на 1°C с 64°C до 60°C проводится стандартная смена циклов ПЦР с фиксированной температурой отжига праймеров в течение всех циклов, равной 62°C.
Использование всех четырех праймеров, гомологичных экзону 4, повышает специфичность предложенной системы и делает ее более универсальной. Кроме того, применение в противоположность Taq-ДНК-полимеразе, Klentaq ДНК-полимеразы, не имеющей 3'-5'-экзонуклеазной активности (proofreeding), также повышает специфичность ПЦР.
Способ осуществляют с использованием программируемого термоциклера "Терцик" (фирма "ДНК-Технология", Россия) при соблюдении оптимального режима амплификации: х1: 95°C - 2 мин; х35: 95°C - 40 с; 62°C - 40 с; 74°C - 40 с; x1: 74°C - 10 мин и состава ПЦР-смеси: в объеме 20 мкл содержится 60 mM Tris-HCL (pH 8,8), 2,5 mM MgCl2, 20 mM KCL, 15 mM (NH4)2SO4, 10 mM меркаптоэтанола, 0,1% тритона Х-100; 0,2 mM дНТФ, 10 ед. Klentaq ДНК-полимеразы (или используют набор реагентов "GenPakR PCR Core" (IsoGene lab., Москва, Россия)), 40 нг ДНК, выделенной из лейкоцитов или цельной крови КРС (набор реагентов DIAtom™ DNA Prep (IsoGene lab., Москва, Россия); два внутренних аллельспецифичных и два внешних праймера. Концентрация внутренних и внешних праймеров составляет соответственно: 0,5 mkM. Внутренние праймеры имеют следующий состав: casFA: SEQ ID NO 9 - 5'-GAGCACTGTAGCTACTCTAGAAGA-3' - 24 п.н. (A-аллель специфичный) и casRB: SEQ ID NO 10 - 5'-GCTCTCAGTAACTTCTGGAGAAG-3' - 23 п.н. (B-аллель специфичный). Последовательность внешних праймеров следующая: casF: SEQ ID NO 11 - 5'-CACCCACACCCACATTTATCATTTATG-3' - 27 п.н. и casR: SEQ ID NO 12 - 5'-CGTTGTCTTCTTTGATGTCTCCTTAG-3' - 26 п.н.
Детекцию полученных продуктов амплификации осуществляют методом гельэлектрофореза в 2% агарозном геле, приготовленном на 1-кратном ТАЕ-буфере следующего состава: 0,04 М трис-ацетета, 0,02 М ЭДТА, pH 8,0, 0,5 мкг/мл бромистого этидия. Используют буфер для нанесения - водный раствор, содержащий 0,25% бромфенолового синего и 40% (вес или объем) сахарозы, разведенный при нанесении с ПЦР-продуктом в 6 раз. Горизонтальный электрофорез проводят при напряжении электрического тока 10 В/см в течение 40 мин в камере "SE-1" ("Helicon" Россия) с применением источника постоянного тока "PowerPack Basic" (Bio-Rad, США). Фоторегистрацию результата электрофореза проводят на УФ-трансиллюминаторе "УВТ-1" (312 нм), с помощью фотодокументирующей системы "ViTran-1" (Biokom, Россия).
При обработке результатов необходимо руководствоваться следующим: наличие трех полос размером 250 п.н. (внутренний контроль), 174 п.н. (аллель В) и 122 п.н. (аллель А) указывает на гетерозиготный генотип; наличие двух полос размером 250 п.н. (внутренний контроль) и 174 п.н. (аллель В) указывает на гомозиготный генотип ВВ; наличие двух полос размером 250 п.н. (внутренний контроль) и 122 п.н. (аллель А) - на гомозиготный генотип АА.
Пример 1
Предложенный способ был апробирован на выборках коров российских пород: калмыцкой и бестужевской, ранее генотипированных на наличие В- и А-аллелей гена CSN3 ПЦР-ПДРФ методом (Шайхаев и др., 1991; Сулимова и др., 2006,2007).
Ниже приведены технические результаты применения предложенного способа в виде фотографий электрофоретического разделения продуктов амплификации в 2%-ном агарозном геле на рисунке (приложение 2). Они позволяют точно и однозначно определять генотипы животных, что может найти применение в селекции и животноводстве.
Заключение
В результате апробации предложенного способа определения А- и B-аллелей гена каппа-казеина крупного рогатого скота, проведенной на образцах крови коров калмыцкой и бестужевской пород КРС, получен обеспечиваемый заявленным способом технический результат, а именно, продемонстрирована возможность генотипирования КРС по А- и В-аллелям гена CSN3 методом тетрапраймерной ПЦР с использованием разработанных праймеров в оптимизированных условиях полимеразной цепной реакции.
Таким образом, убедительно продемонстрировано, что для проведения массовой диагностики КРС на присутствие А- и В-аллелей гена CSN3 наиболее доступным, эффективным и универсальным является предложенный способ определения А- и В-аллелей гена каппа-казеина крупного рогатого скота методом тетрапраймерной ПЦР.
Способ определения А- и В-аллелей гена каппа-казеина у крупного рогатого скота методом тетрапраймерной ПЦР, включающий подготовку пробы нуклеиновой кислоты, проведение полимеразной цепной реакции с использованием двух внутренних аллель-специфичных праймеров и двух внешних праймеров, отличающийся тем, что используемые в ПЦР праймеры имеют следующие нуклеотидные последовательности: внешние - casF 5'-CACCCACACCCACATTTATCATTTATG-3' и casR 5'-CGTTGTCTTCTTTGATGTCTCCTTAG-3', внутренний А-аллель-специфичный - casRA 5'-GAGCACTGTAGCTACTCTAGAAGA-3' и внутренний В-аллель-специфичный casRB: 5'-GCTCTCAGTAACTTCTGGAGAAG-3', причем внутренние праймеры характеризуются отсутствием в 3-ей позиции с 3'-конца нуклеотида негомологичного последовательностям соответствующих цепей ДНК гена каппа-казеина, кроме того большей специфичностью обратного внешнего праймера casR, за счет отжига его в экзоне 4 гена CSN3, а также использованием в качестве ДНК-полимеразы KlenTaq ДНК-полимеразы и следующими параметрами режима ПЦР: х1: 95°С - 2 мин; х35: 95°С - 40 с; 62°С - 40 с; 74°С - 40 с; х1: 74°С - 10 мин, что обеспечивает амплификацию А-аллель-специфичного фрагмента, размером 122 п.н., В-аллель-специфического фрагмента, размером 174 п.н. и фрагмента внутреннего контроля специфичности реакции, размером 250 п.н., при этом гетерозиготному генотипу АВ соответствуют ПЦР-продукты, размером 250 п.н., 174 п.н. и 122 п.н., гомозиготному генотипу ВВ - размером 250 п.н. и 174 п.н., гомозиготному генотипу АА - размером 250 п.н. и 122 п.н.