Циклопропилпиперидиновые ингибиторы транспортера глицина
Иллюстрации
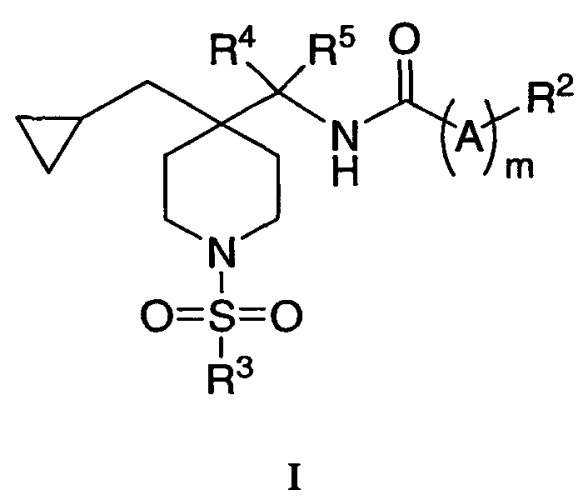
Показать всеИзобретение относится к новым соединениям формулы I:
где R2 выбирается из группы, состоящей из (1) фенила, который является замещенным R2a, R2b и R2c, (2) фуранил, (3) С3-6циклоалкила; R2a, R2b и R2c являются независимо выбранными из группы, состоящей из (1) водорода, (2) галогена, (3) -C1-6алкила, который является незамещенным или замещенным (а) 1-6 атомами галогена, (4) -NR10R11, где R10 и R11 являются водородом; R3 представляет собой C1-6алкил или С3-6циклоалкил, который является независимо незамещенным или замещенным 1-6 атомами галогена; R4 и R5 являются водородом и m равно нулю, R2 присоединяется непосредственно к карбонилу и к его фармацевтически приемлемым солям.
Изобретение также относится к соединениям, которые выбираются из группы, а также к фармацевтической композиции.
Технический результат - получение новых биологически активных соединений, которые обладают активностью в качестве ингибиторов транспортера глицина GlyT1. 3 н. и 7 з.п. ф-лы, 1 табл.
Реферат
Шизофрения представляет собой истощающее психиатрическое расстройство, характеризуемое сочетанием отрицательных (уплощенный аффект, синдром похмелья, ангедония) и положительных (паранойя, галлюцинации, бредовые идеи) симптомов, а также заметными когнитивными дефицитами. Хотя этиология шизофрении в настоящее время является неизвестной, заболевание, видимо, вызывается сложным взаимодействием биологических факторов, факторов окружающей среды и генетических факторов. Более 40 лет назад было обнаружено, что фенциклидин (PCP) вызывает у людей психотическое состояние, которое очень похоже на то, которое наблюдается у шизофренических пациентов. Обнаружение того, что главный способ действия PCP заключается в том, что он представляет собой неконкурентный антагонист N-метил-D-аспартатного (NMDA) субтипа ионотропного рецептора глутамата, стимулировало ряд исследований, которые привели к разработке модели шизофрении, связанной с гипофункцией рецептора NMDA (Jentsch J.D. and Roth R.H., 1999 Neuropsychopharmacology, 20: 201).
Быстрая глутаматергическая нейротрансмиссия в центральной нервной системе млекопитающих опосредуется, прежде всего, возбудительным глутаматом аминокислоты, действующим на ионотропные рецепторы глутамата (iGluR). iGluR состоят из трех главных подклассов, включая субтипы рецепторов α-амино-3-гидрокси-5-метил-4-изоксазолпропионовой кислоты (AMPA), каината и NMDA (Hollmann M. and Heinemann S., 1994, Annu. Rev. Neurosci. 17: 31). Эти три подкласса представляют собой мультимерные катионные каналы, регулируемые лигандами, которые открываются в ответ на связывание глутамата, вызывая деполяризующий возбудительный постсинаптический ток. Молекулярное клонирование показало, что семейство рецепторов NMDA состоит из двух первичных субъединиц, NR1 и NR2. В дополнение к этому недавно была описана новая ингибиторная субъединица, которая регулируется эволюционно, называемая NR3. Высокий уровень молекулярного разнообразия существует в каждом множестве субъединиц. В настоящее время клонирован только один ген субъединицы NR1; однако альтернативное сплайсирование гена NR1 может давать восемь различных субъединиц. В противоположность этому, 4 гена были клонированы для субъединицы NR2 (NR2A, NR2B, NR2C и NR2D), некоторые из которых демонстрируют альтернативное сплайсирование (Hollmann M. and Heinemann S., 1994, Annu. Rev. Neurosci. 17:31). Это множество субъединиц образует гетеромерные ионные каналы, зависимые от глутамата. Хотя точная стехиометрия субъединиц встречающегося в природе рецептора остается неизвестной, субъединицы, как NR1, так и NR2, требуются для экспрессии функционально активных комплексов рецептор-канал в системах экспрессии млекопитающих. Активирование рецептора NMDA требует связывания как глутамата, так и глицина (Johnson JW и Ascher P., 1987, Nature 325: 529). Интересно, что сайты связывания для этих двух ко-агонистов существуют на отдельных субъединицах, как определяется посредством исследования сайт-направленного мутагенеза (Laube B., Hirai H., Sturgess M., Betz H. and Kuhse J., 1997, Neuron 18: 493). На субъединицах NR2A и NR2B карман связывания для глутамата формируется посредством взаимодействий между N-окончанием рецептора и внеклеточными петлями. Аналогичные эксперименты помещают сайт связывания глицина в гомологичной области субъединицы NR1 (Kuryatov A., Laube B., Betz H. and Kuhse J., 1994, Neuron 12: 1291). В зависимости от реальной композиции субъединицы глутамат и глицин активируют рецептор NMDA при значениях EC50 в диапазоне от высоких наномолярных до низких микромолярных пределов. В дополнение к этому, пора рецептора NMDA непроницаема для магния. При нормальных условиях покоя внеклеточный магний может связываться с сайтом внутри поры и осуществлять магниевую блокаду канала. Эта магниевая блокада придает сильную зависимость от напряжения каналу, которая дает возможность рецептору NMDA действовать как детектору совпадений, требующему связывания глутамата, глицина и осуществления постсинаптической деполяризации перед прохождением тока. Особенный интерес представляет обнаружение того, что психотомиметические лекарственные средства MK-801, PCP и кетамин, все, действуют в качестве блокаторов открытых каналов рецептора NMDA посредством связывания с сайтом, который перекрывается с сайтом связывания магния. Очевидно, что богатое разнообразие субъединиц рецептора NMDA и регуляторных сайтов обеспечивает сложный ассортимент физиологически и фармакологически различных гетеромерных рецепторов, делающих рецептор NMDA идеальной мишенью для создания новых терапевтических соединений.
Рецептор NMDA играет критическую роль во множестве нейрофизиологических явлений, включая, но не ограничиваясь этим, синаптическую пластичность, познание, внимание и память (Bliss T. and Collingridge W., 1993, Nature 361: 31; Morris RGM et al., 1986, Nature 319: 774). Психотомиметические лекарственные средства составляют широкий класс лекарственных средств, включая психомоторные стимуляторы (кокаин, амфетамин), галлюциногены (LSD) и антагонисты рецептора NMDA (PCP, кетамин). Среди них только антагонисты рецептора NMDA, видимо, вызывают стойкое индуцирование положительных, отрицательных и когнитивных симптомов шизофрении. Контролируемые исследования кетамин-индуцированного психоза у страдающих им людей, а также наблюдение симптомов у пациентов, принимающих PCP в качестве рекреационного наркотического средства, дают убедительный список сходных особенностей между психозом, индуцируемым антагонистом рецептора NMDA, и шизофренией (Jentsch J.D. and Roth R.H., 1999 Neuropsychopharmacology, 20: 201). Антагонисты рецепторов NMDA превосходно копируют симптомы шизофрении до такой степени, что их трудно различать в клинике. В дополнение к этому, антагонисты рецептора NMDA могут усиливать симптомы у шизофреников и могут запускать повторное появление симптомов у стабильных пациентов. Наконец, обнаружение того, что ко-агонисты рецептора NMDA, такие как глицин, D-циклосерин и D-серин, дают облегчение у шизофренических пациентов, предположительно говорит о гипофункции рецепторов NMDA при этом расстройстве и показывает, что увеличение активирования рецепторов NMDA может обеспечить терапевтическое преимущество (Leiderman E. et al., 1996, Biol. Psychiatry 39:213, Javitt DC et al., 1994, Am. J. Psychiatry 151:1234, Heresco-Levy U., 2000, Int. J. Neuropsychopharmacol. 3:243, Tsai G. et al., 1998, Biol. Psychiatry 44: 1081). Большое количество исследований на животных моделях поддерживает гипотезу гипофункции NMDA при шизофрении. Последнее поколение мутантных мышей, экспрессирующих только 5% от нормальных уровней субъединиц NR1 NMDA показывают, что это уменьшение количества функциональных рецепторов NMDA индуцирует состояние, очень сходное с тем, которое наблюдается у других животных моделей шизофрении (Mohn AR et al., 1999, Cell 98: 427). Кроме шизофрении, дисфункция глутаматергических путей участвует в ряде болезненных состояний центральной нервной системы человека (CNS), включая, но не ограничиваясь этим, когнитивные дефициты, слабоумие, болезнь Паркинсона, болезнь Альцгеймера и биполярное расстройство.
Функция рецептора NMDA может модулироваться посредством изменения доступности ко-агониста глицина. Этот подход имеет критическое преимущество поддержания зависимого от активности активирования рецептора NMD, поскольку увеличение синаптической концентрации глицина не вызывает активирования рецепторов NMDA в отсутствие глутамата. Поскольку синаптические уровни глутамата четко поддерживаются посредством механизмов переноса с высоким сродством, увеличение активирования глицинового сайта будет только увеличивать компонент NMDA активируемых синапсов. Клинические исследования, при которых высокие дозы глицина вводятся перорально, в качестве дополнения к стандартной нейролептической терапии, показывают улучшение симптомов у пациентов с шизофренией (Javitt et al. Int. J. Neuropsychopharmacol. (2001) 4: 385-391). Одним из способов для повышения уровней синаптического глицина без введения экзогенного глицина заключается в ингибировании его удаления из синапса. Доказательство того, что этот подход был бы полезным при лечении шизофрении, приходит из двойных слепых контролируемых исследований с плацебо, при которых саркозин вводят пациентам, которые страдают от шизофрении, но которые малочувствительны к антипсихотическим лекарственным средствам. Наблюдают полезное воздействие на положительные, отрицательные и когнитивные симптомы, которое указывает на то, что ингибирование повторного потребления глицина представляет собой разумный подход к лечению шизофрении.
Идентифицировано два конкретных транспортера глицина, GlyT1 и GlyT2, и показано, что они принадлежат к зависимому от Na+/Cl- семейству нейротрансмиттерных транспортеров, которые включают таурин, γ-аминомасляную кислоту (GABA), пролин, моноамины и «сиротские» транспортеры (Smith K.E. et al., 1992, Neuron 8: 927; Borowsky B. et al., 1993, Neuron 10: 851; Liu Q.R. et al., 1993, J. Biol. Chem. 268: 22802; Kim KM et al., 1994, Mol. Pharmacol. 45: 608; Morrow J.A. et al., 1998, FEBS Lett. 439: 334; Nelson N., 1998, J. Neurochem. 71: 1785). GlyT1 и GlyT2 выделены из различных видов, и показано, что они имеют только 50% идентичность на уровне аминокислот. Они также имеют различный характер экспрессии в центральной нервной системе млекопитающих, при этом GlyT2 экспрессируется в спинном мозге, стволовой области мозга и мозжечке, а GlyT1 присутствует в этих областях, а также в областях переднего мозга, таких как кортекс, гиппокамп, перегородка и таламус (Smith K.E. et al., 1992, Neuron 8: 927; Borowsky B. et al., 1993, Neuron 10: 851; Liu Q.R. et al., 1993, J. Biol. Chem. 268: 22802). На клеточном уровне GlyT2, как сообщается, экспрессируется глицинергическими нервными окончаниями в спинном мозге крыс, в то время как GlyT1, видимо, преимущественно экспрессируется глиальными клетками (Zafra F. et al., 1995, J. Neurosci. 15: 3952). Эти исследования экспрессии приводят к выводу, что GlyT2 в основном является ответственным за пополнение глицина на глицинергических синапсах, в то время как GlyT1 вовлечен в мониторинг концентрации глицина вблизи от синапсов, экспрессирующих рецептор NMDA. Недавние функциональные исследования на крысах показали, что блокада GlyT1 с помощью сильнодействующего ингибитора (N-[3-(4'-фторфенил)-3-(4'-фенилфенокси)пропил])саркозина (NFPS) повышает активность рецептора NMDA и зависимое от рецептора NMDA долговременное усиление у крыс (Bergeron R. et al., 1998, PNAS USA 95: 15730; Kinney G. et al., 2003, J. Neurosci. 23: 7586). Кроме того, NFPS, как сообщается, усиливает ингибирование перед импульсом у мышей, меру сенсорного управления, которое, как известно, является дефицитным у пациентов с шизофренией (Kinney G. et al., 2003, J. Neurosci. 23: 7586). Эти физиологические воздействия GlyT1 в областях переднего мозга вместе с клиническими сообщениями, показывающими полезные воздействия ингибитора GlyT1 саркозина при улучшении симптомов у пациентов с шизофренией (Tsai and Coyle WO99/52519), показывают, что селективные ингибиторы пополнения GlyT1 представляют собой новый класс антипсихотических лекарственных средств.
Сущность изобретения
Настоящее изобретение относится к соединениям, которые ингибируют транспортер глицина GlyT1 и которые являются полезными при лечении неврологических и психиатрических расстройств, связанных с дисфункцией глутаматергической нейротрансмиссии, и заболеваний, в которые вовлечен транспортер глицина GlyT1.
Подробное описание изобретения
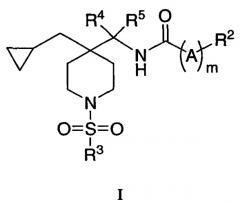
Настоящее изобретение относится к соединению формулы I:
где
R2 выбирается из группы, состоящей из
(1) фенила, который является замещенным R2a, R2b и R2C,
(2) гетероцикла, который является замещенным R2a, R2b и R2C,
(3) C1-8алкила, который является незамещенным или замещенным 1-6 атомами галогена, гидрокси, -NR10R11, фенилом или гетероциклом, где фенил или гетероцикл является замещенным R2a, R2b и R2C,
(4) C3-6циклоалкила, который является незамещенным или замещенным 1-6 атомами галогена, гидрокси или -NR10R11,
где R10 и R11 являются независимо выбранными из
(a) водорода,
(b) -C1-6алкила, который является незамещенным или замещенным гидрокси, 1-6 атомами фтора или -NR12R13, где R12 и R13 являются независимо выбранными из водорода и -C1-6алкила,
(c) -C3-6циклоалкила, который является незамещенным или замещенным гидрокси, 1-6 атомами фтора или -NR12R13,
(d) бензила,
(e) фенила, и
(5) -C1-6алкил-(C3-6циклоалкила), который является незамещенным или замещенным 1-6 атомами галогена, гидрокси или -NR10R11;
R2a, R2b и R2C являются независимо выбранными из группы, состоящей из
(1) водорода,
(2) галогена,
(3) -C1-6алкила, который является незамещенным или замещенным
(a) 1-6 атомами галогена,
(b) фенилом,
(c) C3-6циклоалкилом, или
(d) -NR10R11,
(4) -O-C1-6алкила, который является незамещенным или замещенным 1-6 атомами галогена,
(5) гидрокси,
(6) -SCF3,
(7) -SCHF2,
(8) -SCH3,
(9) -CO2R9,
где R9 является независимо выбранным из
(a) водорода,
(b) -C1-6алкила, который является незамещенным или замещенным 1-6 атомами фтора,
(c) бензила и
(d) фенила,
(10) -CN,
(11) -SO2R9,
(12) -SO2-NR10R11,
(13) -NR10R11,
(14) -CONR10R11 и
(15) -NO2;
R3 представляет собой C1-6алкил или C3-6циклоалкил, которые являются независимо незамещенными или замещенными 1-6 атомами галогена, гидроксилом, -NR10R11 или гетероциклом, который является замещенным R2a, R2b и R2C;
R4 и R5 являются независимо выбранными из группы, состоящей из
(1) водорода и
(2) C1-6алкила, который является незамещенным или замещенным галогеном или гидроксилом, или R4 и R5, взятые вместе, образуют C3-6циклоалкильное кольцо;
A выбирается из группы, состоящей из
(1) -O- и
(2) -NR10-;
m равно нулю или единице, при этом когда m равно нулю, R2 присоединяется непосредственно к карбонилу;
и его фармацевтически приемлемой соли и их индивидуальным энантиомером и диастереомером.
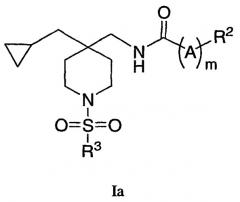
Один из вариантов осуществления настоящего изобретения включает соединения формулы Ia:
где R2, R3, A и m определяются в описании;
или их фармацевтически приемлемую соль, или ее индивидуальный энантиомер или диастереомер.
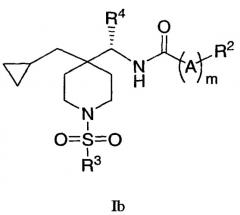
Один из вариантов осуществления настоящего изобретения включает соединения формулы Ib:
где R4 представляет собой C1-6алкил, и R2, R3 и m определяются в описании; или их фармацевтически приемлемую соль, или ее индивидуальный энантиомер или диастереомер.
Один из вариантов осуществления настоящего изобретения включает соединения, где R4 представляет собой C1-3алкил и R5 представляет собой водород или C1-3алкил.
В этом варианте осуществления настоящее изобретение включает соединения, где R4 представляет собой C1-3алкил в (S)-конфигурации и R5 представляет собой водород.
Также в этом варианте осуществления настоящее изобретение включает соединения, где R4 представляет собой метил и R5 представляет собой водород.
Также в этом варианте осуществления настоящее изобретение включает соединения, где R4 представляет собой метил и R5 представляет собой метил.
Также в этом варианте осуществления настоящее изобретение включает соединения, где R4 представляет собой водород и R5 представляет собой водород.
Один из вариантов осуществления настоящего изобретения включает соединения, где m равно нулю.
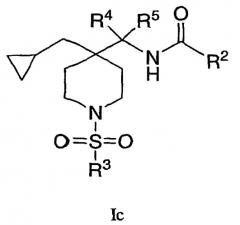
В этом варианте осуществления настоящее изобретение включает соединения формулы Ic:
где R2, R3, R4 и R5 определяются в описании;
или их фармацевтически приемлемую соль, или ее индивидуальный энантиомер или диастереомер.
Кроме того, в этом варианте осуществления настоящее изобретение включает соединения, где R2 выбирается из группы, состоящей из
(1) фенила, который является замещенным R2a, R2b и R2C,
(2) фуранила, который является замещенным R2a, R2b и R2C,
(3) C1-8алкила, который является незамещенным или замещенным 1-6 атомами галогена, фенилом или -NR10R11, где фенил является замещенным R2a, R2b и R2C,
(4) C3-6циклоалкила, который является незамещенным или замещенным 1-6 атомами галогена, гидрокси или -NR10R11, и R2a, R2b и R2C являются независимо выбранными из группы, состоящей из
(1) водорода,
(2) галогена,
(3) -C1-6алкила,
(4) -O-C1-6алкила,
(5) -CF3,
(6) -OCF3,
(7) -OCHF2,
(8) -SCF3,
(9) -SCHF2 и
(10) -NH2.
Кроме того, также в этом варианте осуществления настоящее изобретение включает соединения, где R2 представляет собой фенил или фуранил и R2a, R2b и R2C являются независимо выбранными из группы, состоящей из
(1) водорода,
(2) галогена,
(3) -C1-6алкила,
(4) -O-C1-6алкила,
(5) -CF3,
(6) -OCF3,
(7) -OCHF2,
(8) -SCF3,
(9) -SCHF2 и
(10) -NH2.
Кроме того, также в этом варианте осуществления настоящее изобретение включает соединения, где R2 представляет собой фенил и R2a, R2b и R2C являются независимо выбранными из группы, состоящей из
(1) водорода,
(2) фтора,
(3) хлора,
(4) брома,
(5) -OCH3,
(6) -CF3 и
(7) -NH2.
Кроме того, также в этом варианте осуществления настоящее изобретение направлено на соединения, где R2 представляет собой фенил и R2a, R2b и R2C являются независимо выбранными из группы, состоящей из
(1) водорода,
(2) фтора,
(3) хлора и
(4) брома.
Кроме того, также в этом варианте осуществления настоящее изобретение направлено на соединения, где R2 представляет собой фенил и R2a, R2b и R2C являются независимо выбранными из группы, состоящей из
(1) водорода,
(2) фтора и
(3) хлора.
Кроме того, также в этом варианте осуществления настоящее изобретение направлено на соединения, где R2 представляет собой фенил и R2a, R2b и R2C являются независимо выбранными из группы, состоящей из
(1) водорода и
(2) фтора.
Кроме того, также в этом варианте осуществления настоящее изобретение направлено на соединения, где R2 представляет собой фенил и R2a, R2b и R2C являются независимо выбранными из группы, состоящей из
(1) водорода и
(2) хлора.
Кроме того, также в этом варианте осуществления настоящее изобретение направлено на соединения, где R2 выбирается из группы, состоящей из
(1) 2,3-дифторфенила,
(2) 2,4-дифторфенила,
(3) 2,4-дихлорфенила,
(4) 2-хлор-4-фторфенила,
(5) 2-хлор-6-фторфенила и
(6) 2-хлор-4,6-дифторфенила.
В этом варианте осуществления настоящее изобретение включает соединения формулы Id:
где R2a, R2b, R2C, R3 R4 и R5 определяются выше;
и их фармацевтически приемлемые соли, и их индивидуальные энантиомеры и диастереомеры. В этом варианте осуществления настоящее изобретение включает соединения формулы Id':
где R2a, R2b, R2C и R3 определяются выше;
и их фармацевтически приемлемые соли, и их индивидуальные энантиомеры и диастереомеры.
Также, в этом варианте осуществления настоящее изобретение включает соединения формулы Id":
где R2a, R2b, R2C, R3 и R4 определяются выше;
и их фармацевтически приемлемые соли, и их индивидуальные энантиомеры и диастереомеры.
Один из вариантов осуществления настоящего изобретения включает соединения, где R3 представляет собой C1-6алкил.
В этом варианте осуществления настоящее изобретение включает соединения, где R3 представляет собой -CH2CH3.
В этом варианте осуществления настоящее изобретение включает соединения, где R3 представляет собой -CH2CF3.
В этом варианте осуществления настоящее изобретение включает соединения, где R3 представляет собой -(CH2)2CH3.
В этом варианте осуществления настоящее изобретение включает соединения, где R3 представляет собой -CH(CH3)2.
Также в этом варианте осуществления настоящее изобретение включает соединения, где R3 представляет собой циклопропил.
Конкретные варианты осуществления настоящего изобретения включают соединение, которое выбирается из группы, состоящей из соединений примеров, представленных в описании, и их фармацевтически приемлемых солей, и их индивидуальных энантиомеров и диастереомеров.
Соединения по настоящему изобретению могут содержать один или несколько хиральных центров и могут, таким образом, существовать в виде рацематов и рацемических смесей, отдельных энантиомеров, диастереомерных смесей и индивидуальных диастереомеров. Дополнительные асимметричные центры могут присутствовать в зависимости от природы различных заместителей на молекуле. Каждый такой асимметричный центр будет независимо давать два оптических изомера, и предполагается, что все возможные оптические изомеры и диастереомеры, в смесях и в виде чистых или частично очищенных соединений, включаются в объем настоящего изобретения. Настоящее изобретение, как подразумевается, включает все такие изомерные формы этих соединений. Формула I показывает структуру класса соединений без предпочтительной стереохимии.
Независимые способы синтеза этих диастереомеров или их хроматографическое разделение могут быть достигнуты, как известно в данной области, посредством соответствующей модификации методики, представленной в описании. Их абсолютная стереохимия может быть определена посредством рентгеновской кристаллографии кристаллических продуктов или кристаллических промежуточных соединений, которые дериватизируются, если это необходимо, с помощью реагента, содержащего асимметричный центр с известной абсолютной конфигурацией.
Если это желательно, рацемические смеси соединений могут быть разделены на индивидуальные энантиомеры. Разделение может осуществляться с помощью способов, хорошо известных в данной области, таких как связывание рацемической смеси соединений с энантимерно чистым соединением, с образованием диастереомерной смеси, с последующим разделением индивидуальных диастереомеров с помощью стандартных способов, таких как фракционная кристаллизация или хроматография. Реакция связывания часто представляет собой образование солей с использованием энантимерно чистой кислоты или основания. Диастереомерные производные могут затем преобразовываться в чистые энантиомеры посредством отщепления добавленного хирального остатка. Рацемическая смесь соединений может также разделяться непосредственно с помощью хроматографических способов, использующих хиральные стационарные фазы, эти способы хорошо известны в данной области.
Альтернативно, любой энантиомер соединения может быть получен посредством стереоселективных способов синтеза, с использованием оптически чистых исходных материалов или реагентов известной конфигурации, с помощью способов, хорошо известных в данной области.
Как очевидно специалистам в данной области, галоген, как используется в описании, включает фтор, хлор, бром и йод. Подобным же образом, C1-6, как в C1-6алкиле, определяется для идентификации группы, как имеющей 1, 2, 3, 4, 5 или 6 атомов углерода при линейном или разветвленном расположении, так что C1-8алкил конкретно включает метил, этил, н-пропил, изо-пропил, н-бутил, изо-бутил, трет-бутил, пентил, гексил, гептил и октил. Группа, которая обозначается как являющаяся независимо замещенной заместителями, может независимо замещаться различными количествами таких заместителей. Термин "гетероцикл", как используется в описании, включает как ненасыщенные, так и насыщенные гетероциклические остатки, где ненасыщенные гетероциклические остатки (то есть "гетероарил") включают бензоимидазолил, бензимидазолонил, бензофуранил, бензофуразанил, бензопиразолил, бензотриазолил, бензотиофенил, бензоксазолил, карбазолил, карболинил, циннолинил, фуранил, имидазолил, индолинил, индолил, индолазинил, индазолил, изобензофуранил, изоиндолил, изохинолил, изотиазолил, изоксазолил, нафтпиридинил, оксадиазолил, оксазолил, оксазолин, изоксазолин, оксетанил, пиранил, пиразинил, пиразолил, пиридазинил, пиридопиридинил, пиридазинил, пиридил, пиримидил, пирролил, хиназолинил, хинолил, хиноксалинил, тетрагидропиранил, тетразолил, тетразолопиридил, тиадиазолил, тиазолил, тиенил, триазолил и их N-оксиды, и где насыщенные гетероциклические остатки включают азетидинил, 1,4-диоксанил, гексагидроазепинил, пиперазинил, пиперидинил, пиридин-2-онил, пирролидинил, морфолинил, тетрагидрофуранил, тетрагидротиенил, тиоморфолинил, дигидробензоимидазолил, дигидробензофуранил, дигидробензотиофенил, дигидробензоксазолил, дигидрофуранил, дигидроимидазолил, дигидроиндолил, дигидроизоксазолил, дигидроизотиазолил, дигидрооксадиазолил, дигидрооксазолил, дигидропиразинил, дигидропиразолил, дигидропиридинил, дигидропиримидинил, дигидропирролил, дигидрохинолинил, дигидротетразолил, дигидротиадиазолил, дигидротиазолил, дигидротиенил, дигидротриазолил, дигидроазетидинил и метилендиоксибензоил, и их N-оксиды. В вариантах осуществления настоящего изобретения гетероцикл представляет собой ненасыщенный гетероциклический остаток ("гетероарил"), который представляет собой пиридил или пиримидил, или насыщенный гетероциклический остаток, который представляет собой пиперидин или азетидин.
Термин "фармацевтически приемлемые соли" относится к солям, полученным из фармацевтически приемлемых нетоксичных оснований или кислот, включающих неорганические или органические основания и неорганические или органические кислоты. Соли, полученные из неорганических оснований, включают соли алюминия, аммония, кальция, меди, двухвалентного железа, трехвалентного железа, лития, магния, соли трехвалентного марганца, соли двухвалентного марганца, калия, натрия, цинка и т.п. Особенно предпочтительными являются соли аммония, кальция, магния, калия и натрия. Соли в твердой форме могут существовать с более чем одной кристаллической структурой, и могут также находиться в форме гидратов. Соли, полученные из фармацевтически приемлемых органических нетоксичных оснований, включают соли первичных, вторичных и третичных аминов, замещенных аминов, включая встречающиеся в природе замещенные амины, циклических аминов, и основных ионообменных смол, таких как смолы аргинина, бетаина, кофеина, холина, N,N-дибензилэтилендиамина, диэтиламина, 2-диэтиламиноэтанола, 2-диметиламиноэтанола, этаноламина, этилендиамина, N-этилморфолина, N-этилпиперидина, глюкамина, глюкозаминина, гистидина, гидрабамина, изопропиламина, лизина, метилглюкамина, морфолина, пиперазина, пиперидина, полиамина, прокаина, пуринов, теобромина, триэтиламина, триметиламина, трипропиламина, трометамина и т.п. Когда соединение по настоящему изобретению является основным, соли могут быть получены из фармацевтически приемлемых нетоксичных кислот, включая неорганические и органические кислоты. Такие кислоты включают уксусную, бензолсульфоновую, бензойную, камфорсульфоновую, лимонную, этансульфоновую, фумаровую, глюконовую, глутаминовую, бромистоводородную, хлористоводородную, изетиониновую, молочную, малеиновую, яблочную, миндальную, метансульфоновую, муциновую, азотную, памовую, пантотеновую, фосфорную, янтарную, серную, винную, п-толуолсульфоновую кислоту и т.п. Особенно предпочтительными являются лимонная, бромистоводородная, хлористоводородная, малеиновая, фосфорная, серная, фумаровая и винная кислоты. Будет понятно, что, как используется в описании, ссылки на соединения по настоящему изобретению включают также фармацевтически приемлемые соли.
Примером использования настоящего изобретения является использование соединений, описанных в примерах и в описании. Конкретные соединения в настоящем изобретении включают соединение, которое выбирается из группы, состоящей из соединений, описанных в следующих далее примерах, и их фармацевтически приемлемые соли и их индивидуальные диастереомеры.
Рассматриваемые соединения являются пригодными для использования в способе ингибирования активности транспортера глицина GlyT1 у пациента, такого как млекопитающее, нуждающегося в таком ингибировании, включающем введение эффективного количества соединения. Настоящее изобретение направлено на использование соединений, описанных выше, в качестве ингибиторов глицина активности транспортера GlyT1. Кроме приматов, в частности людей, множество других млекопитающих может лечиться в соответствии со способом по настоящему изобретению.
Настоящее изобретение, кроме того, направлено на способ получения лекарственного средства для ингибирования активности транспортера глицина GlyT1 у людей и животных, включающий объединение соединения по настоящему изобретению с фармацевтическим носителем или разбавителем.
Субъект, которого лечат способом, согласно изобретению, представляет собой, как правило, млекопитающее, предпочтительно человека, мужского или женского пола, у которого является желательным ингибирование активности транспортера глицина GlyT1. Термин "терапевтически эффективное количество" означает количество рассматриваемого соединения, которое будет вызывать биологическую или медицинскую реакцию тканей, системы, животного или человека, которая рассматривается исследователем, ветеринаром, лечащим врачом или другим клиницистом. Ясно, что специалист в данной области может повлиять на неврологические и психиатрические расстройства посредством лечения пациента, в настоящее время страдающего расстройствами, или посредством профилактического лечения пациента, страдающего такими расстройствами, эффективным количеством соединений по настоящему изобретению. Как используется в описании, термины "лечение" и "излечиваемый" относятся ко всем способам, где может наблюдаться замедление, прерывание, приостановка, контроль или прекращение развития неврологических и психиатрических расстройств, описанных ниже, но необязательно указывают на полное устранение всех симптомов расстройств, а также к профилактической терапии для замедления развития или понижению риска отмеченных состояний, в частности, у пациента, который предрасположен к такому заболеванию или расстройству.
Термин "композиция", как используется в описании, охватывает продукт, содержащий указанные ингредиенты в указанных количествах, а также любой продукт, который получают, непосредственно или опосредованно, путем объединения указанных ингредиентов в указанных количествах. Такой термин, по отношению к фармацевтической композиции, охватывает продукт, содержащий активный ингредиент (ингредиенты) и инертный ингредиент (ингредиенты), которые составляют носитель, а также любой продукт, который получают, непосредственно или опосредованно, путем объединения, комплексообразования или агрегации любых двух или более ингредиентов или путем диссоциации одного или нескольких ингредиентов, или путем других типов реакций или взаимодействий одного или нескольких ингредиентов. Соответственно, фармацевтические композиции по настоящему изобретению охватывают любую композицию, приготавливаемую посредством смешивания соединения по настоящему изобретению и фармацевтически приемлемого носителя. Под "фармацевтически приемлемым" подразумевается носитель, разбавитель или наполнитель, который должен быть совместимым со всеми остальными ингредиентами препарата и не вредным для того, кто его принимает.
Термины "введение" и/или "вводимое" соединение должны пониматься как обозначающие доставку соединения по настоящему изобретению или пролекарства соединения по настоящему изобретению индивидууму, нуждающемуся в лечении.
Полезность соединений в соответствии с настоящим изобретением в качестве ингибиторов активности транспортера глицина, в частности активности GlyT1, может демонстрироваться с помощью методологии, известной в данной области. Клетки плацентарной хориокарциномы человека (клетки JAR (ATCC No. HTB-144)), эндогенно экспрессирующие GlyT1, культивируют в 96-луночных сцинтилляционных микропланшетах Cytostar (Amersham Biosciences), в среде RPMI1640, содержащей 10% фетальную сыворотку теленка в присутствии пенициллина (100 мкг/мл) и стрептомицина (100 мкг/мл). Клетки выращивают перед анализом при 37°C в увлажненной атмосфере 5% CO2 в течение 40-48 ч. Культурную среду удаляют из планшета Cytostar и клетки JAR инкубируют с помощью 30 мкл буфера TB1A (120 мМ NaCl, 2 мМ KCl, 1 мМ CaCl2, 1 мМ MgCl2, 10 мМ HEPES, 5 мМ L-аланина, pH 7,5 устанавливают с помощью основания Tris), с соединениями по настоящему изобретению или без них, в течение 1 мин. Затем в каждую лунку добавляют 30 мкл [14C]-глицина, разбавленного TB1A, с получением конечной концентрации 10 мкмоль. После инкубирования при комнатной температуре в течение 3 ч сцинтилляционные микропланшеты Cytostar герметизируют и считают на счетчике сцинтилляций Top Count (Packard). Неспецифическое потребление [l4C]-глицина определяют в присутствии 10 мМ немеченого глицина. Эксперименты по потреблению [14C]-таурина осуществляют в соответствии с таким же протоколом, за исключением того, что для определения неспецифичного потребления используют 10 мМ немеченого таурина. Для определения сильнодействия к клеткам добавляют некоторый диапазон концентраций соединений по настоящему изобретению, а затем фиксированную концентрацию [14C]-глицина. Концентрация настоящего соединения, которая ингибирует половину специфичного потребления [14C]-глицина (величина IC50), определяется по данным анализа с помощью нелинейной подгонки кривой.
В частности, соединения следующих примеров имеют активность при ингибировании специфичного потребления [14C]-глицина при указанном анализе, как правило, при значении IC50, меньшем примерно, чем 10 мкмоль. Предпочтительные соединения по настоящему изобретению имеют активность при ингибировании специфичного потребления [14C]-глицина, при указанном выше анализе, со значением IC50, меньшим, примерно, чем 1 мкмоль. Эти соединения являются селективными относительно потребления [14C]-глицина (посредством GlyT1 в клетках JAR), по сравнению с потреблением [14C]-таурина (посредством транспортера таурина TauT в клетках JAR). Такой результат является показателем собственной активности соединений при использовании в качестве ингибиторов активности транспортера GlyT1.
Рецептор NMDA является центральным в широком диапазоне процессов в CNS и играет роль в различных болезненных состояниях людей или других видов. Влияние транспортера GlyT1 воздействует на локальную концентрацию глицина вокруг рецепторов NMDA. Селективные ингибиторы GlyT1 замедляют удаление глицина из синапса, заставляя расти уровень синаптического глицина. Это, в свою очередь, увеличивает занятость сайта связывания глицина на рецепторе NMDA, что увеличивает активирование рецептора NMDA после высвобождения глутамата из пресинаптического окончания. Поскольку определенное количество глицина является необходимым для эффективного функционирования рецепторов NMDA, любое изменение его локальной концентрации может повлиять на медиируемую NMDA нейротрансмиссию. Изменения медиируемой NMDA нейротрансмиссии присутствуют при определенных невропсихиатрических расстройствах, таких как слабоумие, депрессия и психозы, например шизофрения, и при расстройствах обучения и памяти, например при расстройствах дефицита внимания и аутизма.
Соединения по настоящему изобретению используются при лечении различных неврологических и психиатрических расстройств, связанных с дисфункцией глутаматергической нейротрансмиссии, включая одно или несколько из следующих далее состояний или заболеваний: шизофрению или психоз, включая шизофрению (параноидальную, дезорганизованную, кататоническую или недифференцированную), шизофреноподобное расстройство, шизоаффективное расстройство, бредовое расстройство, преходящее психотическое расстройство, разделяемое психотическое расстройство,