Способ приготовления лекарственного препарата, основанный на увеличении сродства активных агентов к поверхностям кристаллических микрочастиц
Иллюстрации
Показать всеИзобретение относится к способу адсорбирования активного агента, представляющего собой белок или пептид, на поверхности заранее сформированной кристаллической дикетопиперазиновой микрочастицы, который включает стадию модифицирования химического потенциала активного агента, которое предусматривает энергетически благоприятное взаимодействие между активным агентом и дикетопиперазиновой микрочастицей и не включает удаление растворителя, и стадию адсорбирования активного агента на поверхности заранее сформированной кристаллической дикетопиперазиновой микрочастицы. Модифицирование химического потенциала включает изменение условий раствора путем добавления модификатора активного агента к раствору. Изобретение направлено на увеличение адсорбции активного агента на поверхности микрочастицы со снижением его тенденции оставаться в растворе. 2 н. и 29 з.п. ф-лы, 17 ил.
Реферат
Перекрестная ссылка на родственные заявки
Настоящая заявка испрашивает преимущества на основании 35 USC §119(e) по предварительной заявке США серийный №60/717524, поданной 14 сентября 2005, и предварительной заявке США серийный №60/744882, поданной 14 апреля 2006, все содержание которых приведено здесь в качестве ссылки в полном объеме.
Область техники, к которой относится изобретение
Настоящее изобретение относится к приготовлениям лекарственных препаратов и, в частности, относится к способам. Более определенно, оно раскрывает прикрепление или адсорбирование активных агентов на поверхности кристаллических микрочастиц.
Уровень техники
Доставка терапевтических средств является главной проблемой. Пероральное введение является одним из самых распространенных и предпочтительных путей доставки вследствие легкости введения, соблюдения схемы лечения и сниженной стоимости. Однако неудобства этого пути включают низкую или непостоянную эффективность и неэффективную адсорбцию лекарства. Это особенно очевидно, когда доставляемое соединение является нестабильным при условиях, с которыми оно сталкивается в желудочно-кишечном тракте. В данной области техники было разработано множество покрытий и способов заключения в оболочку, но только немногие являются эффективными в решении этого вопроса. Однако имеются терапевтические соединения, которые имеют тенденцию быть менее активными в условиях желудочно-кишечного тракта и которые нужно вводить в более высоких дозировках для их адсорбции в кровоток в эффективном количестве.
Широкий диапазон систем для приготовления лекарственных препаратов был разработан для решения проблемы оптимальной доставки лекарственного препарата и основывается на включении лекарственного препарата в матрицу, которая действует как переносчик. Факторы, которые учитывают при приготовлении лекарственного препарата, включают условия, при которых система должна быть нетоксичной и нереактивной с доставляемым лекарственным препаратом, экономичной в изготовлении, сформированной из легко доступных компонентов и постоянной относительно окончательного состава и физических характеристик, включая стабильность и скорость высвобождения. Также предпочтительно, чтобы система для доставки лекарственного препарата была сформирована из материалов, легко выводимых из организма с помощью нормальных физиологических процессов.
Прогресс в микротехнологии помог разработать улучшенные композиции лекарственных препаратов. Однако, несмотря на эти достижения, все еще сохраняется потребность в области техники для устойчивых композиций лекарственных препаратов, имеющих долгосрочную эффективность и оптимальную адсорбцию при введении в качестве фармацевтического препарата, особенно с помощью легочных средств. Один подход к устранению этого дефицита состоит в том, чтобы нацелиться на структурные характеристики/свойства активного агента, которые стимулировали бы его адсорбцию на поверхности микрочастицы и уменьшали бы его тенденцию оставаться в растворе.
Сущность изобретения
Предоставляются способы прикрепления, покрытия или адсорбирования активного агента на поверхности кристаллической микрочастицы. В большинстве случаев микрочастицы покрывают активным агентом с помощью модифицирования системы, включающей микрочастицы и такой растворенный активный агент, что активный агент имеет большее сродство к поверхности микрочастицы, чем к тому, чтобы остаться в растворе. В особенности, настоящее изобретение стремится дополнительно стимулировать адсорбцию активного агента на поверхности микрочастицы с помощью модифицирования/использования свойств активного агента под влиянием множества условий в растворе.
Таким образом, в настоящем изобретении предоставляется способ стимуляции фиксации активного агента к заранее сформированной кристаллической микрочастице в суспензии, включающий стадии: I) модифицирование химического потенциала активного агента, где изменение предусматривает энергетически благоприятное взаимодействие между активным агентом и микрочастицей, независимое от удаления растворителя; и II) адсорбирование активного агента на поверхности микрочастицы.
В конкретных вариантах осуществления настоящего изобретения модифицирование химического потенциала включает модифицирование структуры, гибкости, жесткости, растворимости или стабильности активного агента, индивидуально или в комбинации. Модифицирование химического потенциала активного агента включает изменение состояния раствора. Изменение состояний раствора включает добавление модификатора активного агента к раствору.
В конкретных вариантах осуществления модификатор активного агента отбирают из группы, состоящей из солей, сурфактантов, ионов, осмолитов, спиртов, хаотропов, космотропов, кислот, оснований и органических растворителей. В одном варианте осуществления соль является хлоридом натрия.
В еще одном варианте осуществления настоящего изобретения способ дополнительно включает стадию растворения активного агента в жидкой фазе суспензии микрочастиц и изменение pH жидкой фазы. В одном аспекте стадия растворения активного агента в жидкой фазе относится к растворению твердой частицы. В другом аспекте стадия растворения активного агента относится к добавлению концентрированного раствора активного агента.
В другом варианте осуществления настоящего изобретения модификатор активного агента улучшает структурную стабильность активного агента.
В еще одном варианте осуществления настоящего изобретения активный агент является белком, пептидом, полипептидом, маленькой молекулой или молекулой нуклеиновой кислоты. В другом варианте осуществления настоящего изобретения активный агент отбирают из группы, состоящей из инсулина, грелина, гормона роста и паратгормона (PTH). Активный агент может включать антитело или фрагмент антитела. В различных аспектах изобретения антитело может распознавать ассоциированный с заболеванием антиген, включая, без ограничения, опухоль-ассоциированный антиген или инфекционный антиген, связанный с патогенным микроорганизмом.
В еще одном варианте осуществления настоящего изобретения маленькая молекула является ионизируемой молекулой или гидрофобной молекулой, такой как циклоспорин А, но не ограниченной им.
В другом варианте осуществления настоящего изобретения модифицирование химического потенциала активного агента включает модуляцию одного или более энергетически благоприятных взаимодействий, таких как, но не ограниченных ими, электростатические взаимодействия, гидрофобные взаимодействия и/или водород-связывающие взаимодействия между активным агентом и поверхностью микрочастицы. В одном варианте осуществления микрочастица включает дикетопиперазин, такой как фумарил дикетопиперазин, но не ограниченный им.
В еще одном варианте осуществления настоящего изобретения способ дополнительно включает стадию удаления или смены растворителя. Применяемый здесь термин растворитель относится к жидкой среде, в которой "купаются" активный агент и микрочастица. Это не должно интерпретироваться как требование, чтобы все компоненты находились в растворе. Действительно во многих случаях он может использоваться в отношении жидкой среды, в которой суспендируются микрочастицы.
В другом варианте осуществления настоящего изобретения предоставляется способ получения композиции для доставки лекарственного препарата, включающего активный агент и кристаллическую микрочастицу, включающий стадии: обеспечение раствора активного агента, включающего молекулу активного агента; модифицирование химического потенциала активного агента; обеспечение микрочастицы в суспензии или порошке; и комбинирование раствора активного агента с суспензией микрочастиц или порошком. Порошок может быть, например, фильтрован, но не высушен.
В другом варианте осуществления настоящего изобретения процесс модифицирования химического потенциала активного агента предусматривает взаимодействие между активным агентом и микрочастицей. В одном варианте осуществления модифицирование химического потенциала активного агента включает добавление модификатора активного агента к раствору. Такой модификатор активного агента может быть отобран из группы, состоящей из солей, сурфактантов, ионов, осмолитов, спиртов, хаотропов, космотропов, кислоты, основания и органических растворителей. В еще одном варианте осуществления модификатор уменьшает растворимость молекулы активного агента, стимулирует ассоциацию между активным агентом и микрочастицей, такой как частица дикетопиперазина, и/или улучшает структурную стабильность молекулы активного агента.
Краткое описание чертежей
Следующие чертежи являются частью настоящего описания изобретения и включены для дополнительной демонстрации определенных аспектов примеров, раскрытых здесь. Изобретение может быть более понятным, исходя из одного или более чертежей в комбинации с детальным описанием определенных вариантов осуществления, представленным здесь.
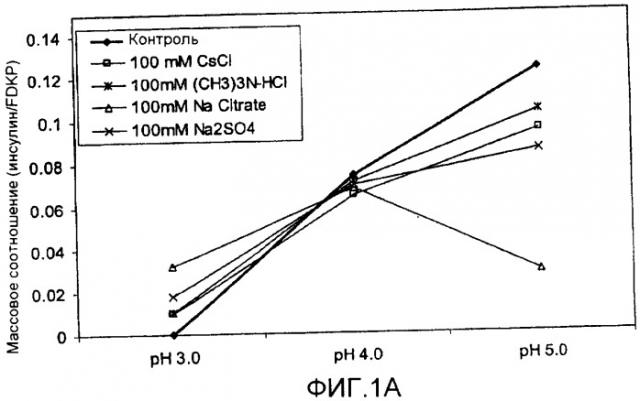
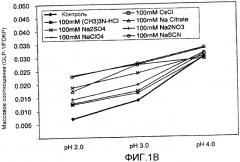
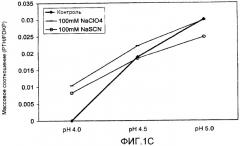
На фиг. 1A-1C представлены воздействия хаотропов и космотропов на кривые загрузки активных агентов на микрочастицы фумарил дикетопиперазина (FDKP) в виде функции pH и 100 ммоль хаотропных/космотропных агентов согласно идеям настоящего изобретения. На фиг.1A представлена загрузка 0,75 мг/мл инсулина на 5 мг/мл микрочастиц FDKP в присутствии хаотропов и космотропов при pH от 3,0 до 5,0. На фиг.1B представлена загрузка 0,25 мг/мл глюкагонподобного пептида 1 (GLP-1) на 5 мг/мл микрочастиц FDKP в присутствии хаотропов и космотропов при pH от 2,0 до 4,0. На фиг.1C представлена загрузка 0,25 мг/мл паратгормона (PTH) на 5 мг/мл микрочастиц FDKP в присутствии сильных хаотропов, NaSCN и NaClO4 при pH между 4,0 и 5,0.
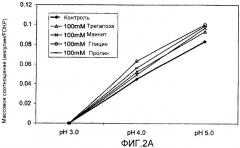
На фиг. 2A-2C представлены воздействия осмолитов на кривые загрузки активных агентов на микрочастицы FDKP в виде функции pH и осмолитов (100 ммоль) согласно идеям настоящего изобретения. На фиг.2A представлена загрузка 0,75 мг/мл инсулина на 5 мг/мл микрочастиц FDKP в присутствии осмолитов при pH от 3,0 до 5,0. На фиг.2B представлена загрузка 0,25 мг/мл GLP-1 на 5 мг/мл микрочастиц FDKP в присутствии осмолитов при pH между 2,0 и 4,0. На фиг.2C представлена загрузка 0,10 мг/мл пептида грелина на 5 мг/мл микрочастиц FDKP в присутствии сильных осмолитов при pH от 4,0 до 5,0.
На фиг. 3A-3D представлены воздействия спиртов на кривые загрузки активных агентов на микрочастицы FDKP в виде функции pH и спиртов согласно идеям настоящего изобретения. На фиг.3A представлена загрузка 0,10 мг/мл грелина на 5 мг/мл микрочастиц FDKP в присутствии гексафлюороизопропанола (HFIP) 5%, 10%, 15% и 20% объем/объем при pH между 2,0 и 4,0. На фиг.3B представлена загрузка 0,10 мг/мл грелина на 5 мг/мл микрочастиц FDKP в присутствии трифлюороэтанола (TFE) 5%, 10%, 15% и 20% объем/объем при pH между 2,0 и 4,0. На фиг.3C и 3D представлена загрузка 0,25 мг/мл GLP-1 на 5 мг/мл микрочастиц FDKP при pH от 2,0 до 5,0 в присутствии HFIP и TFE, соответственно.
На фиг. 4A-4D представлены воздействия соли на кривые загрузки активных агентов на микрочастицы FDKP в виде функции pH и концентрации NaCl согласно идеям настоящего изобретения. На фиг.4A представлена загрузка 0,75 мг/мл инсулина на 5 мг/мл микрочастиц FDKP в присутствии 0-500 ммоль NaCl при pH от 2,0 до 5,0. На фиг.4B представлена загрузка 0,25 мг/мл GLP-1 на 5 мг/мл микрочастиц FDKP в присутствии 0-500 ммоль NaCl при pH от 2,0 до 5,0. На фиг.4C представлена загрузка 0,25 мг/мл пептида PTH на 5 мг/мл микрочастиц FDKP в присутствии 0-1000 ммоль NaCl при pH от 2,0 до 5,0. На фиг.4D представлен анализ вторичной структуры PTH при различных концентрациях соли (20°C). CD короткого ультрафиолетового излучения 4,3 мг/мл PTH при pH 5,8 иллюстрирует, что с увеличением концентрации NaCl вторичная структура пептида принимает более спиральную конформацию.
На фиг. 5A-5B представлена адсорбция гидрофобных молекул на микрочастицы согласно идеям настоящего изобретения. На фиг.5A представлена фиксация циклоспорина А на микрочастицах FDKP с увеличением антирастворителя (вода) до 60%, 80% и 90% концентрации. На фиг.5B представлен процент теоретического максимума загрузки, достигнутого для циклоспорина А в переменных массовых соотношениях циклоспорин A/микрочастицы FDKP в присутствии 90%-ного антирастворителя.
На фиг.6 представлена фармакокинетика отдельной внутривенной инъекции (IV) и легочного вдувания (IS) у крыс с использованием различных массовых соотношений циклоспорин A/микрочастицы FDKP в 90%-ном антирастворителе согласно идеям настоящего изобретения.
Подробное описание изобретения
Здесь описаны способы, пригодные для того, чтобы стабилизировать фармацевтические активные агенты в комбинации с кристаллическими микрочастицами. Получающиеся составы предоставляют устойчивые активные агенты, нанесенные на поверхности кристаллических микрочастиц.
Вещество для нанесения или адсорбирования на кристаллическую микрочастицу упоминается здесь как активный агент. Примеры классов активных агентов включают фармацевтические составы, синтетические соединения и органические макромолекулы, которые имеют терапевтическую, профилактическую и/или диагностическую полезность.
Как правило, большинство активных агентов может быть нанесено или адсорбировано на поверхность кристаллических микрочастиц, включая, но не ограничиваясь ими, органические макромолекулы, нуклеиновые кислоты, синтетические органические соединения, полипептиды, пептиды, белки, полисахариды и другие сахара и липиды. Пептиды, белки и полипептиды - все являются цепями аминокислот, связанных с помощью пептидных связей. Как правило, считают, что пептиды состоят из менее 30 остатков аминокислот, но могут включать больше. Белки являются полимерами, которые могут содержать более 30 остатков аминокислот. Как известно в данной области техники и применяется здесь, термин полипептид может относиться к пептиду, белку или любой другой цепи аминокислот любой длины, содержащей многочисленные пептидные связи, хотя, как правило, содержащей по крайней мере 10 аминокислот. Активные агенты, используемые в наносимой композиции, могут подпадать под разнообразие биологических классов активности, такие как вазоактивные агенты, нейроактивные агенты, гормоны, антикоагулянты, иммуномодулирующие агенты, цитотоксические агенты, антибиотики, антивирусные агенты, антигены и антитела.
Примеры активных агентов, которые могут использоваться в настоящем изобретении, включают без ограничения: гормон роста, антитела и их фрагменты, алкины, циклоспорин (например, циклоспорин A), PPACK (D-фенилаланил-L-пролил-L-аргинин хлорометил кетон), CMFDA (5-хлорометилфлюоресцин диацетат), техасовый красный, клопиогрель, гранулоцитарно-макрофагальный колониестимулирующий фактор (GM-CSF), глюкагонподобный пептид 1 (GLP-1), грелин, паратгормон (PTH), инсулин и аналоги инсулина (например, инсулин аспарт и инсулин) и антитела и их фрагменты, включая, но не ограничиваясь ими, гуманизированные или химерные антитела; F(ab), F(ab)2, или одноцепочечное антитело, в чистом виде или в соединении с другими полипептидами; терапевтические или диагностические моноклональные антитела к раковым антигенам, цитокинам, инфекционным агентам, медиаторам воспаления, гормонам и поверхностным клеточным антигенам. Неограниченные примеры антител к опухолевым антигенам включают анти-SSX-241-49 (синовиальная саркома, X контрольная точка 2), анти-NY-ESO-1 (антиген, ассоциированный с опухолью пищевода), анти-PRAME (предпочтительно экспрессируемый антиген меланомы), анти-PSMA (простат-специфический мембранный антиген), анти-Melan-A (антиген, ассоциированный с меланомой), антитирозиназу (антиген, ассоциированный с меланомой) и анти-MOPC-21 (белок плазмацита миеломы).
Микрочастицы
По существу, термин "микрочастица" относится к частице диаметром приблизительно 0,5-1000 мкм независимо от точной внешней или внутренней структуры. В пределах широкой категории микрочастиц "микросферы" относятся к микрочастицам с однородной сферической формой. Применяемые здесь кристаллические микрочастицы относятся к микрочастицам, которые имеют внутреннюю структуру кристалла, хотя необязательно его наружную форму, и имеют упорядоченное расположение атомов в пространственной решетке. Ионизируемые кристаллические поверхности относятся к кристаллическим микрочастицам, которые имеют дополнительную способность нести электрический заряд. В некоторых вариантах осуществления микрочастица может быть отдельным симметричным кристаллом. В различных предпочтительных вариантах осуществления микрочастица является несимметричной, пористой, имеет доступные для растворенного активного агента внутренние поверхности или включает многочисленные кристаллы в любой комбинации. Такие характеристики будут, как правило, увеличивать площадь поверхности и, таким образом, загрузочную способность. Такие характеристики также могут содействовать выгодным аэродинамическим свойствам, важным, если активный агент нужно доставить с помощью ингаляции сухого порошка, включающего микрочастицы.
Предпочтительно, чтобы химическое вещество, составляющее кристаллическую микрочастицу, являлось обратимо реактивным с доставляемым активным агентом, нетоксичным, а также неметаболизируемым грызунами и людьми. Несмотря на вышесказанное, некоторые уровни токсичности являются допустимыми в зависимости, например, от серьезности состояния, которое лечат, или количества вещества, воздействию которого подвергается пациент. Точно так же не требуется, чтобы вещество было полностью метаболически инертно. Кроме того, кристаллическая структура предпочтительных микрочастиц несущественно разрушается в процессе нанесения или связывания с активным агентом. Состав кристаллической микрочастицы определяет, какими химическими взаимодействиями можно манипулировать, чтобы управлять адсорбцией активного агента на поверхности микрочастицы.
Для формирования кристаллических микрочастиц может использоваться множество веществ. Микрочастицы также имеют поверхности, свойствами которых можно управлять в процессе нанесения, как раскрыто в находящейся в процессе одновременного рассмотрения патентной заявке США No. / (Attorney Docket №51300-00025), зарегистрированной той же самой датой, что и заявка, рассматриваемая в данный момент, и предварительной заявке США серийный № 60/717524, зарегистрированной 14 сентября 2005, которые приведены здесь в качестве ссылки в полном объеме. Показательные материалы, из которых могут быть сформированы кристаллические микрочастицы, включают, но не ограничиваются ими, ароматические аминокислоты или соединения с ограниченной растворимостью в определенном диапазоне pH, такие как дикетопиперазины и сульфаты морфолина.
Как предполагается в настоящем изобретении, одним конкретным примером микрочастиц являются микрочастицы дикетопиперазина (DKP). Обсуждаемые здесь микрочастицы DKP используют для облегчения адсорбции активного агента. Патенты США №№ 5352461 и 5503852, которые приведены здесь в качестве ссылки в полном объеме, описывают систему для доставки лекарственного препарата, основанную на формировании микрочастиц дикетопиперазина (DKP) из производных дикетопиперазина, таких как 3,6-бис[N-фумарил-N-(n-бутил)амино] (также называемый фумарил дикетопиперазин или FDKP; также называемый (E)-3,6-бис[4-(N-карбокси-2-пропенил)амидобутил]-2,5-дикетопиперазин), которые являются стабильными при низком pH и растворяются при pH крови или тонкой кишки. Система, основанная на структурных элементах дикетопиперазина или одной из его альтернативных производных, включающих, но не ограниченных ими, дикетоморфолины и дикетодиоксаны, формирует микрочастицы с желательными распределениями по размерам и диапазонами pH, а также хорошей переносимостью полезной нагрузки. Широкий диапазон стабильных, воспроизводимых характеристик может быть создан с помощью соответствующих манипуляций с замещающими группами. Эти патенты раскрывают осаждение DKP в присутствии активного агента для формирования микрочастиц, включающих активный агент. Дальнейшее подробное описание синтеза, приготовления и применения дикетопиперазинов и микрочастиц дикетопиперазина раскрывается в патентах США 6071497; 6331318; 6428771 и патентных публикациях США №№ 20060040953 и 20060041133, которые приведены здесь в качестве ссылки в полном объеме. Составы, включающие частицы дикетопиперазина, раскрываются в патенте США № 6991779 и патентной публикации США № 20040038865, которые приведены здесь в качестве ссылки в полном объеме.
Другие дикетопиперазины, предполагаемые в настоящем изобретении, включают 3,6-ди(4-аминобутил)-2,5-дикетопиперазин; 3,6-ди(сукцинил-4-аминобутил)-2,5-дикетопиперазин (сукцинил дикетопиперазин или SDKP); 3,6-ди(малеил-4-аминобутил)-2,5-дикетопиперазин; 3,6-ди(цитраконил-4-аминобутил)-2-5-дикетопиперазин; 3,6-ди(глютарил-4-аминобутил)-2,5-дикетопиперазин; 3,6-ди(малонил-4-аминобутил)-2,5-дикетопиперазин; 3,6-ди(оксалил-4-аминобутил)-2,5-дикетопиперазин и их производные. Соли дикетопиперазина также могут использоваться в настоящем изобретении и могут включать, например, фармацевтически приемлемые соли, такие как Na, K, Li, Mg, Ca, аммоний, или моно-, ди- или триалкиламмоний (как полученный из триэтиламина, бутиламина, диэтаноламина, триэтаноламина или пиридинов и т.п.). Соль может быть моно-, ди- или смешанной солью. Соли высшего порядка также предполагаются для дикетопиперазинов, в которых группы R содержат более одной кислотной группы. В других аспектах изобретения основная форма агента может быть смешана с дикетопиперазином для формирования солевой связи между лекарственным препаратом и дикетопиперазином, такой что лекарственный препарат является противокатионом дикетопиперазина. Соли DKP для доставки лекарственного препарата раскрываются в дальнейших деталях в публикации патентной заявки США № 20060040953, приведенной здесь в качестве ссылки в полном объеме.
Патенты США №№ 6444226 и 6652885, которые приведены здесь в качестве ссылки в полном объеме, описывают подготовку и обеспечение микрочастиц DKP в водной суспензии, к которой добавляют раствор активного агента, и затем решающую стадию лиофилизирования суспензии для получения микрочастиц, покрытых активным агентом. Основой этой технологии приготовления является то, что покрытие микрочастицы активным агентом проводят с помощью удаления жидкой среды путем лиофилизации (см. также патент США № 6440463, который приведен здесь в качестве ссылки в полном объеме). В отличие от идей в предшествующей области техники настоящее изобретение предоставляет средства для регулирования ассоциации активного агента с микрочастицей до удаления растворителя. Таким образом, удаление жидкой среды с помощью основных физических способов (например, фильтрация или осаждение) или испаряющих способов (например, лиофилизация или распылительная сушка) может приводить к сопоставимым загрузкам.
Стимуляция адсорбции активных агентов
Адсорбирование активного агента на поверхности кристаллической микрочастицы может приводить к изменению свойств активного агента в растворе или жидкой суспензии при различных состояниях раствора и, таким образом, к стимуляции адсорбции на поверхности микрочастицы и сокращению количества активного агента, остающегося в растворе. Изменение или модификации активного агента могут происходить с применением модификаторов, таких как, но не ограниченных ими, хаотропы и космотропы, соли, органические вещества, такие как, но не ограниченные ими, спирты, осмолиты и сурфактанты. Эти модификаторы могут действовать на активный агент для изменения его химического потенциала и, таким образом, его структуры, гибкости, жесткости или стабильности без химического изменения самого агента. Термин "химический потенциал" является известным любому специалисту в данной области техники. В вариантах осуществления настоящего изобретения "химический потенциал" относится к свободной энергии, необходимой для проведения химической реакции, такой как, например, взаимодействие между активным агентом и растворителем или адсорбция активного агента на микрочастицу. Применяемый здесь термин "энергетически благоприятный" относится к понижению свободных энергетических уровней при состояниях абсорбции активного агента на микрочастице относительно свободного энергетического уровня непокрытой микрочастицы или несвязанного активного агента и/или нерастворимых форм (включая агрегацию или преципитацию) активного агента. Применяемый здесь термин "структура" относится к вторичной структуре молекулы активного агента и включает альфа-спиральную конформацию, бета-складчатые слои или случайный клубок (неупорядоченный) из молекулы активного агента, такой как белок. Кроме того, термин "структура" может также включать третичные и четвертичные структуры молекулы, но не ограничивается этим и может также относиться к самоассоциации, агрегации, мультимеризации, димеризации и т.п. молекулы. Применяемый здесь термин "стабильность" относится к стабилизации или дестабилизации структуры активного агента в присутствии модификатора.
Кроме того, изменение свойств активного агента в растворе или жидкой суспензии способно затрагивать взаимодействия благодаря гидрофобным свойствам, способностям к образованию водородных связей и электростатическим свойствам активного агента и/или микрочастицы.
Гидрофобные взаимодействия являются ассоциациями неполярных групп друг с другом в водных растворах из-за их нерастворимости в воде. Гидрофобные взаимодействия могут затрагивать множество молекулярных процессов, включая, но не ограничиваясь этим, стабилизацию структуры (отдельных молекул, комплексов двух или трех молекул или больших скоплений) и динамические свойства, и вносить существенный вклад в процессы связывания белка с белком и белка с лигандом. Также известно, что эти взаимодействия играют роль в ранних явлениях сворачивания белка и вовлекаются в сложные явления организации и самоорганизации (например, построение мембран).
Водородсвязывающие взаимодействия являются особенно сильными диполь-дипольными силами между молекулами; атом водорода в полярной связи (например, H-F, H-O или H-N) может испытывать силу притяжения с соседней электроотрицательной молекулой или ионом, который имеет неразделенную пару электронов (типично F, O или атом N на другой молекуле). Водородные связи ответственны за уникальные свойства воды и очень важны в организации биологических молекул, особенно во влиянии на структуру белков и ДНК.
Электростатические взаимодействия являются притяжениями между противоположными зарядами или отталкиваниями между подобными зарядами, которые усиливаются с приближением зарядов друг к другу. Электростатические взаимодействия составляют ключевой компонент в понимании взаимодействий между заряженными телами в ионных растворах. Например, стабильность коллоидных частиц, рассеянных в растворителе, можно описать с помощью оценки конкуренции между отталкивающими электростатическими взаимодействиями и притягивающими Ван-дер-Ваальсовыми взаимодействиями. Электростатические взаимодействия также важны для оценки взаимодействия и адгезии между частицами.
Соли
В некоторых вариантах осуществления настоящего изобретения свойства активного агента изменяют с использованием соли, такой как хлорид натрия, но не ограниченной им. Активные агенты, например PTH и GLP-1, подвергаются в присутствии соли значимым структурным изменениям. Как показано в примере 5 (фиг.4D), наличие соли усиливает вторичную структуру PTH с помощью стимуляции большей спиральной конформации пептида. Соли также продемонстрировали действие на структуру GLP-1, как раскрыто в предварительной патентной заявке США серийный № 60/744882, зарегистрированной 14 апреля 2006 и приведенной здесь в качестве ссылки в полном объеме. Кроме того, соли и другие ионные соединения способны или к стабилизации, или к дестабилизации белков и пептидов, особенно когда разница между pH раствора и pl белка или пептида увеличивается с помощью связывания с определенно заряженными остатками (Antosiewiez J, et al., J. Mol. Biol. 238:415-436, 1994).
Хаотропы
В данной области техники известно, что хаотропы являются ионами, которые проявляют слабые взаимодействия с водой и поэтому дестабилизируют молекулы, такие как белки или пептиды. Эти соединения разрушают связанную водородной связью структуру воды и уменьшают ее поверхностное натяжение, таким образом стимулируя большую структурную свободу и денатурацию белков и пептидов. Примеры хаотропов включают, но не ограничиваются ими, NaSCN, (CH3)3N-HCl, Na2NO3 и NaClO4 и хлорид цезия (CsCl).
Космотропы или лиотропы, с другой стороны, являются ионами, которые проявляют сильные взаимодействия с водой и, как правило, стабилизируют макромолекулы, такие как белки и пептиды. Это стабилизирующее воздействие вызывается с помощью упорядочения структуры и увеличения ее поверхностного натяжения. Примеры космотропов включают, но не ограничиваются ими, цитрат натрия (цитрат Na) и сульфат натрия (Na2SO4).
Спирты
Другим классом модификаторов активного агента, используемых в настоящем изобретении, являются спирты. Спирты могут разрушать природную структуру белков и пептидов и также могут стабилизировать и индуцировать α-спиральные конформации в макромолекулах, особенно в пределах неструктурированных белков и полипептидов. Такие спирты могут включать, но не ограничиваются ими, метанол (MeOH), этанол (EtOH), трифлюороэтанол (TFE) и гексафлюороизопропанол (HFIP). Из них TFE и HFIP являются одними из самых сильных спиртов, индуцирующих спиральные преобразования в пептидах и белках (Hirota et al., Protein Sci., 6:416-421; 1997, приведено здесь в качестве ссылки для всего, что относится к спиральным преобразованиям в пептидах и белках). Эти спирты могут затрагивать структуру белков и пептидов посредством их способности нарушать водородсвязывающие свойства растворителя (см. Eggers and Valentine, Protein Sci., 10:250-261; 2001, приведено здесь в качестве ссылки для всего, что относится к воздействию спиртов на структуру белков).
Осмолиты
Другим классом модификаторов, который затрагивает сродство активного агента к микрочастице, являются осмолиты. Специалистам в данной области техники известно, что осмолиты являются маленькими соединениями, которые продуцируются клетками большинства организмов в стрессовых ситуациях (таких как экстремальные температурные колебания, высокое содержание соли в окружающей среде и т.д.) для стабилизации их макромолекул. Они не взаимодействуют с макромолекулой непосредственно, а действуют с помощью изменения растворяющих свойств окружающей среды клетки и, таким образом, их наличие косвенно модифицирует стабильность белков. Эти соединения включают различные полиолы, сахара, полисахариды, органические растворители и различные аминокислоты и их производные. Хотя механизм осмолитов еще должен быть выявлен, предполагается, что эти соединения действуют, вероятно, с помощью повышения химического потенциала денатурированного состояния относительно природного состояния, таким образом увеличивая (позитивную) разницу энергии Гиббса (ΔG) между природными и денатурированными группами (Arakawa and Timasheff, Biochemistry 29:1914-1923;1990).
Как предполагается в настоящем изобретении, осмолиты включают без ограничения гексиленгликоль (Hex-Gly), трегалозу, глицин, полиэтиленгликоль (PEG), триметиламин N-оксид (TMAO), маннит и пролин.
Общее описание способа
В способах по настоящему изобретению по крайней мере три компонента комбинируют в жидкой среде: по крайней мере один активный агент, (заранее сформированные) микрочастицы и по крайней мере один модификатор активного агента, как описанные выше. Компоненты этой системы могут быть скомбинированы в любом порядке. В некоторых вариантах осуществления модификатор и активный агент комбинируют друг с другом перед тем, как эту смесь комбинируют с суспензией микрочастиц. В других вариантах осуществления сначала комбинируют агент и микрочастицы и затем добавляют модификатор. В некоторых вариантах осуществления обеспечивают активный агент или модификатор и комбинируют с другим компонентом или компонентами как раствор. В других вариантах осуществления любой из компонентов можно предоставить в твердой форме и растворить или в случае микрочастиц суспендировать в жидкой среде, содержащей другой из компонентов. Дальнейшие варианты будут очевидны любому специалисту в данной области техники.
Микрочастицы формируют перед тем, как скомбинировать с другими компонентами системы, и они также присутствуют в качестве суспензии. Тем не менее жидкая среда, в которой суспендируются микрочастицы, время от времени упоминается здесь как растворитель. Используемая в способе жидкая среда является чаще всего водной. Однако в некоторых случаях жидкая среда может включать больше органического соединения, например спирта, используемого в качестве модификатора, чем воды.
После объединения всех компонентов системы активный агент будет адсорбироваться на поверхности микрочастицы. Во все более и более предпочтительных вариантах осуществления настоящего изобретения по крайней мере 50, 60, 70, 80, 90, 95% или, по существу, весь активный агент в системе будет адсорбироваться на микрочастицах до 100%. В некоторых вариантах осуществления настоящего изобретения доступная площадь поверхности микрочастиц достаточна для того, чтобы весь адсорбируемый активный агент находился в прямом контакте с поверхностью микрочастицы, то есть покрытие являлось монослоем. Однако необходимо понимать, что могут присутствовать дополнительные взаимодействия. В некоторых случаях, например, самоассоциация активного агента может быть также энергетически предпочтительна, чтобы многочисленные слои активного агента покрывали частицу. Не требуется, чтобы любой из этих слоев являлся сплошным или чтобы толщина покрытия была однородной. Могут быть распознаны две формы самоассоциации: мультимеризация и агрегация. Мультимеризацию характеризуют с помощью специфических межмолекулярных взаимодействий и фиксированной стехиометрии. Агрегацию характеризуют с помощью неспецифических межмолекулярных взаимодействий и неопределенной стехиометрии. Необходимо понимать, что мультимерные активные агенты могут адсорбироваться в мультимерном состоянии или диссоциировать на мономеры или мультимеры более низкого порядка и адсорбироваться на поверхности в таком состоянии. В любом случае, агрегация может содействовать наслаиванию активного агента на микрочастицу.
Нагруженные микрочастицы образуют состав для доставки лекарственного препарата, который может использоваться в разнообразных формах. Частицы можно использовать как порошки в твердых лекарственных формах, таких как таблетки, или заключать в капсулы, или суспендировать в жидком переносчике. Как правило, это потребует смены и/или удаления жидкой среды, в которой происходила загрузка. Это может быть выполнено с помощью любого из разнообразных средств, включая физические способы, такие как, но не ограничиваясь этим, осаждение или фильтрацию, и испаряющие способы, такие как, но не ограничиваясь этим, лиофилизацию или распылительную сушку. Эти методы известны специалистам в данной области техники. В одном варианте осуществления настоящего изобретения растворитель удаляют с помощью распылительной сушки. Способы распылительной сушки микрочастиц дикетопиперазина раскрываются в, например, предварительный патентной заявке США №60/776605, зарегистрированной 22 февраля 2006, приведенной здесь в качестве ссылки для всего, что относится к распылительной сушке микрочастиц дикетопиперазина.
Если загрузка произошла не полностью, то варианты осуществления изобретения с использованием физических способов удаления растворителя будут в основном освобождать неадсорбируемый активный агент, но, например, могут быть пригодными для обеспечения того, чтобы покрытие не превышало пределов монослоя. Наоборот, варианты осуществления с использованием сушки выпариванием для удаления растворителя могут в некоторых случаях осаждать дополнительный активный агент на частицах и таким образом избежать его потери, но вовлеченные адсорбционные взаимодействия