Соединение экстракта какао и способы их получения и применения
Иллюстрации
Показать всеИзобретение относится к области медицины и фармацевтики и касается способа лечения пациента, нуждающегося в лечении NO-модулирующим агентом, путем введения пациенту композиции, содержащей полимерное соединение формулы An, где А представляет мономер формулы (I), и фармакологически приемлемый носитель. Изобретение обеспечивает высокую эффективность лечения. 6 н. и 15 з.п. ф-лы, 235 ил., 17 табл.
Реферат
Делается ссылка на находящиеся на рассмотрении заявки США: №08/709406, поданную 6 сентября 1996 г., 08/631661, поданную 2 апреля 1996 г., и 08/317226, поданную 3 октября 1994 г. (в настоящее время патент США 5554645), и РСТ/US 96/4497, каждая из которых включена в данное описание путем ссылки.
Данное изобретение относится к экстрактам какао и соединениям из них, таким как полифенолы, предпочтительно полифенолы, обогащенные процианидинами. Данное изобретение также относится к способам получения подобных экстрактов и соединений и к их применению, например, в качестве противоопухолевых (антибластомных) агентов, антиоксидантов, ингибиторов ферментативной активности ДНК-топоизомеразы II, модуляторов циклооксигеназы и/или липоксигеназы, модуляторов NO (оксид азота) или NO-синтазы, как нестероидных противовоспалительных агентов, модуляторов апоптоза, модуляторов агрегации тромбоцитов, модуляторов глюкозы в крови или in vitro, антимикробных агентов и ингибиторов окислительного повреждения ДНК.
Полный список всех документов, цитируемых в настоящем описании, приводится в конце описания перед формулой изобретения в разделе "Библиография". Эти документы относятся к области настоящего изобретения, при этом каждый цитируемый документ включен в данное описание путем ссылки.
Полифенолы представляют собой невероятно разнообразную группу соединений (Ferreira et al., 1992), широко распространенную в различных видах растений, некоторые из которых входят в пищевую цепь. В некоторых случаях этот класс соединений имеет важное значение в питании человека. Хотя считается, что некоторые из полифенолов не имеют питательной ценности, интерес к ним растет благодаря тому, что они, как предполагается, могут оказывать благоприятное воздействие на здоровье человека.
Например, исследования на экспериментальных животных показали, что кверцетин (флавоноид) обладает антиканцерогенной активностью (Deshner et al., 1991, and Kato et al., 1983). Показано, что (+)-катехин и (-)-эпикатехин (флаван-3-олы) ингибируют активность обратной транскриптазы вируса лейкоза (Chu et al., 1992). Также показано, что ноботанин (олигомерный гидролизуемый танин) обладает противоопухолевой активностью (Okuda et al., 1992). Также в статистических отчетах сообщается, что смертность от рака желудка значительно ниже в областях Японии, производящих чай. Есть сообщения, что галлат эпигаллокатехина является фармакологически активным веществом, присутствующим в зеленом чае, и ингибирует рост кожных опухолей у мышей (Okuda et al., 1992). Также на модели опухоли у различных животных показано, что эллаговая кислота обладает антиканцерогенной активностью (Bukharta et al., 1992). Наконец, олигомеры проантоцианидина запатентованы Kikoman Corporation для использования в качестве антимутагенов. Действительно, недавно на 202-м Национальном собрании Американского химического общества были представлены доклады, касающиеся областей распространения фенольных соединений в пищевых продуктах и их модуляции развития опухолей на экспериментальных моделях животных (Но et al., 1992; Huang et al., 1992).
Однако ни в одном из этих сообщений не были предложены ни экстракты какао или соединения из них, ни способы получения подобных экстрактов или соединений, или использования экстрактов какао или соединений из них в качестве антибластомных агентов, антиоксидантов, ингибиторов фермента ДНК-топоизомеразы II, модуляторов циклооксигеназы и/или липоксигеназы, модуляторов NO (оксида азота) или NO-синтазы, как нестероидных противовоспалительных агентов, модуляторов апоптоза, модуляторов агрегации тромбоцитов, модуляторов глюкозы в крови и in vitro, антимикробных агентов или ингибиторов окислительного повреждения ДНК.
Так как неферментированные какао-бобы содержат существенное количество полифенолов, авторы настоящего изобретения считают, что подобная активность и возможность использовать экстракты какао, например соединения, присутствующие в какао, могут быть выявлены путем экстрагирования подобных соединений из какао и последующего скрининга данных экстрактов на соответствующую активность. Национальный онкологический институт произвел скрининг различных видов Theobroma и Herrania на противораковую активность в рамках широкой программы по отбору натуральных продуктов. У экстрактов из тканей какао-бобов были обнаружены низкие уровни активности, и работа не была продолжена. Таким образом, исследователи пришли к заключению, что какао и его экстракты не могут использоваться в качестве антибластомных или противораковых средств, и это привело к тому, что специалисты в области противоопухолевой или противораковой терапии отказались от использования какао и его экстрактов для лечения рака.
Поскольку в целях изучения возможности применения полифенолов какао для изготовления ароматизирующих веществ был разработан ряд аналитических методов (Clapperton et al., 1992), настоящие заявители решили применить аналогичные методы к получению образцов для их скрининга на противораковую активность, несмотря на существующее мнение относительно бесполезности использования какао в противоопухолевой или противораковой терапии. Неожиданно и в противовес известному уровню техники, например результатам скрининга, проведенного Национальным онкологическим институтом, авторы настоящего изобретения обнаружили, что полифеноловые экстракты какао, содержащие процианидины, обладают значительным полезным действием в качестве противораковых или антибластомных агентов.
Кроме того, заявители продемонстрировали, что экстракты какао, содержащие процианидины, и соединения из экстрактов какао могут быть использованы в качестве антибластомных агентов, антиоксидантов, ингибиторов ферментативной активности ДНК-топоизомеразы II, модуляторов циклооксигеназы и/или липоксигеназы, модуляторов NO (оксида азота) или NO-синтазы, нестероидных противовоспалительных агентов, модуляторов апоптоза, модуляторов агрегации тромбоцитов, модуляторов глюкозы в крови и in vitro, антимикробных агентов или ингибиторов окислительного повреждения ДНК. Предметом настоящего изобретения являются способы получения экстракта какао и/или соединений из них.
Другим объектом настоящего изобретения является экстракт какао и/или соединения из него.
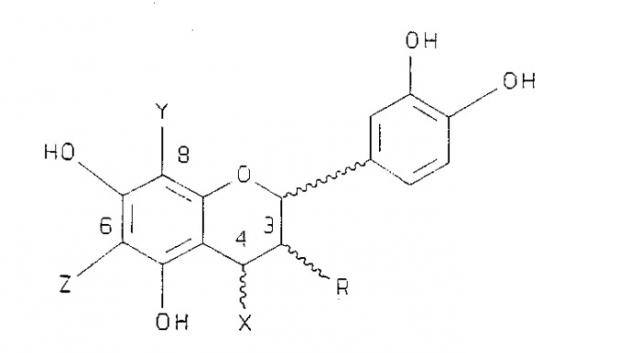
Еще одним объектом настоящего изобретения является полимерное соединение формулы An, где А является мономером, имеющим формулу:
где n представляет целое число от 2 до 18, так чтобы
присутствовала по меньшей мере одна концевая мономерная единица А и множество дополнительных мономерных единиц;
R представляет 3-(α)-ОН, 3-(β)-ОН, 3-(α)-O-caxap или 3-(β)-O-caxap;
связывание между смежными мономерами происходит по положениям 4, 6 или 8,
связывание дополнительных мономерных единиц по положению 4 имеет α или β стереохимию;
X, Y и Z выбраны из группы, состоящей из мономерной единицы А, водорода и сахара, при условии, что по крайней мере одна концевая мономерная единица, связанная с дополнительной мономерной единицей, находится в положении 4, и что Y=Z=водород;
сахар необязательно замещен фенольным остатком в любом положении, например, через сложную эфирную связь,
и фармацевтически приемлемые соли или их производные (включая окисленные продукты).
Еще одним объектом настоящего изобретения является полимерное соединение формулы An, в котором А является мономером, имеющим формулу:
где n представляет целое число от 2 до 18, например 3-18;
R представляет 3-(α)-ОН, 3-(β)-OH, 3-(α)-О-caxap или 3-(β)-O-caxap;
смежные мономеры связываются по положениям 4 путем (4→6) или (4→8);
каждый из X, Y и Z является водородом, сахаром или смежным мономером при условии, что если X и Y являются смежными мономерами, Z представляет собой Н или сахар, и если X и Z являются смежными мономерами, Y представляет собой Н или сахар, и таким образом, чтобы по крайней мере один из двух концевых мономеров, связанных со смежным мономером, находился в положении 4, и необязательно Y=Z=водород;
связывание по положению 4 имеет α или β стереохимию;
сахар необязательно замещен фенольным остатком в любом положении, например, через сложную эфирную связь,
и фармацевтически приемлемые соли или их производные (включая окисленные продукты).
Еще одним объектом изобретения является антиоксидантная композиция.
Еще одним объектом изобретения является способ ингибирования ферментативной активности ДНК-топоизомеразы II.
И еще одним объектом настоящего изобретения является способ лечения опухолей или рака.
Еще одним объектом настоящего изобретения являются противораковые, противоопухолевые или антибластомные композиции.
Еще одним объектом настоящего изобретения является антимикробная композиция.
Еще одним объектом настоящего изобретения является циклооксигеназная и/или липоксигеназная модулирующая композиция.
Еще одним объектом настоящего изобретения является композиция, модулирующая NO или NO-синтазу.
Еще одним объектом настоящего изобретения является нестероидная противовоспалительная композиция.
Еще одним объектом настоящего изобретения является глюкозо-моделирующая композиция в крови и in vitro.
Еще одним объектом настоящего изобретения является способ лечения больных антибластомной, антиоксидантной, антимикробной, модулирующей циклооксигеназу и/или липооксигеназу, или модулирующей NO или NO-синтазу, модулирующей нестероидные противовоспалительные агенты и/или модулирующей глюкозу в крови и in vitro композициями.
Дополнительным объектом настоящего изобретения является композиция и способ ингибирования окислительного повреждения ДНК.
Еще одним дополнительным объектом изобретения является композиция и способы модуляции агрегации тромбоцитов.
Еще одним объектом настоящего изобретения являются композиции и способы модуляции апоптоза.
Еще одним объектом настоящего изобретения является способ получения любой из вышеприведенных композиций.
Еще одним объектом изобретения является набор для применения в вышеперечисленных способах или для получения вышеперечисленных композиций.
Неожиданно было обнаружено, что экстракт какао и композиции из него обладают противоопухолевой, противораковой или антинеопластической активностью или являются антиоксидантом, или обладают способностью ингибировать ферментативную активность ДНК-топоизомеразы II, или являются антимикробным агентом, модулятором циклооксигеназы и/или липоксигеназы, модулятором NO или NO-синтазы, нестероидным противовоспалительным агентом, модулятором апоптоза, модулятором агрегации тромбоцитов или модулятором глюкозы в крови или in vitro, или ингибитором окислительного повреждения ДНК.
В соответствии с этим настоящее изобретение предлагает по существу чистый экстракт какао и соединения из него. Экстракт или соединения предпочтительно содержат полифенол (или полифенолы), такие как полифенол(ы), обогащенный полицианидином(ами) какао, такой как полифенолы, содержащие по меньшей мере один полицианидин какао, выбранный из (-) эпикатехина, (+) катехина, процианидина В-2, олигомеров процианидина от 2 до 18, например 3-18, таких как 2-12 или 3-12, предпочтительно 2-5 или 4-12, более предпочтительно 3-12 и более предпочтительно 5-12, процианидина В-5, процианидина А-2 и процианидина С-1.
Настоящее изобретение также предлагает противоопухолевую, противораковую или антибластомную или антиоксидантную композиции, или композицию, ингибирующую ферментативную активность ДНК-топоизомеразы II, или антимикробную, или модулирующую циклооксигеназу и/или липоксигеназу, или модулирующую NO или NO-синтазу, или композицию, представляющую нестероидный противовоспалительный агент, модулятор апоптоза, модулятор агрегации тромбоцитов или модулятор глюкозы в крови или in vitro, или композицию, являющуюся ингибитором окислительного повреждения ДНК, содержащую, в основном, чистый экстракт какао или соединение из него, или синтетические полифенолы какао, такие как полифенол(ы), обогащенные процианидином(ами), и подходящий носитель, например, приемлемый в фармацевтической, ветеринарной и пищевой отрасли науки. Экстракт или соединения из него предпочтительно содержат процианидин(ы) какао. Экстракт какао или соединения из него предпочтительно получают способом, предусматривающим растирание какао-бобов в порошок, обезжиривание полученного порошка и экстрагирование из этого порошка активных соединений.
Кроме того, настоящее изобретение предлагает способ лечения больных, нуждающихся в лечении противоопухолевым, противораковым или антибластомным агентом, или антиоксидантом, или ингибитором ДНК-топоизомеразы II, или антимикробным агентом, модулятором циклооксигеназы и/или липоксидазы, или модулятором NO или NO-синтазы, или нестероидным противовоспалительным агентом, модулятором апоптоза, модулятором агрегации тромбоцитов или модулятором глюкозы в крови или in vitro, или ингибитором окислительного повреждения ДНК, содержащими эффективное количество в основном чистого экстракта какао или соединения из него, или синтетического полифенола(ов) какао или процианидина(ов) и носитель, например носитель, приемлемый в фармацевтической, ветеринарной и пищевой области. Экстракт какао или соединение из него могут быть процианидином(ами) какао и предпочтительно получаются путем размола зерен какао в порошок, обезжиривания порошка и экстрагирования и очищения активного компонента (или активных компонентов) из порошка.
Кроме того, настоящее изобретение предлагает набор для лечения больных, нуждающихся в лечении противоопухолевым, противораковым или антибластомным агентом, или антиоксидантом, или ингибитором ДНК-топоизомеразы II, или антимикробным агентом, модулятором циклооксигеназы и/или липоксидазы, или модулятором NO или NO-синтазы, или нестероидным противовоспалительным агентом, модулятором апоптоза, модулятором агрегации тромбоцитов или модулятором глюкозы в крови или in vitro, ингибитором окислительного повреждения ДНК, содержащими эффективное количество в основном чистого экстракта какао или соединения из него, или синтетического полифенола(ов) какао или процианидина(ов) и подходящий носитель, например носитель, приемлемый в фармацевтической, ветеринарной и пищевой области, для смешивания с экстрактом или соединением из него, или синтетическим(ими) полифенолом(ами) или процианидином(ами).
Настоящее изобретение предлагает соединения, проиллюстрированные на фиг. 38А-38В и 39А-39АА, причем связи в положениях 4→6 и 4→8 в настоящее время предпочтительны.
Изобретение, кроме того, включает в себя композиции для сохранения и приготовления пищевых продуктов, содержащие соединение изобретения, и способы приготовления или сохранения пищевых продуктов путем добавления в пищу данной композиции.
И, кроме того, изобретение включает ингибитор ДНК-топоизомеразы II, содержащий соединение изобретения и подходящий носитель или разбавитель, и способы лечения больного, нуждающегося в подобном лечении, путем назначения композиции.
Если рассматривать в целом приведенные выше выполнения, включающие экстракты какао, то изобретение также включает такие варианты выполнения, в которых соединение по изобретению используют вместо или в качестве экстрактов какао. Таким образом, изобретение включает наборы, способы и композиции, аналогичные вышеприведенным для экстрактов какао и соединений по изобретению.
Эти и другие объекты и выполнения раскрываются или становятся очевидными из следующего детального описания.
Последующее подробное описание дается со ссылками на прилагаемые чертежи.
Фиг.1 показывает характерную хроматограмму, полученную при фракционировании неочищенных процианидинов какао с помощью гель-проникающей хроматографии;
фиг.2А показывает характерную хроматограмму, полученную с помощью ВЭЖХ с обращенной фазой и показывающую разделение (профиль элюирования) процианидинов какао, экстрагированных из неферментированного какао;
фиг.2В показывает характерное разделение процианидинов какао, экстрагированных из неферментированного какао, с помощью ВЭЖХ с нормальной фазой;
фиг.3 показывает несколько характерных структур процианидина;
фиг.4А-4Е показывают характерные ВЭЖХ хроматограммы пяти фракций, использованных в скрининге на противораковую или антинеопластическую активность;
фиг.5 и 6A-6D показывают дозовую зависимость между экстрактами какао и раковыми клетками ACHN (фиг.5) и РС-3 (фиг.6А-6D) (доля выживших клеток относительно дозы, мкг/мл); М&М2 F4/92, М&МА+Е U12P1, М&МВ+Е Y192P1, М&МС+Е U12P2, M&MD+E U12P2;
фиг.7А-7Н показывают типичную дозовую зависимость между фракциями процианидина какао А, В, С, D, Е, А+В, А+Е и A+D и линией клеток РС-3 (доля выживших клеток относительно дозы, мкг/мл); ММ-1А 0212РЗ, ММ-1 В 0162Р1, ММ-1 С 0122РЗ, ММ-1 D 0122РЗ, ММ-1 Е 0292Р8, ММ-1 А/В 0292Р6, ММ-1 А/Е 0292Р6, ММ-1 A/D 0292P6;
фиг.8А-8Н показывают типичную дозовую зависимость между фракциями процианидина какао А, В, С, D, Е, А+В, В+Е и D+E и клеточной линией носоглоточной KB/HeLa (доля выживших клеток/доза, мкг/мл); ММ-1А 092К3, ММ-1 В 0212К5, ММ-1 С 0162К3, ММ-1 D 0212K5, ММ-1 Е 0292К5, ММ-1 А/В 0292К3, ММ-1 В/Е 0292К4, ММ-1 D/E 0292K5;
фиг.9А-9Н показывают типичную дозовую зависимость между фракциями процианидина какао А, В, С, D, Е, B+D, А+Е и D+E и клеточной линией НСТ-116 (доля выживших клеток/доза, мкг/мл); ММ-1 С 0192Н5, D 019H5, Е 0192Н5, ММ-1 B&D 0262H2, А/Е 0262Н3, ММ-1 D&E 0262H1;
фиг.10А-10Н показывают типичную дозовую зависимость между фракциями процианидина какао А, В, С, D, E, B+D, C+D и А+Е и почечной клеточной линией ACHN (доля выживших клеток/доза, мкг/мл); ММ-1 А 092А5, ММ-1 В 092А5, ММ-1 С 0192А7, ММ-1 D 0192А7, М&М1 Е 0192А7, ММ-1 B&D 0302A6, ММ-1 C&D 0302A6, ММ-1 А&Е 0262А6;
фиг.11А-11Н показывают типичную дозовую зависимость между фракциями процианидина какао А, В, С, D, Е, А+Е, В+Е, и С+Е клеточной линией легких А-549 (доля выживших клеток/доза, мкг/мл); ММ-1 А 019258, ММ-1 В 09256, ММ-1 С 019259, ММ-1 D 019258, ММ-1 Е 019258, А/Е 026254, ММ-1 В&Е 030255, ММ-1 С&Е N6255;
фиг.12А-12Н показывают типичную дозовую зависимость между фракциями процианидина какао А, В, С, D, Е, В+С, C+D и D+E клеточной линией меланомы SK-5 (доля выживших клеток/доза, мкг/мл); ММ-1 A 021S4, ММ-1 В 0212S4, ММ-1 С 0212S4, ММ-1 D 0212S4, ММ-1 Е N32S1, ММ-1 В&С N32S2, ММ-1 C&D N32S3, ММ-1 D&E N32S3;
фиг.13А-13Н показывают типичную дозовую зависимость между фракциями процианидина какао А, В, С, D, Е, В+С, С+Е и D+E клеточной линией молочной железы MCF-7 (доля выживших клеток/доза, мкг/мл); ММ-1 A N22M4, ММ-1 В N22M4, ММ-1 С N22M4, ММ-1 D N22M3, ММ-1 Е 0302М2, ММ-1 В/С 0302М4, ММ-1 С&Е N22M3, ММ-1 D&E N22M3;
фиг.14 показывает типичную дозовую зависимость между процианидином какао (в частности, фракцией D) и клеточной линией CCRF-CEM Т-клеточного лейкоза (клетки/мл относительно дней роста; незакрашенный кружок - контроль, закрашенный кружок - 125 мкг - фракция D, незакрашенный перевернутый треугольник - 250 мкг - фракция D, закрашенный перевернутый треугольник - 500 мкг - фракция D).
фиг.15А показывает сравнение анализов, проведенных с использованием ХТТ и кристаллического фиолетового, на цитотоксичность против клеточных линий рака молочной железы MCF-7 р168, обработанных фракцией D+E (незакрашенный кружок обозначает ХТТ, а закрашенный кружок обозначает кристаллический фиолетовый);
фиг.15В показывает типичную кривую зависимости доза-ответ, построенную для линии клеток молочной железы MDA МВ231, обработанных различными количествами неочищенных полифенолов, полученных из генотипа какао UIT-1 (оптическая плотность (540 нм) - относительно дней; незакрашенный кружок обозначает контроль, закрашенный кружок обозначает носитель, незакрашенный перевернутый треугольник обозначает 250 мкг/мл, закрашенный перевернутый треугольник обозначает 100 мкг/мл, незакрашенный квадрат обозначает 10 мкг/мл; оптическая плотность 2,0 является максимальной для планшет-ридера и необязательно соответствует количеству клеток);
фиг.15С показывает типичную кривую зависимости доза-ответ, построенную для линии клеток рака предстательной железы РС-3, обработанных различными количествами неочищенных полифенолов, полученных из генотипа какао UIT-1 (оптическая плотность (540 нм) - относительно дней; незакрашенный кружок обозначает контроль, закрашенный кружок обозначает носитель, незакрашенный перевернутый треугольник обозначает 250 мкг/мл, закрашенный перевернутый треугольник обозначает 100 мкг/мл, незакрашенный квадрат обозначает 10 мкг/мл);
фиг.15D показывает типичную кривую зависимости доза-ответ, построенную для линии клеток рака молочной железы MCF-7 p168, обработанных различными количествами неочищенных полифенолов, полученных из генотипа какао UIT-1 (оптическая плотность (540 нм) - относительно дней; незакрашенный кружок обозначает контроль, закрашенный кружок обозначает носитель, незакрашенный перевернутый треугольник обозначает 250 мкг/мл, закрашенный перевернутый треугольник обозначает 100 мкг/мл, незакрашенный квадрат обозначает 10 мкг/мл; оптическая плотность 2,0 является максимальной для планшет-ридера и необязательно соответствует количеству клеток);
фиг.15Е показывает типичную кривую доза-ответ, построенную для клеточной линии рака шейки матки Hela, обработанных различными количествами неочищенных полифенолов, полученных из генотипа какао UIT-1 (оптическая плотность (540 нм) - относительно дней; незакрашенный кружок обозначает контроль, закрашенный кружок обозначает носитель, незакрашенный перевернутый треугольник обозначает 250 мкг/мл, закрашенный перевернутый треугольник обозначает 100 мкг/мл, незакрашенный квадрат обозначает 10 мкг/мл; оптическая плотность 2,0 является максимальной для планшет-ридера и необязательно соответствует количеству клеток);
фиг.15F показывает эффект против линии клеток рака шейки матки Hela, обработанных различными фракциями (оптическая плотность (540 нм) - относительно дней; незакрашенный кружок обозначает 100 мкг/мл фракции А-Е, закрашенный кружок обозначает 100 мкг/мл фракции А-С, незакрашенный перевернутый треугольник обозначает 100 мкг/мл фракции D&E; оптическая плотность 2,0 является максимальной для планшет-ридера и необязательно соответствует количеству клеток);
фиг.15G показывает цитотоксический эффект при дозе 100 мкг/мл против линии клеток рака молочной железы SKBR-3, обработанных различными полифеноловыми фракциями какао (оптическая плотность (540 нм) - относительно дней; незакрашенный кружок обозначает фракции А-Е, закрашенный кружок обозначает фракции А-С, незакрашенный перевернутый квадрат обозначает фракции D&E);
Фиг.15Н показывает типичную зависимость доза-ответ между фракцией D+E процианидина какао и клетками Hela (оптическая плотность (540 нм) - относительно дней; незакрашенный кружок обозначает контроль, закрашенный кружок обозначает 100 мкг/мл, незакрашенный перевернутый треугольник обозначает 75 мкг/мл, закрашенный перевернутый треугольник обозначает 50 мкг/мл, незакрашенный квадрат обозначает 25 мкг/мл, закрашенный квадрат обозначает 10 мкг/мл; оптическая плотность 2,0 является максимальной для планшет-ридера и необязательно соответствует количеству клеток);
фиг.15I показывает типичную зависимость доза-ответ между фракцией D+E процианидина какао и клетками SKBR-3 (оптическая плотность (540 нм) - относительно дней; незакрашенный кружок обозначает контроль, закрашенный кружок обозначает 100 мкг/мл, незакрашенный перевернутый треугольник обозначает 75 мкг/мл, закрашенный перевернутый треугольник обозначает 50 мкг/мл, незакрашенный квадрат обозначает 25 мкг/мл, закрашенный квадрат обозначает 10 мкг/мл);
фиг.15J показывает типичную зависимость доза-ответ между фракцией D+E процианидина какао и клетками Hela в анализе, проводимом путем клонирования в мягком агаре (гистограмма; число колоний относительно контроля, 1, 10, 50 и 100 мкг/мл);
фиг.15К показывает ингибирование роста клеток линии Hela, обработанных неочищенными полифеноловыми экстрактами, полученными из восьми различных генотипов какао (% от контроля относительно концентрации, мкг/мл; незакрашенный кружок обозначает С-1, закрашенный кружок представляет С-2, незакрашенный перевернутый треугольник представляет С-3, закрашенный перевернутый треугольник представляет С-4, незакрашенный квадрат представляет С-5, закрашенный квадрат представляет С-6, незакрашенный треугольник представляет С-7, закрашенный треугольник представляет С-8;
C-1=UF-12: сорт культуры Trinitario и описание - неочищенные экстракты полифенолов какао UF-12 (Бразилия) (декофеинированные/детеоброминированные);
C-2=NA-33: сорт культуры = Forastero и описание - неочищенные экстракты полифенолов какао NA-33 (Бразилия) (декофеинированные/детеоброминированные);
C-3=EEG-48: сорт культуры = Forastero и описание - неочищенные экстракты полифенолов какао EEG-48 (Бразилия) (декофеинированные/детеобромированные);
С-4 = неизвестен: сорт культуры = Forastero и описание - неочищенные экстракты неизвестных полифенолов какао (Западная Африка) (декофеинированные/детеоброминированные);
С-5=UF-613: сорт культуры = Trinitario и описание - неочищенные экстракты полифенолов какао UF-613 (Бразилия) (декофеинированные/детеоброминированные);
C-6=ICS-100: сорт культуры = Trinitario (предок Nicaraguan Criollo) и описание - неочищенные экстракты полифенолов какао ICS-100 (Бразилия) (декофеинированные/детеоброминированные);
C-7=ICS-139: сорт культуры = Trinitario (предок Nicaraguan Criollo) и описание - неочищенные экстракты полифенолов какао ICS-139 (Бразилия) (декофеинированные/детеоброминированные);
C-6=UIT-1: сорт культуры = Trinitario и описание - неочищенные экстракты полифенолов какао UIT-1 (Малайзия) (декофеинированные/детеоброминированные);
фиг.15L показывает ингибирование роста клеток линии Hela, обработанных неочищенными экстрактами полифенолов, полученными из ферментированных бобов какао и высушенных бобов какао (во всех случаях проводили стадии ферментации и сушки на солнце; % от контроля относительно концентрации, мкг/мл; незакрашенные кружки представляют фракцию нулевого дня, закрашенный кружок представляет фракцию первого дня, незакрашенный перевернутый треугольник представляет фракцию второго дня, закрашенный перевернутый треугольник представляет фракцию 3 дня, незакрашенный квадрат представляет фракцию 4 дня, закрашенный квадрат представляет фракцию 9 дня);
фиг.15М показывает действие ферментативно окисленных процианидинов какао против клеток линии Hela (дозозависимое действие полифенолов какао, обработанных полифенолоксидазой); % от контроля относительно концентрации; мкг/мл; закрашенный квадрат представляет неочищенный UIT-1 (с кофеином и теобромином), незакрашенный кружок представляет неочищенный UIT-1 (без кофеина и теобромина) и закрашенный кружок представляет неочищенный UIT-1 (катализированный полифенолоксидазой);
фиг.15N показывает характерное разделение объединенных фракций D и Е процианидинов какао с помощью полупрепаративной ВЭЖХ с обращенной фазой;
фиг.15O показывает характерное разделение неочищенного экстракта полифенолов какао с помощью полупрепаративной ВЭЖХ с нормальной фазой;
фиг.16 показывает характерную кривую окисления рацемата для экстракта и фракций полицианидинов какао по сравнению с кривыми, полученными для синтетических антиоксидантов ВНА и ВНТ (условные единицы относительно времени; пунктирная линия и крестики (+) представляют ВНА и ВНТ; * представляет D-E; X представляет неочищенный экстракт; незакрашенные квадраты представляют фракции А-С; незакрашенные ромбы представляют контроль);
фиг.17 показывает типичный агарозный гель, указывающий на ингибирование катализируемой топоизомеразой II декатенации кинетопластной ДНК фракциями процианидинов какао (дорожка 1 содержит 0,5 мкг мономерных колец "маркерной" (М) кинетопластной ДНК; дорожки 2-20 содержат кинетопластную ДНК, которую инкубировали с топоизомеразой II в присутствии 4% ДМСО, но в отсутствие каких-либо процианидинов какао (контроль - С); дорожки 3 и 4 содержат кинетопластную ДНК, которую инкубировали с топоизомеразой II в присутствии 0,5 и 5,0 мкг/мл фракции А процианидинов какао; дорожки 5 и 6 содержат кинетопластную ДНК, которую инкубировали с топоизомеразой II в присутствии 0,5 и 5,0 мкг/мл фракции В процианидинов какао; дорожки 7, 8, 9, 13, 14 и 15 представляют копии кинетопластной ДНК, которые инкубировали в присутствии 0,05, 0,5 и 5,0 мкг/мл фракции D процианидинов какао; дорожки 10, 11, 12, 16, 17 и 18 представляют копии кинетопластной ДНК, которые инкубировали с топоизомеразой II в присутствии 0,05, 0,5 и 5,0 мкг/мл фракции Е процианидинов какао; дорожка 19 представляет копию кинетопластной ДНК, которую инкубировали с топоизомеразой II в присутствии 5,0 мкг/мл фракции Е процианидинов какао);
фиг.18 показывает дозозависимую активность фракции D процианидинов какао против клеточных линий, способных к репарации ДНК, и клеточных линий с недостаточной способностью к репарации ДНК (доля выживших клеток относительно мкг/мл; левый график - клеточная линия xrs-6 с недостаточной способностью к репарации ДНК, ММ-1 D D282X1; правый график - клеточная линия BR1, способная к репарации ДНК, ММ-1 D D282B1);
фиг.19 показывает кривые зависимости "доза-ответ" для сравнения адриамицинрезистентных клеток MCF-7 с родительской клеточной линией MCF-7 р168, обработанной фракцией D+E (% от контроля относительно концентрации, мкг/мл; незакрашенные кружки представляют MCF-7 р168; закрашенные кружки MCF-7 ADR);
фиг.20А и В показывают дозозависимое действие на клетки линий Hela и SKBR-3 при их обработке концентрациями 100 мкг/мл и 25 мкг/мл двадцати фракций, полученных с помощью полупрепаративной ВЭЖХ с нормальной фазой (гистограмма; % от контроля относительно контроля и фракций 1-12);
фиг.21 показывает разделение неочищенных, обогащенных и очищенных пентамеров из экстрактов какао с помощью ВЭЖХ с нормальной фазой;
фиг.22А, В и С показывают MALDI-TOF/MS пентамера, обогащенного процианидинами, фракций А-С и фракций D-E соответственно;
фиг.23А показывает профиль элюирования олигомерных процианидинов, очищенных с помощью модифицированной полупрепаративной ВЭЖХ;
фиг.23В показывает профиль элюирования тримера процианидина, очищенного с помощью модифицированной полупрепаративной ВЭЖХ;
фиг.24А-В показывают структуры с минимальной энергией для всех пентамеров со связью (4→8), основанных на структуре эпикатехина;
фиг.25А показывает относительную флуоресценцию эпикатехина после тиолиза с бензилмеркаптеном;
фиг.25В показывает относительную флуоресценцию катехина после тиолиза с бензилмеркаптеном;
фиг.25С показывает относительную флуоресценцию димеров (В2 и В5) после тиолиза с бензилмеркаптеном;
фиг.26А показывает относительную флуоресценцию димеров после тиолиза;
фиг.26В показывает относительную флуоресценцию В5 димера после тиолиза димера и последующей десульфуризации;
фиг.27А показывает относительный объем опухоли во время лечения на модели голых мышей MDA MB 231 при их обработке пентамером;
фиг.27В показывает относительную кривую выживания обработанных пентамером экспериментальных голых мышей MDA 231;
фиг.28 показывает профиль элюирования при свободном от галогена аналитическом разделении ацетонового экстракта процианидинов, полученного из экстракта какао;
фиг.29 показывает влияние размеров пор стационарной фазы на разделение процианидинов с помощью ВЭЖХ с нормальной фазой;
фиг.30А показывает использование субстрата во время ферментации какао-бобов;
фиг.30В показывает выработку метаболита во время ферментации;
фиг.30D показывает расчеты планшетов во время ферментации какао-бобов;
фиг.30В показывает относительные концентрации каждого компонента в ферментированном растворе какао-бобов;
фиг.31 показывает ацетилхолин-индуцированное расслабление аорты крысы, NO-зависимой и предварительно сокращенной с помощью фенилэфрина;
фиг.32 показывает профили толерантности к глюкозе крови при использовании различных тестируемых смесей;
фиг.33А-В показывают воздействие индометацина на активность СОХ-1 и СОХ-2;
фиг.34А-В показывают корреляцию между уровнем полимеризации и IC50 относительно СОХ-1/СОХ-2 (мкм);
фиг.35 показывает корреляцию между воздействием соединений на активность СОХ-1 и СОХ-2, выраженную в мкм;
фиг.36A-V показывают значения IC50 (мкм) образцов, содержащих процианидины с СОХ-1/СОХ-2;
фиг.37 показывает схему очищения при выделении процианидинов из какао;
фиг.38А-38В показывают предпочтительные структуры пентамеров;
фиг.39А-АА показывают стереохимическую библиотеку пентамеров;
фиг.40А-В показывают 70-минутные градиенты для разделения процианидинов с помощью ВЭЖХ с нормальной фазой, проявленные при УФ-облучении и флуоресценции соответственно;
фиг.41А-В показывают 30-минутные градиенты для разделения процианидов с помощью ВЭЖХ с нормальной фазой, проявленные при УФ-облучении и флуоресцентном исследовании соответственно;
фиг.42 показывает разделение процианидинов с помощью ВЭЖХ с нормальной фазой;
фиг.43А-G показывают CD (круговой дихроизм) спектра димеров, тримеров, тетрамеров, пентамеров, гексамеров, гептамеров и октамеров процианидина соответственно;
фиг.44А показывает структуру и данные 1Н и 13С ЯМР для эпикатехина;
фиг.44В-F показывают спектр APT, COSY, XHCORR, 1Н и 13С ЯМР для эпикатехина;
фиг.45А показывает структуру и данные 1Н и 13С ЯМР для катехина;
фиг.45В-Е показывают спектр 1Н, APT, XHCORR и COSY ЯМР для катехина;
фиг.46А показывает структуру и данные 1Н и 13С ЯМР для В2 димера;
фиг.46В-G показывают спектр 13С, APT, 1H, HMQC и COSY и НОНАНА ЯМР для В2 димера;
фиг.47А показывает структуру и данные 1Н и 13С ЯМР для В5 димера;
фиг.47В-С показывают спектр 1Н, 13С, APT, COSY, HMQC, НОНАНА ЯМР для В5 димера;
фиг.48А-D показывают спектр 1Н, COSY, HMQC и НОНАНА ЯМР для эпикатехин/катехин тримера;
фиг.49А-В показывают спектр 1Н, COSY, HMQC и НОНАНА ЯМР для тримера эпикатехина;
фиг.50А и В показывают действие фракций А и С процианидина какао соответственно на давление крови; уровень давления крови снижается на 21,43% в течение минуты после применения фракции А, возвращается к нормальному через 15 минут, тогда как после применения фракции С давление крови снижается на 50,5% в течение 1 минуты и возвращается к нормальному через 5 минут;
фиг.51 показывает действие фракций процианидина какао на артериальное давление крови находящихся под анестезией морских свинок;
фиг.52 показывает действие L-NMMA на изменение кровяного давления у находящихся под анестезией морских свинок, вызванное фракцией С процианидина какао;
фиг.53 показывает действие брадикинина на выработку NO в HUVEC (клетках эндотелия пупочной вены человека);
фиг.54 показывает действие фракций процианидинов какао на выработку макрофагами NO в HUVEC.
фиг.55 показывает действие фракций процианидинов какао на выработку NO макрофагами;
фиг.56 показывает действие фракций процианидина на LPS -индуцированные и гамма-интерферон-праймированные макрофаги;
фиг.57 показывает мицеллярное электрокинетическое капиллярное хроматографическое разделение олигомеров процианидинов какао;
фиг.58А-F показывают данные масс-спектрального анализа MALDI-TOF для присоединенных к тримеру ионов Cu+2-, Zn+2-, Fe+2-, Fe+3-, Ca+2- и Mg+2- соответственно;
фиг.59 показывает данные масс-спектрального анализа MALDI-TOF олигомеров процианидина какао (от тетрамеров до октадекамеров);
фиг.60 показывает дозозависимое действие олигомеров процианидина какао на кошачью лимфобластную клеточную линию FeA вируса лейкоза;
фиг.61 показывает дозозависимое действие олигомеров процианидинов какао на кошачью клеточную линию CRFK нормальной почки;
фиг.62 показывает дозозависимое действие олигомеров процианидина какао на собачью клеточную линию MDCK нормальной почки;
фиг.63 показывает дозозависимое действие между олигомерами процианидинов какао и собачьей линией клеток GH нормальной почки;
фиг.64 показывает эффект зависимости время - температура на гидролиз гексамера и
фиг.65 показывает эффект зависимости время - температура на образование тримера.
Соединения по изобретению
Как обсуждалось выше, неожиданно было обнаружено, что экстракты какао или соединения, извлеченные из них, проявляют противораковую, противоопухолевую или антинеопластическую активность, антиоксидантную активность, ингибируют фермент ДНК-топоизомеразу II и окислительное повреждение ДНК, обладают антибактериальной активностью, модулируют цик