Вакцины и способы лечения собачьего гриппа
Иллюстрации
Показать всеНастоящее изобретение относится к обеспечению новых вакцин и способов лечения заболеваний, связанных с вирусом собачьего гриппа. Способ иммунизации собаки против вируса гриппа включает введение указанной собаке терапевтически эффективного количества вакцины, содержащей по меньшей мере один аттенюированный или инактивированный вирус гриппа H3N8, где указанный вирус выделен из собаки, причем количество указанного вируса составляет от 10 до 10000 единиц ГА, и вакцина дополнительно содержит адъювант, где адъювант может быть выбран из а) метаболизируемого адъюванта, b) неметаболизируемого адъюванта, с) 2% квасцов, d) 5% квасцов, е) Quil А и f) холестерина или любой их комбинации. Способ получения вакцины против вируса гриппа собак включает приготовление композиции, содержащей терапевтически эффективное количество, по меньшей мере, одного аттенуированного или инактивированного вируса гриппа H3N8, где указанный вирус выделен из собаки. Применение вакцины, полученной способом для иммунизации собак против вируса гриппа. Изобретение обеспечивает повышение эффективности иммунизации. 3 н. и 9 з.п. ф-лы, 7 табл., 2 ил.
Реферат
ОБЛАСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к обеспечению новых вакцин и способов лечения заболеваний, связанных с вирусом собачьего гриппа. В нем раскрыты вирусные антигены гриппа и способы представления этих антигенов у псовых, в особенности у собак. Изобретение касается аттенуированных и инактивированных вакцин. Настоящее изобретение относится к экспериментально созданным вакцинам и вирусам собачьего и конского гриппа. Настоящее изобретение также включает вирусы гриппа A, H3, N8, H3N8 и H7N7, которые содержат по меньшей мере один геномный сегмент из вируса собачьего или конского гриппа. Настоящее изобретение также относится к применению этих вирусов в терапевтических композициях для защиты псовых, в частности собак, от заболеваний, вызванных вирусами гриппа.
УРОВЕНЬ ТЕХНИКИ ИЗОБРЕТЕНИЯ
Примерно с 1956 года вирус конского гриппа признан основным респираторным патогеном у лошадей. Заболевания, вызванные вирусом конского гриппа, могут иметь тяжелую симптоматику и часто сопровождаются вторичными бактериальными инфекциями. Выделены два подтипа вируса конского гриппа, а именно подтип 1, представляющий собой прототип вируса A/Equine/Prague/1/56 (H7N7), и подтип 2, представляющий собой прототип вируса A/Equine/Miami/1/63 (H3N8). В настоящее время преобладающим подтипом вируса является подтип 2, штамм H3N8. Предполагается, что этим штаммом могут быть инфицированы псовые, и он может быть достаточно вирулентным, достигающим по некоторым данным уровня смертности псовых 36%. Возможно, что межвидовая передача собаке полного или части вируса конского гриппа привела к появлению нового собачьего специфического вируса гриппа, связанного с острым респираторным заболеванием. Смотри «Transmission of Equine Influenza to Dogs» (P.C. Crawford et al., Science 310, 482-485 (2005). Существует явная и убедительная потребность в эффективной вакцине для лечения и профилактики этого нового собачьего гриппа.
КРАТКОЕ ОПИСАНИЕ ФИГУР
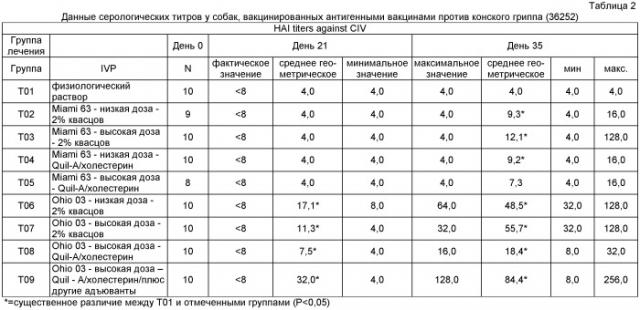
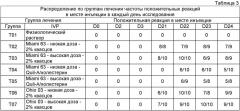
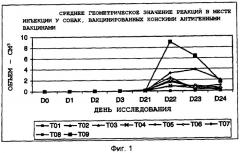
Фигура 1 показывает среднее геометрическое значение реакции в месте инъекции у собак, привитых вакцинами конского антигена. Фигура 2 показывает средний процент легочной консолидации у животных, привитых вакцинами вируса конского гриппа и зараженных вирусом собачьего гриппа.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение обеспечивает антигены, конского и собачьего гриппа, вакцины и способы применения этих вакцин для лечения псовых, в особенности собак, от инфекций, заболеваний и симптомов, вызванных собачьим гриппом. Настоящее изобретение дополнительно обеспечивает терапевтические композиции для защиты животного от заболевания, вызванного вирусом гриппа. В настоящем изобретении описаны способы получения вакцин и способы лечения животных. Антигены настоящего изобретения могут представлять собой любой идентифицированный штамм вируса гриппа, от любой птицы или млекопитающего, включающий грипп, имеющий антигенный подтип H3N8, или более часто называемый штаммом H3N8, но не ограничены ими. Грипп может иметь происхождение от любого из млекопитающих, включая без ограничения свиное, птичье, конское или собачье происхождение. Предпочтительными являются вирусы конского и собачьего гриппа и родственные антигены. Раскрыты штаммы, имеющие белки, обозначаемые H3 или N8. Штаммы, имеющие оба белка H3N8, являются предпочтительными. Также раскрыты штаммы, имеющие белки, обозначаемые H7N7.
Приведено описание концентрации антигена и получение вакцины. Описаны культуральные клеточные среды и рост вирусов. Приведено полное описание получения вакцины аттенуированного, инактивированного вируса, а также вакцинных адъювантов, рецептур, форм и носителей, дозировок, путей введения и анализов.
ПОБРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
ОПРЕДЕЛЕНИЯ И СОКРАЩЕНИЯ
Ниже даны определения, относящиеся к настоящему раскрытию, термины, которые не указаны, имеют значения, обычно используемые специалистами в данной области техники.
"Примерно", используемое в связи с измеряемыми числовыми переменными, относится к указанному значению переменной и ко всем значениям переменной, находящимся в пределах экспериментальной ошибки указанного значения (например, в пределах доверительного интервала 95% для среднего значения) или в пределах 10 процентов указанного значения, независимо от того, что больше.
"Активный иммунитет" включает как гуморальный иммунитет, так и клеточный иммунитет собаки.
"Антитело" относится к молекуле иммуноглобулина, которая может связываться со специфическим антигеном в результате иммунного ответа на этот антиген. Иммуноглобулины представляют собой сывороточные белки, состоящие из "легких" и "тяжелых" полипептидных цепей, имеющих "постоянные" и "вариабельные" участки, и разделенные на классы на основе состава постоянных участков (например, IgA, IgD, IgE, IgG и IgM). Антитело, которое является "специфическим" для данного антигена, указывает, что вариабельные участки антитела распознают и связываются исключительно со специфическим антигеном. Антитела могут представлять собой поликлональную смесь или быть моноклональными. Антитела могут быть интактными иммуноглобулинами, полученными из природных источников или из рекомбинантных источников, или могут быть иммунореактивными участками интактных иммуноглобулинов. Антитела могут существовать в ряде форм, включающих, например, как Fv, Fab', F(ab')2, так и в виде одноцепочечных форм.
Термины "антиген" или "иммуноген" относятся к молекуле, содержащей одну или больше антигенных детерминант (линейных, конформационных или и тех и других), которая после воздействия на субъект вызовет иммунный ответ, являющийся специфическим для этого антигена. Антигенная детерминанта представляет собой определенный участок антигена, который связывается с рецептором T-клетки или со специфическим антителом, и обычно содержит от примерно 3 аминокислотных остатков до примерно 20 аминокислотных остатков. Термин антиген относится к субъединичным антигенам, то есть к антигенам, выделенным и отделенным от целого организма, с которым антиген связан в природе, а также к убитым, аттенуированным или инактивированным бактериям, вирусам, грибам, паразитам или другим микроорганизмам. Термин антиген также относится к антителам, таким как анти-идиотипическим антителам или к их фрагментам, и к синтетическим пептидным мимотопам, которые могут имитировать антиген или антигенную детерминанту (эпитоп). Термин антиген также относится к олигонуклеотиду или полинуклеотиду, который in vivo экспрессирует антиген или антигенную детерминанту, как в случаях применения ДНК-иммунизации.
"Антигенность" относится к способности белка или полипептида иммуноспецифически связываться с антителом, вырабатываемым против белка или полипептида.
"Псовые" включают животных, общепринято называемых собаками, но также включают других представителей семейства Canidae.
"Клеточный иммунный ответ" - см. иммунный ответ.
Выражение "животное-компаньон", используемое в настоящем описании, относится к любому животному, не являющемуся человеком в неволе, которое считается домашним животным. Такие животные могут включать без ограничения собак, кошек, лошадей, овец, кроликов, обезьян и грызунов, включающих мышей, крыс, хомяков, песчанок и хорьков.
"Лошадь" включает животных, общепринято называемых лошадьми, но также включает других представителей семейства Equidae.
"Наполнитель" относится к любому компоненту вакцины, который не является антигеном.
"Первая вакцина", "вторая вакцина", "третья вакцина" и тому подобное относится к отдельно вводимым вакцинам, которые могут быть одинаковыми или разными и которые обычно можно вводить в любом порядке. Таким образом, третью вакцину можно вводить субъекту перед второй вакциной или после нее.
Термин "гетерологичный", используемый в настоящем описании, означает полученный из другого вируса, вида или штамма.
Используемые в настоящем описании термины "гомологичность", "гомологичный" и тому подобные означают степень идентичности между общими полипептидными или полинуклеотидными последовательностями.
Термин "гомологичный", используемый в настоящем описании по отношению к вирусу и виду, означает те же самые виды или штамм вируса.
Используемый в настоящем описании термин "клетка-хозяин" означает бактериальную или эукариотическую клетку, включающую клетки млекопитающих, птиц или насекомых, которая несет плазмиду, вирус или другой вектор.
"Гуморальный иммунный ответ" - см. иммунный ответ.
"Гибридома" - см. моноклональное антитело.
"Иммунный ответ" у субъекта относится к развитию гуморального иммунного ответа, клеточного иммунного ответа или гуморального и клеточного иммунного ответа на антиген. "Гуморальный иммунный ответ" относится к реакции, опосредуемой антителами. "Клеточный иммунный ответ" является реакцией, опосредуемой T-лимфоцитами или другими лейкоцитами или и теми и другими, и включает выработку цитокинов, хемокинов и подобных молекул, вырабатываемых активированными T-клетками, лейкоцитами или и теми и другими. Иммунные ответы можно определять с использованием стандартных иммуноанализов и проб на нейтрализацию, известных в данной области техники.
"Иммуногенность" относится к способности белка или полипептида выявить иммунный ответ, направленный специфично против бактерии или вируса, которые вызывают идентифицированную болезнь.
"Иммунологически защитное количество" или "количество, эффективное для выработки иммунного ответа" антигена является количеством, эффективным для индукции иммунного ответа у реципиента, который достаточен для предотвращения или улучшения признаков или симптомов заболевания, включающих неблагоприятные воздействие на здоровье или его осложнения. Как гуморальный иммунитет, так и клеточный иммунитет или и тот и другой могут быть индуцированными. Можно оценивать иммунногенный ответ животного на композицию вакцины, например, косвенно, посредством измерения титров антител, тестами пролиферации лимфоцитов, или непосредственным контролем признаков и симптомов после заражения штаммом дикого типа. Защитный иммунитет, обеспечиваемый вакциной, можно оценивать путем измерения, например, по уменьшению клинических признаков, таких как смертность, заболеваемость, температурные показатели, общее физическое состояние и общее состояние здоровья и поведения субъекта. Иммунный ответ может включать без ограничения индукцию клеточного и/или гуморального иммунитета. Количество вакцины, являющееся терапевтически эффективным, может варьировать в зависимости от конкретного используемого вируса или состояния прививаемого животного и может быть определено ветеринарным врачом.
"Интраназальное" введение относится к введению вещества, такого как вакцина, в организм субъекта через нос или посредством носа и охватывает транспорт вещества прежде всего через слизистую оболочку носа.
Термин "выделенный", используемый в настоящем описании, означает удаление из природного окружения, как единственного, так и в гетерологичной клетке-хозяине, или хромосоме, или векторе (например, в плазмиде, фаге и т.д.). "Выделенные бактерии", "выделенные анаэробные бактерии", "выделенный бактериальный штамм", "выделенный вирус", "выделенный вирусный штамм" и тому подобное относятся к композиции, в которой бактерии или вирус по существу не содержат других микроорганизмов, например, в культуре, такой как выделенной из окружающей его среды природного происхождения. Если термин "выделенный" используют для описания какого-либо конкретно указанного вещества, такого как полинуклеотид или полипептид, он относится к веществу, которое отделено от исходного клеточного окружения, в котором обычно находится вещество, такое как полипептид или нуклеиновая кислота. Таким образом, согласно использованию в настоящем изобретении, только в качестве примера, рекомбинантная клеточная линия, сконструированная с полинуклеотидом настоящего изобретения, использует "выделенную" нуклеиновую кислоту. Альтернативно, если конкретный белок или специфический иммуногенный фрагмент является заявленным или используемым в качестве вакцины, он будет считаться выделенным, поскольку он был идентифицирован, отделен и до некоторой степени очищен по сравнению с тем, как он мог бы существовать в природе. Если белок или его специфический иммуногенный фрагмент получают в рекомбинантном бактериальном или эукариотическом векторе экспрессии, который продуцирует антиген, считается, что он существует в виде выделенного белка или нуклеиновой кислоты. Например, рекомбинантная клеточная линия, сконструированная с полинуклеотидом, использует "выделенную" нуклеиновую кислоту.
"Метаболизируемые адъюванты" представляют собой адъюванты, состоящие из компонентов, способных к преобразованию у видов-мишеней в ходе обмена веществ, такие как адъюванты на основе растительного масла. Метаболизируемый адъювант может представлять собой метаболизируемое масло. Метаболизируемые масла представляют собой жиры и масла, которые обычно встречаются в растениях и в животных организмах и обычно состоят в основном из смесей триацилглицеринов, также известных, как триглицериды или нейтральные жиры. Эти неполярные, нерастворимые в воде вещества являются триэфирами глицерина и жирных кислот. Триацилглицерины отличаются в зависимости от идентичности и месторасположения в них трех остатков жирных кислот. См. сравнение с "неметаболизируемым адъювантом".
"Неметаболизируемые адъюванты" представляют собой адъюванты, состоящие из компонентов, которые не могут метаболизироваться в организме животного субъекта, которому вводят эмульсию. Неметаболизируемые масла, подходящие для использования в эмульсиях настоящего изобретения, включают алканы, алкены, алкины и их соответствующие кислоты и их спирты, эфиры и сложные эфиры, и их смеси. Предпочтительно, отдельные соединения масел представляют собой легкие углеводородные соединения, то есть такие компоненты имеют от 6 до 30 атомов углерода. Масло может быть получено синтетически или очищено из нефтепродуктов. Предпочтительные неметаболизируемые масла для использования в эмульсиях настоящего изобретения включают, например, минеральное масло, вазелиновое масло и циклопарафины. Термин "минеральное масло" относится к неметаболизируемому адъювантному маслу, которое представляет собой смесь жидких углеводородов, полученных из петролатума посредством технологии дистилляции. Термин является синонимом "сжиженного парафина", "жидкого вазелина" и "белого минерального масла". Также предполагается, что этот термин включает "легкое минеральное масло", то есть масло, которое получено подобным образом путем дистилляции петролатума, но которое обладает немного более низкой удельной массой, чем белое минеральное масло. Смотри, например, Remington's Pharmaceutical Sciences, 18th Edition (Easton, Pa.: Mack Publishing Company, 1990, at pages 788 and 1323). Минеральное масло можно получать из различных коммерческих источников, например, J.T. Baker (Phillipsburg, PA), USB Corporation (Cleveland, OH). Предпочтительным минеральным маслом является легкое минеральное масло, коммерчески доступное под торговым наименованием DRAKEOL®.
"Моноклональное антитело" относится к антителам, продуцируемым единственной линией клеток гибридомы, все из которых нацелены на одну антигенную детерминанту в конкретном антигене. Можно обеспечивать антиген, используемый для создания моноклонального антитела, в виде выделенного белка патогена или целого патогена. "Гибридома" представляет собой клональную клеточную линию, которая состоит из гибридных клеток, образованных слиянием миеломной клетки и специфической антителопродуцирующей клетки. Обычно моноклональные антитела имеют мышиное происхождение; вместе с тем, моноклональное антитело также относится к клональной популяции антитела, созданного против конкретной антигенной детерминанты антигена, полученного технологией фагового дисплея, или способом, эквивалентным фаговому дисплею или гибридным клеткам немышиного происхождения.
Выражение «N дней» или «М дней» после события относятся соответственно к любому времени в день N или в день М после события. Например, вакцинация субъекта второй вакциной через 14 дней после введения первой вакцины подразумевает, что вторую вакцину вводят в любое время на 14-й день после введения первой вакцины.
"ORF" означает "открытую рамку считывания", то есть кодирующую область гена.
"Пероральное" введение относится к введению вещества, такого как вакцина, в организм субъекта через рот или посредством рта и охватывает глотание или транспорт через слизистую оболочку рта (например, применение под язык или буккальное всасывание) или и то и другое. Интратрахеальный путь также относится к пероральному введению.
"Ороназальное" введение относится к введению вещества, такого как вакцина, в организм субъекта через нос и рот или посредством носа и рта, как будет происходить, например, при попадании одной или более капель в нос. Ороназальное введение охватывает процессы транспорта, связанные с пероральным и интраназальным введением.
"Парентеральное введение" относится к введению вещества, такого как вакцина, в организм субъекта через или посредством пути, в который не входит пищеварительный тракт. Парентеральное введение включает подкожное введение, внутримышечное введение, чрескожное введение, внутрикожное введение, интраперитонеальное введение, внутриглазное введение и внутривенное введение. Для задач настоящего раскрытия парентеральное введение исключает пути введения, которые в первую очередь охватывают транспорт вещества через ткань слизистых оболочек во рту, в носу, трахее и легких.
Выражение "фармацевтически приемлемое" относится к веществам, входящим в объем действующих медицинских представлений, подходящим для использования в контакте с тканями субъектов без чрезмерной токсичности, раздражения, аллергической реакции и тому подобного, в сопоставлении с разумным соотношением "пользы и риска" и эффективным для использования по назначению.
"Фармацевтически приемлемый носитель" относится к среде носителя, которая не нарушает эффективности биологического действия активного компонента и не является токсичной для субъекта, которому ее вводят.
"Поликлональное антитело" относится к смешанной популяции антител, созданных против конкретного патогена или антигена. Обычно популяция содержит множество групп антител, и каждая группа направлена против конкретной антигенной детерминанты патогена или антигена. Для создания поликлональных антител целый патоген или выделенный антиген инокуляцией или инфицированием вводят в организм хозяина, что индуцирует выработку антител против патогена или антигена в организме хозяина.
"Профилактика инфекции" означает предотвращение или ингибирование репликации бактерий или вируса, которые вызывают идентифицированное заболевание, ингибирование передачи бактерий или вируса, или предотвращение внедрения бактерии или вируса в хозяина, или облегчение симптомов заболевания, вызванного инфекцией. Лечение считается терапевтическим, если наблюдается снижение бактериальной или вирусной нагрузки.
Термины "защита", "защитная" и т.п., используемые в настоящем описании относительно вакцины, означают, что вакцина предотвращает или уменьшает симптомы заболевания, вызванного организмом, из которого получен антиген (антигены), используемый в вакцине. Термины "защита" и "защитная" и т.п. также подразумевают, что вакцину можно использовать для "лечения" заболевания или одного из нескольких симптомов заболевания, которое у субъекта уже существует.
"Респираторное" введение относится к введению вещества, такого как вакцина, в организм субъекта через или посредством ингаляции распыленного (тонко измельченного) вещества. При ингаляционном введении первичный транспортный механизм включает абсорбцию распыленного вещества через слизистую оболочку трахеи, бронхов и легких и таким образом отличается от интраназального или перорального введения.
Термин "специфический для", используемый для описания антител настоящего изобретения, указывает, что вариабельные области антител настоящего изобретения распознают и связываются исключительно со специфическим штаммом H3N8 (то есть способны отличать специфический белок H3N8 от других известных белков на основании измеримых различий связывающей афинности, несмотря на существование ограниченной идентичности последовательностей, гомологии или подобия между белками H3N8 и такими полипептидами). Подразумевается, что специфические антитела также могут взаимодействовать с другими белками (или другими антителами с применением технологии твердофазного иммуноферментного анализа ELISA) посредством взаимодействий с последовательностями вне вариабельной области антител и, в частности, в постоянной области молекулы. Для определения специфичности связывания антитела настоящего изобретения известно скрининговое исследование, обычно применяемое в данной области. Для всестороннего рассмотрения таких исследований смотри 6 главу руководства Harlow et al. (Eds.), Antibodies: A Laboratory Manual; Cold Spring Harbor Laboratory; Cold Spring Harbor, NY (1988), Chapter 6. Антитела настоящего изобретения можно получать, используя любой способ, известный и обычно используемый в данной области.
"Субъединичная вакцина" относится к типу вакцины, которая включает один или несколько антигенов, но не все антигены, которые получены из патогена или гомологичны антигенам рассматриваемого патогена, такого как вирус, бактерия, паразит или гриб. Такая композиция по существу не содержит интактных патогенных клеток или патогенных частиц или лизат таких клеток или частиц. Таким образом, субъединичную вакцину можно получить из, по меньшей мере, частично очищенных или по существу очищенных иммуногенных полипептидов из патогена или его аналогов. Способы получения антигена или антигенов в субъединичной вакцине включают стандартные технологии очистки, рекомбинантного получения или химического синтеза. Таким образом, «субъединичная вакцина» относится к вакцине, состоящей из определенного антигенного компонента или компонентов полного вирусного, бактериального или другого иммуногена.
"Специфический иммуногенный фрагмент" означает часть последовательности, распознаваемой антителом, которое является специфическим для этой последовательности.
Термин "субъект" относится к любому животному, имеющему иммунную систему, которая включает млекопитающих, таких как собаки.
"TCID50" обозначает "инфекционную дозу в тканевой культуре", и ее определяют как разведение вируса, которое необходимо для инфицирования 50% данной партии инокулированных клеточных культур. Для расчета TCID50 можно использовать разные способы, включая способ Спермана-Карбера (Spearman-Karber), применяемый в настоящем описании. Для описания способа Спермана-Карбера смотри руководство B. W. Mahy & H. O. Kangro, Virology Methods Manual 25-46 (1996).
Термин "терапевтический агент" относится к любой молекуле, соединению, вирусу или способу лечения, предпочтительно к вирусу, аттенуированному или убитому, или к субъединице или соединению, которые способствуют лечению вирусной инфекции или заболевания, или состояния, вызванного таким образом.
"Терапевтически эффективное количество" в контексте настоящего раскрытия относится к количеству антигена или вакцины, которое будет вызывать иммунный ответ у субъекта (например, у собаки), получающего антиген или вакцину, которое является подходящим для предотвращения или улучшения признаков или симптомов заболевания, включающего побочные эффекты для здоровья или его осложнения, вызванного инфицированием патогеном, таким как вирус (например, H3N8), бактерия, паразит или гриб. Может быть индуцирован гуморальный иммунитет или клеточный иммунитет или как гуморальный, так и клеточный иммунитет. Можно оценивать иммунный ответ животного на вакцину, например, косвенно, посредством измерения титров антитела, тестами пролиферации лимфоцитов, или непосредственным контролем признаков и симптомов после заражения штаммом дикого типа. Защитный иммунитет, обеспечиваемый вакциной, можно оценивать путем измерения, например, по уменьшению клинических признаков, таких как смертность, заболеваемость, температурные показатели, общее физическое состояние и общее состояние здоровья и поведение субъекта. Количество вакцины, являющееся терапевтически эффективным, может варьировать в зависимости от конкретного используемого вируса или состояния прививаемого животного и может быть определено специалистом в данной области техники.
Термин "передаваемые" означает вирус, который способен к переносу от первого животного (собака) ко второму животному (собака), при этом вторая собака проявляет серологическую конверсию к переданному вирусу.
"Лечить" означает изменять, облегчать, тормозить развитие или предотвращать нарушения, состояния или заболевания, к которым относится указанный термин, или предотвращать один или больше симптомов такого нарушения, состояния или заболевания.
"Лечение" относится к осуществлению действия "лечить", определение, которое приведено непосредственно выше.
Термин "вакцина" относится к иммуногенной композиции, выбираемой из вируса, или модифицированной живой, аттенуированной или инактивированной вакцины, или субъединичной вакцины, или к любой комбинации из вышеупомянутого. Введение вакцины субъекту приводит к возникновению иммунного ответа. Вакцину можно вводить субъекту непосредственно любым известным путем введения, включающим парентеральный, пероральный и тому подобный путь.
ЧАСТЬ 1. АНТИГЕНЫ И ВИРУСНЫЕ ШТАММЫ, ИХ ПОЛУЧЕНИЕ, ПРОИЗВОДСТВО, СОСТАВЛЕНИЕ РЕЦЕПТУРЫ И ВВЕДЕНИЕ ВАКЦИН.
Один аспект настоящего изобретения обеспечивает вакцины, которые используют для вызова иммунного ответа следующие антигены.
Полезный антиген (антигены) настоящего изобретения. Антигены настоящего изобретения могут быть любым идентифицированным штаммом вируса гриппа, от любой птицы или млекопитающего, включающим без ограничения вирус гриппа, имеющий подтип H3 гемагглютинина, и подтип N8 нейраминидазы, или подтип H3N8, более общепринято называемый вирусом H3N8. Грипп может иметь любое происхождение от млекопитающих или птиц, включающее без ограничения свиное, конское или собачье происхождение. Конские и собачьи антигены гриппа являются предпочтительными. Используют штаммы, определяющие гликопротеины подтипа H3 или N8, и более предпочтительными являются штаммы, имеющие как H3, так и N8.
Штаммы и варианты и их мутанты и варианты также являются предпочтительными, как описано в руководстве Transmission of Equine Influenza to Dogs (P.C. Crawford et al, Science 310, 482- 485 (2005). Вирусный НА представляет собой критическую детерминанту специфичности вируса гриппа от видов хозяев.
Антигены гриппа настоящего изобретения могут быть выделены из собак, лошадей, свиней, и кур, как домашних, так и диких. У животных, выбранных для сбора образцов, должны проявляться острые и/или подострые клинические синдромы, которые могут включать респираторные симптомы от умеренных до тяжелых и лихорадку. Животные могут также проявлять симптомы анорексии и летаргии. Способы выделения вирусов известны специалистам в данной области техники: инокуляция клеточных культур млекопитающих или птиц, оплодотворенных яиц образцами слизи из носа или глотки от представителей с клиническими проявлениями, сбор мазков из носового прохода или зева или сбор тканей, таких как селезенка, легкие, миндалины и печень, и смывы из легких. Цитопатическое действие вируса можно наблюдать в клеточной культуре, и можно тестировать аллантоисную жидкость или клеточные лизаты на их способность агглютинировать эритроциты человека, петуха, индейки или морской свинки, что является предполагаемым свидетельством присутствия вируса гриппа.
Номенклатура вирусных штаммов и возможных антигенов. Тип штамма вируса гриппа подразделяют на подтипы на основе антигенных характеристик их гликопротеинов на поверхности вириона. Эти вирусные гликопротеины представляют собой гемагглютинин (НА) и нейраминидазу (NА). Обычно НА-подтип называют первым и NА-подтип называют вторым, таким образом, H3N8 относится к вирусу с подтипом 3 гемагглютинина и подтипом 8 нейраминидазы. Подтип определяют на основе серологического анализа НА и NА. Используя методики, раскрытые в настоящем изобретении, можно создать вакцину для любого из этих подтипов. В настоящее время имеется 16 идентифицированных подтипов НА и 9 идентифицированных подтипов NА. Их может быть больше среди диких подтипов, которые еще не были описаны. Конкретно, идентифицированные подтипы включают H1, H2, H3, H4, H5, H6, H7, H8, H9, H10, H11, H12, H13, H14, H15 и H16 и N1, N2, N3, N4, N5, N6, N7, N8 и N9. Все из этих комбинаций подтипов и любые комбинации указанных и какого-либо подтипа и комбинации будущих подтипов, которые будут идентифицированы в будущем, используя описанные выше методики или по существу подобные методики, описаны в настоящем изобретении и заявлены в формуле изобретения в качестве полезных антигенов настоящего изобретения. Раскрыты все другие комбинации НА- и NА-подтипов. Они включают без ограничения предпочтительные подтипы H3N8 и H7N7.
Гемагглютинин (НА) вируса гриппа является гликопротеином на поверхности вириона, который присоединяет вирус к его рецепторам на клетках-хозяевах и растворяет вирусную оболочку с мембранами эндоцитозных пузырьков, чтобы инициировать инфекционный процесс. Он также является наиболее важным вирионным компонентом в индукции и образовании защитных антител. Аминокислотная последовательность НА и, следовательно, расположение ее сайтов N-гликозилирования определяется вирусным геномом.
Сегментированный, геном РНК-отрицательной цепи вируса гриппа реплицируется РНК-зависимой РНК-полимеразой, которая не имеет эффективной функции считывания, что приводит к высокой частоте ошибок транскрипции, которые могут привести к заменам аминокислот в поверхностных гликопротеинах НА и NA. Одним из последствий этой высокой частоты мутации является содержание в вирусных популяциях мутантов, которые отличаются от большинства по количеству и положению N-связанных гликанов на НА. Структуры этих олигосахаридов можно определить их положением на НА и размещением ферментов биосинтеза и расщепления, представленных в клетке-хозяине, в которой растет вирус. Таким образом, пластичность вирусного генома и хозяин-специфические механизмы гликозилирования вместе могут создать вирусные популяции, которые являются более гетерогенными по структуре и функции, чем разработанные только каком-либо одним способом. Считается, что это многообразие отвечает за выживание этих вирусов в ряде биологических ниш и за их способность преодолевать ингибирующее действие нейтрализующих антител и противовирусных средств. Были идентифицированы мутации вирусного генома различных штаммов, и эти мутированные штаммы также заявлены в формуле настоящего изобретения. Например, некоторые из этих мутантов описаны в руководстве Transmission of Equine Influenza to Dogs (P.C. Crawford et al., Science 310, 482-485 (2005), включенном в настоящее изобретение посредством ссылки.
В настоящем изобретении также раскрыта вакцина, созданная из специфичного штамма, собранного и идентифицированного как штамм конского гриппа A/Equine/2/Miami/l/63. Это штамм депонирован в Американской коллекции типовых культур, American Type Culture Collection, 10801 University Boulevard, Manassas, VA 20110-2209 под номером АТСС VR 317. Это штамм был первоначально выделен из мазков из носовой полости больной лошади в Майами в 1963 году. Вирус перевивали 5 раз на куриных эмбрионах. Вирус дополнительно классифицирован как H3N8.
Другим примером североамериканского вируса гриппа H3N8, полученного из лошади, является A/Equine/Kentucky/1998. Дополнительными примерами H3N8, полученного из лошади, является A/Equine/Kentucky/15/2002, A/Equine/Ohio/1/2003, A/Equine/Kentucky/1/1994, A/Equine/Massachusetts/213/2003, A/Equine/Wisconsin/2003 и A/Equine/New York/1999. Другими примерами является европейский вирус гриппа H3N8, полученный из A/Equine/Newmarket/A2/1993.
Настоящее изобретение также раскрывает вакцину, полученную из определенного штамма, собранного и идентифицированного как штамм собачьего гриппа A/canine/Iowa/13628/2005 и штамм A/canine/Iowa/9Al/B5/08/Dl2. Последний штамм, штамм A/canine/Iowa/9Al/B5/08/D12 был депонирован как UC 25509 29 июня 2006 года в Американской коллекции типовых культур 10801 PC33104A University Boulevard, Manassas, VA 20U0-2209, под инвентарным ATCC номером PTA 7694. Вирус дополнительно классифицирован как H3N8.
В дополнение к вышеупомянутым штаммам авторы раскрывают штамм, полученный следующим образом. Идентифицировали собаку или группу собак, проявляющих клинические признаки респираторного заболевания, получали образцы слизи изо рта или носа или образцы, полученные из ткани респираторных органов или тканей внутренних органов собак, проводили анализы образцов и идентифицировали присутствие вируса гриппа H3N8. Используя методики, описанные в настоящем изобретении, выделяли, очищали, культивировали, выращивали, получали, концентрировали этот вирусный антиген и идентифицировали его как вирус собачьего гриппа Pfizer. Его адаптировали и перевивали или в оплодотворенные яйца, или в клетки собак, или как в то, так и в другое, идентифицировали как исходный вакцинный вирус (Master Seed), вирус собачьего гриппа H3N8. Предпочтительным являлся вирус гриппа H3N8 собачьего происхождения. Также можно использовать вирус H3N8 конского или свиного происхождения, а также вирус гриппа подтипа H3 или N8. Авторы настоящего изобретения раскрывают штамм, полученный следующим образом. Собаку или группу собак инфицировали вирусом конского гриппа H3N8. От собак, проявляющих клинические признаки респираторного заболевания, получали образцы слизи изо рта или носа или образцы, полученные из тканей респираторных органов, смывы из легких или тканей внутренних органов собак, проводили анализы образцов и идентифицировали присутствие вируса гриппа H3N8. Используя методики, описанные в настоящем изобретении, выделяли, очищали, культивировали, выращивали, получали, концентрировали этот вирусный антиген и идентифицировали его как вирус собачьего гриппа. Его адаптировали и перевивали или в оплодотворенные яйца, или в клетки собак, или как в то, так и в другое, идентифицировали как исходный вакцинный вирус, вирус собачьего гриппа H3N8. Предпочтительным являлся вирус гриппа H3N8 собачьего происхождения. Также можно использовать вирус H3N8 конского или свиного происхождения, а также вирус гриппа подтипа H3 или N8. Вирус H3N8 свиного происхождения лечат тем же образом, как и вирус конского или собачьего происхождения, описание которых полностью приведено в настоящем изобретении.
ЧАСТЬ 2. ПОДРОБНОЕ ОПИСАНИЕ ПОЛУЧЕНИЯ, ПРОИЗВОДСТВА, СОСТАВЛЕНИЯ РЕЦЕПТУР И ВВЕДЕНИЯ ВАКЦИН, ПОЛУЧЕННЫХ ИЗ АНТИГЕНОВ ЧАСТИ 1.
Часть 2a) Обсуждение . Вирусные антигены из части 1 можно превращать в рассматриваемые полезные композиции, содержащие вирусный антиген, модифицированный для уменьшения его вирулентности и созданный в виде полезной рецептуры или рецептуры вакцины. Далее приведено описание, обеспечивающее подробности для получения, производства, составления рецептуры и введения вакцин, полезных для профилактики или лечения клинических симптомов, связанных с инфекцией вирусом гриппа у собак, или для профилактики заболевания у собак, вызываемого вирусом собачьего или конского гриппа. Инфекция собачьего гриппа, которую нужно лечить, может быть вызвана вирусом конского гриппа, или она может представлять собой новый модифицированный вирус собачьего гриппа, происходящий из вируса конского гриппа. Действие способов лечения, описанных в настоящем изобретении, способно предотвратить смертность заболевших собак от вируса собачьего или конского гриппа.
В настоящем изобретении описаны способы и материалы для лечения и иммунизации вакциной животных и, конкретно, собак, против вирусов конского и собачьего гриппа. Способ включает введение собаке терапевтически эффективного количества первой, второй и или третьей вакцины, которая способна индуцировать иммунный ответ, и конкретно, введение собаке вакцины против вирусов гриппа H3N8. Вакцина настоящего изобретения обычно предназначена для профилактического лечения, при котором собак имм