Фармацевтическая композиция
Иллюстрации
Показать всеизобретение относится к химико-фармацевтической промышленности и касается препарата для перорального применения, включающего пептизированный крахмал, N-[4-[4-(1,2-бензизотиазол-3-ил)-1-пиперазинил]-(2R,3R)-2,3-тетраметилен-бутил]-(1'R,2'S,3'R,4'S)-2,3-бицикло[2,2,1]гептандикарбоксиимида гидрохлорид (луразидон), представленный формулой (1), водорастворимый эксципиент и водорастворимое полимерное связующее соединение, в заявленном препарате содержание луразидона на таблетку составляет от 10 до 160 мг или от 20 до 45% (мас./мас.) от массы препарата, и пептизированный крахмал включен в количестве от 10 до 50% (мас./мас.) от массы препарата. Препарат проявляет неизменный характер режима высвобождения даже при изменении содержания активного ингредиента. 5 н. и 12 з.п. ф-лы, 39 табл., 3 ил.
Реферат
Область техники, к которой относится изобретение
Настоящее изобретение относится к пероральному препарату, обладающему хорошими дезинтеграционными свойствами, который включает в качестве активного ингредиента N-[4-[4-(1,2-бензизотиазол-3-ил)-1-пиперазинил]-(2R,3R)-2,3-тетраметилен-бутил]-(1'R,2'S,3'R,4'S)-2,3-бицикло[2,2,1]гептандикарбоксиимида гидрохлорид (луразидон). В особенности настоящее изобретение относится к препарату для перорального применения, в частности в таблетированной форме, включающему луразидон в качестве активного ингредиента, который обладает одинаковым профилем растворения активного ингредиента при различном содержании в нем активного ингредиента.
Уровень техники
В Патентном Документе 1 раскрывается, что такое соединение, как луразидон, может применяться перорально и пероральный препарат может быть изготовлен путем перемешивания активного ингредиента с традиционным носителем, эксципиентом, связующим соединением, стабилизатором и т.п., но в нем не раскрывается пероральный препарат, который характеризуется быстрой растворимостью и обладает одинаковым профилем растворения активного ингредиента, даже если содержание активного ингредиента в нем меняется в широких пределах, в особенности пероральный препарат с высоким содержанием активного ингредиента, который обладает таким же профилем растворения, как и большое количество таблеток с низким содержанием активного ингредиента в таблетке.
С целью обеспечения биоэквивалентности, когда вводят фармацевтические препараты с различным содержанием активного ингредиента так, чтобы дозы были одинаковыми, была выпущена инструкция, например, "Guideline for Bioequivalence Studies of Oral Solid Dosage Forms with Different Content" (Notification No. 64 of the Evaluation and Licensing Division, Pharmaceutical and Food Safety Bureau, опубликовано 14 февраля 2000 г.), где было сформулировано требование того, что фармацевтические препараты с различным содержанием должны обладать эквивалентным профилем растворения в каждом тестовом растворе, таком как буферы со значениями от рН 1,2, от 3,0 до 5,0 и 6,8 (что соответствует значениям рН в желудке, кишечнике и ротовой полости соответственно), вода и солевой раствор.
В Патентном Документе 2 раскрывается пероральный препарат, включающий луразидон в качестве активного компонента и обладающий быстрой растворимостью и эквивалентным профилем растворения, даже если содержание активного ингредиента в нем различно, в особенности пероральный препарат с высоким содержанием активного ингредиента, который обладает таким же профилем растворения, как и большое количество таблеток с низким содержанием активного ингредиента в каждой таблетке, и может высвобождать водорастворимый активный ингредиент из препарата в необходимой концентрации.
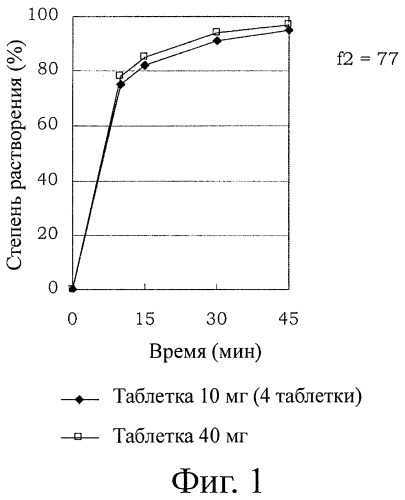
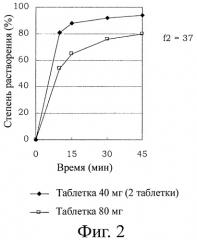
В Патентном Документе 2 далее раскрывается пероральный препарат, в частности в таблетированной форме, который проявляет быструю растворимость активного ингредиента, даже если содержание активного ингредиента в нем меняется в пределах от нескольких мг до нескольких десятков мг (например, в пределах от 5 мг до 20 мг или в пределах от 5 мг до 40 мг), и далее обладает эквивалентным профилем растворения при аналогичном соотношении компонентов. Зачастую требуется, чтобы пероральный препарат представлял собой препарат с повышенным содержанием активного ингредиента для достижения более выраженного клинического эффекта или препарат, обладающий профилем растворения, эквивалентным таковому при применении большого количества таблеток, из которого активный ингредиент может высвобождаться в необходимой концентрации, меняющейся в широких пределах, для достижения клинических эффектов, зависящих от состояния пациентов. Уровень техники, раскрытый в Патентном Документе 2, может обеспечить пероральный препарат, который обладает эквивалентным профилем растворения в пределах от 5 мг до 40 мг луразидона на таблетку, как показано на фиг.1. Однако, как показано на фиг.2, когда содержание активного ингредиента в таблетке увеличивалось вдвое, как, например, в случае таблетки 80 мг, препарат мог не обладать эквивалентным профилем растворения. Следовательно, необходимо применение большого количества таблеток одновременно либо использование таблеток большого размера, неудобных для применения. Поэтому для такого слабо растворимого в воде активного ингредиента, как луразидон, было сложно предоставить пероральный препарат, обладающий эквивалентным профилем растворения даже при высоком содержании, либо в широких рамках содержания активного ингредиента.
В Патентном Документе 2 водорастворимое полимерное связующее соединение включает крахмал, однако в документе не упоминается предварительно пептизированный крахмал. Известно, что пептизированный крахмал значительно улучшает дезинтеграцию и растворимость фармацевтической композиции, как описано, например, в Патентном Документе 3, а также он часто используется обычно при содержании 10% или менее, как описано в Непатентном Документе 1.
| Патентный Документ 1: | JP2800953 |
| Патентный Документ 2: | WO2002/024166 |
| Патентный Документ 3: | JP2000-26292 |
| Непатентный Документ 1: | Handbook of Pharmaceutical |
| Excipients, 2nd edition, 491, 1994, | |
| The Pharmaceutical Press. |
Раскрытие изобретения
Задачи, решаемые изобретением
Настоящее изобретение направлено на обеспечение перорального препарата, включающего луразидон в качестве активного ингредиента, который характеризуется быстрой растворимостью и обладает эквивалентным профилем растворения, даже если содержание активного ингредиента в нем меняется в широких пределах, в частности, пероральный препарат с увеличенным содержанием активного ингредиента, который обладает сходным профилем растворения по сравнению с большим количеством таблеток с более низким содержанием активного ингредиента на таблетку и может высвобождаться из него в требуемой концентрации.
Настоящее изобретение направлено на обеспечение препарата для перорального применения, который включает в качестве активного ингредиента N-[4-[4-(l,2-бензизотиазол-3-ил)-1-пиперазинил]-(2R,3R)-2,3-тетраметилен-бутил]-(1'R,2'S,3'R,4'S)-2,3-бицикло[2,2,1]гептандикарбоксиимида гидрохлорид (здесь упоминаемый как луразидон), который обладает эквивалентным профилем растворения активного ингредиента, даже если содержание в нем активного ингредиента различно.
Способы решения задач
Авторы настоящего изобретения интенсивно изучали описанные выше задачи и нашли решение указанных задач приведенными ниже способами.
Настоящее изобретение включает следующие воплощения:
(1) Пероральный препарат, который включает N-[4-[4-(1,2-бензизотиазол-3-ил)-1-пиперазинил]-(2R,3R)-2,3-тетраметилен-бутил]-(1'R,2'S,3'R,4'S)-2,3-бицикло[2,2,1]гептандикарбоксиимида гидрохлорид (луразидон) с формулой (I):
,
пептизированный крахмал, водорастворимый эксципиент и водорастворимое полимерное связующее.
(2) Пероральный препарат, который изготовлен путем гранулирования порошкообразной смеси, включающей луразидон, пептизированный крахмал и водорастворимый эксципиент с использованием раствора водорастворимого полимерного связующего соединения.
(3) Пероральный препарат, который изготовлен путем гранулирования порошкообразной смеси, включающей пептизированный крахмал и водорастворимый эксципиент с использованием раствора или дисперсии луразидона и водорастворимого полимерного связующего соединения.
(4) Пероральный препарат по любому из п.п.(1)-(3), где водорастворимый эксципиент представлен маннитом или лактозой.
(5) Способ гранулирования порошкообразной смеси, который включает гранулирование порошкообразной смеси, включающей луразидон, пептизированный крахмал и водорастворимый эксципиент, с использованием раствора водорастворимого полимерного связующего.
(6) Способ гранулирования порошкообразной смеси, включающей пептизированный крахмал и водорастворимый эксципиент, с использованием раствора или дисперсии луразидона и водорастворимого полимерного связующего.
(7) Способ гранулирования по п.(5), где водорастворимый эксципиент представлен маннитом или лактозой.
(8) Пероральный препарат по любому из п.п.(1)-(4), где пептизированный крахмал включен в количестве от 10 до 50% (вес./вес.) от веса препарата в целом.
(9) Пероральный препарат по любому из п.п.(1)-(4), где пептизированный крахмал включен в количестве от 20 до 30% (вес./вес.) от веса препарата в целом.
(10) Пероральный препарат по любому из п.п.(1)-(4), где содержание луразидона в препарате - 20-45% (вес./вес.).
(11) Пероральный препарат по любому из п.п.(1)-(4), где содержание луразидона в препарате - 25-40% (вес./вес.).
(12) Пероральный препарат по любому из п.п.(1)-(4), где содержание луразидона в таблетке - 10-160 мг.
(13) Пероральный препарат по любому из п.п.(1)-(4), где содержание луразидона в таблетке - 20-120 мг.
(14) Пероральный препарат по любому из п.п.(1)-(4), где содержание луразидона в таблетке - 40-120 мг.
(15) Пероральный препарат по любому из п.п.(1)-(4), где водорастворимый эксципиент представлен маннитом или лактозой, и пептизированный крахмал включен в количестве от 10 до 50% (вес./вес.) от веса препарата в целом.
(16) Пероральный препарат по любому из п.п.(1)-(4), где водорастворимый эксципиент представлен маннитом или лактозой, и содержание луразидона в препарате - 25-40% (вес./вес.).
(17) Пероральный препарат по любому из п.п.(1)-(4), где пептизированный крахмал включен в количестве от 10 до 50% (вес./вес.) от веса препарата в целом, и содержание луразидона в препарате - 25-40% (вес./вес.).
(18) Пероральный препарат по любому из п.п.(1)-(4), где водорастворимый эксципиент представлен маннитом или лактозой, пептизированный крахмал включен в количестве от 10 до 50% (вес./вес.) от веса препарата в целом, и содержание луразидона в препарате - 25-40% (вес./вес.).
(19) Пероральный препарат по любому из п.п.(1)-(4), где водорастворимый эксципиент представлен маннитом или лактозой, пептизированный крахмал включен в количестве от 20 до 30% (вес./вес.) от веса препарата в целом, и содержание луразидона в препарате - 25-40% (вес./вес.).
(20) Пероральный препарат по любому из п.п.(1)-(4), где водорастворимый эксципиент представлен маннитом или лактозой, пептизированный крахмал включен в количестве от 20 до 30% (вес./вес.) от веса препарата в целом, и содержание луразидона в таблетке - 40-120 мг.
(21) Пероральный препарат по любому из п.п.(1)-(4), где степень желатинизированности пептизированного крахмала составляет от 50 до 95%.
(22) Пероральный препарат по любому из п.п.(1)-(4), где средний размер частиц луразидона составляет от 0,1 до 8 мкм.
(23) Пероральный препарат по любому из п.п.(1)-(4), где пептизированный крахмал содержит 30% или менее растворимого в воде вещества.
(24) Пероральный препарат по любому из п.п.(1)-(4), где водорастворимый эксципиент представлен маннитом или лактозой, пептизированный крахмал включен в количестве от 20 до 30% (вес./вес.) от веса препарата в целом, содержание луразидона в препарате - 25-40% (вес./вес.), и содержание луразидона в таблетке - 20-120 мг.
Результаты изобретения
В уровне техники, раскрытом в Патентном Документе 2, было подтверждено, что фармацевтический препарат с низким содержанием луразидона до 40 мг на таблетку может обеспечивать пероральный препарат с эквивалентным профилем растворения.
Однако фармацевтический препарат с более высоким содержанием луразидона не мог обладать эквивалентным профилем растворения. Поэтому следовало применять удвоенное или большее количество препарата низкого содержания у пациентов, нуждающихся в высоких дозах луразидона, что означало дополнительную нагрузку на пациента, и, следовательно, в этой области было необходимо усовершенствование техники. Препарат настоящего изобретения, который включает пептизированный крахмал, может обеспечить пероральный препарат с повышенным содержанием луразидона, который возлагает меньшую нагрузку на пациента. Дополнительно настоящее изобретение может обеспечить пероральный препарат с высоким содержанием луразидона и препарат для перорального применения, который обладает эквивалентным профилем растворения, даже если содержание луразидона в нем меняется. Кроме этого, препараты настоящего изобретения прекрасно хранятся в течение длительного срока.
Наилучший способ осуществления настоящего изобретения
N-[4-[4-(1,2-бензизотиазол-3-ил)-1-пиперазинил]-(2R,3R)-2,3-тетраметилен-бутил]-(1'R,2'S,3'R,4'S)-2,3-бицикло[2,2,1]гептандикарбоксиимида гидрохлорид (луразидон) представляет собой соединение со следующей формулой:
(см., например, JP 2800953). Известно, что луразидон обладает психотропным эффектом и полезен при терапии шизофрении и т.п. Указанное соединение включают в препараты, например, в пределах от 10 до 50% по весу, предпочтительно в пределах от 20 до 45% по весу, особенно в пределах от 20 до 45% по весу от общего веса таблетки в целом. В дополнение предпочтительно мелкое перемалывание препарата, например, чтобы 90% по объему или более всех частиц обладали размером частиц 27 мкм или менее, и средний размер частиц в объемном соотношении (т.е. размер частиц, составляющих 50% общего объема) включал, например, значения в пределах от 0,1 до 8 мкм, предпочтительно в пределах от 1 до 4 мкм. Содержание луразидона - от 10 до 160 мг, предпочтительно от 20 до 120 мг, более предпочтительно от 40 до 120 мг на таблетку.
Термин «пептизированный крахмал» относится к соединениям, полученным путем пептизирования различных типов крахмала (например, кукурузного крахмала, картофельного крахмала, пшеничного крахмала, рисового крахмала, крахмала тапиоки и т.д.), и может включать пептизированный крахмал или частично пептизированный крахмал, описанный в «Japanese Pharmaceutical Excipients». Пептизированный крахмал характеризуется степенью предварительной желатинизации, например, в пределах от 50 до 100%, предпочтительно в пределах от 50 до 95%, более предпочтительно в пределах от 80 до 95%. В дополнение пептизированный крахмал содержит растворимое в воде вещество в количестве, например, 40% или менее, более предпочтительно 30% или менее. Такой пептизированный крахмал обычно используют в виде порошка, средний размер частиц которого находится в пределах от 1 до 1000 мкм, предпочтительно в пределах от 1 до 500 мкм, более предпочтительно в пределах от 10 до 100 мкм. Коммерчески доступный пептизированный крахмал, подходящий для целей настоящего изобретения, включает, например, частично пептизированный крахмал, такой как PCS (торговая марка, производства компании Asahi Kasei Corporation) или Starch 1500 (торговая марка, производства компании Colorcon, Inc.) и т.д. Среди перечисленных выше пептизированных крахмалов частично пептизированный крахмал, такой как PCS (торговая марка, производства компании Asahi Kasei Corporation) предпочтителен для использования. Степень предварительной желатинизации частично пептизированного крахмала предпочтительно находится в пределах от 50 до 95%, более предпочтительно в пределах от 80 до 95%. Использованный в настоящем изобретении пептизированный крахмал составляет от 10% до 50%, предпочтительно в пределах от 10% до 40%, в частности, в пределах от 20% до 30% по весу от всего препарата.
«Водорастворимый эксципиент» включает, например, маннит, лактозу, сахарозу, сорбит, D-сорбит, эритрит, ксилит и т.д. Более предпочтительно он включает маннит и лактозу. Еще более предпочтительный включает маннит. Также указанный водорастворимый эксципиент может использоваться по отдельности либо два или более из них могут использоваться совместно. Водорастворимый эксципиент включают в количестве, например, в пределах от 30 до 80% по весу, предпочтительно в пределах от 40 до 60% по весу от общего веса таблетки. Средний размер частиц маннита находится, например, в пределах от 10 до 200 мкм.
«Водорастворимое полимерное связующее соединение» включает, например, гидроксипропилцеллюлозу, гидроксипропилметилцеллюлозу, поливинилпирролидон, поливиниловый спирт и т.д. Более предпочтительно он включает гидроксипропилцеллюлозу, гидроксипропилметилцеллюлозу, поливинилпирролидон или поливиниловый спирт. Указанное водорастворимое полимерное связующее соединение может использоваться по отдельности либо два или более из них могут использоваться совместно. Водорастворимое полимерное связующее соединение включают в количестве, например, в пределах от 0,5 до 10% по весу, предпочтительно в пределах от 1 до 5% по весу от общего веса таблетки.
Пероральный препарат в форме фармацевтической композиции настоящего изобретения относится к фармацевтическому препарату, который сформирован в виде таблетки, капсулы, гранулы или мелкодисперсной гранулы. Указанный препарат может быть сформирован в виде таблетки, капсулы, гранулы или мелкодисперсной гранулы традиционным способом с использованием водорастворимого эксципиента, а также нерастворимого в воде эксципиента, связующего соединения, дезинтегрирующего соединения, вещества, облегчающего скольжение и т.д. Следующие ниже соединения могут быть добавлены к препарату.
«Нерастворимый в воде эксципиент» включает, например, кукурузный крахмал, кристаллическую целлюлозу и т.д. Указанный неводорастворимый эксципиент может использоваться по отдельности либо два или более из них могут использоваться совместно.
«Дезинтегрирующее соединение» включает, например, кукурузный крахмал, кристаллическую целлюлозу, низкозамещенную гидроксипропилцеллюлозу, кармеллозу, кальция кармеллозу, натрия кармеллозу, натрия кроскармеллозу, натрия карбокиметил-крахмала, кросповидон и т.д. Указанное дезинтегрирующее соединение может использоваться по отдельности либо два или более из них могут использоваться совместно. Дезинтегрирующее соединение используют в количестве, например, в пределах, от 0 до 10% по весу, предпочтительно в пределах от 0,5 до 5% по весу от веса таблетки в целом.
«Любрикант» включает, например, стеарат магния, тальк, полиэтиленгликоль, кремния диоксид, гидрогенизированное растительное масло и т.д.
Пероральный препарат настоящего изобретения может быть изготовлен в соответствии с традиционным способом, выбор которого зависит от необходимой формы дозирования.
(1) Изготовление водного раствора водорастворимого полимерного связующего соединения:
Водорастворимое полимерное связующее соединение растворяют в очищенной воде. Количество водорастворимого полимерного связующего соединения находится, например, в пределах от 1 до 20% по весу, предпочтительно в пределах от 2 до 8% веса очищенной воды.
(2) Изготовление гранул, включающих луразидон:
На гранулятор с псевдоожиженным слоем подают эксципиент, включающий луразидон, маннит и частично пептизированный крахмал и дезинтегрирующее соединение, туда же впрыскивают водорастворимое полимерное связующее соединение, изготовленное вышеуказанным способом (1), для последующей грануляции.
Установка для гранулирования включает, например, установку для гранулирования в псевдоожиженном слое, гранулирования при высоком усилии сдвига, роторного гранулирования в псевдоожиженном слое и т.д., но не ограничивается только ими.
(3) Высушивание гранул:
Полученные на предыдущем этапе гранулы высушивают либо при пониженном давлении, либо при атмосферном давлении. Сушку проводят так, чтобы потери в весе во время высушивания, измеренные инфракрасным анализатором влажности, составляли, например, до 3% по весу, предпочтительно от 1 до 2% по весу.
(4) Добавление вещества, облегчающего скольжение, при перемешивании:
К высушенным на предыдущем этапе гранулам (3) добавляют вещество, облегчающее скольжение, и перемешивают. Для перемешивания используют установку, например, с диффузионным типом смешивания [барабанного типа]. В частности, могут быть использованы барабанные смесители, V-образные смесители, биконусные смесители, вращающийся барабан, но не только они.
(5) Прессование:
Смесь, полученную, как описано выше, спрессовывают в форме таблетки.
Установка для прессования включает, например, таблеточный пресс. Степень прессования выбирают, например, в пределах от 30 до 200 Н.
(6) Необязательный этап покрытия гладкой оболочкой:
При необходимости возможно покрытие полученной, как описано выше, таблетки оболочкой. Установка для нанесения покрытия, например, включает барабан для нанесения покрытия. Предпочтительно использование перфорированной системы для нанесения покрытия.
Наносимое покрытие включает, например, смесь основного материала (например, гидроксипропилметилцеллюлозы, гидроксипропилцеллюлозы, поливинилпирролидона, поливинилового спирта и т.д.) и пластификатора (например, полиэтиленгликоля, пропиленгликоля, триацетина, триэтилцитрата, глицерина, глицеринового эфира жирной кислоты, полиэтиленгликоля и т.д.). Если необходимо, могут быть сделаны дополнительные добавки, как, например, оксид титана. После нанесения покрытия также может быть добавлен карнаубский воск и т.п. в качестве полирующего вещества.
(7) Высушивание:
Полученную, как описано выше, таблетку высушивают. Сушку проводят либо при пониженном давлении, либо при атмосферном давлении так, чтобы потери в весе во время высушивания, измеренные инфракрасным анализатором влажности, составляли, например, до 3% по весу, предпочтительно от 1 до 2% по весу.
Ниже приведены примеры, иллюстрирующие настоящее изобретение. Указанные примеры служат примерами настоящего изобретения, но оно не ограничивается только ими.
ПРИМЕРЫ
Пример 1
А. Покрытая оболочкой таблетка, включающая 80 мг луразидона (Пример 1)
Последовательно изготавливают гранулы, таблетки без оболочки и таблетки с пленочным покрытием, включающие перечисленные ниже компоненты. Используемые количества, указанные в скобках в нижеследующем описании, представляют собой примерную композицию Примера 1.
В соответствии с этим способом изготовления в принципе, могут быть изготовлены и другие примеры, в зависимости от композиции которых необходимо изменение используемых количеств.
В. Способ изготовления
(1) Изготовление раствора связующего соединения (5%-ный водный раствор гидроксипропилметилцеллюлозы):
Гидроксипропилметилцеллюлозу (32 г) в качестве водорастворимого полимерного связующего растворяли в очищенной воде (608 г) для получения раствора связующего соединения.
(2) Гранулирование:
Луразидон (320 г), маннит (576 г), частично пептизированный крахмал (320 г) и натрия кармеллозу (16 г) загружали в гранулятор с псевдоожиженным слоем (Multiplex МР-01/ производства компании Powrex Corporation), после чего смесь гранулировали путем распыления в соответствующих условиях с использованием раствора связующего соединения, изготовленного на этапе (1), для получения порошка гранул. К полученному порошку гранул добавляли стеарат магния, после чего получались гранулы для сжатия, обладающие композицией (b) после перемешивания (40 об/мин, 5 минут). Стеарат магния добавляли в количествах, рассчитанных с учетом выхода порошка гранул.
Условия грануляции
Температура подачи воздуха: 60°С
Расход воздуха: от 50 до 65 м3/час
Скорость распыления: 13 г/мин
Диаметр распыляющих сопел: 1,2 мм
Давление распыления: 0,12 МПа
Положение пистолета: среднее
(3) Прессование:
Гранулы для прессования, полученные на этапе (2), спрессовывали с помощью установки HT-AP12SS-II (производства компании Hata Iron Works Co., Ltd.) для получения таблеток.
Размер пестика: ⌀10 мм 14R
Толщина: от 4,20 до 4,30 мм
Давление пресса: 10 кН
(4) Покрытие оболочкой:
На таблетки без оболочки, полученные на этапе (3), наносили покрытие с использованием High Coater HCT30N (производства компании Freund Industrial Co., Ltd.) при соблюдении условий, указанных выше, так, чтобы количество нанесенного покрытия составляло 5 мг, после нанесения покрытия добавляли карнаубский воск для получения таблеток с пленочным покрытием.
Условия нанесения покрытия:
Температура подачи воздуха: 80°С
Расход воздуха: 0,6 м3/мин
Скорость вращения барабана: 25 об/мин
Давление распыления: 0,15 МПа
Скорость жидкого потока: 5 г/мин
Качество полученного описанным способом препарата оценивали с помощью способов, приведенных ниже, и результаты этой оценки использовали для достижения цели настоящего изобретения.
С. Оценка качества
(1) Тест на растворимость
Изготовленный препарат подвергали тесту на растворимость в соответствии с руководством «Japanese Pharmacopoeia, Dissolution test, Method 2». Условия измерения приведены ниже.
Тестовый раствор: разбавленный буфер McIlvaine, pH 4,0
Скорость вращения лопасти: 50 об/мин
Жидкость для проведения теста: 900 мл
(2) Подобие профилей растворения
Фактор подобия f2, приведенный в Scale-Up и Past-Approval Changes для Intermediate Release Products (SUPAC-IR), использовали в качестве показателя при оценке подобия профилей растворения. Значение f2 рассчитывают с помощью приведенного ниже уравнения. Для каждого из изготовленных препаратов считалось, что препарат обладает сходным профилем растворения в случае, когда значение f2, рассчитанное из степени растворения каждого отдельного препарата с помощью SUPAC-IR, было в пределах 50≤f2≤100. Значения степени растворения в трех временных точках - через 15 мин, 30 мин и 45 мин после начала теста использовали для расчета значения f2.
Ti и Ri - процент растворенного вещества в каждой временной точке,
n - количество сравниваемых точек.
(3) Гранулометрический состав
Гранулометрический состав луразидона анализировали методом сухого распыления с помощью анализатора Laser Diffraction Particle Size Analyzer (SLAD-3000/Shimadzu Corporation). Условия определения приведены ниже:
| Amounts of sample: 2 g | |||
| Air pressure: 0.4 MРa or more | |||
| Turntable rotation speed: 2 | |||
| Parameter setting | |||
| Environmental setting | |||
| Monitoring average: | Measuring optimum range | ||
| 16 | 1500 | ||
| (Max): | |||
| Dark measuring average: | 2 | (Min): | 700 |
| Light intensity | (CH-1) baud rate | ||
| 2000 | 9600 | ||
| display Max: | (bps): | ||
| Previous blank: | reading | Blank measurable Max: | 300 |
| Printer: monochrome | Blank measurable | ||
| 20 | |||
| variation range: | |||
| Refractive parameter | |||
| Standard refraction: | 1.70-0.20i | ||
| Measuring conditions setting | |||
| Measuring average: | 1 | Dry permissible Min: | 300 |
| Measuring interval (sec): | 1 | Max: | 2500 |
| Average: | Granule range | ||
| 64 | 0.1 | ||
| for evaluation (Min): | |||
| Measured absorbance | Granule range | ||
| 0.1 | 2000 | ||
| range (Max): | for evaluation (Max): | ||
| (Min): | 0.05 | Start position of sensor usage: | 1 |
| Trigger mode: | OFF | ||
| Dry threshold: | 300 |
<Тест 1>
В примерах 1, 2 и 3 были изготовлены таблетки, включающие специфические фармацевтические композиции, включающие водорастворимый эксципиент, включающий 20 мг, 40 мг и 80 мг соответственно, луразидона на одну таблетку, частично пептизированный крахмал и водорастворимое полимерное связующее соединение. В Сравнительных экспериментах 1 и 2 таблетки, включающие 40 мг и 80 мг соответственно, луразидона на одну таблетку, изготавливали на основе композиции, раскрытой в Патентном документе 2.
Изготовленные препараты подвергали тестам на растворимость в условиях, указанных в пунктах (d) и (е), после чего оценивали подобие профилей растворения. Дополнительно предварительная подготовка к Сравнительным экспериментам 1 и 2 описана в Тесте 8.
Результаты приведены в таблицах 4 и 5. Коэффициенты растворения в зависимости от времени в (d) приведены на фиг.2 и 3.
(а) Композиции гранулярных порошков
| Таблица 1 | |||||
| Единица измерения: мг | |||||
| Компонент | Пример № | Сравн. эксп. № | |||
| 1 | 2 | 3 | 1 | 2 | |
| Луразидон | 80 | 40 | 20 | 40 | 80 |
| Маннит | 144 | 72 | 36 | 188 | 148 |
| Частично пептизированный крахмал | 80 | 40 | 20 | - | - |
| Натрия кроскармеллоза | 4 | 2 | 1 | 16 | 16 |
| Гидроксипропилметилцеллюлоза | 8 | 4 | 2 | 10 | 10 |
(b) Композиции гранул для прессования/таблеток без оболочки
| Таблица 2 | |||||
| Единица измерения: мг | |||||
| Компонент | Пример № | Сравн. эксп. № | |||
| 1 | 1 | 1 | 1 | 2 | |
| Гранулы, как описано выше (а) | 316 | 158 | 79 | 254 | 254 |
| Лактоза | - | - | - | 62 | 62 |
| Стеарат магния | 4 | 2 | 1 | 4 | 4 |
(с) Композиции таблеток с пленочным покрытием
| Таблица 3 | |||||
| Единица измерения: мг | |||||
| Компонент | Пример № | Сравн. эксп. № | |||
| 1 | 2 | 3 | 1 | 2 | |
| Таблетки без оболочки, как описано выше (b) | 320 | 160 | 80 | 320 | 320 |
| Гидроксипропилметилцеллюлоза | 3,25 | 1,95 | 1,3 | 2,6 | 2,6 |
| Оксид титана | 1 | 0,6 | 0,4 | 0,8 | 0,8 |
| Полиэтиленгликоль 6000 | 0,75 | 0,45 | 0,3 | 0,6 | 0,6 |
| Карнаубский воск | 0,01 | 0,006 | 0,004 | 0,01 | 0,01 |
(d) Тест на растворимость в системе, включающей 80 мг луразидона в каждом сосуде
Каждую таблетку с пленочным покрытием, включающую 80 мг, 40 мг или 20 мг луразидона в системе, включающей 80 мг луразидона в каждом сосуде, подвергали тесту на растворимость, после чего оценивали подобие профилей растворения, используя значение f2.
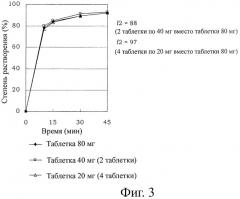
Как видно из таблицы 4, значения t2 в Примерах 2 и 3 указывают на сходство профилей с Примером 1, однако значения f2 в Сравнительном эксперименте 2 не указывают на сходство со Сравнительным экспериментом 1. Другими словами, как видно из таблицы 4 и фиг.3, в Примерах 1-3 значения f2, указывающие на сходство профилей растворения, были в пределах 50≤f2≤100 и были получены препараты, обладающие сходными профилями растворения, не меняющимися в зависимости от содержания ингредиента в таблетке (силы одной таблетки) даже в препаратах с различным содержанием. С другой стороны, как видно из таблицы 4 и фиг.2, растворение композиции, раскрытой в Патентном Документе 2, в Сравнительном эксперименте 2 было значительно медленнее, чем растворение двух таблеток препаратов в Сравнительном эксперименте 1, и не было продемонстрировано сходство профиля растворения, что детально описано в Тесте 8.
| Таблица 4 | |||||
| Фактор подобия | Пример № | Сравн. эксп. № | |||
| 1 | 2 | 3 | 1 | 2 | |
| f2 | - | 88 | 97 | - | 37 |
(е) Тест на растворимость в системе, включающей 40 мг луразидона в каждом сосуде
Каждую таблетку с пленочным покрытием, включающую 40 мг или 20 мг луразидона в системе, включающей 40 мг луразидона в каждом сосуде, подвергали тесту на растворимость, после чего оценивали подобие профилей растворения, используя значение f2, аналогичным способом.
Как видно из таблицы 5, значения f2 в Примере 3 и Сравнительном эксперименте 1 указывают на сходство с Примером 2. Другими словами, значения f2 были в пределах 50≤f2≤100 даже в системе, включающей 40 мг луразидона в каждом сосуде, и была продемонстрирована схожесть профилей растворения, не меняющихся в зависимости от содержания ингредиента в таблетке (силы одной таблетки).
| Таблица 5 | |||
| Фактор подобия | Пример № | Сравн. эксп. № | |
| 2 | 3 | 1 | |
| f2 | - | 88 | 97 |
<Тест 2>
Препараты, включающие фармацевтическую композицию, включающую водорастворимый эксципиент и водорастворимое полимерное связующее соединение, и частично пептизированный крахмал, были изготовлены в Примерах 1 и 4. Препараты, включающие фармацевтическую композицию, включающую водорастворимый эксципиент и водорастворимое полимерное связующее соединение и кукурузный крахмал, не являющийся предварительно пептизированным крахмалом, были изготовлены в Сравнительных экспериментах 3,4 и 5. Каждый препарат подвергали тесту на растворимость и сходство каждого профиля растворения оценивали по значению f2. Результаты приведены в таблице 9.
(а) Композиции гранулярных порошков
| Таблица 6 | |||||
| Единица измерения: мг | |||||
| Компонент | Пример № | Сравн. эксп. № | |||
| 1 | 4 | 3 | 4 | 5 | |
| Луразидон | 80 | 80 | 80 | 80 | 80 |
| Маннит | 144 | 176 | 108 | 108 | - |
| Лактоза | - | - | - | - | 108 |
| Частично пептизированный крахмал | 80 | 40 | - | - | - |
| Кукурузный крахмал | - | - | 40 | 40 | 40 |
| Натрия кроскармеллоза | 4 | 8 | 16 | 16 | 16 |
| Гидроксипропилметилцеллюлоза | 8 | 12 | 10 | 10 | 10 |
(b) Композиции гранул для прессования/таблеток без оболочки
| Таблица 7 | |||||
| Единица измерения: мг | |||||
| Компонент | Пример № | Сравн. эксп. № | |||
| 1 | 4 | 3 | 4 | 5 | |
| Гранулы, как описано выше (а) | 316 | 316 | 254 | 254 | 254 |
| Маннит | - | - | 62 | - | - |
| Стеарат магния | 4 | 4 | 4 | 4 | 4 |
(с) Композиции таблеток с пленочным покрытием
| Таблица 8 | |||||
| Единица измерения: мг | |||||
| Компонент | Пример № | Сравнительный эксперимент № | |||
| 1 | 4 | 3 | 4 | 5 | |
| Таблетки без оболочки, как описано выше (b) | 320 | 320 | 320 | 258 | 258 |
| Гидроксипропилметилцеллюлоза | 3,25 | - | 2,6 | 2,6 | 2,6 |
| Оксид титана | 1 | - | 0,8 | 0,8 | 0,8 |
| Полиэтиленгликоль 6000 | 0,75 | - | 0,6 | 0,6 | 0,6 |
(d) Тест на растворимость
Как видно из таблицы 9, Пример 4 был сходен с Примером 1, но значения f2 в Сравнительных экспериментах 3, 4 и 5 не обладали сходством с Примером 1. Другими словами, препараты, содержавшие кукурузный крахмал, в Сравнительных экспериментах 3, 4 и 5 демонстрировали отличные профили растворения и медленное растворение по сравнению с препаратами, содержавшими частично пептизированный крахмал в Примерах 1 и 4.
| Таблица 9 | |||||
| Фактор подобия | Пример № | Сравнительный эксперимент № | |||
| 1 | 4 | 3 | 4 | 5 | |
| f2 | - | 67 | 44 | 29 | 26 |
<Тест 3>
Оценивали эффект добавления частично пептизированного крахмала в различных количествах в Примерах 4, 5, 6 и 7 на растворимость. Результаты приведены в таблице 13.
(а) Композиции гранулярных порошков
| Таблица 10 | |||||
| Единица измерения: мг | |||||
| Компонент | Пример № | ||||
| 1 | 4 | 5 | 6 | 7 | |
| Луразидон | 80 | 80 | 80 | 80 | 80 |
| Маннит | 144 | 176 | 116 | 136 | 156 |
| Частично пептизированный крахмал | 80 | 40 | 100 | 80 | 60 |
| Натрия кроскармеллоза | 4 | 8 | 8 | 8 | 8 |
| Гидроксипропилметилцеллюлоза | 8 | 12 | 12 | 12 | 12 |
(b) Композиции гранул для прессования/таблеток без оболочки
| Таблица 11 | |||||
| Единица измерения: мг | |||||
| Компонент | Пример № | ||||
| 1 | 4 | 5 | 6 | 7 | |
| Гранулы, как описано выше (а) | 316 | 316 | 316 | 316 | 316 |
| Стеарат магния | 4 | 4 | 4 | 4 | 4 |
(с) Композиции таблеток с пленочным покрытием
| Таблица 12 | |||||
| Единица измерения: мг | |||||
| Компонент | Пример № | ||||
| 1 | 4 | 5 | 6 | 7 | |
| Таблетки без оболочки, как описано выше (b) | 320 | 320 | 320 | 320 | 320 |
| Гидроксипропилметилцеллюлоза | 3,25 | - | - | - | - |
| Оксид титана | 1 | - | - | - | - |
| Полиэтиленгликоль 6000 | 0,75 | - | - | - | - |
| Карнаубский воск | 0,01 | - | - | - | - |
(d) Тест на