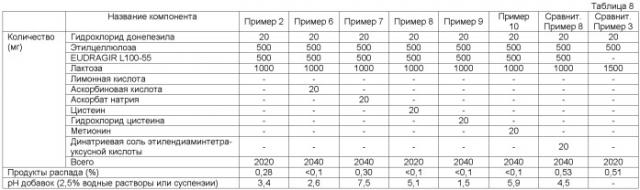
Способ стабилизации лекарственного средства против деменции
Иллюстрации
Показать всеИзобретение относится к фармакологическим средствам. Способ стабилизации лекарственного средства против деменции, в частности донепезила или его фармацевтически приемлемой соли, включает добавление высокомолекулярного кислого вещества. Кроме того, настоящее изобретение предлагает фармацевтическую композицию, содержащую лекарственное средство против деменции и высокомолекулярное основное вещество, а также высокомолекулярное кислое вещество, обеспечивающее стабилизацию лекарственного средства против деменции. Изобретение раскрывает способ промышленного получения фармацевтической композиции, который включает в себя стадии, на которых к смеси лекарственного средства против деменции и высокомолекулярного основного вещества добавляют раствор или суспензию, содержащие высокомолекулярное кислое вещество, с целью стабилизации лекарственного средства против деменции. Изобретение обеспечивает получение стабилизированного лекарственного средства против деменции. 6 н. и 14 з.п. ф-лы, 1 ил., 11 табл.
Реферат
Область техники
Настоящее изобретение относится к стабилизации лекарственного средства против деменции в композиции, содержащей лекарственное средство против деменции. Более конкретно, настоящее изобретение относится к стабилизации лекарственного средства против деменции в фармацевтической композиции, которая обладает параметрами замедленного высвобождения и включает в себя лекарственное средство против деменции, содержащее третичную аминогруппу.
Предпосылки создания изобретения
В последние годы лечение деменции, в том числе сенильной деменции, деменции альцгеймеровского типа и др., стало социальной проблемой и в связи с этим разрабатываются многочисленные лекарственные средства. Наиболее часто в качестве лекарственного средства для лечения легкой и умеренной формы деменции Альцгеймера используют донепезил, ингибирующий действие ацетилхолинэстеразы, который продается в виде гидрохлорида в форме таблеток или гранул. В последнее время для пациентов, имеющих проблемы с глотанием, разработаны таблетки, распадающиеся во рту, а в случаях, когда затруднено пероральное введение, предлагают чрезкожное введение с использованием препарата мази (например, см. патентный документ 1: выложенная патентная заявка Японии № H11-315016).
Разработка такой фармацевтической композиции, подходящей для пациентов с определенными состояниями и симптомами, является крайне важной с точки зрения совместимости или качества жизни. В данном контексте в качестве лекарственного средства против деменции можно использовать препарат с замедленным высвобождением, поскольку параметры замедленного высвобождения позволяют снизить число введений и при этом сохранить или улучшить терапевтические эффекты с потенциальным повышением совместимости.
Как правило, препараты с замедленным высвобождением, содержащие физиологически активное средство, можно подразделить на два типа, а именно (1) препараты матриксного типа, в которых равномерно распределены лекарственное средство и основа, обеспечивающая замедленное высвобождение, и (2) препараты с покрытием, в которых высвобождение регулируется покрытием поверхности центрального ядра частицы или таблетки, содержащей физиологически активное средство.
Матриксные препараты с замедленным высвобождением содержат матрикс, в котором однородно распределены лекарственное средство и основа, обеспечивающая замедленное высвобождение. Матрикс обычно используют в виде таблетки или гранулы, он может иметь светозащитное покрытие и т.п. Покрытые препараты с замедленным высвобождением включают в себя препараты, в которых покрытие, содержащее основу, обеспечивающую замедленное высвобождение, наносят на центральное ядро гранулы, таблетки или т.п., содержащую лекарственное средство, или препараты, в которых центральное ядро, состоящее из кристаллической целлюлозы или сахарозы, так называемую "нонпарель", покрывают вначале слоем, содержащим лекарственное средство, а затем покрытием, обеспечивающим замедленное высвобождение. В некоторых случаях параметры замедленного высвобождения также обеспечиваются несколькими слоями покрытия, содержащего лекарственное средство, или покрытия, содержащего основу, обеспечивающую замедленное высвобождение.
Однако, поскольку указанные препараты с замедленным высвобождением содержат основу, обеспечивающую замедленное высвобождение, и другие добавки, которые не входят в состав традиционных быстрорастворяющихся таблеток и т.п., следует соблюдать осторожность и следить, чтобы данные добавки не повлияли на стабильность лекарственного средства. В частности, многие лекарственные средства против деменции являются основными и содержат аминогруппу, зачастую, высоко реакционноспособную функциональную группу, такую как аминогруппа, которая является нуклеофильной и может легко продуцировать продукты распада при взаимодействии с карбонильным углеродом, пероксидом, кислородом и т.п.
Поскольку продукты распада лекарственного средства или добавок могут влиять на стабильность или эффективность фармацевтических продуктов, в области разработки препаратов проводится изучение способов предотвращения или существенного подавления образования таких продуктов распада. Что касается способов стабилизации лекарственного средства против деменции, раскрыта композиция, содержащая органическую кислоту, для стабилизации донепезила при воздействии света (например, см. патентный документ 2: выложенная патентная заявка Японии № H11- 106353). Описано, что светозащитный эффект обусловлен добавлением органической кислоты к донепезилу в водно-этанольном растворе и что доля оставшегося донепезила выше в растворе, к которому добавлена паратолуолсульфоновая кислота, метилсульфоновая кислота, лимонная или другая кислота, чем в растворе, не содержащем органических кислот.
Описание изобретения
Таким образом, существует потребность в фармацевтической композиции, которая улучшает совместимость лекарственного средства против деменции, такой как фармацевтическая композиция с параметрами замедленного высвобождения. С другой стороны, как и обычные лекарственные средства, препарат с замедленным высвобождением должен удовлетворять требованиям стабильности при хранении. Кроме того, поскольку лекарственное средство против деменции зачастую вводят в течение длительного периода, даже в случае препарата, имеющего свойство замедленного высвобождения, существует потребность в разработке фармацевтической композиции, а также простого и дешевого способа промышленного получения такой композиции. Соответственно, целью настоящего изобретения является обеспечение стабилизации лекарственного средства против деменции в фармацевтической композиции, содержащей лекарственное средство против деменции. Более конкретно, целью настоящего изобретения является предоставление фармацевтической композиции, содержащей лекарственное средство против деменции, которая обладает параметрами замедленного высвобождения и обеспечивает превосходную стабильность лекарственного средства против деменции, а также способа промышленного получения фармацевтической композиции и способа стабилизации лекарственного средства против деменции в фармацевтической композиции.
Для достижения указанных целей авторы настоящего изобретения провели обширные исследования фармацевтических композиций, содержащих лекарственные средства против деменции. В результате было обнаружено, что в матриксном препарате с замедленным высвобождением, содержащем гидрохлорид донепезила в качестве лекарственного средства против деменции и этилцеллюлозу, которая представляет собой высокомолекулярное основное вещество, в качестве основы, обеспечивающей замедленное высвобождение, образуются продукты распада гидрохлорида донепезила, а высокомолекулярное кислое вещество эффективно предотвращает или подавляет образование продуктов распада, образующихся при контактировании лекарственного средства против деменции с высокомолекулярным основным веществом, которым является основа, обеспечивающая замедленное высвобождение, причем высокомолекулярное кислое вещество оказывает совместное действие с низкомолекулярным кислым веществом и антиоксидантом, что и составляет предмет настоящего изобретения.
Соответственно, настоящее изобретение относится к фармацевтической композиции, содержащей лекарственное средство против деменции и основу, обеспечивающую замедленное высвобождение, причем лекарственное средство против деменции обладает превосходной стабильностью при хранении, где композиция содержит высокомолекулярное кислое вещество, обеспечивающее стабильность лекарственного средства против деменции. В качестве высокомолекулярного кислого вещества можно использовать коммерчески доступное энтеросолюбильное полимерное вещество и т.п., которое легко смешивается или гранулируется вместе с лекарственным средством против деменции и основой, обеспечивающей замедленное высвобождение, и тем самым позволяет разработать простой способ промышленного получения фармацевтической композиции настоящего изобретения.
В первом аспекте настоящее изобретение относится к способу стабилизации лекарственного средства против деменции, который включает в себя добавление высокомолекулярного кислого вещества в фармацевтическую композицию, содержащую лекарственное средство против деменции и высокомолекулярное основное вещество. Добавление высокомолекулярного кислого вещества может подавлять образование продуктов распада лекарственного средства против деменции, которые образуются в результате контакта лекарственного средства против деменции с высокомолекулярным основным веществом. Кроме того, в предпочтительном аспекте настоящего изобретения предлагается способ стабилизации лекарственного средства против деменции, включающий в себя добавление в фармацевтическую композицию настоящего изобретения, по меньшей мере, одного вещества, выбранного из низкомолекулярного кислого вещества и антиоксиданта.
Во втором аспекте настоящее изобретение предлагает фармацевтическую композицию, содержащую лекарственное средство против деменции и высокомолекулярное основное вещество, причем для стабилизации лекарственного средства против деменции в состав композиции вводят высокомолекулярное кислое вещество. Фармацевтическая композиция настоящего изобретения также содержит, по меньшей мере, одно вещество, выбранное из низкомолекулярного кислого вещества и антиоксиданта. Более конкретно, фармацевтическая композиция представляет собой такую композицию, как матриксный препарат с замедленным высвобождением, который содержит матрикс, представляющий собой смесь лекарственного средства против деменции, высокомолекулярного основного вещества и высокомолекулярного кислого вещества для стабилизации лекарственного средства против деменции, или такую композицию, как покрытый препарат с замедленным высвобождением, который содержит центральное ядро с лекарственным средством против деменции и покрывающий слой, включающий в себя высокомолекулярное основное вещество, нанесенное на вышеуказанное центральное ядро, где высокомолекулярное кислое вещество смешивают, по меньшей мере, с центральным ядром или вышеуказанным покрывающим слоем.
В частности, фармацевтическая композиция настоящего изобретения представляет собой фармацевтическую композицию, содержащую: (1) основное лекарственное средство, или его соль, растворимость которых в 0,1 N растворе хлористоводородной кислоты и 50 мМ фосфатном буфере, pH 6, составляет 1 мг/мл или более, а растворимость в 50 мМ фосфатном буфере, pH 8, составляет 0,2 мг/мл или менее, причем растворимость основного лекарственного средства или его соли в 50 мМ фосфатном буфере, pH 6,8, по меньшей мере, в два раза превышает их растворимость в 50 мМ фосфатном буфере, pH 8, и составляет не более половины от их растворимости в 50 мМ фосфатном буфере, pH 6; (2), по меньшей мере, одно энтеросолюбильное полимерное вещество (высокомолекулярное кислое вещество) и (3), по меньшей мере, одно нерастворимое в воде полимерное вещество (высокомолекулярное основное вещество).
В третьем аспекте настоящее изобретение предлагает способ промышленного получения, обеспечивающий эффективное достижение стабилизации лекарственного средства против деменции настоящего изобретения, другими словами, способ промышленного получения фармацевтической композиции, содержащей лекарственное средство против деменции и высокомолекулярное основное вещество, включающий в себя стадии смешивания и гранулирования, где к смеси лекарственного средства против деменции и высокомолекулярного основного вещества добавляют высокомолекулярное кислое вещество для стабилизации лекарственного средства против деменции в процессе, по меньшей мере, одной из стадий смешивания и гранулирования. В соответствии с предпочтительным аспектом способа промышленного получения настоящего изобретения, для стабилизации лекарственного средства против деменции помимо высокомолекулярного кислого вещества можно добавить, по меньшей мере, низкомолекулярное кислое вещество или антиоксидант. В более предпочтительном аспекте, по меньшей мере, высокомолекулярное кислое вещество, низкомолекулярное кислое вещество и антиоксидант добавляют в виде раствора или суспензии в процессе, по меньшей мере, одной из стадий смешивания и гранулирования. В особенно предпочтительном аспекте способа промышленного получения настоящего изобретения, после добавления высокомолекулярного кислого вещества в виде порошка на стадии смешивания, по меньшей мере, низкомолекулярное кислое вещество или антиоксидант можно добавить к смеси в виде раствора или суспензии на стадии гранулирования.
Кроме того, в третьем аспекте настоящее изобретение предлагает способ промышленного получения фармацевтической композиции, включающий в себя стадии: смешивания (1) основного лекарственного средства, или его соли, растворимость которых в 0,1 N растворе хлористоводородной кислоты и 50 мМ фосфатном буфере, pH 6, составляет 1 мг/мл или более, а растворимость в 50 мМ фосфатном буфере, pH 8, составляет 0,2 мг/мл или менее, причем растворимость в 50 мМ фосфатном буфере, pH 6,8, по меньшей мере, в два раза превышает их растворимость в 50 мМ фосфатном буфере, pH 8, и составляет не более половины от его растворимости в 50 мМ фосфатном буфере, pH 6; с (2), по меньшей мере, одним энтеросолюбильным полимерным веществом (высокомолекулярное кислое вещество) и (3), по меньшей мере, одним нерастворимым в воде полимерным веществом (высокомолекулярное основное вещество); и формование прессованием смеси, полученной на стадии смешивания.
Далее, в четвертом аспекте настоящее изобретение предлагает применение высокомолекулярного кислого вещества для подавления образования продуктов распада лекарственного средства против деменции в результате контактирования лекарственного средства против деменции с высокомолекулярным основным веществом. Это новый способ применения, который раскрывается для высокомолекулярных кислых веществ. В данном случае образование продуктов распада можно эффективно подавлять путем дополнительного применения низкомолекулярного кислого вещества и антиоксиданта.
В соответствии с предпочтительным аспектом настоящего изобретения лекарственное средство против деменции представляет собой соединение, содержащее третичную аминогруппу. В соответствии с более предпочтительным аспектом настоящего изобретения лекарственное средство против деменции выбрано из группы, состоящей из ривастигмина, галантамина, донепезила, 3-[1-(фенилметил)пиперидин-4-ил]-1-(2,3,4,5-тетрагидро-1H-1-бензазепин-8-ил)-1-пропана, 5,7-дигидро-3-[2-[1-(фенилметил)-4-пиперидинил]этил]-6H-пирроло[4,5-f]-1,2-бензизоксазол-6-она и их фармацевтически приемлемых солей. В особенно предпочтительном аспекте лекарственное средство против деменции представляет собой донепезил или его фармацевтически приемлемую соль.
Кроме того, в соответствии с предпочтительным аспектом настоящего изобретения высокомолекулярное основное вещество представляет собой, по меньшей мере, одно вещество, выбранное из группы, состоящей из этилцеллюлозы, сополимера этилакрилата и метилметакрилата и полиэтиленоксида. В более предпочтительном аспекте высокомолекулярное основное вещество представляет собой либо этилцеллюлозу, либо сополимер этилакрилата и метилметакрилата, и в особенно предпочтительном аспекте высокомолекулярное основное вещество представляет собой этилцеллюлозу. В качестве высокомолекулярного основного вещества также можно использовать любое нерастворимое в воде полимерное вещество.
Далее, в соответствии с предпочтительным аспектом настоящего изобретения, высокомолекулярное кислое вещество представляет собой энтеросолюбильное полимерное вещество. В более предпочтительном аспекте высокомолекулярное кислое вещество представляет собой, по меньшей мере, одно вещество, выбранное из группы, состоящей из сополимера метакриловой кислоты и этилакрилата, сополимера метакриловой кислоты и метилметакрилата, фталата гидроксипропилметилцеллюлозы и ацетата сукцината гидроксипропилметилцеллюлозы. В особенно предпочтительном аспекте высокомолекулярное кислое вещество представляет собой сополимер метакриловой кислоты и этилакрилата. В предпочтительном аспекте количество высокомолекулярного кислого вещества обычно составляет от 0,1 до 90 частей по массе, предпочтительно от 1 до 70 частей по массе, более предпочтительно от 5 до 60 частей по массе, еще более предпочтительно от 10 до 50 частей по массе, по отношению к 100 массовым частям фармацевтической композиции настоящего изобретения.
Далее, в соответствии с предпочтительным аспектом настоящего изобретения низкомолекулярное кислое вещество представляет собой, по меньшей мере, одно, выбранное из группы, состоящей из карбоновых кислот, сульфоновых кислот, гидроксильных кислот, кислых аминокислот и неорганических кислот. В более предпочтительном аспекте низкомолекулярное кислое вещество представляет собой, по меньшей мере, одно, выбранное из группы, состоящей из гидроксильных кислот, кислых аминокислот и неорганических кислот. В особенно предпочтительном аспекте низкомолекулярное кислое вещество представляет собой, по меньшей мере, одно, выбранное из группы, состоящей из гидроксильных кислот и кислых аминокислот.
Более конкретно, низкомолекулярное кислое вещество представляет собой, по меньшей мере, одно, выбранное из группы, состоящей из янтарной кислоты, винной кислоты, лимонной кислоты, фумаровой кислоты, малеиновой кислоты, яблочной кислоты, аспарагиновой кислоты, глутаминовой кислоты, гидрохлорида глутаминовой кислоты, хлористоводородной кислоты и фосфорной кислоты. В более предпочтительном аспекте низкомолекулярное кислое вещество представляет собой, по меньшей мере, одно, выбранное из группы, состоящей из янтарной кислоты, винной кислоты, лимонной кислоты, яблочной кислоты, аспарагиновой кислоты, глутаминовой кислоты, гидрохлорида глутаминовой кислоты, хлористоводородной кислоты и фосфорной кислоты. В особенно предпочтительном аспекте низкомолекулярное кислое вещество представляет собой, по меньшей мере, одно, выбранное из группы, состоящей из лимонной кислоты, аспарагиновой кислоты и хлористоводородной кислоты. Количество низкомолекулярного кислого вещества обычно составляет от 0,05 до 4 частей по массе, предпочтительно от 0,1 до 3 частей по массе, более предпочтительно от 0,15 до 2 частей по массе, еще более предпочтительно от 0,15 до 1,5 частей по массе, по отношению к 100 массовым частям фармацевтической композиции настоящего изобретения. В соответствии с предпочтительным аспектом настоящего изобретения антиоксидант представляет собой, по меньшей мере, одну из аскорбиновых кислот и серосодержащих аминокислот. В более предпочтительном аспекте антиоксидант представляет собой, по меньшей мере, одно вещество, выбранное из группы, состоящей из метионина, аскорбиновой кислоты и гидрохлорида цистеина. Количество антиоксиданта обычно составляет от 0,01 до 10 частей по массе, предпочтительно от 0,02 до 5 частей по массе, более предпочтительно от 0,05 до 2 частей по массе, по отношению к 1 массовой части лекарственного средства. Хотя количество антиоксиданта особо не ограничивается, обычно оно составляет, например, от 0,001 до 5 частей по массе, предпочтительно от 0,01 до 3 частей по массе, более предпочтительно от 0,1 до 2 частей по массе, еще более предпочтительно от 0,15 до 1,5 частей по массе, по отношению к 100 массовым частям фармацевтической композиции настоящего изобретения.
Фармацевтическая композиция в соответствии с первым-третьим аспектами настоящего изобретения предпочтительно представляет собой препарат с замедленным высвобождением, более предпочтительно матриксный препарат с замедленным высвобождением. Примеры лекарственных форм фармацевтической композиции предпочтительно включают в себя таблетки, капсулы, гранулы или мелкие гранулы. Таким образом, фармацевтическая композиция в соответствии с особенно предпочтительным аспектом настоящего изобретения представляет собой матриксный препарат с замедленным высвобождением, содержащий донепезил или его фармацевтически приемлемую соль, высокомолекулярное основное вещество и высокомолекулярное кислое вещество, или матриксный препарат с замедленным высвобождением, содержащий донепезил или его фармацевтически приемлемую соль, высокомолекулярное основное вещество, высокомолекулярное кислое вещество и, по меньшей мере, один из низкомолекулярного кислого вещества и антиоксиданта.
Преимущества данного изобретения
В соответствии с настоящим изобретением для фармацевтической композиции, содержащей лекарственное средство против деменции и основу, обеспечивающую замедленное высвобождение, предлагается способ предотвращения или подавления образования продуктов распада в результате контактирования лекарственного средства против деменции с основой, обеспечивающей замедленное высвобождение, а именно, настоящее изобретение предлагает способ стабилизации лекарственного средства против деменции в фармацевтической композиции. Кроме того, поскольку фармацевтическая композиция настоящего изобретения обладает высоким качеством и соответствует требованиям совместимости, настоящее изобретение предлагает фармацевтические продукты, в частности лекарственные средства против деменции, употребление которых не причиняет беспокойства и является необременительным для пациентов и лиц, ухаживающих за ними. Настоящее изобретение также предлагает простой способ промышленного получения фармацевтической композиции с контролируемыми параметрами замедленного высвобождения и стабилизацией лекарственного средства против деменции без применения особых методов нанесения покрытия или особого оборудования.
Краткое описание чертежей
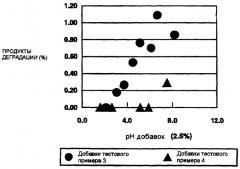
На фиг. 1 показана зависимость количества продуктов распада, образующихся после хранения гранул, содержащих разные добавки, в открытом (негерметичном) контейнере в течение 2 недель при 60°С и 75% RH от pH 2,5% водных растворов или суспензий, содержащих разные добавки.
Наилучший способ осуществления изобретения
Далее разъясняются воплощения настоящего изобретения. Нижеследующие воплощения приводятся в качестве примеров для разъяснения настоящего изобретения и не должны восприниматься как ограничение настоящего изобретения. Настоящее изобретение можно осуществлять разными способами, не отступая от сущности и объема изобретения.
(Лекарственное средство против деменции)
Специальных ограничений по лекарственному средству против деменции, используемому в настоящем изобретении, не существует, при условии, что лекарственное средство против деменции представляет собой основное лекарственное средство, содержащее первичную, вторичную или третичную аминогруппу, однако предпочтительно, если лекарственное средство против деменции содержит третичную аминогруппу. Примеры лекарственного средства против деменции, содержащего первичную аминогруппу, включают в себя такрин, мемантин и их фармацевтически приемлемые соли. Примеры лекарственного средства против деменции, содержащего третичную аминогруппу, включают в себя ривастигмин, галантамин, донепезил, 3-[1-(фенилметил)пиперидин-4-ил]-1-(2,3,4,5-тетрагидро-1H-1-бензазепин-8-ил)-1-пропан и 5,7-дигидро-3-[2-[1-(фенилметил)-4-пиперидинил]этил]-6H-пирроло[4,5-f]-1,2-бензизоксазол-6-она и их фармацевтически приемлемые соли. Предпочтительными примерами лекарственного средства против деменции, содержащего первичную аминогруппу, являются такрин и гидрохлорид мемантина. Предпочтительными примерами лекарственного средства против деменции, содержащего третичную аминогруппу, являются тартрат ривастигмина, гидробромид галантамина, гидрохлорид донепезила (химическое название моногидрохлорид (+-)-2-[(1-бензилпиперидин-4-ил)метил]-5,6-диметоксииндан-1-она), фумарат 3-[1-(фенилметил)пиперидин-4-ил]-1-(2,3,4,5-тетрагидро-1H-1-бензазепин-8-ил)-1-пропана (TAK-147) и малеат 5,7-дигидро-3-[2-[1-(фенилметил)-4-пиперидинил]этил]-6H-пирроло[4,5-f]-1,2-бензизоксазол-6-она (CP118954). Более предпочтительно, лекарственное средство против деменции представляет собой гидрохлорид донепезила, TAK-147 или CP118954, и наиболее предпочтительно лекарственное средство против деменции представляет собой гидрохлорид донепезила. Следует отметить, что лекарственное средство против деменции можно использовать либо в свободном виде, либо в виде органической или неорганической соли, причем предпочтительно его использовать в виде органической или неорганической соли, особенно предпочтительно в виде неорганической соли. Конкретные примеры солей включают в себя, без ограничения, гидрохлориды, сульфаты, ацетаты, фосфаты, карбонаты, мезилаты, тартраты, цитраты, тозилаты и т.п.
Не существует особых ограничений по растворимости основного лекарственного средства или его соли, используемых в настоящем изобретении, в случае кислых водных растворов, нейтральных водных растворов или основных водных растворов, однако растворимость основного лекарственного средства или его соли в кислом водном растворе и нейтральном водном растворе должна быть выше, чем растворимость в основном водном растворе. Примеры указанных водных растворов, используемых в настоящем изобретении, включают в себя, без ограничения, фосфатный буфер (например, буфер, полученный с использованием 50 мM раствора фосфата натрия и хлористоводородной кислоты), такие буферы как буфер Миллера (G. L. Miller's buffer), буфер Аткинса-Пантина (Atkins-Pantin's buffer), буфер Гуда (Good's buffer) и т.п., 0,1 N хлористоводородную кислоту, 0,1 моль/л раствор гидроксида натрия и т.п. Следует отметить, что упоминаемую в настоящем изобретении растворимость определяют в растворе при 25°C.
Термин "растворимость в кислом водном растворе" в настоящем изобретении относится к растворимости основного лекарственного средства или его соли в растворе, имеющем кислые свойства, при растворении основного лекарственного средства или его соли в буфере и т.п. Подобным образом термин "растворимость в нейтральном (основном) водном растворе" в настоящем изобретении относится к растворимости основного лекарственного средства или его соли в растворе, имеющем нейтральные (основные) свойства, при растворении основного лекарственного средства или его соли в буфере и т.п.
Например, растворимость используемого в настоящем изобретении основного лекарственного средства или его соли в кислом водном растворе, pH 3,0, и нейтральном водном растворе, pH 6,0, выше, чем в основном водном растворе, pH 8,0. Термин "растворимость в кислом водном растворе, pH 3,0" в данном описании относится к растворимости основного лекарственного средства или его соли в кислом растворе, имеющем pH 3,0, при растворении основного лекарственного средства или его соли в буфере и т.п. Термин "растворимость в нейтральном водном растворе, pH 6,0" в данном описании относится к растворимости основного лекарственного средства или его соли в растворе, имеющем pH 6,0, при растворении основного лекарственного средства или его соли в буфере и т.п. Подобным образом термин "растворимость в основном водном растворе, pH 8,0" в данном описании относится к растворимости основного лекарственного средства или его соли в растворе, имеющем pH 8,0, при растворении основного лекарственного средства или его соли в буфере и т.п.
В другом примере растворимость используемого в настоящем изобретении основного лекарственного средства или его соли в 0,1 N растворе хлористоводородной кислоты и нейтральном водном растворе, pH 6,0, выше, чем в основном водном растворе, pH 8,0. Термин "растворимость в 0,1 N растворе хлористоводородной кислоты" в данном описании относится к растворимости основного лекарственного средства или его соли при растворении основного лекарственного средства или его соли в 0,1 N растворе хлористоводородной кислоты. Например, раствор гидрохлорида донепезила в 0,1 N растворе хлористоводородной кислоты имеет pH в интервале приблизительно от 1 до 2.
Предпочтительно растворимость используемого в настоящем изобретении основного лекарственного средства или его соли в 0,1 N растворе хлористоводородной кислоты и нейтральном водном растворе, pH 6,0, выше, чем в основном водном растворе, pH 8,0, а растворимость в нейтральном водном растворе, pH 6,8, по меньшей мере, в два раза превышает его растворимость в основном водном растворе, pH 8,0, и составляет не более половины от его растворимости в нейтральном водном растворе, pH 6,0. Термин "растворимость в нейтральном водном растворе, pH 6,8" в данном описании относится к растворимости основного лекарственного средства или его соли в растворе, имеющем pH 6,8, при растворении основного лекарственного средства или его соли в буфере и т.п.
Более конкретно, не существует особых ограничений, при условии, что растворимость основного лекарственного средства или его соли в 0,1 N растворе хлористоводородной кислоты и нейтральном водном растворе, pH 6,0, составляет 1 мг/мл или более, растворимость основного лекарственного средства или его соли в основном водном растворе, pH 8,0, составляет 0,2 мг/мл или менее, и растворимость основного лекарственного средства или его соли в нейтральном водном растворе, pH 6,8, в два или более раз превышает его растворимость в основном водном растворе, pH 8,0, и составляет не более половины от его растворимости в нейтральном водном растворе, pH 6,0. То есть растворимость основного лекарственного средства или его соли в 0,1 N растворе хлористоводородной кислоты и нейтральном водном растворе, pH 6,0, особо не ограничивается, при условии, что вышеуказанная растворимость составляет 1 мг/мл или более. Вышеуказанная растворимость обычно составляет от 1 до 1000 мг/мл, предпочтительно от 5 до 200 мг/мл, более предпочтительно от 5 до 100 мг/мл, еще более предпочтительно от 10 до 80 мг/мл. Растворимость основного лекарственного средства или его соли в основном водном растворе, pH 8,0, особо не ограничивается, при условии, что вышеуказанная растворимость составляет 0,2 мг/мл или менее. Вышеуказанная растворимость обычно составляет от 0,0001 до 0,2 мг/мл, предпочтительно от 0,0005 до 0,1 мг/мл, более предпочтительно от 0,001 до 0,05 мг/мл, еще более предпочтительно от 0,002 до 0,03 мг/мл. Кроме того, растворимость основного лекарственного средства или его соли в нейтральном водном растворе, pH 6,8, особо не ограничивается, при условии, что вышеуказанная растворимость, по меньшей мере, в два раза превышает его растворимость в основном водном растворе, pH 8,0, и составляет не более 1/2 от его растворимости в нейтральном водном растворе, pH 6,0. Вышеуказанная растворимость предпочтительно, по меньшей мере, в 3 раза превышает растворимость в основном водном растворе, pH 8,0, и составляет не более 1/3 от растворимости в нейтральном водном растворе, pH 6,0, более предпочтительно, по меньшей мере, в 5 раз превышает растворимость в основном водном растворе, pH 8,0, и составляет не более 1/5 от растворимости в нейтральном водном растворе, pH 6,0, еще более предпочтительно, по меньшей мере, в 10 раз превышает растворимость в основном водном растворе, pH 8,0, и составляет не более 1/10 от растворимости в нейтральном водном растворе, pH 6,0.
В следующем примере растворимость используемого в настоящем изобретении основного лекарственного средства или его соли в 0,1 N растворе хлористоводородной кислоты и 50 мМ фосфатном буфере, pH 6,0, выше, чем его растворимость в 50 мМ фосфатном буфере, pH 8,0. Термин "растворимость в 50 мМ фосфатном буфере, pH 6,0" в данном описании относится к растворимости основного лекарственного средства или его соли в 50 мМ фосфатном буфере, имеющем pH 6,0, при растворении основного лекарственного средства или его соли в 50 мМ фосфатном буфере. Подобным образом термин "растворимость в 50 мМ фосфатном буфере, pH 8,0" в данном описании относится к растворимости основного лекарственного средства или его соли в 50 мМ фосфатном буфере, имеющем pH 8,0, при растворении основного лекарственного средства или его соли в 50 мМ фосфатном буфере.
Предпочтительно растворимость основного лекарственного средства или его соли в 0,1 N растворе хлористоводородной кислоты и 50 мМ фосфатном буфере, pH 6,0, выше, чем его растворимость в 50 мМ фосфатном буфере, pH 8,0, и растворимость в 50 мМ фосфатном буфере, pH 6,8, в два или более раз превышает растворимость в 50 мМ фосфатном буфере, pH 8,0, и составляет не более половины от его растворимости в 50 мМ фосфатном буфере, pH 6,0. Более конкретно, не существует особых ограничений, при условии, что растворимость основного лекарственного средства или его соли в 0,1 N растворе хлористоводородной кислоты и 50 мМ фосфатном буфере, pH 6,0, составляет 1 мг/мл или более, растворимость основного лекарственного средства или его соли в 50 мМ фосфатном буфере, pH 8,0, составляет 0,2 мг/мл или менее, и растворимость основного лекарственного средства или его соли в 50 мМ фосфатном буфере, pH 6,8, в два или более раз превышает его растворимость в 50 мМ фосфатном буфере, pH 8,0, и составляет не более половины от его растворимости в 50 мМ фосфатном буфере, pH 6,0. То есть растворимость основного лекарственного средства или его соли в 0,1 N растворе хлористоводородной кислоты и 50 мМ фосфатном буфере, pH 6,0, особо не ограничивается, при условии, что вышеуказанная растворимость составляет 1 мг/мл или более. Вышеуказанная растворимость обычно составляет от 1 до 1000 мг/мл, предпочтительно от 5 до 200 мг/мл, более предпочтительно от 5 до 100 мг/мл, еще более предпочтительно от 10 до 80 мг/мл. Растворимость основного лекарственного средства или его соли в 50 мМ фосфатном буфере, pH 8,0, особо не ограничивается, при условии, что вышеуказанная растворимость составляет 0,2 мг/мл или менее. Вышеуказанная растворимость обычно составляет от 0,0001 до 0,2 мг/мл, предпочтительно от 0,0005 до 0,1 мг/мл, более предпочтительно от 0,001 до 0,05 мг/мл, еще более предпочтительно от 0,002 до 0,03 мг/мл. Более того, растворимость основного лекарственного средства или его соли в 50 мМ фосфатном буфере, pH 6,8, особо не ограничивается, при условии, что вышеуказанная растворимость, по меньшей мере, в два раза превышает его растворимость в 50 мМ фосфатном буфере, pH 8,0, и составляет не более 1/2 от его растворимости в 50 мМ фосфатном буфере, pH 6,0. Вышеуказанная растворимость предпочтительно, по меньшей мере, в 3 раза превышает растворимость в 50 мМ фосфатном буфере, pH 8,0, и составляет не более 1/3 от растворимости в 50 мМ фосфатном буфере, pH 6,0, более предпочтительно по меньшей мере, в 5 раз превышает растворимость в 50 мМ фосфатном буфере, pH 8,0, и составляет не более 1/5 от растворимости в 50 мМ фосфатном буфере, pH 6,0, еще более предпочтительно, по меньшей мере, в 10 раз превышает растворимость в 50 мМ фосфатном буфере, pH 8,0, и составляет не более 1/10 от растворимости в 50 мМ фосфатном буфере, pH 6,0.
Например, растворимость гидрохлорида донепезила в кислом водном растворе, pH 3,0, и в нейтральном водном растворе, pH 6,0, составляет от 11 до 16 мг/мл, а в основном водном растворе, pH 8,0, она составляет 0,1 мг/мл или менее. Более того, гидрохлорид донепезила представляет собой слабоосновное лекарственное средство, или его соль, содержащее одну третичную аминогруппу, которое широко используется для лечения деменции при болезни Альцгеймера, и характеризуется растворимостью в нейтральном водном растворе, pH 6,8, которая, по меньшей мере, в два раза превышает растворимость в основном водном растворе, pH 8,0, и составляет не более 1/2 от растворимости в нейтральном водном растворе, pH 6,0.
Альтернативно, гидрохлорид донепезила представляет собой слабоосновное лекарственное средство, или его соль, содержащее одну третичную аминогруппу, которое широко используется для лечения деменции при болезни Альцгеймера. Растворимость гидрохлорида донепезила составляет от 11 до 16 мг/мл в 0,1 N растворе хлористоводородной кислоты и 50 мМ фосфатном буфере, pH 6,0, и 0,1 мг/мл или менее в 50 мМ фосфатном буфере, pH 8,0, причем растворимость в 50 мМ фосфатном буфере, pH 6,8, по меньшей мере, в два раза превышает растворимость в 50 мМ фосфатном буфере, pH 8,0, и составляет не более 1/2 от растворимости в 50 мМ фосфатном буфере, pH 6,0.
Не существует особых ограничений по величине дозы лекарственного средств