Производные 4-фенил-5-оксо-1, 4, 5, 6, 7, 8-гексагидрохинолина в качестве лекарственных средств для лечения бесплодия
Иллюстрации
Показать всеИзобретение относится к новым производным 4-фенил-5-оксо-1,4,5,6,7,8-гексагидрохинолина, представленным формулой I,
где R1 представляет собой (1-6С)алкил; R2 представляет собой галоген, (1-4С)алкокси; R3 представляет собой ОН, NO2, CN, фторированный (1-4С)алкокси, (1-4С)алкокси(2-4С)алкокси, гидрокси(2-4С)алкокси, (1-4С)алкоксикарбонил, R7,R8-амино, R9,Rl0-амино, R9,Rl0-аминокарбонил, R9,Rl0-аминосульфонил или фенил(1-4С)алкокси, где фенильное кольцо в составе фенил(1-4С)алкокси необязательно замещено одним или несколькими заместителями, выбранными из (1-4С)алкокси; R4 представляет собой R11-фенил или R11-(4-5С)гетероарил, который представляет собой гетероароматическую группу, содержащую 4-5 атомов углерода и по меньшей мере один гетероатом, выбранный из N и S, где фенильная или гетероарильная группа необязательно дополнительно замещена одним или несколькими заместителями, выбранными из нитро, (1-4С)алкила, (1-4С)алкокси; R7 представляет собой Н, (1-4С)алкил; R8 представляет собой (1-4С)алкилсульфонил, (1-4С)алкилкарбонил, (1-4С)алкоксикарбонил, (1-4С)алкокси(1-4С)алкилкарбонил, фурилкарбонил; фенил(1-4С)алкилкарбонил, где фенильное кольцо необязательно замещено одним или несколькими заместителями, выбранными из (1-4С)алкокси; R9 и R10 необязательно выбраны из Н, (1-6С)алкила и (1-4С)алкокси(2-4С)алкила; или R9 и R10 могут быть соединены вместе с образованием морфолинильного кольца; R11 представляет собой Н, R12,R13-амино, R14,R15-аминокарбонил или R14,R15-аминосульфонил; R12 представляет собой H;R13 представляет собой (1-4С)алкилсульфонил, (1-4С)алкилкарбонил, (1-4С)алкоксикарбонил или пиперазинил(1-4С)алкилкарбонил; R14 и R15 независимо выбраны из Н, (1-6С)алкила, (1-4С)алкокси(2-4С)алкила и имидазолил(1-4С)алкила; Х представляет собой О или R16-N; Y представляет собой СН2 или C(O); Z представляет собой CN; R16 представляет собой Н, (1-4С)алкил, (1-4С)алкилкарбонил; или к их фармацевтически приемлемым солям.
Изобретение также относится к фармацевтической композиции, а также к применению производных 4-фенил-5-оксо-1,4,5,6,7,8-гексагидрохинолина по любому из п.п.1-10. Технический результат - получение новых биологически активных соединений, обладающих агонистической активностью в отношении рецептора FSH. 3 н. и 10 з.п. ф-лы.
Реферат
Настоящее изобретение относится к производным 4-фенил-5-оксо-1,4,5,6,7,8-гексагидрохинолина, фармацевтическим композициям, их содержащих, и применению указанных производных для получения лекарственных средств для лечения нарушений фертильности.
Гонадотропины выполняют важные функции в целом ряде процессов живого организма, включая метаболизм, терморегуляцию и репродуктивный цикл. Гонадотропины действуют на специфические типы клеток половых желез, стимулируя овариальную и тестикулярную дифференцировку и стероидогенез. Гипофизарный гонадотропный гормон FSH (фолликулостимулирующий гормон), например, играет ключевую роль в стимуляции развития и созревания фолликулов, тогда как LH (лютеинизирующий гормон) индуцирует овуляцию (Sharp, R.M. Clin Endocrinol. 33:787-807, 1990; Dorrington and Armstrong, Recent Prog. Horm. Res. 35:301-342, 1979). В настоящее время FSH применяют клинически, для стимуляции яичников, т.е. гиперстимуляции яичников для in vitro оплодотворения (яйцеклетки) (IVF) и индукции овуляции у бесплодных ановуляторных женщин (Insler, V., Int. J. Fertility 33:85-97, 1988, Navot and Rosenwaks, J. Vitro Fert. Embryo Transfer 5:3-13, 1988), а также в случае мужского гипогонадизма и мужского бесплодия.
Гонадотропный FSH высвобождается из передней доли гипофиза под влиянием гонадотропин-высвобождающего гормона и эстрогенов и из плаценты во время беременности. У женщин FSH действует на яичники, стимулируя развитие фолликулов, и является основным гормоном, регулирующим секрецию эстрогенов. У мужчин FSH отвечает за целостность семенных канальцев и действует на клетки Сертоли, поддерживая гаметогенез. Очищенный FSH применяют клинически для лечения бесплодия у женщин и для лечения некоторых типов нарушения сперматогенеза у мужчин. Гонадотропины, предназначенные для терапевтических целей, могут быть выделены из мочи человека и имеют низкую чистоту (Morse et al, Amer. J. Reproduct. Immunol, and Microbiology 17:143, 1988). Альтернативно, они могут быть получены в виде рекомбинантных гонадотропинов. Рекомбинантный человеческий FSH доступен коммерчески и его используют для вспомогательной репродукции (Olijve et al. Mol. Hum. Reprod. 2:371, 1996; Devroey et al. Lancet 339:1170, 1992).
Действия FSH гормона опосредованы специфическим рецептором плазматической мембраны, который является представителем большого семейства рецепторов, связанных с G-белком. Эти рецепторы состоят из единственного полипептида с семью трансмембранными доменами и способны взаимодействовать с Gs белком, что приводит к активации аденилатциклазы.
Рецептор FSH является высокоспецифической мишенью в процессе роста овариальных фолликулов и экспрессируется исключительно в яичнике. Блокирование рецептора или ингибирование передачи сигнала, который обычно индуцируется после FSH-опосредованной активации рецептора, может нарушить развитие фолликулов и, соответственно, нарушать овуляцию и фертильность. Низкомолекулярные антагонисты FSH могут составлять основу для новых противозачаточных средств, в то время как низкомолекулярные агонисты FSH могут быть использованы для тех же самых клинических целей, как и нативный FSH, т.е. для лечения бесплодия и для овариальной гиперстимуляции при in vitro оплодотворении (яйцеклетки).
Низкомолекулярные миметики FSH с агонистическими свойствами были раскрыты в международной заявке WO 2000/08015 (Applied Research Systems ARS Holding N.V.) и в WO 2002/09706 (Affymax Research Institute). Недавно в международной заявке WO 2003/004028 (AKZO NOBEL N.V.) были раскрыты некоторые производные тетрагидрохинолина в качестве модулирующих FSH веществ, имеющих либо агонистические свойства, либо антагонистические свойства. В настоящее время остается потребность в низкомолекулярных миметиках гормона, которые могли бы селективно активировать рецептор FSH.
Для этой цели настоящее изобретение предлагает производные 4-фенил-5-оксо-1,4,5,6,7,8-гексагидрохинолина общей формулы I
где
R1 представляет собой (1-6C)алкил, (2-6C)алкенил или (2-6C)алкинил;
R2 представляет собой галоген, (1-4C)алкокси, фторированный (1-4C)алкокси, (1-4C)алкил или фторированный (1-4C)алкил; или R2 может быть H, когда R3 представляет собой R9,R10-аминосульфонил;
R3 представляет собой OH, NO2, CN, фторированный (1-4C)алкокси, (1-4C)алкокси(2-4C)алкокси, гидрокси(2-4C)алкокси, (1-4C)алкоксикарбонил, (3-4C)алкенилоксикарбонил, (1-4C)алкоксикарбонилокси, (3-4C)алкенилоксикарбонилокси, R7,R8-амино, R9,R10-амино, R9,R10-аминокарбонил, R9,R10-аминосульфонил или фенил(1-4C)алкокси, где фенильное кольцо необязательно замещено одним или несколькими заместителями, выбранными из гидрокси, амино, галогена, нитро, трифторметила, циано, (1-4C)алкила, (2-4C)алкенила, (2-4C)алкинила, (1-4C)алкокси, (ди)(1-4C)алкиламино;
R4 представляет собой R11-фенил или R11-(2-5C)гетероарил, где фенильная или гетероарильная группа необязательно дополнительно замещена одним или несколькими заместителями, выбранными из гидрокси, амино, галогена, нитро, трифторметила, циано, (1-4C)алкила, (1-4C)алкилтио, (1-4C)алкокси, (2-4C)алкенила, (2-4C)алкинила;
R7 представляет собой H, (1-4C)алкил;
R8 представляет собой (1-4C)алкилсульфонил, (1-4C)алкилкарбонил, (2-4C)алкенилкарбонил, (3-6C)циклоалкилкарбонил, (1-4C)алкоксикарбонил, (3-4C)алкенилоксикарбонил, (1-4C)алкокси(1-4C)алкилкарбонил, (3-4C)алкенилокси(1-4C)алкилкарбонилфенилкарбонил, (2-5C)гетероарилкарбонил, фенил(1-4C)алкилкарбонил, (2-5C)гетероарил(1-4C)алкилкарбонил, где фенильное кольцо или гетероароматическое кольцо необязательно замещено одним или несколькими заместителями, выбранными из гидрокси, амино, галогена, нитро, трифторметила, циано, (1-4C)алкила, (2-4C)алкенила, (2-4C)алкинила, (1-4C)алкокси, (ди)(1-4C)алкиламино;
R9 и R10 независимо выбраны из Н, (1-6C)алкила (3-6C)циклоалкила, (3-6C)циклоалкил(1-4С)алкила и (1-4C)алкокси(2-4C)алкила;
или R9 и R10 могут быть соединены вместе с образованием (4-6C)гетероциклоалкенильного кольца или (2-6C)гетероциклоалкильного кольца, необязательно замещенного одним или несколькими (1-4C)алкильными заместителями;
R11 представляет собой H, (1-6C)алкоксикарбонил, R12,R13-амино, (1-6C)алкилкарбонил, (1-6C)алкилсульфонил, R14-окси, R14,R15-амино, R14,R15-аминокарбонил, R14,R15-аминосульфонил;
R12 представляет собой Н, (1-4C)алкил;
R13 представляет собой (1-4C)алкилсульфонил, (1-4C)алкилкарбонил, (3-6C)циклоалкилкарбонил, (1-4C)алкоксикарбонил, (3-4C)алкенилоксикарбонил, (ди)(1-4C)алкиламино(1-4C)алкилкарбонил, (2-6C)гетероциклоалкил(1-4C)алкилкарбонил, (4-6C)гетероциклоалкенил(1-4C)алкилкарбонил или (1-4C)алкокси(1-4C)алкилкарбонил;
R14 и R15 независимо выбраны из H, (1-6C)алкила, (3-4C)алкенила, (3-4C)алкинила, (3-6C)циклоалкила, (3-6C)циклоалкил(1-4C)алкила, гидрокси(2-4C)алкила, амино(2-4C)алкила, (1-4C)алкокси(2-4C)алкила, (ди)(1-4C)алкиламино(2-4C)алкила, (2-6C)гетероциклоалкил(2-4C)алкила, (4-6C)гетероциклоалкенил(2-4C)алкила, фенил(1-4C)алкила и (2-5C)гетероарил(1-4C)алкила;
X представляет собой O или R16-N;
Y представляет собой CH2, C(O) или SO2;
Z представляет собой CN или NO2;
R16 представляет собой H, (1-4C)алкил, (1-4C)алкилкарбонил;
или их фармацевтически приемлемую соль.
Производные 4-фенил-5-оксо-1,4,5,6,7,8-гексагидрохинолина по данному изобретению являются сильнодействующими активаторами рецептора FSH и могут быть использованы для тех же самых клинических целей, что и природный FSH, поскольку они ведут себя как агонисты, с преимуществом, заключающимся в том, что они могут быть получены синтетическим путем, могут демонстрировать измененные свойства стабильности и могут вводиться по-разному.
Таким образом, агонисты рецептора FSH по данному изобретению могут быть использованы для лечения нарушений фертильности, например, в регулируемой гиперстимуляции яичников и методах IVF.
Термины (1-4C)алкил и (1-6C)алкил, используемые для определения, означают алкильные группы с линейной или разветвленной цепью, содержащие соответственно 1-4 и 1-6 углеродных атомов, и представляют собой метил, этил, пропил, изопропил, бутил, втор-бутил, изобутил и трет-бутил и т.д.
Термин (2-4С)алкокси(2-4С)алкил означает алкоксигруппу, алкильная группа которой содержит 2-4 углеродных атома, присоединенную к алкильной группе, содержащей 2-4 атома углерода.
Термины фторированный (1-4C)алкил и фторированный (1-4C)алкокси означают линейные или разветвленные алкильные и алкоксигруппы, содержащие соответственно 1-4 атома углерода, и которые являются замещенными, по меньшей мере, одним атомом фтора.
Термины (2-4C)алкенил, (3-4C)алкенил и (2-6C)алкенил означают линейные или разветвленные алкенильные группы, содержащие 2-4, 3-4 и 2-6 атомов углерода, соответственно, такие как этенил, 2-бутенил и н-пентенил.
Термин (2-4C)алкенил означает линейные или разветвленные алкинильные группы, содержащие 2-4 атома углерода, такие как этинил и пропинил.
Термин (3-6C)циклоалкил означает циклоалкильную группу, содержащую 3-6 атомов углерода, и представляет собой циклопропил, циклобутил, циклопентил и циклогексил.
Термин (3-6C)циклоалкил(1-4C)алкил означает (1-4C)алкильную группу, определенную выше, замещенную определенной ранее (3-6C)циклоалкилалкильной группой.
Термин (2-6C)гетероциклоалкил означает гетероциклоалкильную группу, содержащую 2-6 атомов углерода, предпочтительно 3-5 атомов углерода, и включающую, по меньшей мере, один гетероатом, выбранный из N, О и/или S, которая может быть присоединена через гетероатом, если это возможно, или атом углерода. Предпочтительными гетероатомами являются N или O. Наиболее предпочтительными группами являются пиперидин-1-ил, морфолин-4-ил, пирролидин-1-ил и пиперазин-1-ил.
Термин (4-6C)гетероциклоалкенил означает гетероциклоалкенильную группу, содержащую 4-6 атомов углерода, предпочтительно 5-6 атомов углерода, и включающую, по меньшей мере, один гетероатом, выбранный из N, О и/или S, которая может быть присоединена через гетероатом, если это возможно, или атом углерода. Предпочтительными гетероатомами являются N или O.
Термин (2-5C)гетероарил означает гетероароматическую группу, содержащую 2-5 атомов углерода и, по меньшей мере, один гетероатом, выбранный из N, О и S, такие как имидазолил, тиадиазолил, пиридинил, тиенил или фурил. Предпочтительными гетероарильными группами являются тиенил, фурил и пиридинил.
(2-5C)Гетероарильная группа может быть присоединена через атом углерода или гетероатом, если это возможно.
Используемый в описании термин (ди)(1-4C)алкиламино означает аминогруппу, монозамещенную или дизамещенную алкильными группами, каждая из которых содержит 1-4 атома углерода и имеет такое же значение, как определено ранее.
Термин галоген означает фтор, хлор, бром или иод, при этом предпочтительны хлор, бром или иод.
Термин “фармацевтически приемлемая соль” представляет собой соли, которые, с точки зрения специалиста-медика, пригодны для использования путем введения в контакт с тканями людей и низшими животными без проявления нежелательной токсичности, раздражения, аллергической реакции и т.п., и которые соответствуют разумному соотношению польза/риск. Фармацевтически приемлемые соли общеизвестны в данной области техники. Они могут быть получены в процессе окончательного выделения и очистки соединений по данному изобретению, или отдельно путем взаимодействия функциональной группы свободного основания с подходящей неорганической кислотой, такой как хлористоводородная кислота, фосфорная кислота или серная кислота, или с органической кислотой, такой как, например, аскорбиновая кислота, лимонная кислота, винная кислота, молочная кислота, малеиновая кислота, малоновая кислота, фумаровая кислота, гликолевая кислота, янтарная кислота, пропионовая кислота, уксусная кислота, метансульфокислота и т.п. Кислотная функциональная группа может быть подвергнута взаимодействию с органическим или неорганическим основанием, подобным гидроксиду натрия, гидроксиду калия или гидроксиду лития.
Один аспект данного изобретения относится к соединениям формулы I, где R1 представляет собой (1-6C)алкил. В частности, данное изобретение относится к соединениям, где R1 представляет собой (1-4C)алкил.
Другой аспект данного изобретения относится к соединениям, представленным формулой I, где R2 представляет собой галоген. В частности, R2 представляет собой Br.
В другом аспекте данного изобретения R3 в соединении формулы I представляет собой R9,R10-аминосульфонил. В частности, R9 и R10 представляют собой, независимо, (1-6C)алкил.
Другой аспект данного изобретения относится к соединениям формулы I, где R4 представляет собой R11-фенил или R11-(2-5C)гетероарил, при этом фенильная или гетероарильная группа необязательно, кроме того, замещена одним (1-4C)алкокси. В частности, данное изобретение относится к соединениям, где R11 представляет собой H или R12,R13-амино.
Дополнительный аспект данного изобретения относится к соединениям формулы I, где X представляет собой O.
В другом аспекте данное изобретение касается соединений формулы I, где Y представляет собой CH2.
Другой аспект данного изобретения относится к соединениям, где Z представляет собой CN.
Следующий аспект данного изобретения касается соединений, где одно или несколько из конкретных определений групп R1 посредством R16 и X, Y и Z, определенных здесь выше, объединены в определении соединения 4-фенил-5-оксо-1,4,5,6,7,8-гексагидрохинолина формулы I.
Очередной аспект данного изобретения касается соединений, представленных формулой I, которые имеют EC50 в анализе связывания меньше чем 10-8M (как описано в примере 43).
Подходящие общие способы получения соединений описаны в общих чертах ниже.
В некоторых случаях Rx-группы, содержащие функциональные группы, могут нуждаться в дополнительной временной защите, в зависимости от типа реакции, подлежащей осуществлению, что должно быть очевидно специалисту в данной области (см. Protective groups in Organic Synthesis, T.W. Greene and P.G.M. Wuts, John Wiley & sons, Inc., New York, 1999).
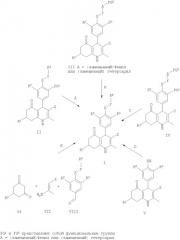
Производные 4-фенил-5-оксо-1,4,5,6,7,8-гексагидрохинолина формулы I, где R1, R2, R3, R4, X, Y и Z такие, как определено выше, можно получить, следуя нижеследующим стратегиям. Способ А исходит из соответствующим образом функционализированных производных 4-фенил-5-оксо-1,4,5,6,7,8-гексагидрохинолина общей структуры II, где R1, R2, R4, X, Y и Z такие, как определены выше, и FG1 представляет собой функциональную группу, такую как нитро, азидо, (необязательно защищенную) амино, (необязательно защищенный) гидроксил, карбоновую кислоту, сульфонилхлорид и т.п., которая может быть превращена в группы, определенные для R3.
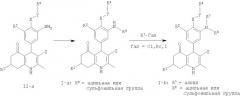
Например, N-ацилирование или N-сульфонилирование соединений формулы II-а дает соединения общей формулы I-a, где R1, R2, R4, X, Y и Z такие, как определены ранее, R7 представляет собой H и R8 представляет собой ацильную или сульфонильную группу.
В типичном эксперименте соединения II-а подвергают взаимодействию в растворителе, таком как дихлорметан, N,N-диметилформамид, диметилсульфоксид, этанол, тетрагидрофуран, 1,4-диоксан, толуол, 1-метилпирролидин-2-он или пиридин, с соответствующим образом замещенным ацилгалогенидом (галогенангидрид карбоновой кислоты), ангидридом кислоты или сульфонилгалогенидом в присутствии основания, такого как триэтиламин, N,N-диизопропилэтиламин (DiPEA) или пиридин, с получением N-ацилированных или N-сульфонилированных производных формулы I-a, соответственно. Альтернативно, N-ацилированные соединения общей формулы I-a можно получить взаимодействием производных II-а с соответствующим образом замещенными карбоновыми кислотами в присутствии конденсирующего реагента, такого как диизопропилкарбодиимид (DIC), (3-диметиламинопропил)этилкарбодиимид (EDCI), O-(бензотриазол-1-ил)-N,N,N',N'-тетраметилуроний тетрафторборат (TBTU) или O-(7-азабензотриазол-1-ил)-N,N,N',N'-тетраметилуроний гексафторфосфат (HATU) и третичное аминное основание (например, DiPEA), в растворителе, таком как N,N-диметилформамид или дихлорметан, при температуре окружающей среды или повышенной температуре.
Соединения общей формулы I-b, где R1, R2, R4, R8, X, Y и Z такие, как определены выше, и R7 представляет собой (1-4C)алкильную группу, можно получить путем N-алкилирования производных I-a соответствующим образом замещенными алкилгалогенидами общей формулы R7-Гал. Эту реакцию обычно проводят в присутствии основания, такого как карбонат калия, карбонат цезия, гидроксид натрия или гидрид натрия, в подходящих растворителях, таких как дихлорметан, N,N-диметилформамид, этанол, диметилсульфоксид, тетрагидрофуран или 1,4-диоксан.
Альтернативно, соединения формулы I-b могут быть получены восстановительным алкилированием, известным в данной области, алкилальдегидами (например, ацетальдегид, (изо)бутиральдегид), ацетоном или бутаноном. Как правило, соединения общей формулы II-a обрабатывают соответствующим карбонильным соединением и восстановителем, таким как цианоборгидрид натрия или триацетоксиборгидрид натрия, в подходящем растворителе, таком как метанол, этанол, дихлорметан, N,N-диметилформамид или их смеси, необязательно в присутствии кислот, таких как уксусная кислота, с получением соединений общей формулы II-b. Соединения общей формулы II-b могут быть затем N-ацилированы или N-сульфонилированы, получая соединения общей формулы I-b такими же способами, как описано для получения соединений общей формулы I-a из II-a.
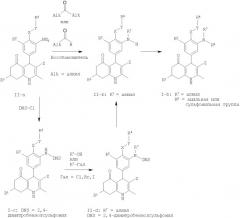
Соединения общей формулы II-b можно также получить посредством последовательности из 3 стадий. Сначала соединения формулы II-а могут быть превращены в производные 2,4-динитробензолсульфонамида II-с реакцией N-сульфонилирования 2,4-динитробензолсульфонилхлоридом (DNS-Cl).
Сульфонамид может быть алкилирован с получением соединений общей формулы II-b, используя известные в данной области реакции Мицунобу, соответствующим образом замещенными первичными или вторичными спиртами формулы R7-OH (R7=алкил), трифенилфосфином (необязательно связанным с полимером) и диалкилазодикарбоксилатом в подходящих растворителях, таких как 1,4-диоксан, тетрагидрофуран или дихлорметан, при повышенной температуре или температуре окружающей среды. Альтернативно, сульфонамид общей формулы II-с может быть алкилирован, используя алкилгалогениды формулы R7-Гал (Гал = Cl, Br, I) и подходящее основание, такое как K2CO3, в растворителе, таком как N,N-диметилформамид, тетрагидрофуран или 1,4-диоксан. Расщепление сульфонамидной связи N-S первичным амином, таким как пропиламин, в подходящем растворителе, таком как дихлорметан, дает затем соединения формулы II-b. Альтернативно, сульфонамидная связь N-S может быть расщеплена с использованием меркаптоуксусной кислоты и третичного аминного основания в растворителе, таком как дихлорметан. Примеры проведения этих реакций можно найти в литературе. Например, см.: Tetrahedron Lett. 38 (1997) 5831-5834, Bioorg. Med. Chem. Lett. 10 (2000) 835-838.
Используя такие же способы, как описаны для получения производных II-b, получают соединения общей формулы I-с, где R1, R2, R4, R9, X, Y и Z такие, как определены выше, путем взаимодействия соединений II-а с (замещенными) алкилальдегидами или (циклическими) кетонами (например, пропиональдегид, циклогексанон, ацетон или ацетальдегид) в условиях восстановления или путем алкилирования производных II-с посредством R9-OH или R9-Гал, с последующим удалением DNS-группы. Соединения I-с могут быть восстановлены алкилированием снова, используя соответствующим образом замещенные альдегиды или кетоны, чтобы ввести R10, получая соединения общей формулы I-d, где R1, R2, R4, R9, R10, X, Y и Z такие, как определены выше. В некоторых случаях восстановительное алкилирование II-а может быть проведено дважды с получением соединений общей формулы I-d, где R9 = R10 (например, когда используют формальдегид, R9 = R10 = метил).
Соединения общей формулы II-а можно получить восстановлением нитрогруппы в соединениях общей формулы II-е в соответствующую аминогруппу. Обычно соединения II-е обрабатывают цинковой пылью и уксусной кислотой в подходящем растворителе, таком как ТГФ или диоксан, при температурах в диапазоне от 0°C до температуры образования флегмы. Альтернативные способы включают обработку железом, SnCl2 или водородом в присутствии катализатора на основе переходных металлов, такого как палладий или платина на угле, используя способы и реагенты, известные специалистам в данной области. Альтернативно, соединения общей формулы II-а могут быть получены отщеплением известных N-защитных групп (=PG в формуле II-f), таких как аллилоксикарбонильной (Alloc), флуорен-9-илметоксикарбонильной (Fmoc) или трет-бутоксикарбонильной (Boc) группы в соединениях общей формулы II-f, получая соответствующие производные II-а. Родственные манипуляции с защитными группами можно найти в Protective groups in Organic Synthesis, T.W. Greene and P.G.M. Wuts, John Wiley & sons, Inc., New York, 1999.
Производные карбоновой кислоты общей формулы II-h, доступные в результате омыления соответствующих алкиловых сложных эфиров II-g, могут быть конденсированы с аминами общей структуры R9R10NH, используя конденсирующий реагент, как описано ранее для получения производных I-a из II-а, с получением соединений формулы I-е, где R1, R2, R4, R9, R10, X, Y и Z такие, как определены выше. Альтернативно, соединения общей формулы II-h могут быть превращены в соответствующие хлорангидриды кислот общей формулы II-i способами, известными в данной области: обработка карбоновых кислот общей формулы II-h
тионилхлоридом или оксалилхлоридом и ДМФА в подходящем растворителе, таком как дихлорметан или толуол, дает соответствующие хлорангидриды кислот II-i. Последующая реакция с аминами общей структуры R9R10NH, необязательно в присутствии подходящего третичного аминного основания, дает соединения общей формулы I-е.
Соединения общей формулы I-f, где R1, R2, R4, X, Y и Z такие, как определены выше, и R представляет собой циано, можно получить дегидратацией амидов общей формулы I-g в присутствии ангидрида трифторуксусной кислоты и подходящего основания, такого как триэтиламин или пиридин, в подходящем растворителе, таком как дихлорметан, 1,4-диоксан или тетрагидрофуран, при 0°C или температуре окружающей среды. Родственные дегидратации амидов с получением арилнитрилов можно найти в литературе, например, см.: Org. Prep. Proced. Int. 26 (1994) 429-438, Acta Chem. Scand. 53 (1999) 714-720, J. Org. Chem. 57 (1992) 2700-2705. Соединения формулы I-g получают согласно синтезу, в общих чертах описанного для производных I-е.
Соединения общей формулы II-j, где R1, R2, R4, X, Y и Z такие, как определены выше, могут быть O-алкилированы (замещенными) алкилгалогенидами E-Гaл (E = алкил, фторированный алкил, алкоксиалкил, гидроксиалкил, (замещенный) фенилалкил или (замещенный) гетероарилалкил; Гaл =Cl, Br, I) путем обработки основанием, таким как карбонат калия или карбонат цезия, в подходящем растворителе, таком как N,N-диметилформамид, ацетон, тетрагидрофуран, 1,4-диоксан или 1-метилпирролидин-2-он, получая соединения общей формулы I-h, где R1, R2, R4, X, Y и Z такие, как определены выше, и E представляет собой алкил, фторированный алкил, алкоксиалкил, гидроксиалкил, (замещенный) фенилалкил или (замещенный) гетероарилалкил. Альтернативно, для осуществления этого превращения могут быть использованы условия реакции Мицунобу, описанные для превращения производных II-с в соединения II-d.
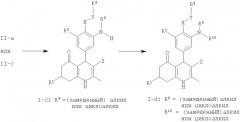
Соединения общей формулы I можно также получить манипуляцией функциональных групп FG2 в соединениях общей формулы III (способ B). Например, функционализирование аминогруппы соединений общей формулы III-а таким же способом, как описан для превращения производных II-а в I-a и I-b, дает соединения общей формулы I-k, где R1, R2, R3, R12, R13, X, Y и Z такие, как определены выше, A представляет собой (замещенное) фенильное или (замещенное) гетероарильное кольцо.
Соединения общей формулы I-l, где R1, R2, R3, R14, X, Y и Z такие, как определены выше, R15 представляет собой H и A представляет собой (замещенное) фенильное или (замещенное) гетероарильное кольцо, можно получить восстановительным алкилированием соединений общей формулы III-а, используя такие же способы, как описаны для получения соединений формулы II-b из II-а или путем последовательности из 3 стадий, описанной для получения производных II-b из II-а через II-c и II-d. Восстановительное алкилирование соединений I-l альдегидами или кетонами в присутствии цианоборгидрида натрия или триацетоксиборгидрида натрия может привести к получению соединений общей формулы I-m, где R1, R2, R3, R14, R15, X, Y и Z такие, как определены выше, и A представляет собой (замещенное) фенильное или (замещенное) гетероарильное кольцо.
Соединения общей формулы III-a могут быть получены из соединений общей формулы III-b или III-c по аналогии с получением соединений II-а из II-е или II-f, соответственно.
Производные амида I-n, где R1, R2, R3, R14, R15, X, Y и Z такие, как определены выше, и A представляет собой (замещенное) фенильное или (замещенное) гетероарильное кольцо, можно получить из карбоновых кислот III-е такими же способами (с помощью хлорангидрида кислоты или путем использования конденсирующих реагентов), которые описаны для получения соединений I-е из II-h.
Аналогично, сложные эфиры общей формулы I-o, где R1, R2, R3, R14, X, Y и Z такие, как определены выше, и A представляет собой (замещенное) фенильное или (замещенное) гетероарильное кольцо, можно получить из производных III-e и спиртов общей формулы R14-OH, используя такие же способы, как описаны для превращения III-e в соответствующие амиды I-n.
Соединения общей формулы III-e могут быть получены из соответствующих алкиловых сложных эфиров III-d путем опосредованного основанием или кислотой расщепления сложного эфира, хорошо известного специалистам в данной области.
Производные общей формулы I-p, где R1, R2, R3, R14, X, Y и Z такие, как определены выше, и A представляет собой (замещенное) фенильное или (замещенное) гетероарильное кольцо, можно получить алкилированием гидроксильной группы в соединениях общей формулы III-g алкилгалогенидом общей формулы R14-Гал, в котором Гал может представлять собой Br, Cl или I. Как правило, такую реакцию осуществляют в апротонном растворителе, таком как N,N-диметилформамид, 1,4-диоксан или тетрагидрофуран, в присутствии основания, такого как гидрид натрия, карбонат калия, карбонат цезия или триэтиламин, при температуре окружающей среды или повышенной температуре. Альтернативно, превращение соединений общей формулы III-g в ариловые эфиры общей формулы I-p, может быть осуществлено в условиях алкилирования Мицунобу. В таком превращении алкилирование гидроксильной группы в соединениях формулы III-g осуществляют спиртами общей формулы R14-OH при воздействии (связанного с полимером) трифенилфосфина и диэтилазодикарбоксилата или его производных в подходящем апротонном растворителе, таком как тетрагидрофуран или дихлорметан.
Производные общей формулы III-g можно получить отщеплением гидроксил-защитной группы в соединениях общей формулы III-f. Подходящими защитными группами, общеизвестными специалистам в данной области, являются тетрагидропиранильные (THP) или трет-бутилдиметилсилильные (TBS) защитные группы. Отщепление THP и TBS групп обычно осуществляют обработкой кислотами, такими как хлористоводородная кислота, трифторметансульфокислота или трифторуксусная кислота, в подходящем растворителе, таком как тетрагидрофуран или метанол. Альтернативно, TBS группу можно удалить обработкой фторидом тетра-н-бутиламмония в тетрагидрофуране. Родственные манипуляции с защитными группами можно найти в Protective groups in Organic Synthesis, T.W. Greene and P.G.M. Wuts, John Wiley & sons, Inc., New York, 1999.
Соединения общей формулы I могут быть также получены манипулированием обеих функциональных групп FG1 и FG2 в соединениях общей формулы IV (способ C), в направлении, описанном для превращений соединений общей формулы II и III. Две функциональные группы могут быть, но могут и не быть, идентичными. Специалистам в данной области очевидно, что порядок, в соответствии с которым модифицируют функциональные группы FG1 и FG2, может иметь решающее значение для успешного завершения синтеза. Очевидно, что в некоторых случаях использование (ортогональных) защитных групп может быть необходимо.
Например, динитросоединения общей формулы IV-a могут быть восстановлены в диаминосоединения IV-b, используя способы, описанные для получения производных II-а из II-е. Обычное N-ацилирование или N-сульфонилирование дает соединения общей формулы I-q, где R1, R2, R3, X, Y и Z такие, как определены выше, и A представляет собой (замещенное) фенильное или (замещенное) гетероарильное кольцо и R13 = R8.
Чтобы сделать возможным независимую вариацию заместителей (например, R8 и R13), функциональные группы в соединениях общей формулы IV должны подвергаться превращениям ортогональным способом. Например, соединения общей формулы IV-c могут быть функционализированы, используя такие же способы, как описаны для синтеза производных I-a, I-b, I-е и I-d из соединений II-а, с получением соединений общей формулы IV-d, где R1, R2, X, Y и Z такие, как определены выше, A представляет собой (замещенное) фенильное или (замещенное) гетероарильное кольцо и G представляет собой NR7R8 или NR9R10. Эти соединения могут быть превращены в производные I-r, где R1, R2, X, Y и Z такие, как определены выше, A представляет собой (замещенное) фенильное или (замещенное) гетероарильное кольцо и G представляет собой NR7R8 или NR9R10 и К представляет собой NR12R13 или NR14R15.
Очередной возможностью достигнуть желаемых соединений общей формулы I может быть функционализация соединений общей формулы V (способ D). Соединения общей формулы V-a, где X = О, могут быть использованы для получения соединений I-s, где R1, R2, R3, R4, Y и Z такие, как определены выше, и X = O, путем О-алкилирования, O-ацилирования или О-сульфонилирования, используя обычные условия, общеизвестные для специалистов в данной области. Картина замещения (гетеро)арильного кольца в R4 такая, как определена выше. В типичном эксперименте соединения V-a подвергают взаимодействию в растворителе, таком как дихлорметан, N,N-диметилформамид, диметилсульфоксид, этанол, тетрагидрофуран, 1,4-диоксан, толуол, 1-метилпирролидин-2-он или пиридин, с соответствующим образом замещенным (гетеро)ароматическим алкилгалогенидом формулы IX, ацилхлоридом формулы X или сульфонилхлоридом формулы XII в присутствии основания, такого как триэтиламин, N,N-диизопропилэтиламин (DiPEA), пиридин, карбонат калия, карбонат цезия или гидрид натрия, необязательно в присутствии каталитического количества иодида калия или иодида тетрабутиламмония, с получением O-алкилированных, О-ацилированных или O-сульфонилированных производных формулы I-s соответственно.
Альтернативно, О-алкилированные соединения общей формулы I-s, в которой Y = CH2, можно получить, используя известные в данной области реакции Мицунобу со спиртами формулы XIII, трифенилфосфином (необязательно связанного с полимером) и диалкилазодикарбоксилатом (например, диэтилазодикарбоксилатом) в подходящих растворителях, таких как 1,4-диоксан, тетрагидрофуран или дихлорметан, при повышенной температуре или температуре окружающей среды.
Кроме того, О-ацилированные соединения общей формулы I-s, где Y = C(O), могут быть получены взаимодействием (гетеро)ароматической карбоновой кислоты формулы XI в присутствии конденсирующего реагента, такого как диизопропилкарбодиимид (DIC), (3-диметиламинопропил)этилкарбодиимид (EDCI), О-(бензотриазол-1-ил)-N,N,N',N'-тетраметилуроний тетрафторборат (TBTU) или O-(7-азабензотриазол-1-ил)-N,N,N',N'-тетраметилуроний гексафторфосфат (HATU), и третичного аминного основания (например, DiPEA) в растворителе, таком как N,N-диметилформамид или дихлорметан, при температуре окружающей среды или повышенной температуре.
Аналогично, соединения общей формулы I-t можно получить из соединений V-b N-алкилированием, N-ацилированием или N-сульфонилированием, используя такие же способы, как описаны для синтеза соединений I-s, используя реагенты формулы IX-XIII. Кроме того, соединения общей формулы I-t, в которой Y = CH2, могут быть получены восстановительным аминированием (гетеро)ароматических альдегидов формулы XIV с соединениями V-b и подходящим восстановителем, таким как цианоборгидрид натрия или триацетоксиборгидрид натрия. Альтернативно, соединения общей формулы V-b могут быть превращены в соответствующие бензимины по реакции с (гетеро)ароматическими альдегидами XIV способами, известными специалистам в данной области, с последующим восстановлением в присутствии восстановителя, такого как боргидрид натрия, с получением соединений I-t, в которых Y = CH2.
Соединения общей формулы I-t, где R1, R2, R3, R4, Y и Z такие, как определены выше, и X представляет собой NH, могут быть N-алкилированы такими же способами, как описано для получения производных I-b из I-a (если Y = C(O) или SO2), или такими же способами, как описано для получения соединений-производных II-b из II-а (если Y = CH2), с получением соединений общей формулы I-u, где R16 представляет собой (1-4C)алкильную группу.
Соединения общей формулы I, где R1, R2, R3, R4, X, Y и Z такие, как определены выше, можно также получить в соответствии с основательно документально подтвержденной реакцией поликонденсации типа Ганча с участием трех компонентов (способ E), исходя из циклогексан-1,3-дионов общей формулы VI, енаминов общей формулы VII и бензальдегидов общей формулы VIII-a-b
Родственные реакции циклоконденденсации типа Ганча можно найти в: Bioorg. Med. Chem. Lett. 12 (2002) 1481-1484, J. Chem. Soc., Perkin Trans. 1 (2002) 1141-1156, Synlett (2002) 89-92, Drug Dev. Res. 51 (2000) 225-232, Drug Dev. Res. 51 (2000) 233-243, J. Med. Chem. 42 (1999) 1422-1427, там же 5266-5271, там же 41 (1998) 2643-2650, WO 9408966, Arzneim.-Forsch./Drug Res. 45 (1995) 1054-1056, J. Med. Chem. 34 (1991) 2248-2260, там же 17 (1974) 956-65, Indian J. Chem., Sect В (1994) 526-531, Chem. Rev. 72 (1972), 1-42. Вышеупомянутую реакцию обычно проводят при повышенной температуре в подходящих растворителях, таких как уксусная кислота, (изо)пропанол, этанол, метанол или их смеси.
Соединения общей формулы I-w, где R2 представляет собой H и R3 представляет собой R9,R10-аминосульфонил и R1, R4, X, Y и Z такие, как определены выше, могут быть синтезированы каталитическим гидрированием соединений общей формулы I-v, используя водород и катализатор на основе переходных металлов, такой как палладий на угле, в подходящих растворителях, таких как этанол, метанол, этилацетат или их смеси.
Соединения общей формулы II достижимы исходя из производных общей формулы XV-a и XV-b, используя такие же способы, как описаны для получения соединений общей формулы I-s и I-t соответственно, используя реагенты формулы IX-XIV.
Подобно N-алкилированию соединений общей формулы I-t с получением I-u, соединения общей формулы II-k, где R1, R2, R4, Y, Z такие, как определены выше, и X = NH, могут быть N-алкилированы с получением соединений общей формулы II-l, где R16 представляет собой (1-