Замещенные амиды тиенопирролкарбоновой кислоты, амиды пирролотиазолкарбоновой кислоты и родственные аналоги в качестве ингибиторов казеинкиназы i
Иллюстрации
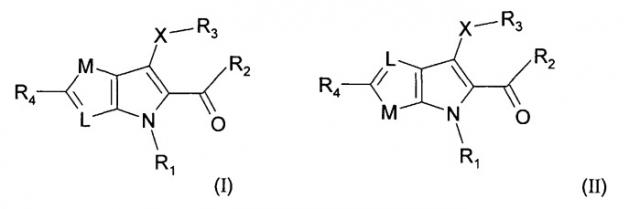
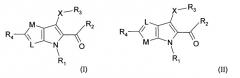
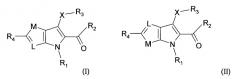
Показать всеНастоящее изобретение относится к соединениям формулы (I) и формулы (II), их таутомерам и фармацевтически приемлемым солям. Соединения настоящего изобретения обладают свойствами ингибитора казеинкиназы Iε. В формуле (I) и в формуле (II)
Х - S; R1 - Н; R2 - NR5R6; R3 - 5-6-членный гетероарил с 1 гетероатомом, выбранным из N и S, или фенил, необязательно замещенный одним или двумя заместителями, выбранными из галогена, амино, C1-С6-алкила, C1-С6-алкокси, C1-С6-галогеналкила и C1-С6-галогеналкокси; R4 - Н, C1-С6 алкил, C1-С6 алкокси или XR3, где Х и R3 определены выше; R5 - Н; R6 - Н; L - N или CR7, где R7 - Н; М - S. Изобретение также относится к фармацевтической композиции, содержащей в качестве активного компонента соединение изобретения, к способу ингибирования активности казеинкиназы I ε и к способу получения соединений формулы (I) или формулы (II). 4 н. и 9 з.п. ф-лы, 5 табл.
Реферат
Предпосылки к созданию изобретения
1. Область изобретения
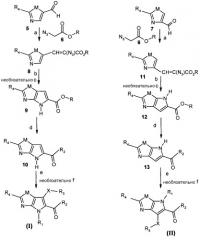
Настоящее изобретение относится к ряду замещенных амидов 4H-тиено[3,2-b]пиррол-5-карбоновой кислоты, амидов 4H-пирроло[2,3-d]тиазол-5-карбоновой кислоты, амидов 6H-тиено[2,3-b]пиррол-5-карбоновой кислоты, амидов 4H-пирроло[3,2-d]тиазол-5-карбоновой кислоты и родственных аналогов. Более конкретно настоящее изобретение относится к 3-арилтиозамещенным и 3-гетероциклотиозамещенным амидам 4H-тиено[3,2-b]пиррол-5-карбоновой кислоты, амидам 4H-пирроло[2,3-d]тиазол-5-карбоновой кислоты, амидам 6H-тиено[2,3-b]пиррол-5-карбоновой кислоты, амидам 4H-пирроло[3,2-d]тиазол-5-карбоновой кислоты и родственным аналогам, а также к способам получения соединений изобретения. Соединения настоящего изобретения являются ингибиторами фосфорилирования человеческой казеинкиназой Iε человеческого белка clock Period (hPER), а потому являются полезными в качестве фармацевтических средств, особенно для лечения и/или профилактики заболеваний или нарушений, связанных с центральной нервной системой.
2. Описание уровня техники
Ритмические колебания в поведении проявляются у многих организмов, от одноклеточных до человека. Если при постоянных условиях ритм сохраняется и имеет период около одного дня при малой зависимости от температуры, то такой ритм называется «циркадным» (Konopka, R.J. and Benzer, S. (1971) Proc. Nat. Acad. Sci. USA 68, 2112-2116).
Циркадные ритмы генерируются эндогенными биологическими ритмоводителями (циркадными часами) и существуют в различных организмах, включая человека, грибы, насекомых и бактерии (Dunlap, J.C. (1999) Cell 96, 271-290; Hastings, J.W. et al. Circadian Rhythms, The Physiology of Biological Timing. In: Prosser, C.L. ed. Neural and Integrative Animal Physiology, New York: Wiley-Liss (1991) 435-546; Allada, R. et al. (1998) Cell 93, 791-804; Kondo et al. (1994) Science 266, 1233-1236; Crosthwaite, S.K. et al. (1997) Science 276, 763-769; Shearman, L.P. et al. (1997) Neuron, 19, 1261-1269). Циркадные ритмы являются самоподдерживающимися и постоянными даже в условиях полной темноты, но могут быть синхронизованы (включены) с новым режимом день/ночь посредством таких внешних сигналов, как световые и температурные циклы (Pittendrigh, C.S. (1993) Annu. Rev. Physiol., 55, 16-54; Takahashi, J.S. (1995) Annu. Rev. Neurosci. 18, 531-553; Albrecht, U. et al. (1997) Cell, 91, 1055-1064). Циркадные часы имеют важное значение для поддержания биологических циклов и регулируют разнообразные формы циркадного поведения, например дневные колебания поведения, прием пищи и цикл сна/пробуждения, а также физиологические изменения, например секрецию гормонов и колебания температуры тела (Hastings, M. (1997) Trends Neurosci. 20, 459-464; Reppert, S.M. and Weaver, D.R. (1997) Cell 89, 487-490).
Генетические и молекулярные исследования плодовой мушки Drosophila melanogaster прояснили роль некоторых генов, участвующих в циркадной ритмичности. Подобные исследования привели к выявлению пути, который жестко авторегулируется и включает транскрипционную/трансляционную обратную связь (Dunlap, J.C. (1999) Cell, 96, 271-290; Dunlap, J.C. (1996) Annu. Rev. Genet. 30, 579-601; Hall, J.C. (1996) Neuron, 17, 799-802). Основными элементами циркадного осциллятора в Drosophila являются два стимулирующих белка dCLOCK/dBMAL (CYCLE) и два ингибирующих белка dPERIOD (dPER) и dTIMELESS (dTIM). dCLOCK и dBMAL гетеродимеризуются и образуют транскрипционный фактор dCLOCK/dBMAL, который промотирует экспрессию двух генов, называемых Drosophila Period (dper) и Drosophila Timeless (dtim). В конечном счете происходит считывание мРНК этих генов, чтобы обеспечить синтез белков dPER и dTIM соответственно. В течение нескольких часов происходит синтез и фосфорилирование белковых производных dPER и dTIM в цитоплазме, затем их уровень достигает критического, они образуют гетеродимеры и транслоцируются в ядро. Попав в ядро, dPER и dTIM функционируют как отрицательные регуляторы собственной транскрипции, накопление dPER и dTIM тормозится и вновь начинается активация dper и dtim за счет присутствия dCLOCK/dBMAL (Zylka, M.J. et al. (1998) Neuron 20, 1103-1110; Lowrey, P.L. et al. (2000) 288, 483-491). Было показано, что ген dper является необходимым элементом контроля циркадных ритмов вылупления взрослой особи (появление взрослой мухи из куколки), поведения и локомоторной деятельности (Konopka, R.J., & Benzer, S. (1971) Proc. Natl. Acad. Sci. USA, 68, 2112-2116). Миссенс-мутации гена per могут либо укоротить (per S), либо удлинить (per L) период циркадного ритма, тогда как нонсенс-мутации (per o) порождают аритмичность в их поведении (Hall, J.C. (1995) Trends Neurosci. 18, 230-240).
У млекопитающих супрахиазматическое ядро (СХЯ) переднего гипоталамуса является местом нахождения главных биологических часов (см. обзор Panda et al., (2002) Nature 417, 329-335; Reppert, S.M. and Weaver, D.R. (1997) Cell, 89, 487-490). Часы СХЯ включены в 24-часовой дневной цикл за счет ежедневного цикла день-ночь, причем свет действует через прямые или непрямые пути сетчатка-СХЯ (Klein, D.C. et al. (1991) Suprachiasmatic Nuclei: The Mind's Clock, Oxford Univeristy Press, New York). В СХЯ грызунов выявлены и клонированы три гена Per, которые обозначаются как мышиные гены Per1 (mPer1), mPer2 и mPer3. Белки, соответствующие таким генам млекопитающих (mPER1, mPER2, mPER3), имеют несколько общих областей гомологии друг с другом, и каждый ген млекопитающих Per кодирует белок с доменом димеризации белка, который обозначается как PAS (PAS является инициальной аббревиатурой для первых трех белков PER, ARNT и SIM, которые, как было установлено, обладают таким функционально важным доменом димеризации), который высоко гомологичен домену PAS PER насекомых. Уровни матричных РНК Per (мРНК) и белка колеблются в течение циркадных суток и непосредственно участвуют в положительном и отрицательном регулировании биологических часов, но только mPER1 и mPER2 осциллируют в результате воздействия света (Zylka, M.J. et al. (1998) Neuron 20, 1103-1110; Albrecht, U. et al., (1997) Cell 91, 1055-1064; Shearman, L.P. et al. (1997) Neuron 19, 1261-1269). Гомолог гена Drosophila tim у млекопитающих был клонирован и обозначен как mTim. Тем не менее, не наблюдалось никаких доказательств взаимодействия mPER-mTIM, аналогичных регистрируемым у Drosophila, и было высказано предположение о том, что взаимодействия PER-PER могут быть заменены функциональными группами димеров PER-TIM при молекулярном действии циркадных часов млекопитающих (Zylka, M.J. et al., (1998) Neuron 21, 1115-1122). Другая возможность заключается в том, что ритмы в PER1 и PER2 образуют отрицательные обратные связи, которые регулируют транскрипционную активность белка Clock (через их домены PAS), что, в свою очередь, приводит в действие экспрессию любого или обоих генов Per (Shearman, L.P. et al. (1997) Neuron 19, 1261-1269).
Осмысление роли трех генов mPer в действии часового механизма млекопитающих были предметом множества исследований. Структурная гомология белков mPER по отношению к dPER позволила надеяться на то, что белки mPER будут функционировать в качестве отрицательных элементов в цепи обратной связи млекопитающих. Предполагается, что PER1 участвует в отрицательном регулировании собственной транскрипции в цепи обратной связи, но недавно полученные данные указывают на то, что он участвует во входном канале (Hastings, M.H. et al. (1999) Proc. Natl. Acad. Sci. USA 26, 15211-15216). PER2 является наиболее подробно описанным белком, а мутантный белок мыши mPER2 (mPer2 Brdm1), потерявший 87 остатков в карбоксильной части домена димеризации PAS, обладает укороченным циркадным циклом в нормальных условиях день-ночь, но проявляет аритмичность в полной темноте. Мутация также уменьшает осциллирующую экспрессию обоих mPer1 и mPer2 в СХЯ, показывая, что mPer2 может регулировать mPer1 «in vivo» (Zheng, B. et al. (1999) Nature 400, 169-173). Было показано, что PER2 обладает двойной функцией в регулировании «колесиков» в центральных часах (Shearman, L.P. et al. (2000) Science 288, 1013-1018). Данное исследование позволило продемонстрировать, что PER2 связывается с криптохромными (CRY) белками и транслоцируется в ядро, в котором отрицательно регулируемая транскрипция CRY приводится в действие положительными транскрипционными комплексами CLOCK и BMAL1. После проникновения в ядро PER2 инициирует положительный рычаг часов за счет положительного регулирования транскрипции BMAL1 по еще неизвестному механизму. Функция PER3 изучена недостаточно, однако, в mPer3 нокаутных мышей наблюдается слабое воздействие на циркадную активность и поэтому предполагалось, что PER3 участвует в циркадно регулируемых выходных каналах (Shearman, L.P. et al. (2000) Mol. Cell. Biol. 17, 6269-6275). Как сообщалось, белки mPER взаимодействуют друг с другом, и mPER3 может служить носителем mPER1 и mPER2 для доставки их в ядро, что имеет важнейшее значение для генерации циркадных сигналов в СХЯ (Kume, K. et al. (1999) Cell 98, 193-205; Takano, A. et al. (2000), FEBS Letters, 477, 106-112).
Постулировалось, что фосфорилирование компонентов циркадных часов регулирует продолжительность цикла. Первым генетическим свидетельством того, что специфическая протеинкиназа регулирует циркадный ритм Drosophila, было открытие нового гена doubletime (dbt), кодирующего протеин серин-треонин киназу (Price J.L. et al. (1998) Cell 94, 83-95; Kloss B. et al. (1998) Cell 94, 97-107). Миссенс-мутации в dbt приводят к измененному циркадному ритму. Нулевые аллели dbt вызывают гипофосфорилирование dPER и аритмию.
К киназам млекопитающих, наиболее близкородственным DBT, относятся казеинкиназа Iε (CKIε) и казеинкиназа Iδ (CKIδ). Показано, что обе киназы связываются с mPER1; в нескольких исследованиях было продемонстрировано, что CKIε фосфорилирует и мышиный, и человеческий PER1 (Price J.L. et al. (1998) Cell 94, 83-95; Kloss B. et al. (1998) Cell 94, 97-107). В исследовании клеток эмбриона почки человека 293T при совместном трансфицировании с hCKIε дикого типа hPER1 продемонстрировал значительное повышение фосфорилирования (продемонстрированное на примере сдвига молекулярной массы). В указанном исследовании фосфорилированный hPER1 имеет период полураспада, равный примерно двенадцати часам, тогда как нефосфорилированный hPER1 остается стабильным в клетке более 24 часов, указывая на то, что фосфорилирование hPER1 приводит к падению стабильности белка (Kessler, G.A. et al. (2000) NeuroReport, 11, 951-955). Другое исследование также позволило продемонстрировать, что последовательность фосфорилирования PER1 посредством hCKIε включает цитоплазматическую фиксацию и нестабильность белка (Vielhaber, E. et al. (2000) Mol. Cell. Biol. 13, 4888-4899; Takano, A. et al. (2000) FEBS Letters 477, 106-112).
Не было никаких биохимических причин выбирать между CKIε или CKIδ как потенциальным регулятором у млекопитающих до тех пор, пока в работе Lowery et al. [(2000) Science 288, 483-491] не было обнаружено, что у сирийского золотистого хомячка полудоминантные мутации в CKIε (мутация tau, Ralph, M.R. and Menaker, M. (1988) Science 241, 1225-1227) вызывали сокращение циркадных суток как у гетерозиготных (22 ч), так и у гомозиготных (20 ч) животных. В этом случае пониженные уровни активности CKIε приводили к меньшему фосфорилированию PER при предположительно более высоких уровнях цитоплазмического белка PER, что вызывало повышенное проникновение в ядро и изменение циркадных циклов. Позднее было предложено, что CKIδ может также участвовать в регулировании циркадной ритмичности за счет посттрансляционной модификации clock белков млекопитающих hPER1 и hPER2 [Camacho, F. et al., (2001) FEBS Letters 489(2,3), 159-165]. Соответственно ингибиторы, включая ингибиторы из числа малых молекул, CKIε и/или CKIδ человека или млекопитающих предоставляют новые возможности фазового сдвига или сброса циркадных часов. Как показано ниже, изменение циркадного ритма может оказаться полезным для лечения расстройств сна или настроения.
В патенте США 6555328 B1 раскрываются методы скрининга в клетках для выявления соединений, которые изменяют циркадные ритмы, основанные на тестовом соединении, меняющем способность человеческой казеинкиназы 1ε и/или человеческой казеинкиназы 1δ фосфорилировать человеческие clock белки hPER1, hPER2 и hPER3. Например, клетки HEK293T трансфицируются совместно с hCKIε и Per1 или Per2. В целях оценки значимости ингибирования CKIε и ингибиторов CKIε для циркадной биологии была создана высокопродуктивная клеточная культура (33rd Annual Meeting, Soc. for Neurosci., November 8-12, 2003, Abstract numbers 284.1, 284.2, and 284.3), в которой циркадные ритмы могут отслеживаться стандартным образом. Культура включает фибробласты Rat-1, стабильно экспрессирующие конструкцию Mper1-luc, тем самым позволяя определить ритмическую активацию промотера Mper1 в живых клетках посредством периодической оценки активности люциферазы с помощью мониторинга интенсивности света в течение нескольких дней. Формат периодического контроля культуры обеспечивает точную и воспроизводимую оценку концентрационно-зависимых эффектов воздействия ингибиторов CKIε на циркадный ритм и дает возможность, установить связь ингибирования CKIε с изменениями циркадного периода.
Нарушения сна подразделяют на четыре основные категории, которые включают первичные нарушения сна (диссомнии и парасомнии), расстройства сна, связанные с медицинскими/психическими нарушениями, и категорию предполагаемых расстройств сна для таких нарушений сна, которые невозможно классифицировать из-за недостатка данных. Считается, что первичные нарушения сна возникают из-за отклонений непосредственно в системах, ответственных за инициацию сна-пробуждения (гомеостатическая система) или регистрацию времени (циркадная система). Диссомнии относятся к нарушениям формирования или поддержания сна и включают первичную бессонницу, гиперсомнию (чрезмерную сонливость), нарколепсию, нарушения сна, связанные с дыханием, нарушения сна, связанные с циркадным ритмом, и диссомнии, не вошедшие в указанные категории. Первичная бессонница характеризуется сохраняющимися (>1 месяца) проблемами инициации и поддержания сна или невосстановительного сна. Проблемы сна, связанные с первичной бессонницей, приводят к значительным нарушениям или расстройствам, включая раздражительность в дневное время, потерю внимания и концентрации, усталость и недомогание и ухудшение настроения и мотивации. Нарушения сна, связанные с циркадным ритмом, включают синдром десинхроноза при перелетах, синдром нарушения сна при посменной работе, синдром преждевременной фазы сна и синдром задержки фазы сна (J. Wagner, M.L. Wagner and W.A. Hening, Annals of Pharmacotherapy (1998) 32, 680-691). Лица с режимом вынужденного сна демонстрируют более высокий уровень бодрствования в процентах от времени сна в определенные периоды циркадных суток (Dijk and Lockley, J. Appl. Physiol. (2002) 92, 852-862). Принято считать, что с возрастом происходит смещение циркадного ритма сна, которое часто приводит к менее качественному сну (Am J Physiol Endocrinol Metab. (2002) 282, E297-E303). Таким образом, сон, возникающий вне циркадной фазы, может быть ущербным с точки зрения качества и количества, что подкрепляется дополнительными примерами изменений сна при посменной работе и десинхронозе при перелетах. Изменение циркадных часов человека может вызывать нарушения сна, и агенты, которые модулируют циркадную ритмичность, например ингибитор CKIε и/или CKIδ, могут оказаться эффективными для лечения нарушений сна, в особенности тех из них, которые связаны с циркадным ритмом.
Нарушения настроения подразделяются на депрессивные расстройства («монополярные депрессии»), биполярные расстройства и два вида расстройств, основанных на этиологии, которые включают нарушения настроения, вызванные общим состоянием здоровья, и нарушение настроения, возникающие под воздействием наркотиков. Депрессивные расстройства дополнительно подразделяются на большие депрессивные расстройства, дистимические расстройства и депрессивные расстройства, не отнесенные к другим категориям. Биполярные расстройства дополнительно подразделяются на биполярные расстройства I и II типа. Отмечалось, что термин «сезонный характер» может применяться в отношении больших депрессивных расстройств, которые носят периодический характер, а также в отношении проявления приступов больших депрессивных расстройств в биполярных расстройствах I и II типа. Заметная анергия, гиперсомния, переедание, набор веса и потребность в углеводах часто характеризуют большие депрессивные проявления, которые носят сезонный характер. Неясно, являются ли подобные сезонные проявления нарушения настроения более характерными для больших депрессивных расстройств, носящих периодический характер, либо для биполярных расстройств. Тем не менее, в рамках биполярных расстройств сезонный характер представляется более вероятным при биполярных расстройствах II типа, чем при биполярных расстройствах I типа. У некоторых лиц вспышки маний или гипоманий могут быть также связаны с определенным временем года. Сезонность зимнего типа, как правило, различается в зависимости от географической широты, возраста и пола. Распространенность заболевания увеличивается в более высоких широтах, подверженность риску зимних вспышек депрессии уменьшается с возрастом, а женщины составляют от 60% до 90% от общего количества сезонно зависимых людей. Сезонные аффективные расстройства (SAD) - термин, широко используемый в литературе - являются подтипом расстройств настроения, которые в Руководстве по диагностике и статистике психических расстройств (DSM-IV) (American Psychiatric Association: "Diagnostic and Statistical Manual of Mental Disorders", Fourth Edition, Text Revision. Washington, DC, American Psychiatric Association, 2000) обозначаются термином «сезонного характера» при описании сезонного характера приступов больших депрессивных расстройств при биполярных расстройствах I типа, биполярных расстройствах II типа или периодических больших депрессивных расстройствах (E. M. Tam et al., Can. J. Psychiatry (1995) 40, 457-466). Характеристики и диагнозы депрессивных нарушений, больших депрессивных расстройств, приступов больших депрессивных расстройств, биполярных расстройств I типа, биполярных расстройств II типа и сезонных эффектов описаны в DSM-IV.
Пациенты, страдающие большими депрессивными расстройствами, в том числе SAD, которые характеризуются периодическими приступами депрессии, обычно зимой, продемонстрировали позитивную ответную реакцию на световую терапию (Kripke, Journal of Affective Disorders (1998) 49(2), 109-117). Успех применения терапии, основанной на использовании яркого света, для пациентов, страдающих SAD и большой депрессией, позволили выдвинуть несколько гипотез для объяснения фундаментального механизма действия терапевтического эффекта света. К таким гипотезам относится «гипотеза циркадного ритма», согласно которой антидепрессивный эффект яркого света может быть связан с фазовым сдвигом циркадного водителя ритма по отношению ко сну (E. M. Tam et al., Can. J. Psychiatry (1995) 40, 457-466). Подтверждением связи между световой терапией и циркадным ритмом стал тот факт, что клинически эффективная световая терапия при больших депрессивных расстройствах вызывает сопутствующий сдвиг в циркадной фазе, следовательно, клиническая эффективность световой терапии должна зависеть от способности световой терапии обеспечивать световой сдвиг (Czeisler et al., The Journal of Physiology (2000) 526 (Part 3), 683-694; Terman et al., Arch. Gen. Psychiatry (2001) 58, 69-75). Кроме того, было показано, что световая терапия ускоряет и усиливает эффективность фармакологического лечения больших депрессивных расстройств (Benedetti et al., J. Clin. Psychiatry (2003) 64, 648-653). В связи с этим можно предположить, что ингибирование казеинкиназы Iε и/или казеинкиназы Iδ вызовет сдвиг циркадной фазы, и такое ингибирование представляет собой потенциально клинически эффективную моно- или комбинированную терапию для нарушений настроения.
Следует отметить, что нарушение сна является критическим симптомом для многих психиатрических расстройств (W.V.McCall, J. Clin. Psychiatry (2001) 62 (suppl 10), 27-32). Нарушения сна представляют собой общую особенность депрессивных нарушений, в частности бессонница является нарушением сна, которое часто наблюдается при депрессии, присутствуя у более чем 90% пациентов, страдающих депрессией (M.E. Thase, J. Clin. Psychiatry (1999) 60 (suppl 17), 28-31). Накопленные данные подтверждают общий патогенез для первичной бессонницы и больших депрессивных расстройств. Высказывалась гипотеза о том, что гиперактивность рилизинг-фактора кортикотропина (CRF) (в связи с генетической предрасположенностью или, возможно, из-за раннего стресса) и стресс вызывают процесс, приводящий к повышенным и протяженным нарушениям сна и в конечном счете к первичной бессоннице. Циркадная ритмичность при секреции CRF в отсутствии стресса может играть роль обычной экспрессии сон-пробуждение (G.S. Richardson and T. Roth, J. Clin Psychiatry (2001) 62 (suppl 10), 39-45). Следовательно, вещества, которые модулируют циркадную ритмичность, например, посредством ингибирования казеинкиназы Iε и/или казеинкиназы Iδ, могут оказаться эффективными при лечении депрессивных нарушений, связанных с эффектами секреции CRF.
Все ссылки, упомянутые выше в настоящем документе, посредством ссылки на них полностью включаются в настоящий документ.
Таким образом, целью настоящего изобретения является получение ряда замещенных амидов 4H-тиено[3,2-b]пиррол-5-карбоновой кислоты, амидов 4H-пирроло[2,3-d]тиазол-5-карбоновой кислоты, амидов 6H-тиено[2,3-b]пиррол-5-карбоновой кислоты, амидов 4H-пирроло[3,2-d]тиазол-5-карбоновой кислоты и родственных аналогов, которые являются ингибиторами казеинкиназы Iε. Данная цель и другие цели настоящего изобретения раскрываются в приведенном ниже подробном описании изобретения.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение предлагает замещенные амиды 4H-тиено[3,2-b]пиррол-5-карбоновой кислоты, амиды 4H-пирроло[2,3-d]тиазол-5-карбоновой кислоты, амиды 6H-тиено[2,3-b]пиррол-5-карбоновой кислоты, амиды 4H-пирроло[3,2-d]тиазол-5-карбоновой кислоты и родственные аналоги формулы (I) и формулы (II), а также стереизомеры, энантиомеры, рацематы и таутомеры упомянутых соединений и их фармацевтически приемлемые соли в качестве ингибиторов казеинкиназы Iε, а также способы применение соединений формулы (I) и формулы (II) в качестве фармацевтических средств для лечения заболеваний и расстройств центральной нервной системы, таких как нарушения настроения, в том числе большие депрессивные расстройства, биполярные расстройства I типа, биполярные расстройства II типа и нарушения сна, включая нарушения сна, связанные с циркадным ритмом, например, расстройство сна при посменной работе, синдром десинхроноза при перелетах, синдром преждевременной фазы сна и синдром задержки фазы сна. В настоящем изобретении также приводятся способы получения соединений формулы (I) и формулы (II) настоящего изобретения.
Соответственно, общее воплощение настоящего изобретения сосредоточено на соединении формулы (I) или формулы (II):
где X - S или S(O)n;
R1 - H или C1-C6 алкил;
R2 - NR5R6;
R3 - арил или гетероцикл;
R4 - H, C1-C6 алкил, C2-C6 алкенил, C2-C6 алкинил, арил-(C1-C6 алкил), гетероцикл-(C1-C6 алкил), C1-C6 алкокси, арил-(C1-C6 алкокси), гетероцикл-(C1-C6 алкокси), CF3, галоген, SH, C1-6 алкилтио, арил-(C1-C6 алкилтио), гетероцикл-(C1-C6 алкилтио), NO2, NH2, NR5R6, арил-(C1-C6 алкиламино), гетероцикл-(C1-C6 алкиламино) или XR3, где X и R3 соответствуют вышеприведенному определению;
R5 - H или C1-C6 алкил;
R6 - H или C1-C6 алкил;
L - N или CR7, где R7 - H или C1-C6 алкил;
M - S, O или NR8, где R8 - H, C1-C6 алкил, арил-(C1-C6 алкил), гетероцикл-(C1-C6 алкил) или ацил;
n равно 1 или 2; или
его стереоизомере, энантиомере, рацемате или таутомере; или
их фармацевтически приемлемой соли.
Другое осуществление настоящего изобретения относится к способу ингибирования активности казеинкиназы Iε у пациента, включающему введение упомянутому пациенту терапевтически эффективного количества соединения формулы (I) или формулы (II).
Еще одно осуществление настоящего изобретения относится к способу лечения пациента, страдающего заболеванием или нарушением, которое улучшается при ингибировании активности казеинкиназы Iε, включающему введение упомянутому пациенту терапевтически эффективного количества соединения формулы I или формулы II.
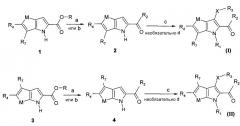
Дальнейшее осуществление настоящего изобретения относится к способу получения соединения формулы (I) или формулы (II).
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Используемый в настоящем документе термин «стереоизомер» является общим названием, применяемым для всех изомеров индивидуальных молекул, которые отличаются только пространственной ориентацией своих атомов. Термин «стереоизомер» включает зеркальные изомеры (энантиомеры), смеси зеркальных изомеров (рацематы, рацемические смеси), геометрические (цис/транс или E/Z) изомеры и изомеры соединений с несколькими хиральными центрами, не являющиеся зеркальными отображениями друг друга (диастереоизомеры). Соединения настоящего изобретения могут иметь асимметрические центры и существовать в виде рацематов, рацемических смесей, индивидуальных диастереоизомеров или энантиомеров, или же могут существовать в форме геометрических изомеров, причем все изомерные формы упомянутых соединений включены в настоящее изобретение.
Используемые в настоящем документе обозначения «R» и «S» применяются как повсеместно используемые в органической химии обозначения для указания специфической конфигурации хирального центра. Обозначение «R» (rectus, правый) относится к конфигурации хирального центра с расположением старших по рангу групп по часовой стрелке (от группы с наибольшим рангом к группе со вторым наименьшим), если смотреть вдоль связи в направлении группы, наименьшей по старшинству. Обозначение «S» (sinister, левый) относится к конфигурации хирального центра с расположением старших по рангу групп против часовой стрелки (от группы с наибольшим рангом к группе со вторым наименьшим), если смотреть вдоль связи в направлении группы, наименьшей по старшинству. Старшинство групп определяется правилами последовательности, причем приоритет, в первую очередь, основан на атомном номере (в порядке убывания атомных номеров). Перечень и обсуждение старшинства групп приводится в книге Stereochemistry of Organic Compounds, Ernest L. Eliel, Samuel H. Wilen and Lewis N. Mander, editors, Wiley-Interscience, John Wiley & Sons, Inc., New York, 1994.
Кроме системы (R)-(S), в настоящем документе может также применяться более ранняя система D-L для обозначения абсолютной конфигурации, особенно в отношении аминокислот. В данной системе формула проекции Фишера ориентируется таким образом, чтобы первый атом углерода основной цепи находился в верхней части. Префикс «D» используется для описания абсолютной конфигурации изомера, в которой функциональная (определяющая) группа находится справа от углерода хирального центра, а «L» - для изомера, в котором она расположена слева.
Используемые в настоящем документе термины «таутомер» или «таутомерия» описывают одновременное существование двух (или более) соединений, которые отличаются друг от друга только положением одного (или нескольких) подвижных атомов, а также распределением электронов, например кето-енольные таутомеры или таутомерия.
Применяемый в настоящем документе термин «алкил» относится к насыщенной алифатической углеводородной группе с линейной или разветвленной цепью, имеющей от одного до шести атомов углерода, и включает метил, этил, пропил, изопропил, бутил, втор-бутил, трет-бутил и подобные им группы. С термином «алкил» связаны также термины «алкилен» или «алкиленил», определение которых приводится ниже.
Использованные ниже в настоящем документе термины «алкилен» или «алкиленил» относятся к линейной или разветвленной двухвалентной насыщенной алифатической цепи, имеющей от одного до шести углеродов, и включают метиленил, этиленил, пропиленил, изопропиленил, бутиленил, изобутиленил, трет-бутиленил, пентиленил, изопентиленил, гексиленил и подобные им группы.
Используемый в настоящем документе термин «алкенил» относится к линейной или разветвленной, моновалентной ненасыщенной алифатической цепи, которую образуют от двух до шести атомов углерода, и включает этенил (также известный как винил), 1-метилэтенил, 1-метил-1-пропенил, 1-бутенил, 1-гексенил, 2-метил-2-пропенил, 2,4-гексадиенил, 1-пропенил, 2-пропенил, 2-бутенил, 2-пентенил и подобные им группы.
Упомянутый в настоящем документе термин «алкинил» относится к линейному или разветвленному моновалентному ненасыщенному углеводороду, содержащему от двух до шести атомов углерода, связанных по крайней мере одной тройной связью, и включает этинил, 1-пропинил, 1-бутинил, 1-гексинил, 2-пропинил, 2-бутинил, 2-пентинил и подобные им группы.
Использованный в настоящем документе термин «алкокси» или «алкилокси» относится к моновалентному заместителю, который включает линейную или разветвленную алкильную цепь, содержащую от одного до шести атомов углерода, связанную через атом кислорода простого эфира, и имеет свободную валентную связь от эфирного кислорода. Данное понятие объединяет метокси, этокси, пропокси, изопропокси, бутокси, втор-бутокси, трет-бутокси и подобные им группы.
Применяемый в настоящем документе термин «алкилтио» относится к моновалентному заместителю, который включает линейную или разветвленную алкильную цепь, содержащую от одного до шести атомов углерода, связанную через атом серы, и имеет свободную валентную связь от серы. Сюда относятся метилтио, этилтио, пропилтио, изопропилтио, бутилтио, втор-бутилтио, трет-бутилтио и подобные им группы.
Используемый в настоящем документе термин «алкенилокси» относится к линейной или разветвленной, моновалентной ненасыщенной алифатической цепи, которую образуют от двух до шести атомов углерода, связанной через атом кислорода простого эфира, и имеет свободную валентную связь от эфирного кислорода. Данное понятие включает этенилокси (также известный как винилокси), 1-метилэтенилокси, 1-метил-1-пропенилокси, 1-бутенилокси, 1-гексенилокси, 2-метил-2-пропенилокси, 2,4-гексадиенилокси, 1-пропенилокси, 2-пропенилокси, 2-бутенилокси, 2-пентенилокси и подобные им группы.
Используемый в настоящем документе термин «алкинилокси» относится к линейной или разветвленной, моновалентной, ненасыщенной алифатической цепи, включающей от двух до шести атомов углерода с по крайней мере одной тройной связью, связанной через атом кислорода простого эфира и имеющей свободную валентную связь от эфирного кислорода, и включает этинилокси, 1-пропинилокси, 1-бутинилокси, 1-гексинилокси, 2-пропинилокси, 2-бутинилокси, 2-пентинилокси и подобные им группы.
Применяемый в настоящем документе термин C3-C8 циклоалкил относится к насыщенной углеводородной циклической структуре, содержащей от трех до восьми атомов углерода, и включает циклопропил, циклобутил, циклопентил, циклогексил, циклогептил и им подобные.
Используемый в настоящем документе термин «арил» или «Ar» означает любое стабильное моноциклическое, бициклическое или трициклическое углеродное кольцо (до семи членов в каждом кольце), причем по крайней мере одно кольцо является ароматическим и незамещенным или содержащим от одного до трех заместителей, выбранных из группы, включающей метилендиокси, гидрокси, C1-C6 алкокси, галоген, C1-C6 алкил, C2-C6 алкенил, C2-C6 алкинил, трифторметокси, -NO2, -NH2, -NH(C1-C6 алкил), -N(C1-C6 алкил)2, -NH-ацил и -N(C1-C6 алкил)ацил. Примеры «арил» или «Ar» включают фенил, 2-хлорфенил, 3-хлорфенил, 4-хлорфенил, 2-фторфенил, 3-фторфенил, 4-фторфенил, 2-бромфенил, 3-бромфенил, 4-бромфенил, 2-трифторметилфенил, 3-трифторметилфенил, 4-трифторметилфенил, 2-метоксифенил, 3-метоксифенил, 4-метоксифенил, 2-аминофенил, 3-аминофенил, 4-аминофенил, 2-метилфенил, 3-метилфенил, 4-метилфенил, 2-нитрофенил, 3-нитрофенил, 4-нитрофенил, 2,4-дихлорфенил, 2,3-дихлорфенил, 3,5-диметилфенил, 2-трифторметоксифенил, 3-трифторметоксифенил, 4-трифторметоксифенил, нафтил, тетрагидронафтил и бифенил.
Используемый в настоящем документе термин «арил-(C1-C6 алкил)» относится к арильной группе, соответствующей приведенному выше определению, связанной посредством линейной или разветвленной алкиленовой цепи, содержащей от одного до шести атомов углерода и имеющей свободную валентную связь у одного из углеродов алкиленовой цепи. Примеры «арил-(C1-C6 алкила)» включают фенилметил (бензил), фенилэтил, п-метоксибензил, п-фторбензил, п-хлорбензил и подобные им группы.
Применяемый в настоящем документе термин «арил-(C1-C6 алкокси)» относится к арильной группе, соответствующей приведенному выше определению, связанной посредстовом линейной или разветвленной алкиленовой цепи, содержащей от одного до шести атомов углерода, связанной через атом кислорода простого эфира и имеющей свободную валентную связь у атома кислорода простого эфира. Примеры арил-(C1-C6 алкокси) включают фенилметокси (бензилокси), фенилэтокси и подобные им группы.
Используемый в настоящем документе термин «арил-(C1-C6 алкиламино)» относится к арильной группе, соответствующей приведенному выше определению, связанной линейной или разветвленной алкиленовой цепью, содержащей от одного до шести атомов углерода, связанной через атом азота и имеющей свободную валентную связь у атома азота, при этом упомянутый атом азота может быть замещен водородом или C1-C6 алкилом. Примеры арил-(C1-C6 алкиламино) включают фенилметиламино (бензиламино), фенилэтиламино, N-метил-N-бензиламино и подобные им группы.
Используемый в настоящем документе термин «арил-(C1-C6 алкилтио)» относится к арильной группе, соответствующей приведенному выше определению, связанной линейной или разветвленной алкиленовой цепью, содержащей от одного до шести атомов углерода, связанной через атом серы и имеющей свободную валентную связь у атома серы. Примеры арил-(C1-C6 алкилтио) включают фенилметилтио (бензилтио), фенилэтилтио и подобные им группы.
Применяемый в настоящем документе термин «ацил» относится к H-(C=O)-, C1-C6 алкил-(C=O)-, арил-(C=O)-, арил(C1-C6 алкил)-(C=O)-, гетероцикл-(C=O)- или гетероцикл(C1-C6 алкил)-(C=O)- группе, где алкил, арил и гетероцикл соответствуют определению, приведенному в настоящем документе, и имеют свободную валентную связь при карбонильной группе (C=O). В определение ацила включаются ацетил, пропионил, бутирил, изобутирил, трифторацетил, трихлорацетил, бензоил и подобные им группы.
Используемый в настоящем документе термин «гетероцикл» или «гетероциклил» применяется для описания стабильного 5-7-членного моноциклического или стабильного 8-11-членного бициклического гетероциклического кольца, которое является насыщенным или ненасыщенным и состоит из атомов углерода и одного-трех гетероатомов, выбираемых из группы, включающей N, O и S, и в котором гетероатомы азота и серы могут быть окислены, а гетероатом азота может быть кватернизирован, также включает любую бициклическую группу, в которой любое из определенных выше гетероциклических колец конденсировано с бензольным кольцом. Гетероциклическое кольцо может быть присоединено через любой гетероатом или атом углерода, что приводит к образованию стабильной структуры. Гетероциклическое кольцо может быть незамещенным или замещенным одним, двумя или тремя заместителями, выбранными из группы, включающей C1-C6 алкокси, гидрокси, галоген, C1-C6 алкил, C2-C6 алкенил, C2-C6 алкинил, трифторметил, трифторметокси, -NO2, -NH2, -NH(C1-C6 алкил), -N(C1-C6 алкил)2, -NH-ацил и -N(C1-C6 алкил)ацил. Примеры таких гетероциклических групп включают пиперидинил, пиперазинил, 2-оксопиперазинил, 2-оксопиперидинил, 2-оксопирролидинил, 2-оксоазепинил, азепинил, пирролил, пирролидинил, пиразолил, пиразолидинил, имидазолил, имидазолинил, имидазолидинил, пиридил, пиразинил, пиримидинил, пиридазинил, оксазолил, оксазолидинил, изоксазолил, изоксалидинил, морфолинил, тиазолил, тиазолидинил, изотиазолил, хинуклидинил, изотиазолидинил, индолил, хинолинил, изохинолинил, бензимидазолил, тиадиазолил, бензопиранил, бензотиазолил, бензооксазолил, фурил, тетрагидрофурил, бензофуранил, тетрагидропиранил, тиенил, бензотиенил, тиаморфолинил и оксадиазолил.
Используемый в настоящем документе термин «гетероцикл-(C1-C6 алкил)» или «гетероциклил-(C1-C6 алкил)» относится к гетероциклу или гетероциклическому кольцу, соответствующему приведенному выше определению, связанному посредством линейной или разветвленной алкиленовой цепи, содержащей от одного до шести атомов углерода, с другим атомом углерода или гетероатомом, выбираемым из груп