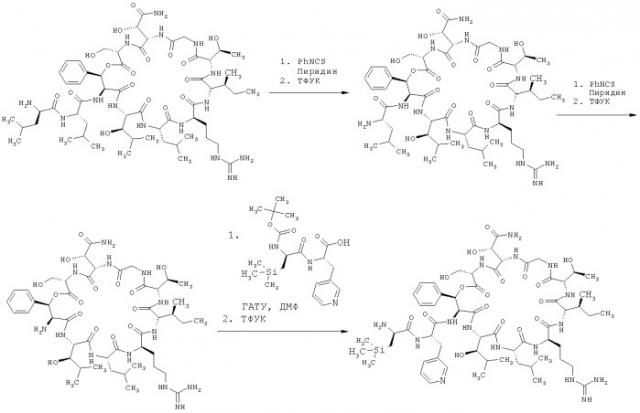
Ацилированные нонадепсипептиды в качестве производных лизобактина
Иллюстрации
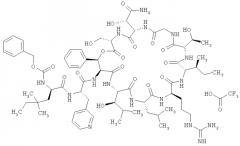
Показать всеПредложены производные лизобактина, способ их получения, а также их применение для приготовления лекарственных средств, предназначенных для лечения и/или профилактики заболеваний, вызываемых бактериями. Производные лизобактина отличаются от природного вещества наличием N-концевой пептидной цепи, содержащей 3-(3-пиридил)аланильный остаток. 5 н. и 5 з.п. ф-лы, 1 табл.
Реферат
Настоящее изобретение относится к нонадепсипептидам и способу их получения, а также к их применению для приготовления лекарственных средств, предназначенных для лечения и/или профилактики различных болезней, прежде всего вызываемых бактериями инфекционных болезней.
Клеточная стенка бактерий синтезируется целым рядом ферментов (биосинтез клеточной стенки) и играет важную роль в выживании, соответственно размножении микроорганизмов. Структура этой макромолекулы, равно как и участвующие в ее синтезе белки, надежно законсервированы внутри бактерий. Биосинтез клеточной стенки с учетом его важного значения и единообразия его протекания является идеальной мишенью для вновь разрабатываемых антибиотиков (D.W.Green, The bacterial cell wall as a source of antibacterial targets. Expert Opin. Ther. Targets, 6, 2002, cc.1-19).
В качестве типичных примеров ингибиторов биосинтеза клеточной стенки бактерий можно назвать ванкомицин и пенициллины, в основе антибиотической активности которых лежит указанный механизм действия. Эти антибиотики на протяжении нескольких десятилетий используются во врачебной практике для лечения бактериальных инфекций, прежде всего инфекций, вызываемых грамположительными возбудителями. Однако в связи с непрерывным появлением все новых и новых устойчивых к антибиотикам микроорганизмов, например устойчивых к метициллину стафилококков, устойчивых к пенициллину пневмококков и устойчивых к ванкомицину энтерококков (F. Baquero, Gram-positive resistance: challenge for the development of new antibiotics, J. Antimicrob. Chemother., 39, 1997, дополн. А, cc.1-6; A.P.Johnson, D.M.Livermore, G.S.Tillotson, Antimicrobial susceptibility of Gram-positive bacteria: what's current, what's anticipated?, J. Hosp.Infect., (49), 2001, дополн. А, cc.3-11), а также недавно впервые обнаруженных устойчивых к ванкомицину стафилококков (В. Goldrick, First reported case of VRSA in the United States, Am. J. Nurs., 102, 2002, с.17), терапевтическая эффективность от применения подобных антибиотиков постоянно снижается.
В настоящем изобретении предлагаются соединения, образующие новый класс ингибиторов биосинтеза клеточной стенки бактерий, к которым в отличие от антибиотиков известных классов у бактерий отсутствует устойчивость.
В US 4754018 описано природное вещество лизобактин и некоторые его производные как обладающие антибактериальным действием. Выделение лизобактина и его антибактериальное действие описаны также в ЕР-А-196042 и JP 01-132600. В WO 04/099239 описаны производные лизобактина с антибактериальным действием.
Антибактериальное действие лизобактина и катаносина А описано далее у O'Sullivan J. и др., J. Antibiot., 41, 1988, cc.1740-1744, у Bonner D.P. и др., J. Antibiot., 41, 1988, cc.1745-1751, у Shoji J. и др., J. Antibiot., 41, 1988, cc.713-718, а также у Tymiak А.А. и др., J. Org. Chem., 54, 1989, cc.1149-1157.
В основу настоящего изобретения была положена задача предложить другие соединения с антибактериальным действием, сравнимым с антибактериальным действием известных веществ или превосходящим его, с лучшей по сравнению с известными веществами переносимостью, например с пониженной нефротоксичностью, и лучшим распределением в организме, т.е. с лучшими фармакокинетическими свойствами, проявляющимися, например, в повышении свободной фракции (fu), для лечения бактериальных заболеваний у человека и животных.
Объектом настоящего изобретения являются соединения формулы
,
в которой R1 обозначает водород, а
R2 обозначает 2,2-диметилбут-1-ил, 2-этил-2-метилбут-1-ил, 2,2-диэтилбут-1-ил, 2,2-диметилпент-1-ил или триметилсилилметил либо
R1 обозначает трифторметил, а
R2 обозначает 2,2-диметилпроп-1-ил, 2,2-диметилбут-1-ил, 2-этил-2-метилбут-1-ил, 2,2-диэтилбут-1-ил, 2,2-диметилпент-1-ил или триметилсилилметил,
и их соли, их сольваты и сольваты их солей.
К предлагаемым в изобретении соединениям относятся соединения формулы (I) и их соли, сольваты, сольваты солей и пролекарства, подпадающие под формулу (I) соединения приведенных ниже формул и их соли, сольваты, сольваты солей и пролекарства, а также подпадающие под формулу (I), указанные ниже в качестве примеров соединения и их соли, сольваты, сольваты солей и пролекарства, при условии, что подпадающие под формулу (I), указанные ниже соединения уже не представляют собой соли, сольваты, сольваты солей и пролекарства.
Предлагаемые в изобретении соединения могут в зависимости от их структуры существовать в стереоизомерных формах (энантиомеров, диастереомеров). В соответствии с этим в объем изобретения включены все такие энантиомеры или диастереомеры и их соответствующие смеси. Из подобных смесей энантиомеров и/или диастереомеров индивидуальные стереоизомеры можно выделять известными методами.
Поскольку предлагаемые в изобретении соединения могут существовать в таутомерных формах, все они также включены в объем изобретения.
К предпочтительным солям согласно настоящему изобретению относятся физиологически безвредные соли предлагаемых в изобретении соединений. Однако в объем изобретения включены также соли, которые как таковые не пригодны для фармацевтического применения, но могут использоваться, например, для выделения или очистки предлагаемых в изобретении соединений, или смешанные соли. Под смешанной солью согласно настоящему изобретению подразумеваются аддитивная соль, образованная с двумя или более различными кислотами, соответственно основаниями, например трифторацетат-мезилат.
К физиологически безвредным солям предлагаемых в изобретении соединений относятся кислотно-аддитивные соли, образованные с минеральными кислотами, карбоновыми кислотами и сульфоновыми кислотами, например соли, образованные с хлористоводородной кислотой, бромистоводородной кислотой, серной кислотой, фосфорной кислотой, метансульфоновой кислотой, этансульфоновой кислотой, толуолсульфоновой кислотой, бензолсульфоновой кислотой, нафталиндисульфоновой кислотой, уксусной кислотой, трифторуксусной кислотой, пропионовой кислотой, молочной кислотой, винной кислотой, яблочной кислотой, лимонной кислотой, фумаровой кислотой, малеиновой кислотой и бензойной кислотой.
К физиологически безвредным солям предлагаемых в изобретении соединений относятся также образованные с обычными основаниями соли, в качестве предпочтительных примеров которых можно назвать соли, образованные с щелочными металлами (например, натриевые и калиевые соли), соли, образованные с щелочноземельными металлами (например, кальциевые и магниевые соли), и аммониевые соли, полученные взаимодействием с аммиаком или органическими аминами с 1-16 С-атомами, в качестве предпочтительных примеров которых можно назвать этиламин, диэтиламин, триэтиламин, этилдиизопропиламин, моноэтаноламин, диэтаноламин, триэтаноламин, дициклогексиламин, диметиламиноэтанол, прокаин, дибензиламин, N-метилморфолин, аргинин, лизин, этилендиамин и N-метилпиперидин.
Сольватами согласно настоящему изобретению называют те формы предлагаемых в изобретении соединений, которые в твердом или жидком состоянии образуют комплекс в результате координационной реакции с молекулами растворителя. Гидраты являются частной формой сольватов, образующихся в результате координационной реакции с водой.
Предпочтительны соединения формулы (I), в которой
R1 обозначает водород, а
R2 обозначает 2,2-диметилбут-1-ил или триметилсилилметил либо
R1 обозначает трифторметил, а
R2 обозначает 2,2-диметилпроп-1-ил, 2,2-диметилбут-1-ил или триметилсилилметил,
и их соли, их сольваты и сольваты их солей.
Предпочтительны также соединения формулы (I), в которой
R1 обозначает водород, а
R2 обозначает 2,2-диметилбут-1-ил, 2-этил-2-метилбут-1-ил, 2,2-диэтилбут-1-ил или триметилсилилметил,
и их соли, их сольваты и сольваты их солей.
Предпочтительны далее соединения формулы (I), в которой
R1 обозначает водород, а
R2 обозначает 2,2-диметилбут-1-ил, 2-этил-2-метилбут-1-ил, 2,2-диэтилбут-1-ил, 2,2-диметилпент-1-ил или триметилсилилметил.
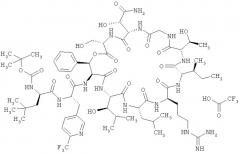
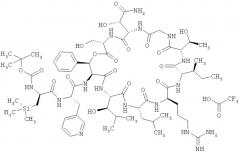
Наиболее предпочтительным соединением является 3-(триметилсилил)-D-аланил-3-(пиридин-3-ил)-L-аланилдез(1-D-лейцил-2-L-лейцил)лизобактин
,
или одна из его солей, один из его сольватов или один из сольватов его солей.
Объектом изобретения является далее способ получения соединений формулы (I), заключающийся в том, что соединение формулы
,
подвергают взаимодействию с соединениями формулы
,
в которой R1 и R2 имеют указанные выше значения, а
Х1 обозначает галоген, предпочтительно бром, хлор или фтор, или гидроксигруппу.
Если Х1 обозначает галоген, то указанное взаимодействие в общем случае проводят в инертных растворителях, при необходимости в присутствии основания, предпочтительно при температуре в интервале от -30 до 50°С и при нормальном давлении.
В качестве примера инертных растворителей можно назвать тетрагидрофуран, метиленхлорид, пиридин, диоксан или диметилформамид, при этом предпочтительно использовать метиленхлорид или диметилформамид.
В качестве примера оснований можно назвать триэтиламин, диизопропилэтиламин или N-метилморфолин, при этом предпочтительно использовать диизопропилэтиламин.
Если Х1 обозначает гидроксигруппу, то вышеуказанное взаимодействие в общем случае проводят в инертных растворителях в присутствии дегидратирующего агента и при необходимости в присутствии основания, предпочтительно при температуре в интервале от -30 до 50°С и при нормальном давлении.
В качестве примера инертных растворителей можно назвать галогенированные углеводороды, такие как дихлорметан или трихлорметан, и углеводороды, такие как бензол, нитрометан, диоксан, диметилформамид или ацетонитрил. Равным образом возможно использование и смесей растворителей. Наиболее предпочтительно использовать в качестве растворителя дихлорметан или диметилформамид.
Для применения в качестве дегидратирующих агентов пригодны, например, карбодиимиды, такие как N,N'-диэтил-, N,N'-дипропил-, N,N'-диизопропил-, N,N'-дициклогексилкарбодиимид, гидрохлорид N-(3-диметиламиноизопропил)-N'-этилкарбодиимида (ЭДК), N-циклогексилкарбодиимид-N'-пропилоксиметил-полистирол (ПС-карбодиимид), карбонильные соединения, такие как карбонилдиимидазол, 1,2-оксазолиевые соединения, такие как 2-этил-5-фенил-1,2-оксазолий-3-сульфат или 2-трет-бутил-5-метилизоксазолийперхлорат, ациламиносоединения, такие как 2-этокси-1-этоксикарбонил-1,2-дигидрохинолин, либо пропанфосфоновый ангидрид, изобутилхлорформиат, бис-(2-оксо-3-оксазолидинил)фосфорилхлорид, гексафторфосфат бензотриазолилокситри(диметиламино)фосфония, гексафторфосфат О-(бензотриазол-1-ил)-N,N,N',N'-тетраметилурония (ГБТУ), тетрафторборат 2-(2-оксо-1-(2Н)-пиридил)-1,1,3,3-тетраметилурония (ТФТУ), гексафторфосфат O-(7-aзaбeнзoтpиaзoл-1-ил)-N,N,N',N'-тeтpaмeтилypoния (ГАТУ), 1-гидроксибензотриазол (ГОБТ), гексафторфосфат бензотриазол-1-илокси-трис-(диметиламино)фосфония (БОФ), N-гидроксисукцинимид или их смеси с основаниями.
В качестве примера оснований можно назвать карбонаты щелочных металлов, такие, например, как карбонат натрия или калия, или гидрокарбонаты щелочных металлов, либо органические основания, такие как триалкиламины, например триэтиламин, N-метилморфолин, N-метилпиперидин, 4-диметиламинопиридин или диизопропилэтиламин.
В реакции конденсации предпочтительно использовать ГАТУ либо ЭДК в присутствии ГОБТ.
В некоторых случаях соединения формулы (III) могут нести защитные группы, и поэтому в подобных случаях по завершении взаимодействия соединения формулы (II) с соединениями формулы (III) такие защитные группы отщепляют обработкой трифторуксусной кислотой по известным методам.
Свободное основание из солей соединений формулы (I) можно получать, например, добавлением основания с последующей экстракцией, осаждением или хроматографическим отделением свободного соединения по известным методам, прежде всего за счет применения связанных с полимером оснований, например связанного с полимером гидрокарбоната.
Еще одним объектом изобретения является способ получения соединений формулы (I) или их сольватов, заключающийся в том, что соли таких соединений или сольваты солей таких соединений путем добавления основания переводят в свободные соединения.
Соединение формулы (II) можно синтезировать из лизобактина (пример 1А) путем двойной деградации по Эдману по описанной в экспериментальной части в примере 2А методике.
Соединения формулы (III) известны либо их можно синтезировать по известным методам из соответствующих эдуктов.
Получение предлагаемых в изобретении соединений можно пояснить с помощью приведенной ниже схемы синтеза.
Схема синтеза
Предлагаемые в изобретении соединения обладают ценным фармакологическим и фармакокинетическим спектром действия, который невозможно было предсказать заранее. Предлагаемые в изобретении соединения обладают, в частности, антибактериальным действием.
В соответствии с этим предлагаемые в изобретении соединения пригодны для их применения в качестве лекарственных веществ для лечения и/или профилактики различных заболеваний у человека и животных.
Предлагаемые в изобретении соединения обладают меньшей по сравнению с лизобактином нефротоксичностью.
Предлагаемые в изобретении соединения обладают также лучшими по сравнению с лизобактином фармакокинетическими свойствами. Предлагаемые в изобретении соединения при таком же или лучшем по сравнению с лизобактином фармакологическом действии обладают лучшим в сопоставлении с ним распределением в организме, что позволяет применять их в меньшей терапевтической дозе, а также расширить область их терапевтического применения.
Для предлагаемых в изобретении соединений характерно также их более высокое по сравнению с лизобактином содержание в виде свободной фракции (fu) в плазме.
Предлагаемые в изобретении нонадепсипептиды обладают действием ингибиторов биосинтеза бактериальной клеточной стенки.
Предлагаемые в изобретении соединения наиболее эффективны при борьбе с бактериями и сходными с ними микроорганизмами. Поэтому предлагаемые в изобретении соединения наиболее пригодны для профилактики и химиотерапии вызываемых этими возбудителями локальных и системных инфекционных болезней в медицине и ветеринарии.
В принципе предлагаемые в изобретении соединения могут применяться для борьбы со всеми бактериями и сходными с ними микроорганизмами, которые имеют бактериальную клеточную стенку (Murein sacculus), соответственно относящуюся к ней ферментативную систему, например, могут применяться для профилактики и химиотерапии инфекционных болезней, вызываемых одним или несколькими возбудителями, к которым относятся следующие: грамотрицательные кокки (Neisseria gonorrhoeae) и грамотрицательные палочки, такие как кишечные бактерии, например Escherichia coli, Hämophilus influenzae, бактерии рода псевдомонас, бактерии рода клебсиелл, бактерии рода цитробактер (С.freundii, С.divernis), бактерии рода сальмонелл, бактерии рода шигелл, бактерии рода энтеробактер (Е. aerogenes, Е. agglomerans) и бактерии рода Hafhia, бактерии рода Serratia (S. marcescens), бактерии рода провиденция, бактерии рода иерсиний, а также бактерии родов ацинетобактер, бранхамелл и хламидий. Помимо этого антибактериальный спектр действия предлагаемых в изобретении соединений охватывает облигатные анаэробные бактерии, такие, например, как Bacteroides fragilis, представители рода пептококков, рода пептострептококков и рода клостридий, а также микобактерии, например М. tuberculosus. Наиболее выраженное действие предлагаемые в изобретении соединения проявляют против грамположительных кокков, например, стафилококков (S. aureus, S. epidermidis, S. haemolyticus, S. carnosus), энтерококков (E. faecalis, E. faecium) и стрептококков (S. agalactiae, S. pneumoniae, S. pyogenes).
Перечисленные выше возбудители инфекционных болезней представлены лишь в качестве примера, и их перечень не исчерпывается приведенным выше.
В качестве примера болезней, которые вызываются вышеуказанными возбудителями или смешанными инфекциями и которые можно предупредить или вылечить либо при которых можно добиться улучшения за счет применения предлагаемых в изобретении соединений, можно назвать инфекционные болезни человека, такие как неосложненные и осложненные инфекции мочевых путей, неосложненные кожные и поверхностные инфекции, осложненные инфекции кожи и мягких тканей, приобретенная в больнице или амбулаторно-поликлиническом учреждении пневмония, внутрибольничные пневмонии, острые обострения и вторичные бактериальные инфекции при хроническом бронхите, острый средний отит, острый синусит, стрептококковый фарингит, бактериальный менингит, неосложненные гонококковые и негонококковые уретрит/цервицит, острый простатит, эндокардит, неосложненные и осложненные внутрибрюшные инфекции, гинекологические инфекции, воспаление в области таза, бактериальный вагиноз, острый и хронический остеомиелит, острый бактериальный артрит, гранулоцитопения (нейротропения) у лихорадящих пациентов, для лечения которых применяется эмпирическая терапия, а также бактериемии, вызываемые MRSA-штаммами инфекции, острая инфекционная диарея, вызываемые бактерией Helicobacter pylori инфекции, одонтогенные инфекции, офтальмологические инфекции, послеоперационные инфекции (включая перипроктальный абсцесс, раневые инфекции, инфекции желчных путей, мастит и острый аппендицит), кистозный фиброз и бронхоэктазия.
Предлагаемые в изобретении соединения можно использовать не только для профилактики или лечения инфекционных болезней человека, но и при бактериальных инфекциях у других видов. В качестве примеров при этом можно назвать диарею, энтеротоксемию, сепсис, дизентерию, сальмонеллез, синдром метрита-мастита-агалактита и мастит у свиней, диарею, сепсис, бронхопневмонию, сальмонеллез, пастереллез и инфекции половых органов у жвачных животных (крупного рогатого скота, овец, коз), бронхопневмонии, суставолом, пуэрперальные инфекции и сальмонеллез у лошадей, бронхопневмонию, диарею, дерматит, отит, инфекции мочевых путей и простатит у собак и кошек, вызываемые Е. coli инфекции, хронические заболевания дыхательных путей, сальмонеллез, пастереллез и пситтакоз у домашней птицы (кур, индеек, перепелов, голубей, декоративных птиц и других).
Предлагаемые в изобретении соединения могут также использоваться для лечения бактериальных заболеваний промысловых рыб и декоративных рыбок при их разведении и содержании, и в этом случае антибактериальный спектр действия предлагаемых в изобретении соединений помимо вышеуказанных возбудителей охватывает и других возбудителей, таких, например, как бактерии рода пастерелл, бактерии рода бруцелл, бактерии рода кампилобактер, бактерии рода листерий, бактерии рода эризипилотрикс, коринебактерии, бактерии рода боррелий, бактерии рода трепонем, бактерии рода нокардий, бактерии рода риккетсий и бактерии рода иерсиний.
Следующим объектом настоящего изобретения является применение предлагаемых в нем соединений для лечения и/или профилактики заболеваний, прежде всего бактериальных инфекционных болезней.
Следующим объектом настоящего изобретения является применение предлагаемых в нем соединений для лечения и/или профилактики заболеваний, прежде всего указанных выше заболеваний.
Следующим объектом настоящего изобретения является применение предлагаемых в нем соединений для приготовления лекарственного средства, предназначенного для лечения и/или профилактики заболеваний, прежде всего указанных выше заболеваний.
Предлагаемые в изобретении соединения предпочтительно применять для приготовления лекарственных средств, пригодных для профилактики и/или лечения бактериальных заболеваний.
Следующим объектом настоящего изобретения является способ лечения и/или профилактики заболеваний, прежде всего указанных выше заболеваний, с применением предлагаемых в изобретении соединений в антибактериально эффективном количестве.
Следующим объектом настоящего изобретения являются лекарственные средства, содержащие по меньшей мере одно предлагаемое в изобретении соединение и по меньшей мере одно или несколько других действующих веществ и предназначенных прежде всего для лечения и/или профилактики указанных выше заболеваний. К предпочтительным действующим веществам, которые могут использоваться в сочетании с предлагаемыми в изобретении соединениями, относятся соединения с антибактериальным действием, которые обладают спектром действия, отличным от спектра действия предлагаемых в изобретении соединений, прежде всего дополняющим его спектром действия, и/или при применении которых в комбинации с предлагаемыми в изобретении соединениями проявляется синергетический эффект.
Предлагаемые в изобретении соединения могут обладать системным и/или местным действием. Для этого их можно применять или вводить в организм соответствующим способом, например перорально, парентерально, через легкие, назально, подъязычно, лингвально, трансбуккально, ректально, накожно, чрескожно, конъюнктивально, в уши или в виде имплантата, соответственно стента.
Для подобного применения предлагаемые в изобретении соединения можно использовать в составе соответствующих лекарственных форм.
Для перорального применения пригодны действующие в соответствии с известными из уровня техники принципами лекарственные формы с быстрым и/или модифицированным высвобождением предлагаемых в изобретении соединений, содержащихся в таких лекарственных формах в кристаллическом, и/или аморфном, и/или растворенном виде, например таблетки (таблетки без покрытия или с покрытием, например, устойчивыми к действию желудочного сока или начинающими растворяться с задержкой либо нерастворимыми покрытиями, регулирующими или контролирующими высвобождение предлагаемых в изобретении соединений), быстро распадающиеся в полости рта таблетки или пленки/облатки, пленки/лиофилизаты, капсулы (например, твердо- или мягкожелатиновые капсулы), драже, грануляты, пеллеты, порошки, эмульсии, суспензии, аэрозоли или растворы.
Парентеральное введение предлагаемых в изобретении соединений в организм либо может происходить, минуя стадию их резорбции (например, внутривенно, внутриартериально, внутрисердечно, интраспинально или внутрилюмбально), либо может происходить, включая стадию резорбции (например, внутримышечно, подкожно, внутрикожно, чрескожно или внутрибрюшинно). Для парентерального применения в качестве лекарственных форм пригодны помимо прочего составы для инъекций и инфузий в виде растворов, суспензий, эмульсий, лиофилизатов или стерильных порошков.
Для применения предлагаемых в изобретении соединений остальными способами пригодны, например, ингаляционные лекарственные формы (в частности, для порошковых ингаляторов, небулайзеров), назальные капли, растворы и спреи, таблетки для лингвального, подъязычного или трансбуккального применения, пленки/облатки либо капсулы, суппозитории, ушные или глазные препараты, вагинальные капсулы, водные суспензии (примочки, болтушки), липофильные суспензии, мази, кремы, трансдермальные терапевтические системы (например, пластыри), эмульсии типа "молочко", пасты, пены, присыпки, имплантаты или стенты.
Предлагаемые в изобретении соединения можно переводить или перерабатывать в указанные выше лекарственные формы (формы применения). Для этого предлагаемые в изобретении соединения можно по известной технологии смешивать с инертными, нетоксичными, фармацевтически приемлемыми вспомогательными веществами. К таким вспомогательным веществам относятся, в частности, носители (например, микрокристаллическая целлюлоза, лактоза, маннит), растворители (например, жидкие полиэтиленгликоли), эмульгаторы и диспергаторы или смачиватели (например, додецилсульфат натрия, полиоксисорбитанолеат), связующие (например, поливинилпирролидон), синтетические и природные полимеры (например, альбумин), стабилизаторы (например, антиокислители, такие как аскорбиновая кислота), красители (например, неорганические пигменты, такие как оксиды железа) и улучшители вкуса и/или запаха.
Следующим объектом настоящего изобретения являются лекарственные средства, содержащие по меньшей мере одно предлагаемое в изобретении соединение, обычно совместно с одним или несколькими инертными, нетоксичными, фармацевтически приемлемыми вспомогательными веществами, а также применение таких лекарственных средств в вышеуказанных целях.
Для достижения требуемого эффекта предлагаемые в изобретении соединения предпочтительно применять в дозе, которая при внутривенном введении составляет примерно от 0,001 до 100 мг/кг веса тела, предпочтительно примерно от 0,1 до 10 мг/кг веса тела, а при пероральном введении составляет примерно от 0,01 до 50 мг/кг веса тела, предпочтительно от 0,5 до 10 мг/кг веса тела.
Тем не менее в некоторых случаях может потребоваться применять предлагаемые в изобретении соединения в дозах, отличающихся в ту или иную сторону от указанных выше количеств, а именно: в зависимости от веста тела, пути введения действующего вещества в организм, индивидуальной реакции на действующее вещество, типа лекарственной формы и момента времени, в который применяют действующее вещество, соответственно интервала времени, через который применяют действующее вещество. Так, в частности, в некоторых случаях вполне может оказаться достаточным применять предлагаемые в изобретении соединения в дозе, меньшей указанного выше минимального количества, тогда как в других случаях предлагаемые в изобретении соединения может потребоваться применять в дозе, превышающей вышеуказанный верхний предел. При применении предлагаемых в изобретении соединений в сравнительно высокой дозировке может оказаться целесообразным дробить суточную дозу на несколько более мелких разовых доз и распределить их прием на все сутки.
В приведенных ниже описаниях опытов, экспериментов и исследований и в примерах выраженные в процентах данные представляют собой, если не указано иное, массовые проценты (мас.%), а выраженные в частях данные представляют собой массовые части. Соотношения между растворителями, степень разбавления и данные о концентрации жидкостно-жидкостных растворов в каждом случае относятся к объему.
А. Примеры
Сокращения
| рассч. | рассчитано |
| BHI | среда с сердечно-мозговым экстрактом ("Brain Heart Infusion") |
| Воc | трет-бутилоксикарбонил |
| шир. | широкий сигнал (в ЯМР-спектрах) |
| d | дублет (в ЯМР-спектрах) |
| ГХ | газовая хроматография |
| DCI | прямая химическая ионизация ("Direct Chemical Ionization") (при МС) |
| ДМАП | 4-N,N-диметиламинопиридин |
| ДМСО | диметилсульфоксид |
| ДМФ | N,N-диметилформамид |
| ЭДК | 1-этил-3-(3-диметиламинопропил)карбодиимид (также ЭДКИ) |
| ЭДК×НСl | гидрохлорид 1-этил-3-(3-диметиламинопропил)карбодиимида |
| EI | ионизация электронным ударом ("Electron Impact Ionization") (при МС) |
| ESI | ионизация электроспреем ("Electrospray Ionization") (при МС) |
| ESIneg | регистрация в режиме определения отрицательно заряженных ионов (анионов) при масс-спектроскопии с ESI-ионизацией |
| ESIpos | регистрация в режиме определения положительно заряженных ионов (анионов) при масс-спектроскопии с ESI-ионизацией |
| обнаруж. | обнаружено |
| ч | час(ы) |
| ГАТУ | гексафторфосфат O-(7-азабензотриазол-1-ил)-N,N,N',N'-тетраметилурония |
| ЖХВД | жидкостная хроматография высокого давления или высокого разрешения |
| ВР | высокое разрешение |
| ЖХ-МС | масс-спектроскопия в сочетании с жидкостной хроматографией |
| m | средний ("middle") (в УФ- и ИК-спектрах) |
| m | мультиплет (в ЯМР-спектрах) |
| MALDI | матричная лазерная десорбционная ионизация ("Matrix-Assisted Laser Desorption/Ionization") |
| МИК | минимальная ингибирующая концентрация |
| мин | минута(ы) |
| MRSA | устойчивый к метициллину штамм Staphylococcus aureus |
| МС | масс-спектроскопия |
| NCCLS | Национальный комитет по клиническим и лабораторным стандартам (США) ("National Committee for Clinical Laboratoy Standards") |
| ЯМР | ядерный магнитный резонанс |
| а.ч. | аналитически чистый |
| Pd | палладий |
| Pd-C | палладий на угле |
| количеств. | количественный выход |
| ОФ-ЖХВД | ЖХВД с обращенной фазой |
| КT | комнатная температура |
| Rt | время удерживания (при ЖХВД) |
| s | сильный ("strong") (в УФ- и ИК-спектрах) |
| s | синглет (в ЯМР-спектрах) |
| ТФУК | трифторуксусная кислота |
| ТГФ | тетрагидрофуран |
| ВП | время пролета (времяпролетная МС) |
| УФ | ультрафиолетовое излучение |
| видим. | видимое излучение |
| VRSA | устойчивый к ванкомицину штамм Stapylococcus aureus |
| w | слабый ("weak") (в УФ- и ИК-спектрах) |
| Z, Cbz | бензилоксикарбонил |
Литература
Названия пептидов и циклодепсипептидов даны в соответствии со следующей номенклатурой:
1. A Guide to IUPAC Nomenclature of Organic Compounds (Recommendations 1993), изд-во Blackwell Scientific publications, 1993;
2. Nomenclature and symbolism for amino acids and peptides. Recommendations 1983. IUPAC-IUB Joint Commission on Biochemical Nomenclature, UK. Biochemical Journal, 219, 1984, с. 345-373, включая цитируемую литературу.
Общие методы ГХ-МС, ЖХ-МС МС-ВР, ЖХВД и гель-хроматографии
Метод 1 (ВП-МС-ВР): BП-MC-BP(ESI+)-спектры регистрируют с помощью прибора Micromass LCT (напряжение на капилляре 3,2 кВ, напряжение на конусе 42 В, температура источника 120°С, температура десольвации 280°С). Для подачи образцов используют шприц-насос (фирма Harvard Apparatus). Стандартом служит лейцин-энкефалин (Tyr-Gly-Gly-Phe-Leu).
Метод 2 (препаративная ЖХВД): Прибор: Gilson Abimed HPLC; УФ-детектор на 210 нм; система из двух насосов; колонка: Waters SymmetryPrepTM C18, 7 мкм, 300×19 мм; элюент А: 0,2% трифторуксусной кислоты в воде, элюент Б: ацетонитрил; скорость потока 25 мл/мин; температура колонки: КТ; 0-я минута 20% элюента Б, увеличение концентрации элюента Б с 0-й по 10-ю до 70%, уменьшение концентрации элюента Б с 10-й по 10,1-ю минуту до 20%, по 15-ю минуту 20% элюента Б.
Метод 3 (гель-хроматография на сорбенте Sephadex LH-20): Гель-хроматографию проводят без давления на сорбенте Sephadex LH-20 (фирма Pharmacia). После регистрации УФ-активности (УФ-детектор на 254 нм, фирма Knauer) фракционируют (коллектор фракций ISCO Foxy 200). Размеры колонки: 32×7 см (для интервала концентраций 1000-100 мкмолей), 30×4 см (для интервала концентраций 100-10 мкмолей) и 25×2 см (для интервала концентраций 10-1 мкмоль). Для интервала концентраций от 1 до 11 ммолей используют колонку размером 80×30 см. В этом случае фракции собирают вручную без использования предвключенного УФ-детектора. Соотнесение фракций осуществляют с помощью ЖХВД (метод 9).
Метод 4 (препаративная ЖХВД, сорбент Kromasil, уксусная кислота): Прибор: Gilson Abimed HPLC; УФ-детектор на 210 нм; система с двойным насосом; колонка: Kromasil-100A C18, 5 мкм, 250×20 мм; скорость потока 25 мл/мин; элюент А: вода/0,25-0,5% уксусной кислоты, элюент Б: ацетонитрил; градиент: с 0-й по 3-ю минуту 5% элюента Б, с 3-й по 30-ю минуту 5-100% элюента Б, с 30-й по 38-ю минуту 100% элюента Б, в завершение регенерация хроматографической колонки.
Метод 5 (ЖХ-МС): Прибор: Micromass Quattro LCZ в сочетании с HPLC Agilent Serie 1100; колонка: Phenomenex Synergi 2µ Hydro-RP Mercury, 20×4 мм; элюент А: 1 л воды+0,5 мл 50%-ной муравьиной кислоты, элюент Б: 1 л ацетонитрила+0,5 мл 50%-ной муравьиной кислоты; градиент: с 0,0-й минуты 90% элюента А → с 2,5-й минуты 30% элюента А → с 3,0-й минуты 5% элюента А → с 4,5-й минуты 5% элюента А; скорость потока: с 0,0-й минуты 1 мл/мин, с 2,5-й/с 3,0-й/с 4,5-й минуты 2 мл/мин; печь: 50°С; УФ-обнаружение на 208-400 нм.
Метод 6 (ЖХ-МС): Тип прибора для МС: Micromass ZQ; тип прибора для ЖХВД: Waters Alliance 2795; колонка: Phenomenex Synergi 2µ Hydro-RP Mercury, 20×4 мм; элюент А: 1 л воды +0,5 мл 50%-ной муравьиной кислоты, элюент Б: 1 л ацетонитрила +0,5 мл 50%-ной муравьиной кислоты; градиент: с 0,0-й минуты 90% элюента А → с 2,5-й минуты 30% элюента А → с 3,0-й минуты 5% элюента А → с 4,5-й минуты 5% элюента А; скорость потока: с 0,0-й минуты 1 мл/мин, с 2,5-й/с 3,0-й/с 4,5-й минуты 2 мл/мин; печь: 50°С; УФ-обнаружение на 210 нм.
Метод 7 (ЖХ-МС): Тип прибора для МС: Micromass ZQ; тип прибора для ЖХВД: HP 1100 Series; УФ-детектор с диодной матрицей (УФ-ДДМ); колонка: Phenomenex Synergi 2µ, Hydro-RP Mercury, 20×4 мм; элюент А: 1 л воды +0,5 мл 50%-ной муравьиной кислоты, элюент Б: 1 л ацетонитрила +0,5 мл 50%-ной муравьиной кислоты; градиент: с 0,0-й минуты 90% элюента А → с 2,5-й минуты 30% элюента А → с 3,0-й минуты 5% элюента А → с 4,5-й минуты 5% элюента А; скорость потока: с 0,0-й минуты 1 мл/мин, с 2,5-й/с 3,0-й/с 4,5-й минуты 2 мл/мин; печь: 50°С; УФ-обнаружение на 210 нм.
Метод 8 (аналитическая ЖХВД): Тип прибора для ЖХВД: HP 1050 Series; УФ-ДДМ: UV DAD 1100 Series; колонка: Kromasil C18, 60×2 мм, 3,5 мкм; элюент А: вода/0,5% перхлорной кислоты, элюент Б: ацетонитрил; градиент: с 0-й по 0,5-ю минуту 2% элюента Б, с 0,5-й по 4,5-ю минуту с 2 до 90% элюента Б, с 4,5-й по 9,0-ю минуту 90% элюента Б, с 9,0-й по 9,2-ю минуту с 90 до 2% элюента Б, с 9,2-й по 10,0-ю минуту 2% элюента Б; скорость потока: 0,75 мл/мин, печь: 30°С, УФ-обнаружение на 210 нм.
Метод 9 (аналитическая ЖХВД, сорбент Agilent Zorbax Cg): Прибор: Agilent 1100 в сочетании с ДДМ (G 1315 В), сдвоенный насос (G1312A), автоматический пробоотборник (G 1313 А), дегазатор растворителя (G1379A) и термостат хроматографической колонки (G1316A); колонка: Agilent Zorbax Eclipse XDB-C8, 4,6×150×5 мм; элюент А: 0,05% 70%-ной перхлорной кислоты в воде; элюент Б: ацетонитрил; градиент: с 0-й по 1-ю минуту 10% элюента Б, увеличение концентрации элюента Б, с 4-й по 5-ю минуту 90% элюента Б, уменьшение концентрации элюента Б, по 5,5-ю минуту 10% элюента Б; скорость потока: 2,00 мл/мин; температура колонки: 30°С.
Метод 10 (гель-хроматография на сорбенте Sephadex LH-20): Гель-хроматографию проводят без давления на сорбенте Sephadex LH-20 (фирма Pharmacia). После регистрации УФ-активности (УФ-детектор на 254 нм, фирма Knauer) фракционируют (коллектор фракций ISCO Foxy 200). Размеры колонки: 32×7 см (для интервала концентраций 1000-100 мкмолей), 30×4 см (для интервала концентраций 100-10 мкмолей) и 25×2 см (для интервала концентраций 10-1 мкмоль).
Метод 11 (препаративная ЖХВД, сорбент Symmetry): Прибор: Gilson Abimed HPLC; система с двойным насосом; колонка: SymmetryPrepTM C18, фирма Waters, 7 мкм, 300×19 мм; элюент А: вода/0,2% трифторуксусной кислоты, элюент Б: ацетонитрил; градиент: с 0-й по 10-ю минуту увеличение концентрации элюента Б с 15 до 65%, в завершение регенерация хроматографической колонки; скорость потока: 25 мл/мин; УФ-обнаружение на 210 нм.
Метод 12 (препаративная ЖХВД, сорбент Kromasil): Прибор: Gilson Abimed HPLC; система с двойным насосом; колонка: Kromasil C18, 5 мкм, 100 Å, 250×20 мм; элюент А: 0,05% трифторуксусной кислоты в воде, элюент Б: 0,05% трифторуксусной кислоты в ацетонитриле; градиент: с 0-й по 3-ю минуту 10% элюента Б, увеличение концентрации элюента Б, с 30-й по 38-ю минуту 90% элюента Б, с 38-й по 45-ю минуту 10% элюента Б; скорость потока: 20 мл/мин; УФ-обнаружение на 210 нм.
Метод 13 (препаративная ЖХВД, сорбент Waters Symmetry): Прибор: Gilson Abimed HPLC; система с двойным насосом; колонка: Waters SymmetryPrepТМ C18, 7 мкм, 300×19 мм; элюент А: 0,05% трифторуксусной кислоты в воде, элюент Б: 0,05% трифторуксусной кислоты в ацетонитриле; градиент: с 0-й по 3-ю минуту 10% элюента Б, увеличение концентрации элюента Б, с 30-й по 38-ю минуту 90% элюента Б, с 38-й по 45-ю минуту 10% элюента Б; скорость потока: 20 мл/мин; УФ-обнаружение на 210 нм.
Метод 14 (препаративная ЖХВД): Прибор: Gilson Abimed HPLC; система с двойным насосом; колонка: Waters SymmetryPrepTM C18, 7 мкм, 300×19 мм; элюент А: вода/0,2% трифторуксусной кислоты, элюент Б: ацетонитрил; градиент: с 0-й по 10-ю минуту увеличение концентрации элюента Б с 25 до 65%, в завершение регенерация хроматографической колонки; скорость потока: 25 мл/мин; УФ-обнаружение на 210 нм.
Метод 15 (хиральная ЖХВД, сорбент Daicel Chiralpak): Прибор: Agilent 1100 HPLC; колонка: Daicel Chiralpak AD-H, 5 мкм, 250×20 мм; изократически: 75% изогексана, 25% 2-пропанола с 0,2% трифторуксусной кислоты и 1% воды; скорость потока: 1,0 мл/мин; печь: 25°С; УФ-детектор на 212 нм.
Метод 16 (препаративная ЖХВД): Прибор: Gilson Abimed HPLC; система с двойным насосом; колонка: YMC ODS-AQ, 5 мкм, 250×30 мм; элюент А: 0,05% трифторуксусной кислоты в воде, элюент Б: 0,05% трифторуксусной кислоты в ацетонитриле; градиент: с 0-й по 3-ю минуту 10% элюента Б, увеличение концентрации элюента Б, с 30-й по 38-ю минуту 90% элюента Б, с 38-й по 45-ю минуту 10% элюен