Тиенопиридины
Иллюстрации
Показать всеИзобретение относится к конкретным производным тиенопиридина и к их фармацевтически пригодным солям, которые указаны в пункте 1 формулы. Изобретение также относится к лекарственным средствам на основе указанных соединений, являющихся ингибиторами HSP90. Технический результат - получены новые соединения и лекарственные средства на их основе, которые могут применяться для лечения заболеваний, на которые влияет ингибирование, регуляция и/или модуляция HSP90. 3 н.п. ф-лы, 1 табл.
Реферат
Предпосылки создания изобретения
Объектом изобретения является выявление новых соединений, обладающих ценными свойствами, в особенности тех, которые могут применяться для получения лекарственных средств.
Настоящее изобретение относится к соединениям, которые принимают участие в ингибировании, регуляции и/или модуляции HSP90, кроме того, к фармацевтическим композициям, которые содержат эти соединения, и к применению соединений для лечения заболеваний, в которых задействованы HSP90.
Правильная укладка и конформация белков в клетках обеспечивается молекулярными шаперонами и является чрезвычайно важной для регуляции равновесия между синтезом и распадом белков. Шапероны являются важными для регуляции многих главных функций в клетках, таких как, например, пролиферация клеток и апоптоз (Jolly и Morimoto, 2000; Smith и др., 1998; Smith, 2001).
Белки теплового шока (HSP)
Клетки в ткани реагируют на внешние стрессы, такие как, например, нагревание, гипоксия, окислительный стресс или токсические вещества, такие как тяжелые металлы или спирты, путем активации многих шаперонов, которые известны под термином "белки теплового шока" (HSP).
Активация белков HSP в клетках при повреждении, инициируемая такими стрессовыми факторами, ускоряет восстановление физиологического состояния и приводит к стресс-толерантному состоянию в клетке. Дополнительно к первоначально открытому защитному механизму по отношению к внешнему стрессу, опосредуемому HSP, в дальнейшем также были описаны другие важные функции шаперонов для конкретных HSP в нормальных условиях без стресса. Таким образом, различные HSP регулируют, например, правильную укладку, внутриклеточную локализацию и функцию или регулируемый распад многих биологически важных белков в клетках.
HSP образуют семейство генов с отдельными генными продуктами, с помощью которых различается клеточная экспрессия, функция и локализация в различных клетках. Наименование и классификация в пределах этого семейства основывается на их молекулярном весе, например HSP27, HSP70 и HSP90.
Причиной некоторых заболеваний человека является неправильная укладка белков (см. обзор, например, Tytell и др., 2001; Smith и др., 1998). Следовательно, в таких случаях будет являться пригодным развитие терапевтических подходов, основывающихся на механизме шаперон-зависимой укладки белков. Например, некорректная укладка белков приводит к агрегации белков с нейродегенеративной прогрессией в случае болезни Альцгеймера, прионных заболеваний или синдрома Хантингтона. Неправильная укладка белков также может приводить к потере функции дикого типа, вследствие чего может происходить неправильная регуляции молекулярной и физиологической функции.
HSP также приписывают важное значение в опухолевых заболеваниях. Получены данные, указывающие на то, что, например, экспрессия определенных HSP коррелирует со стадией прогрессии опухолей (Martin и др., 2000; Conroy и др., 1996; Kawanishi и др., 1999; Jameel и др., 1992; Hoang и др., 2000; Lebeau и др., 1991).
Тот факт, что HSP90 задействованы во многих центральных онкогенных путях передачи сигналов в клетках и определенные естественные продукты, обладающие противораковым действием, нацелены на HSP90, привел к появлению концепции, что ингибирование функционирования HSP90 должно быть целесообразным при лечении опухолевых заболеваний. В настоящее время клиническое исследование проходит ингибитор HSP90, 17-аллиламино-17-деметоксигельданамицин (17AAG), производное гельданамицина.
HSP90
HSP90 составляет около 1-2% общей массы белков в клетке. Обычно он находится в виде димера в клетке и связан со многими белками, так называемыми ко-шаперонами (см., например, Pratt, 1997). HSP90 является чрезвычайно важным для жизнеспособности клеток (Young и др., 2001) и играет решающую роль в ответной реакции на клеточный стресс путем взаимодействия со многими белками, нативная укладка которых модифицирована вследствие внешнего стресса, такого как, например, тепловой шок, для восстановления исходной укладки или предотвращения агрегации белков (Smith и др., 1998).
Получены также данные, указывающие на то, что HSP90 является важным в качестве буфера против действия мутаций, предположительно, путем коррекции некорректной укладки белков, вызванной мутацией (Rutherford и Lindquist, 1998).
Дополнительно, HSP90 также является регуляторно важным. В физиологических условиях HSP90, вместе с его гомологом в эндоплазматическом ретикулуме GRP94, принимает участие в клеточном равновесии для обеспечения стабильности конформации и созревания различных взаимосвязанных с ними ключевых белков. Их можно разделить на три группы: рецепторы стероидных гормонов, Ser/Thr или тирозин киназы (например, ERBB2, RAF-1, CDK4 и LCK) и совокупность различных белков, таких как, например, мутированный р53 или каталитическая субъединица теломеразы hTPET. Каждый из этих белков является существенно важным для регуляции физиологических и биохимических процессов в клетках. Фиксированное семейство HSP90 у людей состоит из четырех генов, цитозольная HSP90α, индуцибельная изоформа HSP90β (Hickey и др., 1989), GRP94 в эндоплазматическом ретикулуме (Argon и др., 1999) и HSP75/TRAP1 в митохондриальном матриксе (Felts и др., 2000). Предполагают, что все представители этого семейства имеют сходный образ действия, однако, в зависимости от их локализации в клетке, связываются с различными взаимосвязанными с ними белками. Например, ERBB2 является специфическим взаимосвязанным белком для GRP94 (Argon и др., 1999), в то время как обнаружено, что рецептор 1 типа фактора некроза опухоли (TNFR1) или белок ретинобластомы (Rb) являются взаимосвязанными с TRAP1 (Song и др., 1995; Сhen и др., 1996).
HSP90 вовлечен в различные комплексные взаимодействия с большим количеством взаимосвязанных с ним белков и регуляторных белков (Smith, 2001). Несмотря на то, что точные молекулярные данные до сих пор еще не установлены, с помощью биохимических опытов и исследования путем кристаллографического анализа с помощью рентгеновских лучей в последние годы повысили возможность расшифровки деталей функционирования шаперонов HSP90 (Prodromou и др., 1997; Stebbins и др., 1997). Следовательно, HSP90 представляет собой АТФ-зависимый молекулярный шаперон (Prodromou и др, 1997), с димеризацией, которая является важной для гидролиза АТФ. Связывание АТФ приводит к образованию тороидальной димерной структуры, в которой два N-концевых домена вступают в тесный контакт друг с другом и действуют в качестве переключателя конформации (Prodromou и Pearl, 2000).
Известные ингибиторы HSP90
Первым открытым классом ингибиторов HSP90 были бензохиноновые анзамицины с соединениями гербимицина А и гельданамицина. Первоначально для них была идентифицирована реверсия злокачественного фенотипа в фибробластах, которая индуцируется трансформацией с v-Src онкогеном (Uehara и др., 1985).
Позже было показано сильное противоопухолевое действие в условиях in vitro (Schulte и др., 1998) и на животных моделях в условиях in vivo (Supko и др., 1995).
Затем при проведении иммунной преципитации и исследований на аффинных матрицах было показано, что в основной механизм действия гельданамицина задействовано связывание с HSP90 (Whitesell и др., 1994; Schulte и Neckers, 1998). Дополнительно при проведении кристаллографического анализа с помощью рентгеновских лучей было показано, что гельданамицин конкурирует за АТФ-связывающий сайт и ингибирует внутреннюю АТФ-азную активность HSP90 (Prodromou и др., 1997; Panaretou и др., 1998). Это предотвращает образование мультимерного HSP90 комплекса, который функционирует в качестве шаперона для взаимосвязанных с ним белков. Вследствие этого взаимосвязанные с ним белки распадаются путем убиквитин-протеасомного механизма.
Производное гельданамицина, 17-аллиламино-17-деметоксигельданамицин (17AAG), проявляет неизмененные свойства при ингибировании HSP90, деградации взаимосвязанных с ним белков и противоопухолевой активностью в клеточных культурах и на моделях ксенотрансплантированных опухолей у мышей (Schulte и др. 1998; Kelland и др. 1999), но обладает значительно сниженной цитотоксичностью на печень по сравнению с гельданамицином (Page и др., 1997). В настоящее время 17AAG проходит фазу 1/11 клинических исследований.
Радикикол, макроциклический антибиотик, также вызывает ревизию v-Src и v-Ha-Ras-индуцированного злокачественного фенотипа фибробластов (Kwon и др., 1992; Zhao и др., 1995). Радикикол разрушает большое количество сигнальных белков в результате ингибирования HSP90 (Schulte и др., 1998). С помощью кристаллографического анализа с помощью рентгеновских лучей было показано, что радикикол также связывается с N-концевым доменом HSP90 и ингибирует внутреннюю АТФ-азную активность (Roe и др., 1998).
Как известно, антибиотики кумаринового типа связываются с АТФ-связывающимся сайтом HSP90 гомолога ДНК-гиразы у бактерий. Кумарин, новобиоцин, связывается с карбокситерминальным концом HSP90, то есть с другим сайтом в HSP90, чем бензохинон-анзамицины и радикикол, которые связываются с N-терминальным концом HSP90 (Marcu и др., 2000b).
Ингибирование HSP90 новобиоцином приводит к распаду большого количества Н8Р90-зависимых сигнальных белков (Marcu и др., 2000а).
Распад сигнальных белков, например ERBB2, показан с применением PU3, ингибитора HSP90, который является производным пуринов. PU3 вызывает остановку клеточного цикла и дифференциацию клеточных линий рака молочной железы (Chiosis и др., 2001).
HSP90 в качестве терапевтической цели
Вследствие участия HSP90 в регуляции большого количества путей передачи сигналов, которые являются чрезвычайно важными для фенотипа опухоли, и открытия, что определенные природные продукты проявляют их биологическое действие путем ингибирования активности HSP90, HSP90 в настоящее время исследуется в качестве новой цели для развития противоопухолевого терапевтического средства (Neckers и др., 1999).
Основным механизмом действия гельданамицина, 17AAG и радикикола является ингибирование связывание АТФ с АТФ-связывающим сайтом в N-терминальном конце белка и результирующие ингибирование внутренней АТФ-азной активности HSP90 (см., например, Prodromou и др., 1997; Stebbins и др., 1997; Panaretou и др., 1998). Ингибирование АТФ-азной активности HSP90 предотвращает пополнение ко-шаперонами и способствует образованию HSP90 гетерокомплекса, который вызывает распад взаимосвязанных с ним белков с помощью убиквитин-протеасомного механизма (см., например, Neckers и др., 1999; Kelland и др., 1999). Лечение опухолевых клеток с помощью ингибиторов HSP90 приводит к селективному распаду важных белков, обладающих чрезвычайной значимостью при таких процессах, как пролиферация клеток, регуляция клеточного цикла и апоптоз. Это зачастую проявляется нарушением регуляции в опухолях (см., например, Hostein и др., 2001).
Благоприятным логическим обоснованием развития ингибитора HSP90 является тот факт, что можно достичь эффективного противоопухолевого действия путем одновременного распада множества белков, которые связаны с трансформированным фенотипом.
Более подробно, настоящее изобретение относится к соединениям, которые ингибируют, регулируют и/или модулируют HSP90, к композициям, которые содержат эти соединения, и к способам их применения для лечения HSP90-индуцированных заболеваний, таких как опухолевые заболевания, вирусные заболевания, такие как, например, гепатит В (Waxman, 2002); иммуносупрессия в трансплантантах (Bijlmakers, 2000. и Yorgin, 2000); заболевания, индуцированные воспалением (Bucci, 2000), такие как ревматоидний артрит, астма, рассеянный склероз, диабет I типа, красная волчанка, псориаз и воспалительное заболевание кишечника; фиброзно-кистозная дегенерация (Fuller, 2000); заболевания, связанные с ангиогенезом (Hur, 2002, и Kurebayashi, 2001), такие как, например, диабетическая ретинопатия, гемангиома, эндометриоз и опухолевый ангиогенез; инфекционные заболевания; аутоиммунные заболевания; ишемия; стимуляция регенерации нервов (Rosen и др., WO 02/09696; Degranco и др., WO 99/51223; Gold, US 6210974 Bl); фиброгенетические заболевания, такие как, например, склеродерма, болезнь Вагнера, системная волчанка, цирроз печени, келоидное образование, интерстициальный нефрит и фиброз легких (Strehlow, WO 02/02123).
Изобретение также относится к применению соединений в соответствии с изобретением для защиты нормальных клеток от токсичности, вызванной химиотерапией, и к применению при заболеваниях, основной причиной которых является неправильная укладка или агрегация белков, таких как, например, почесуха, болезнь Якоба-Крейтцфельдта, Хантингтона или Альцгеймера (Sittler, Hum. Mol. Genet., 10, 1307, 2001; Tratzelt и др., Рrос.Nat. Acad. Sci., 92, 2944, 1995; Winklhofer и др., J. Biol. Chem., 276, 45160, 2001). В заявке WO 01/72779 описаны пуриновые соединения и их применение для лечения GRP94 (гомолога или паралога НSР90)-индуцированных заболеваний, таких как опухолевые заболевания, где злокачественная ткань включает саркому или карциному, выбранную из группы, включающей фибросаркому, злокачественную миксому, липосаркому, хондросаркому, остеогенную саркому, хордому, ангиосаркому, эндотелиосаркому, лимфангиосаркому, лимфангиоэндотелиосаркому, синовиальную эндотелиому, мезотелиому, саркому Юинга, лейосаркому, рабдомиосаркому, рак ободочной кишки, рак поджелудочной железы, рак молочной железы, рак яичников, рак предстательной железы, плоскоклеточный рак, базально-клеточный рак, аденокарциному, рак протока потовой железы, рак клеток сальной железы, папиллярный рак, папиллярные аденокарциномы, цистаденокарциномы, рак костного мозга, бронхогенный рак, почечно-клеточный рак, печеночно-клеточную аденому, рак желчного протока, хориокарциному, сперматоцитому, эмбриональную карциному, опухоль Вильма, рак шейки матки, рак яичек, рак легких, мелкоклеточный рак легких, рак мочевого пузыря, эпителиальный рак, глиому, астроцитому, медуллобластому, краниофарингиому, эпендимому, пинеалому, гемангиобластому, невриному слухового нерва, олигодендроглиому, менингиому, меланому, нейробластому, ретинобластому, лейкоз, лимфому, множественную миелому, макроглобулинемию Вальденстрема и болезнь тяжелых цепей.
A.Kamal и др. в Trends in Molecular Medicine, том 10, №6, июнь 2004, описали терапевтические и диагностические применения активации HSP90, в частности, для лечения заболеваний центральной нервной системы и сердечно-сосудистых заболеваний.
Следовательно, является желательным идентифицировать небольшие соединения, которые специфически ингибируют, регулируют и/или модулируют HSP90, и это является задачей настоящего изобретения.
Было обнаружено, что соединения формулы I и их соли обладают чрезвычайно ценными фармакологическими свойствами, а также хорошей переносимостью. В частности, они обладают ингибирующими свойствами по отношению к HSP90.
Следовательно, настоящее изобретение относится к соединениям формулы I в качестве лекарственных средств и/или активных компонентов лекарственных средств для лечения и/или профилактики указанных заболеваний и к применению соединений формулы I для получения лекарственного средства для лечения и/или профилактики указанных заболеваний, а также к способу лечения указанных заболеваний, который включает введение одного или более соединений формулы I пациенту, который нуждается в таком введении.
Хозяин или пациент может принадлежать к любому виду млекопитающих, например, такому как, приматы, предпочтительно человек; грызуны, включая мышей, крыс и хомячков; кролики; лошади; коровы, собаки, коты и т.д. Животные модели представляют интерес для экспериментальных исследований, поскольку они обеспечивают модель для лечения заболевания человека.
Уровень техники
Другие производные пиридотиофена описаны в качестве ингибиторов HSP90 в WO 2005/034950 и в WO 2005/021552.
В заявке WO 2005/00300 А1 описаны производные триазола в качестве ингибиторов HSP90.
В заявке WO 00/53169 описано ингибирование HSP90 кумарином или производным кумарина.
В заявке WO 03/041643 А2 описаны производные зеараланола, которые ингибируют HSP90.
Производные пиразола, которые ингибируют HSP90, замещенные ароматическим радикалом в 3-м или 5-м положении, описаны в заявках WO 2004/050087 А1 и WO 2004/056782 А1.
В заявке WO 03/055860 А1 описаны 3,4-диарилпиразолы в качестве ингибиторов HSP90.
Производные пурина, обладающие ингибирующими свойствами по отношению к HSP90, описаны в заявке WO 02/36075 А2.
В заявке WO 01/72779 описаны пуриновые соединения и их применение для лечения GRP94 (гомолога или паралога HSP90)-индуцированных заболеваний, таких как опухолевые заболевания, где злокачественная ткань включает саркому или карциному, выбранную из группы, включающей фибросаркому, злокачественную миксому, липосаркому, хондросаркому, остеогенную саркому, хордому, ангиосаркому, эндотелиосаркому, лимфангиосаркому, лимфангиоэндотелиосаркому, синовиальную эндотелиому, мезотелиому, саркому Юинга, лейосаркому, рабдомиосаркому, рак ободочной кишки, рак поджелудочной железы, рак молочной железы, рак яичников, рак предстательной железы, плоскоклеточный рак, базально-клеточный рак, аденокарциному, рак протока потовой железы, рак клеток сальной железы, папиллярный рак, папиллярные аденокарциномы, цистаденокарциномы, рак костного мозга, бронхогенный рак, почечно-клеточный рак, печеночно-клеточную аденому, рак желчного протока, хориокарциному, сперматоцитому, эмбриональную карциному, опухоль Вильма, рак шейки матки, рак яичек, рак легких, мелкоклеточный рак легких, рак мочевого пузыря, эпителиальный рак, глиому, астроцитому, медуллобластому, краниофарингиому, эпендимому, пинеалому, гемангиобластому, невриному слухового нерва, олигодендроглиому, менингиому, меланому, нейробластому, ретинобластому, лейкоз, лимфому, множественную миелому, макроглобулинемию Вальденстрема и болезнь тяжелых цепей.
Кроме того, в WO 01/72779 описано применение указанных соединений для лечения вирусных заболеваний, где вирусный патоген выбран из группы, включающей гепатит типа А, гепатит типа В, гепатит типа С, грипп, ветряную оспу, аденовирус, вирус простого герпеса I типа (HSV-I), вирус простого герпеса II типа (HSV-II), чуму крупного рогатого скота, риновирус, эховирус, ротавирус, респираторно-синцитиальный вирус (RSV), папилломавирус, паповавирус, цитомегаловирус, эхиновирус, арбовирус, хунтавирус, коксаки-вирус, вирус паротита, вирус кори, вирус краснухи, вирус полиомиелита, вирус иммунодефицита человека I типа (HIV-I) и вирус иммунодефицита человека II типа (HIV-II).
Кроме того, в WO 01/72779 описано применение указанных соединений для модуляции GRP94, где модуляции биологической активности GRP94 вызывают иммунную реакцию у особи, транспортирование белка из эндоплазматического ретикулума, восстановление после гипоксического/аноксического стресса, восстановление после недостаточного питания, восстановление после теплового стресса или их комбинации, и/или где заболевание представляет собой тип злокачественного новообразования, инфекционное заболевание, расстройство, связанное с нарушенным транспортом белка из эндоплазматического ретикулума, расстройство, связанное с ишемией/реперфузией или их комбинации, где расстройство, связанное с ишемией/реперфузией, представляет собой последствие остановки сердца, асистолию и отсроченную аритмию желудочков, операцию на сердце, операцию сердечно-легочного шунтирования, пересадку органа, травму спинного мозга, травму головы, удар, тромбоэмболический удар, геморрагический удар, спазм сосудов головного мозга, гипотонию, гипогликемию, эпилептическое состояние, эпилептический припадок, тревогу, шизофрению, нейродегенеративное расстройство, болезнь Альцгеймера, болезнь Хантингтона, боковой амиотрофический склероз (ALS) или неонатальный стресс.
В завершение, в WO 01/72779 описано применение эффективного количества белкового модулятора GRP94 для приготовления лекарственного средства для изменения последующей клеточной реакции на ишемическое состояние в участке ткани особи путем обработки клеток в участке ткани белковым модулятором GRP94 для такого повышения активности GRP94 в клетках, чтобы изменялась последующая реакция клеток на ишемическое состояние, где последующее ишемическое состояние предпочтительно представляет собой последствие остановки сердца, асистолию и отсроченную аритмию желудочков, операцию на сердце, операцию сердечно-легочного шунтирования, пересадку органа, травму спинного мозга, травму головы, удар, тромбоэмболический удар, геморрагический удар, спазм сосудов головного мозга, гипотонию, гипогликемию, эпилептическое состояние, эпилептический припадок, тревогу, шизофрению, нейродегенеративное расстройство, болезнь Альцгеймера, болезнь Хантингтона, боковой амиотрофический склероз (ALS) или неонатальный стресс, или где участок ткани представляет собой донорскую ткань для трансплантации.
Сущность изобретения
Изобретение относится к соединениям формулы I
в которой Y представляет собой ОН, ОА, SH, SA, NH2, NHA, NAA′ или NHR5,
R1 представляет собой Hal, ОН, ОА, SH, SA, H или А,
R2, R3 каждый, независимо друг от друга, представляет собой -NHCO-(X)s-Q, -CONH-(X)s-Q, -CONA-(X)s-Q, -NH(CO)NH-(X)s-Q, -NH(CO)O-(X)s-Q, - NHSO2-(X)s-Q, -SO2NH-(X)s-Q, -SO2NA-(X)s-Q, -(X)s-Q или H, где,
если R2≠H, то R3=H или Cl,
или если R3≠H, то R2=H или Cl,
R4 представляет собой Н, Hal, CN, NO2, А, ОН, ОА, SH, SA, (СН2)nCOOH, (CH2)nCOOA, CONH2, CONHA, CONAA′, NH2, NHA, NAA′, NHCOOA, NHCONH2, NHCONHA, SOA, SO2A, SO2NH2, SO2NHA и/или SO2NAA′,
два смежных радикала, выбранных из группы R1, R2, R3, R4,
вместе также представляют собой метилендиокси или этилендиокси,
R5 представляет собой -(CH2)0-Het1, -(CH2)o-NH2, -(CH2)o-NHA или -(CH2)o-NA2,
А, А′ каждый, независимо друг от друга, представляет собой неразветвленный или разветвленный алкил, содержащий 1-10 атомов углерода, в котором 1-5 атомов водорода могут быть заменены F, Cl и/или Br,
Alk или циклический алкил, содержащий 3-7 атомов углерода, А и А′ вместе также представляют собой алкиленовую цепь, содержащую 2, 3, 4, 5 или 6 атомов углерода, в которой одна или две СН2-группы могут быть заменены О, S, SO, SO2, NH, NA и/или N-СООА,
Alk представляет собой алкенил, содержащий 2-6 атомов углерода,
Х представляет собой неразветвленный или разветвленный С1-С10 алкилен или С2-С10 алкенилен, каждый из которых незамещен или одно-, дву-, три- или тетразамещен А, ОА, ОН, SH, SA, Hal, NO2, CN, Ar, OAr, COOH, COOA, CHO, C(=O)A, C(=O)Ar, SO2A, CONH2, SO2NH2, CONHA, CONAA′, SO2NHA, SO2NAA′, NH2, NHA, NAA′, OCONH2, OCONHA, OCONAA′, NHCOA, NHCOOA, NACOOA, NHSO2OA, NASO2OA, NHCONH2, NACONH2, NHCONHA, NACONHA, NHCONAA′, NACONAA′ и/или =O и в котором одна, две или три группы С могут быть заменены О, S, SO, SO2, NHCO, NACO, CONH, CONA, SO2NH, SO2NA, NHSO2, NASO2 и/или NH группами,
Q представляет собой Н, Carb, Ar или Het,
Carb представляет собой циклоалкил, содержащий 3-7 атомов углерода, или циклоалкенил, содержащий 3-7 атомов углерода, каждый из которых незамещен или одно-, дву-, три-, тетра- или пентазамещен А, ОА, ОН, SH, SA, Hal, NO2, CN, (CH2)nAr′, (СН2)nCOOH, (СН2)nCOOA, CHO, СОА, SO2A, CONH2, SO2NH2, CONHA, CONAA′, SO2NHA, SO2NAA′, NH2, NHA, NAA′, OCONH2, OCONHA, OCONAA′, NHCOA, NHCOOA, NACOOA, NHSO2OA, NASO2OA, NHCONH2, NACONH2, NHCONHA, NACONHA, NHCONAA′ и/или NACONAA′,
Ar представляет собой фенил, нафтил или бифенил, каждый из которых незамещен или одно-, дву-, три-, тетра- или пентазамещен А, ОА, ОН, SH, SA, Hal, NO2, CN, (CH2)nAr′, (CH2)nCOOH, (CH2)nCOOA, СНО, СОА, SO2A, CONH2, SO2NH2, CONHA, CONAA′, SO2NHA, SO2NAA′, NH2, NHA, NAA1, OCONH2, OCONHA, OCONAA′, NHCOA, NHCOOA, NACOOA, NHSO2OA, NASO2OA, NHCONH2, NACONH2, NHCONHA, NACONHA, NHCONAA′, NACONAA′, NHCO(CH2)nNH2 и/или -O-(CH2)o-Het1,
Ar′ представляет собой фенил, нафтил или бифенил, каждый из которых незамещен или одно-, дву- или тризамещен А, ОА, ОН, SH, SA, Hal, NO2, CN, (СН2)nфенилом, (СН2)nCOOH, (СН2)nCOOA, СНО, СОА, SO2A, CONH2, SO2NH2, CONHA, CONAA′, SO2NHA, SO2NAA′, NH2, NHA, NAA′, OCONH2, OCONHA, OCONAA′, NHCOA, NHCOOA, NACOOA, NHSO2OA, NASO2OA, NHCONH2, NACONH2, NHCONHA, NACONHA, NHCONAA′ и/или NACONAA′,
Het представляет собой моно- или бициклический насыщенный, ненасыщенный или ароматический гетероцикл, содержащий от 1 до 4 атомов N, О и/или S, который может быть одно-, дву- или тризамещен А, ОА, ОН, SH, SA, Hal, NO2, CN, (CH2)nAr′, (CH2)nCOOH, (СН2)nCOOA, СНО, СОА, SO2A, CONH2, SO2NH2, CONHA, CONAA′, SO2NHA, SO2NAA′, NH2. NHA, NAA′, OCONH2, OCONHA, OCONAA′, NHCOA, NHCOOA, NACOOA, NHSO2OA, NASO2OA, NHCONH2, NACONH2, NHCONHA, NACONHA, NHCONAA′, NACONAA′, SO2A, =S, =NH, =NA и/или =O (карбонильным кислородом),
Het1 представляет собой моноциклический насыщенный гетероцикл, содержащий от 1 до 2 атомов N и/или О, который может быть одно- или двузамещен А, ОА, ОН, Hal и/или =O (карбонильным кислородом),
Hal представляет собой F, Cl, Br или I,
n представляет собой 0, 1, 2, 3 или 4,
о представляет собой 1, 2, 3 или 4,
s представляет собой 0 или 1,
и к их фармацевтически пригодным производным, солям, сольватам, таутомерам и стереоизомерам, включая их смеси во всех соотношениях.
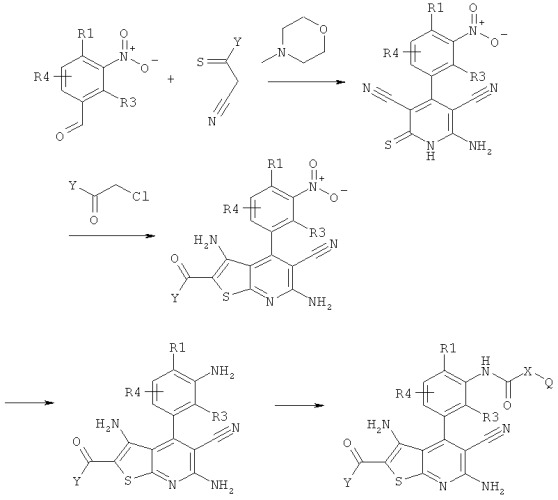
Изобретение также относится к соединениям формулы I и их солям и к способу получения соединений формулы I в соответствии с пунктами 1-14 и их фармацевтически пригодных производных, сольватов, солей, таутомеров и стереоизомеров, который характеризуется тем, что
а) соединение формулы II
в которой R1, R2 и R3 имеют значения, указанные в пункте 1,
подвергают реакции с соединением формулы III
в которой Y имеет значение, указанное в пункте 1, и
Z представляет собой Cl, Br, I или свободную или реакционноспособную функционально модифицированную ОН-группу,
или
б) в котором один или несколько радикалов R1, R2, R3, R4 и/или Y в соединении формулы I превращают в один или несколько радикалов R1, R2, R3, R4 и/или Y, например, путем
i) восстановления нитрогруппы до аминогруппы,
ii) гидролиза сложноэфирной группы до карбоксильной группы,
iii) превращения аминогруппы в алкилированный амин путем восстановительного аминирования,
iv) алкилирования и/или ацилирования гидроксильной и/или аминогруппы
и/или основание или кислоту формулы I превращают в одну из его солей.
Изобретение также относится к гидратам и сольватам этих соединений. Под сольватами соединений подразумевают аддукты молекул инертного растворителя на соединениях, которые образуются благодаря их силе взаимного притяжения. Сольваты представляют собой, например, моно- или дигидраты или алкоголяты.
Соединения формулы I в соответствии с изобретением также могут существовать в таутомерных формах. Формула I охватывает все такие таутомерные формы.
Под фармацевтически пригодными производными подразумевают, например, соли соединений в соответствии с изобретением, а также так называемые пролекарства соединений.
Под производными пролекарств подразумевают соединения формулы I, которые являются модифицированными алкильной или ацильной группами, сахарами или олигопептидами и которые быстро расщепляются в организме с образованием активных соединений в соответствии с изобретением.
Это понятие также включает производные биоразлагаемых полимеров соединений в соответствии с изобретением, как описано, например, в Int. J. Pharm. 115, 61-67 (1995).
Выражение "эффективное количество" обозначает количество лекарственного средства или фармацевтического активного компонента, которое вызывает биологическую или медицинскую ответную реакцию, которую предполагает или стремится получить, например, исследователь или лечащий врач в ткани, системе, животном или человеке.
Дополнительно выражение "терапевтически эффективное количество" обозначает то количество, которое имеет следующие последствия по сравнению с соответствующим субъектом, который не получал этого количества:
улучшение лечения, излечение, предотвращение или элиминацию заболевания, картины заболевания, болезненного состояния, жалобы, расстройства или побочных действий, или также уменьшение прогрессирования заболевания, жалобы или расстройства.
Выражение "терапевтически эффективное количество" также охватывает количества, которые эффективны для повышения нормальной физиологической функции.
Изобретение также относится к смесям соединений формулы I в соответствии с изобретением, например к смесям двух диастереомеров, например, в соотношении
1:1, 1:2, 1:3, 1:4, 1:5, 1:10, 1:100 или 1:1000. Особенно предпочтительными являются смеси стереоизомерных соединений.
Для всех радикалов, которые встречаются более одного раза, их значения являются независимыми друг от друга.
При упоминании выше и ниже, радикалы и параметры R1, R2, R3, R4 и Y имеют значения, указанные для формулы I, если специально не указано иначе.
А или А′ предпочтительно представляет собой алкил, который является неразветвленным (линейным) или разветвленным и имеет 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 атомов углерода. А или А′ более предпочтительно представляет собой метил, этил, пропил, изопропил, бутил, изобутил, втор-бутил или трет-бутил, кроме того, также пентил, 1-, 2- или 3-метилбутил, 1,1-, 1,2- или 2,2-диметилпропил, 1-этилпропил, гексил, 1-, 2-, 3- или 4-метилпентил, 1,1-, 1,2-, 1,3-, 2,2-, 2,3- или 3,3-диметилбутил, 1- или 2-этилбутил, 1-этил-1-метилпропил, 1-этил-2-метилпропил, 1,1,2- или 1,2,2-триметилпропил. А или А′ наиболее предпочтительно представляет собой алкил, содержащий 1, 2, 3, 4, 5 или 6 атомов углерода, предпочтительно этил, пропил, изопропил, бутил, изобутил, втор-бутил, трет-бутил, пентил, гексил, трифторметил, пентафторэтил или 1,1,1-трифторэтил, кроме того, также фторметил, дифторметил или бромметил.
А или А′ также представляет собой циклоалкил. Циклоалкил предпочтительно представляет собой циклопропил, циклобутил, циклопентил, циклогексил или циклогептил.
А или А′ также представляет собой Alk. Alk представляет собой алкенил, содержащий 2-6 атомов углерода, такой как, например, винил или пропенил.
Циклоалкилалкилен представляет собой, например, циклогексилметил, циклогексилэтил, циклопентилметил или циклопентилэтил.
С1-С10 алкилен предпочтительно представляет собой метилен, этилен, пропилен, бутилен, пентилен, гексилен, гептилен, октилен, нонилен или децилен, изопропилен, изобутилен, втор-бутилен, 1-, 2- или 3-метилбутилен, 1,1-, 1,2- или 2,2-диметилпропилен, 1-этилпропилен, 1-, 2-, 3- или 4-метилпентилен, 1,1-, 1,2-, 1,3-, 2,2-, 2,3- или 3,3-диметилбутилен, 1- или 2-этилбутилен, 1-этил-1-метилпропилен, 1-этил-2-метилпропилен, 1,1,2- или 1,2,2-триметилпропилен, более предпочтительно метилен, этилен, пропилен, бутилен, пентилен или гексилен.
Алкенилен представляет собой углеводородную цепь, содержащую 2-10 атомов углерода, имеющую 2 две свободные валентности и содержащую по меньшей мере одну двойную связь.
Ас представляет собой ацетил, Bzl представляет собой бензил, Ms представляет собой -SO2CH3.
Y предпочтительно представляет собой амино; NHA предпочтительно метиламино; NAA′ предпочтительно диметиламино или диэтиламино; NHR5 предпочтительно -NH-(CH2)o-NA2, такой как, например, 2-диметиламиноэтиламино, или -NH-(CH2)o-Het1, такой как, например, 2-(морфолин-4-ил)этиламино.
Y более предпочтительно представляет собой NH2.
R1 предпочтительно представляет собой Н, ОН или ОА, такой как, например, метокси.
R2, R3 предпочтительно каждый, независимо друг от друга, представляет собой -NHCO-(X)s-Q, -CONH-(X)s-Q, -NH(CO)NH-(X)s-Q, -NH(CO)O-(X)s-Q, -(X)s-Q или Н, где,
если R2≠Н, то R3=Н или Cl, или
если R3≠H, то R2=H или Cl.
R4 предпочтительно представляет собой H или Hal, более предпочтительно Н.
X предпочтительно представляет собой неразветвленный или разветвленный С1-С10 алкилен, который незамещен или одно-, дву-, три- или тетразамещен ОА, ОН, Hal, COOH, CONH2, NH2 и/или NHCOOA и в котором одна, две или три группы С могут быть заменены О, NHCO, CONH, SO2NH, NHSO2 и/или NH-группами.
Ar представляет собой, например, фенил, о-, м- или п-толил, о-, м- или п-этилфенил, о-, м- или п-пропилфенил, о-, м- или п-изопропилфенил, о-, м- или п-трет-бутилфенил, о-, м- или п-гидроксифенил, о-, м- или п-нитрофенил, о-, м- или п-аминофенил, о-, м- или п-(N-метиламино)фенил, о-, м- или п-(N-метиламинокарбонил)фенил, о-, м- или п-ацетамидофенил, о-, м- или п-метоксифенил, о-, м- или п-этоксифенил, о-, м- или п-этоксикарбонилфенил, о-, м- или п-(N,N-диметиламино)фенил, о-, м- или п-(N,N-диметиламинокарбонил)фенил, о-, м- или п-(N-этиламино)фенил, о-, м- или п-(N,N-диэтиламино)фенил, о-, м- или п-фторфенил, о-, м- или п-бромфенил, о-, м- или п-хлорфенил, о-, м- или п-(метилсульфонамидо)фенил, о-, м- или п-(метилсульфонил)фенил, о-, -м- или п-цианофенил, о-, м- или п-уреидофенил, о-, м- или п-формилфенил, о-, м- или п-ацетилфенил, о-, м- или п-аминосульфонилфенил, о-, м- или п-карбоксифенил, о-, -м или п-карбоксиметилфенил, о-, м- или п-карбоксиметоксифенил, более предпочтительно 2,3-, 2,4-, 2,5-, 2,6-, 3,4- или 3,5-дифторфенил, 2,3-, 2,4-, 2,5-, 2,6-, 3,4- или 3,5-дихлорфенил, 2,3-, 2,4-, 2,5-, 2,6-, 3,4- или 3,5-дибромфенил, 2,4- или 2,5-динитрофенил, 2,5- или 3,4-диметоксифенил, 3-нитро-4-хлорфенил, 3-амино-4-хлор-, 2-амино-3-хлор-, 2-амино-4-хлор-, 2-амино-5-хлор- или 2-амино-6-хлорфенил, 2-нитро-4-N,N-диметиламино- или 3-нитpo-4-N,N-диметиламинофенил, 2,3-диаминофенил, 2,3,4-, 2,3,5-, 2,3,6-, 2,4,6- или 3,4,5- трихлорфенил, 2,4,6-триметоксифенил, 2-гидрокси-3,5-дихлорфенил, n-йодфенил, 3,6-дихлор-4-аминофенил, 4-фтор-3-хлорфенил, 2-фтор-4-бромфенил, 2,5-дифтор-4-бромфенил, 3-бром-6-метоксифенил, 3-хлор-6-метоксифенил, 3-хлор-4-ацетамидофенил, 3-фтор-4-метоксифенил, 3-амино-6-метилфенил, 3-хлор-4-ацетамидофенил или 2,5-диметил-4-хлорфенил.
Ar предпочтительно представляет собой фенил, который незамещен или одно-, дву-, три-, тетра- или пентазамещен A, Hal, OA, (СН2)nCOOH, (СН2)nCOOA, NHCO(CH2)nNH2 и/или -O-(CH2)o-Het1.
Ar более предпочтительно представляет собой фенил, который незамещен или одно- или двузамещен A, Hal, (СН2)nCOOH, (СН2)nCOOA, NHCO(CH2)nNH2 и/или-O-(СН2)o-Het1.
Ar′ предпочтительно представляет собой, например, фенил, который незамещен или одно-, дву- или тризамещен Hal.
Независимо от дальнейших замещений Het представляет собой, например, 2- или 3-фурил, 2- или 3-тиенил, 1-, 2- или 3-пирролил, 1-, 2, 4- или 5-имидазолил, 1-, 3-, 4- или 5-пиразолил, 2-, 4- или 5-оксазолил, 3-, 4- или 5-изоксазолил, 2-, 4- или 5-тиазолил, 3-, 4- или 5-изотиазолил, 2-, 3- или 4-пиридил, 2-, 4-, 5- или 6-пиримидинил, более предпочтительно 1,2,3-триазол-1-, -4- или -5-ил, 1,2,4-триазол-1-, -3- или 5-ил, 1- или 5-тетразолил, 1,2,3-оксадиазол-4- или -5-ил, 1,2,4-оксадиазол-3- или -5-ил, 1,3,4-тиадиазол-2- или -5-ил, 1,2,4-тиадиазол-3- или -5-ил, 1,2,3-тиадиазол-4- или -5-ил, 3- или 4-пиридазинил, пиразинил, 1-, 2-, 3-, 4-, 5-, 6- или 7-индолил, 4- или 5-изоиндолил, 1-, 2-, 4- или 5-бензимидазолил, 1-, 2-, 3-, 4-, 5-, 6- или 7-индазолил, 1-, 3-, 4-, 5-, 6- или 7-бензопиразолил, 2-, 4-, 5-, 6- или 7-бензоксазолил, 3-, 4-, 5-, 6- или 7-бензизоксазолил, 2-, 4-, 5-, 6- или 7-бензотиазолил, 2-, 4-, 5-, 6- или 7-бензизотиазолил, 4-, 5-, 6- или 7-бенз-2,1,3-оксадиазолил, 2-, 3-, 4-, 5-, 6-, 7- или 8-хинолил, 1-, 3-, 4-, 5-, 6-, 7- или 8-изохинолил, 3-, 4-, 5-, 6-, 7- или 8-циннолинил, 2-, 4-, 5-, 6-, 7- или 8-хиназолинил, 5- или 6-хиноксалинил, 2-, 3-, 5-, 6-, 7- или 8-2Н-бензо-1,4-оксазинил, более предпочтительно 1,3-бенздиоксол-5-ил, 1,4-бенздиоксан-6-ил, 2,1,3-бензотиадиазол-4- или -5-ил или 2,1,3-бензоксадиазол-5-ил.
Гетероциклические радикалы также могут быть частично или полностью гидрированы.
Het также может представлять собой, например, 2,3-дигидро-2-, -3-, -4- или -5-фурил, 2,5-дигидро-2-, -3-, -4- или 5-фурил, тетрагидро-2- или -3-фурил, 1,3-диоксолан-4-ил, тетрагидро-2- или -3-тиенил, 2,3-дигидро-1-, -2-, -3-, -4- или -5-пирролил, 2,5-дигидро-1-, -2-, -3-, -4- или -5-пирролил, 1-, 2- или 3-пирролидинил, тетрагидро-1-, -2- или -4-имидазолил, 2,3-дигидро-1-, -2-, -3-, -4- или -5-пиразолил, тетрагидро-1-, -3- или -4-пиразолил, 1,4-дигидро-1-, -2-, -3- или -4-пиридил, 1,2,3,4-тетрагидро-1-, -2-, -3-, -4-, -5- или-6- пиридил, 1-, 2-, 3- или 4-пиперидинил, 2-, 3- или 4-морфолинил, тетрагидро-2-, -3- или -4-пиранил, 1,4-диоксанил, 1,3-диоксан-2-, -4- или -5-ил, гексагидро-1-, -3- или -4-пиридазинил, гексагидро-1-, -2-, -4- или -5-пиримидинил, 1-, 2- или 3-пиперазинил, 1,2,3,4-тетрагидро-1-, -2-, -3-, -4-, -5-, -6-, -7- или -8-хинолил, 1,2,3,4-тетрагидро-1-, -2-, -3-, -4-, -5-, -6-, -7- или -8-изохинолил, 2-, 3-, 5-, 6-, 7- или 8-3,4-дигидро-2Н-бензо-1,4-оксазинил, более предпочтительно 2,3-метилендиоксифенил, 3,4-метилендиоксифенил, 2,3-этилендиоксифенил, 3,4-этилендиоксифенил, 3,4-(дифторметилендиокси)фенил, 2,3-дигидробензофуран-5- или 6-ил, 2,3-(2-оксометилендиокси)фенил или также 3,4-дигидро-2Н-1,5-бенздиокс