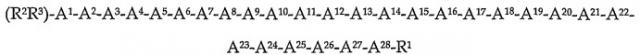Композиции и способы стимуляции двигательной функции желудочно-кишечного тракта
Иллюстрации
Показать всеГруппа изобретений относится к медицине, а именно к гастроэнтерологии и может быть использована для стимуляции двигательной функции желудочно-кишечного тракта. Изобретения предполагают введение терапевтически эффективного количества пептидильного аналога грелина, имеющего последовательность H-Inp-D-Bal-D-Trp-Phe-Apc-NH2 (BIM-28131), его фармацевтически приемлемой соли или в составе фармацевтических композиций. Для этого предлагают способы, характеризующие различные пути введения указанных средств при разных состояниях, сопровождающихся такими нарушениями. Изобретения позволяют обеспечить наиболее эффективную стимуляцию двигательной активности желудочно-кишечного тракта при различных типах нарушений, за счет выбранного аналога грелина, который обладает на порядок большей эффективностью и продолжительностью действия по сравнению с грелином. 7 н. и 23 з.п. ф-лы, 6 ил., 1 табл.
Реферат
Область техники, к которой относится изобретение
Настоящее изобретение направлено на способы стимуляции двигательной функции желудочно-кишечного тракта у пациента, которые предусматривают введение пептидильного аналога, обладающего агонистической активностью в отношении грелина, его пролекарства или фармацевтически приемлемой соли указанного аналога или указанного пролекарства.
Уровень техники
Двигательная функция желудочно-кишечного тракта (ЖКТ) представляет собой координированный нейромышечный процесс, обеспечивающий транспорт питательных веществ через пищеварительную систему (Scarpignato, C, Dig. Dis., (1997), 15:112), нарушение которого может приводить к развитию различных заболеваний, включающих гастроэзофагеальную рефлюксную болезнь (GERD), парез желудка (например, диабетический и после хирургической операции), синдром раздраженной кишки (IBS), констипацию (например, связанную с фазой гипокинезии IBS), рвоту (например, вызываемую противораковыми химиотерапевтическими средствами), непроходимость кишечника и псевдонепроходимость толстой кишки (патент США № 6548501; патентная заявка США № 20040266989). Указанные осложнения при нарушении двигательной функции ЖКТ относятся к серьезным проблемам здравоохранения промышленно развитых государств (патент США № 6548501; Feighner, S.D. et al., Science, (1999), 284:2184-8).
Термин "непроходимость кишечника" относится к закупорке кишки или пищеварительного канала, особенно толстой кишки (см., например, Dorland's Illustrated Medical Dictionary, p. 816, 27th ed. (W.B. Saunders Company, Philadelphia 1988)). Как правило, любая травма кишечника, сопровождающаяся высвобождением медиаторов воспаления для активации рефлексов нервного торможения, приводит к развитию непроходимости кишечника. Непроходимость кишечника можно диагностировать по нарушению нормальных согласованных движений кишечника, обеспечивающих продвижение его содержимого (Resnick, J., Am. J. of Gastroentero., (1997), 92:751; Resnick, J., Am. J. of Gastroentero., (1997), 92:934). Непроходимость кишечника следует отличать от констипации, которая характеризуется редкими или затрудненными испражнениями (см., например, Dorland's Illustrated Medical Dictionary, p. 375, 27th ed. (W.B. Saunders Company, Philadelphia 1988)).
Непроходимость кишечника может быть обусловлена разными причинами, такими как родовая деятельность; ишемия кишечника; ретроперитонеальная гематома; сепсис брюшной полости; воспаление брюшной полости, например, острый аппендицит, холецистит, панкреатит; переломы позвоночника; мочеточниковая колика; торакальные повреждения; базальная пневмония; переломы ребер; инфаркт миокарда; и нарушения метаболизма. Непроходимость кишечника является распространенной проблемой для женщин в послеродовой период, считается, что она обусловлена колебаниями уровней природных опиоидов в результате стресса, полученного при родах. Пациенты, подвергшиеся таким процедурам, как большая хирургическая операция брюшной полости, включая лапаротомию абдоминального абсцесса или трансплантацию тонкой кишки (SITx), хирургическая операция грудной клетки, таза или ортопедическая хирургия, часто страдают от временного ухудшения функции кишечника, называемого послеоперационная непроходимость кишечника (далее обозначаемая как POI).
POI обычно наблюдается в течение 24-72 часов после хирургической операции. В некоторых случаях дисфункция кишечника может стать очень тяжелой и может длиться более недели и поражать несколько участков ЖКТ (Livingston, E.H. et al., Digest. Dis. and Sei., (1990), 35:121). Обычно самое тяжелое нарушение моторики желудочно-кишечного тракта, связанное с POI, наблюдается в толстой кишке. POI характеризуется абдоминальной тошнотой, вздутием живота, рвотой, обстипацией, неспособностью есть и спазмами. POI не только замедляет нормальное возобновление потребления пищи после хирургической операции, но и приводит к развитию послеоперационных осложнений, особенно аспирационной пневмонии.
Введение опиоидных обезболивающих средств после хирургической операции зачастую может вносить вклад в развитие дисфункции кишечника у пациента или усиливать уже существующую дисфункцию кишечника, и, следовательно, замедлять восстановление нормальной функции кишечника. Поскольку практически все пациенты получают опиоидные обезболивающие средства, например морфин или другие наркотические средства, для облегчения боли после хирургической операции, особенно полостной операции, существующие в настоящее время способы лечения послеоперационной боли могут существенно замедлять восстановление нормальной функции кишечника и задерживать выписку из больницы, увеличивая стоимость медицинского обслуживания.
Средства, влияющие на двигательную функцию желудочно-кишечного тракта, также могут оказывать благоприятное действие на пациентов, страдающих от рвоты. Рвоте или тошноте часто предшествуют позывы к рвоте, которые могут сопровождаться сухими рвотными движениями. Рвоту могут вызывать нарушения в пищеварительном тракте, такие как непроходимость кишечника, диспепсия или воспаление стенки желудка, или нарушения в сенсорной системе мозга, такие как укачивание, мигрень или опухоли. Рвота может возникать самопроизвольно, например, при анорексии или булимии, она также может происходить в ответ на тяжелую боль, эмоциональные реакции (например, на неприятные образы или запахи) или беременность. Рвота является распространенным осложнением после введения многих лекарственных средств, особенно противораковых средств, таких как химиотерапевтические средства. Продолжительные приступы повторяющейся рвоты могут приводить к различным повреждениям организма, включая обезвоживание и электролитный дисбаланс (Quigley, E.M. et al., Gastroentero., (2001), 120:263-86).
Средства, влияющие на двигательную функцию желудочно-кишечного тракта, также могут оказывать благоприятное действие на пациентов, страдающих от пареза желудка. Парез желудка, также называемый замедленным опорожнением желудка, представляет собой заболевание, при котором нервы, связанные с желудком, повреждаются или прекращают функционировать, и в результате опорожнение желудка занимает слишком много времени. Например, после повреждения блуждающего нерва, который контролирует движение пищи через пищеварительный тракт, мышцы желудка и кишечника перестают работать нормально и движение пищи замедляется или останавливается. Высокий уровень глюкозы в крови вызывает химические изменения в нервах и повреждения кровеносных сосудов, которые несут кислород и питательные вещества к нервам. Если уровень глюкозы остается высоким в течение длительного времени, как это обычно бывает при диабете, может произойти повреждение блуждающего нерва; парез желудка часто встречается у людей с диабетом типа 1 или типа 2 (Murray, C. D. et al., Gut, (2005), 54:1693-8).
Традиционные способы лечения нарушений двигательной функции ЖКТ, таких как кишечная непроходимость, парез желудка и рвота, считаются неэффективными. Существующие в настоящее время способы лечения кишечной непроходимости предусматривают функциональную стимуляцию кишечника, применение средств, разжижающих стул, слабительных, таких как Dulcolax®, смазывающих средств, внутривенную гидратацию, назогастральную аспирацию, применение прокинетических средств, раннее энтеральное питание и назогастральную декомпрессию. Кроме того, для лечения кишечной непроходимости часто используют назогастральную интубацию с целью декомпрессии желудка.
Традиционные фармацевтические средства, используемые для лечения нарушений двигательной функции ЖКТ, таких как кишечная непроходимость, включают лекарственные средства, усиливающие двигательную функцию толстой кишки, такие как Leu13-мотилин и простагландин F2α, а также прокинетические средства, такие как Cisapride®. PROPULSID®, содержащий моногидрат Cisapride®, представляет собой пероральное желудочно-кишечное средство (патент США № 4962115), которое назначают для симптоматического лечения взрослых пациентов с ночной изжогой, как следствием гастроэзофагеальной рефлюксной болезни. Другие прокинетические средства включают, например, метоклопрамид, домперидон, ондансетрон, трописетрон, мосаприд и итоприд. Другие способы лечения предусматривают введение пиразолопиридиновых соединений в качестве антагонистов аденозина (патент США № 6214843); антагониста рецептора гипофизарного аденилатциклаза-активирующего пептида (PACAP) в сочетании с антагонистом рецептора вазоактивного пептида кишечника (VIP) (патент США № 6911430); федотозина (патент США № 5362756); нейропептидов (патент США № 5929035) и антагонистов активируемого протеинкиназой рецептора-2 (патент США № 5929035). В крайних случаях кишечную непроходимость лечат путем хирургического вмешательства для разблокирования толстой кишки.
Однако перечисленные способы лечения имеют многочисленные недостатки. Например, PROPULSID® недавно изъяли из продажи, поскольку он может вызывать сердечную аритмию (патент США № 6548501). Adolor Corporation в настоящее время проводит клинические испытания, фаза III, способа лечения послеоперационной кишечной непроходимости с использованием Alvimopan (Entereg®). Однако в способе лечения Adolor используются антагонисты опиоидных рецепторов, которые только блокируют побочные эффекты опиатных обезболивающих средств, не облегчая реально состояние кишечной непроходимости. Фаза III испытаний показывает, что указанный способ лечения кишечной непроходимости, в частности послеоперационной кишечной непроходимости, обладают низкой эффективностью и минимальной применимостью.
Кроме того, существующие на известном уровне техники способы лечения нарушений двигательной функции ЖКТ не обладают специфичностью в отношении различных типов нарушений, например послеоперационной кишечной непроходимости или послеродовой кишечной непроходимости. Существующие на известном уровне техники способы также не обеспечивают профилактики нарушений двигательной функции ЖКТ, таких как кишечная непроходимость, парез желудка и рвота. Если бы нарушения двигательной функции ЖКТ, такие как кишечная непроходимость, парез желудка и рвота, можно было предотвращать или более эффективно лечить, время пребывания в стационаре, время восстановления и стоимость медицинского обслуживания можно было значительно снизить при дополнительной минимизации дискомфорта пациента.
Лекарственные средства, обладающие селективностью в отношении двигательной функции пищеварительного тракта и способные корректировать дисфункцию желудочно-кишечного тракта, вызванную послеоперационной кишечной непроходимостью, могут быть идеальными кандидатами для профилактики и/или лечения послеоперационной или послеродовой кишечной непроходимости. Такие лекарственные средства также могут быть превосходными кандидатами для лечения пареза желудка и/или рвоты, особенно рвоты, связанной с дисфункцией желудочно-кишечного тракта, вызванной химиотерапевтическими или другими лекарственными средствами. Среди указанных лекарственных средств особенно полезными являются такие, которые не препятствуют действию опиоидных обезболивающих, поскольку их можно вводить одновременно со средствами для лечения боли при ограниченных побочных эффектах.
В настоящее время считают, что пептиды, влияющие на высвобождение гормона роста (GH), оказывают гастрокинетические или "прокинетические" эффекты (патент США № 6548501; Peeters, T.L., J Physiol. Pharmacol., (2003), 54 (supp 4):95-103, а также приведенные в данном патенте ссылки; Trudel, L. et al, J. Physiol. Gastrointest. Liver Physiol., (2002), 282:G948-52). Такие пептиды, высвобождающие гормон роста, или GHRP, также называют стимуляторами секреции гормона роста (GHS). Примеры пептидов, высвобождающих гормон роста (GHRP) и предположительно обладающих прокинетическими эффектами, включают GHRP-I, GHRP-2 и грелин.
Грелин, недавно открытый гормон возбуждения аппетита, продуцируется в виде препрогормона, который после протеолитического процессинга превращается в пептид, имеющий следующую последовательность: H-Gly-Ser-Ser-Phe-Leu-Ser-Pro-Glu-His-Gln-Arg-Val-Gln-Gln-Arg-Lys-Glu-Ser-Lys-Lys-Pro-Pro-Ala-Lys-Leu-Gln-Pro-Arg-NH2 (Kojima, M. et al., Nature, (1999), 402(6762):656-60). Грелин продуцируется эпителиальными клетками, выстилающими дно желудка, его функция заключается в стимуляции аппетита; уровень грелина повышается перед едой и уменьшается после приема пищи.
Грелин эффективно стимулирует секрецию GH из передней доли гипофиза, в основном, на уровне гипоталамуса, через взаимодействие с рецептором стимулятора секреции гормона роста (GHS-R), как у животных, так и у людей (Ukkola, O. et al., Ann. Med., (2002), 34:102-8; (Kojima, M. et al., Nature, (1999), 402(6762):656-60).
Известны природные структуры грелина из нескольких видов млекопитающих и отличных от млекопитающих видов (Kaiya, H. et al., J. of Biol. Chem., (2001), 276:40441-8 и Международная патентная заявка РСТ/JР00/04907 [WO 01/07475]). Центральный участок грелина отвечает за наблюдаемую активность рецептора GHS. Центральный участок содержит четыре N-концевые аминокислоты, причем серин в положении три обычно модифицирован н-октановой кислотой. Помимо ацилирования н-октановой кислотой нативный грелин может быть ацилирован н-декановой кислотой (Kaiya, H. et al., J. of Biol. Chem., (2001), 276:40441-8).
До открытия того факта, что грелин является природным лигандом рецептора GHS, было известно, что GHRP контролируют высвобождение гормона роста из гипофизарных соматотропных клеток. Обнаружено, что у некоторых видов, включая человека, гексапептид His-D-Trp-Ala-Trp-D-Phe-Lys-амид (GHRP-6) высвобождает гормон роста из соматотропных клеток в зависимости от дозы (Bowers, C.Y. et al., Endocrinology, (1984), 114(5):1537-45). Последующие химические исследования GHRP-6 привели к идентификации других активных синтетических GHS, таких как GHRP-I, GHRP-2 и гексарелин (Cheng, K. et al., Endocrinology, (1989), 124(6):2791-8; Bowers, C.Y., Novel GH-Releasing Peptides. Molecular and Clinical Advances in Pituitary Disorders, Ed: Melmed, S., Endocrine Research and Education, Inc., Los Angeles, CA, USA, (1993), 153-7; и Deghenghi, R. et al., Life Sei., (1994), 54(18):1321-8). Данные соединения имеют следующие структуры:
GHRP-I Ala-His-D-(2')-Nal-Ala-Trp-D-Phe-Lys-NH2;
GHRP-2 D-Ala-D-(2')-Nal-Ala-Trp-D-Nal-Lys-NH2 и
Гексарелин His-D-2-MeTrp-Ala-Trp-D-Phe-Lys-NH2.
GHRP-I, GHRP-2, GHRP-6 и гексарелин относятся к классу синтетических GHS.
Проведенные в последнее время исследования показали, что GHS, такие как грелин, GHRP-6 и другие, можно использовать для стимуляции двигательной активности кишечного тракта и для лечения таких состояний, как кишечная непроходимость и рвота. Например, было показано, что грелин и GHRP-6 ускоряют опорожнение желудка у крыс и мышей (Peeters, T. L., J Physiol. Pharmacol., (2003), 54 (supp 4):95-103). Обнаружено, что грелин уменьшает замедление опорожнения желудка на крысиной модели послеоперационной кишечной непроходимости (Peeters, T.L., J Physiol. Pharmacol., (2003), 54 (supp 4):95-103; Trudel, L. et al., J. Physiol. Gastrointest. Liver Physiol., (2002), 282(6):G948-52) и у собак после лапарэктомии, показано, что грелин улучшает POI у обработанных животных (Trudel, L. et al, Peptides, (2003), 24:531-4). У септических мышей грелин и GHRP-6 ускоряют опорожнение желудка, но мало влияют на повышение скорости передачи пищевой массы в тонкий кишечник (De Winter, B. Y. et al., Neurogastroenterol. Motil., (2004), 16:439-46).
В экспериментах по имитированию условий госпитализации для пациентов-людей, страдающих от POI, крысам после лапарэктомии вводят опиаты и аналог грелина RC-1139 (Poitras, P. et al., Peptides, (2005), 26:1598-601). Анализ с измерением опорожнения желудка показал, что RC-1139 уменьшает POI у контрольных крыс и крыс после лапарэктомии в присутствии морфина. Следовательно, можно предположить, что грелин оказывает гастрокинетическое действие, не влияя на активность опиатов.
У хорьков, получающих цитотоксическое противораковое средство цисплатин, после церебровентрикулярного введения грелина гораздо реже наблюдаются позывы к рвоте и рвота (Rudd, J.A. et al., Neurosci. Lett, (2006), 392:79-83), что подтверждает способность грелина уменьшать рвоту в соответствии с ролью, которую он играет в модуляции функций желудочно-кишечного тракта. Полагают, что роль грелина в модуляции двигательной функции желудка зависит от активации секреции GH и может опосредоваться вагально-холинергическим мускариновым путем (патентная заявка США № 20060025566).
Кроме того, показано, что грелин ускоряет опорожнение желудка у пациентов с диабетическим парезом желудка (Murray, C. D. et al., Gut, (2005), 54:1693-8).
Следует отметить, что в приведенных выше исследованиях грелин или аналог грелина вводят путем внутрибрюшинной (в.б.), внутривенной (в.в.) или интрацеребровентрикулярной (и.ц.в.) инъекции. В других работах (патент США № 6548501; патентная заявка США № 20020042419; патентная заявка США № 20050187237; патентная заявка США № 20060025566) описано пероральное введение GHS для лечения нарушений двигательной функции желудочно-кишечного тракта.
В данной области известно очень мало соединений, которые можно использовать для лечения двигательной функции ЖКТ, следовательно, существует настоятельная потребность в увеличении количества соединений, оказывающих влияние, такое как стимуляция, на моторику желудочно-кишечного тракта. Соединения, оказывающие влияние на двигательную функцию желудочно-кишечного тракта, можно использовать для лечения нарушений нормальных функций ЖКТ, таких как кишечная непроходимость и рвота.
Раскрытие изобретения
Настоящее изобретение относится к способу стимуляции двигательной функции желудочно-кишечного тракта у пациента (например, у млекопитающего, такого как человек). Данный способ предусматривает стадию введения терапевтически эффективного количества пептидильного аналога грелина указанному пациенту, страдающему от нарушения моторики желудочно-кишечного тракта или имеющему риск такого нарушения.
В одном аспекте настоящее изобретение предлагает способ лечения состояний с нарушением двигательной функции желудочно-кишечного тракта путем введения терапевтически эффективного количества пептидильного аналога грелина или его пролекарства, подходящих для облегчения таких состояний желудочно-кишечного тракта, где аналог или его пролекарство включает соединение формулы (I), формулы (II) или формулы (III), или его фармацевтически приемлемую соль. Способ данного изобретения можно использовать для стимуляции двигательной функции желудка и желудочно-кишечного тракта у пациента (например, у млекопитающего, такого как человек) и, как таковой, его можно использовать для лечения состояний, на которые благоприятное действие оказывает улучшение двигательной функции желудка и желудочно-кишечного тракта, таких как гастроэзофагеальная рефлюксная болезнь (GERD), IBS, констипация, кишечная непроходимость, рвота, парез желудка, псевдонепроходимость толстой кишки и т.п.
В другом аспекте данное изобретение предлагает способ лечения кишечной непроходимости, пареза желудка или рвоты путем введения терапевтически эффективного количества пептидильного аналога грелина, подходящего для облегчения кишечной непроходимости, рвоты или пареза желудка. В следующем аспекте состояние, подлежащее лечению с помощью способа данного изобретения, представляет собой кишечную непроходимость, например послеоперационную кишечную непроходимость, после хирургической операции на желудочно-кишечном тракте. В следующем аспекте данного изобретения состояние, подлежащее лечению с помощью способа данного изобретения, представляет собой рвоту, например рвоту, связанную с введением противоракового химиотерапевтического средства или вызванную введением такого средства. В следующем аспекте состояние, подлежащее лечению с помощью способа данного изобретения, представляет собой парез желудка, например диабетический парез желудка. Диабет может представлять собой диабет типа I или типа II.
В одном аспекте изобретение предлагает способ лечения желудочно-кишечных состояний, таких как GERD, IBS, констипация, кишечная непроходимость, рвота, парез желудка, псевдонепроходимость толстой кишки и т.п., путем введения терапевтически эффективного количества пептидильного аналога грелина формулы (I):
где
A1 обозначает Gly, Aib, Ala, β-Ala или Асc;
A2 обозначает Ser, Aib, Act, Ala, Acc, Abu, Ava, Thr или Val;
A3 обозначает Ser, Ser(C(О)-R4), Asp(О-R8), Asp(NH-R9), Cys(S-R14), Dap(S(O)2-R10), Dab(S(О)2-R11), Glu(O-R6), Glu(NH-R7), Thr, Thr(C(O)-R5) или HN-CH((CH2)n-N(R12R13))-C(O);
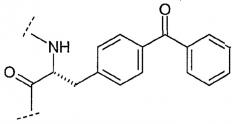
A4 обозначает Phe, Acc, Aic, Cha, 2-Fua, 1-Nal, 2-Nal, 2-Pal, 3-Pal, 4-Pal, hPhe, (X1,X2,X3,X4,X5)Phe, Taz, 2-Thi, 3-Thi, Trp или Tyr;
A5 обозначает Leu, Abu, Acс, Aib, Ala, Cha, Ile, hLeu, Nle, Nva, Phe, Tle или Val;
A6 обозначает Ser, Abu, Acc, Act, Aib, Ala, Gly, Thr или Val;
A7 обозначает Pro, Dhp, Dmt, 3-Hyp, 4-Hyp, Inc, Ktp, Oic, Pip, Thz, Tic или исключен;
A8 обозначает Glu, Acс, Aib, Arg, Asn, Asp, Dab, Dap, Gln, Lys, Orn, HN-CH((CH2)n-N(R12R13))-C(O) или исключен;
A9 обозначает His, Apc, Aib, Acc, 2-Fua, 2-Pal, 3-Pal, 4-Pal, Taz, 2-Thi, 3-Thi, (X1,X2,X3,X4,X5)Phe или исключен;
A10 обозначает Gln, Acc, Aib, Asn, Asp, Glu или исключен;
A11 обозначает Arg, Apс, hArg, Dab, Dap, Lys, Orn, HN-CH((CH2)n-N(R12R13))-C(O) или исключен;
A12 обозначает Val, Abu, Acс, Aib, Ala, Cha, Nva, Gly, Ile, Leu, Nle, Tle или исключен;
A13 обозначает Gln, Acc, Aib, Asn, Asp, Glu или исключен;
A14 обозначает Gln, Acc, Aib, Asn, Asp, Glu или исключен;
A15 обозначает Arg, hArg, Acc, Aib, Apc, Dab, Dap, Lys, Orn, HN-CH((CH2)n-N(R12R13))-C(O) или исключен;
A16 обозначает Lys, Acc, Aib, Apc, Arg, hArg, Dab, Dap, Orn, HN-CH((CH2)n-N(R12R13))-C(O) или исключен;
A17 обозначает Glu, Arg, Asn, Asp, Dab, Dap, Gln, Lys, Orn, HN-CH((CH2)n-N(R12R13))-C(O) или исключен;
A18 обозначает Ser, Abu, Acc, Act, Aib, Ala, Thr, Val или исключен;
A19 обозначает Lys, Acc, Aib, Apc, Arg, hArg, Dab, Dap, Orn, HN-CH((CH2)n-N(R12R13))-C(O) или исключен;
A20 обозначает Lys, Acc, Aib, Apc, Arg, hArg, Dab, Dap, Orn, HN-CH((CH2)n-N(R12R13))-C(O) или исключен;
A21 обозначает Pro, Dhp, Dmt, 3-Hyp, 4-Hyp, Inc, Ktp, Oic, Pip, Thz, Tic или исключен;
A22 is Pro, Dhp, Dmt, 3-Hyp, 4-Hyp, Inc, Ktp, Oic, Pip, Thz, Tic или исключен;
A23 обозначает Abu, Acc, Act, Aib, Ala, Apc, Gly, Nva, Val или исключен;
A24 обозначает Lys, Acс, Aib, Apc, Arg, hArg, Dab, Dap, Orn, HN-CH((CH2)n-N(R12R13))-C(O) или исключен;
A25 обозначает Leu, Abu, Acс, Aib, Ala, Cha, Ile, hLeu, Nle, Nva, Phe, Tle, Val или исключен;
A26 обозначает Gln, Aib, Asn, Asp, Glu или исключен;
A27 обозначает Pro, Dhp, Dmt, 3-Hyp, 4-Hyp, Inc, Ktp, Oic, Pip, Thz, Tic или исключен;
A28 обозначает Acc, Aib, Apc, Arg, hArg, Dab, Dap, Lys, Orn, HN-CH((CH2)n-N(R12R13))-C(O) или исключен;
R1 представляет собой -OH, -NH2, -(С1-С30)алкокси или NH-X6-CH2-Z0, где X6 представляет собой (C1-C12)алкил, (C2-C12)алкенил, и Z0 представляет собой -H, -OH, -CO2H или -C(O)-NH2;
R2 и R3, каждый независимо, в каждом случае представляет собой H, (C1-C20)алкил или (C1-C20)ацил;
R4, R5, R6, R7, R8, R9, R10, R11 и R14, каждый независимо, в каждом случае представляет собой (C1-C40)алкил, (C2-C40)алкенил, замещенный (C1-C40)алкил, замещенный (C2-C40)алкенил, алкиларил, замещенный алкиларил, арил или замещенный арил;
R12 и R13, каждый независимо, в каждом случае представляет собой H, (C1-C40)алкил, (C1-C40)ацил, (C1-C30)алкилсульфонил или -C(NH)-NH2, где, если R12 представляет собой (C1-C40)ацил, (C1-C30)алкилсульфонил или -C(NH)-NH2, то R13 представляет собой H или (C1-C40)алкил;
n в каждом случае независимо равен 1, 2, 3, 4 или 5;
X1, X2, X3, X4 и X5, каждый независимо, в каждом случае представляет собой H, F, Cl, Br, I, (C1-C10)алкил, замещенный (C1-C10)алкил, арил, замещенный арил, OH, NH2, NO2 или CN;
при условии, что пептид содержит по меньшей мере одну аминокислоту, выбранную из группы, состоящей из:
A2, который обозначает Aib, Acс или Act;
A3, который обозначает Dap(S(O)2-R10), Dab(S(O)2-R11), Glu(NH-гексил) или Cys(S-децил);
A5, который обозначает Abu, Acс, Aib, Ala, Cha, Ile, hLeu, Nle, Nva, Phe, Tle или Val;
A6, который обозначает Abu, Acс, Act, Aib, Ala, Gly, Thr или Val;
A7, который обозначает Dhp, Dmt, 3-Hyp, 4-Hyp, Inc, Ktp, Oic, Pip, Thz или Tic;
A8, который обозначает Acс, Aib, Arg, Asn, Asp, Dab, Dap, Gln, Lys, Orn или HN-CH((CH2)n-N(R12R13))-C(O);
A9, который обозначает Aib, Acс, Apс, 2-Fua, 2-Pal, 3-Pal, 4-Pal, Taz, 2-Thi, 3-Thi или (X1,X2,X3,X4,X5-)Phe; и
A10, который обозначает Acс, Aib, Asn, Asp или Glu;
и при дополнительном условии, что пептид не является (Lys8)hгрелин(1-8)-NH2 или (Arg8)hгрелин(1-8)-NH2; или его фармацевтически приемлемой соли.
В другом аспекте данное изобретение предлагает группу предпочтительных соединений формулы (I), где:
A1 обозначает Gly или Aib;
A2 обозначает Ser, Aib, A5c, Act или Ava;
A3 обозначает Ser(C(O)-R4), Glu(O-R6), Glu(NH-R7), Dap(S(O)2-R10) или Dab(S(O)2-R11);
A4 обозначает Phe;
A5 обозначает Leu, Acс, Aib, Cha или hLeu;
A6 обозначает Ser, Abu, Act, Aib или Thr;
A7 обозначает Pro, Dhp, Dmt, 4-Hyp, Ktp, Pip, Tic или Thz;
A8 обозначает Glu или Aib;
A9 обозначает His, Aib, Apc, 2-Fua, 2-Pal, 3-Pal, 4-Pal, Taz или 2-Thi;
A10 обозначает Gln или Aib;
A11 обозначает Arg;
A12 обозначает Aib, Val или Ace;
A13 обозначает Gln;
A14 обозначает Gln;
A15 обозначает Arg или Orn;
A16 обозначает Lys или Apс;
A17 обозначает Glu;
A18 обозначает Ser;
A19 обозначает Lys;
A20 обозначает Lys;
A21 обозначает Pro;
A22 обозначает Pro;
A23 обозначает Ala;
A24 обозначает Lys;
A25 обозначает Leu;
A26 обозначает Gln;
A27 обозначает Pro; и
A28 обозначает Arg, или их фармацевтически приемлемые соли.
В следующем аспекте данное изобретение предлагает группу предпочтительных соединений формулы (I), где:
R2 и R3, каждый независимо, представляет собой H, ацил, н-бутирил, изобутирил или н-октаноил;
R4 представляет собой октил;
R6 представляет собой гексил;
R7 представляет собой гексил;
R10 представляет собой октил; и
R11 представляет собой октил, или их фармацевтически приемлемые соли, где Acс в каждом случае независимо обозначает A5c или A6c.
В следующем аспекте данное изобретение предлагает группу предпочтительных соединений формулы (I), включающую следующие соединения:
(Dap3(октансульфонил))hгрелин(1-28)-NH2; Пример 75
(Aib2, A6c5)hгрелин(1-28)-NH2; Пример 96
(A6c5)hгрелин(1-28)-NH2;
(Aib2,6)hгрелин(1-28)-NH2; Пример 108
(Aib2, A5c12)hгрелин(1-28)-NH2;
(Aib2, A5c12, Orn15)hгрелин(1-28)-NH2;
(Aib2, A5c12, Apc16)hгрелин(1-28)-NH2;
(Aib2, Act6)hгрелин(1-28)-NH2;
(Aib2, 3-Pal9)hгрелин(1-28)-NH2; Пример 29
(Aib2, Dmt7)hгрелин(1-28)-NH2;
(Aib2, Thz7)hгрелин(1-28)-NH2;
(A5c2)hгрелин(1-28)-NH2; Пример 52
(Act2)hгрелин(1-28)-NH2; Пример 94
(Aib2, A5c5)hгрелин(1-28)-NH2;
(Aib2, A6c5)hгрелин(1-28)-NH2;
(Aib2,5)hгрелин(1-28)-NH2;
(Aib2, hLeu5)hгрелин(1-28)-NH2;
(Aib2, Cha5)hгрелин(1-28)-NH2;
(Aib2,6)hгрелин(1-28)-NH2;
(Aib2, Act6)hгрелин(1-28)-NH2; Пример 114
(Aib2, Thr6)hгрелин (1-28)-NH2;
(Aib2, Abu6)hгрелин(1-28)-NH2; Пример 88
(Aib2, 4-Hyp7)hгрелин (1-28)-NH2; Пример 36
(Aib2, Thz7)hгрелин(1-28)-NH2; Пример 54
(Aib2, Pip7)hгрелин(1-28)-NH2; Пример 65
(Aib2, Dhp7)hгрелин (1-28)-NH2; Пример 44
(Aib2, Ktp7)hгрелин(1-28)-NH2;
(Aib2,8)hгрелин(1-28)-NH2; Пример 49
(Aib2, 2-Pal9)hгрелин(1-28)-NH2;
(Aib2, 3-Pal9)hгрелин(1-28)-NH2;
(Aib2, 4-Pal9)hгрелин(1-28)-NH2; Пример 55
(Aib2, Taz9)hгрелин(1-28)-NH2; Пример 27
(Aib2, 2-Thi9)hгрелин(1-28)-NH2;
(Aib2, 2-Fua9)hгрелин(1-28)-NH2;
(Aib2, Apc9)hгрелин(1-28)-NH2;
(Aib2,9)hгрелин(1-28)-NH2;
(Aib2,10)hгрелин(1-28)-NH2; Пример 48
(Aib2, Tic7)hгрелин(1-28)-NH2; Пример 53
(Aib6)hгрелин(1-28)-NH2;
(A5c5)hгрелин(1-28)-NH2;
(A6c5)hгрелин(1-28)-NH2; Пример 102
(Act6)hгрелин(1-28)-NH2;
(3-Pal9)hгрелин(1-28)-NH2; Пример 32
(Dmt7)hгрелин(1-28)-NH2;
(Thz7)hгрелин(1-28)-NH2;
(Aib5)hгрелин(1-28)-NH2;
(hLeu5)hгрелин(1-28)-NH2;
(Cha5)hгрелин(1-28)-NH2;
(Thr6)hгрелин(1-28)-NH2;
(Abu6)hгрелин(1-28)-NH2;
(4-Hyp7)hгрелин(1-28)-NH2;
(Pip7)hгрелин(1-28)-NH2;
(Dhp7)hгрелин(1-28)-NH2;
(Ktp7)hгрелин(1-28)-NH2;
(Aib8)hгрелин(1-28)-NH2; Пример 10
(2-Pal9)hгрелин(1-28)-NH2;
(3-Pal9)hгрелин(1-28)-NH2;
(4-Pal9)hгрелин(1-28)-NH2;
(Taz9)hгрелин(1-28)-NH2;
(2-Thi9)hгрелин(1-28)-NH2; Пример 26
(2-Fua9)hгрелин(1-28)-NH2;
(Apc9)hгрелин(1-28)-NH2;
(Aib9)hгрелин(1-28)-NH2;
(Aib10)hгрелин(1-28)-NH2;
(Aib2, Dap3(октансульфонил), A6c5)hгрелин(1-28)-NH2;
(Dap3(октансульфонил), A6c5)hгрелин(1-28)-NH2;
(Aib2,6, Dap3(октансульфонил))hгрелин(1-28)-NH2;
(Aib2, Dap3(октансульфонил), A5c12)hгрелин(1-28)-NH2;
(Aib2, Dap3(октансульфонил), A5c12, Orn15)hгрелин(1-28)-NH2;
(Aib2, Dap3(октансульфонил), A5c12, Apc16)hгрелин(1-28)-NH2;
(Aib2, Dap3(октансульфонил), Act6)hгрелин(1-28)-NH2;
(Aib2, Dap3(октансульфонил), 3-Pal9)hгрелин(1-28)-NH2;
(Aib2, Dap3(октансульфонил), Dmt7)hгрелин(1-28)-NH2;
(Aib2, Dap3(октансульфонил), Thz7)hгрелин(1-28)-NH2;
(A5c2, Dap3(октансульфонил))hгрелин(1-28)-NH2;
(Act2, Dap3(октансульфонил))hгрелин(1-28)-NH2;
(Aib2, Dap3(октансульфонил), A5c5)hгрелин(1-28)-NH2;
(Aib2,5, Dap3(октансульфонил))hгрелин(1-28)-NH2;
(Aib2, Dap3(октансульфонил), hLeu5)hгрелин(1-28)-NH2;
(Aib2, Dap3(октансульфонил), Cha5)hгрелин(1-28)-NH2;
(Aib2,6, Dap3(октансульфонил))hгрелин(1-28)-NH2;
(Aib2, Dap3(октансульфонил), Thr6)hгрелин(1-28)-NH2;
(Aib2, Dap3(октансульфонил), Abu6)hгрелин(1-28)-NH2;
(Aib2, Dap3(октансульфонил), 4-Hyp7)hгрелин(1-28)-NH2;
(Aib2, Dap3(октансульфонил), Pip7)hгрелин(1-28)-NH2;
(Aib2, Dap3(октансульфонил), Dhp7)hгрелин(1-28)-NH2;
(Aib2, Dap3(октансульфонил), Ktp7)hгрелин(1-28)-NH2;
(Aib2,8, Dap3(октансульфонил))hгрелин(1-28)-NH2;
(Aib2, Dap3(октансульфонил), 2-Pal9)hгрелин(1-28)-NH2;
(Aib2, Dap3(октансульфонил), 3-Pal9)hгрелин(1-28)-NH2
(Aib2, Dap3(октансульфонил), 4-Pal9)hгрелин(1-28)-NH2;
(Aib2, Dap3(октансульфонил), Taz9)hгрелин(1-28)-NH2;
(Aib2, Dap3(октансульфонил), 2-Thi9)hгрелин(1-28)-NH2;
(Aib2, Dap3(октансульфонил), 2-Fua9)hгрелин(1-28)-NH2;
(Aib2, Dap3(октансульфонил), Apc9)hгрелин(1-28)-NH2;
(Aib2,9, Dap3(октансульфонил))hгрелин(1-28)-NH2;
(Aib2,10, Dap3(октансульфонил))hгрелин(1-28)-NH2;
(Dap3(октансульфонил), A6c5)hгрелин(1-28)-NH2;
(Dap3(октансульфонил), Aib6)hгрелин(1-28)-NH2;
(Dap3(октансульфонил), A5c12)hгрелин(1-28)-NH2;
(Dap3(октансульфонил), A5c12, Orn15)hгрелин(1-28)-NH2;
(Dap3(октансульфонил), A5c12, Apc16)hгрелин(1-28)-NH2;
(Dap3(октансульфонил), Act6)hгрелин(1-28)-NH2;
(Dap3(октансульфонил), 3-Pal9)hгрелин(1-28)-NH2;
(Dap3(октансульфонил), Dmt7)hгрелин(1-28)-NH2;
(Dap3(октансульфонил), Thz7)hгрелин(1-28)-NH2;
(Dap3(октансульфонил), A5c5)hгрелин(1-28)-NH2;
(Dap3(октансульфонил), Aib5)hгрелин(1-28)-NH2;
(Dap3(октансульфонил), hLeu5)hгрелин(1-28)-NH2;
(Dap3(октансульфонил), Cha5)hгрелин(1-28)-NH2;
(Dap3(октансульфонил), Thr6)hгрелин(1-28)-NH2;
(Dap3(октансульфонил), Abu6)hгрелин(1-28)-NH2;
(Dap3(октансульфонил), 4-Hyp7)hгрелин(1-28)-NH2;
(Dap3(октансульфонил), Pip7)hгрелин(1-28)-NH2;
(Dap3(октансульфонил), Dhp7)hгрелин(1-28)-NH2;
(Dap3(октансульфонил), Ktp7)hгрелин(1-28)-NH2;
(Dap3(октансульфонил), Aib8)hгрелин(1-28)-NH2;
(Dap3(октансульфонил), 2-Pal9)hгрелин(1-28)-NH2;
(Dap3(октансульфонил), 3-Pal9)hгрелин(1-28)-NH2;
(Dap3(октансульфонил), 4-Pal9)hгрелин(1-28)-NH2;
(Dap3(октансульфонил), Taz9)hгрелин(1-28)-NH2;
(Dap3(октансульфонил), 2-Thi9)hгрелин(1-28)-NH2;
(Dap3(октансульфонил), 2-Fua9)hгрелин(1-28)-NH2;
(Dap3(октансульфонил), Apc9)hгрелин(1-28)-NH2;
(Dap3(октансульфонил), Aib9)hгрелин(1-28)-NH2;
(Dap3(октансульфонил), Aib10)hгрелин(1-28)-NH2;
(Dap3(октансульфонил), A5c12, Orn15)hгрелин(1-28)-NH2;
(Dab3(октансульфонил), A5c12, Orn15)hгрелин(1-28)-NH2;
(Aib2, A6c5, A5c12, Orn15)hгрелин(1-28)-NH2;
(А6с5, A5c12, Orn15)hгрелин(1-28)-NH2;
(Aib2,6, A5c12, Orn15)hгрелин(1-28)-NH2;
(Aib2, Act6, A5c12, Orn15)hгрелин(1-28)-NH2;
(Aib2, 3-Pal9, A5c12, Orn15)hгрелин(1-28)-NH2;
(Aib2, Dmt7, A5c12, Orn15)hгрелин(1-28)-NH2;
(Aib2, Thz7, A5c12, Orn15)hгрелин(1-28)-NH2;
(Aib2, A5c5, A5c12, Orn15)hгрелин(1-28)-NH2;
(Aib2,5, A5c12, Orn15)hгрелин(1-28)-NH2;
(Aib2, hLeu5, A5c12, Orn15)hгрелин(1-28)-NH2;
(Aib2, Cha5, A5c12, Orn15)hгрелин(1-28)-NH2;
(Aib2,6, A5c12, Orn15)hгрелин(1-28)-NH2;
(Aib2, Thr6, A5c12, Orn15)hгрелин(1-28)-NH2;
(Aib2, Abu6, A5c12, Orn15)hгрелин(1-28)-NH2;
(Aib2, 4Hyp7, A5c12, Orn15)hгрелин(1-28)-NH2;
(Aib2, Pip7, A5c12, Orn15)hгрелин(1-28)-NH2;
(Aib2, Dhp7, A5c12, Orn15)hгрелин(1-28)-NH2;
(Aib2, Ktp7, A5c12, Orn15)hгрелин(1-28)-NH2;
(Aib2,8, A5c12, Orn15)hгрелин(1-28)-NH2;
(Aib2, 2-Pal9, A5c12, Orn15)hгрелин(1-28)-NH2;
(Aib2, 3-Pal9, A5c12, Orn15)hгрелин(1-28)-NH2;
(Aib2, 4-Pal9, A5c12, Orn15)hгрелин(1-28)-NH2;
(Aib2, Taz9, A5c12, Orn15)hгрелин(1-28)-NH2;
(Aib2, 2-Thi9, A5c12, Orn15)hгрелин(1-28)-NH2;
(Aib2, 2-Fua9, A5c12, Orn15)hгрелин(1-28)-NH2;
(Aib2, Apc9, A5c12, Orn15)hгрелин(1-28)-NH2;
(Aib2,9, A5c12, Orn15)hгрелин(1-28)-NH2;
(Aib2,10, A5c12, Orn15)hгрелин(1-28)-NH2;
(Dap3(октансульфонил), A5c12, Apc16)hгрелин(1-28)-NH2;
(Dab3(октансульфонил), A5c12, Apc16)hгрелин(1-28)-NH2;
(Aib2, А6с5, A5c12, Apc16)hгрелин(1-28)-NH2;
(А6с5, A5c12, Apc16)hгрелин(1-28)-NH2;
(Aib2,6, A5c12, Apc16)hгрелин(1-28)-NH2;
(Aib2, Act6, A5c12, Apc16)hгрелин(1-28)-NH2;
(Aib2, 3-Pal9, A5c12, Apc16)hгрелин(1-28)-NH2;
(Aib2, Dmt7, A5c12, Apc16)hгрелин(1-28)-NH2;
(Aib2, Thz7, A5c12, Apc16)hгрелин(1-28)-NH2;
(Aib2, A5c5,12, Apc16)hгрелин(1-28)-NH2;
(Aib2,5, A5c12, Apc16)hгрелин(1-28)-NH2;
(Aib2, hLeu5, A5c12, Apc16)hгрелин(1-28)-NH2;
(Aib2, Cha5, A5c12, Apc16)hгрелин(1-28)-NH2;
(Aib2,6, A5c12, Apc16)hгрелин(1-28)-NH2;
(Aib2, Thr6, A5c12, Apc16)hгрелин(1-28)-NH2;
(Aib2, Abu6, A5c12, Apc16)hгрелин(1-28)-NH2;
(Aib2, 4-Hyp7, A5c12, Apc16)hгрелин(1-28)-NH2;
(Aib2, Pip7, A5c12, Apc16)hгрелин(1-28)-NH2;
(Aib2, Dhp7, A5c12, Apc16)hгрелин(1-28)-NH2;
(Aib2, Ktp7, A5c12, Apc16)hгрелин(1-28)-NH2;
(Aib2,8, A5c12, Apc16)hгрелин(1-28)-NH2;
(Aib2, 2-Pal9, A5c12, Apc16)hгрелин(1-28)-NH2;
(Aib2, 3-Pal9, A5c12, Apc16)hгрелин(1-28)-NH2;
(Aib2, 4-Pal9, A5c12, Apc16)hгрелин(1-28)-NH2;
(Aib2, Taz9, A5c12, Apc16)hгрелин(1-28)-NH2;
(Aib2, 2-Thi9, A5c12, Apc16)hгрелин(1-28)-NH2;
(Aib2, 2-Fua9, A5c12, Apc16)hгрелин(1-28)-NH2;
(Aib2, Apc9, A5c12, Apc16)hгрелин(1-28)-NH2;
(Aib2,9, A5c12, Apc16)hгрелин(1-28)-NH2;
(Aib2,10, A5c12, Apc16)hгрелин(1-28)-NH2;
(A6c5, A5c12, Orn15)hгрелин(1-28)-NH2;