Способ получения пуриновых рибонуклеозидов и рибонуклеотидов
Иллюстрации
Показать всеИзобретение относится к области биотехнологии, конкретно к бактерии, принадлежащей к роду Bacillus, обладающей способностью к продукции пуриновых нуклеозидов, способу получения пуринового нуклеозида и способу получения пуринового нуклеотида. В способе используют бактерию, принадлежащую к роду Bacillus, модифицированную таким образом, что в ней инактивирован ген, кодирующий 3-гексулозо-6-фосфатсинтазу. Способ включает культивирование данной бактерии в питательной среде. После чего осуществляют выделение указанного пуринового нуклеозида из культуральной жидкости. Предложенное изобретение позволяет увеличить продукцию пуриновых нуклеозидов, таких как инозин, ксантозин, гуанозин или аденозин. 3 н. и 6 з.п. ф-лы, 2 ил., 2 табл.
Реферат
Область техники
Настоящее изобретение относится к микробиологической промышленности, конкретно к способу продукции пуриновых рибонуклеозидов, представляющих ценность в качестве сырья для синтеза пуриновых нуклеотидов. В способе используется бактерия Bacillus, модифицированная таким образом, что экспрессия гена, кодирующего 3-гексулозо-6-фосфатсинтазу, в модифицированной бактерии ослаблена.
Описание предшествующего уровня техники
Существуют известные способы ферментативной продукции пуриновых нуклеозидов с использованием ауксотрофных по аденину штаммов. Кроме того, таким штаммам может быть придана устойчивость к различным соединениям, таким как аналоги пурина и сульфагуанидин. Примеры таких штаммов включают различные штаммы, принадлежащие к роду Bacillus (опубликованные патенты Японии Nos. 38-23039 (1963), 54-17033 (1979), 55-2956 (1980) и 55-45199 (1980), выложенная патентная заявка Японии No. 56-162998 (1981), опубликованные патенты Японии Nos. 57-14160 (1982) и 57-41915 (1982) и выложенная патентная заявка Японии No. 59-42895 (1984)), к роду Brevibacterium (опубликованные патенты Японии Nos. 51-5075 (1976) и 58-17592 (1972), и Agric. Biol. Chem., 42, 399 (1978)), к роду Escherichia (международная заявка РСТ WO 9903988) и подобные им.
Традиционное получение таких мутантных штаммов включает мутагенную обработку микроорганизмов, такую как УФ-облучение и обработка нитрозогуанидином (N-метил-N'-нитро-N-нитрозогуанидин), отбор искомого штамма с использованием соответствующей селективной среды. С другой стороны, получение таких мутантных штаммов с использованием методов генной инженерии также практикуется для штаммов, принадлежащих к роду Bacillus (выложенные патентные заявки Японии Nos. 58-158197 (1983), 58-175493 (1983), 59-28470 (1984), 60-156388 (1985), 1-27477 (1989), 1-174385 (1989), 3-58787 (1991), 3-164185 (1991), 5-84067 (1993) и 5-192164 (1993), патент США 7,326,546 (2008)) и к роду Brevibacterium (выложенная патентная заявка Японии No. 63-248394 (1988)). Продуктивность этих штаммов - продуцентов инозина - может быть дополнительно улучшена путем увеличения способности к секреции инозина (патентные заявки РФ 2002101666, 2002104463 и 2002104464).
Рибулозомонофосфатный путь (ribulose monophosphate - RuMP) является одним из метаболических путей для синтеза соединений, содержащих углерод-углеродные связи, из одноуглеродных соединений и этот путь обнаружен во многих метан- и метанолутилизирующих бактериях, известных как метилотрофы. Характерные ферменты этого пути 3-гексулозо-6-феосфатсинтаза (3-гексулозо-6-фосфатсинтаза - HPS) и 6-фосфо-3-гексулоизомераза (6-phospho-3-hexuloisomerase - PHI), которые, как считается, не существуют вне метилотрофов. Однако предполагаемый продукт гена yckG - YckG Bacillus subtilis имеет первичную структуру, сходную с таковой для HPS из метилотрофов. Также было исследовало сходство последовательностей продукта гена yckF - YckF и PHI из метилотрофов и было обнаружено, что гены yckG и yckF из В. subtilis экспрессируют белки с ферментативными активностями HPS и PHI, соответственно. Обе этих активности индуцировались в В. subtilis формальдегидом, что демонстрирует зависимость от гена yckH, но не индуцировались метанолом, формиатом и метиламином. Разрушение обоих генов вызывало умеренную зависимость от формальдегида, что наводит на предположение, что эти ферменты могут функционировать в В. subtilis как система детоксификации для формальдегида. Активная yckG (для HPS)-yckF (для PHI) генная структура (в настоящий момент называемая hxlA-hxlB) обнаружена в не являющихся метилотрофом В. subtilis, изначально сохранившим RuMP путь (Yasueda, H. et al., J. Bacteriology, 181(23), р.7154-7160 (1999)).
Однако в настоящее время отсутствуют сообщения об инактивации гена, кодирующего 3-гексулозо-6-фосфатсинтазу, для улучшения продукции пуриновых рибонуклеозидов.
Описание изобретения
Целью настоящего изобретения является усовершенствование микроорганизма, предназначенного для продукции пуриновых нуклеозидов путем ферментации, и предоставление способа получения нуклеотидов с использованием полученного штамма.
Эта цель была достигнута благодаря обнаружению того факта, что ослабление экспрессии гена, кодирующего гексулозо-6-фосфатсинтазу, может приводить к увеличению продукции пуриновых нуклеозидов, таких как инозин, ксантозин, гуанозин или аденозин.
Настоящее изобретение предоставляет бактерию, принадлежащую к роду Bacillus, конкретно Bacillus subtilis и Bacillus amyloliquefaciens, обладающую повышенной способностью к продукции пуриновых нуклеозидов.
Целью настоящего изобретения является предоставление бактерии, принадлежащей к роду Bacillus, способной к продукции пуриновых нуклеозидов, отличающейся тем, что указанная бактерия модифицирована таким образом, что экспрессия гена, кодирующего 3-гексулозо-6-фосфатсинтазу, в указанной бактерии ослаблена.
Также целью настоящего изобретения является предоставление описанной выше бактерии, отличающейся тем, что указанная экспрессия ослаблена за счет инактивации указанного гена.
Также целью настоящего изобретения является предоставление описанной выше бактерии, отличающейся тем, что указанным геном, кодирующим 3-гексулозо-6-фосфатсинтазу, является ген hxlA.
Также целью настоящего изобретения является предоставление описанной выше бактерии, отличающейся тем, что указанной бактерией является бактерия В. subtilis.
Также целью настоящего изобретения является предоставление описанной выше бактерии, отличающейся тем, что указанной бактерией является бактерия В. amyloliquefaciens.
Также целью настоящего изобретения является предоставление описанной выше бактерии, отличающейся тем, что указанный пуриновый нуклеозид выбран из группы, состоящей из инозина, ксантозина, гуанозина и аденозина.
Также целью настоящего изобретения является предоставление способа получения пуринового нуклеозида, включающего культивирование описанной выше бактерии в питательной среде, приводящее к секреции указанного пуринового нуклеозида в указанную питательную среду, и выделение указанного пуринового нуклеотида из культуральной жидкости.
Также целью настоящего изобретения является предоставление описанного выше способа продукции пуринового нуклеозида, отличающегося тем, что указанный пуриновый нуклеозид выбран из группы, состоящей из инозина, ксантозина, гуанозина и аденозина.
Также целью настоящего изобретения является предоставление способа продукции пуринового нуклеозида, включающего культивирование описанной выше бактерии в питательной среде, приводящее к секреции указанного пуринового нуклеозида в указанную питательную среду, выделение указанного пуринового нуклеозида из культуральной жидкости, фосфорилирование указанного пуринового нуклеозида и выделение пуринового нуклеотида.
Также целью настоящего изобретения является предоставление описанного выше способа продукции пуринового нуклеотида, отличающегося тем, что пуриновый нуклеотид выбран из группы, состоящей из 5'-инозиновой кислоты, ксантозин-5'-фосфата, 5'-гуаниловой кислоты и 5'-адениловой кислоты.
Настоящее изобретение более подробно будет описано ниже.
Наилучший способ осуществления настоящего изобретения
1. Бактерия согласно настоящему изобретению
Бактерия согласно настоящему изобретению способна к продукции пуринового нуклеозида и модифицирована таким образом, что экспрессия гена, кодирующего 3-гексулозо-6-фосфатсинтазу, в указанной бактерии ослаблена. Бактерия принадлежит к роду Bacillus.
Примеры микроорганизмов, принадлежащих к роду Bacillus, которые можно использовать в настоящем изобретении, включают Bacillus subtilis subsp. subtilis strain 168 (В. subtilis 168) или Bacillus amyloliquefaciens (B. amyloliquefaciens). Бактерии В. amyloliquefaciens - довольно гетерогенные виды. Известен ряд штаммов В. amyloliquefaciens: SB, Т, Р, W, F, N, K и Н (Welker N.E., Campbell L.L., Unrelatedness of Bacillus amyloliquefaciens and Bacillus subtilis. J. BacterioL, 94:1124-1130, 1967). Недавно из растений выделили штаммы Bacillus, которые можно рассматривать как отдельный экотип В. amyloliquefaciens (Reva et al., Taxonomic characterization and plant colonizing abilities of some bacteria related to Bacillus amyloliquefaciens and Bacillus subtilis. FEMS Microbiol. Ecol., 48:249-259, 2004). Определена нуклеотидная последовательность одного из штаммов, В. amyloliquefaciens FZB42 (Chen et al.. Comparative analysis of the complete genome sequence of the plant growth-promoting bacterium Bacillus amyloliquefaciens FZB42. Nat. Biotechnol., 25:1007-1014, 2007).
Примеры бактерий, принадлежащих к роду Bacillus, также включают следующие виды: Bacillus licheniformis, Bacillus pumilis, Bacillus megaterium, Bacillus brevis, Bacillus polymixa, Bacillus stearothermophilus.
Кроме уже упомянутых свойств бактерии настоящего изобретения могут обладать другими характерными свойствами, такими как потребность в различных питательных веществах, устойчивость к антибиотику, чувствительность к антибиотику, что не выходит за рамки настоящего изобретения.
Фраза "пуриновый нуклеозид", как она используется здесь, включает инозин, ксантозин, гуанозин и аденозин, предпочтительно инозин.
Фраза "способность к продукции пуринового нуклеозида", используемая здесь, означает способность синтезировать и накапливать пуриновый нуклеозид в питательной среде. Фраза "бактерия способна к продукции пуринового нуклеозида" означает, что бактерия, принадлежащая к роду Bacillus, способна синтезировать и накапливать в среде пурины, такие как пуриновые нуклеозиды, в количестве большем, чем штамм дикого типа или немодифицированный штамм В. subtilis, такой как В. subtilis 168. Предпочтительно эта фраза означает, что микроорганизм способен синтезировать и накапливать в питательной среде не менее 10 мг/л, более предпочтительно не менее 50 мг/л инозина, ксантозина, гуанозина или/и аденозина.
Термин "активность 3-гексулозо-6-фосфатсинтазы (HPS)" означает активность, катализирующую реакцию образования D-арабино-3-гексулозо-6-фосфата путем Mg2+-зависимой альдольной конденсации формальдегида с рибулозо-5-фосфатом. Активность HPS можно измерить так, как описано Yasueda, H. et al., (J. Bacteriology, 181(23), р.7154-7160(1999)).
Ген, кодирующий HPS из Bacillus subtilis, более конкретно ген hxlA (синоним - yckG) из Bacillus subtilis subsp. subtilis штамма 168, известен (нуклеотиды, комплементарные нуклеотидам с 374725 по 375357 в последовательности с инвентарным номером NC_000964 в базе данных GenBank). Ген hxlA В. subtilis расположен на хромосоме между генами hxlB и hxlR. Нуклеотидная последовательность гена В. subtilis hxlA и аминокислотная последовательность, кодируемая геном hxlA, приведены в Перечне последовательностей под номерами 1 (SEQ ID NO:1) и 2 (SEQ ID NO:2), соответственно.
Ген, кодирующий HPS из Bacillus amyloliquefaciens, более конкретно ген hxlA Bacillus amyloliquefaciens штамма FZB42, известен (нуклеотиды, комплементарные нуклеотидам с 340797 по 341432 в последовательности с инвентарным номером NC_009725 в базе данных GenBank). Ген hxlA из В. amyloliquefaciens расположен на хромосоме между генами hxlB и hxlR. Нуклеотидная последовательность гена hxlA из В. amyloliquefaciens и аминокислотная последовательность, кодируемая геном hxlA, приведены в Перечне последовательностей под номерами 3 (SEQ ID NO:3) и 4 (SEQ ID NO:4) соответственно.
Обычно ген перед введением в бактерию следует клонировать в векторе, способном функционировать в бактерии, принадлежащей к роду Bacillus. Для этих целей можно использовать челночные векторы: pHY300PLK, pMWMX1, pLF22, pKS1. Замена гена дикого типа мутантным геном происходит благодаря гомологичной рекомбинации.
Поскольку у представителей различных штаммов рода Bacillus возможны некоторые различия в нуклеотидных последовательностях, понятие инактивируемого гена hxlA не ограничивается генами, последовательности которых приведены в Перечне последовательностей под номерами SEQ ID NO:1 и SEQ ID NO:3, но также может включать и гены, гомологичные SEQ ID NO:1 и SEQ ID NO:3, кодирующие вариант белка HPS. Термин "вариант белка HPS", используемый в настоящем изобретении, означает белок с изменениями в последовательности, будь то делеции, вставки, добавления или замены аминокислот, в котором сохраняется активность белка HPS. Число изменений в варианте белка зависит от положения или типа аминокислотного остатка в третичной структуре белка. Оно может быть от 1 до 30, предпочтительно от 1 до 15, более предпочтительно от 1 до 5 в SEQ ID NO:2 и SEQ ID No:4. Данные изменения в вариантах могут иметь место в областях, не критичных для функции белка. Данные изменения возможны потому, что некоторые аминокислоты имеют высокую гомологию друг другу, поэтому такие изменения не влияют на третичную структуру или активность. Следовательно, вариант белка, кодируемого геном hxlA, может быть представлен белками с гомологией не менее 80%, предпочтительно, не менее 90%, и, наиболее предпочтительно, не менее 95%, по отношению к полным аминокислотным последовательностям, приведенным в Перечне последовательностей под номерами SEQ ID NO:2 и SEQ ID NO:4, при условии, что до инактивации гена hxlA сохраняется активность белка HPS.
Гомология между двумя аминокислотными последовательностями может быть определена с использованием известных методов, например компьютерной программы BLAST 2.0, которая считает три параметра: число аминокислот, идентичность и сходство.
Кроме того, ген hxlA может быть вариантом, который гибридизуется в жестких условиях с нуклеотидной последовательностью, приведенной в Перечне последовательностей под номерами SEQ ID NO:1 или SEQ ID NO:3, или с зондом, который может быть синтезирован на основе указанной нуклеотидной последовательности, при условии, что до инактивации он кодирует функциональный белок HPS. «Жесткие условия» включают такие условия, при которых специфические гибриды, например гибриды с гомологией не менее 60%, предпочтительно не менее 70%, более предпочтительно не менее 80%, еще более предпочтительно не менее 90% и наиболее предпочтительно не менее 95%, образуются, а неспецифические гибриды, например гибриды с меньшей гомологией, чем указано выше, - не образуются. Практическим примером жестких условий является однократная отмывка, предпочтительно двух- или трехкратная, при концентрации солей 1×SSC, 0.1% SDS, предпочтительно 0.1×SSC, 0.1% SDS, при 60°C. Продолжительность отмывки зависит от типа используемой для блоттинга мембраны и, как правило, такова, как рекомендовано производителем. Например, рекомендуемая продолжительность отмывки для нейлоновой мембраны Hybond™ N+ (Amersham) при строгих условиях - 15 минут. Предпочтительна двух- и трехкратная отмывка. Длина зонда может быть выбрана в зависимости от условий гибридизации, в данном конкретном случае она может быть около 100-1000 п.н.
Экспрессия гена hxlA может быть ослаблена путем введения в гены на хромосоме таких мутаций, что внутриклеточная активность кодируемого геном белка уменьшена по сравнению с таковой в немодифицированном штамме. Такой мутацией гена может быть замена одного или более оснований для аминокислотной замены в кодируемом геном белке («миссенс»-мутация), введение стоп-кодона («нонсенс»-мутация), делеция одного или более оснований для сдвига рамки считывания, вставка гена устойчивости к антибиотику или деления гена либо его части (J. Biol. Chem., 1997, 272 (13): 8611-8617, J. Antimicrobial Chemotherapy, 2000, 46: 793-96). Экспрессия гена chaC или оперона chaBC также может быть ослаблена модификацией экспрессии регуляторных последовательностей, таких как промотор, последовательность Shine-Dalgamo (SD) и т.д.
Например, могут применяться следующие методы для введения мутаций путем генной рекомбинации. Конструируется мутантный ген, кодирующий мутантный белок со сниженной активностью, и бактерия для ее модификации трансформируется фрагментом ДНК, содержащим мутантный ген. Затем нативный ген на хромосоме замещается гомологичной рекомбинацией мутантным геном, отбирается полученный штамм. Такое замещение гена с использованием гомологичной рекомбинации может быть проведено методом с использованием линейной ДНК, известный как "Red-зависимая интеграция" или "интеграция посредством Red-системы" (Datsenko, K.A., Wanner, B.L., Proc.Natl.Acad.Sci.USA, 97, 12, 6640-6645(2000), заявка РСТ WO 2005/010175), или методом с использованием плазмиды, репликация которой чувствительна к температуре (патент США 6,303,383 или патентная заявка Японии JP 05-007491A). Далее введение сайт-специфической мутации путем замещения гена с использованием вышеупомянутой гомологичной рекомбинации может также быть осуществлено с использованием плазмиды с пониженной способностью к репликации в клетке хозяина.
Экспрессия гена также может быть ослаблена вставкой транспозона или IS фактора в кодирующую область гена (патент США 5,175,107), или традиционными методами, такими как мутагенез с использованием УФ-излучения или обработка нитрозогуанидином (N-метил-N'-нитро-N-нитрозогуанидин).
Инактивация гена также может быть осуществлена такими традиционными методами, как мутагенез с использованием УФ-излучения или обработка нитрозогуанидином (N-метил-N'-нитро-N-нитрозогуанидин), сайт-специфический мутагенез, разрушение гена с использованием гомологичной рекомбинации или/и мутагенеза за счет вставки-делеции.
Бактерия согласно настоящему изобретению может быть получена путем ослабления экспрессии гена, кодирующего HPS в бактерии, уже обладающей способностью к продукции пуринового нуклеозида. С другой стороны, бактерия согласно настоящему изобретению может быть получена путем придания бактерии, в которой экспрессия гена, кодирующего HPS, уже ослаблена, способности к продукции пуринового нуклеозида.
Пример родительского штамма, принадлежащего к роду Bacillus, который может быть использован в настоящем изобретении, - штамм-продуцент инозина В. subtilis KMBS375 (KMBS375: Ppur*-Δatt ΔpurA ΔpurR ΔpupG ΔdeoD guaB24; см. Справочный пример). Другие родительские штаммы, принадлежащие к роду Bacillus, которые могут использоваться в настоящем изобретении, включают штамм В. subtilis AJ12707 (FERM Р-12951) (патентная заявка Японии JP6113876A2), штамм В. subtilis AJ3772 (FERM P-2555) (патентная заявка Японии JP62014794A2), Bacillus pumilus NA-1102 (FERM BP-289), Bacillus subtilis NA-6011 (FERM BP-291), Bacillus subtilis G1136A (ATCC No. 19222) (патент США 3,575,809), реидентифицированный как Bacillus amyloliquefaciens AJ1991, депонированный 3 октября 2005 г. в ВКПМ как Bacillus amyloliquefaciens G1136A (VKPM В-8994), 13 октября 2006 г. было осуществлено международное депонирование штамма, Bacillus subtilis NA-6012 (FERM BP-292) (патент США 4,701,413), В. pumilis Gottheil No. 3218 (ATCC No. 21005) (патент США 3,616,206), штамм В. amyloliquefaciens AS115-7 (VKPM B-6134) (патент РФ 2003678) и подобные им. Также может использоваться штамм В. subtilis KMBS16. Этот штамм является производным известного штамма В. subtilis 168 trpC2 с мутациями, введенными в ген purr, кодирующий репрессор пурина (purR::spc), ген purA, кодирующий сукцинил-АМФ-синтазу (purA::erm) и ген deoD, кодирующий пуриннуклеозидфосфорилазу (deoD::kan) (патентная заявка РФ 2002103333, патент США 7,326,546, 2008).
Бактерия согласно настоящему изобретению может быть дополнительно улучшена путем усиления экспрессии одного или нескольких генов, вовлеченных в биосинтез пурина. Примеры таких генов включают оперон pur из В. subtilis (Ebbole D.J. and Zaikin H. J. Biol. Chem., 262: 8274-87 (1987), Bacillus subtilis and Its Closest Relatives, Editor in Chief: A.L. Sonenshein, ASM Press, Washington D.C., 2002). Описан штамм - продуцент инозина В. subtilis с модифицированной регуляторной областью оперона pur (патент США 7,326,546, 2008).
Методы приготовления плазмидной ДНК, рестрикции и лигирования ДНК, трансформации, выбора нуклеотидов в качестве праймера и т.п. могут быть обычными методами, известными специалисту в этой области. Эти методы описаны в Sambrook, J., Fritsch, E.F., and Maniatis, Т., "Molecular Cloning: A Laboratory Manual, Third Edition", Cold Spring Harbor Laboratory Press (2001), и т.п.
2. Способ продукции нуклеозидов
Способ настоящего изобретения включает способ продукции нуклеозида, такого как инозин и/или гуанозин, включающий стадии культивирования бактерии настоящего изобретения в питательной среде для продукции и накапливания нуклеозида в среде и выделение нуклеозида из культуральной жидкости.
В настоящем изобретении культивирование бактерии, выделение нуклеозидов из культуральной жидкости и ее очистка и т.п. может быть осуществлено способом, подобным традиционным способам ферментации, в которых с использованием микроорганизма получают нуклеозид. Питательная среда для продукции пуринового нуклеозида может быть обычной средой, содержащей источник углерода, источник азота, неорганические ионы, органические компоненты и другие необходимые компоненты. В качестве источника углерода можно использовать сахариды, такие как глюкоза, лактоза, галактоза, фруктоза, арабиноза, мальтоза, ксилоза, трегалоза, рибоза и гидролизаты крахмала; спирты, такие как глицерин, маннитол и сорбитол; органические кислоты, такие как глюконовая кислота, фумаровая кислота, лимонная кислота, янтарная кислота и т.п. В качестве источника азота можно использовать неорганические аммонийные соли, такие как сульфат аммония, хлорид аммония и фосфат аммония; органический азот, такой как гидролизаты соевых бобов; аммиачный газ; водный раствор аммиака и т.д. Желательно, чтобы витамины, такие как витамин B1, необходимые вещества, например органические добавки, такие как нуклеиновые кислоты, аденин и РНК, или дрожжевой экстракт и т.п. могли присутствовать в соответствующих или даже в минимальных количествах. Кроме того, при необходимости могут быть добавлены малые количества фосфата кальция, сульфата магния, ионы железа, ионы марганца и т.п.
Выращивание осуществляется предпочтительно в аэробных условиях в течение 16-72 часов, поддерживают температуру культивирования 30-45°C, рН 5-8. рН можно регулировать с использованием неорганических или органических кислых или щелочных веществ, таких как аммиачный газ.
После выращивания твердые остатки, такие как клетки, могут быть удалены из культуральной жидкости методом центрифугирования или фильтрацией через мембрану, а затем целевой пуриновый нуклеозид может быть выделен из культуральной жидкости и очищен с использованием любой комбинации традиционных методов, таких как ионообменная хроматография и осаждение.
3. Способ продукции пуриновых нуклеотидов
Способ продукции пуриновых нуклеотидов включает стадии выращивания бактерии настоящего изобретения в питательной среде, приводящего к секреции бактерией пуринового нуклеозида в питательную среду, фосфорилирования полученного пуринового нуклеозида и выделения пуринового нуклеотида. Кроме того, способ 5'-инозиновой кислоты включает стадии выращивания бактерии настоящего изобретения в питательной среде, приводящего к секреции инозина в питательную среду, фосфорилирования инозина и выделения 5'-инозиновой кислоты. Кроме того, способ продукции 5'-ксантиловой кислоты включает стадии выращивания бактерии настоящего изобретения в питательной среде, приводящего к секреции ксантозина в питательную среду, фосфорилирования инозина и выделения 5'-ксантиловой кислоты. Кроме того, способ продукции 5'-гуаниловой кислоты включает стадии выращивания бактерии настоящего изобретения в питательной среде, приводящего к секреции гуанозина в питательную среду, фосфорилирования гуанозина и выделения 5'-гуаниловой кислоты. И способ продукции 5'-гуаниловой кислоты включает стадии выращивания бактерии настоящего изобретения в питательной среде, позволяющего секрецию ксантозина в питательную среду, фосфорилирования ксантозина, аминирования 5'-ксантиловой кислоты и выделения 5'-гуаниловой кислоты.
В настоящем изобретении выращивание бактерии, выделение инозина из питательной среды и очистка и т.п. могут быть осуществлены сходным образом с традиционными способами ферментации, при которых получают инозин с использованием микроорганизма. Кроме того, в настоящем изобретении стадии фосфорилирования инозина и выделения 5'-инозиновой кислоты могут быть осуществлены традиционными способами ферментации, при которых пуриновый нуклеотид, такой как 5'-инозиновая кислота, образуется из пуринового нуклеозида, такого как инозин.
Фосфорилирование пуринового нуклеозида может быть ферментативным, с использованием различных фосфатаз, нуклеозидкиназ или нуклеозидфосфотрансфераз или химическим с использованием фосфорилирующих агентов, таких как POCl3 и т.п. Можно использовать фосфатазу, способную катализировать С-5'-селективный перенос фосфорильной группы пирофосфата к нуклеозидам (Mihara et. al. Phosphorylation of nucleosides by the mutated acid phosphatase from Morganella morganii. Appl. Environ. Microbiol., 66:2811-2816 (2000)), или кислую фосфатазу, использующую в качестве донора фосфорной кислоты полифосфорную кислоту (соли), фенилфосфорную кислоту (соли) или карбамилфосфорную кислоту (соли) (WO 9637603 A1), или подобные им. Также в качестве примера фосфатазы можно использовать фосфатазу, катализирующую перенос фосфорильной группы на С-2', 3' или 5' нуклеотида с использованием в качестве субстрата п-нитрофенилфосфата (Mitsugi, K., et al. Agric. Biol. Chem., 28, 586-600 (1964)), неорганического фосфата (выложенная патентная заявка Японии No. JP42-1186) или ацетилфосфата (выложенная патентная заявка Японии No. JP61-41555), или подобные ей. В качестве примера нуклеозидкиназы можно использовать нуклеозидкиназу, гуанозин/инозинкиназу Е.coli (Mori, H. et. al. Cloning of a guanosine-inosine kinase gene of Escherichia coli and characterization of the purified gene product. J. Bacteriol. 177:4921-4926 (1995); WO 9108286) или подобные им. В качестве примера нуклеозидфосфотрансферазы можно использовать нуклеозидфосфотрансферазу, описанную Hammer-Jespersen, K. (Nucleoside catabolism, p.203-258. In A Munch-Petesen (ed.), Metabolism of nucleotides, nucleosides, and nucleobases in microorganism. 1980, Academic Press, New York) или подобные им. Химическое фосфорилирование можно провести с использованием таких агентов как POCl3 (Yoshikawa, K. et. al. Studies of phosphorylation. III. Selective phosphorylation of unprotected nucleosides. Bull. Chem. Soc. Jpn. 42:3505-3508 (1969)) или подобных.
Аминирование 5'-ксантиловой кислоты может быть ферментативным с использованием, например, ГМФ-синтетеазы Е.coli (Fujio et. al. High level of expression of XMP aminase in Escherichia coli and its application for the industrial production of 5'-guanylic acid. Biosci. Biotech. Biochem. 1997, 61:840-845; EP0251489B1).
Краткое описание чертежей
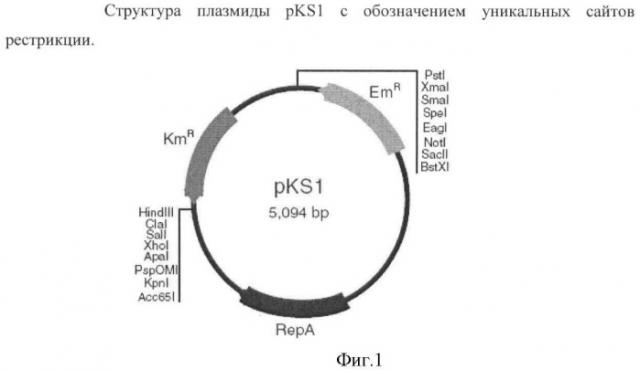
На Фиг.1 изображена структура плазмиды pKS1 с обозначением уникальных сайтов рестрикции.
Наилучший способ осуществления настоящего изобретения
Настоящее изобретение будет более подробно описано ниже со ссылкой на следующие не ограничивающие настоящее изобретение Примеры.
Пример 1. Конструирование штамма с инактивированным геном hxlA
Для инактивации гена hxlA на хромосоме В. subtilis KMBS375 (конструирование штамма KMBS375 описано в Справочном примере) клонировали области, локализованные перед геном hxlA и после него, по двум сайтам плазмиды pKS1 (Shatalin K.Y. and Neyfakh A.A., FEMS Microbiology Letters, 245:315-9 (2005)) (Fig.1). Амплифицировали фрагмент величиной 886 п.н., кодирующий область перед геном hxlA, в ПЦР с использованием праймеров P1 (SEQ ID NO:5) и Р2 (SEQ ID NO:6) и хромосомной ДНК В. subtilis KMBS375 в качестве матрицы. Праймеры Р1 и Р2 содержат сайты узнавания для эндонуклеаз SacII и PstI, соответственно. Амплифицировали фрагмент величиной 923 п.н., кодирующий область после гена hxlA, в ПЦР с использованием праймеров Р3 (SEQ ID NO:7) и Р4 (SEQ ID NO:8) и хромосомной ДНК В. subtilis KMBS375 в качестве матрицы. Праймеры Р3 и Р4 содержат сайты узнавания для эндонуклеаз ClaI и KpnI, соответственно. Очищенный продукт ПЦР, полученный с использованием праймеров Р1 и Р2, обрабатывали эндонуклеазами SacII и PstI и затем клонировали по соответствующим сайтам в плазмиде pKS1. Очищенный продукт ПЦР, полученный с использованием праймеров P3 и P4, обрабатывали эндонуклеазами ClaI и KpnI и также клонировали по соответствующим сайтам в плазмиде pKS1. После клонирования обоих фрагментов плазмиду, содержащую кассету KmR и области, локализованные перед геном hxlA и после него, обрабатывали эндонуклеазами SacII и KpnI и полученный фрагмент (3194 п.н.) субклонировали в нерепликативном векторе pBluescript II KS (Stratagene) из Bacillus. Полученную плазмиду использовали для трансформации В. subtilis KMBS375 и выделили 12 KmR трансформантов. Для подтверждения инактивации гена hxlA в результате интеграции кассеты KmR провели проверочную ПЦР с использованием праймеров Р1 и Р4. Величина фрагмента ДНК, полученного в ПЦР с использованием праймеров Р1 и Р4 с природным аллелем гена hxlA, составляет 2476 п.н.; однако, наличие фрагмента ДНК величиной 3194 п.н. подтверждает интеграцию кассеты KmR в область гена hxlA. В дополнительных проверочных ПЦР с использованием праймеров Р5 (SEQ ID NO:9 - праймер Р5 содержит 20 н., комплементарных области, локализованной в положении - 1013 п.н. от старта трансляции гена hxlA, перед областью, комплементарной праймеру Р1) и Р6 (SEQ ID NO:10 - праймер Р6 содержит 21 н., комплементарный области, локализованной внутри кассеты KmR), наличие полученного в ПЦР фрагмента величиной 1491 п.н. подтверждает интеграцию кассеты KmR в ген hxlA на хромосоме KMBS375. Один из трансформантов KMBS375, содержащий интегрированную кассету KmR, использовали в дальнейшей работе. Этот штамм назван KMBS375Δhxl::Km.
Пример 2. Продукция инозина штаммом В.subtilis KMBS375Δhxl::Km
Для оценки влияния инактивации гена hxlA на продукцию инозина штаммы В. subtilis KMBS375 и KMBS375Δhxl::Km культивировали при 34°С в течение 18 часов в L-бульоне, затем по 0.3 мл культуры инокулировали в 3 мл ферментационной среды в пробирках 20×200 мм и культивировали при 34°С в течение 72 часов на роторной качалке.
Состав ферментационной среды (г/л):
| Глюкоза | 30.0 |
| NH4Cl | 32.0 |
| KH2PO4 | 1.0 |
| MgSO4·7H2O | 0.4 |
| FeSO4·7H2O | 0.01 |
| MnSO4·5H2O | 0.01 |
| Мамено-общий азот | 1.35 |
| DL-Метионин | 0.3 |
| Аденин | 0.1 |
| Гуанин | 0.05 |
| Пеногаситель(adecanol) | 0.5 мл |
| CaCO3 | 50.0 |
| рН | 6.0 (доводится KOH) |
После культивирования определяли количество накопленного в среде инозина методом ВЭЖХ.
Условия проведения ВЭЖХ:
Колонка: Luna С18(2) 250×3 мм, 5u (Phenomenex, USA). Буфер: 2% v/v C2H5OH; 0.8% v/v триэтиламин; 0.5% v/v уксусная кислота (ледяная); рН 4.5. Температура: 30°С. Скорость протока: 0.3 мл/мин. Объем введения: 5 мкл. Детекция: UV 250 нм.
Время удерживания (мин):
| Ксантозин | 13.7 |
| Инозин | 9.6 |
| Гипоксантин | 5.2 |
| Гуанозин | 11.4 |
| Аденозин | 28.2 |
| Таблица 1 | ||||
| Штамм | OD562 | Инозин, г/л | Продуктивность, инозин, г/л/OD | Выход, % |
| KMBS375 | 13.6 | 4.72±0.1 | 0.347±0.006 | 15.73±0.33 |
| KMBS375Δhxl::Km | 12.8 | 5.13±0.01 | 0.401±0.001 | 17.09±0.02 |
Как видно из Таблицы 1, штамм KMBS375Δhxl::Km продуцирует больше инозина, чем штамм KMBS375.
Справочный пример. Конструирование штамма KMBS375
<Конструирование прототрофа В. subtilis 168 Marburg>
В. subtilis 168 Marburg (ATCC6051) является ауксотрофом по Trp вследствие присутствия на хромосоме мутантного аллеля trpC2 (trpC; ген индол-3-глицеринфосфатсинтазы) (Albertini A.M., and A. Galizzi. 1999. The sequence of the trp operon of Bacillus subtilis 168 (trpC2) revisited. Microbiology. 145:3319-3320). Аллель trpC2, в котором три нуклеотида "att" добавлены в положении за 328-м от стартового кодона trpC2, амплифицировали в ПЦР и ввели в В. subtilis 168 Marburg, как изложено далее.
(1) Амплификация аллеля trpC+ allele by recombinant PCR
Для амплификации 5'-конца аллеля trpC+ и предшествующей ему области сконструировали ПЦР-праймеры 34 (SEQ ID NO. 38) и 35 (SEQ ID NO. 39) на основании информации из базы данных GenBank (Accession No. NC_000964) и Albertini and Galizzi (Microbiology. 145:3319-3320).
ПЦР (94°C, 30 секунд; 53°C, 1 минута; 72°C, 1 минута; 30 циклов; Gene Amp PCR System Model 9600 (Perkins Elmer)) проводили с использованием вышеописанных праймеров и хромосомной ДНК штамма В. subtilis 168 Marburg в качестве матрицы для амплификации фрагментов, содержащих область 5'-конца аллеля trpC+ и предшествующую ему область.
Для амплификации 3'-конца аллеля trpC+ и следующей за ним области сконструировали ПЦР-праймеры 36 (SEQ ID NO. 40) и 37 (SEQ ID NO. 41) на основании информации из базы данных GenBank (Accession No. NC_000964) и Albertini and Galizzi (Microbiology. 145:3319-3320).
ПЦР (94°C, 30 секунд; 53°C, 1 минута; 72°C, 1 минута; 30 циклов; Gene Amp PCR System Model 9600 (Perkins Elmer)) проводили с использованием вышеописанных праймеров и хромосомной ДНК штамма В. subtilis 168 Marburg в качестве матрицы для амплификации фрагментов, содержащих область 3'-конца аллеля trpC+ и следующую за ним область.
Для амплификации полной последовательности аллеля trpC+ методом рекомбинантной ДНК два фрагмента ДНК, амплифицированные как описано выше, очищали с использованием MicroSpin Column S-400 (Amersham Pharmacia Biotech), надлежащее количество их смеси использовали в качестве матрицы в ПЦР (94°C, 30 секунд; 55°C, 1 минута; 72°C, 2 минуты; 30 циклов; Gene Amp PCR System Model 9600 (Perkins Elmer)) с использованием праймеров 34 (SEQ ID NO. 38) и 37 (SEQ ID NO. 41), таким образом получили амплифицированный фрагмент (около 1.2 т.п.н.) аллеля trpC+.
(2) Конструирование прототрофа по Trp из штамма В. subtilis 168 Marburg
Целевой фрагмент аллеля trpC+ выделили из геля после электрофореза в агарозном геле. Компетентные клетки штамма В. subtilis 168 Marburg, приготовленные как описано Dubnau and Davidoff-Abelson (Dubnau, D., and R. Davidoff-Abelson, J. Mol. Biol., 56:209-221 (1971)), трансформировали этим фрагментом ДНК и отбирали колонии, способные расти на чашках с минимальной агаризованной средой. Из этих колоний выделили хромосомную ДНК. Амплифицировали фрагменты ДНК методом ПЦР с использованием этой хромосомной ДНК в качестве матрицы и праймеров 34 (SEQ ID NO. 38) и 37 (SEQ ID NO. 41), затем проводили секвенирование для подтверждения вставки трех нуклеотидов в аллель trpC2 и отсутствия других мутаций, который могли появиться в результате ПЦР. Полученный таким образом рекомбинант не был ауксотрофным по Trp; этот штамм был назван KMBS275.
<Конструирование ауксотрофного по His В. subtilis 168 Marburg>
Делецию без нарушения рамки считывания выполнили в гене hisC, кодирующем гистидинолфосфатаминотрансферазу (ΔhisC: делеция 204 нуклеотидов 403-606) и вводили в штамм В. subtilis 168 Marburg (trpC2), как изложено далее.
(1) Амлификация ΔhisC методом рекомбинантной ПЦР
Для амплификации 5'-конца аллеля ΔhisC и предшествующей ему области сконструировали ПЦР-праймеры 38 (SEQ ID NO. 42) и 39 (SEQ ID NO. 43) на основании информации из базы данных GenBank (Accession No. NC_000964). Праймер 38 содержит на 5'-конце сайт EcoRI. Праймер содержит 39 стык, образованный при делеции без нарушения рамки считывания.
ПЦР (94°C, 30 секунд; 55°C, 1 минута; 72°C, 1 минута; 30 циклов; Gene Amp PCR System Model 9600 (Perkins Elmer)) проводили с использованием вышеописанных праймеров и хромосомной ДНК штамма В. subtilis 168 Marburg в качестве матрицы для амплификации фрагментов, содержащих область 5'-конца аллеля ΔhisC и предшествующую ему область.
Для амплификации 3'-конца аллеля ΔhisC и следующей за ним области сконструировали ПЦР-праймеры 40 (SEQ ID NO. 44) и 41 (SEQ ID NO. 45) на основании информации из базы данных GenBank (Accession No. NC_000964). Праймер 40 содержит стык, образованный при делеции без нарушения рамки считывания. Праймер 41 содержит на 5'-конце сайт BamHI.
ПЦР (94°C, 30 секунд; 55°C, 1 минута; 72°C, 1 минута; 30 циклов; Gene Amp PCR System Model 9600 (Perkins Elmer)) проводили с использованием вышеописанных праймеров и хромосомной ДНК штамма В. subtilis 168 Marburg в качестве матрицы для амплификации фрагментов, содержащих область 3'-конца аллеля ΔhisC и следующую за ним область.
Для амплификации полной последовательности ΔhisC методом рекомбинантной ПЦР два фрагмента ДНК, амплифицированные как описано выше, очищали с использованием MicroSpin Column S-400 (Amersham Pharmacia Biotech), надлежащее количество их смеси использовали в качестве матрицы в ПЦР с использованием праймеров 38 (SEQ ID NO. 42) и 41 (SEQ ID NO. 45), провели ПЦР (94°C, 30 секунды; 55°C, 1 минута; 72°C, 2 минуты; 30 циклов; Gene Amp PCR System Model 9600 (Perkins Elmer)), таким образом получили амплифицированный фрагмент (около 1.5 т.п.н.) ΔhisC.
(2) Клонирование гена ΔhisC
Амплифицированный фрагмент обрабатывали рестриктазами EcoRI и BamHI (37°C, в течение ночи) и сепарировали в агарозном геле. Целевой фрагмент выделяли из геля и лигировали с интегративным вектором pJPM1 хромосомы В. subtilis (Mueller, J.P., G. Bukusoglu, and A. L. Sonenshein. 1992. Transcriptional regulation of Bacillus subtilis glucose starvation-inducible genes: control of gsiA by the ComP-ComA signal transduction system. J. Bacteriol. 174:4361-4373), который предварительно обрабатывали теми же ферментами (37°C, 3 часа). Отобрали плазмиду, в которую ген ΔhisC был правильно интегрирован, путем секвенирования подтвердили отсутствие мутаций, которые могли появиться в результате проведения ПЦР, плазмиду назвали pKM186.
(3) Конструирование ауксотрофа по His из штамма В. subtilis 168 Marburg
Компетентные клетки штамма В. subtilis 168 Marburg, приготовленные как описано выше, трансформировали плазмидой рКМ186 и отбирали колонии (рекомбинанты, образовавшиеся в результате единичного кроссинговера), способные расти на чашках с LB-агаром, содержащим 2.5 мкг/мл хлорамфеникола (Cm).
Один из полученных рекомбинантов инокулировали в 10 мл среды LB с добавлением 20 мг/л Gua (среда LB+Gua) и культивировали в течение 2 дней при 37°C. Колонии, проявляющие чувствительность к хлорамфениколу, отбирали с использованием агаризованной среды LB+Gua с/без Cm. Из полученных чувствительных к Cm колоний выделили хромосомную ДНК. Провели ПЦР таким же образом, как описано выше, с использованием праймеров 38 (SEQ ID NO. 42) и 41 (SEQ ID NO. 45). Идентифицировали штаммы, в которых ген hisC на хромосоме замещен разрушенным геном hisC (ΔhisC) в результате двойного рекомбинантного кроссинговера. Полученный штамм-двойной рекомбинант был назван KMBS276 (ΔhisC trpC2).
<Конструирование штамма В. subtilis KMBS375>
1. Конструирование штамма KMBS350 (ΔpurA ΔpurR ΔpupG)
Разрушенные гены pupG, purR и purA (гуанозин/инозинфосфорилаза, репрессор пур