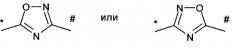Замещенные арилсульфонамиды как противовирусные средства
Иллюстрации
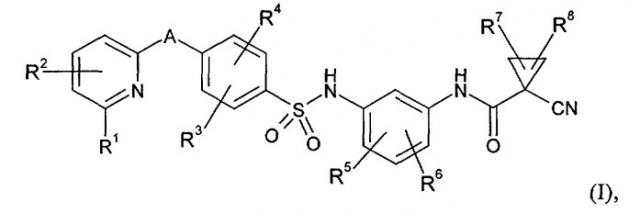
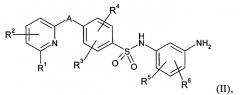
Показать всеИзобретение относится к соединению формулы
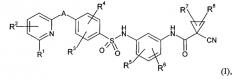
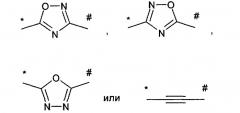
в которой А обозначает группу формулы которой * указывает место связывания с атомом углерода пиридинильного кольца, и # указывает место связывания с атомом углерода фенильного кольца, R1 обозначает аминогруппу или метилкарбониламиногруппу, R2 обозначает водород, R3 обозначает водород, R4 обозначает водород, R5 обозначает водород или галоген, R6 обозначает водород или галоген, R7 обозначает водород, R8 обозначает водород, или одна из его солей, его сольват или сольват его соли, к способу его получения, к лекарственному средству, предназначенному для лечения и/или профилактики вирусных инфекций, на основе этого соединения. Также изобретение относится к применению соединения формулы I для приготовления лекарственного средства и способу борьбы с вирусной инфекцией. Технический результат: получены и описаны новые арилсульфонамиды, которые могут быть полезны в качестве противовирусных средств, предпочтительно для борьбы с цитомегаловирусами. 5 н. и 4 з.п. ф-лы, 2 табл., 1 ил.
Реферат
Настоящее изобретение относится к замещенным арилсульфонамидам и к способам их получения, а также к их применению для приготовления лекарственных средств, предназначенных для лечения и/или профилактики заболеваний, в особенности к применению в качестве противовирусных средств, предпочтительно - для борьбы с цитомегаловирусами.
В WO 02/085869 описаны замещенные арилсульфонамиды в качестве притивовирусных средств, в особенности для борьбы с цитомегаловирусами.
Одним объектом настоящего изобретения являются новые соединения, обладающие такой же или большей противовирусной активностью, улучшенной фармакокинетикой, в особенности большим периодом полувыведения и/или улучшенной доступностью при пероральном введении, пути метаболического разложения которых для людей и обычных подопытных животных, таких как крысы и собаки, значительно не различаются, предназначенные для лечения вирусных инфекционных заболеваний у людей и животных.
Согласно изобретению неожиданно было установлено, что замещенные арилсульфонамиды, описанные в настоящем изобретении, обладают противовирусной активностью, обладают улучшенными фармакокинетическими характеристиками и что пути их метаболического разложения у людей, крыс и собак значительно не различаются.
Настоящее изобретение относится к соединениям формулы
в которой
А обозначает группу формулы
в которой
* указывает место связывания с атомом углерода пиридинильного кольца, и
# указывает место связывания с атомом углерода фенильного кольца,
R1 обозначает водород, аминогруппу или метилкарбониламиногруппу,
R2 обозначает водород или галоген,
R3 обозначает водород, галоген или цианогруппу,
R4 обозначает водород, галоген или цианогруппу,
R5 обозначает водород или галоген,
R6 обозначает водород или галоген,
R7 обозначает водород, галоген или C1-С3-алкил,
R8 обозначает водород, галоген или C1-С3-алкил,
и к их солям, их сольватам и к сольватам их солей.
Соединения, предлагаемые в настоящем изобретении, представляют собой соединения формулы (I) и их соли, сольваты и сольваты солей; а также соединения, указанные ниже, в качестве типичного варианта (вариантов) осуществления и описываемые формулой (I) и (Ia), и их соли сольваты и сольваты солей, если только соединения, указанные ниже и описываемые формулой (I), уже не являются солями, сольватами и сольватами солей.
Соединения, предлагаемые в настоящем изобретении, в зависимости от структуры могут существовать в стереоизомерных формах (энантиомеры, диастереоизомеры). В соответствии с этим настоящее изобретение относится к энантиомерам или диастереоизомерам и соответствующим их смесям. Из таких смесей энантиомеров и/или диастереоизомеров по известным методикам можно выделить стереоизомерно чистые компоненты.
Если соединения, предлагаемые в настоящем изобретении, могут существовать в таутомерных формах, то настоящее изобретение включает все такие таутомерные формы.
Солями, предпочтительными для задач настоящего изобретения, являются физиологически приемлемые соли соединений, предлагаемых в настоящем изобретении. Однако в объем настоящего изобретения включены и соли, которые сами не пригодны для применения в фармацевтике, но которые все же можно использовать, например, для выделения или очистки соединений, предлагаемых в настоящем изобретении.
Физиологически приемлемые соли соединений, предлагаемых в настоящем изобретении, включают соли присоединения неорганических кислот, карбоновых кислот и сульфоновых кислот, например, соли хлористоводородной кислоты, бромистоводородной кислоты, серной кислоты, фосфорной кислоты, метансульфоновой кислоты, этансульфоновой кислоты, толуолсульфоновой кислоты, бензолсульфоновой кислоты, нафталиндисульфоновой кислоты, уксусной кислоты, трифторуксусной кислоты, пропионовой кислоты, молочной кислоты, винной кислоты, яблочной кислоты, лимонной кислоты, фумаровой кислоты, малеиновой кислоты и бензойной кислоты.
Физиологически приемлемые соли соединений, предлагаемых в настоящем изобретении, также включают соли обычных оснований, таких как, например и предпочтительно, соли щелочных металлов (например, соли натрия и калия), соли щелочноземельных металлов (например, соли кальция и магния) и соли аммония, полученные из аммиака или органических аминов, содержащих от 1 до 16 атомов углерода, таких как, например и предпочтительно, этиламин, диэтиламин, триэтиламин, этилдиизопропиламин, моноэтаноламин, диэтаноламин, триэтаноламин, дихлоргексиламин, диметиламиноэтанол, прокаин, дибензиламин, N-метилморфолин, аргинин, лизин, этилендиамин и N-метилпиперидин.
Сольваты, для задач настоящего изобретения, означают такие формы соединений, предлагаемых в настоящем изобретении, которые в твердом или жидком состоянии образуют комплекс путем координации с молекулами растворителя. Гидраты являются особой формой сольватов, в которых координация происходит с водой.
Кроме того, настоящее изобретение также относится к пролекарствам соединений, предлагаемых в настоящем изобретении. Термин "пролекарства" включает соединения, которые сами могут быть биологически активными или неактивными, но во время присутствия в организме превращаются в соединения, предлагаемые в настоящем изобретении (например, вследствие метаболизма или гидролиза).
Для задач настоящего изобретения, если не указано иное, заместители обладают следующими значениями.
Алкил означает линейный или разветвленный алкильный радикал, обычно содержащий от 1 до 3, особенно предпочтительно - от 1 до 2, атомов углерода, например и предпочтительно - метил, этил, н-пропил и изопропил.
Галоген означает фтор, хлор, бром или йод, предпочтительно фтор или хлор.
В формуле группы, которая может представлять собой А, концевые точки соседних отрезков, рядом с которыми находятся значки * или #, обозначают не атом углерода и не группу СН2, а участки связей с атомами, к которым присоединены А.
Предпочтение отдается соединениям формулы (I), в которой
А обозначает группу формулы
в которой
* указывает место связывания с атомом углерода пиридинильного кольца,
и
# указывает место связывания с атомом углерода фенильного кольца,
R1 обозначает водород, аминогруппу или метилкарбониламиногруппу,
R2, R3 и R4 обозначают водород,
R5 обозначает водород или галоген,
R6 обозначает водород или галоген,
R7 и R8 обозначают водород,
и их солям, их сольватам и сольватам их солей.
Предпочтение также отдается соединениям формулы (I), в которой А обозначает группу формулы
в которой
* указывает место связывания с атомом углерода пиридинильного кольца,
и
# указывает место связывания с атомом углерода фенильного кольца,
R1 обозначает аминогруппу или метилкарбониламиногруппу,
R2, R3 и R4 обозначают водород,
R5 обозначает водород,
R6 обозначает водород или галоген,
R7 и R8 обозначают водород,
и их солям, их сольватам и сольватам их солей.
Предпочтение также отдается соединениям формулы (I), в которой
А обозначает группу формулы
в которой
* указывает место связывания с атомом углерода пиридинильного кольца,
и
# указывает место связывания с атомом углерода фенильного кольца.
Предпочтение также отдается соединениям формулы (I), в которой R1 обозначает аминогруппу.
Предпочтение также отдается соединениям формулы (I), в которой R2 обозначает водород.
Предпочтение также отдается соединениям формулы (I), в которой R3 обозначает водород.
Предпочтение также отдается соединениям формулы (I), в которой R4 обозначает водород.
Предпочтение также отдается соединениям формулы (I), в которой R5 обозначает водород.
Предпочтение также отдается соединениям формулы (I), в которой R6 обозначает фтор.
Предпочтение также отдается соединениям формулы (I), в которой R5 обозначает водород и R6 обозначает фтор.
Предпочтение также отдается соединениям формулы (I), в которой R7 обозначает водород.
Предпочтение также отдается соединениям формулы (I), в которой R8 обозначает водород.
Определения радикалов, указанные для соответствующих комбинаций и предпочтительных комбинаций радикалов, при необходимости заменяются на определения радикалов другой комбинации, независимо конкретной комбинации радикалов, которая указана.
Особое предпочтение также отдается комбинациям двух или большего количества указанных выше предпочтительных диапазонов.
Настоящее изобретение также относится к способу получения соединений формулы (I), в которой соединения формулы
в которой
А, R1, R2, R3, R4, R5 и R6 обладают указанными выше значениями,
вводят в реакцию с соединениями формулы
в которой
R7 и R8 обладают указанными выше значениями и
Х1 обозначает галоген, предпочтительно - хлор или бром, или гидроксигруппу.
В случае, если Х1 обозначает галоген, реакцию обычно проводят в инертных растворителях, в присутствии основания, предпочтительно - в температурном диапазоне от 0 до 40°С при атмосферном давлении.
Примеры инертных растворителей включают галогенированные углеводороды, такие как метиленхлорид, трихлорметан или 1,2-дихлорэтан, простые эфиры, такие как диоксан, тетрагидрофуран или 1,2-диметоксиэтан, или другие растворители, такие как ацетон, диметилформамид, диметилацетамид, 2-бутанон или ацетонитрил, предпочтительными являются тетрагидрофуран или метиленхлорид.
Примеры оснований включают карбонаты щелочных металлов, такие как карбонат цезия, карбонат натрия или калия, или органические основания, такие как триалкиламины, например, триэтиламин или диизопропилэтиламин или N-метилморфолин, N-метилпиперидин, 4-диметиламинопиридин или пиридин, предпочтительным является диизопропилэтиламин.
В случае, если Х1 обозначает гидроксигруппу, реакцию обычно проводят в инертных растворителях, в присутствии дегидратирующего реагента, если это целесообразно, то в присутствии основания, предпочтительно - в температурном диапазоне от 0°С до комнатной температуры при атмосферном давлении.
Примеры подходящих для настоящего изобретения дегидратирующих реагентов включают карбодиимиды (КДИ), такие как N,N'-диэтил-, N,N'-дипропил-, N,N'-диизопропил-, N,N'-дициклогексилкарбодиимид, N-(3-диметиламиноизопропил)-N'-этилкарбодиимидгидрохлорид (ЭДХ) (если это целесообразно, то в присутствии пентафторфенола (ПФФ)), N-циклогексилкарбодиимид-N'-пропилоксиметилполистирол (ПС-карбодиимид) или карбонильные соединения, такие как карбонилдиимидазол, или 1,2-оксазолиевые соединения, такие как 2-этил-5-фенил-1,2-оксазолий-3-сульфат или 2-трет-бутил-5-метил-изоксазолийперхлорат, или ациламиновые соединения, такие как 2-этокси-1-этоксикарбонил-1,2-дигидрохинолин, или ангидрид пропанфосфиновой кислоты, или изобутилхлорформиат, или бис(2-оксо-3-оксазолидинил)фосфорилхлорид, или бензотриазолилокси-три(диметиламино)фосфонийгексафторфосфат, или O-(бензотриазол-1-ил)-N,N,N',N'-тетраметилуронийгексафторфосфат (HBTU), 2-(2-оксо-1-(2Н)-пиридил)-1,1,3,3-тетраметилуронийтетрафторборат (TPTU) или O-(7-азабензотриазол-1-ил)-N,N,N',N'-тетраметилуронийгексафторфосфат (HATU), или 1-гидроксибензотриазол (HOBt) или бензотриазол-1-илокситрис-(диметиламино)фосфонийгексафторфосфат (ВОР), или их смеси с основаниями. Конденсацию предпочтительно проводить с использованием HATU.
Примеры оснований включают карбонаты щелочных металлов, такие как, например, карбонаты или гидрокарбонаты натрия или калия, и органические основания, такие как триалкиламины, например, триэтиламин или диизопропилэтиламин, или N-метилморфолин, N-метилпиперидин или 4-диметиламинопиридин, предпочтительным является диизопропилэтиламин.
Примеры инертных растворителей включают галогенированные углеводороды, такие как дихлорметан или трихлорметан, углеводороды, такие как, например, бензол, или нитрометан, диоксан, диметилсульфоксид, диметилформамид, ацетонитрил, тетрагидрофуран, или триамид гексаметилфосфорной кислоты, или смеси растворителей, особенно предпочтительными являются дихлорметан, тетрагидрофуран или диметилформамид.
Соединения формулы (III) являются известными или их можно синтезировать по известным методикам из соответствующих исходных веществ.
Соединения формулы (II) являются известными или их можно получить по реакции соединений формулы
в которой
A, R1, R2, R3, R4, R5 и R6 обладают указанными выше значениями,
с кислотой.
Реакцию обычно проводят в полярных растворителях, предпочтительно в температурном диапазоне от комнатной температуры до температуры кипения растворителя при атмосферном давлении.
Примеры кислот включают хлористоводородную кислоту, бромистоводородную кислоту, серную кислоту, фосфорную кислоту, метансульфоновую кислоту, этансульфоновую кислоту, толуолсульфоновую кислоту, бензолсульфоновую кислоту, нафталинсульфоновую кислоту и трифторуксусную кислоту особенно предпочтительной является хлористоводородная кислота.
Примеры полярных растворителей включают спирты, такие как метанол, этанол, н-пропанол, изопропанол, н-бутанол или трет-бутанол, или тетрагидрофуран, диоксан и уксусную кислоту, или смеси растворителей или растворителя с водой, особенно предпочтительным является этанол.
Соединения формулы (IV) являются известными или их можно получить по методике
[А] реакции соединений формулы
в которой
R3, R4, R5 и R6 обладают указанными выше значениями,
с соединениями формулы
в которой
R1 и R2 обладают указанными выше значениями,
с получением соединений формулы
в которой
R1, R2, R3, R4, R5 и R6 обладают указанными выше значениями,
или
[В] реакции соединений формулы
в которой
R3, R4, R5 и R6 обладают указанными выше значениями,
с соединениями формулы
в которой
R1 и R2 обладают указанными выше значениями,
с получением соединений формулы
в которой
R1, R2, R3, R4, R5 и R6 обладают указанными выше значениями,
или
[С] на первой стадии реакции соединений формулы (Vb) с соединениями формулы
в которой
R1 и R2 обладают указанными выше значениями,
и на второй стадии с оксихлоридом фосфора, с получением соединений формулы
в которой
R1, R2, R3, R4, R5 и R6 обладают указанными выше значениями,
или
[D] реакции соединений формулы
в которой
R3, R4, R5 и R6 обладают указанными выше значениями, и
Х2 обозначает галоген, предпочтительно - йод или бром,
с соединениями формулы
в которой
R1 и R2 обладают указанными выше значениями,
с получением соединений формулы
в которой
R1, R2, R3, R4, R5 и R6 обладают указанными выше значениями.
Во время синтеза аминогруппу группы R1, если это целесообразно, защищают аминогруппой, известной специалисту в данной области техники, такой как, например, ацильная, которую после синтеза удаляют при условиях, известных специалисту в данной области техники.
Соединения формул (IVa), (IVb), (IVc) и (IVd) совместно образуют соединения формулы (IV).
Реакцию в способе [А], [В] и на первой стадии способа [С] обычно проводят в инертных растворителях, в присутствии дегидратирующего реагента, предпочтительно в температурном диапазоне от комнатной температуры до 100°С при атмосферном давлении.
Примеры инертных растворителей включают углеводороды, такие как бензол или толуол, или другие растворители, такие как диоксан, диметилформамид, диметилсульфоксид или ацетонитрил, или смеси растворителей, особенно предпочтительным является диметилформамид.
Примеры дегидратирующих реагентов включают карбодиимиды, такие как N,N'-диэтил-, N,N'-дипропил-, N,N'-диизопропил-, N,N'-дициклогексилкарбодиимид, N-(3-диметиламиноизопропил)-N'-этилкарбодиимидгидрохлорид (ЭДХ) (если это целесообразно, то в присутствии пентафторфенола (ПФФ)), N-циклогексилкарбодиимид-N'-пропилоксиметилполистирол (ПС-карбодиимид) или карбонильные соединения, такие как карбонилдиимидазол, или 1,2-оксазолиевые соединения, такие как 2-этил-5-фенил-1,2-оксазолий-3-сульфат или 2-трет-бутил-5-метил-изоксазолийперхлорат, или ациламиновые соединения, такие как 2-этокси-1-этоксикарбонил-1,2-дигидрохинолин, или ангидрид пропанфосфиновой кислоты, или изобутилхлорформиат, или бис(2-оксо-3-оксазолидинил)фосфорилхлорид, или бензотриазолилокси-три(диметиламино)фосфонийгексафторфосфат, или O-(бензотриазол-1-ил)-N,N,N',N'-тетраметилуронийгексафторфосфат (HBTU), 2-(2-оксо-1-(2Н)-пиридил)-1,1,3,3-тетраметилуронийтетрафторборат (TPTU) или O-(7-азабензотриазол-1-ил)-N,N,N'N'-тетраметилуронийгексафторфосфат (HATU), или 1-гидроксибензотриазол (HOBt) или бензотриазол-1-илокситрис-(диметиламино)фосфонийгексафторфосфат (ВОР), или их смеси с основаниями. Особенно предпочтительным является карбонилдиимидазол.
Реакцию на второй стадии способа [С] обычно проводят в инертных растворителях, предпочтительно в температурном диапазоне от 50 до 100°С при атмосферном давлении. Также можно использовать смеси растворителей, смесь растворителя с POCl3 или чистый POCl3.
Примеры инертных растворителей включают углеводороды, такие как бензол или толуол, или другие растворители, такие как диоксан, диметилсульфоксид, диметилформамид или ацетонитрил, или смеси растворителей, особенно предпочтительными являются диоксан и/или диметилформамид.
Реакцию в способе [D] обычно проводят при условиях реакции Соногашира в атмосфере аргона в инертных и дегазированных растворителях, в присутствии катализатора, если это целесообразно, то в присутствии дополнительного реагента, в присутствии основания и, если это целесообразно, трифенилфосфина, предпочтительно в температурном диапазоне от комнатной температуры до температуры кипения растворителя при атмосферном давлении (R.R. Tykwinski, Angew. Chem. Int. Ed. 2003, 42, 1566-1568, К. Sonogashira in Handbook of organopalladium chemistry for organic synthesis (Ed. E. - I. Negishi), 1133-1178 Wiley-Interscience, New York (2002)).
Примеры катализаторов включают палладиевые катализаторы, обычные для реакции Соногашира, предпочтительными являются такие катализаторы, как, например, три(дибензилиденацетон)дипалладий, дихлорбис(трифенилфосфин)палладий, тетракистрифенилфосфинпалладий(0), ацетат палладия(II), комплекс 1,1'-бис[(бифенилфосфино)ферроцен]палладий-II-хлорида с дихлорметаном состава (1:1).
Примеры дополнительных реагентов включают йодид меди(I) и трифенилфосфин.
Примеры оснований включают аминовые основания, такие как триэтиламин.
Примеры инертных растворителей включают простые эфиры, такие как диоксан, тетрагидрофуран или 1,2-диметоксиэтан, углеводороды, такие как бензол, ксилол или толуол, или другие растворители, такие как нитробензол, диметилформамид, диметилацетамид, диметилсульфоксид или N-метилпирролидон, предпочтительными являются такие растворители, как, например, диметилформамид, диметилацетамид, диметилсульфоксид или 1,2-диметоксиэтан.
Соединения формул (VIa), (VIb), (VIc) и (VId) являются известными или их можно синтезировать по известным методикам из соответствующих исходных веществ.
Соединения формул (Va), (Vb) и (Vc) являются известными или их можно получить по реакции соединений формулы
в которой
R3 и R4 обладают указанными выше значениями, и
Х3 обозначает галоген, предпочтительно - йод или бром, гидроксикарбонил или цианогруппу,
с соединениями формулы
в которой
R5 и R6 обладают указанными выше значениями.
Реакции обычно проводят в инертных растворителях в присутствии основания, предпочтительно в температурном диапазоне от 0 до 40°С при атмосферном давлении.
Примеры инертных растворителей включают спирты, такие как метанол, этанол, н-пропанол, изо-пропанол, н-бутанол или трет-бутанол, или тетрагидрофуран, ацетон, диоксан или пиридин, или смеси растворителей или смеси растворителя с водой, особенно предпочтительными являются тетрагидрофуран или изопропанол с небольшим количеством воды.
Примеры оснований включают ацетат натрия, ацетат калия, карбонат натрия, карбонат калия или аминные основания, такие как триэтиламин или диизопропилэтиламин, особенно предпочтительным является ацетат натрия.
Соединения формул (VII) и (VIII) являются известными или их можно синтезировать по известным методикам из соответствующих исходных веществ.
В альтернативном способе соединения формулы (IV) можно получить с использованием другого порядка реакций синтеза.
Получение соединений, предлагаемых в настоящем изобретении, можно проиллюстрировать с помощью приведенных ниже схем синтеза.
Схема синтеза 1:
Схема синтеза 2:
Схема синтеза 3:
Схема синтеза 4:
Соединения, предлагаемые в настоящем изобретении, характеризуются неожиданным диапазоном эффектов, которые нельзя было предсказать. Они обладают противовирусной активностью по отношению к представителям группы herpes viridae (вирусы герпеса), в частности, по отношению к цитомегаловирусам (ЦМВ) и в особенности по отношению к цитомегаловирусу человека (ЦМВЧ).
Областями показаний, которые можно отметить в качестве примера, являются:
1) Лечение и профилактика инфицирования посредством ЦМВЧ у пациентов со СПИД (синдром приобретенного иммунодефицита) (ретинита, пневмонит, желудочно-кишечных инфекционных заболеваний).
2) Лечение и профилактика инфицирования цитомегаловирусом пациентов, которым трансплантирован костный мозг или орган и у которых развивается часто опасный для жизни вызванный ЦМВЧ пневмонит или энцефалит, или желудочно-кишечные и системные вызванные ЦМВЧ инфекционные заболевания.
3) Лечение и профилактика вызванных ЦМВЧ инфекционных заболеваний у новорожденных и младенцев.
4) Лечение острого инфицирования посредством ЦМВЧ у беременных женщин.
5) Лечение инфицирования посредством ЦМВЧ пациентов с ослабленным иммунитетом, вызванным раком и противораковой терапией.
6) Лечение инфицированных посредством ЦМВЧ страдающих раком пациентов с целью ослабления опосредуемого ЦМВЧ прогрессирования опухоли (см. J. Cinati, et al., FEMC Microbiology Reviews 2004, 28, 59-77).
Настоящее изобретение также относится к применению соединений, предлагаемых в настоящем изобретении, для лечения и/или профилактики заболеваний, в частности инфицирования вирусами, предпочтительно -указанными выше вирусами, и вызванных ими инфекционных заболеваний. Инфицирование вирусами ниже в настоящем изобретении означает и инфицирование вирусами, и заболевание, вызванное инфицированием вирусом.
Настоящее изобретение также относится к применению соединений, предлагаемых в настоящем изобретении, для лечения и/или профилактики заболеваний, предпочтительно указанных выше заболеваний.
Настоящее изобретение также относится к применению соединений, предлагаемых в настоящем изобретении, для приготовления лекарственного средства, предназначенного для лечения и/или профилактики заболеваний, предпочтительно указанных выше заболеваний.
Соединения, предлагаемые в настоящем изобретении, предпочтительно используют для приготовления лекарственных средств, которые являются подходящими для профилактики и/или лечения инфицирования представителями группы herpes viridae (вирусы герпеса), предпочтительно цитомегаловирусом, предпочтительно цитомегаловирусом человека.
Настоящее изобретение также относится к способу лечения и/или профилактики заболеваний, предпочтительно указанных выше заболеваний, с применением противовирусно эффективного количества соединений, предлагаемых в настоящем изобретении.
Настоящее изобретение также относится к лекарственным средствам, включающим по меньшей мере одно соединение, предлагаемое в настоящем изобретении, и по меньшей мере одно или большее количество дополнительных активных ингредиентов, в частности, предназначенным для лечения и/или профилактики указанных выше заболеваний. Активными ингредиентами, подходящими для комбинации, которые, например и предпочтительно, можно отметить, являются: противовирусно активные ингредиенты, такие как вальганцикловир, ганцикловир или ацикловир.
Соединения, предлагаемые в настоящем изобретении, могут воздействовать системно и/или местно. Для этого их можно вводить подходящим путем, таким как, например, пероральный, парентеральный, пульмональный, назальный, сублингвальный, лингвальный, трансбуккальный, ректальный, кожный, чрескожный, конъюнктивальный, ушной или местный, или в виде имплантата или стента.
При этих путях введения соединения, предлагаемые в настоящем изобретении, можно вводить в подходящих препаративных формах.
Для перорального введения подходящими являются препаративные формы, которые воздействуют в соответствии с предшествующим уровнем техники и выделяют соединения, предлагаемые в настоящем изобретении, быстро и/или модифицированным образом и которые включают соединения, предлагаемые в настоящем изобретении, в кристаллической и/или аморфизированной и/или растворенной форме, такие как, например, таблетки (таблетки без покрытия или с покрытием, например, содержащие покрытия, которые устойчивы к воздействию желудочного сока или растворяются с задержкой или нерастворимы и регулируют высвобождение соединения, предлагаемого в настоящем изобретении), таблетки или пленки/облатки, которые быстро распадаются в полости рта, пленки/лиофилизаты, капсулы (например, капсулы из мягкого или твердого желатина), таблетки, покрытие сахаром, гранулы, пеллеты, порошки, эмульсии, суспензии, аэрозоли или растворы.
Парентеральное введение можно проводить без стадии всасывания (например, внутривенно, внутриартериально, внутрикардиально, внутриспинально или внутрилюмбально) или с включением стадии всасывания (например, внутримышечно, подкожно, внутрикожно, чрескожно или внутрибрюшинно). Препаративными формами, подходящими для парентерального введения, являются, в частности, препараты для инъекции и вливания в виде растворов, суспензий, эмульсий, лиофилизатов или стерильных порошков.
Примерами форм, подходящих для других путей введения, являются препаративные формы для ингаляции (в частности, предназначенные для порошковых ингаляторов и распыляющих устройств), капли, растворы, спреи для носа; таблетки, пленки/облатки или капсулы, которые вводят лингвально, сублингвально или трансбуккально, суппозитории, препараты для глаз и ушей, вагинальные капсулы, водные суспезии (лосьоны, микстуры, которые необходимо взбалтывать), липофильные суспензии, мази, кремы, чрескожные терапевтические системы, молочко, пасты, пенки, распыляющиеся порошки, имплантаты или стенты.
Соединения, предлагаемые в настоящем изобретении, можно приготовить в виде стандартных препаративных форм. Это выполняют по известным технологиям, включая смешивание с инертными, нетоксичными, фармацевтически приемлемыми инертными наполнителями. Эти инертные наполнители, в частности, включают носители (например, микрокристаллическая целлюлоза, лактоза, маннит), растворители (например, жидкие полиэтиленгликоли), эмульгаторы и диспергирующие агенты или смачивающие агенты (например, додецилсульфат натрия, полиоксисорбитанолеат), связующие (например, поливинилпирролидон), синтетические и натуральные полимеры (например, альбумин), стабилизаторы (например, антиоксиданты, такие как аскорбиновая кислота), красители (например, неорганические пигменты, такие как оксиды железа) или агенты, меняющие вкус и/или запах.
Настоящее изобретение также относится к лекарственным средствам, которые включают по меньшей мере одно соединение, предлагаемое в настоящем изобретении, обычно совместно с одним или большим количеством инертных, нетоксичных, фармацевтически приемлемых инертных наполнителей, и их применению для указанных выше целей.
Для обеспечения эффективных результатов при внутривенном введении обычно предпочтительно вводить количества, составляющие примерно от 0,001 до 10 мг/кг, предпочтительно - примерно 0,01 до 5 мг/(кг массы тела), и при пероральном введении доза составляет примерно от 0,01 до 25 мг/кг, предпочтительно - от 0,1 до 10 мг/(кг массы тела).
Тем не менее в соответствующих случаях может оказаться целесообразным отклонение от указанных количеств, в особенности в зависимости от массы тела, пути введения, индивидуальной реакции на активный ингредиент, типа препарата и времени введения или интервалов между введениями. Так, в некоторых случаях может оказаться достаточным введение количества, меньшего, чем указанное минимальное, а в других случаях будет необходимо превысить указанное верхнее предельное количество. В случае введения больших количеств может оказаться целесообразным их разделение на несколько отдельных доз, вводимых в течение суток.
Если не указано иное, то выраженные в процентах содержания в описаниях исследований и примерах являются массовыми; выраженные в частях содержания также являются массовыми. Отношение количеств растворителей, соотношения при разбавлении и значения концентраций растворов жидкостей в жидкостях во всех случаях являются объемными.
А. Примеры
Аббревиатуры:
| Boc | трет-бутоксикарбонил |
| CDCl3 | дейтерохлороформ |
| ПХИ | прямая химическая ионизация (в МС) |
| ДХМ | дихлорметан |
| ДИЭА | N,N'-диизопропилэтиламин |
| ДМСО | диметилсульфоксид |
| ДМФ | N,N'-диметилформамид |
| ЭДХ | N-(3-диметиламиноизопропил)-N'- |
| этилкарбодиимидгидрохлорид | |
| ЭА | этилацетат (этиловый эфир уксусной кислоты) |
| ЭУ | ионизация электронным ударом (в МС) |
| ИЭР | ионизация электрораспылением (в МС) |
| Fmoc | 9-флуоренилметоксикарбонил |
| ч | часы |
| ВЭЖХ | высокоэффективная жидкостная хроматография |
| ВВ | высокий вакуум |
| ЖХ-МС | объединенная жидкостная хроматография - масс- |
| Спектроскопия | |
| ДАЛ | диизопропиламид лития |
| мин | минуты |
| МС | масс-спектроскопия |
| МТБЭ | метил-трет-бутиловый эфир |
| ЯМР | спектроскопия ядерного магнитного резонанса |
| Pd-C | палладий на угле |
| РуВОР | 1- |
| бензотриазолилокситрипирролидинофосфонийгексафторфосфат | |
| ОФ-ВЭЖХ | ВЭЖХ с обращенной фазой |
| Rt | время удерживания (в ВЭЖХ) |
| ТГФ | тетрагидрофуран |
Общие методики ЖХ-МС и ВЭЖХ:
Методика 1 (ЖХ-МС): Тип прибора для МС: Micromass ZQ, Тип прибора для ВЭЖХ: HP 1100 series; УФ DAD; колонка: Phenomenex Synergi 2µ. Hydro-ОФ Mercury 20×4 мм; элюент А: 1 л воды + 0,5 мл 50% муравьиной кислоты, элюент В: 1 л ацетонитрила + 0,5 мл 50% муравьиной кислоты; градиентный режим: 0,0 мин 90%А→2,5 мин 30%А→3,0 мин 5%А→4,5 мин 5%А; скорость потока: 0,0 мин 1 мл/мин, 2,5 мин/3,0 мин/4,5 мин 2 мл/мин; печь: 50°С; УФ-детектирование: 210 нм.
Методика 2 (ЖХ-МС): Прибор: Micromass Quattro LCZ с ВЭЖХ Agilent series 1100; колонка: Phenomenex Synergi 2µ. Hydro-ОФ Mercury 20×4 мм; элюент А: 1 л воды + 0,5 мл 50% муравьиной кислоты, элюент В: 1 л ацетонитрила + 0,5 мл 50% муравьиной кислоты; градиентный режим: 0,0 мин 90%А→2,5 мин 30%А→3,0 мин 5%А→4,5 мин 5%А; скорость потока: 0,0 мин 1 мл/мин, 2,5 мин/3,0 мин/4,5 мин 2 мл/мин; печь: 50°С; УФ-детектирование: 208-400 нм.
Методика 3 (ЖХ-МС): Тип прибора для МС: Micromass ZQ; Тип прибора для ВЭЖХ: Waters Alliance 2795; колонка: Phenomenex Synergi 2µ Hydro-ОФ Mercury 20×4 мм; элюент А: 1 л воды + 0,5 мл 50% муравьиной кислоты, элюент В: 1 л ацетонитрила + 0,5 мл 50% муравьиной кислоты; градиентный режим: 0,0 мин 90%А→2,5 мин 30%А→3,0 мин 5%А→4,5 мин 5%А; скорость потока: 0,0 мин 1 мл/мин, 2,5 мин/3,0 мин/4,5 мин 2 мл/мин; печь: 50°С; УФ-детектирование: 210 нм.
Методика 4 (ЖХ-МС): Прибор: Micromass Platform LCZ с ВЭЖХ Agilent series 1100; колонка: Thermo Hypersil GOLD 3µ 20×4 мм; элюент А: 1 л воды + 0,5 мл 50% муравьиной кислоты, элюент В: 1 л ацетонитрила + 0,5 мл 50% муравьиной кислоты; градиентный режим: 0,0 мин 100%А→0,2 мин 100%А→2,9 мин 30%А→3,1 мин 10%А→5,5 мин 10%А; печь: 50°С; скорость потока: 0,8 мл/мин; УФ-детектирование: 210 нм.
Методика 5 (ВЭЖХ): Прибор: HP 1100 с детектированием DAD; колонка: Kromasil ОФ-18, 60×2 мм, 3,5 мкм; элюент А: 5 мл хлорной кислоты/л воды, элюент В: ацетонитрил; градиентный режим: 0 мин 2%В, 0,5 мин 2%В, 4,5 мин 90%В, 9 мин 90%В, 9,2 мин 2%В, 10 мин 2%В; скорость потока: 0,75 мл/мин; oven 30°С; УФ-детектирование: 210 нм.
Методика 6 (ВЭЖХ): Прибор: HP 1100 с детектированием DAD; колонка: Kromasil ОФ-18, 60×2 мм, 3,5 мкм; элюент А: 5 мл хлорной кислоты/л воды, элюент В: ацетонитрил; градиентный режим: 0 мин 2%В, 0,5 мин 2%В, 4,5 мин 90%В, 6,5 мин 90%В, 6,7 мин 2%В, 7,5 мин 2%В; скорость потока: 0,75 мл/мин; oven 30°С; УФ-детектирование: 210 нм.
Методика 7 (ЖХ/МС): Тип прибора для МС: Micromass ZQ; Тип прибора для ВЭЖХ: HP 1100 series; УФ DAD; колонка: Phenomenex Gemini 3µ 30×3,00 мм; элюент А: 1 л воды + 0,5 мл 50% муравьиной кислоты, элюент В: 1 л ацетонитрила + 0,5 мл 50% муравьиной кислоты; градиентный режим: 0,0 мин 90%А→2,5 мин 30%А→3,0 мин 5%А→4,5 мин 5%А; скорость потока: 0,0 мин 1 мл/мин, 2,5 мин/3,0 мин/4,5 мин 2 мл/мин; печь: 50°С; УФ-детектирование: 210 нм.
Исходные соединения
Пример 1А
4-(Бензилтио)бензонитрил
Гидрид натрия (5 г 60% дисперсии в масле) промывают гексаном и сушат в вакууме. Остаток диспергируют в сухом ДМФ (100 мл) при 0°С и в течение 30 мин по каплям прибавляют бензилмеркаптан (14,82 г). Затем реакционную смесь перемешивают в течение 30 мин при комнатной температуре. Осторожно прибавляют 4-фторбензонитрил (14,45 г) и реакционную смесь перемешивают до вступления в реакцию всего исходного вещества (монитроринг с помощью ВЭЖХ, примерно 3 ч). Реакционную смесь выливают в воду со льдом (400 мл) и перемешивают в течение 5 мин. Продукт собирают фильтрованием, промывают водой (три раза) и сушат на фильтре. Неочищенный продукт перекристаллизовывают из циклогексана, собирают фильтрованием и промывают петролейным эфиром и сушат. Получают 23,04 г (86% от теоретического выхода) продукта.
ЖХ-МС (методика I): Rt=2,85 мин
МС (ИЭР): m/z=226 [M+H]+
Пример 2А
4-(Бензилтио)-N'-гидроксибензокарбоксимидамид
4-(Бензилтио)бензонитрил (23,00 г) и гидроксиламингидрохлорид (10,66 г) готовят в сухом этаноле (10 мл) и прибавляют триэтиламин (17 мл). Реакционную смесь сначала перемешивают в течение 30 мин при 50°С и затем кипятят с обратным холодильником в течение 2 ч. Затем прибавляют воду, пока раствор не станет мутным. Реакционную смесь охлаждают до комнатной температуры и полученное твердое вещество собирают фильтрованием. Твердое вещество промы