Метод определения распределения веществ в сферических аморфных наночастицах
Иллюстрации
Показать всеИзобретение относится к области биотехнологии, более конкретно к средствам доставки лекарственных и диагностических субстанций на основе наночастиц, и описывает метод определения распределения веществ, в том числе лекарственных и диагностических субстанций, в сферических аморфных наночастицах с помощью последовательной экстракции дисперсий этих частиц органическими растворителями несмешивающимися с дисперсионной средой и ограниченно растворяющими материал наночастиц, с последующим определением концентраций высвобожденного вещества в экстрактах. Данный метод позволяет определить функциональные группы на поверхности сферических аморфных наночастиц и, как результат, направления возможных модификаций их поверхности. 1 табл., 3 ил.
Реферат
Изобретение относится к нанотехнологии, а именно к средствам доставки лекарственных и диагностических субстанций на основе наночастиц, которые обладают рядом преимуществ (например, повышение биодоступности субстанции, снижение побочных эффектов, увеличение времени действия) по сравнению с традиционными лекарственными формами.
Существуют разнообразные способы, применяемые для определения функциональных групп на поверхности наночастиц. Среди них: титриметрия (Аверко-Антонович И.Ю., Бикмуллин Р.Т. Методы исследования структуры и свойств полимеров. КГТУ, Казань, 2002), фотометрический анализ (Дарбре А. Практическая химия белка. Пер. с англ. М., «Мир», 1989), флуоресцентный анализ (Udenfriend S., Stein S., Böhlen P., Dairman W., Leimgruber W., Weigele М. Fluorescamine: a reagent for assay of amino acids, peptides, proteins, and primary amines in the picomole range. Science. 1972. Vol.178. P.871-872). Выбор метода, как правило, зависит от необходимой точности определения. Общим существенным недостатком вышеперечисленных методов является необходимость подобрать реагент, специфично реагирующий с функциональными группами на поверхности наночастиц.
Техническим результатом предлагаемого изобретения является определение распределения веществ в сферических аморфных наночастиц (САНЧ).
Настоящее изобретение описывает экономичный и эффективный метод определения распределения веществ, в том числе лекарственных и диагностических субстанций внутри САНЧ, отличающийся от ранее предложенных своей универсальностью.
Данный технический результат достигается предлагаемым методом, заключающимся в последовательной экстракции дисперсий САНЧ органическими растворителями: несмешивающимися с дисперсионной средой, и ограниченно растворяющих материал САНЧ, с последующим определением концентраций высвобожденного вещества в экстрактах.
Метод был опробован на двух видах САНЧ: САНЧ, полученных из смеси лупановых тритерпеноидов (СЛТ, бетулин 60±5%, лупеол 30±4%, 3-О-кофеат бетулина 9±3%) и САНЧ, полученных из индивидуального лупанового тритерпеноида - 3-О-кофеата бетулина (КБ). Для определения распределения веществ в САНЧ, в наночастицы загружали следующие субстанции: 3-метоксибензантрон (МБА, 0.5% мас.) и доксорубицин (ДОКСО, 2%, 5%, 10% мас.).
Пример 1. Распределение 3-метоксибензантрона в САНЧ, полученных из смеси лупановых тритерпеноидов.
Дисперсии САНЧ и САНЧ с загруженными веществами получали по методу (А.Н.Бастрич и др. Солюбилизация тритерпеноидов лупанового ряда, выделенных из бересты. Биотехнология, 2008, 6, С.51-59).
Распределение МБА в САНЧ определяли следующим образом.
5 мл свежеприготовленной дисперсии САНЧ с включенным МБА (0.5% мас.) смешивали с 1 мл толуола и встряхивали в течение 30 с. Через 10 мин органический слой заменяли 1 мл свежей порции толуола. Концентрацию высвобожденного МБА (% мас.) в толуольных экстрактах определяли спектрофотометрически в максимуме поглощения при 418 нм, используя формулу в соответствии с законом Бугера-Ламберта-Бэра:
W=(Aλ·Vp·M/ξλ·l·mв)·100%,
где Aλ - оптическая плотность; Vp - объем органического растворителя (1 мл); M - молярная масса вещества; ξλ - коэффициент молярного поглощения при длине волны λ; l - длина оптического пути; mв - начальная масса вещества в САНЧ.
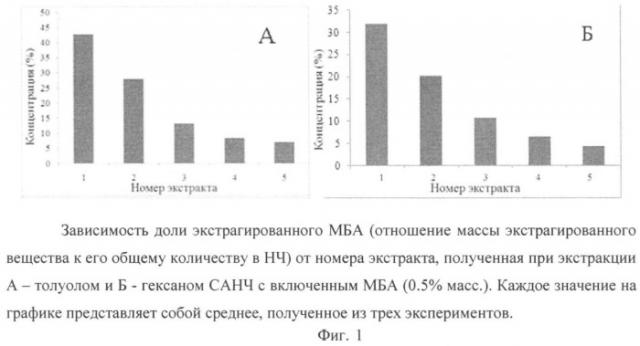
На фиг.1 представлен график зависимости концентрации экстрагированного МБА от номера экстракта. За 30 с экстракции дисперсий САНЧ толуолом устанавливается равновесие - образуется насыщенный раствор материала наночастиц в толуоле, значит, если МБА в монодисперсных САНЧ распределяется равномерно, то при каждой экстракции растворяется одинаковая масса МБА. В этом случае, график зависимости концентрации экстрагированного МБА от номера экстракта должен быть параллельным оси абсцисс. Сравнением экспериментальных и гипотетических данных определяем, что МБА распределяется неравномерно, концентрируется в поверхностных слоях САНЧ, поскольку толщина экстрагируемого слоя САНЧ не превышает 10 нм (по данным динамического светорассеивания).
Пример 2. Распределение 3-метоксибензантрона в САНЧ, полученных из смеси лупановых тритерпеноидов.
Распределение МБА в САНЧ определяли методом, описанным в примере 1, с той разницей, что в качестве экстрагента был использован гексан (фиг.1Б). Из фиг.1 (А и Б) видно, что данные о распределении МБА в САНЧЛТ полученные с использованием разных экстрагентов, толуола и гексана, схожи. Различие в концентрации экстрагированного МБА при каждой экстракции объясняется разной растворяющей способностью двух растворителей. По причине высокой летучести гексана, толуол предпочтителен.
Пример 3. Распределение доксорубицина в САНЧ, полученных из смеси лупановых тритерпеноидов.
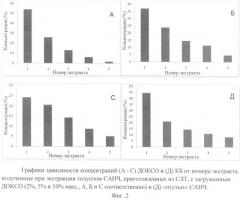
Распределение ДОКСО, загруженного в САНЧ, определяли по методу, описанному в примере 1, с той разницей, что концентрацию высвобожденного ДОКСО определяли при 480 нм. Включение ДОКСО в возрастающих концентрациях (2%, 5% и 10% мас.) в САНЧ привело к снижению доли ДОКСО, содержавшегося в первом экстракте почти втрое (фиг.2А, Б и С). Это означает, что увеличение доли ДОКСО загружаемого в САНЧ, способствует его более равномерному распределению.
Пример 4. Распределение 3-О-кофеат бетулина в САНЧ, полученных из смеси лупановых тритерпеноидов.
Смесь лупановых тритерпеноидов состоит из трех гидрофобных компонентов, из них только 3-О-кофеат бетулина поглощает в электронных спектрах, что дает возможность определить его распределение внутри САНЧ. Методом, описанным в примере 1, с той разницей, что максимум поглощения КБ находится при 325 нм, определили, КБ распределяется в САНЧ аналогично МБА и ДОКСО, т.е. локализуется в поверхностных слоях САНЧ (фиг.2Д).
Результаты экспериментов, проиллюстрированных в примерах 1, 3, 4, сведены в таблице.
| Таблица | |||||
| Параметры распределения исследуемых субстанций внутри САНЧ, образованных из смеси лупановых тритерпеноидов. | |||||
| Название субстанции | 3-метоксибензантрон (0.5% мас.) | 3-О-кофеат бетулина | доксорубицин | ||
| (2% мас.) | (5% мас.) | (10% мас.) | |||
| Концентрация вещества в первом экстракте (% масс.) | 43 | 45 | 54 | 37 | 24 |
Пример 5. Распределение 3-метоксибензантрона в САНЧ, полученных из 3-О-кофеат бетулина.
Методом, описанным в примере 1, определили, что загруженный МБА (0.5% мас.) внутри САНЧ, образованных из КБ, распределяется наиболее равномерно из всех изученных веществ (фиг.3).
Предложенный метод позволяет определить функциональные группы на поверхности сферических аморфных наночастиц и, как результат, направления возможных модификаций их поверхности.
Метод определения распределения веществ в сферических аморфных наночастицах с помощью нескольких последовательных экстракций данного вещества из дисперсии наночастиц равными объемами органического растворителя, не смешивающегося с дисперсионной средой и ограниченно растворяющего материал сферических аморфных наночастиц с последующим определением концентраций экстрагированного вещества в экстрактах при каждой экстракции и оценкой равномерности распределения вещества в наночастицах по указанным концентрациям.