Аналоги грелина
Иллюстрации
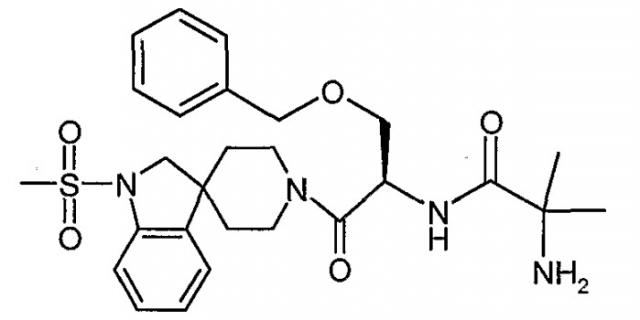
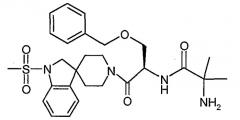
Показать все(57) Изобретение относится к пептидным аналогам формул (I) и (II):
(R2R3)-A1-A2-A3-A4-A5-A6-A7-A8-A9-A10-A11-A12-A13-A14-A15-A16-A17-A18-A19-A20-A21-A22-A23-A24-A25-A26-A27-A28-R1, в которых определения А1-А28 и R2-R3 приведены в описании для каждой из формул (I) и (II), их фармацевтически приемлемым солям и фармацевтическим композициям, содержащим эффективное количество соединения формулы (I), которые могут быть использованы в способе подавления секреции гормона роста и в способе скрининга соединения, способного связываться с рецептором GHS. 6 н. и 25 з.п.ф-лы, 6 табл.
Реферат
Уровень техники
Область техники, к которой относится изобретение
Настоящее изобретение относится к пептидиловым аналогам, которые обладают агонистической или антагонистической активностью грелина, и их терапевтическим применениям.
Описание предшествующего уровня техники
Грелин, недавно открытый, стимулирующий аппетит гормон, продуцируется в виде препрогормона, который процессируется протеолитическим путем с образованием пептида следующей последовательности: H-Gly-Ser-Ser-Phe-Leu-Ser-Pro-Glu-His-Gln-Arg-Val-Gln-Gln-Arg-Lys-Glu-Ser-Lys-Lys-Pro-Pro-Ala-Lys-Leu-Gln-Pro-Arg-NH2 (Kojima M. et al., Nature (1999), 402 (6762): 656-60). Грелин продуцируется эпителиальными клетками дна желудка, и его функция заключается в стимуляции аппетита; его концентрация повышается перед едой и снижается после.
Известны природные структуры грелина от нескольких видов млекопитающих и видов, не относящихся к млекопитающим (Kaiya H. et al., J. Biol. Chem. (2001), 276 (44): 40441-8; и международная заявка на патент PCT/JP00/04907 [WO 01/07475]). Ядро, имеющееся в грелине, ответственно за активность, наблюдаемую на рецепторе GHS, которое содержит четыре N-концевых аминокислоты, где серин в положении 3 в норме модифицирован н-октановой кислотой. В дополнение к ацилированию октановой кислотой нативный грелин может также подвергаться ацилированию н-декановой кислотой (Kaiya H. et al., J. Biol. Chem. (2001), 276 (44): 40441-8).
Концентрации грелина у индивидуумов с ожирением ниже по сравнению с худыми людьми и концентрации грелина повышаются в течение суток от полуночи к рассвету у более худых людей, на основании чего можно предположить о его недостаточности в крови у индивидуумов с ожирением (Yildiz B.O. et al., Proc. Natl. Acad. Sci. USA (2004), 101 (28): 10434-9). Было установлено, что у людей, страдающих таким нарушением приема пищи, как нервно-психическая анорексия, и пациентов с индуцированной злокачественным заболеванием кахексией имеются более высокие концентрации грелина в плазме крови (Garcia J.M., et al., J. Clin. Endocrin. Metab. (2005), 90 (5): 2920-6).
У животных и людей грелин эффективно стимулирует секрецию гормона роста (GH) из передней части гипофиза, в основном на уровне гипоталамуса, посредством его взаимодействия с рецептором вещества, стимулирующего секрецию гормона роста (GHS) (GHS-R) (Ukkola O. et al., Ann. Med. (2002), 34 (2): 102-8 и Kojima M. et al., Nature (1999), 402 (6762): 656-60). Способность грелина высвобождать GH опосредуется активацией рецепторов GHS в гипофизе и в основном на уровне гипоталамуса (Kojima M. et al., Nature (1999), 402 (6762): 656-60).
Перед установлением того, что грелин является природным лигандом рецептора GHS, было известно, что пульсирующее высвобождение GH из соматотропов гипофиза регулируется под действием двух нейропептидов гипоталамуса: высвобождающего GH гормона (GHRH) и соматостатина. GHRH стимулирует высвобождение GH, в то время как соматостатин ингибирует секрецию GH (Frohman L.A. et al., Endocrinol. Rev. (1986), 7 (3): 223-53 и Strobl J.S. et al., Pharmacology Review (1994) 46: 1-34). Вероятно, грелин усиливает активность GHRH-секретирующих нейронов, одновременно действуя в качестве функционального антагониста соматостатина (Ghigo E. et al., Eur. J. Endocri. (1997): 136 (5): 445-60).
Высвобождение GH из соматотропов гипофиза может также регулироваться GH-высвобождающими пептидами (GHRH). Было установлено, что гексапептид His-D-Trp-Ala-Trp-D-Phe-Lys-амид (GHRH-6) высвобождает GH из соматотропов в зависимости от дозы у нескольких видов, включая человека (Bowers C.Y. et al., Endocrinology (1984), 114(5): 1537-45). Результаты последующих химических исследований GHRH-6 привели к установлению других эффективных синтетических веществ, стимулирующих секрецию, таких как GHRР-1, GHRР-2 и гексарелин (Cheng K. et al., Endocrinology (1989), 124(6): 2791-8; Bowers C.Y., Novel GH-releasing Peptides, Molecular and Clinical Advances in Pituitary Disorders, Ed.: Melmed S., Endocrine Research and Education, Inc., Los Angeles, CA, USA (1993), 153-7; и Deghenghi R. et al., Life Science (1994), 54(18): 1321-8). Данные три соединения имеют строение:
GHRР-1 Ala-His-D-(2')-Nal-Ala-Trp-D-Phe-Lys-NH2;
GHRР-2 D-Ala-D-(2')-Nal-Ala-Trp-D-Nal-Lys-NH2; и
гексарелин His-D-2-MeTrp-Ala-Trp-D-Phe-Lys-NH2.
GHS может стимулировать секрецию GH посредством иного механизма чем GHRH (Bowers C.Y. et al., Endocrinology (1984), 114(5): 1537-45; Cheng K. et al., Endocrinology (1989), 124(6) 2791-8; Bowers C.Y., Novel GH-releasing Peptides, Molecular and Clinical Advances in Pituitary Disorders, Ed.: Melmed S., Endocrine Research and Education, Inc., Los Angeles, CA, USA (1993), 153-7; и Deghenghi R. et al., Life Science (1994), 54(18): 1321-8).
Низкая биодоступность (<1%) пептидных GHS при пероральном введении стимулировала поиск соединений, отличных от пептидов, с действием, напоминающим действие GHRР-6 в гипофизе. Сообщалось о нескольких производных бензолактамов и спироинданов, стимулирующих высвобождение GH у различных видов животных, включая людей (Smith R.G. et al., Science (1993), 260(5114): 1640-3; Patchett A.A. et al., Proc. Natl. Acad. Sci. USA (1995), 92(15): 7001-5; Chen M.-H. et al., Bioorg. Mod. Chem. Lett. (1996), 6(18): 2163-8). Конкретным примером спироиндана с небольшой молекулой является МК-0677 (Patchett A.A. et al., Proc. Natl. Acad. Sci. USA (1995), 92(15): 7001-5):
Оказалось, что действие GHS (пептида и непептида) опосредуется специфическим рецептором (Howard A.D. et al., Science (1996), 273(5277): 974-7; и Pong S.S. et al., Mol. Endocrin. (1996), 10(1): 57-61). Данный рецептор находится в гипофизе и гипоталамусе различных видов млекопитающих (GHSR1a) и отличается от рецептора GH-высвобождающего гормона. Рецептор GHS также обнаружен в других областях центральной нервной системы и периферических тканях, например в надпочечниках, щитовидной железе, сердце, легких, почках и мышцах (Chen M.-H. et al., Bioorg. Med. Chem. Letts. (1996), 6(18): 2163-9; Howard A.D. et al., Science (1996), 273(5277): 974-7; Pong S.S. et al., Mol. Endocrin. (1996), 10(1): 57-61; Guan X.-M. et al., Mol. Brain Res. (1997), 48(1): 23-9 и McKee K.K. et al., Genomics (1997), 46(3): 426-34). Сообщалось об усеченном варианте GHSR1a (Howard A.D. et al., Science (1996), 273(5277): 974-7).
Рецептор GHS представляет собой сопряженный с G-белком рецептор. Активирующее действие на рецептор GHS включает деполяризацию и ингибирование калиевых каналов, повышение межклеточных концентраций инозинтрифосфата (IP3) и кратковременное увеличение концентрации внутриклеточного кальция (Pong S.S. et al., Mol. Endocrin. (1996), 10(1): 57-61; Guan X.-M. et al., Mol. Brain Res. (1997), 48(1): 23-9 и McKee K.K. et al., Genomics (1997), 46(3): 426-34).
Молекулы GHS, такие как грелин и его аналоги, имеют различные терапевтические (патент США № 6566337; Inui A., FASEB J. (2004), 18(3): 439-56; Muller E.E. et al., Neurobiol. Aging (2002), 23(5): 907-19; Casanueva F.F. et al., Trends Endocrinol. Metab. (1999), 10(1): 30-8 и Ankerson M. et al., Drug Discovery Today (1999), 4: 497-506) и диагностические применения. Соединения, проявляющие агонистическое действие на рецептор GHS, показаны для лечения недостаточности GH (патенты США № 6861409 и 6967237; и Casanueva F.F. et al., Trends Endocrinol. Metab. (1999), 10(1): 30-8), для увеличения мышечной массы (патенты США № 6861409 и 6967237) и/или физической силы (Ankerson M. et al., Drug Discovery Today (1999), 4: 497-506), повышения плотности костей (патенты США № 6861409, 6967237 и 6251902; и Sibilia V. et al., Growth Horm. IGF Res. (1999), 9(4): 219-27), лечения остеопороза (международная заявка на патент № PCT/IB96/01353 [WO 97/24369] и PCT/IB98/00873 [WO 98/58947] и Casanueva F.F. et al., Trends Endocrinol. Metab. (1999), 10(1): 30-8), при половой дисфункции (патент США № 6967237 и Casanueva F.F. et al., Trends Endocrinol. Metab. (1999), 10(1): 30-8), для лечения сердечно-сосудистого заболевания (международная заявка на патент № PCT/IB96/01353 [WO 97/24369] и PCT/IB98/00873 [WO 98/58947]; патент США № 6251902; De Gennaro Colonna V. et al., Eur. J. Pharmacol. (1997), 334(2-3): 201-7 и Casanueva F.F. et al., Trends Endocrinol. Metab. (1999), 10(1): 30-8), ослабления болей при артрите (Granado M., Am. J. Endo. Metab. (2005), 288: 486-92), профилактики или предупреждения начала развития болезни Альцгеймера (патенты США № 6686359 и 6566337) и/или лечения системной красной волчанки или воспалительного заболевания кишечника, например болезни Крона или язвенного колита (публикация патента США № 2002/0013320).
Аналоги-агонисты грелина могут способствовать увеличению массы тела (патент США № 6967237; Tschop M. et al., Nature (2000), 407(6806): 908-13; и Tschop M. et al., Endocrinology (2002), 143(2): 558-68), что, в свою очередь, можно использовать для поддержания желаемой массы тела (патенты США № 6861409 и 6967237) и/или для восстановления физической функции (патенты США № 6967237 и 6251902; и международная заявка на патент № PCT/IB96/01353 [WO 97/24369]).
Грелин также повышает аппетит (патент США № 6967237; и Okada K. et al., Endocrinology (1996), 137(11): 5155-8). В результате этого грелин часто применяют для лечения пациентов, страдающих некоторыми заболеваниями или нарушениями, или проходящими курс лечения, которые, как правило, сопровождаются нежелательной потерей массы тела, такими как анорексия (патент США № 6967237; и Tschop M. et al., Endocrinology (2002), 143(2): 558-68), булимия (патент США № 6967237), кахексия (патенты США № 6967237 и 6251902), в частности кахексия, вызванная злокачественными заболеваниями (патент США № 6967237; международная заявка на патент № PCT/DK2004/000529 [WO 05/014032]) и Tschop M. et al., Endocrinology (2002), 143(2): 558-68), СПИД (патенты США № 6861409 и 6967237; и Tschop M. et al., Endocrinology (2002), 143(2): 558-68), синдром истощения у ослабленных и пожилых людей (патенты США № 6861409 и 6967237; международная заявка на патент № PCT/IB96/01353 [WO 97/24369]; и Ankerson M. et al., Drug Discovery Today (1999) 4: 497-506) и хроническая почечная недостаточность (Casanueva F.F. et al., Trends Endocri. Metab. (1999), 10(1): 30-8). Виды лечения, как правило, сопровождающиеся потерей массы тела, включают химиотерапию, лучевую терапию, временную или постоянную иммобилизацию и/или диализ (патенты США № 6967237 и 6251902).
Ожирение является важным фактором риска для развития диабета, и большая часть пациентов с инсулиннезависимым сахарным диабетом (иначе обозначенным как «NIDDM») страдают ожирением. Оба заболевания характеризуются повышенными концентрациями инсулина в крови и пониженными уровнями GH. Было показано, что лечение GH у взрослых с недостаточностью GH (Jorgensen J.O. et al., Lancet (1989), 1(8649): 1221-5), женщин с ожирением (Richelsen B. et al., Am. J. Physiol. (1994), 266(2 Pt 1): E211-6) и пожилых людей (Rudman D. et al., Horm. Res. (1991), 36 (suppl 1) приводит к увеличению тканей без жира, массы печени и мышц с одновременным снижением массы жира. Следовательно, введение агониста грелина представляет собой весьма привлекательный вид лечения ожирения для проявления диабетогенного действия GH (патент США № 6251902; Ankerson M. et al., Drug Discovery Today (1999) 4: 497-506; и Casanueva F.F. et al., Trends Endocri. Metab. (1999), 10(1): 30-8). Также грелином можно опосредовано лечить осложнения при диабете, такие как ретинопатия, и/или лечить сердечно-сосудистые заболевания (патент США № 6967237 и публикация заявки на патент США № 2003/0211967).
Парадоксально, но антагонисты грелина можно использовать для снижения массы тела у индивидуумов с ожирением, у которых указанное ожирение возникло не за счет NIDDM (патент США № 6967237 и публикация заявки на патент США № 2003/0211967), а также по некоторым другим указанным показаниям. Соединения, проявляющие антагонистическое действие на рецептор GHS с подавлением секреции GH, например антагонисты грелина, показаны для ингибирования избыточной секреции GH (публикация заявки на патент США № 2002/0187938), для снижения массы тела у субъектов без ожирения (патент США № 6967237), для поддержания идеальной массы тела и/или снижения аппетита (патент США № 6967237). Избыточная масса тела вносит свой вклад в развитие многих заболеваний или состояний, таких как повышенное давление, дислипидемия и сердечно-сосудистые заболевания (публикация заявки на патент США № 2003/0211967 и патент США № 6967237), а также образование желчных камней, остеоартрит (патент США № 6967237), некоторые злокачественные заболевания (публикации заявок на патент США № 2003/0211967 и 2004/0157227; и патент США № 6967237) и синдром Прадера-Вилли (патент США № 6950707; международная заявка на патент № РСТ/US2004/008385 [WO 04/084943]; Haqq A.M. et al., J. Clin. Endocri. Metab. (2003), 88(1):174-8 и Cummings D.E. et al., Nat. Med. (2002), 8(7):643-4). Антагонисты грелина, которые способствуют потере массы тела, будут, следовательно, снижать вероятность развития таких заболеваний или состояний, и/или составлять, по меньшей мере, часть лечения таких заболеваний или состояний. Также было установлено, что антагонисты молекул GHS связываются с онкогенной тканью, результатом чего является снижение количества онкогенных клеток в тканях-мишенях, например, опухолях легких, молочной железы или поджелудочной железы (международная заявка на патент № РСТ/ЕР99/08662 [WO 00/29011]).
Также аналоги веществ, стимулирующих секрецию GH, использовали для усиления подвижности желудочно-кишечного тракта, в частности, у пациентов с пониженной подвижностью желудочно-кишечного тракта в результате послеоперационного илеуса или гастропареза, характерного для начала развития диабета или хронического диабета (патент США № 6548501).
Кроме того, грелин является эффективным при лечении воспаления у млекопитающих (международная заявка на патент № РСТ/US2005/016565 [WO 2005/110463]). В частности, воспаление может быть связано с вирусной, бактериальной, паразитарной или грибковой инфекцией. Вирусные инфекции, которые поддаются лечению грелином, могут включать инфекции, вызванные вирусом герпеса простого типа-1, вирусом герпеса простого типа-2, цитомегаловирусом, вирусом Эпштейна-Барра, вирусом ветряной оспы, человеческим герпесвирусом 6, человеческим герпесвирусом 7, человеческим герпесвирусом 8, вирусом натуральной оспы, вирусом везикулярного стоматита, вирусом гепатита А, вирусом гепатита В, вирусом гепатита С, вирусом гепатита D, вирусом гепатита Е, риновирусом, коронавирусом, вирусом гриппа А, вирусом гриппа В, вирусом кори, полиомавирусом, человеческим папиломавирусом, респираторным синцитиальным вирусом, аденовирусом, вирусом Коксаки, вирусом Денге, вирусом паратита, полиовирусом, вирусом бешенства, вирусом саркомы Руса, вирусом желтой лихорадки, вирусом Эбола, вирусом Марбурга, вирусом лихорадки Ласа, вирусом восточного энцефалита лошадей, вирусом японского энцефалита, вирусом энцефалита Сент-Луис, вирусом лихорадки долины Мюррей, вирусом Западного Нила, вирусом лихорадки долины Рифт, ротавирусом А, ротавирусом В, ротавирусом С, вирусом Синдбис, обезьяним вирусом иммунодефицита, вирусом типа-1 человеческой Т-клеточной лейкемии, гантавирусом, вирусом коревой краснухи, обезьяним вирусом иммунодефицита, вирусом типа-1 иммунодефицита человека и вирусом типа-2 иммунодефицита человека (международная заявка на патент № РСТ/US2005/016565 [WO 2005/110463]).
Бактериальные инфекции, вызывающие воспаление, которые можно лечить грелином (международная заявка на патент № РСТ/US2005/016565 [WO 2005/110463], включают инфекции, вызванные M. tuberculosis, M. bovis, M. bovis штаммом BCG, cубштаммами BCG, M. avium, M. intracellulare, M. africanum, M. kansasii, M. marinum, M. ulcerans, M. avium cубштаммами paratuberculosis, Nocardia asteroides, другими видами Nocardia, Legionella pneumophila, другими видами Legionella, Salmonella typhi, другими видами Salmonella, видами Shigella, Yersinia pestis, Pasteurella haemolytica, Pasteurella multocida, другими видами Pasteurella, Actinobacillus pleuropneumoniaе, Listeria monocytogenes, Listeria ivanovii, Brucella abortus, другими видами Brucella, Cowdria ruminantium, Chlamydia pneumoniae, Chlamydia trachomatis, Chlamydia psittaci, Coxiella burnetti, другими видами Rickettsia, видами Ehrlichia, Staphylococcus aureus, Staphylococcus epidermidis, Streptococcus pyogenes, Streptococcus agalactiae, Bacillus anthracis, Escherichia coli, Vibrio cholerae, видами Campylobacter, Neiserria meningitidis, Neiserria gonorrhea, Pseudomonas aeruginosa, другими видами Pseudomonas, Haemophilus influenzae, Haemophilus ducreyi, другими видами Haemophilus, Clostridium tetani, другими видами Clostridium, Yersinia enterolitica и другими видами Yersinia (международная заявка на патент № РСТ/US2005/016565 [WO 2005/110463]).
Воспаление, поддающееся лечению грелином (международная заявка на патент № РСТ/US2005/016565 [WO 2005/110463]), также может быть вызвано паразитами, включая инфекции, вызванные Toxoplasma gondii, Plasmodium, Trypanosoma brucei, Trypanosoma cruzi, Leishmania, Schistosoma и Entamoeba histolytica, или инфекции, вызванные грибами, такими как Candida albicans, Cryptococcus neoformans, Histoplama capsulatum, Aspergillus fumigatus, Coccidiodes immitis, Paracoccidiodes brasiliensis, Blastomyces dermitidis, Pneomocystis carnii, Penicillium marneffi и Alternaria alternatа (международная заявка на патент № РСТ/US2005/016565 [WO 2005/110463]).
Воспаление, причиной которого является токсичность для печени или отторжение трансплантата, также подвергается лечению грелином (международная заявка на патент № РСТ/US2005/016565 [WO 2005/110463]). Токсичность для печени может быть связана с лечением злокачественного заболевания. В некоторых случаях лечение злокачественного заболевания, такое как химиотерапия, может привести к токсичности для печени. Токсичность для печени, возникшая в результате химиотерапии и апоптоза, может подвергаться лечению введением грелина, агонистов грелина или антагонистов грелина (международная заявка на патент № РСТ/US2005/016565 [WO 2005/110463]).
Воспаление, ассоциированное со злокачественными заболеваниями, также поддается лечению грелином (международная заявка на патент № РСТ/US2005/016565 [WO 2005/110463]). Такие злокачественные заболевания включают лимфому, лейкемию, грибовидный микоз, карциному, аденокарциному, саркому, глиому, бластому, нейробластому, плазмоцитому, гистиоцитому, меланому, аденому, гипоксическую опухоль, миелому, связанную со СПИДом лимфому или связанную со СПИДом саркому, метастазирующую злокачественную опухоль, злокачественную опухоль мочевого пузыря, злокачественную опухоль мозга, злокачественную опухоль нервной системы, глиобластому, злокачественную опухоль яичников (международная заявка на патент № РСТ/АU02/00582 [WO 02/090387] и Gaytan F. et al., J. Clin. Endocri. Metab. (2005), 90(3): 1798-804), рак кожи, злокачественную опухоль печени, плоскоклеточные карциномы ротовой полости, горла, гортани и легких, злокачественную опухоль ободочной кишки, рак шейки матки (международная заявка на патент № РСТ/АU02/00582 [WO 02/090387], злокачественную опухоль молочной железы (международная заявка на патент № РСТ/АU02/00582 [WO 02/090387] и Cassoni P. et al., J. Clin. Endocri. Metab. (2001), 86(4): 1738-45), эпителиальную злокачественную опухоль, злокачественную опухоль почек (Jungwirth A. et al., Proc. Natl. Acad. Sci. USA (1997), 94(11): 5810-3), злокачественную опухоль органов половой и мочевой системы, злокачественную опухоль легких (Ghe C. et al., Endocrinology (2002), 143(2): 484-91), карциному пищевода (Nwokolo C.U. et al., Gut (2003), 52(5): 637-40), карциному головы и шеи (Jozkow P. et al., Head Neck (2005), 27(3): 243-7), злокачественное заболевание крови, рак яичка (Gaytan F. et al., J. Clin. Endocrinol. Metab. (2004), 89(1): 400-9), злокачественную опухоль ободочной и прямой кишки (Dagnaes-Hansen H. et al., Anticancer Res. (2004), 24(6): 3735), злокачественную опухоль простаты (Jeffery P.L., et al., Endocrinology (2002), 172: R7-11) и злокачественную опухоль поджелудочной железы (Volante M. et al., J. Clin. Endocri. Metab. (2002), 87(3): 1300-8) и международная заявка на патент № РСТ/US2005/016565 [WO 2005/110463].
Наконец, было показано, что грелин лечит воспалительные заболевания (международная заявка на патент № РСТ/US2005/016565 [WO 2005/110463]), такие как астма, реактивный артрит, гепатит (Wallace J.D. et al., J. Clin. Endocri. Metab. (2002), 87(6): 2751-9), спондиартрит, синдром Шергена, болезнь Альцгеймера (патенты США № 6686359 и 6566337; и Obermayr R.P. et al., Gerontology (2003), 49(3): 191-5) и атопический дерматит, или воспалительные заболевания, связанные с аутоиммунным заболеванием, такие как системная красная волчанка, ревматоидный артрит (Otero M. et al., Rhеumatology (Oxford) (2004), 43(3): 306-10), системный васкулит, инсулинзависимый сахарный диабет (Nieves-Riviera F. et al., Growth Regul. (1993), 3: 235-44), рассеянный склероз и мышечная дистрофия (публикация патента США № 2003/0139348), экспериментальный аллергический энцефаломиелит (Ikushima H. et al., J. Immunol. (2003), 171: 2769-72), псориаз (Edmondson S.R. et al., Endocri. Rev. (2003), 24(6): 737-64), болезнь Крона (Slonim A.E. et al., N. Engl. J. Med. (2000), 342(22): 1633-7), воспалительное заболевание кишечника (Chen K. et al., Surgery (1997), 121(2): 212-8), язвенный колит, болезнь Аддисона (Arvat E. et al., Neuroendocrinology (1999), 70(3): 200-6), гнездную алопецию, заболевание органов брюшной полости (Peracchi M. et al., Am. J. Gastroenterology (2003), 98(11): 2474-8) и Capristo E. et al., Scand. J. Gastroenterol. (2005), 40(5): 430-6), заболевание щитовидной железы (Riis A.L. et al., J. Clin. Endocrin. Metab. (2003), 88(2): 853-7) и склеродерму. Также воспаление, развившееся в результате ожога, можно лечить грелином, как и воспаление легких (международная заявка на патент № РСТ/US2005/016565 [WO 2005/110463]). Воспаление также может привести к потере аппетита у субъекта, особенно когда воспаление является низкой степени и/или имеет место у пожилого субъекта (международная заявка на патент № РСТ/US2005/016565 [WO 2005/110463]).
Можно также использовать антагонисты грелина для достижения лечебного действия у пациента (публикация патента США № 2002/187938, 2003/0211967 и 2004/0157227; и патент США № 6967237). Например, антагонист грелина можно использовать для уменьшения массы тела или снижения аппетита, для поддержания идеальной массы тела, для лечения ожирения, для контроля диабета, включая его осложнения, такие как ретинопатия, и/или лечения сердечно-сосудистых расстройств. Избыточная масса тела вносит свой вклад в развитие многих заболеваний или состояний, таких как повышенное давление, диабет, дислипидемия и сердечно-сосудистые заболевания, образование желчных камней, остеоартрит и синдром Прадера-Вилли, а также некоторые формы злокачественных опухолей. Снижение массы тела, будет, следовательно, снижать вероятность развития таких заболеваний или составлять часть лечения таких заболеваний.
С учетом широкого ряда лечебных эффектов, которые можно получить при использовании GHS, в данной области имеется потребность в эффективном агонисте или антагонисте молекул аналогов грелина.
Сущность изобретения
Было установлено, что аналоги грелина, в которых аминокислоты в остатках А15, А16, А17, А18, А19 или А20 замещены на Asp(NH-R9), Asp(O-R8), Cys(S-R14), Cys(R15), hCys(S-R14), hCys(R17), Dab(S(O)2-R11), Dap(S(O)2-R10), Glu(NH-R7), Glu(O-R6), Gly(миристил), Ser(C(O)-R4), Thr(C(O)-R5) или HN-CH((CH2)n-N(R12R13))-C(O) или, в частности, Lys(биотинил)17 или Lys(миристил)17, проявляют более высокую аффинность связывания с клеточной мембраной и, как было установлено, более эффективно взаимодействуют со связанными с мембраной рецепторами и, таким образом, являются более сильными в биологическом отношении по сравнению с природным грелином.
В свете данного установленного факта настоящее относится к аналогам грелина, активным на рецепторе GHS, в которых остатки А15, А16, А17, А18, А19 или А20 замещены на Asp(NH-R9), Asp(O-R8), Cys(S-R14), Cys(R15), hCys(S-R16), hCys(R17), Dab(S(O)2-R11), Dap(S(O)2-R10), Glu(NH-R7), Glu(O-R6), Gly(миристил)1, Lys(биотинил)17, Lys(миристил)17, Ser(C(O)-R4), Thr(C(O)-R5) или HN-CH((CH2)n-N(R12R13))-C(O).
Таким образом, первый аспект настоящего изобретения относится к аналогу грелина формулы (I), в которой первая аминокислота, перечисленная при определении А1-А28, представляет аминокислоту, обнаруженную в таком же положении в последовательности природного грелина, т.е. H-Gly-Ser-Ser-Phe-Leu-Ser-Pro-Glu-His-Gln-Arg-Val-Gln-Gln-Arg-Lys-Glu-Ser-Lys-Lys-Pro-Pro-Ala-Lys-Leu-Gln-Pro-Arg-NH2;
(R2R3)-A1-A2-A3-A4-A5-A6-A7-A8-A9-A10-A11-A12-A13-A14-A15-A16-A17-A18-A19-A20-A21-A22-A23-A24-A25-A26-A27-A28-R1
(I)
в которой:
A1 представляет Gly, Acс, Aib, Ala или β-Ala;
A2 представляет Ser, Abu, Acс, Act, Aib, Ala, Ava, Thr или Val;
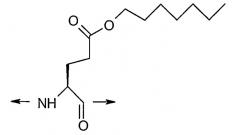
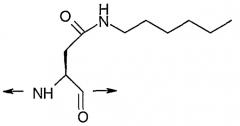
A3 представляет Ser, Asp(NH-R9), Asp(O-R8), Cys(S-R14), Dab(S(О)2-R11), Dap(S(O)2-R10), Glu(NH-R7), Glu(O-R6), Ser(C(O)-R4), Thr(C(O)-R5) или HN-CH((CH2)n-N(R12R13))-C(O);
A4 представляет Phe, Acс, Aic, Cha, 2-Fua, 1-Nal, 2-Nal, 2-Pal, 3-Pal, 4-Pal, hPhe, (X1,X2,X3,X4,X5)Phe, Taz, 2-Thi, 3-Thi, Trp или Tyr;
A5 представляет Leu, Abu, Acс, Aib, Ala, Cha, Ile, hLeu, Nle, Nva, Phe, Tle или Val;
A6 представляет Ser, Abu, Acс, Act, Aib, Ala, Gly, Thr или Val;
A7 представляет Pro, Dhp, Dmt, 3-Hyp, 4-Hyp, Inc, Ktp, Oic, Pip, Thz или Tic;
A8 представляет Glu, Acс, Aib, Arg, Asn, Asp, Dab, Dap, Gln, Lys, Orn или HN-CH((CH2)n-N(R12R13))-C(O);
A9 представляет His, Acс, Apс, Aib, 2-Fua, 2-Pal, 3-Pal, 4-Pal, (X1,X2,X3,X4,X5)Phe, Taz, 2-Thi или 3-Thi;
A10 представляет Gln, Acс, Aib, Asn, Asp или Glu;
A11 представляет Arg, Apс, hArg, Dab, Dap, Lys, Orn или HN-CH((CH2)n-N(R12R13))-C(O);
A12 представляет Val, Abu, Acс, Aib, Ala, Cha, Gly, Ile, Leu, Nle, Nva или Tle;
A13 представляет Gln, Acс, Aib, Asn, Asp или Glu;
A14 представляет Gln, Acс, Aib, Asn, Asp или Glu;
A15 представляет Arg, Acс, Aib, Apc, hArg, Dab, Dap, Lys, Orn, Asp(NH-R9), Asp(O-R8), Cys(S-R14), Cys(R15), hCys(S-R16), hCys(R17), Dab(S(O)2-R11), Dap(S(O)2-R10), Glu(NH-R7), Glu(O-R6), Ser(C(O)-R4), Thr(C(O)-R5) или HN-CH((CH2)n-N(R12R13))-C(O);
A16 представляет Lys, Acс, Aib, Apc, Arg, hArg, Dab, Dap, Orn, Asp(NH-R9), Asp(O-R8), Cys(S-R14), Cys(R15), hCys(S-R16), hCys(R17), Dab(S(O)2-R11), Dap(S(O)2-R10), Glu(NH-R7), Glu(O-R6), Ser(C(O)-R4), Thr(C(O)-R5), HN-CH((CH2)n-N(R12R13))-C(O) или подвергается делеции;
A17 представляет Glu, Arg, Asn, Asp, Dab, Dap, Gln, Lys, Orn, Asp(NH-R9), Asp(О-R8), Cys(S-R14), Cys(R15), hCys(S-R16), hCys(R17), Dab(S(O)2-R11), Dap(S(O)2-R10), Glu(NH-R7), Glu(O-R6), Lys(биотинил), Ser(C(O)-R4), Thr(C(O)-R5), HN-CH((CH2)n-N(R12R13))-C(O) или подвергается делеции;
A18 представляет Ser, Abu, Acс, Act, Aib, Ala, Thr, Val, Asp(NH-R9), Asp(O-R8), Cys(S-R14), Cys(R15), hCys(S-R16), hCys(R17), Dab(S(O)2-R11), Dap(S(O)2-R10), Glu(NH-R7), Glu(O-R6), Ser(C(O)-R4), Thr(C(O)-R5), HN-CH((CH2)n-N(R12R13))-C(O) или подвергается делеции;
A19 представляет Lys, Acс, Aib, Apс, Arg, hArg, Dab, Dap, Orn, Asp(NH-R9), Asp(O-R8), Cys(S-R14), Cys(R15), hCys(S-R16), hCys(R17), Dab(S(O)2-R11), Dap(S(O)2-R10), Glu(NH-R7), Glu(O-R6), Ser(C(O)-R4), Thr(C(O)-R5), HN-CH((CH2)n-N(R12R13))-C(O) или подвергается делеции;
A20 представляет Lys, Acс, Aib, Apс, Arg, hArg, Dab, Dap, Orn, Asp(NH-R9), Asp(O-R8), Cys(S-R14), Cys(R15), hCys(S-R16), hCys(R17), Dab(S(O)2-R11), Dap(S(O)2-R10), Glu(NH-R7), Glu(O-R6), Ser(C(O)-R4), Thr(C(O)-R5), HN-CH((CH2)n-N(R12R13))-C(O) или подвергается делеции;
A21 представляет Pro, Dhp, Dmt, 3-Hyp, 4-Hyp, Inc, Ktp, Oic, Pip, Thz, Tic или подвергается делеции;
A22 представляет Pro, Dhp, Dmt, 3-Hyp, 4-Hyp, Inc, Ktp, Oic, Pip, Thz, Tic или подвергается делеции;
A23 представляет Abu, Acс, Act, Aib, Ala, Apс, Gly, Nva, Val или подвергается делеции;
A24 представляет Lys, Acс, Aib, Apс, Arg, hArg, Dab, Dap, Orn, HN-CH((CH2)n-N(R12R13))-C(O) или подвергается делеции;
A25 представляет Leu, Abu, Acс, Aib, Ala, Cha, Ile, hLeu, Nle, Nva, Phe, Tle, Val или подвергается делеции;
A26 представляет Gln, Aib, Asn, Asp, Glu или подвергается делеции;
A27 представляет Pro, Dhp, Dmt, 3-Hyp, 4-Hyp, Inc, Ktp, Oic, Pip, Thz, Tic или подвергается делеции;
A28 представляет Acс, Aib, Apc, Arg, hArg, Dab, Dap, Lys, Orn, HN-CH((CH2)n-N(R12R13))-C(O) или подвергается делеции;
R1 представляет -OH, -NH2, -(C1-C30)алкокси или NH-X6-CH2-Z0, где X6 представляет (C1-C12)алкил или (C2-C12)алкенил, и Z0 представляет -H, -OH, -CO2H или -C(O)-NH2;
каждый из R2 и R3 независимо в каждом случае выбран из группы, состоящей из Н, (С1-С30)алкила, (С1-С30)гетероалкила, (С1-С30)ацила, (С2-С30)алкенила, (С2-С30)алкинила, арил(С1-С30)алкила, арил(С1-С30)ацила, замещенного (С1-С30)алкила, замещенного (С1-С30)гетероалкила, замещенного (С2-С30)ацила, замещенного (С2-С30)алкенила, замещенного арил(С1-С30)алкила, замещенного (С2-С30)алкинила и замещенного арил(С1-С30)ацила;
каждый из R4, R5, R6, R7, R8, R9, R10, R11, R14, R15, R16 и R17 независимо в каждом случае выбран из группы, состоящей из (С1-С40)алкила, (С2-С40)алкенила, замещенного (С1-С40)алкила, замещенного (С2-С40)алкенила, алкиларила, замещенного алкиларила, арила и замещенного арила;
каждый из R12 и R13 независимо в каждом случае выбран из группы, состоящей из Н, (С1-С40)алкила, (С1-С40)гетероалкила, (С1-С40)ацила, (С2-С40)алкенила, (С2-С40)алкинила, арил(С1-С40)алкила, арил(С1-С40)ацила, замещенного (С1-С40)алкила, замещенного (С1-С40)гетероалкила, замещенного (С1-С40)ацила, замещенного (С2-С40)алкенила, замещенного (С2-С40)алкинила, замещенного арил(С1-С40)алкила, замещенного арил(С1-С40)ацила, (С1-С40)алкилсульфонила, -C(NH)-NH2 и биотинила;
n независимо в каждом случае представляет 1, 2, 3, 4 или 5;
каждый из Х1, Х2, Х3, Х4 и Х5 в каждом случае независимо выбран из группы, состоящей из Н, F, Cl, Br, I, (C1-C10)алкила, замещенного (C1-C10)алкила, арила, замещенного арила, ОН, NH2, NO2 и CN;
при условии, что:
(I) когда R2 представляет (С1-С30)ацил, арил(С1-С30)ацил, замещенный (С2-С30)ацил или замещенный арил(С1-С30)ацил, то тогда R3 является Н, (С1-С30)алкилом, (С1-С30)гетероалкилом, (С2-С30)алкенилом, арил(С1-С30)алкилом, замещенным (С1-С30)алкилом, замещенным (С1-С30)гетероалкилом, замещенным (С2-С30)алкенилом, замещенным (С2-С30)алкинилом или замещенным арил(С1-С30)алкилом;
(II) когда R12 представляет (С1-С40)ацил, арил(С1-С40)ацил, замещенный (С1-С40)ацил, замещенный арил(С1-С40)ацил, (С1-С40)алкилсульфонил или -C(NH)-NH2, то тогда R13 является Н или (С1-С40)алкилом, (С1-С40)гетероалкилом, (С2-С40)алкенилом, (С2-С40)алкинилом, арил(С1-С40)алкилом, замещенным (С1-С40)алкилом, замещенным (С1-С40)гетероалкилом, замещенным (С2-С40)алкенилом, замещенным (С2-С40)алкинилом или замещенным арил(С1-С40)алкилом;
(III) по меньшей мере, одна из A15, A16, A17, A18, A19 или A20 указанного аналога грелина выбрана из группы, состоящей из Asp(NH-R9), Asp(O-R8), Cys(S-R14), Cys(R15), hCys(S-R16), hCys(R17), Dab(S(O)2-R11), Dap(S(O)2-R10), Glu(NH-R7), Glu(O-R6), Ser(C(O)-R4), Thr(C(O)-R5) или HN-CH((CH2)n-N(R12R13))-C(O); и
(IV) когда любая группа, состоящая из A15, A16, A17, A19 или A20, представляет HN-CH((CH2)n-N(R12R13))-C(O), то тогда R12 должен быть биотинилом;
или его фармацевтически приемлемой соли.
Предпочтительной группой соединений формулы (I), названной группой соединений 1, является та, где:
А1 представляет Gly или Aib;
А2 представляет Ser, Act, Aib, Ava или A5c;
А3 представляет Dab(S(O)2-R11), Dap(S(O)2-R10), Glu(NH-R7), Glu(O-R6) или Ser(C(O)-R4) ;
А4 представляет Phe;
А5 представляет Leu, Acc, Aib, Cha или hLeu;
А6 представляет Ser, Abu, Act, Aib или Thr;
А7 представляет Pro, Dhp, Dmt, 4-Hyp, Ktp, Pip или Thz;
А8 представляет Glu или Aib;
А9 представляет His, Aib, Apc, 2-Fua, 2-Pal, 3-Pal, 4-Pal, Taz или 2-Thi;
А10 представляет Gln или Aib;
А11 представляет Arg;
А12 представляет Val или Acc;
А13 представляет Gln;
А14 представляет Gln;
А15 представляет Arg или Orn;
А16 представляет Lys или Apc;
А17 представляет Glu;
А18 представляет Ser;
А19 представляет Lys;
А20 представляет Lys;
А21 представляет Pro;
А22 представляет Pro;
А23 представляет Ala;
А24 представляет Lys;
А25 представляет Leu;
А26 представляет Gln;
А27 представляет Pro; и
А28 представляет Arg;
или их фармацевтически приемлемая соль.
Другой предпочтительной группой соединений формулы (I), названной группой соединений 2, является та, где:
каждый из R2 и R3 независимо в каждом случае выбран из группы, состоящей из Н, ацила, н-бутирила, изобутирила и н-октаноила;
R4 представляет гептил;
R6 представляет гексил;
R7 представляет гексил;
R10 представляет октил;
R11 представляет гептил; и
при условии, что когда имеется Асс вместо одного из природных остатков, то она независимо в каждом случае выбрана из А3с, А4с, А5с или А6с;
или их фармацевтически приемлемая соль.
Еще одной предпочтительной группой соединений формулы (I), названной группой соединений 3, является та, где:
А3 представляет Asp(NH-гексил), Asp(1-гептанол), Cys(S-(CH2)9CH3), Dap(октансульфонил), Glu(NH-гексил) или Glu(1-гептанол);
А5 представляет Leu;
А6 представляет Ser;
А7 представляет Pro, Dhp, 4-Hyp, Pip, Thz или Tic;
А9 представляет His, 3-Pal, 4-Pal, Taz или 2-Thi;
А12 представляет Val;
А15 представляет Arg, Glu(NH-гексил) или Ser(н-октаноил);
А16 представляет Lys, Glu(NH-гексил) или Ser(н-октаноил);
А17 представляет Glu, Lys(биотинил), Asp(NH-гексил), Asp(1-гептанол), Cys(S-(CH2)9CH3), Dap(октансульфонил), Glu(NH-гексил), Glu(1-гептанол) или Ser(н-октаноил);
А18 представляет Ser, Glu(NH-гексил) или Ser(н-октаноил);
А19 представляет Lys, Glu(NH-гексил) или Ser(н-октаноил);
А20 представляет Lys, Glu(NH-гексил) или Ser(н-октаноил);
или их фармацевтически приемлемая соль.
Более предпочтительная группа соединений формулы (I), названная группой соединений 4, включает соединения формулы:
(Ser(н-октаноил)15)hгрелин(1-28)-NH2; (SEQ ID NO:1)
(Glu(NH-гексил)15)hгрелин(1-28)-NH2; (SEQ ID NO:2)
(Glu(NH-гексил)3,15)hгрелин(1-28)-NH2; (SEQ ID NO:3)
(Glu(NH-гексил)3,Ser(н-октаноил)15)hгрелин(1-28)-NH2; (SEQ ID NO:4)
(Aib2,Glu(NH-гексил)15)hгрелин(1-28)-NH2; (SEQ ID NO:5)
(Aib2,Glu(NH-гексил)3,15)hгрелин(1-28)-NH2; (SEQ ID NO:6)
(Aib2,8,Glu(NH-гексил)15)hгрелин(1-28)-NH2; (SEQ ID NO:7)
(Aib2,8,Glu(NH-гексил)3,15)hгрелин(1-28)-NH2; (SEQ ID NO:8)
(Aib2,10,Glu(NH-гексил)15)hгрелин(1-28)-NH2; (SEQ ID NO:9)
(Aib2,10,Glu(NH-гексил)3,15)hгрелин(1-28)-NH2; (SEQ ID NO:10)
(Ser(н-октаноил)16)hгрелин(1-28)-NH2; (SEQ ID NO:11)
(Glu(NH-гексил)16)hгрелин(1-28)-NH2; (SEQ ID NO:12)
(Glu(NH-гексил)3,16)hгрелин(1-28)-NH2; (SEQ ID NO:13)
(Glu(NH-гексил)3,Ser(н-октаноил)16)hгрелин(1-28)-NH2; (SEQ ID NO:14)
(Aib2,Glu(NH-гексил)16)hгрелин(1-28)-NH2; (SEQ ID NO:15)
(Aib2,Glu(NH-гексил)3,16)hгрелин(1-28)-NH2; (SEQ ID NO:16)
(Aib2,8,Glu(NH-гексил)16)hгрелин(1-28)-NH2; (SEQ ID NO:17)
(Aib2,8,Glu(NH-гексил)3,16)hгрелин(1-28)-NH2; (SEQ ID NO:18)
(Aib2,10,Glu(NH-гексил)16)hгрелин(1-28)-NH2; (SEQ ID NO:19)
(Aib2,10,Glu(NH-гексил)3,16)hгрелин(1-28)-NH2; (SEQ ID NO:20)
(Ser(н-октаноил)17)hгрелин(1-28)-NH2; (SEQ ID NO:21)
(Glu(NH-гексил)17)hгрелин(1-28)-NH2; (SEQ ID NO:22)
(Glu(NH-гексил)3,17)hгрелин(1-28)-NH2; (SEQ ID NO:23)
(Glu(NH-гексил)3,Ser(н-октаноил)17)hгрелин(1-28)-NH2; (SEQ ID NO:24)
(Dap(октансульфонил)17)hгрелин(1-28)-NH2; (SEQ ID NO:25)
(Dap(октансульфонил)3,17)hгрелин(1-28)-NH2; (SEQ ID NO:26)
(Dap(октансульфонил)3,Glu(NH-гексил)17)hгрелин(1-28)-NH2; (SEQ ID NO:27)
(Dap(октансульфонил)3,Ser(н-октаноил)17)hгрелин(1-28)-NH2; (SEQ ID NO:28)
(Glu(NH-гексил)3,Dap(октансульфонил)17)hгрелин(1-28)-NH2; (SEQ ID NO:29)
(Cys(S-(CH2)9CH3)17)hгрелин(1-28)-NH2; (SEQ ID NO:30)
(Cys(S-(CH2)9CH3)3,17)hгрелин(1-28)-NH2; (SEQ ID NO:31)
(Glu(NH-гексил)3,Cys(S-(CH2)9CH3)17)hгрелин(1-28)-NH2; (SEQ ID NO:32)
(Cys(S-(CH2)9CH3)3),Glu(NH-гексил)17)hгрелин(1-28)-NH2; (SEQ ID NO:33)
(Cys(S-(CH2)9CH3)3),Ser(н-октаноил)17)hгрелин(1-28)-NH2; (SEQ ID NO:34)
(Aib2,Glu(NH-гексил)17)hгрелин(1-28)-NH2; (SEQ ID NO:35)
(Aib2,Glu(NH-гексил)3,17)hгрелин(1-28)-NH2; (SEQ ID NO:36)
(Aib2,Thz7,Glu(NH-гексил)17)hгрелин(1-28)-NH2; (SEQ ID NO:37)
(Aib2,4-Hyp7,Glu(NH-гексил)17)hгрелин(1-28)-NH2; (SEQ ID NO:37)
(Aib2,Dhp7,Glu(NH-гексил)17)hгрелин(1-28)-NH2; (SEQ ID NO:37)
(Aib2,Pip7,Glu(NH-гексил)17)hгрелин(1-28)-NH2; (SEQ ID NO:37)
(Aib2,Tic7,Glu(NH-гексил)17)hгрелин(1-28)-NH2; (SEQ ID NO:37)
(Aib2,Glu(NH-гексил)3,17,Thz7)hгрелин(1-28)-NH2; (SEQ ID NO:38)
(Aib2,Glu(NH-гексил)3,17,4-Hyp7)hгрелин(1-28)-NH2; (SEQ ID NO:38)
(Aib2,Glu(NH-гексил)3,17,Dhp7)hгрелин(1-28)-NH2; (SEQ ID NO:38)
(Aib2,Glu(NH-гексил)3,17,Pip7)hгрелин(1-28)-NH2; (SEQ ID NO:38)
(Aib2,Glu(NH-гексил)3,17,Tic7)hгрелин(1-28)-NH2; (SEQ ID NO:38)
(Aib2,8,Glu(NH-гексил)17)hгрелин(1-28)-NH2; (SEQ ID NO:39)
(Aib2,8,Glu(NH-гексил)3,17)hгрелин(1-28)-NH2; (SEQ ID NO:40)
(Aib2,3-Pal9,Glu(NH-гексил)17)hгрелин(1-28)-NH2; (SEQ ID NO:41)
(Aib2,4-Pal9,Glu(NH-гексил)17)hгрелин(1-28)-NH2; (SEQ ID NO:41)
(Aib2,Taz9,Glu(NH-гексил)17)hгрелин(1-28)-NH2; (SEQ ID NO:41)
(Aib2,2-Thi9,Glu(NH-гексил)17)hгрелин(1-28)-NH2; (SEQ ID NO:41)
(Aib2,Glu(NH-гексил)3,17,3-Pal9)hгрелин(1-28)-NH2; (SEQ ID NO:42)
(Aib2,Glu(NH-гексил)3,17,4-Pal9)hгрелин(1-28)-NH2; (SEQ ID NO:42)
(Aib2,Glu(NH-гексил)3,17,Taz9)hгрелин(1-28)-NH2; (SEQ ID NO:42)
(Aib2,Glu(NH-гексил)3,17,2-Thi9)hгрелин(1-28)-NH2; (SEQ ID NO:42)
(Aib2,10,Glu(NH-гексил)17)hгрелин(1-28)-NH2; (SEQ ID NO:43)
(Aib2,10,Glu(NH-гексил)3,17)hгрелин(1-28)-NH2; (SEQ ID NO:44)
(Aib8,Glu(NH-гексил)17)hгрелин(1-28)-NH2; (SEQ ID NO:45)
(Taz9,Glu(NH-гексил)17)hгрелин(1-28)-NH2; (SEQ ID NO:46)
(3-Pal9,Glu(NH-гексил)17)hгрелин(1-28)-NH2; (SEQ ID NO:46)
(4-Pal9,Glu(NH-гексил)17)hгрелин(1-28)-NH2; (SEQ ID NO:46)
(2-Thi9,Glu(NH-гексил)17)hгрелин(1-28)-NH2; (SEQ ID NO:46)
(Glu(NH-гексил)3,17,Aib8)hгрелин(1-28)-NH2; (SEQ ID NO:47)
(Glu(NH-гексил)3,17