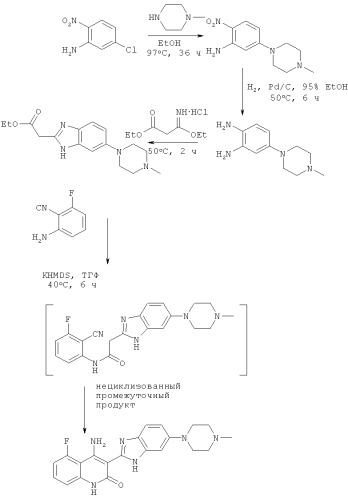
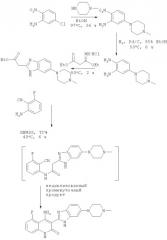
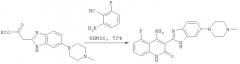
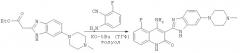
Композиции хинолинонов
Иллюстрации
Показать всеИзобретение относится к композициям хинолиноновых производных, способам получения и применению таких композиций. Фармацевтическая композиция содержит лактат соединения 4-амино-5-фтор-3-[6-(4-метилпиперазин-1-ил)-1Н-бензимидазол-2-ил]-1Н-хинолин-2-она, или его таутомер, или их смесь в количестве от 10 до 80 мас.% и по меньшей мере один ингредиент, выбранный из группы, которая включает (I) целлюлозу; (II) диоксид кремния; (III) стеарат магния и (IV) ингредиент, выбранный из кросповидона, крахмала и лактозы. Композиция включена в состав капсулы или таблетки. Композиции по изобретению проявляют удовлетворительные свойства в отношении скоростей растворения и стабильности. 8 н. и 41 з.п. ф-лы, 2 ил., 21 табл.
Реферат
Область техники, к которой относится изобретение
Настоящее изобретение относится в целом к композициям хинолиноновых производных. Более конкретно представленное в настоящем описании изобретение относится к композициям в виде твердых лекарственных форм, содержащим фармацевтически приемлемые соли, такие как лактаты 4-амино-5-фтор-3-[6-(4-метилпиперазин-1-ил)-1Н-бензимидазол-2-ил]-1Н-хинолин-2-она, и способам получения и применению таких композиций.
Предпосылки создания изобретения
Известно большое количество разнообразных химических соединений и композиций, обладающих активностью в отношении одной или нескольких рецепторных тирозинкиназ сосудистого эндотелиального фактора роста (VEGF-RTK). Их примерами являются хинолиновые производные, такие как соединения, описанные в WO 98/13350, аминоникотинамидные производные (см, например, WO 01/55114), антисмысловые соединения (см., например, WO 01/52904), пептидомиметики (см., например, WO 01/52875), хиназолиновые производные (см., например, US 6258951), моноклональные антитела (см., например, ЕР 1086705 А1), различные 5,10,15,20-тетраарилпорфирины и 5,10,15-триарилкорролы (см., например, WO 00/27379), гетероциклические производные алкансульфоновой и алканкарбоновой кислот (см., например, DE19841985), оксиндолилхиназолиновые производные (см., например, WO 99/10349), 1,4-диазаантрациновые производные (см., например US 5763441) и циннолиновые производные (см., например, WO 97/34876) и различные индазольные производные (см., например, WO 01/02369 и WO 01/53268).
Синтез 4-гидроксихинолоновых и 4-гидроксихинолиновых производных описан в многочисленных публикациях. Например, Ukrainets с соавторами описал синтез 3-(бензимидазол-2-ил)-4-гидрокси-2-оксо-1,2-дигидрохинолина - (Ukrainets I. и др. Tetrahedron Lett. 42, 1995, cc.7747-7748; Ukrainets I. и др. - Khimiya Geterotsiklicheskikh Soedinii, 2, 1992, сс.239-241). Ukrainets описал также синтез, противосудорожную и антитиреоидную активность других 4-гидроксихинолонов и тиоаналогов, таких как 1Н-2-оксо-3-(2-бензимидазолил)-4-гидроксихинолин (Ukrainets I. и др. Khimiya Geterotsiklicheskikh Soedinii, 1, 1995, сс.105-108; Ukrainets I. и др. Khimiya Geterotsiklicheskikh Soedinii, 8, 1993, сс.1105-1108; Ukrainets I. и др. Chem. Heterocyclic Comp. 33, 1997, сс.600-604. Синтез различных хинолиновых производных описан в WO 97/48694. Описано, что эти соединения обладают способностью связываться с рецепторами ядерных гормонов и что их можно применять для стимулирования пролиферации остеобластов и роста кости. Указано также, что эти соединения можно применять для лечения или предупреждения заболеваний, ассоциированных с семействами рецепторов ядерных гормонов.
Различные хинолиновые производные, в которых бензольное кольцо хинолина замещено группой, представляющей собой серу, описаны в WO 92/18483. Указано, что эти соединения можно применять в фармацевтических композициях и в качестве лекарственных средств.
Хинолоновые и кумариновые производные описаны в качестве соединений, которые находят применение в различных областях, не связанных с медициной и фармацевтическими композициями. Получение хинолоновых производных, предназначенных для применения в фотополимеризующихся композициях или в областях, связанных с люминисцентными свойствами, описано, в частности, в US 5801212 на имя Okamoto и др.; JP 8-29973; JP 7-43896; JP 6-9952; JP 63-258903; EP 797376 и DE 2363459.
Многочисленные замещенные хинолиноновые производные, включая хинолинонбензимидазолильные производные и 4-аминозамещенные хинолинонбензимидазолильные производные, такие как 4-амино-5-фтор-3-[5-(4-метилпиперазин-1-ил)-1Н-бензимидазол-2-ил]хинолин-2(1Н)-он, описаны в последние годы, например, в WO 02/22598, WO 2004/043389, WO 2005/047244, US 2004/0220196, US 2005/0137399, WO 2005/046590 и WO 2005/046589. Описано, что такие соединения обладают способностью ингибировать VEGF-RTK. Такие соединения описаны также в опубликованных заявках US 2002/0107392 и US 2003/0028018 и в патентах US 6605617, 6774237, 6762194 и 6800760. Другие такие соединения, а также новые применения таких соединений для ингибирования серин/треониновых киназ и тирозиновых киназ описаны в WO 2004/018419 и US 2004/0092535, зарегистрированной 19 августа 2003 г. и претендующей на приоритет каждой из следующих предварительных заявок на патент: предварительной заявки на патент США №60/405729, зарегистрированной 23 августа 2002 г.; предварительной заявки на патент США №60/426107, зарегистрированной 13 ноября 2002 г.; предварительной заявки на патент США №60/426226, зарегистрированной 13 ноября 2002 г.; предварительной заявки на патент США №60/426282, зарегистрированной 13 ноября 2002 г.; предварительной заявки на патент США №60/428210, зарегистрированной 21 ноября 2002 г.; предварительной заявки на патент США №60/460327, зарегистрированной 3 апреля 2003 г.; предварительной заявки на патент США №, зарегистрированной 3 апреля 2003 г.; предварительной заявки на патент США №60/460493, зарегистрированной 3 апреля 2003 г.; предварительной заявки на патент США №60/478916, зарегистрированной 16 июня 2003 г., и предварительной заявки на патент США №60/484048, зарегистрированной 1 июля 2003 г. Дополнительная информация, касающаяся хинолиноновых производных и их применений, приведена в предварительной заявке на патент США №60/680722, зарегистрированной 13 мая 2005 г.; предварительной заявке на патент США №60/681893, зарегистрированной 17 мая 2005 г.; предварительной заявке на патент США №60/546395, зарегистрированной 20 февраля 2004 г.; предварительной заявке на патент США №60/547103, зарегистрированной 23 февраля 2004 г.; предварительной заявке на патент США №60/554771, зарегистрированной 19 мая 2004 г.; предварительной заявке на патент США №60/647568, зарегистрированной 27 января 2005 г.; предварительной заявке на патент США №60/669245, зарегистрированной 6 апреля 2005 г.; предварительной заявке на патент США №60/538594, зарегистрированной 23 января 2004; предварительной заявке на патент США №60/683999, зарегистрированной 23 мая 2005 г. заявке на патент США №11/061386, зарегистрированной 18 февраля 2005 г.; заявке на патент США №11/041191, зарегистрированной 21 января 2005 г., и заявке РСТ №PCT/US2005/05316, зарегистрированной 18 февраля 2005 г. Гетероциклические соединения, родственные бензимидазолилхинолинонам, описаны в последние годы в WO 02/18383, US 2002/0103230 и US 6756383. Каждый из перечисленных в данном параграфе документов включен в настоящее описание в качестве ссылки во всей полноте и для всех целей, которые полностью изложены в настоящем описании.
Хотя в литературе уже описаны различные хинолиноновые производные, существует необходимость в новых стабильных композициях, лекарственных средствах и способах введения таких соединений, поскольку эти соединения находят важное фармацевтическое применение при ингибировании ангиогенеза и лечении рака.
Краткое изложение сущности изобретения
Настоящее изобретение относится к фармацевтическим композициям хинолиноновых производных, таким как композиции в виде капсулы или таблетки, которые содержат лактаты 4-амино-5-фтор-3-[6-(4-метилпиперазин-1-ил)-1Н-бензимидазол-2-ил]-1Н-хинолин-2-она, и к способам получения и применения таких композиций. Композиции можно получать с помощью методов сухого смешения или мокрой грануляции.
Одним из объектов настоящего изобретения является фармацевтическая композиция, которая содержит соединение формулы I, таутомер соединения, фармацевтически приемлемую соль соединения, фармацевтически приемлемую соль таутомера или их смесь
;
и по меньшей мере один ингредиент, выбранный из группы, включающей (I) целлюлозу; (II) лактозу, крахмал или их смесь; (III) повидон; (IV) диоксид кремния или тальк; (V) фармацевтически приемлемый замасливатель и (VI) ингредиент, выбранный из кросповидона, кроскармеллозы натрия и натрийгликолят крахмала.
Другой объект настоящего изобретения относится к фармацевтической композиции, которая содержит соединение формулы I, таутомер соединения, фармацевтически приемлемую соль соединения, фармацевтически приемлемую соль таутомера или их смесь; по меньшей мере один ингредиент, выбранный из группы, включающей целлюлозу, повидон, диоксид кремния, тальк и фармацевтически приемлемый замасливатель, и по меньшей мере один ингредиент, выбранный из группы, включающей лактозу, крахмал, кросповидон, кроскармеллозу натрия и натрийгликолят крахмала.
В определенных вариантах осуществления изобретения композиция содержит: (I) целлюлозу; (II) диоксид кремния; (III) стеариновую кислоту или соль стеариновой кислоты и (IV) по меньшей мере один ингредиент, выбранный из кросповидона, крахмала, лактозы, кроскармеллозы натрия и натрийгликолята крахмала. В некоторых из таких вариантов осуществления изобретения композиция содержит кросповидон. В некоторых других вариантах осуществления изобретения композиция содержит крахмал, такой как частично предварительно желированный крахмал. В других вариантах осуществления изобретения композиция содержит лактозу.
В определенных вариантах осуществления изобретения композиция содержит лактат соединения формулы I.
В других вариантах осуществления изобретения композиция включена в состав капсулы или таблетки. В некоторых из таких вариантов осуществления изобретения общая масса соединения формулы I, таутомера соединения, лактата соединения, лактата таутомера или их смеси в капсуле составляет от 25 до 500 мг.
В следующих вариантах осуществления изобретения композиция содержит лактат соединения в количестве от 10 до 50 мас.% в пересчете на общую массу композиции. В некоторых из таких вариантов осуществления изобретения композиция содержит лактат соединения в количестве от 20 до 45 мас.% в пересчете на общую массу композиции. В некоторых других из таких вариантов осуществления изобретения композиция содержит лактат соединения в количестве от 30 до 40 мас.% в пересчете на общую массу композиции.
В определенных вариантах осуществления изобретения целлюлоза, применяемая в композиции, представляет собой микрокристаллическую целлюлозу.
В определенных вариантах осуществления изобретения композиция содержит целлюлозу в количестве от 10 до 70 мас.% в пересчете на общую массу композиции. В некоторых из таких вариантов осуществления изобретения композиция содержит целлюлозу в количестве от 20 до 50 мас.% в пересчете на общую массу композиции и композиция содержит кросповидон в количестве от 2 до 6 мас.% в пересчете на общую массу композиции.
В определенных вариантах осуществления изобретения композиция содержит крахмал в количестве от 10 до 40 мас.% в пересчете на общую массу композиции, и крахмал представляет собой частично предварительно желированный крахмал.
В определенных вариантах осуществления изобретения композиция содержит диоксид кремния в количестве от 0,3 до 2 мас.% в пересчете на общую массу композиции.
В определенных вариантах осуществления изобретения композиция содержит стеарат магния в количестве от 0,1 до 2 мас.% в пересчете на общую массу композиции.
В определенных вариантах осуществления изобретения композиция содержит лактат соединения в количестве от 30 до 40 мас.% в пересчете на общую массу композиции; диоксид кремния в количестве от 0,3 до 2 мас.% в пересчете на общую массу композиции, целлюлозу в количестве от 25 до 40 мас.% в пересчете на общую массу композиции, стеарат магния в количестве от 0,1 до 2 мас.% в пересчете на общую массу композиции и кросповидон в количестве от 2 до 4 мас.% в пересчете на общую массу композиции.
В определенных вариантах осуществления изобретения композиция содержит лактат соединения в количестве от 50 до 80 мас.% в пересчете на общую массу композиции; диоксид кремния в количестве от 0,3 до 2 мас.% в пересчете на общую массу композиции, целлюлозу в количестве от 0 до 50 мас.% в пересчете на общую массу композиции, стеарат магния в количестве от 0,1 до 2 мас.% в пересчете на общую массу композиции и крахмал в количестве от 10 до 40 мас.% в пересчете на общую массу композиции.
Объектом изобретения являются также контейнеры для упаковки фармацевтических продуктов. В одном из вариантов осуществления изобретения контейнер для упаковки представляет собой сосуд для хранения, содержащий две или более капсул или таблеток, где капсулы или таблетки содержат фармацевтическую композицию, предлагаемую в одном из вариантов осуществления изобретения. В некоторых из таких вариантов осуществления изобретения сосуд для хранения сделан из полиэтилена высокой плотности (ПЭВП). В некоторых из таких вариантов осуществления изобретения сосуд для хранения содержит прокладку из хлопка или искусственного волокна и в определенных вариантах осуществления изобретения включает термокрышку. Другой вариант осуществления изобретения относится к контейнеру для упаковки фармацевтических продуктов, который представляет собой блистерную упаковку, где блистерная упаковка содержит по меньшей мере одну капсулу или таблетку, которая включает фармацевтическую композицию, предлагаемую в одном из вариантов изобретения.
Изобретение относится также к нанесению на таблетку, предлагаемую в настоящем изобретении, покрытия из вещества, выбранного из группы, включающей сахар, полимер на основе целлюлозы и полиметакрилатный полимер. В некоторых вариантах осуществления изобретения на таблетку можно наносить также желатиновое покрытие или капсулировать таблетку в желатиновую оболочку.
Изобретение относится также к окрашиванию таблетки или капсулы, предлагаемой в настоящем изобретении, фармацевтически приемлемым красителем или замутнителем.
Одним из объектов изобретения является способ получения фармацевтической композиции. Способ заключается в том, что (а) смешивают первую смесь с получением первой перемешанной смеси, где первая смесь содержит: (I) соединение формулы I, таутомер соединения, фармацевтически приемлемую соль соединения, фармацевтически приемлемую соль таутомера или их смесь и (II) по меньшей мере один ингредиент, выбранный из группы, включающей целлюлозу; лактозу, крахмал или их смесь; повидон; диоксид кремния или тальк; фармацевтически приемлемый замасливатель; и ингредиент, выбранный из кросповидона, кроскармелозы натрия и натрийгликолят крахмала. В некоторых из таких вариантов осуществления изобретения соединение формулы I смешивают с (I) целлюлозой; (II) диоксидом кремния и (III) ингредиентом, выбранным из кросповидона, крахмала и лактозы. Кроме того, способ заключается в том, что (б) смешивают стеариновую кислоту, соль стеариновой кислоты или их смесь с первой перемешанной смесью с получением второй перемешанной смеси и/или (в) изготавливают по меньшей мере одну капсулу или по меньшей мере одну таблетку из второй перемешанной смеси.
Другой объект изобретения относится к способу получения фармацевтической композиции. Способ заключается в том, что (а) смешивают смесь ингредиентов с получением первой перемешанной смеси. Первая перемешанная смесь содержит: (I) соединение формулы I, таутомер соединения, фармацевтически приемлемую соль соединения, фармацевтически приемлемую соль таутомера или их смесь, (II) по меньшей мере один ингредиент, выбранный из группы, включающей целлюлозу; крахмал; лактозу; и повидон; (III) по меньшей мере один ингредиент, выбранный из группы, включающей кросповидон, кроскармелозу натрия и натрийгликолят крахмала; жидкость для грануляции, выбранную из группы, включающей водную кислоту, спирт, водный спирт или смесь любых двух или большего количества из этих компонентов. Способ заключается также в том, что (б) удаляют жидкость для грануляции. Кроме того, способ заключается в том, что (в) получают вторую перемешанную смесь путем смешения первой перемешанной смеси с по меньшей мере одним дополнительным ингредиентом, выбранным из группы, включающей (I) кросповидон, кроскармеллозу натрия или натрийгликолят крахмала; (II) стеариновую кислоту или соль стеариновой кислоты и (III) диоксид кремния или тальк. Способ может заключаться также в том, что (г) изготавливают по меньшей мере одну капсулу или по меньшей мере одну таблетку из второй перемешанной смеси.
Изобретение относится также к способам получения фармацевтической композиции, в которых фармацевтическую композицию приготавливают с использованием по меньшей мере одного аппарата, выбранного из группы, включающей (I) гранулятор с псевдоожиженным слоем, снабженный механизмом нижнего распыления, верхнего распыления или тангенциального распыления; (II) гранулятор с высокими сдвиговыми усилиями; (III) гранулятор с низкими сдвиговыми усилиями; (IV) роллерный уплотнитель и (V) таблеточный пресс.
В определенных вариантах осуществления изобретения общая масса соединения формулы I, таутомера соединения, фармацевтически приемлемой соли соединения, фармацевтически приемлемой соли таутомера или их смеси в капсуле или таблетке составляет от 25 до 500 мг.
В определенных вариантах осуществления способа вторая перемешанная смесь содержит лактат соединения формулы I. В других вариантах осуществления изобретения вторая перемешанная смесь содержит лактат соединения в количестве от 10 до 50 мас.% в пересчете на общую массу второй перемешанной смеси.
В некоторых вариантах способа получения фармацевтической композиции целлюлоза представляет собой микрокристаллическую целлюлозу. В определенных вариантах осуществления изобретения крахмал представляет собой предварительно желированный крахмал.
В определенных вариантах способа вторая перемешанная смесь содержит целлюлозу в количестве от 10 до 70 мас.% в пересчете на общую массу второй перемешанной смеси. В некоторых из таких вариантов осуществления изобретения вторая перемешанная смесь содержит целлюлозу в количестве от 20 до 50 мас.% в пересчете на общую массу второй перемешанной смеси и вторая перемешанная смесь содержит кросповидон в количестве от 2 до 6 мас.% в пересчете на общую массу второй перемешанной смеси.
В определенных вариантах способа вторая перемешанная смесь содержит крахмал в количестве от 20 до 40 мас.% в пересчете на общую массу второй перемешанной смеси, и крахмал представляет собой частично предварительно желированный крахмал.
В конкретных вариантах способа вторая перемешанная смесь содержит диоксид кремния в количестве от 0,3 до 2 мас.% в пересчете на общую массу второй перемешанной смеси.
В конкретных вариантах способа получения фармацевтической композиции вторая перемешанная смесь содержит стеарат магния в количестве от 0,1 до 2 мас.% в пересчете на общую массу второй перемешанной смеси.
В конкретных вариантах способа вторая перемешанная смесь содержит лактат соединения в количестве от 50 до 80 мас.% в пересчете на общую массу второй перемешанной смеси, в количестве от 55 до 75 мас.% в пересчете на общую массу второй перемешанной смеси или в количестве от 60 до 70 мас.% в пересчете на общую массу второй перемешанной смеси.
В некоторых из вариантов способа диоксид кремния присутствует в количестве от 0,3 до 2 мас.% в пересчете на общую массу второй перемешанной смеси. В других вариантах этого способа целлюлоза присутствует в количестве от 20 до 45 мас.% в пересчете на общую массу второй перемешанной смеси. В следующих вариантах этого способа стеарат магния присутствует в количестве от 0,1 до 2 мас.% в пересчете на общую массу второй перемешанной смеси. В других вариантах этого способа вторая перемешанная смесь дополнительно содержит кросповидон в количестве от 2 до 6 мас.% в пересчете на общую массу второй перемешанной смеси. В следующих вариантах этого способа вторая перемешанная смесь содержит диоксид кремния в количестве от 0,5 до 2 мас.% в пересчете на общую массу второй перемешанной смеси, целлюлозу в количестве от 20 до 45 мас.% в пересчете на общую массу второй перемешанной смеси, стеарат магния в количестве от 0,5 до 2 мас.% в пересчете на общую массу второй перемешанной смеси и кросповидон в количестве от 2 до 4 мас.% в пересчете на общую массу второй перемешанной смеси.
Конкретным объектом изобретения является способ лечения рака и/или ингибирования ангиогенеза у индивидуума. Способ заключается в том, что индивидууму вводят композицию, предлагаемую в одном из представленных в настоящем описании вариантов осуществления изобретения. В некоторых из вариантов осуществления изобретения композиция представляет собой капсулу. В других вариантах осуществления этого способа композиция представляет собой таблетку.
В конкретных вариантах способа лечения рака и/или ингибирования ангиогенеза у индивидуума композицию вводят в количестве, достаточном для обеспечения концентрации Cmax соединения формулы I, таутомера соединения, лактата соединения, лактата таутомера или их смеси в плазме индивидуума, составляющей примерно от 20 до 4000 нг/мл, или концентрации Cmax соединения формулы I, таутомера соединения, лактата соединения, лактата таутомера или их смеси в крови индивидуума, составляющей примерно от 40 до 8000 нг/мл.
В конкретных вариантах осуществления способа лечения рака и/или ингибирования ангиогенеза у индивидуума композицию вводят в количестве, достаточном для обеспечения концентрации соединения формулы I, таутомера соединения, лактата соединения, лактата таутомера или их смеси в плазме индивидуума, составляющей примерно от 10 до 2000 нг/мл через 24 ч после введения, или концентрации соединения формулы I, таутомера соединения, лактата соединения, лактата таутомера или их смеси в крови индивидуума, составляющей примерно от 20 до 4000 нг/мл через 24 ч после введения.
В конкретных вариантах способа лечения рака и/или ингибирования ангиогенеза у индивидуума композицию вводят в количестве, достаточном для обеспечения величины AUC соединения формулы I, таутомера соединения, лактата соединения, лактата таутомера или их смеси в плазме индивидуума, составляющей примерно от 500 до 60000 нг·ч/мл, или величины AUC соединения формулы I, таутомера соединения, лактата соединения, лактата таутомера или их смеси в крови индивидуума, составляющей примерно от 750 до 120000 нг·ч/мл.
В конкретных вариантах способа лечения рака и/или ингибирования ангиогенеза у индивидуума композицию вводят один, два, три или четыре раза в день.
В конкретных вариантах способа лечения рака и/или ингибирования ангиогенеза у индивидуума количество соединения формулы I, таутомера соединения, лактата соединения, лактата таутомера или их смеси, вводимое индивидууму, составляет от 0,25 до 30 мг/кг веса тела индивидуума.
В конкретных вариантах способа лечения рака и/или ингибирования ангиогенеза у индивидуума рак, подлежащий лечению, выбирают из группы, включающей рак предстательной железы, колоректальный рак, рак молочной железы, множественную миелому, рак поджелудочной железы, мелкоклеточный рак, острый миелогенный лейкоз, хронический миелогенный лейкоз, миелопролиферативное заболевание, немелкоклеточный рак легкого, мелкоклеточный рак легкого, хронический лимфолейкоз, саркому, меланому, лимфому, рак щитовидной железы, нейроэндокринный рак, почечно-клеточный рак, рак желудка, желудочно-кишечный стромальный рак, глиому, рак головного мозга или рак мочевого пузыря. В определенных вариантах осуществления изобретения рак является метастазирующим.
В конкретных вариантах способа лечения рака и/или ингибирования ангиогенеза у индивидуума способ дополнительно заключается в том, что композицию вводят в качестве элемента цикла лечения, где цикл лечения предусматривает ежедневное введение композиции в течение 7, 14, 21 или 28 дней, после чего следует 7- или 14-дневный период без введения композиции. В конкретных вариантах осуществления изобретения цикл лечения предусматривает ежедневное введение определенного количества соединения в течение 7 дней, после чего следует 7-дневный период без введения соединения. В некоторых вариантах осуществления изобретения цикл лечения повторяют один или несколько раз.
Другие объекты, отличительные признаки и преимущества изобретения станут очевидными после ознакомления с чертежами и прилагаемым подробным описанием.
Краткое описание чертежей
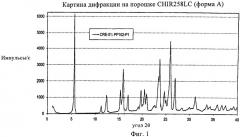
На фиг.1 показана картина дифракции рентгеновских лучей на порошке (XRPD) для формы А,
на фиг.2 - схема, изображающая различные стадии процесса приготовления капсул, содержащих композицию.
Подробное описание изобретения
Настоящее изобретение относится к композициям хинолиноновых производных. Такие композиции можно применять в качестве антагонистов рецепторных тирозинкиназ и более конкретно для ингибирования функции PDGFRα и PDGFRβ, bFGF и/или VEGF-RTK. Такие композиции можно применять также для ингибирования других тирозинкиназ и различных сериновых/треониновых киназ. Композиции можно применять, например, для лечения пациентов, страдающих раком и/или нуждающихся в ингибировании VEGF-RTK. Композиции можно применять также для лечения индивидуума, нуждающегося в ингибировании ангиогенеза.
В настоящем описании используются следующие сокращения и определения.
Сокращение «AUC» относится к площади под кривой на графике зависимости концентрации соединения в плазме крови от времени.
Сокращение «API» обозначает фармацевтическое действующее вещество.
Сокращение «bFGF» обозначает основной фактор роста фибробластов.
Сокращение «bFGFR», синонимом которого является «FGFR1», относится к тирозинкиназе, которая взаимодействует с фактором роста фибробластов FGF.
Сокращение «Cmax» обозначает максимальную концентрацию соединения в плазме, ткани или крови индивидуума, которому ввели соединение. Как правило, Cmax достигается в течение нескольких часов после введения соединения индивидууму.
Сокращение «DVS» обозначает динамическую сорбцию паров.
Сокращение «ПЭВП» обозначает полиэтилен высокой плотности.
Сокращение «LLOQ» обозначает нижний предел количественной оценки.
Сокращение «PDGF» обозначает тромбоцитарный фактор роста. PDGF взаимодействует с тирозинкиназами PDGFRα и PDGFRβ.
Сокращение «PIB» обозначает композицию типа «порошок в пузырьке».
Сокращение «RH» обозначает относительную влажность.
Сокращение «RTK» обозначает рецепторную тирозинкиназу.
Сокращение «VEGF» обозначает сосудистый эндотелиальный фактор роста.
Сокращение «VEGF-RTK» обозначает рецепторную тирозинкиназу сосудистого эндотелиального фактора роста.
Сокращение «XRPD» обозначает дифракцию рентгеновских лучей на порошке.
Понятие «фармацевтически приемлемая соль» обозначает соль неорганического основания, органического основания, неорганической кислоты, органической кислоты или оснòвной или кислотной аминокислоты. В контексте изобретения к солям неорганических оснований относятся, например, соли щелочных металлов, таких как натрий и калий, щелочно-земельных металлов, таких как кальций и магний или алюминий, и соли аммония. В контексте изобретения к солям органических оснований относятся, например, соли триметиламина, триэтиламина, пиридина, пиколина, этаноламина, диэтаноламина и триэтаноламина. В контексте настоящего изобретения к солям неорганических кислот относятся, например, соли таких кислот, как соляная кислота, бромистоводородная кислота, азотная кислота, серная кислота и фосфорная кислота. В контексте настоящего изобретения к солям органических кислот относятся, например, соли таких кислот, как муравьиная кислота, уксусная кислота, фумаровая кислота, щавелевая кислота, винная кислота, малеиновая кислота, молочная кислота, лимонная кислота, янтарная кислота, яблочная кислота, метансульфоновая кислота, бензолсульфоновая кислота и пара-толуолсульфоновая кислота. В контексте изобретения к солям оснòвных аминокислот относятся, например, соли таких кислот, как аргинин, лизин и орнитин. К кислотным аминокислотам относятся, например, аспарагиновая кислота и глутаминовая кислота.
Понятие «индивидуум» в контексте настоящего описания относится к любому животному, на которое можно оказывать благоприятное воздействие с помощью способов, предлагаемых в изобретении. Так, соединение формулы I, его фармацевтически приемлемые соли, таутомеры или фармацевтически приемлемую соль таутомера можно вводить любому животному, на которое может оказывать благоприятное воздействие соединение, предлагаемое в изобретении, при его применении с помощью способов лечения рака, предлагаемых в изобретении. Предпочтительно животное представляет собой млекопитающее и прежде всего человека, хотя объем изобретения не ограничен только им. Примерами других пригодных животных являются (но не ограничиваясь только ими) крысы, мыши, обезьяны, собаки, кошки, крупный рогатый скот, лошади, свиньи, овцы и т.п.
Понятие «лечение» в контексте настоящего изобретения обозначает ослабление симптомов, ассоциированных с нарушением или заболеванием, или прекращение дальнейшего развития или ухудшения этих симптомов, или предупреждение или профилактику заболевания или нарушения. Например, касательно рака успешное лечение может заключаться в ослаблении симптомов или прекращении развития заболевания, что оценивают по уменьшению скорости роста опухоли, прекращению роста опухоли, уменьшению размера опухоли, частичной или полной ремиссии рака, или по увеличению коэффициента выживаемости или клиническому благоприятному действию.
Одним из объектов настоящего изобретения является фармацевтическая композиция, которая содержит соединение формулы I, таутомер соединения, фармацевтически приемлемую соль соединения, фармацевтически приемлемую соль таутомера или их смесь
и по меньшей мере один ингредиент, выбранный из группы, включающей (I) целлюлозу; (II) лактозу, крахмал или их смесь; (III) повидон; (IV) диоксид кремния или тальк; (V) фармацевтически приемлемый замасливатель и (VI) ингредиент, выбранный из кросповидона, кроскармеллозы натрия и натрийгликолята крахмала. В других вариантах осуществления изобретения фармацевтическая композиция включает по меньшей мере два, три или четыре ингредиента, выбранных из (I) целлюлозы; (II) лактозы, крахмала или их смеси; (III) повидона; (IV) диоксида кремния или талька; (V) фармацевтически приемлемого замасливателя и (VI) ингредиента, выбранного из кросповидона, кроскармеллозы натрия и натрийгликолята крахмала.
Другим объектом настоящего изобретения является фармацевтическая композиция, которая содержит соединение формулы I, таутомер соединения, фармацевтически приемлемую соль соединения, фармацевтически приемлемую соль таутомера или их смесь и по меньшей мере один ингредиент, выбранный из группы, включающей целлюлозу, повидон, диоксид кремния, тальк, фармацевтически приемлемый замасливатель; и по меньшей мере один ингредиент, выбранный из группы, включающей лактозу, крахмал, кросповидон, кроскармеллозу натрия и натрийгликолят крахмала.
Композиция может содержать фармацевтически приемлемый замасливатель, который уменьшает способность порошков прилипать к металлическим частям машин для заполнения капсул или таблетировочных машин. Такие замасливатели хорошо известны в данной области и к ним относятся жирная С16-С22-кислота, соль жирной С16-С22-кислоты, эфир жирной С16-С22-кислоты; полиэтиленгликоль со средней молекулярной массой от 6000 до 10000 и смесь любых двух или большего количества из указанных веществ. В конкретных вариантах осуществления изобретения фармацевтически приемлемый замасливатель представляет собой стеариновую кислоту, ее соли, ее эфиры, соли эфиров или их смеси. Например, композиция может содержать стеарат магния, стеарат натрия, стеарат кальция, стеарат цинка, моностеарат глицерила, пальмитостеарил глицерила, бегенат глицерила или стеарилфумарат натрия. Как должно быть очевидно специалистам в данной области, стеариновая кислота, ее соли, эфиры и соли эфиров, включая смеси жирных C16- и C18-кислот, подпадают под объем изобретения.
Композиция может содержать, практически состоять или состоять из соединения формулы I, таутомера соединения, фармацевтически приемлемой соли соединения, фармацевтически приемлемой соли таутомера или их смеси и (I) целлюлозы; (II) диоксида кремния; (III) стеариновой кислоты, соли стеариновой кислоты или их смеси и (IV) по меньшей мере одного ингредиента, выбранного из кросповидона, крахмала, лактозы, кроскармеллозы натрия и натрийгликолята крахмала. В конкретных вариантах осуществления изобретения композиции содержат (I) микрокристаллическую целлюлозу; (II) диоксид кремния; (III) стеарат магния; (IV) по меньшей мере один ингредиент, выбранный из кросповидона, частично предварительно желированного крахмала и лактозы.
Композиция может содержать лактат соединения формулы I. В конкретных вариантах осуществления изобретения лактат может находиться в безводной кристаллической форме, такой как форма А, которая более подробно описана и охарактеризована в разделе «Примеры» настоящего документа.
Композиция может содержаться в капсуле или таблетке. В некоторых из таких вариантов осуществления изобретения общая масса соединения формулы I, таутомера соединения, лактата соединения, лактата таутомера или их смеси в капсуле или таблетке составляет от 25 до 500 мг. В качестве капсул можно использовать, например, белые непрозрачные желатиновые капсулы размера №0, такие как CS-капсулы, поступающие от фирмы Capsugel, или ГПМЦ-капсулы, поступающие от фирм Quali-V и Shinogi.
В конкретных вариантах осуществления изобретения композиция содержит лактат соединения в количестве от 10 до 50 мас.% в пересчете на общую массу композиции. В некоторых из таких вариантов осуществления изобретения композиция содержит лактат соединения в количестве от 20 до 45 мас.% в пересчете на общую массу композиции. В других вариантах осуществления изобретения композиция содержит лактат соединения в количестве от 30 до 40 мас.% в пересчете на общую массу композиции.
В конкретных вариантах осуществления изобретения целлюлоза, применяемая в композиции, представляет собой микрокристаллическую целлюлозу. В других вариантах осуществления изобретения применяемая целлюлоза представляет собой силикатированную микрокристаллическую целлюлозу, натрийкарбоксиметилцеллюлозу или гидроксипропилцеллюлозу.
В конкретных вариантах осуществления изобретения композиция содержит целлюлозу в количестве от 10 до 70 мас.% в пересчете на общую массу композиции. В некоторых из таких вариантов осуществления изобретения композиция содержит целлюлозу в количестве от 20 до 50 мас.% в пересчете на общую массу композиции и композиция содержит кросповидон в количестве от 2 до 6 мас.% в пересчете на общую массу композиции. В определенных вариантах осуществления изобретения композиция содержит целлюлозу в количестве от 20 до 45 мас.% в пересчете на общую массу композиции и композиция содержит крахмал или лактозу в количестве от 10 до 40 мас.% в пересчете на общую массу композиции.
В конкретных вариантах осуществления изобретения композиция содержит крахмал в количестве от 10 до 40 мас.% в пересчете на общую массу композиции, и крахмал представляет собой частично предварительно желированный крахмал.
Композиции могут содержать диоксид кремния в количестве от 0,3 до 2 мас.% в пересчете на общую массу композиции. В конкретных вариантах осуществления изобретения диоксид кремния присутствует в количествах от 0,2 до 5 мас.%, от 0,4 до 4 мас.%, от 0,5 до 2 мас.%, от 0,75 до 1,5 мас.% или от 0,8 до 1,2 мас.% в пересчете на общую массу композиции. В определенных вариантах осуществления изобретения диоксид кремния присутствует в количестве, составляющем примерно 1 мас.% в пересчете на общую массу композиции. В других вариантах осуществления изобретения диоксид кремния можно заменять на коллоидный диоксид кремния, силикат магния, трисиликат магния или тальк в таком же или близком процентном содержании (мас.%).
Композиции могут содержать стеарат магния в количестве от 0,1 до 2 мас.% в пересчете на общую массу композиции. В конкретных вариантах осуществления изобретения стеарат присутствует в количествах от 0,2 до 5 мас.%, от 0,4 до 4 мас.%, от 0,5 до 2 мас.%, от 0,75 до 1,5 мас.% или от 0,8 до 1,2 мас.% в пересчете на общую массу композиции. В определенных вариантах осуществления изобретения стеарат присутствует в количестве, составляющем примерно 1 мас.% в пересчете на общую массу композиции. В других вариантах осуществления изобретения стеарат магния можно заменять на стеариновую кислоту, ее соли, их смеси и/или другие фармацевтически приемлемые замасливатели в таком же или близком процентном содержании (мас.%).
В некоторых вариантах осуществления изобретения композиция содержит, практически состоит