Гетероциклические ингибиторы янус-киназы 3
Иллюстрации
Показать всеНастоящее изобретение относится к соединению формулы I
в которой X обозначает N или CR3, М обозначает (СН2)m; m=0 или 1, R1 обозначает -Н или низший алкил, который может быть замещен группой, выбранной из группы, состоящей из моно- или ди-низший алкиламино и -О-низшего алкила, R2 обозначает -Н или низший алкил, R3 обозначает -Н или низший алкил, замещенный группой, выбранной из группы, состоящей из галогена, моно- или ди-низший алкиламино и циклического амино, R41 обозначает -Н или пиридин, который может быть замещен цианогруппой, R42 обозначает соединенный мостиковой связью полициклический углеводород или соединенный мостиковой связью азациклический углеводород, каждый из которых может быть замещен, R5 обозначает группу, выбранную из группы, состоящей из галогена, циано, низшего алкил-карбонила, низшего алкил-оксикарбонила, гидроксикарбонила, формила, амидинооксикарбонила, гуанидинооксикарбонила, гуанидино, карбамоила, -С(=O)-5- или -6-членного гетероциклоалкила, -С(=O)-5- или -6-членного гетероарила, низшего алкила, низшего алкенила, -О-низшего алкила, 5- или 6-членного гетероциклоалкила и 5-членного гетероарила, каждый из которых может быть замещен, при условии, что, когда R5 обозначает 5-членный гетероарил, X обозначает -CR3; или R41 и R5 могут быть связаны через определенную функциональную группу с образованием двухвалентных групп, показанных ниже:
в которых RA обозначает -Н или ацил, который может быть замещен, при условии, что термин «замещенный» в отношении R42 и/или R5 означает замещенный одним или более заместителями, выбранными из группы, состоящей из следующих заместители: (а) галоген; (b) -ОН, -O-R2, -O-фенил, -OCO-RZ -OCONH-RZ оксо (=O); (с) -SH, -S-R2, -S-фенил, -S-гетероарил, -SO-RZ, -SO-фенил, -SO-гетероарил, -SO3H, -SO2-RZ, -SO2-фенил, -SO2-гетероарил, сульфамоил, который может быть замещен одной или двумя группами RZ; (d) амино, который может быть замещен одной или двумя группами RZ, -NHCO-RZ, -NHCO-фенил, -NHCO2-RZ, -NHCONH2, -NHCONH-RZ, -NHSO2-R0, -NHSO2-фенил, -NHSO2NH2, -NO2,=N-O-RZ; (e) -CHO, -CO-RZ, -CO2H, -CO2-RZ, карбамоил, который может быть замещен одной или двумя группами RZ, -СО-циклический aмино, -COCO-RZ, циано; (f) RZ; (g) фенил, который может быть замещен одной или более группами, выбранными из заместителей, описанных выше в параграфах от (а) до (f), 5- или 6-членный гетероциклоалкил, 5- или 6-членный гетероарил, 5- или 6-членный гетероциклоарил; или к его фармацевтически приемлемой соли. Кроме того, изобретение относится к способу получения соединения формулы II, к фармацевтической композиции на основе этих соединений и представляющей собой ингибитор Янус-киназы 3, к способу лечения и/или профилактики различных иммунопатологических заболеваний, включая аутоиммунные заболевания, воспалительные заболевания и аллергические заболевания. Технический результат: получены и описаны новые соединения, которые могут быть использованы в качестве активного ингредиента средства для лечения или профилактики заболеваний, вызванных нежелательной передачей сигнала цитокина (например, отторжение в ходе трансплантации органа/ткани, аутоиммунные заболевания, рассеянный склероз, ревматоидный артрит, псориаз, астма, аллергический дерматит, болезнь Альцгеймера и атеросклеротическое заболевание), или заболеваний, вызванных патологической передачей сигнала цитокина (например, рак и лейкоз). 10 н. и 4 з.п. ф-лы, 72 табл.
Реферат
Настоящее изобретение относится к новому конденсированному гетероциклическому соединению и к лекарственному средству, содержащему это соединение в качестве активного ингредиента, и более конкретно, к средству для лечения иммунопатологического заболевания.
УРОВЕНЬ ТЕХНИКИ
Янус-киназа 3 (далее обозначенная как JAK3) составляет семейство протеинкиназ. Хотя киназы этого семейства, кроме JAK3, экспрессируются в различных тканях, JAK3 экспрессируется локально в гематопоэтических клетках. Это не противоречит тому факту, что JAK3 играет важную роль в передаче сигналов через различные рецепторы, такие как интерлейкин (далее обозначенный как IL)-2, IL-4, IL-7, IL-9, IL-15 и IL-21, нековалентной ассоциацией с общей цепью γ (см. непатентную литературу 1 и непатентную литературу 2).
В популяции пациентов с XSCID (X-связанный тяжелый комбинированный иммунодефицит) понижено содержание белка JAK3 или обнаруживается генетический дефект в общей цепи γ. Указывается, что эта проблема имеет место, потому что иммуносупрессия блокирует JAK3-зависимые пути передачи сигналов (см. непатентную литературу 3 и непатентную литературу 4). Эксперименты на животных показали, что JAK3 играет важную роль не только в созревании B-лимфоцитов и Т-лимфоцитов, но также и в поддержании функции Т-клеток. Следовательно, ожидается, что заболевания, включающие пролиферативную аномалию Т-клеток, такую как отторжение в ходе трансплантации органа/ткани и аутоиммунные заболевания, могут быть подвергнуты лечению путем контроля иммунного ответа через этот механизм.
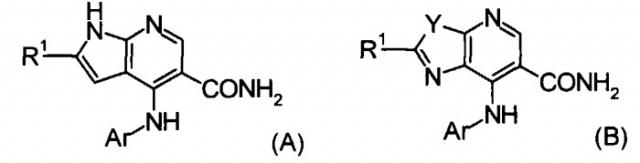
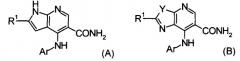
С другой стороны, производное пирролопиридина (патентная литература 1), представленное формулой (A) или (B), или производное имидазопиридина (см. патентную литературу 2) известно как соединение, имеющее активность в отношении ингибирования JAK3.
(в отношении символов в формулах см. соответствующие патентные публикации)
Кроме того, производное пирролопиримидина (см. патентную литературу 3, патентную литературу 4, патентную литературу 5 и патентную литературу 6), представленное формулой (C), также известно как соединение, имеющее активность в отношении ингибирования JAK3.
(в отношении символов в формуле см. соответствующие патентные публикации)
Кроме того, производное пирролопиридина (см. патентную литературу 7), представленное формулой (D), также известно как соединение, имеющее активность в отношении ингибирования JAK3.
(в отношении символов в формуле см. соответствующие патентные публикации)
Однако ни в одном из литературных источников соединение согласно настоящему изобретению специфически не раскрыто.
[Непатентная литература 1] J. J. O'shea et al, Cell, Vol. 109 (suppl.), S121, 2002
[Непатентная литература 2] K. Ozaki et al, Science, Vol. 298, p. 1630, 2002
[Непатентная литература 3] P. Macchi et al, Nature, Vol. 377, p. 65, 1995
[Непатентная литература 4] S. M. Russell et al, Science, Vol. 270, p. 797, 1995
[Патентная литература 1] WO 2004/099205
[Патентная литература 2] WO 2004/099204
[Патентная литература 3] WO 99/065908
[Патентная литература 4] WO 99/065909
[Патентная литература 5] WO 01/042246
[Патентная литература 6] WO 02/000661
[Патентная литература 7] WO 2006/069080
РАСКРЫТИЕ ИЗОБРЕТЕНИЯ
ПРОБЛЕМА, РЕШАЕМАЯ В СООТВЕТСТВИИ С ИЗОБРЕТЕНИЕМ
В результате интенсивных исследований с целью получения полезной фармацевтической композиции, имеющей активность в отношении ингибирования JAK3, авторы изобретения обнаружили, что новое конденсированное гетероциклическое соединение имеет превосходную активность в отношении ингибирования JAK3, и осуществили настоящее изобретение.
Более конкретно, настоящее изобретение относится к новому конденсированному гетероциклическому соединению, представленному следующей формулой (I), или к его фармацевтически приемлемым солям и к фармацевтической композиции, содержащей соединение, более конкретно, фармацевтической композиции, служащей средством для лечения и/или профилактики аутоиммунных заболеваний, воспалительных заболеваний и аллергических заболеваний.
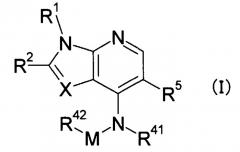
Конденсированное гетероциклическое соединение является конденсированным пиридином, представленным следующей формулой (I):
в которой
X обозначает N или CR3,
М обозначает (CH2)m; m = 0 или 1,
R1 обозначает -H или низший алкил, который может быть замещен,
R2 обозначает -H или низший алкил, который может быть замещен,
R3 обозначает -H, галоген или низший алкил, который может быть замещен,
R41 обозначает -H или гетероарил, который может быть замещен,
R42 обозначает соединенную мостиковой связью кольцевую группу, которая может быть замещена,
R5 обозначает группу, выбранную из группы, состоящей из галогена, циано, ацила, ациламино, низшего алкила, низшего алкенила, -O-низшего алкила, 5- или 6-членного гетероциклоалкила, 5- или 6-членного гетероциклоалкенила и 5-членного гетероарила, каждый из которых может быть замещен,
при условии, что, когда R5 обозначает 5-членный гетероарил, X обозначает -CR3,
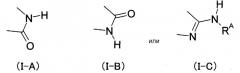
или R41 и R5 могут быть связаны через определенную функциональную группу с образованием двухвалентных групп, показанных ниже:
в которых RA обозначает -H или ацил, который может быть замещен,
или его фармацевтически приемлемыми солями.
ЭФФЕКТ ИЗОБРЕТЕНИЯ
Соединение согласно настоящему изобретению имеет активность в отношении ингибирования JAK3 и, таким образом, может быть использовано в качестве активного ингредиента средства для лечения и/или профилактики заболеваний, вызванных нежелательной передачей сигнала цитокина (например, отторжение в ходе трансплантации органа/ткани, аутоиммунные заболевания, астма, аллергический дерматит, болезнь Альцгеймера и атеросклеротическое заболевание), или заболеваний, вызванных патологической передачей сигнала цитокина (например, рак и лейкоз).
ЛУЧШИЕ СПОСОБЫ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Соединение согласно настоящему изобретению, представленное формулой (I), характеризуется в своей химической структуре тем, что соединение имеет поперечно сшитый амин и также имеет скелет, в котором 5- и 6-членный гетероциклы конденсированы, как в 1H-пирроло[2,3-b]пиридине, 1H-имидазо[4,5-b]пиридине или пиразоло[1,5-a]пиримидине, и далее характеризуются в фармакологическом отношении тем, что соединение имеет активность в отношении ингибирования JAK3.
Настоящее изобретение описано подробно ниже.
Термин "алкил" в настоящем описании обозначает прямую или разветвленную моновалентную группу.
Термин "низший алкил" в описании обозначает прямой или разветвленный C1-C6 алкил и может включать такие радикалы, как метил, этил, н-пропил, изопропил, н-бутил, изобутил, трет-бутил, н-пентил, неопентил и н-гексил, предпочтительно метил, этил, н-пропил, изопропил и изобутил, и особенно предпочтительно метил и этил.
Термин "низший алкенил" в описании обозначает прямой или разветвленный C2-C6 алкенил, имеющий двойную связь в каждом возможном положении, и может включать такие радикалы, как этенил (винил), 1-пропенил, 2-пропенил (аллил), 1-метилэтен-1-ил, 1-бутен-1-ил, 2-бутен-1-ил, 3-бутен-1-ил, 1-метил-1-пропен-1-ил, 2-метил-1-пропен-1-ил, 1-метил-2-пропен-1-ил и 2-метил-2-пропен-1-ил, предпочтительно 1-метил-2-пропен-1-ил.
Термин "галоген" означает фтор, хлор, бром и йод, предпочтительно фтор.
Термин "циклоалкил" обозначает моновалентную неароматическую карбоциклическую группу C3-C8 и может частично иметь ненасыщенные связи или может конденсироваться с бензольным кольцом. Однако соединенные мостиковой связью циклические углеводороды из этого определения исключены. Циклоалкил может включать такие радикалы, как циклопропил, циклобутил, циклогексил, циклогептил, циклооктил, циклобутенил, циклогексенил, циклооктадиенил, инданил и тетрагидронафтил, предпочтительно циклогексил.
Термин "гетероциклоалкил" обозначает 5-6-членный неароматический насыщенный гетероцикл, который может иметь один или более одинаковых или разных гетероатомов, выбранных из группы, состоящей из атомов азота, атомов кислорода и атомов серы, которые могут быть окислены. Гетероциклоалкил может быть частично ненасыщенным или может конденсироваться с бензольным кольцом. Однако соединенные мостиковой связью азациклические углеводороды из этого определения исключены. Гетероциклоалкил может включать такие радикалы, как азиридинил, азетидинил, пирролизинил, пиперидинил, гомопиперидинил, морфолинил, тиоморфолинил, пиперазинил, тетрагидрофуранил, тетрагидротиофенил, дигидрооксазолил, тетрагидропиранил, тетрагидротиопиранил, индолинил, тетрагидрохинолил, тетрагидроизохинолил и бензоксазинил, предпочтительно дигидрооксазолил, оксадиазолил, оксадиазоланил и фуранил.
Термин "гетероциклоалкенил” означает частично замещенный "гетероциклоалкил”.
Термин "циклический амино" означает, среди групп, определенных в "гетероциклоалкиле", моновалентный 3-8-членный неароматический циклический амин, который имеет по меньшей мере один атом азота и может иметь один или более одинаковых или разных гетероатомов, выбранных из группы, состоящей из атомов азота, атомов кислорода и атомов серы, которые могут быть окислены, причем по меньшей мере один атом азота имеет связь. Однако соединенные мостиковой связью азациклические углеводороды из этого определения исключены. “Циклический амино” может включать такие радикалы, как азиридино, азетидино, пирролидино, пиперидино, гомопиперидино, морфолино, тиоморфолино и пиперазино.
Термин "арил" обозначает ароматическую углеводородную группу и может включать фенил, нафтил и инденил, предпочтительно C6-C10 арил, и более предпочтительно фенил.
Термин "гетероарил" означает моновалентную 5- или 6-членную ароматическую гетероциклическую группу, имеющую один или более одинаковых или разных гетероатомов, выбранных из группы, состоящей из атомов азота, кислорода и серы, и может конденсироваться с бензольным кольцом. "Гетероарил" может включать такие радикалы, как пиридил, пиразинил, пиримидинил, пиридазинил, пирролил, пиразолил, имидазолил, оксазолил, тиазолил, тиенил, фурил, оксадиазолил, тиадиазолил, хинолил, изохинолил, бензотиазолил, бензоксазолил, индолил, индазолил, хиноксалил и хиназолил, предпочтительно пиридазинил, пиридил, пиразинил, тиазолил, пиразолил и тиоксазолил.
Термин "соединенная мостиковой связью кольцевая группа" означает "соединенный мостиковой связью циклический углеводород" и " соединенный мостиковой связью азациклический углеводород".
Термин "соединенный мостиковой связью циклический углеводород" является насыщенной или ненасыщенной, бициклической или полициклической соединенной мостиковой связью углеводородной группой, имеющей два или три C3-C10 циклоалкильных кольца. Не соединенные мостиковой связью циклоалкилы из этого определения исключены. Бициклические или полициклические соединенные мостиковой связью C4-C16 углеводородные группы являются особенно предпочтительными. Соединенный мостиковой связью циклический углеводород может включать такие радикалы, как бицикло[2.1.1]гексил, бицикло[2.2.1]гептил, бицикло[2.2.2]октил, бицикло[4.3.1]децил, бицикло[3.3.1]нонил, борнил, борненил, норборнил, норборненил, 6,6-диметилбицикло[3.1.1]гептил, трициклобутил и адамантантил, предпочтительно адамантантил или бицикло[2.2.1]гептил.
Термин "соединенный мостиковой связью азациклический углеводород" является насыщенной или ненасыщенной, бициклической или полициклической соединенной мостиковой связью углеводородной группой, в которой по меньшей мере один из атомов, составляющих кольцо, является атомом азота. Не соединенные мостиковой связью гетероциклоалкилы из этого определения исключены. Бициклические или полициклические C4-C16 соединенные мостиковой связью азауглеводородные группы являются особенно предпочтительными. Термин “соединенный мостиковой связью азациклический углеводород” может включать такие радикалы, как азанорборнил, хинуклидинил, изохинуклидинил, тропанил, азабицикло[3.2.1]октанил, азабицикло[2.2.1]гептанил, 2-азабицикло[3.2.1]октанил, азабицикло[3.2.1]октанил, азабицикло[3.2.2]нонанил, азабицикло[3.3.0]нонанил и азабицикло[3.3.1]нонанил, предпочтительно тропанил, 2-окса-5-азабицикло[2.2.1]гепт-5-ил.
Термин "ацил" означает -C (=0) -низший алкил, -C (=0) -циклоалкил, -C (=0) -гетероциклоалкил, -C (=0) -арил, -C (=0) -гетероарил, карбамоил, низший алкилкарбамоил, -C (=0) -C (=0)-NH-низший алкил, циклоалкилкарбамоил, гетероциклоалкилкарбамоил, арилкарбамоил и гетероарилкарбамоил. Термин "низший алкил," "циклоалкил," "гетероциклоалкил", "арил" и "гетероарил" имеют указанные выше значения.
X в формуле (I) предпочтительно обозначает CH.
R1 в формуле (I) предпочтительно обозначает -H. R2 в формуле (I) предпочтительно обозначает -H или CH3 и более предпочтительно -H.
R41 в формуле (I) предпочтительно обозначает -H.
Кроме того, R42 в формуле (I) предпочтительно обозначает адамантантил или тропанил, каждый из которых может быть замещен ОН.
Кроме того, R5 в формуле (I) предпочтительно обозначает карбамоил, который может быть замещен либо -C (=O) -низший алкил, который может иметь ОН, более предпочтительно -CONH2, либо гидроксиацетил. Как вариант, R41 и R5 связаны через определенную функциональную группу с образованием циклической структуры, описанной выше, предпочтительно формулы (I-C).
В качестве заместителей, которые могут использоваться для "который может быть замещен" в отношении R1, R2, R3, R41, R42 и/или R5, включены следующие группы, описанные в параграфах от (a) до (g):
(a) Галоген
(b) -OH, -O-RZ, -O-фенил, -OCO-RZ, -OCONH-RZ, оксо (=O);
(c) -SH, -S-RZ, -S-фенил, -S-гетероарил, -SO-RZ, -SO-фенил, -SO-гетероарил, -SO3H, -SO2-RZ, -SO2-фенил, -SO2-гетероарил, сульфамоил, который может быть замещен одной или двумя группами RZ.
(d) Амино, который может быть замещен одной или двумя группами RZ, -NHCO-RZ, -NHCO-фенил, -NHCO2-RZ, -NHCONH2, -NHCONH-RZ, -NHSO2-R0, -NHSO2-фенил, -NHSO2NH2, -NO2, =N-O-RZ;
(e) -CHO, -CO-RZ, -CO2H, -CO2-RZ, карбамоил, который может быть замещен одной или двумя группами RZ, -СО-циклический амино, -COCO-RZ, циано;
(f) RZ;
(g) Фенил, который может быть замещен одной или более группами, выбранными из заместителей, описанных выше в параграфах от (a) до (f), 5- или 6-членный гетероциклоалкил, 5- или 6-членный гетероарил, 5- или 6-членный гетероциклоарил.
RZ в вышеупомянутых параграфах от (a) до (g) может включать "циано; -ОН; и низший алкил, который может быть замещен одной-тремя группами, выбранными из группы, состоящей из -O-низшего алкила, -NH-низшего алкила, -CONН-низшего алкила, 5- или 6-членного гетероциклоалкила и 5- или 6-членный гетероарила".
Соединение согласно настоящему изобретению может включать геометрические изомеры и таутомерные изомеры в зависимости от типа компонента. Кроме того, соединение согласно настоящему изобретению может иметь асимметрические атомы углерода. Все изомеры, включая разделенные изомеры и их смеси, включены в рамки настоящего изобретения. Кроме того, меченые соединения, то есть соединения, полученные замещением одного или более атомов соединения согласно настоящему изобретению радиоактивными или нерадиоактивными изотопами, также включены в рамки настоящего изобретения.
Кроме того, фармацевтически приемлемое пролекарство соединения согласно настоящему изобретению также включено в рамки настоящего изобретения. Фармацевтически приемлемое пролекарство представляет собой соединение, имеющее группу, которая может быть преобразована в аминогруппу, гидроксильную группу, карбоксильную группу и т.д. через сольволиз или в физиологических условиях. Группы, описанные в Prog. Med., Vol. 5, p. 2157-2161, 1985 и "Iyakuhin No Kaihatsu (Development of Medicines)" (Hirokawa Pub. Co., 1990), Vol. 7, Molecular Design, p. 163-198, взяты в качестве примеров групп, образующих такие пролекарства.
Соединение, представленное формулой (I), может образовывать соли присоединения с кислотой или основанием. Эти соли должны быть фармацевтически приемлемыми солями. Более конкретно, соли могут включать соль присоединения с неорганической кислотой (например, соляной кислотой, бромистоводородной кислотой, йодистоводородной кислотой, серной кислотой, азотной кислотой и фосфорной кислотой), и соль присоединения с органической кислотой (например, муравьиной кислотой, уксусной кислотой, пропионовой кислотой, щавелевой кислотой, малоновой кислотой, янтарной кислотой, фумаровой кислотой, малеиновой кислотой, молочной кислотой, яблочной кислотой, винной кислотой, лимонной кислотой, метансульфоновой кислотой, этансульфоновой кислотой, аспарагиновой кислотой и глутаминовой кислотой); соль с неорганическим основанием (например, натрием, калием, магнием, кальцием и алюминием) и соль с органическим основанием (например, метиламином, этиламином, этаноламином, лизином и орнитином); соль аммония; и т.п.
Кроме того, различные гидраты, сольваты и кристаллические полиморфные формы соединения, представленного формулой (I), и его солей также включены в рамки настоящего изобретения.
СПОСОБ
Соединение согласно настоящему изобретению может быть получено с использованием характеристик, основанных на основном скелете или типе его заместителя и с применением различных известных способов синтеза. В ходе получения защита соответствующей функциональной группы подходящей защитной группой или замена соответствующей функциональной группы группой, которая может быть легко преобразована в функциональную группу на стадии исходного вещества или промежуточного соединения, может иногда оказаться эффективной в зависимости от типа функциональной группы в технологии получения. Этот вид функциональной группы может включать, например, аминогруппу, гидроксильную группу и карбоксильную группу. Защитная группа для такой функциональной группы может включать, например, защитные группы, описанные в "Protective Groups in Organic Synthesis (3rd. Ed, 1999)", T. W. Greene и P. G. Wuts, и могут выбираться и использоваться по мере необходимости в зависимости от условий реакции. В этом виде способа желаемый компонент может быть получен путем введения защитной группы, выполнения реакции и удаления защитной группы при необходимости или преобразования группы в желаемую группу.
Кроме того, пролекарство соединения согласно настоящему изобретению может быть получено путем введения определенной группы или выполнения реакции с использованием полученного соединения, представленного формулой (I), на стадии исходного вещества или промежуточного соединения, так же, как в случае вышеупомянутой защитной группы. Реакция может быть выполнена с использованием способов, известных специалисту, таких как обычная этерификация, амидирование и дегидрирование.
Сокращения, используемые в описании, являются следующими:
Получ: Пример получения номер; Прим: Пример номер; Структура: химическая структура; Rf-Syn: номер Примера, на который была сделана ссылка (номер указывает, что соответствующее соединение было получено согласно способу получения, подобному способу получения соединения, описанного в Примере, определяемом этим номером); ВЭЖХ: высокоэффективная жидкостная хроматография; TLC: тонкослойная хроматография; Rf: скорость расхода жидкости; Данные: данные ЯМР и/или данные MS; 1H-ЯМР: 1H-ядерный магнитный резонанс; MS: масс-спектрометрия; (M+H)+: (M+H)+; (M+Na)+: (M+Na)+; (М-Н)-: (М-Н)-.
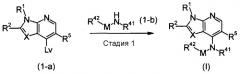
Первый способ
[где R1, R2, R41, R42, R5, М и Х имеют указанные выше значения, а Lv обозначает удаляемую группу].
В этом способе соединение, представленное формулой (I-a) и содержащее удаляемую группу, вводят в реакцию с амином, представленным формулой (I-b), чтобы получить соединение согласно настоящему изобретению, представленное формулой (I). Удаляемая группа Lv может включать галоген (например, хлор и бром); сульфонилокси (например, метансульфонилокси, этансульфонилокси, бензолсульфонилокси, п-толуолсульфонилокси, п-нитробензолсульфонилокси и трифторметансульфонилокси); и т.д.
На Стадии 1 удаляемую группа Lv соединения, представленного формулой (I-a) замещают амином. Эту реакцию выполняют при атмосферном давлении или под давлением в отсутствие растворителя или в присутствии подходящего растворителя.
Растворитель может включать, например, ароматические углеводороды (например, толуол и ксилол); кетоны (например, ацетон и метилэтилкетон); простые эфиры (например, диэтиловый эфир, тетрагидрофуран (ТГФ), диоксан и диэтоксиэтан); спирты (например, метанол (MeOH), этанол (EtOH), 2-пропанол (i-PrOH), и 1-бутанол (н-BuOH)); галогенированные углеводороды (например, дихлорметан, 1,2-дихлорэтан, хлороформ и тетрахлорметан); ацетонитрил; апротонные растворители (например, диметилформамид (DMF), 1,3-диметил-2-имидазолидинон, N-метилпирролидон (NMP) и диметилсульфоксид (диметилсульфоксид)); воду; или их смесь. Предпочтительно, реакцию выполняют в присутствии основания, и основание может включать, например, карбонаты щелочных металлов (например, карбонат натрия и карбонат калия); гидрокарбонаты щелочных металлов (например, гидрокарбонат натрия и гидрокарбонат калия); алкоголяты (например, метилат натрия, этилат натрия и трет-бутоксид калия); третичные амины (например, триэтиламин, трибутиламин и диизопропилэтиламин); органические основания (например, 1,8-диазабицикло[5.4.0]ундека-7-ен, пиридин и диметилпиридин). Однако может также использоваться избыток соединения (I-b). Хотя температура реакции отличается в зависимости от типа исходного соединения и условий реакции, реакция может обычно выполняться при температуре приблизительно в пределах от температуры окружающей среды до температуры кипения растворителя. Реакция может также обычно выполняться в присутствии основания, такого как гидроксид натрия и карбонат натрия, в органическом растворителе, инертном к реакции, таком как N,N-диметилформамид и N,N-диметилацетамид, при температуре окружающей среды при нагревании. Кроме того, амин, представленный формулой (I-b), может также использоваться в качестве соли для реакции.
Кроме того, при нагревании также может быть выполнено микроволновое облучение. Кроме того, реакция может также быть выполнена путем реакции сочетания с использованием реагентов фосфора, таких как 2-(ди-трет-бутилфосфино)дифенил, и палладиевого катализатора, такого как ацетат палладия, в присутствии основания, такого как карбонат цезия.
Для реакции возможно использовать способы, описанные в Примере(ах) получения или в Примере(ах) настоящего описания, или подобные им способы. Соединение, представленное формулой (I-a), может таким образом быть получено с использованием известных способов, способов, очевидных для специалиста, или способов, описанных в сравнительных примерах или Примерах настоящего описания или подобных им способов.
Второй способ
[где R1, R2, R41, R42, R5, М и Lv имеют указанные выше значения].
В этом способе соединение нитропиридина, представленное формулой (2-a), вводят в реакцию с амином, представленным формулой (2-b), и удаляемую группу во втором положении замещают амином, чтобы получить соединение аминонитропиридина, представленное формулой (2-c). Полученное соединение используют, чтобы получить соединение согласно настоящему изобретению, представленное формулой (i-2).
Способ, используемый на Стадии 1 первого способа, может быть включен в Стадию 2-1. Амин, представленный формулой (2-b), может также использоваться в качестве соли для реакции.
На Стадии 2-2 в случае, когда -R2 обозначает -H, имидазольное кольцо может быть образовано реакцией ортоформиата, такого как этилортоформиат, в присутствии кислотного катализатора. Желательно, чтобы нитрогруппа была восстановлена перед использованием ортоформиата для реакции. Кроме того, способ, который используется в случае, когда синтезируют соединение, представленное формулой (I-2), в которой -R2 не обозначет -H, может включать, например, способ, в котором аминогруппа соединения, представленного формулой (2-c), ацилируется заранее, способ, в котором тетраалкилортокарбонат или алкилизотиоцианат используются вместо ортоформиата, и способ, в котором карбоновая кислота или ангидрид карбоновой кислоты вводят в реакцию с сильной кислотой, такой как сульфокислота. Эти действия могут быть выполнены в растворителе, инертном к реакциям, или в отсутствие растворителя, при температуре окружающей среды при нагревании или при нагревании с обратным холодильником.
Третий способ
[где R1, R2, R42, X и М имеют значения, определенные выше].
В этом способе соединение согласно настоящему изобретению, представленное формулой (3-a) и содержащее карбоксильную группу, используется как исходное соединение для получения соединения согласно настоящему изобретению, представленное формулой (I-3).
На Стадии 3 карбоксильную группу соединения, представленного формулой (3-a), вводят в реакцию с азидирующим агентом, таким как дифенилфосфорилазид (DPPA) и азид натрия, с образованием имидазолонового кольца согласно так называемой реакции перегруппировки Куртиуса. Предпочтительно, реакцию проводят в присутствии основания.
Обычно в качестве основания может использоваться триэтиламин, пиридин и т.д., и реакция может быть выполнена при температуре окружающей среды при нагревании или при нагревании с обратным холодильником.
Четвертый способ
[где R1, R2, R42, М, Х и Lv имеют указанные выше значения].
В этом способе соединение с карбоксильной группой, представленное формулой (4-a), вводят в реакцию с гидразиновым производным, представленным формулой (4-b), чтобы получить гидразид, представленный формулой (4-c). Из этого гидразида получают соединение согласно настоящему изобретению, представленное формулой (i-4).
Стадия 4-1 может быть выполнена аналогично реакции, в которой соединение, представленное формулой (4-a), и соединение, представленное формулой (4-b), конденсируют амидированием. Соединение (4-a) может использоваться в форме свободной кислоты для реакции, и его реакционоспособное производное может также использоваться для реакции. Реакционоспособное производное соединения (4-a) может включать галогенангидрид кислоты (например, хлорангидрид кислоты и бромангидрид кислоты); обычный сложный эфир (например, сложный метиловый эфир, сложный этиловый эфир и сложный бензиловый эфир); азид кислоты; активированный сложный эфир с N-гидроксибензотриазолом (HOBt), п-нитрофенилом или N-гидроксисукцинимидом); симметричный ангидрид кислоты; смешанный ангидрид кислоты с алкиловым эфиром галогенкарбоновой кислоты (например, карбонат галогеналкила), пивалоилгалогенид, хлорангидрид п-толуолсульфоновой кислоты и т.д.; и смешанный ангидрид кислоты, такой как смешанный ангидрид фосфорной кислоты, полученный реакцией с дифенилфосфорилхлоридом или N-метилморфолином; и т.д.
Когда соединение (4-a) вводят в реакцию в форме свободной кислоты или вводят в реакцию без выделения активированного сложного эфира, предпочтительно использовать конденсирующее средство, такое как дициклогексилкарбодиимид (DCC), 1,1'-карбонилбис-1H-имидазол (CDI), дифенилфосфорилазид (DPPA), диэтилфосфорилцианид (DEPC) и 1-этил-3-(3-диметиламинопропил)карбодиимид гидрохлорид (EDCI HCl).
Реакцию проводят в органическом растворителе, инертном к реакции, таком как галогенированные углеводороды, ароматические углеводороды, простые эфиры, сложные эфиры (например, этилацетат), ацетонитрил, DMF и ДМСО, при охлаждении, при охлаждении до температуры окружающей среды или при температуре окружающей среды при нагревании, хотя условия отличаются в зависимости от реакционоспособного производного или конденсирующего средства, которые используются.
Для спокойного протекания реакции иногда предпочтительно использовать для реакции избыток соединения (4-b), или реакцию проводят в присутствии основания, такого как N-метилморфолин, триметиламин, триэтиламин, диизопропилэтиламин, N,N-диметиланилин, пиридин, 4-(N,N-диметиламино)пиридин, пиколин и диметилпиридин. Пиридин может также использоваться в качестве растворителя.
Способ, используемый на Стадии 1 первого способа, может быть включен в Стадию 4-2.
Пятый способ
[где R1, R2, R41, R42 и М имеют значения, определенные выше, R' является подходящим заместителем. Карбоновая кислота, представленная формулой (5-f), может быть коммерческим продуктом или может быть получена с использованием коммерческого продукта].
На стадии 5-2, стадии 5-4 и стадии 5-6 проводят реакцию с образованием оксадиазольного кольца на R5.
На стадии 5-1 проводят реакцию для синтеза гидразида кислоты из карбоновой кислоты, представленной формулой (5-a). Кроме того, промежуточное соединение, представленное формулой (5-c), может также синтезироваться из карбоновой кислоты, представленной формулой (5-a). Реакция на стадии 4-1 может быть включена в каждую из этих реакций.
На стадии 5-2, стадии 5-4 и стадии 5-6 реакцию с образованием оксадиазольного кольца проводят при температуре окружающей среды при нагревании. Для развития реакции может быть добавлено органическое основание.
На стадии 5-5 ароматическое нитрильное соединение, представленное формулой (5-d), вводят в реакцию с гидроксиламином, чтобы получить гидроксиамидин, представленный формулой (5-e). Полученный гидроксиамидин вводят в реакцию с карбоновой кислотой, представленной формулой (5-f), чтобы получить соединение согласно настоящему изобретению, представленное формулой (I-53).
На стадии 5-5 реакцию со свободным гидроксиламином или гидрохлоридом гидроксиламина проводят в присутствии основания, в результате чего может быть получен гидроксиамидин, представленный формулой (5-e).
Реакция может быть выполнена в растворителе, инертном к реакции. Растворитель может включать, например, спирты (например, метанол (MeOH), этанол (EtOH) и 2-пропанол (iPrOH)); ароматические углеводороды (например, толуол и ксилол); простые эфиры (например, диэтиловый эфир, тетрагидрофуран (ТГФ), диоксан и диэтоксиэтан); галогенированные углеводороды (например, дихлорметан, 1,2-дихлорэтан, хлороформ и тетрахлорметан); апротонные растворители (например, DMF, 1,3-диметил-2-имидазолидинон и диметилсульфоксид); воду или их смесь. Обычно для реакции используются спирты. В случае, когда для реакции используется гидрохлорид гидроксиламина, как описано выше, предпочтительно реакцию проводят в присутствии основания, и основание может включать, например, карбонаты щелочных металлов (например, карбонат натрия и карбонат калия); гидрокарбонаты щелочных металлов (например, гидрокарбонат натрия и гидрокарбонат калия); алкоголяты (например, метилат натрия, этилат натрия и трет-бутоксид калия); третичные амины (например, триэтиламин и диизопропилэтиламин); и органические основания (например, 1,8-диазабицикло[5.4.0]ундека-7-ен, пиридин и диметилпиридин). Хотя температура реакции различается в зависимости от типа исходного соединения и условий реакции, реакция может обычно выполняться при температуре приблизительно в пределах от температуры окружающей среды до температуры кипения растворителя. Реакция может обычно выполняться в присутствии основания, такого как карбоната натрия, в органическом растворителе, инертном к реакции, таком как метанол, при температуре окружающей среды при нагревании.
Стадия 5-6 состоит из двух стадий: ацилирование гидроксиамидина и последующая циклизация. Промежуточный способ получения на стадии 4-1 может быть включен в ацилирование на первой стадии. Однако реакция обычно выполняется при температуре окружающей среды при нагревании или при нагревании с обратным холодильником. Циклизация на второй стадии может быть осуществлена путем выделения и очистки ацила и нагревания ацила в органическом растворителе, инертном к реакции, таком как этанол и диоксан, в присутствии или в отсутствие основания. Основание может включать неорганическое основание, такое как ацетат натрия, или органическое основание, такое как диизопропилэтиламин. Реакция, состоящая из этих двух стадий, может быть выполнена в одно действие путем проведения обычного ацилирования и затем непосредственным нагреванием реакционной смеси или осуществлением реакции под микроволновым облучением.
Растворитель может включать, например, ароматические соединения (например, толуол, ксилол и пиридин); простые эфиры (например, диэтиловый эфир, тетрагидрофуран, диоксан и диэтоксиэтан); галогенированные углеводороды (например, дихлорметан, 1,2-дихлорэтан, хлороформ и тетрахлорметан); ацетонитрил; апротонные растворители (например, DMF, N,N-диметилацетамид (DMA), 1,3-диметил-2-имидазолидинон, N-метилпирролидон (NMP) и диметилсульфоксид)); воду; или их смесь. Хотя температура реакции различается в зависимости от типа исходного соединения и условий реакции, реакция может быть выполнена при температуре окружающей среды при нагревании.
Шестой способ
[где R1, R2, R42, М и Lv имеют значения, определенные выше; R" является подходящим заместителем].
На стадии 6, в случае, когда соединение, представленное формулой (6-a), вводят в реакцию с первичным амином, представленным формулой (6-b), после ipso-замещения, оксадиазольное кольцо раскрывают, чтобы создать аминопиразолоновое кольцо. Условия реакции, описанные на стадии 1, могут быть включены в качестве условий этой реакции. Реакцию можно выполнять при температуре от температуры окружающей среды до температуры кипения.
Кроме того, некоторые из соединений, представленных формулой (I), могут также быть получены из соединения согласно настоящему изобретению, полученного, как описано выше, соответствующей комбинацией способов, обычно используемых специалистом, таких как известное алкилирование, ацилирование, замещение, окисление, восстановление, гидролиз, удаление защитной группы, галогенирование и реакция Манниха. Например, когда соединение согласно настоящему изобретению, в котором -R5 обозначает -CO2H, получают из соединения согласно настоящему изобретению, в котором R5 обозначает низший алкилоксикарбонил, может использоваться гидролиз, как в способе, описанном в "Jikken Kagaku Koza (Courses in Experimental Chemistry) (5th Ed., 2003)". Кроме того, когда соединение согласно настоящему изобретению, в котором R5 обозначает галоген, получают из соединения согласно настоящему изобретению, в котором как R3, так и R5 обозначают -H, может использоваться галогенирование, как в способе, описанном в "Jikken Kagaku Koza (Courses in Experimental Chemistry) (5th Ed., 2003)." Кроме того, когда соединение согласно настоящему изобретению, в котором R3 обозначает низший алкил, замещенный группой, выбранной из группы, состоящей из моно(низший алкил)амино, ди(низший алкил)амино и циклического амино, получают из соединения согласно настоящему изобретению, в котором R3 обозначает -H, может использоваться реакция Манниха, как в способах, описанных в "Jikken Kagaku Koza (Courses in Experimental Chemistry) (5th Ed., 2003)"; C. Mannich et al., Arch. Pharm., 1912, Vol. 250, p. 647; J. H. Brewster et al., Org. React., 1953, Vol. 7, p. 99; F. F. Blicke, Org. React., 1942, Vol. 1, p. 303; K. W. Merz et al., Pharmazie, 1956, Vol. 11, p. 505; и т.д.
Способы, которые обычно используются специалистом, не только используются для получения соединения согласно настоящему изобретению, но могут также использоваться для получения промежуточных соединений, которые образуются в процессе получения. Эти способы могут также использоваться в последующих способах.
Соединение, полученное, как описано выше, находится в свободной форме или подвергается солеобразующей обработке с использованием обычного способа, и его выделяют и очищают в форме его соли. Выделение и очистку проводят, выполняя обычные химические операции, такие как экстракция, к