Способ ионообменного разделения метионина и глицина
Иллюстрации
Показать всеИзобретение относится к способу ионообменного разделения метионина и глицина и может найти применение в биохимической, фармацевтической и пищевой промышленности. Способ заключается в том, что разделение метионина и глицина осуществляют в две стадии, на первой стадии проводят сорбцию аминокислот с обогащением фазы сорбента глицином, а раствора на выходе - метионином, для этого готовят полиамфолит Purolite S950 в H+-форме, проводят сорбцию смеси двух алифатических аминокислот в противоточной колонне с неподвижным слоем сорбента, для этого снизу пропускают раствор, содержащий смесь глицина и метионина, при этом глицин сорбируется на полиамфолите Purolite S950, на выходе появляется метионин, водный раствор которого собирают в приемник на выходе из колонны, через некоторое время - смесь аминокислот, сорбцию останавливают, в течение сорбции производят отбор проб через определенные промежутки времени, контролируют суммарную концентрацию аминокислот иодометрическим методом, метионина - спектрофотометрическим методом, глицина - по разности концентраций: суммарной и метионина, степень разделения исходного раствора составляет 60%, на второй стадии проводят элюирование глицина раствором соляной кислоты с рН 1,2 из сорбента с подачей сверху, элюат, содержащий глицин, собирают в приемник, степень концентрирования глицина составляет 70%, после десорбции глицина проводят полную десорбцию смеси аминокислот, полиамфолит принимает исходную форму и готов к работе, при этом также отбирают пробы через определенные промежутки времени и проводят анализ каждой пробы иодометрическим и спектрофотометрическим методами, для полного отделения глицина от метионина повторяют двустадийный процесс разделения смеси аминокислот, полученной на выходе из колонны. Предлагаемый способ позволяет эффективно разделять метионин и глицин сочетанием процессов сорбции и десорбции, исключив при этом стадию регенерации сорбента, и уменьшить объемы промывных вод без использования значительного количества вспомогательных реактивов. 2 ил., 2 табл.
Реферат
Изобретение относится к способам разделения и выделения индивидуальных алифатических аминокислот из их смесей и может быть использовано в биохимической, фармацевтической и пищевой промышленности.
Наиболее близким по технической сущности и достигаемому эффекту является способ классической ионообменной хроматографии [А.с. СССР N 979991, G01N 31/08, 1981], в основе которого лежит сорбция молекул вещества неподвижной фазой, обусловленная их электростатическим связыванием с поверхностью пористых гранул твердого гидрофильного сорбента, находящегося в контакте с раствором.
Недостатками являются использование для регенерации сорбента большого количества вспомогательных реактивов, наличие стадии предварительной подготовки растворов аминокислот перед пропусканием их через ионообменник и протекание в системе ионообменник - сорбент различных необменных взаимодействий, что осложняет процесс выделения аминокислот и приводит к большим объемам промывных вод и низкой эффективности разделения.
Техническая задача изобретения заключается в разработке способа ионообменного разделения метионина и глицина, позволяющего увеличить эффективность разделения смеси аминокислот, исключить из технологического процесса большое количество вспомогательных реактивов, уменьшить объемы и степень загрязнения сточных вод.
Для решения технической задачи изобретения предложен способ ионообменного разделения метионина и глицина, характеризующийся тем, что разделение алифатических аминокислот метионина и глицина осуществляют в две стадии, на первой стадии проводят сорбцию аминокислот с обогащением фазы сорбента глицином, а раствора на выходе - метионином, для этого готовят полиамфолит Purolite S950 в H+-форме, проводят сорбцию смеси двух алифатических аминокислот в противоточной колонне с неподвижным слоем сорбента, для этого снизу пропускают раствор, содержащий смесь глицина и метионина, при этом глицин сорбируется на полиамфолите Purolite S950, на выходе появляется метионин, водный раствор которого собирают в приемник на выходе из колонны, через некоторое время - смесь аминокислот, сорбцию останавливают, в течение сорбции производят отбор проб через определенные промежутки времени, контролируют суммарную концентрацию аминокислот йодометрическим методом, метионина - спектрофотометрическим методом, глицина - по разности концентраций: суммарной и метионина, степень разделения исходного раствора составляет 60%, на второй стадии проводят элюирование глицина раствором соляной кислоты pH 1,2 из сорбента с подачей сверху, элюат, содержащий глицин, собирают в приемник, степень концентрирования глицина составляет 70%, после десорбции глицина проводят полную десорбцию смеси аминокислот, полиамфолит принимает исходную форму и готов к работе, при этом также отбирают пробы через определенные промежутки времени и проводят анализ каждой пробы йодометрическим и спектрофотометрическим методами, для полного отделения глицина от метионина повторяют двустадийный процесс разделения смеси аминокислот, полученной на выходе из колонны.
Технический результат заключается в увеличении эффективности разделения смеси аминокислот, исключении из технологического процесса вспомогательных реактивов, повышении выхода аминокислот и уменьшении объемов промывных вод.
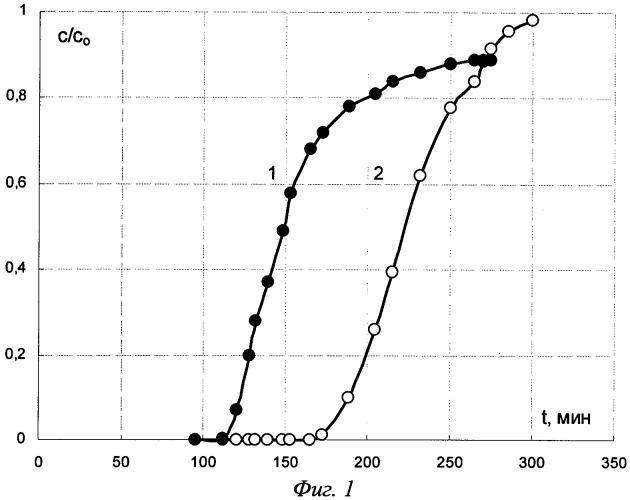
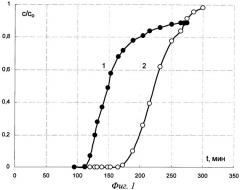
На фиг.1 представлены зависимости отношения концентрации аминокислоты в растворе на выходе из колонны к исходной концентрации (c/c0) от времени сорбции (t, мин) метионина (кривая 1) и глицина (кривая 2) на Purolite S950 (H+) при 298 К и скорости пропускания 7 см3/мин.
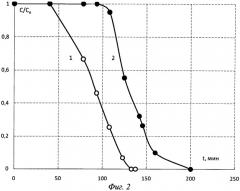
На фиг.2 представлены зависимости отношения концентрации аминокислоты в элюате к концентрации в смоле (c/c0) от времени десорбции (t, мин) глицина (кривая 1) и метионина (кривая 2) из Purolite S950 раствором соляной кислоты с рН 1,2 и скоростью пропускания 8 см3/мин.
Способ ионообменного разделения алифатических аминокислот глицина и метионина из водных растворов реализуют следующим образом.
Разделение аминокислот проводится в две стадии: первая стадия - сорбция смеси аминокислот с обогащением жидкой фазы метионином, а твердой фазы глицином, вторая стадия - элюирование с обогащением раствора глицином.
В колонну загружают полиамфолит Purolite S950; подготовку смолы осуществляют следующим образом: пропускают через слой ионообменника последовательно раствор КОН с концентрацией 0,5 моль/дм3, дистиллированную воду, раствор соляной кислоты с концентрацией 0,5 моль/дм3, воду до полного удаления соляной кислоты из межгранульного пространства, полиамфолит переведен в Н+-форму и готов к использованию; проводят сорбцию, для этого снизу пропускают раствор, содержащий смесь глицина и метионина, на выходе из колонны первым появляется метионин, через некоторое время - смесь аминокислот, степень разделения исходного раствора составляет 60%, сорбцию прекращают. В течение сорбции через определенные промежутки времени отбирают пробы раствора на выходе из колонны. Суммарную концентрацию аминокислот в растворе определяют йодометрическим методом. Концентрацию метионина в отобранных пробах определяют спектрофотометрическим методом. Концентрацию глицина рассчитывают по разнице между суммарной концентрацией аминокислот и метионина.
На второй стадии осуществляют десорбцию глицина из полиамфолита раствором соляной кислоты с pH 1,2 с подачей элюента сверху. Степень концентрирования глицина составляет 70%. В течение десорбции проводят анализ отобранных через определенные промежутки времени растворов йодометрическим и спектрофотометрическим методами. После элюирования глицина и смеси аминокислот полиамфолит принимает исходную форму и готов к работе.
Для более глубокого разделения аминокислот ионообменный цикл, состоящий из двух стадий, повторяют.
Использование сорбента полиамфолитной природы позволяет достичь высокой степени разделения алифатических аминокислот (глицина и метионина), которые имеют схожие физико-химические характеристики и различаются длиной углеводородного радикала. Объемы разделяемых растворов и исходная концентрация аминокислот могут быть различны, поэтому требуемая производительность ионообменников варьируется, в связи с этим характеристики ионообменных колонн (высота, диаметр, скорость подачи раствора, объем сорбента и т.д.) подбираются для каждого случая отдельно.
Способ ионообменного разделения метионина и глицина поясняется следующим примером.
Пример. Разделение аминокислот проводят из водного раствора с содержанием глицина 0,025 моль/дм3 и метионина 0,0026 моль/дм3, приготовленного растворением аминокислот марки «Reanal» в дистиллированной воде. Сорбцию и десорбцию глицина осуществляют на амфолите Purolite S950 в H+-форме в колоне с внутренним диаметром 56 мм и высотой 158 мм. В колонну загружают полиамфолит Purolite S950, пропускают через слой ионообменника раствор КОН с концентрацией 0,5 моль/дм3, затем дистиллированную воду, после нее раствор соляной кислоты с концентрацией 0,5 моль/дм3 и снова воду до полного удаления соляной кислоты из межгранульного пространства. На первой стадии разделения проводят сорбцию, подавая в колонну раствор аминокислот снизу вверх со скоростью 7 см3/мин. Отбор проб на выходе из колонны осуществляют через 10 мин с точно фиксируемым временем для дальнейшего построения выходных кривых. Данные о ходе сорбции смеси глицин-метионин из водного раствора представлены в таблице 1.
Определение суммарной концентрации аминокислот в элюате осуществляют йодометрическим титрованием. Для этого в мерную колбу на 50 см3 пипеткой вносят 5 см3 исследуемого щелочного раствора, содержащего аминокислоту. Из цилиндра приливают 30 см3 свежеприготовленного фосфата меди, содержимое колбы доводят водой до метки, перемешивают и фильтруют через фильтр с синей лентой. Фильтрат должен быть прозрачным. Затем 10 см3 фильтрата пипеткой вносят в коническую колбу, добавляют 0,5 см3 ледяной уксусной кислоты и 7 см3 10% раствора йодида калия. После перемешивания выделившийся йод титруют из микробюретки раствором тиосульфата натрия с концентрацией 0,01 моль/дм3, прибавляя в конце титрования 1-2 капли свежеприготовленного раствора крахмала, точку эквивалентности определяют по исчезновению синей окраски.
Наличие метионина в отобранных пробах определяют спектрофотометрическим методом. Для этого в мерную колбу вносят объем раствора метионина, такой, чтобы его концентрация находилась в пределах градуировочного графика от 0,0005 до 0,001 моль/дм3, затем добавляют раствор азотной кислоты до pH 1 и доводят объем раствора до метки дистиллированной водой. Перед началом измерений на портативном спектрофотометре UVMini-1240 проводят калибровку прибора по дистиллированной воде. Затем в кювету наливают растворы, содержащие метионин (met), и измеряют оптическую плотность (A) в интервале длин волн от 190 до 250 нм. Для проверки соответствия максимума строят дифференциальный спектр поглощения, определяют оптическую плотность раствора при λ=211 нм. По градуировочной функции, построенной в координатах A=f(cmet), устанавливают концентрацию метионина и пересчитывают концентрацию в исходном растворе.
Концентрацию глицина в водном растворе определяют по разнице между суммарной концентрацией аминокислот и метионина. Результаты исследований представлены на фиг.1 и фиг.2.
Как видно на фиг.1, выделение метионина из раствора с глицином происходит в интервале времени от 110 до 175 мин от начала сорбции. Оптимальное время разделения глицина и метионина при сорбции составляет 150 мин от начала процесса, при этом степень разделения составляет 60%.
Процесс десорбции глицина из раствора с метионином осуществляется раствором соляной кислоты с концентрацией 0,1 моль/дм3, которая подается в колонну сверху вниз, со скоростью пропускания 8 см3/мин.
Контроль осуществляют отбором проб на выходе из колонны через каждые 10 мин и дальнейшим их анализом. Определения концентраций аминокислот осуществляют приведенным выше способом. Данные о ходе десорбции смеси глицин-метионин представлены в таблице 2.
Как видно из фиг.2, выходные кривые десорбции глицина и метионина расположены практически параллельно. Концентрирование глицина происходит на 70% в интервале времени элюирования от 40-110 мин.
При необходимости через колонну повторно пропускают смесь аминокислот, полученную ранее на выходе из колонны (содержащую глицин и оставшийся метионин). В результате на выходе получают раствор метионина, глицин сорбируется на смоле. После этого процесс элюирования глицина соляной кислотой и промывки сорбента водой повторяют.
Как видно из примера, таблиц и фигур, выделение метионина происходит на стадии сорбции смеси аминокислот, а выделение глицина - при элюировании, при этом ионит переходит в исходное рабочее состояние.
Предлагаемый способ ионообменного разделения метионина и глицина позволяет эффективно разделять алифатические аминокислоты - глицин и метионин из гидролизатов различного генезиса и биохимических сточных вод сочетанием процессов сорбции и десорбции, исключить стадию регенерации сорбента, использование значительного количества вспомогательных реактивов и стадию предварительной подготовки растворов аминокислот перед пропусканием через ионообменник, уменьшить объемы промывных вод.
| Таблица 1 | |||||||||||
| Способ ионообменного разделения метионина и глицина | |||||||||||
| № пробы | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 |
| Время отбора, мин | 95 | 112 | 132 | 162 | 215 | 250 | 265 | 270 | 275 | 285 | 300 |
| Суммарная концентрация, моль/дм3 | 0 | 0,00001 | 0,0007 | 0,0017 | 0,0118 | 0,022 | 0,0236 | 0,0248 | 0,0256 | 0,0264 | 0,027 |
| Концентрация метионина, моль/дм3 | 0 | 0,00001 | 0,0007 | 0,0017 | 0,00172 | 0,00219 | 0,00223 | 0,00218 | 0,00224 | 0,00205 | 0,00196 |
| Концентрация глицина, моль/дм3 | 0 | 0 | 0 | 0 | 0,01 | 0,02 | 0,021 | 0,0226 | 0,023 | 0,024 | 0,025 |
| Cгл/c0 гл | 0 | 0 | 0 | 0 | 0,395 | 0,777 | 0,838 | 0,887 | 0,916 | 0,955 | 0,982 |
| Cмет/c0 мет | 0 | 0,004 | 0,28 | 0,68 | 0,84 | 0,88 | 0,89 | 0,87 | 0,89 | 0,82 | 0,79 |
| Таблица 2 | |||||||||
| Способ ионообменного разделения метионина и глицина | |||||||||
| Номер пробы | 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 |
| Время отбора, мин | 40 | 78 | 93 | 108 | 123 | 142 | 147 | 160 | 200 |
| Суммарная концентрация, моль/дм3 | 0,03 | 0,02 | 0,0124 | 0,0076 | 0 | - | - | - | - |
| Концентрация глицина, моль/дм3 | 0,025 | 0,017 | 0,01 | 0,0053 | 0,0012 | 0 | - | - | - |
| Концентрация метионина, моль/дм3 | 0,0026 | 0,0026 | 0,0026 | 0,0025 | 0,0014 | 0,0008 | 0,0007 | 0,00002 | 0 |
| Cсумм/c0 сумм | 1 | 0,67 | 0,41 | 0,25 | 0 | - | - | - | - |
| Cгл/c0 гл | 1 | 0,68 | 0,4 | 0,212 | 0,048 | 0 | - | - | - |
| Cмет/c0 мет | 1 | 1 | 1 | 0,95 | 0,55 | 0,32 | 0,26 | од | 0 |
Способ ионообменного разделения метионина и глицина, характеризующийся тем, что разделение алифатических аминокислот метионина и глицина осуществляют в две стадии, на первой стадии проводят сорбцию аминокислот с обогащением фазы сорбента глицином, а раствора на выходе - метионином, для этого готовят полиамфолит Purolite S950 в Н+-форме, проводят сорбцию смеси двух алифатических аминокислот в противоточной колонне с неподвижным слоем сорбента, для этого снизу пропускают раствор, содержащий смесь глицина и метионина, при этом глицин сорбируется на полиамфолите Purolite S950, на выходе появляется метионин, водный раствор которого собирают в приемник на выходе из колонны, через некоторое время - смесь аминокислот, сорбцию останавливают, в течение сорбции производят отбор проб через определенные промежутки времени, контролируют суммарную концентрацию аминокислот иодометрическим методом, метионина - спектрофотометрическим методом, глицина - по разности концентраций: суммарной и метионина, степень разделения исходного раствора составляет 60%, на второй стадии проводят элюирование глицина раствором соляной кислоты с рН 1,2 из сорбента с подачей сверху, элюат, содержащий глицин, собирают в приемник, степень концентрирования глицина составляет 70%, после десорбции глицина проводят полную десорбцию смеси аминокислот, полиамфолит принимает исходную форму и готов к работе, при этом также отбирают пробы через определенные промежутки времени и проводят анализ каждой пробы иодометрическим и спектрофотометрическим методами, для полного отделения глицина от метионина повторяют двустадийный процесс разделения смеси аминокислот, полученной на выходе из колонны.