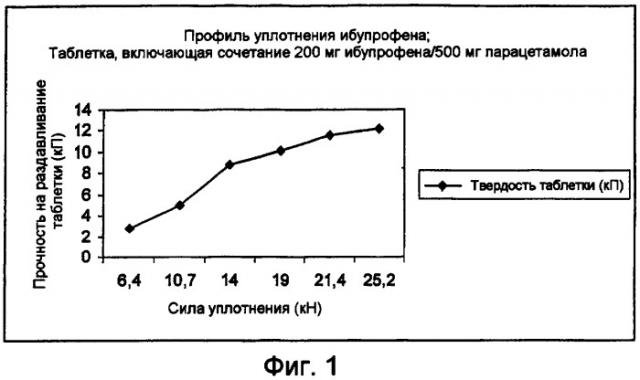
Композиция, включающая нпвс и парацетамол
Иллюстрации
Показать всеПредложен способ получения гранулированной композиции, включающий множество гранул отвержденного расплава, которые содержат нестероидное противовоспалительное средство (НПВС), выбранное из арилпропионовых кислот и арилуксусных кислот и парацетамол; причем способ включает стадии: (а) получение расплавленной смеси путем смешивания расплавленного НПВС в форме свободной кислоты и парацетамола, необязательно при наличии одного или нескольких эксципиентов; и (b) формирование на основе расплавленной смеси гранул отвержденного расплава. Предложены также гранулированная композиция, полученная заявленным способом, для лечения боли и/или воспаления, и/или лихорадочного состояния и соответствующая фармацевтическая композиция. Показано: заявленная гранулированная композиция позволяет сформировать таблетки с достаточной степенью твердости (прочность на раздавливание 6,9-7,1 кП) при растворимости 89% ибупрофена и парацетамола уже через 10 мин. 7 н. и 30 з.п. ф-лы, 6 ил., 4 табл.
Реферат
Настоящее изобретение относится к композициям, содержащим нестеридные противовоспалительные лекарственные средства, к способам их получения и применения.
Нестеридные противовоспалительные лекарственные средства (НПВС) представляют собой широко распространенный класс лекарственных средств. Они составляют четко определенную группу соединений и включают фенилпропионовые кислоты, такие как ибупрофен, напроксен, кетопрофен и флурбипрофен. Они используются преимущественно для лечения одного из нескольких состояний: боли, воспаления и лихорадки, например, ревматоидного артрита, анкилозирующего спондилита, остеоартрита, послеоперативной боли, послеродовой боли и повреждения мягких тканей.
НПВС представляют собой в основном кислотные и по существу нерастворимые лекарственные средства. Они обычно вводятся в виде пероральной фармацевтической композиции, имеющей форму таблеток. Соответственно, для сочетания с НПВС могут быть выбраны фармацевтически приемлемые эксципиенты, с которыми НПВС совместимы и с которыми могут быть сформированы таблетки с достаточной степенью твердости, способные быстро высвобождать лекарственное средство в организм с тем, чтобы оно было доступно для всасывания.
Основной проблемой, связанной с указанными выше расстройствами, является оптимизация начала действия НПВС, особенно в случае лечения боли. Считается, что быстрое разложение композиции приводит к быстрому разложению лекарственного средства в организме, что ведет к более раннему началу терапевтического действия в сравнении со стандартной дозированной формой. Соответственно, желательно получить твердую дозированную форму для перорального введения, которая была бы адаптирована для целей быстрого разложения в желудочно-кишечном тракте. Однако поскольку многие НПВС представляют собой кислые лекарственные средства, их всасывание может стать проблематичным в кислой среде желудка. Кроме того, хотя в литературе имеется много сообщений о композициях, приспособленных для быстрого высвобождения, тем не менее, основной проблемой, связанной с приемом ибупрофена и других НПВС, является то, что их необходимо вводить в относительно высоких дозах, то есть до 800 мг на стандартную дозу. Таким образом, возникает проблема, связанная с созданием дозированной формы, которая бы включала НПВС вместе с эксципиентами, используемыми для создания таблетированной дозированной формы, а также с эксципиентами, применяемыми для достижения быстрого разложения, но при этом таблетка не должна быть слишком большой, с тем, чтобы быть удобной для приема и чтобы такие таблетки можно было производить в стандартных условиях крупномасштабного производства. Кроме того, твердые стандартные дозированные формы должны обладать достаточной твердостью для получения в условиях жесткого процесса производства (например, в тех случаях, когда в процесс производства включается стадия нанесения пленочного покрытия в перфорированном вращающемся барабане, а также стадия упаковки в соответствующих условиях и т.п.), но при этом она должна обладать соответствующими характеристиками по разложению, с тем чтобы достигалось быстрое высвобождение лекарственного средства из композиции, и поддерживались соответствующие показатели растворения. Другой существенной проблемой, которую также необходимо преодолеть, является то, что композиция должна быть пригодна для прессования в условиях стандартной машины для таблетирования, так чтобы при этом удалось избежать прилипания композиции к штамповочным частям машины для таблетирования.
В заявке на Европейский патент №362728 (1990 год) описывается процедура получения порошка ибупрофена, который характеризуется легкой текучестью и улучшенными показателями хранения и соответствующими свойствами такой композиции, подходящими для непосредственного таблетирования. Считается, что процесс затвердевания расплавленного ибупрофена представляет собой чрезвычайно непростую задачу, поскольку расплавленный ибупрофен, который застывает при температуре примерно 74,8°С, становится маслянистым и вязким при охлаждении с тенденцией к переохлаждению и преобразуется в кристаллическое состояние лишь очень медленно. В соответствии с EP 362728 было предложено получать частицы ибупрофена в процессе отверждения расплавленного ибупрофена на контактном охлаждающем устройстве (например, на роллере или охлаждающем транспортере) при температуре 0-50°С, при введении затравки, с последующим дроблением. Было предложено вносить затравку путем нанесения расплавленного слоя, который застывает на контактном охладителе. Указанная затравка также может быть добавлена к роллеру в форме частиц или внесена в расплавленный продукт. Предполагается, что любой процесс получения расплавленного ибупрофена может использоваться для образования частиц ибупрофена, хотя наиболее подходящей является процедура получения расплавленного продукта путем ректификации ибупрофена, в соответствии со способом, описанным в заявке на патент Германии №3802619. Единственный пример, приведенный в указанном описании, позволяет увидеть, что порошок ибупрофена, получаемый в соответствии с описанным способом, должен быть смешан со значительным количеством дополнительных эксципиентов перед таблетированием.
В заявке на Европейский патент №686392 (1995 г.) описывается термический процесс получения гранул, пригодных для непосредственного таблетирования, который включает процесс экструзии в расплавленном состоянии активного соединения с низкой точкой плавления и необходимых для таблетирования вспомогательных веществ, при повышенной температуре с образованием гомогенного неагглютинирующего экструдата, который затем измельчают с образованием таблетируемых гранул. За счет функционирования смешивающих и разминающих элементов экструдера, смесь переводят в компактную форму с образованием экструдата в условиях температуры, при которой часть активного соединения плавится. Указанный экструдат прессуют через перфорированную пластинку с получением тонких тяжей диаметром 0,3-2,0 мм и измельчают после охлаждения с получением гранул с желательным размером частиц. Получаемые таким образом гранулы могут быть сразу подвергнуты таблетированию и при этом требуется только один замасливающий агент. Соответственно, активный ингредиент в этом случае имеет форму нерасплавленных кристаллов в отвержденном расплаве других активных ингредиентов. Отмечается, что в рамках данного процесса все вспомогательные компоненты, такие как связующее вещество, вспомогательные добавки, применяемые для разложения, наполнители и другие вспомогательные компоненты, могут быть включены непосредственно в состав гранул.
В контексте вышеуказанного следует отметить документ WO 01/41733 (The Boots Company PLC), в котором описывалось, что если включать агент, способствующий разложению, в расплавленный НПВС и тщательно смешать его с другими компонентами и затем охладить и размолоть до получения гранул, то будет создана композиция, подходящая для таблетирования с минимальным числом эксципиентов, нужных для таблетирования, и обладающая хорошими показателями для таблетирования, показателями разложения и растворения, если в эту композицию будет также включен диоксид кремния. Указанный способ был существенно усовершенствован в сравнении со способом, описанным в WO 02/098391. Таким образом, в рамках указанного способа НПВС образуется в виде гомогенного экструдата в ходе процесса экструзии расплава. В документе описаны предпочтительные условия охлаждения и обработки.
Все указанные выше способы относятся к производству таблеточных композиций, включающих НПВС в качестве единственного основного терапевтического агента. Поскольку наличие других агентов не исключается, то авторы изобретения уделяли первостепенное внимание получению НПВС.
Может возникнуть потребность в получении фармацевтической композиции, которая будет включать другой активный агент анальгетического действия, кроме НПВС, например, сочетанного продукта. Одним из таких анальгетических агентов, который был объединен с НПВС, является ацетаминофен (также измассатный как парацетамол), который проявляет анальгетические (ослабление боли) и антипиретические (ослабление лихорадки) свойства, но по существу не оказывает противовоспалительного эффекта. Такие продукты, в числе других свойственных им показателей, чрезвычайно эффективны для лечения боли и лихорадочного состояния, например, головой боли, мышечной боли и боли в суставах, боли в спине, при кашле, простуде и группе. Однако имеются также проблемы, связанные с созданием пероральной дозированной формы (например, таблеточной формы), содержащей парацетамол.
В частности, парацетамол представляет собой тонкоизмельченный мягкий порошок, и в качестве такового он не подходит для непосредственного прессования в таблетки. Соответственно, необходимо провести предварительную обработку парацетамола перед его прессованием до твердой дозированной формы. В типичном случае парацетамол подвергают влажной грануляции, в коде которой образуется гранулированная форма парацетамола и которую впоследствии смешивают с дополнительными таблеточными эксципиентами, а полученную смесь прессуют с получением таблеток. Альтернативно формы парацетамола, подходящие для непосредственного прессования, которые уже были подвергнуты предварительной обработке, могут быть получены от специализированных поставщиков. Такая потребность в предварительной обработке, как правило, повышает сложность и стоимость процесса получения твердых дозированных форм парацетамола. Кроме того, парацетамол в типичном случае вводится в относительно высоких дозах, например, до 500 мг на стандартную дозу. Соответственно, возникает проблема получения дозированной формы, которая включает парацетамол вместе с эксципиентами, применяемыми для создания таблеточной дозированной формы, и эксципиентами, используемыми для достижения быстрого разложения, но при этом такая таблетка не должна быть слишком крупной и должна быть комфортной для приема пациентом, а получение таких таблеток должно быть совместимо с процессом стандартного крупномасштабного производства. Соответственно, указанная проблема возрастает в случае объединения парацетамола с другим фармацевтически активным агентом (например, НПВС), который также может вводиться в относительно высокой дозе.
Настоящее изобретение направлено на поиски способа получения композиций, включающих и парацетамол, и НПВС, с тем чтобы указанный способ позволил преодолеть по меньшей мере некоторые из указанных выше недостатков. В частности, настоящее изобретение относится к разработке композиций, которые обладают свойствами к таблетированию с минимальным набором таблеточных эксципиентов, и характеризуется выгодными свойствами по таблетированию, показателями разложения и растворения.
Авторы изобретения обнаружили, что если смесь, включающую расплавленный НПВС и парацетамол, содержащиеся в ней, отверждать и формировать в гранулы, то указанные гранулы в типичном случае будут демонстрировать улучшенные показатели текучести, улучшенную способность к прессованию и могут быть подвергнуты непосредственному формированию в таблетки, которые в типичном случае будут также демонстрировать хорошие показатели разложения и растворения.
Соответственно, в первом аспекте настоящего изобретения предлагается способ получения гранулированной композиции, включающей множество отвержденных расплавленных гранул, содержащих нестероидное противовоспалительное средство (НПВС) и парацетамол, где указанный способ включает стадии
(а) формирования расплавленной смеси путем перемешивания расплавленного НПВС в форме свободной кислоты и парацетамола, необязательно при наличии одного или нескольких эксципиентов; и
(b) получения из расплавленной смеси отвержденных расплавленных гранул.
Такой способ далее в тексте называется как «способ согласно настоящему изобретению».
Предпочтительно стадия (а) согласно способу по настоящему изобретению имеет место при расплавлении в экструдере. Предпочтительно на стадии (b) расплавленную смесь охлаждают с получением отвержденного расплава и на основе отвержденного расплава получают множество отвержденных гранул расплава. Множество отвержденных гранул расплава может быть получено при измельчении отвержденного расплава.
Неожиданно было обнаружено, что гранулированная композиция, получаемая по способу согласно настоящему изобретению, в типичном случае демонстрирует улучшенные показатели текучести и легкость прессования, которые отличаются от варианта необработанного парацетамола. Соответственно, гранулированная композиция может быть подвергнута непосредственно прессованию с получением таблеток, при наличии минимального набора таблеточных эксципиентов. При этом таблетки, полученные на основе гранулированной композиции, в типичном случае демонстрируют повышенную твердость в сравнении с более мягкими таблетками, получаемыми на основе сухой смеси парацетамола и ибупрофена. Таблетки, формируемые из гранулированной композиции, в типичном случае обладают достаточной твердостью для введения их в условия жесткой обработки, имеющиеся в процессе производства, например, на стадии нанесения пленочного покрытия. Соответственно, гранулированная композиция позволяет получать препарат в твердой дозированной форме, поскольку легко прессуется и не прилипает к штамповочным частям таблеточной машины. В этой связи выход продукта в процессе прессования при использовании гранулированной композиции, полученной согласно способу настоящего изобретения, существенно возрастает в сравнении с вариантом использования смеси из необработанного парацетамола и НПВС. Кроме того, в типичном случае отсутствует необходимость проводить предварительную обработку парацетамола (например, в рамках процесса грануляции, который повышает текучесть продукта) или использовать непосредственно прессуемые формы парацетамола в способе согласно настоящему изобретению, поскольку парацетамол может быть взят непосредственно без предварительной обработки из объемной формы продукта в процесс производства. Соответственно, способ согласно настоящему изобретению может позволить снизить общую стоимость производства и упростить сложный процесс производства твердых дозированных форм, содержащих НПВС и парацетамол.
Другие преимущества гранулированной композиции, получаемой по способу согласно настоящему изобретению, связаны с относительно малым количеством дополнительных таблеточных эксципиентов, необходимых для получения дозированной формы, в частности, твердой дозированной формы для перорального введения, что, в свою очередь, позволяет получать более мелкие дозированные формы, содержащие относительно высокую концентрацию НПВС и парацетамола, что сопровождается увеличением комфорта для пациента.
Неожиданно было обнаружено, что фармацевтические композиции, в частности, твердые дозированные формы для перорального введения, полученные на основе гранулированной композиции, производимой в соответствии со способом согласно настоящему изобретению, обладают ценными свойствами по разложению. Кроме того, результаты оценки показателя растворимости таких фармацевтических композиций в типичном случае демонстрируют неожиданно высокий уровень растворенных в водной среде НПВС и парацетамола после относительно коротких периодов времени.
Таким образом, способ согласно настоящему изобретению в типичном случае обеспечивает преимущества в процессе обработки НПВС и парацетамола, увеличении комфорта для пациента, увеличении прочности твердых дозированных форм, обладающих желательными показателями разложения и растворения, и в снижении общей стоимости таблеток, изготавливаемых на основе НПВС и парацетамола.
В способе согласно настоящему изобретению НПВС в форме свободной кислоты подвергают расплавлению. Соответственно, термины «расплав» и «расплавленный» в контексте настоящего описания означает, что НПВС в форме свободной кислоты должен быть расплавлен либо полностью, либо по меньшей мере частично, в процессе формирования гранулированной композиции. Предпочтительно НПВС в форме свободной кислоты подвергают полному расплавлению при получении гранулированной композиции.
Термин «НПВС в форме свободной кислоты» авторы используют для обозначения того факта, что НПВС включает кислотную группу, которая не дериватизирована, например, при образовании соли. Термин «НПВС в форме свободной кислоты» включает НПВС, которые включают недериватизированные группы карбоновой кислоты per se (например, пропионовые кислоты) и/или НПВС, которые включают недериватизированные кислотные енольные группы (например, оксикамы). Для специалистов в данной области понятно, что НПВС в форме свободной кислоты отличается по физическим и химическим свойствам от того же НПВС в форме соли. Соответственно, расплавленные смеси, образуемые при расплавлении только солей НПВС (например, без включения в процесс расплава каких-либо НПВС в форме свободной кислоты), не охватываются способом согласно настоящему изобретению. Предпочтительно расплавленную смесь получают путем расплавления НПВС только в форме свободных кислот. Соответственно, расплавленные гранулы, получаемые в соответствии со способом настоящего изобретения, представляют собой по существу формы, свободные от солей НПВС.
Способ по настоящему изобретению позволяет получать гранулярный компонент, включающий множество НПВС, в частности, НПВС, которые предпочтительно ингибируют Cox-1.
Подходящие типы НПВС, которые предпочтительно ингибируют Cox-1, могут быть выбраны из следующих групп:
(1) пропионовые кислоты;
(2) уксусные кислоты;
(3) фенамовые кислоты;
(4) бифенилкарбоновые кислоты;
(5) оксикамы.
Подходящие пропионовые кислоты, которые могут применяться согласно настоящему изобретению, включают, без ограничения, ибупрофен, напроксен, беноксапрофен, флурбипрофен, фенопрофен, фенбуфен, кетопрофен, индопрофен, пирпрофен, карпрофен, оксапрозин, прапопрофен, миропрофен, тиоксапрофен, супрофен, альминопрофен, тиапрофеновую кислоту, флупрофен и буклоксиновую кислоту. Предпочтительные представители группы пропионовой кислоты включают ибупрофен, напроксен, флурбипрофен, фенопрофен, кетопрофен и фенбуфен, в особенности ибупрофен.
Подходящие уксусные кислоты, которые могут применяться согласно настоящему изобретению, включают, без ограничения, индометацин, сулиндак, толметин, зомепирак, диклофенак, фенклофенак, алклофенак, ибуфенак, изоксепак, фурофенак, тиопинак, зидометацин, ацеметацин, фентиазак, клиданак и оксипинак. Предпочтительные представители группы уксусной кислоты включают толметин-натрий, зомепинак-натрий, сулиндак и индометацин.
Подходящие фенамовые кислоты, которые могут применяться согласно настоящему изобретению, включают, без ограничения, мефенамовую кислоту, меклофенамовую кислоту, флуфенамовую кислоту, нифлуминовую кислоту и толфенамовую кислоту. Предпочтительные представители группы фенамовой кислоты включают мефенамовую кислоту и меклофенамовую кислоту.
Бифенилкарбоновые кислоты, подходящие для применения согласно настоящему изобретению, включают, без ограничения, дифлунизал и флуфенизал.
Оксикамы, подходящие для использования согласно настоящему изобретению, включают, без ограничения, мелоксикам, пироксикам, субоксикам, изоксикам. Предпочтительные представители группы оксикамов включают пироксикам и мелоксикам.
Соответственно, НПВС, подходящие для использования согласно настоящему изобретению, демонстрируют в типичном случае изомерию. Соответственно, все стереоизомеры, диастереоизомеры, энантиомеры и их смеси, включающие рацемические смеси НПВС, охватываются областью настоящего изобретения.
Особенно предпочтительный класс НПВС, подходящий для применения в способе согласно настоящему изобретению, представлен пропионовыми кислотами, в особенности 2-арилпропионовыми кислотами, и в частности 2-фенилпропионовыми кислотами.
Особенно предпочтительные пропионовые кислоты включают напроксен, флурбипрофен, ибупрофен и кетопрофен, в частности их рацемические смеси и S(+)-энантиомеры данных соединений. Более предпочтительные 2-арилпропионовые кислоты включают флурбипрофен и ибупрофен, в частности их рацемические смеси и их S(+)-энантиомеры. Еще более предпочтительные 2-арилпропионовые кислоты включают рацемический флурбипрофен и рацемический ибупрофен, в особенности рацемический ибупрофен.
Предпочтительные НПВС, подходящие для применения, согласно настоящему изобретению обладают относительно низкой точкой плавления, так что в этом случае процесс расплавления не требует использования значительных количеств энергии, что позволяет снизить стоимость производства. Как указывалось выше, наиболее подходящий класс соединений включает 2-арилпропионовые кислоты, которые в основном относятся по существу к нерастворимым соединениям с неприятными вкусовыми свойствами. Соответственно, типичные точки плавления низкоплавких НПВС находятся в диапазоне от 30 до 300°С. Предпочтительные НПВС имеют точки плавления в диапазоне 30-200°С (например, рацемический напроксен, имеющий точку плавления 156°С), более предпочтительно в диапазоне 30-160°С и еще более предпочтительно в диапазоне 40-120°С (например, рацемический ибурофен, имеющий точку плавления 114°С), наиболее предпочтительно 40-100°С (например, рацемический ибупрофен, имеющий точку плавления в диапазоне 75-77°С), S(+)-ибупрофен (имеющий точку плавления 52-54°С) и рацемический кетопрофен (имеющий точку плавления 96°С). Предпочтительные низкоплавкие НПВС включают напроксен, кетопрофен, флурбипрофен, ибупрофен. Предпочтительно НПВС имеет форму рацемический смеси или энантиомера (в особенности S(+)-энантиомеров) указанных соединений.
Настоящее изобретение особенно хорошо адаптировано к лекарственному средству, содержащему ибупрофен. Термин «лекарственное средство, содержащее ибупрофен» предпочтительно включает рацемический ибупрофен и S(+)-ибупрофен. Самые удачные результаты были получены при использовании рацемического ибупрофена в форме свободной кислоты, который характеризуется слабой растворимостью и вводится в высокой дозировке.
Соответственно, гранулированные композиции и расплавленные гранулы могут включать одно или несколько разных НПВС согласно настоящему описанию. Однако предпочтительно гранулированная композиция и расплавленные гранулы включают один НПВС. Наиболее предпочтительно гранулированная композиция и расплавленные гранулы включают один НПВС в виде одного энантиомера или рацемической смеси, например, только S(+)-ибупрофен или только рацемический ибупрофен. Кроме того, согласно настоящему описанию гранулированная композиция (например, гранулы расплава) или фармацевтическая композиция, созданная на ее основе, может включать один или несколько других фармацевтических активных агентов, кроме НПВС и парацетамола. Однако высокопредпочтительная гранулированная композиция (например, гранулы расплава) или фармацевтическая композиция, созданная на ее основе, включает НПВС и парацетамол в качестве единственных активных ингредиентов, наиболее предпочтительно один НПВС согласно настоящему описанию и парацетамол.
Соответственно, в том случае, когда НПВС в форме свободной кислоты подвергают расплавлению, образуется жидкая форма продукта. Парацетамол имеет точку плавления в диапазоне 169-172°С, и в зависимости от используемого НПВС в форме свободной кислоты и условий способа производства указанный парацетамол может быть частично или полностью расплавлен в процессе создания гранулированной композиции. Предпочтительно парацетамол по существу не расплавляется в ходе получения гранулированной композиции. Соответственно, парацетамол может частично растворяться в расплавленном НПВС в форме свободной кислоты, однако большая часть парацетамола в типичном случае диспергирована в расплавленном НПВС в форме свободной кислоты. Таким образом, НПВС в форме свободной кислоты растворяется и образует расплавленную фазу, в которую включены парацетамол и другие необязательные эксципиенты.
При охлаждении расплавленной смеси НПВС в форме свободной кислоты и парацетамола указанный НПВС в типичном случае образует непрерывную твердую фазу кристаллического типа, которая облекает или покрывает парацетамол. Отвержденный расплав может быть перемолот непосредственно с получением гранул, которые приемлемы для дальнейшего непосредственного прессования в фармацевтически дозированную форму с минимальным набором таблеточных эксципиентов. Иными словами, НПВС в форме свободной кислоты, по меньшей мере, частично теряет свое кристаллическое состояние и действует как носитель для парацетамола. Предпочтительно, когда НПВС в форме свободной кислоты полностью расплавляется, расплавленный НПВС в форме свободной кислоты при охлаждении образует одну непрерывную фазу, а именно одну непрерывную твердую кристаллическую фазу, то есть кристаллическая структура НПВС не прерывается НПВС, имеющим структуру, отличную от кристаллической. Такое может произойти, например, в том случае, когда НПВС лишь частично расплавлен, и в этом случае кристаллическая структура расплавленного НПВС прерывается наличием нерасплавленного НПВС, то есть в этом случае НПВС не имеет единую кристаллическую структуру, поскольку кристаллическая структура отвержденного расплавленного НПВС отличается (например, по размеру частиц) от соответствующего параметра в кристаллической структуре нерасплавленного НПВС.
Таким образом, в контексте настоящего описания термин «отвержденные гранулы расплава» обозначает гранулы, полученные при смешивании расплавленного НПВС в форме свободной кислоты и парацетамола, необязательно при наличии одного или нескольких таблеточных эксципиентов, с последующим охлаждением до температуры ниже точки плавления НПВС и образованием гранул на основе твердой массы. Гранулированная композиция включает множество таких гранул.
Неожиданно было обнаружено, что если НПВС в форме свободной кислоты полностью расплавляется в процессе получения гранулированной композиции, то полученная фармацевтическая композиция (например, в виде твердой дозированной формы), образованная из такой гранулированной композиции, в типичном случае лучше растворяется и демонстрирует улучшенный профиль растворимости в сравнении с соответствующей фармацевтической композицией, образованной при частичном расплавлении НПВС в форме свободной кислоты. В этой связи фармацевтическая композиция, образованная из гранулированной композиции, в которой НПВС в форме свободной кислоты полностью расплавлен, в типичном случае высвобождает более высокую концентрацию НПВС в водную среду в течение относительно короткого периода времени в сравнении с соответствующей фармацевтической композицией, образованной из гранулированной композиции, в которой НПВС в форме свободной кислоты расплавлен частично.
Неожиданно было обнаружено, что только в случае НПВС в форме свободной кислоты необходимо, чтобы он был расплавлен на стадии (а) согласно способу настоящего изобретения. Парацетамол в типичном случае диспергируется в расплавленном НПВС в форме свободной кислоты и нет необходимости, чтобы он был расплавлен.
Все преимущества, описанные выше применительно к улучшенным показателями текучести, обрабатываемости и показателям растворения гранулированной композиции, в типичном случае сохраняются даже в том случае, когда парацетамол не расплавлен. Соответственно, способ согласно настоящему изобретению может быть осуществлен при такой температуре, когда парацетамол не расплавлен (например, при температуре, которая существенно ниже, чем точка плавления парацетамола), что снижает и/или устраняет возможность разложения парацетамола в процессе получения гранулированной композиции.
Кроме того, и это выглядит еще более неожиданно, такие благоприятные эффекты в типичном случае сохраняются даже в том случае, когда масса парацетамола, присутствующего в расплавленных гранулах, выше, чем масса ибупрофена, также присутствующего в расплавленных гранулах. В частности, было обнаружено, что расплавленная смесь, включающая расплавленный НПВС в форме свободной кислоты, парацетамол и любые другие необязательные эксципиенты, в типичном случае все еще обладает требуемой текучестью, так что она может быть обработана и сформована в расплавленные гранулы с использованием стандартных методик (например, расплавленная смесь может быть сформована в экструдере и затем выпущена из экструдера на охлаждающее полотно, как будет описано ниже), несмотря на то, что расплавленная смесь содержит относительно малую пропорцию расплавленной фазы (то есть расплавленного НПВС в форме свободной кислоты). Неожиданно было обнаружено, что расплавленные гранулы, содержащие большее по массе количество парацетамола, чем ибупрофена, также демонстрируют в типичном случае существенно улучшенные показатели текучести и прессуемости в сравнении с необработанным парацетамолом. В этой связи указанная смесь может подвергаться непосредственному прессованию в таблетки, обладающие желательной твердостью, при использовании минимального набора эксципиентов. Это в особенности удивительно, поскольку известно, что парацетамол представляет собой вещество, плохоподдающееся прессованию, и тем не менее расплавленные гранулы, содержащие избыток парацетамола, демонстрируют существенно улучшенные показатели прессуемости в сравнении с самим парацетамолом. Фармацевтические композиции (например, таблетки), образованные на основе таких гранул, содержащих избыток парацетамола, также демонстрируют желательные показатели растворения парацетамола, в соответствии с которыми достигаются высокие уровни растворенных НПВС и парацетамола в водной среде, в частности, в водно-кислой среде, после относительно коротких периодов времени. Соответственно, такие фармацевтические композиции могут доставлять более высокие количества НПВС и парацетамола в кислых условиях желудочно-кишечного тракта или желудка, когда при наличии такой необходимости их принимает пациент, при этом может быть достигнуто ускорение начала терапевтического действия парацетамола НПВС. Считается, пока лишь в теории, что улучшенный уровень растворения связан с физической структурой расплавленной гранулы. Поскольку парацетамол присутствует в избытке, отвержденные гранулы расплава включают частицы парацетамола, которые частично покрыты оболочкой и прилипают друг к другу в связи с НПВС в форме свободной кислоты. Парацетамол представляет собой легко растворимое вещество в кислых водных условиях, тогда как НПВС в форме свободной кислоты таким не является. Таким образом, в водной среде частицы парацетамола начинают растворяться и тонкие слои НПВС, имеющиеся между такими частицами, уменьшаются и их растворение происходит значительно быстрее. В этой связи другим преимуществом такой гранулированной композиции является ее легкая растворимость.
Соответственно, такие характеристики высокожелательны при проведении комбинированного лечения ибупрофеном и парацетамолом, поскольку парацетамол в типичном случае вводится в относительно высоких дозах (например, 500 мг на стандартную дозу), в сравнении с НПВС (например, 200 мг на стандартную дозу).
Таким образом, в соответствии с предпочтительным аспектом настоящего изобретения масса парацетамола в отвержденных гранулах расплава выше или равна массе НПВС в отвердженных гранулах расплава, применительно к общей массе гранул расплава. Более предпочтительно масса парацетамола в отвержденных гранулах расплава выше, чем масса НПВС в отвержденных гранулах расплава, применительно к общей массе гранул расплава.
Соответственно, масса парацетамола в гранулированной композиции выше или равна, предпочтительно выше чем масса НПВС в гранулированной композиции, применительно к общей массе гранулированной композиции.
Предпочтительно масса парацетамола к массе НПВС в отвержденных гранулах расплава выше чем 1:1, более предпочтительно выше или равна 1,5:1, еще более предпочтительно выше или равна 2:1. Предпочтительно весовое соотношение парацетамола к НПВС в отвержденных гранулах расплава меньше или равно 10:1, более предпочтительно меньше или равно 5:1 и еще более предпочтительно меньше или равно 3:1.
Особенно предпочтительно весовое соотношение парацетамола к НПВС в отвержденных гранулах расплава составляет от 2,2:1 до 2,8:1 и конкретно составляет примерно 2,5:1.
Предпочтительно весовое соотношение парацетамола к НПВС в гранулированной композиции больше чем 1:1, более предпочтительно больше или равно 1,5:1, еще более предпочтительно больше или равно 2:1. Предпочтительно весовое соотношение парацетамола к НПВС в гранулированной композиции меньше или равно 10:1, более предпочтительно меньше или равно 5:1 и еще более предпочтительно меньше или равно 3:1.
Особенно предпочтительно весовое соотношение парацетамола к НПВС в гранулированной композиции составляет от 2,2:1 до 2,8:1 и конкретно составляет примерно 2,5:1.
Предпочтительно парацетамол присутствует в количестве, большем или равном 40 масс.%, более предпочтительно в количестве, большем или равном 45 масс.%, еще более предпочтительно в количестве, большем или равном 50 масс.%, и еще более предпочтительно в количестве, большем или равном 55 масс.% гранулированной композиции, применительно к общей массе гранулированной композиции.
Предпочтительно парацетамол присутствует в количестве, меньшем или равном 80 масс.%, более предпочтительно в количестве, меньшем или равном 75 масс.%, и наиболее предпочтительно в количестве, меньшем или равном 70 масс.%, от гранулированной композиции применительно к общей массе гранулированной композиции.
Предпочтительно парацетамол присутствует в количестве, большем или равном 40 масс.%, более предпочтительно в количестве, большем или равном 45 масс.%, еще более предпочтительно в количестве, большем или равном 50 масс.%, и наиболее предпочтительно в количестве, большем или равном 55 масс.% от отвержденных гранул расплава, применительно к общей массе отвержденных гранул расплава.
Предпочтительно парацетамол присутствует в количестве, меньшем или равном 80 масс.%, более предпочтительно в количестве, меньшем или равном 75 масс.%, еще более предпочтительно в количестве, меньшем или равном 70 масс.%, от отвержденных гранул расплава применительно к общей массе отвержденных гранул расплава.
Предпочтительно НПВС присутствует в количестве, меньшем или равном 45 масс.%, более предпочтительно в количестве, меньшем или равном 40 масс.% от гранулированной композиции, применительно к общей массе гранулированной композиции.
Предпочтительно НПВС присутствует в количестве, большем или равном 20 масс.%, более предпочтительно в количестве, большем или равном 25 масс.% от гранулированной композиции, применительно к общей массе гранулированной композиции.
Предпочтительно НПВС присутствует в количестве, меньшем или равном 45 масс.%, более предпочтительно в количестве, меньшем или равном 40 масс.% от отвержденных гранул расплава, применительно к общей массе отвержденных гранул расплава.
Предпочтительно НПВС присутствует в количестве, большем или равном 20 масс.%, более предпочтительно в количестве, большем или равном 25 масс.% от отвержденных гранул расплава применительно к общей массе отвержденных гранул расплава.
Предпочтительно парацетамол и любые другие необязательные таблеточные эксципиенты однородно диспергируют в расплавленном НПВС в форме свободной кислоты. Таким образом, получают однородную смесь. Указанную смесь оставляют охлаждаться с использованием методик, приведенных в данном описании, до образования твердого вещества. По мере охлаждения смесь становится более вязкой. Таким образом, отвержденная смесь преобразуется в гранулы.
Согласно способу по настоящему изобр