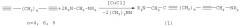Способ получения , -ди(аминометил)-алкадиинов
Иллюстрации
Показать всеИзобретение относится к способу получения α,ω-ди(аминометил)алкадиинов общей формулы (1)
где R2N=пиперидил, морфолил, N-метилпиперазил, характеризующийся тем, что α,ω-диацетилены НС=С-(СН2)n-С≡СН, где n=4, 6, 8, подвергают взаимодействию с гем-диаминами R2NCH2NR2, где R2N такое же, как определено выше, в присутствии катализатора однохлористой меди (CuCl), взятыми в мольном соотношении α,ω-диацетилен:бисамин:CuCl=10:20:(0.3-0.7), предпочтительно 10:20:0.5 ммолей, при температуре 80°С и атмосферном давлении в течение 4-6 ч. α,ω-Аминометилированные диацетилены могут найти применение в тонком органическом синтезе, в частности, для получения труднодоступных полициклических соединений. Технический результат - способ позволяет увеличить выход целевых продуктов. 1 табл.
Реферат
Изобретение относится к органической химии, в частности к способу получения α,ω-ди(аминометил)алкадиинов общей формулы (1)
где R2N=пиперидил, морфолил, N-метилпиперазил.
α,ω-Аминометилированные диацетилены могут найти применение в тонком органическом синтезе, в частности в синтезе труднодоступных полициклических соединений (А.Т.Бабаян. Внутримолекулярные перегруппировки солей четырехзамещенного аммония. Ереван: Изд. АН АрмССР, 1976, с.159-348).
Известен способ (G.W.Kabalka, L.L.Zhou, L.Wang, M.Pagni. A microwave-enhanced, solventless Mannich condensation of terminal alkynes and secondary amines with para-formaldehyde on cuprous iodide doped aluminia. Tetrahedron 62 (2006) 857-867) получения аминометилированных диацетиленов, в частности 1,4-ди(2-алкинил)пиперазинов общей формулы (2), взаимодействием терминальных ацетиленов с пиперазином и формальдегидом в присутствии стехиометрических количеств иодида меди и окиси алюминия при ультразвуковом облучении с выходом 49-65% по схеме
Известным способом не могут быть получены α,ω-ди(аминометил)алкадиины общей формулы (1).
Известен способ (G.W.Kabalka, L.L.Zhou, L.Wang, M.Pagni. A microwave-enhanced, solventless Mannich condensation of terminal alkynes and secondary amines with para-formaldehyde on cuprous iodide doped aluminia. Tetrahedron 62 (2006) 857-867) получения аминометилированных диацетиленов (3) взаимодействием 1 экв. диацетиленового соединения с избытком параформальдегида и 2 экв. вторичного амина в присутствии стехиометрических количеств иодида меди и окиси алюминия при ультразвуковом облучении с выходом 51-56% по схеме:
Известным способом может быть осуществлен синтез α,ω-ди(аминометил)алкадиинов общей формулы (1) при условии вовлечения в реакцию в качестве исходных вторичных аминов (R1R2NH) пиперидина, морфолина и N-метилпиперазина.
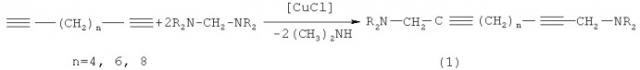
Предлагается новый способ получения α,ω-ди(аминометил)алкадиинов общей формулы (1). Сущность способа заключается во взаимодействии α,ω-диацетиленов общей формулы HC≡С-(СН2)n-С≡СН, где n=4, 6, 8, с двукратным избытком гем-диамина R2NCH2NR2, где R2N=пиперидил, морфолил, N-метилпиперазил, в присутствии катализатора однохлористой меди (CuCl), взятыми в соотношении α,ω-диацетилен:гем-диамин:CuCl=10:20:(0.3-0.7), предпочтительно 10:20:0.5 ммолей, без растворителя при температуре 80°С и атмосферном давлении в течение 4-6 ч. Выход α,ω-ди(аминометил)алкадиинов (1) составляет 64-78%. Реакция протекает по схеме
где R2N=пиперидил, морфолил, N-метилпиперазил.
α,ω-Ди(аминометил)алкадиины (1) образуются только лишь с участием α,ω-диацетиленов и двукратного избытка гем-диаминов. В присутствии дизамещенных ацетиленов или диаминов другой структуры целевые продукты (1) не образуются.
Проведение указанной реакции в присутствии катализатора CuCl больше 0.7 ммолей не приводит к существенному увеличению выхода целевого продукта (1). Использование катализатора CuCl менее 0.3 ммолей снижает выход (1), что связано, возможно, со снижением каталитически активных центров в реакционной массе. Реакции проводили при температуре 80°С. При более высокой температуре (например, 90°С) увеличиваются энергозатраты, а при меньшей температуре (например, 70°С) снижается скорость реакции.
Изменение соотношения исходного гем-диамина в сторону увеличения его содержания по отношению к исходному α,ω-диацетилену не приводит к существенному повышению выхода целевых продуктов (1).
Существенные отличия предлагаемого способа.
В известном способе для аминометилирования α,ω-диацетиленов используются параформальдегид и вторичные амины, реакция идет с участием стехиометрических количеств CuI и Al2O3 при ультразвуковом облучении, при этом выход целевых продуктов не превышает 56%.
В предлагаемом способе для аминометилирования α,ω-диацетиленов применяются гем-диамины, взятые в двукратном избытке по отношению к α,ω-диацетиленам, реакция идет под действием каталитических количеств CuCl. Выход целевых продуктов достигает 78%.
Способ поясняется следующими примерами.
ПРИМЕР 1. В стеклянный реактор, установленный на магнитной мешалке, в атмосфере аргона помещают 10 ммолей 1,7-октадиина, 20 ммолей (пиперидинометил)пиперидина, 0.5 ммолей катализатора CuCl, перемешивают 5 ч при температуре 80°С. Из реакционной массы выделяют 1-[10-(1-пиперидинил)-2,8-декадиенил]пиперидин с выходом 73%.
Спектральные характеристики 1-[10-(1-пиперидинил)-2,8-декадиенил]пиперидина (1).
Спектр ЯМР 13C (CDCl3, δ, м.д.) 1-[10-(1-пиперидинил)-2,8-декадиенил]пиперидина (1): 14.45, 17.64, 25.69, 26.93, 47.27, 53.62, 75.14, 83.05.
Другие примеры, подтверждающие способ, приведены в табл.1.
| Таблица 1 | |||||
| №№ п/п | Исходный гем-диамин | Исходные α,ω-диацетилены | Соотношение α,ω-диацетилен:гем-диамин:CuCl, ммоль | Время реакции, ч | Выход α,ω-ди(амино-метил)алкадиинов (1), % |
| 1 | 1-(пиперидинометил)-пиперидин | 1,7-октадиин | 10:20:0.5 | 5 | 1-[10-(1-пиперидинил)-2,8-декадиенил]-пиперидин, 73 |
| 2 | -//- | -//- | 10:20:0.7 | 5 | -//-, 78 |
| 3 | -//- | -//- | 10:20:0.3 | 5 | -//-, 68 |
| 4 | -//- | -//- | 10:20:0.5 | 6 | -//-, 76 |
| 5 | -//- | -//- | 10:20:0.5 | 4 | -//-, 69 |
| 6 | -//- | 1,9-декадиин | 10:20:0.5 | 5 | 1-[12-(1-пиперидинил)-2,10-додекадиенил]-пиперидин, 67 |
| 9 | -//- | 1,11-додекадиин | 10:20:0.5 | 5 | 1-[14-(1-пиперидинил)-2,12 -тетрадекадиенил]-пиперидин, 64 |
| 10 | 4-(морфолинометил)-морфолин | 1,7-октадиин | 10:20:0.5 | 5 | 4-[10-(4-морфолинил)-2,8-декадиинил]-морфолин, 74 |
| 11 | 1-метил-4-[(4-метил-пиперазино)метил]-пиперазин | 1,7-октадиин | 10:20:0.5 | 5 | 1-метил-4-[10-(4-метил-1-пиперазинил)-2,8-дека-диинилпиперазин, 71 |
Реакции проводили при температуре 80°С без растворителя.
Способ получения α,ω-ди(аминометил)алкадиинов общей формулы (1): где R2N - пиперидил, морфолил, N-метилпиперазил,характеризующийся тем, что α,ω-диацетилены НС=С-(СН2)n-С≡СН, где n=4, 6, 8, подвергают взаимодействию с гем-диаминами R2NCH2NR2, где R2N такое же, как определено выше, в присутствии катализатора однохлористой меди (CuCl), взятыми в мольном соотношении α,ω-диацетилен: бисамин: CuCl=10:20:(0,3-0,7), предпочтительно 10:20:0,5 ммолей, при температуре 80°С и атмосферном давлении в течение 4-6 ч.