Меченные тритием n-фениллепидиниевые соли и способ их получения
Иллюстрации
Показать всеНастоящее изобретение относится к солям N-фениллепидиния, меченным тритием по фенильному заместителю, общей формулы
Также изобретение относится к способу получения солей N-фениллепидиния, меченных тритием. Технический результат: получены новые соединения, обладающие антибактериальной и противогрибковой активностью, а также разработан способ их получения. 2 н.п. ф-лы. 1 ил. 1 табл.
Реферат
Настоящее изобретение относится к радиохимии, касается неизвестной реакции прямого фенилирования атома азота в лепидине, а именно к получению новых биологически важных меченных тритием N-фениллепидиниевых солей общей формулы
и одностадийному способу их получения.
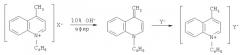
Непосредственное фенилирование хинолина не приводит к образованию N-арилчетвертичных солей хинолиния [Pausacker K.H. Arylation of aromatic compounds. VI. Benzoyl Peroxide with Pyridine and Quinoline // Australian Journal of Chemistry 1958. V.11 (2). Р.200-210]. Галоидные арилы и арильные эфиры ароматических сульфокислот не образуют четвертичных солей при нагревании с хинолином и его производными ввиду их малой реакционной способности. Методом синтеза N-арильных солей хинолиния является циклизация вторичных ароматических аминов с карбонилсодержащими органическими соединениями, это могут быть паральдегид, уксусный альдегид, виниловые эфиры и т.д. [Пилюгин Г.Т., Гуцуляк Б.М. Успехи в области синтеза, исследования и применения хинолиниевых соединений // Успехи химии. 1963. Т.32 (4). С.389-432; Джилкрист Т. Химия гетероциклических соединений. М., 1996; Katritzky A.R., Pozharski A.F. Handbook of Heterocyclic Chemistry. Pergamon, 2000]. Применив реакцию Дебнера-Миллера к диариламинам, Пилюгин и Крайнер [Пилюгин Г.Т., Крайнер З.Я. Фенилзамещенные хиноцианины // ДАН СССР. 1951. Т.8 (4). С.609-612] разработали метод получения N-фенилхинальдиниевых четвертичных солей:
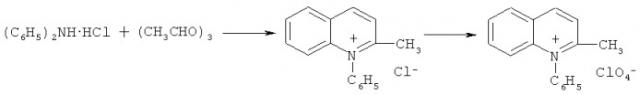
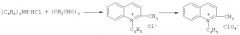
Соли N-фениллепидиния были получены по видоизмененной реакции Бейера из дифениламина и формалина в присутствии ацетона и нитробензола [Пилюгин Г.Т., Гуцуляк Б.М. Исследования в области синтетических красителей. XIV. Синтез N-фениллепидинийперхлората и некоторые его превращения // ЖОХ. 1959. Т.29 (9). С.3076-3079]:
Необходимо отметить, что разработанные методы получения четвертичных N-фенилхинолиниевых производных трудоемки и не позволяют получать соединения с высокими выходами (выход соли порядка 10-20%). Кроме того, синтез данным методом меченных тритием N-фениллепидиниевых производных практически не осуществим.
Лепидиниевые соли, обладающие подвижной метильной группой, весьма реакционноспособные соединения и легко вступают в реакцию конденсации, образуя красители различных классов, они являются полупродуктами для синтеза красителей сенсибилизаторов фотоэмульсий, красителей для окрашивания природных и синтетических волокон и биологических препаратов [Пилюгин Г.Т., Гуцуляк Б.М. Успехи в области синтеза, исследования и применения хинолиниевых соединений // Успехи химии. 1963. Т.32 (4). С.389-432; Пилюгин Г.Т., Гуцуляк Б.М. Исследования в области синтетических красителей. XIV. Синтез N-фениллепидинийперхлората и некоторые его превращения // ЖОХ. 1959. Т.29 (9). С.3076-3079; Пилюгин Г.Т., Шинкоренко С.В., Станкевич О.М., Станкевич В.В. Исследования в области синтетических красителей. LVI. Синтезы бисазокрасителей, производные N-ариллепидиниевых солей // ХГС. 1966. Т.2 (3). С.406-408; Пилюгин Г.Т., Розум Ю.С., Горичок Ю.О., Гуцуляк Б.М. Синтетические красители. XLV. Структура и адсорбционные спектры солей лепидиния // ЖОХ. 1965. Т.35 (3). С.506-509; Бойко И.И., Шинкоренко С.В., Опанасенко Е.П., Лизин В.В. Хиногептаметинцианины с мостиковыми хромофорами // ЖОрХ. 1985. Т.21 (4). С.859-862; Geddes C.D., Douglas P.M., Moore C.P., Wear T.J., Egerton P.L. New indolinium and quinolinium dyes sensitive to aqueous halide ions at physiological concentrations // J. Heterocyc. Chem. 1999. V.36 (4). P.949-952; Tolmachev O.I., Pilipchuk N.V., Kachkovsky O.D., Slominski Yu.L., Gayvoronsky V.Ya., Shepelyavyy E.V., Yakunin S.V., Brodun M.S. Spectral and non-linear properties of cyanine bases′ derivatives of benzo[c,d]indole // Dyes and Pigments. 2007. V.74 (1). P.195-201]. Хинолиниевые производные обладают рядом интересных биологических свойств: антисептическими, химикотерапевтическими, гипотензивными, канцеростатическими, а также регулирующими рост растений [Гуцуляк Б.М. Соли хинолиния как биологически активные вещества. Успехи химии. 1972. Т.41, №2. С.346-373; Шинкоренко С.В., Пилюгин Т.Г., Сидорчук И.И., Яворский В.М. Синтез и некоторые биологические свойства азометинов хинальдиния. Хим.-фарм. журнал. 1972, №1. С 25-29; Сидорчук И.И., Стаднийчук Р.Ф., Тищенко Е.Н., Бордяковская Л.Т. Антимикробная активность четвертичных солей хинолиния. // Хим.-фарм. журнал. 1978. Т.12 (7). С.78-80; Возняк В.И., Савитская Л.Г., Непорадный Д.Д. Антимикробная активность четвертичных солей 4-(п-диметиламиностирил)хинолина // Хим.-фарм. ж. 1984. Т.18 (8). С.951-954; Abd El-Aala R.M., Younis M. Synthesis and antimicrobial activity of meso-substituted polymethine cyanine dyes // Bioorganic Chemistry. 2004. V.32. P.193-210; Джоуль Дж., Миллс К. Химия гетероциклических соединений, 2-е изд., перераб. Мир. 2009. 728 с.; Зациха Ю.В., Гуцуляк Б.М., Горичок Ю.О. Производные лепидиния как регуляторы роста и развития растений. III. Выращивание пихтовых саженцев с использованием некоторых хиноцианокрасителей производных лепидиния // Физиолог. активные вещества. 1971. №.3. С.218-227]. К сожалению, трудность получения арильных четвертичных лепидиниевых соединений во многом сдерживает широкое исследование и соответственно использование полезных и уникальных свойств данных производных.
Ранее нами, благодаря использованию нуклеогенных фенил-катионов, удалось преодолеть невозможность прямого синтеза и успешно разработать способ получения N-фенилхинолиниевых и хинальдиниевых четвертичных солей, меченных тритием [Меченные тритием N-фенилхинолиниевые и хинальдиниевые соли и способ их получения. Патент РФ №2320647 от 27.03.2008 г.].
Задачей данного изобретения является разработка простого по исполнению, доступного по реагентам с высокими радиохимическими выходами одностадийного способа получения новых меченных тритием N-фениллепидиниевых солей, которые могут быть использованы для биологических и медицинских исследований.
Поставленная задача достигается новыми меченными тритием N-фениллепидиниевыми солями общей формулы
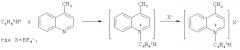
Поставленная задача достигается описываемым новым способом получения новых меченных тритием N-фениллепидиниевых солей, заключающимся в том, что лепидин (4-метилхинолин) подвергают ион-молекулярным реакциям со свободными меченными тритием нуклеогенными фенил-катионами, которые генерируются самопроизвольно при бета-распаде трития в составе третированного бензола.
Вышеперечисленная совокупность существенных признаков позволяет получить следующий технический результат: авторами создан простой по исполнению, доступный по реагентам с высокими радиохимическими выходами одностадийный способ получения новых меченных тритием N-фениллепидиниевых производных, которые могут быть использованы для биологических и медицинских исследований. Введение индукционного метильного заместителя в пара-положение существенно увеличивает радиохимический выход и усиливает биологическую активность.
Изобретение иллюстрируется следующими примерами.
Пример 1.
Соли N-фениллепидиния. В качестве свидетеля и носителя был использован неактивный борофторид N-фениллепидиния. Перхлорат N-фениллепидиния получен конденсацией дифениламина с формальдегидом и ацетоном аналогично методике [Пилюгин Г.Т., Гуцуляк Б.М. Исследования в области синтетических красителей. XIV. Синтез N-фениллепидинийперхлората и некоторые его превращения // ЖОХ. 1959. Т.29 (9). С.3076-3079]. В трехгорлую колбу с мешалкой, обратным холодильником и двумя бюретками помещено 75 мл 57% хлорной кислоты, 50 мл нитробензола, в одну бюретку 100 мл (1,4 моль) ацетона, в другую 70 мл (0,2 моль) формалина. Содержимое колбы нагревают на кипящей водяной бане и при перемешивании приливают из бюреток по 2 мл растворов в течение часа. Реакционную смесь нагревают 4 часа. Горячий раствор отфильтровывают. При охлаждении выпадают светло-желтые кристаллы. Оставшуюся смолу экстрагируют кипящей водой. Водные вытяжки упаривают. После перекристаллизации из воды получают почти бесцветные кристаллы 15,9 г (24,4%), т.пл. 172-173°С (т.пл. 172°С [Пилюгин Г.Т., Гуцуляк Б.М. Исследования в области синтетических красителей. XIV. Синтез N-фениллепидинийперхлората и некоторые его превращения // ЖОХ. 1959. Т.29 (9). С.3076-3079]). В результате конверсии анионной части соли из перхлората был получен соответствующий тетрафтороборат:
Т.пл. борофторида N-фениллепидиния 136-137°С.
Двукратно меченный тритием бензол
Схема синтеза:
Из 3,4 мг (0,014 ммоль) дибромбензола, 5,0 мкл (0,020 ммоль) три-н-бутиламина в гексане и 3,3 (0,054 ммоль) кюри газообразного трития путем гидрирования на катализаторе 5% Pd/BaSO4 при комнатной температуре в течение 1 часа был получен двукратно меченный тритием бензол. Добавка амина необходима для связывания образующегося бромоводорода. Химическая чистота синтезированного двукратно меченого бензола - не менее 99%. Объемная удельная активность полученного раствора в гексане составила 1 Ки/мл.
Синтез меченного тритием борофторида N-фениллепидиния:
В стеклянную ампулу объемом 0,5 мл вносят кристаллы стабилизирующей соли KBF4, затем 7,3 мкл (0,055 ммоль) 4-метилхинолина и при охлаждении ампулы жидким азотом добавляют 1 мкл (0,011 ммоль) C6H4 3H2. Ампулу запаивают и выдерживают 1-2 месяца для накопления продуктов ядерно-химического синтеза. Ампулу вскрывают, содержимое переносят в специальную виалу, добавляют 0,5 мл бензола и 0,5 мл ацетонового раствора носителя - неактивной соли - борофторида N-фениллепидиния (1 мг/мл). Не прореагировавший третированный бензол отгоняют в вакууме. К сухому остатку добавляют 0,5 мл ацетона и отбирают пробы по 5 мкл для разделения меченых соединений методом ТСХ.
На чертеже приведена радиохроматограмма меченых продуктов ион-молекулярных реакций в системе: C6H4 3H2 - 4-метилхинолин - KBF4. Первый пик принадлежит борофториду N-фениллепидиния.
Радиохимический выход борофторида N-фениллепидиния составляет 33±2%. Существенно отметить, что по сравнению с солью хинальдиния (выход 18±2%, патент РФ №2320647 от 27.03.2008 г.]) выход целевого продукта увеличился почти в два раза. Аналогично могут быть получены другие соли N-фениллепидиния, если в случае стабилизирующей соли будут взяты KClO4 или KI.
Для количественного выделения меченного тритием борофторида N-фениллепидиния, образца для проведения биологических исследований, весь реакционный раствор был перенесен на большую хроматографическую пластинку (5 см шириной) и проведено разделение продуктов в ацетонитриле. Полоса силикагеля, соответствующая борофториду N-фениллепидиния, была счищена в ацетоновый раствор неактивной соли (2 мг), раствор отделен от осадка и растворитель отогнан. Получен борофтрорид N-фениллепидиния, меченный тритием, с удельной активностью 0,2 мКи/мг.
Пример 2.
Борофториды и перхлораты N-фениллепидиния были исследованы на предмет выявления противомикробного действия по общепринятому методу двукратных серийных разведении (Г.А.Першин, М.: Медицина, 1971 г.). Для проведения экспериментов готовили исходные разведения микробных тел по оптическому стандарту из суточной агаровой культуры. Микробная нагрузка соответствовала 2,5·105 микробных тел в 1 мл, приготовленная по оптическому стандарту (10 ME) из 18-20-часовой агаровой культуры. Микробную взвесь вносили в приготовленные разведения препаратов в питательной среде. Результаты регистрировали после 20-часового и 7-суточного термостатирования при 37°C. Противомикробную: бактериостатическую (МИК) и бактерицидную (МБК) активность, оценивали по минимально действующей концентрации. Максимально испытанные концентрации новых соединений соответствуют 1000 мкг/мл. Результаты биологических исследований представлены в таблице.
| Результаты биологических исследований | |||||
| Соединение | Растворитель | St. aureus | Candida albicans | ||
| МИК | МБК | МИК | МБК | ||
| N-фениллепидиний борофторид | ДМСО | 15,6 | >62,5<125,0 | ||
| N-фениллепидиний борофторид, меченный тритием | ДМСО | 57,14 | 95,23 | ||
| N-фениллепидиний перхлорат | ДМСО | 250,0 | 1000,0 | 250,0 | <250,0>125,0 |
| Н2О | 15,6 | 125,0 | |||
| Структурные аналоги: | ДМСО | 125,0 | 250,0 | ||
| N-фенилхинальдиний борофторид | ДМСО | <500,0>250,0 | 1000,0 | ||
| Н2О | 500,0 | 1000,0 | |||
| N-фенилхинальдиний перхлорат | |||||
| Эталон сравнения: | <1000,0 | 1000,0 | - | - | |
| хинозол (8-оксихинолина сульфат)* | |||||
| нитроксолин (5-нитро-8-оксихинолин)** | 5000,0 | ||||
| *М.Д.Машковский. Лекарственные средства. Новая волна, Москва, 2005. С.841. | |||||
| **М.Д.Машковский. Лекарственные средства. Новая волна, Москва, 2005. С.347. |
Результаты биологических испытаний показывают, что наличие тритиевой метки в борофториде N-фениллепидиния сохраняет бактерицидные свойства соли по отношению к музейному тест-штаму Staphylococcus aureus 906, что важно при проведении детальных исследований биологического воздействия препарата с помощью радиоактивной метки. При сравнении заявляемых солей со структурными аналогами (N-фенилхинальдиниевые соли) видно, что как для борофторида, так и для перхлората N-фениллепидиниевые производные обладают в несколько раз превышающим бактерицидным действием. Данная тенденция сохраняется и для различных растворителей (в водном растворе эффект ингибирования увеличился более чем в 30 раз). Сравнение с эталоном также говорит в пользу N-фениллепидиниевых производных. Кроме того, крайне важным является то, что N-фениллепидиниевые производные обладают ярко выраженными фунгицидными свойствами по отношению к трудно излечимому дрожжеподобному грибку Candida albicans.
Приведенные примеры подтверждают осуществимость изобретения. Новые соединения представляют интерес в качестве радиоактивных индикаторов для изучения механизма действия БАС, потенциальных лекарственных средств.
1. Меченные тритием N-фениллепидиниевые соли общей формулы:
2. Способ получения солей N-фениллепидиния, меченных тритием по фенильному заместителю, общей формулы: отличающийся тем, что лепидин (4-метилхинолин) подвергают ион-молекулярным реакциям со свободными меченными тритием нуклеогенными фенил-катионами, которые генерируются самопроизвольно при бета-распаде трития в составе двукратно третированного бензола в замкнутой системе в присутствии стабилизирующей соли - тетрафторобората или перхлората или йодида калия.