Способ получения лекарственной композиции, основанный на увеличении сродства поверхностей кристаллических микрочастиц к активным агентам
Иллюстрации
Показать всеИзобретение относится к кристаллической микрочастице для доставки активных агентов, которая содержит дикетопиперазин и полисорбат 80. Изобретение также относится к способу получения указанной микрочастицы. Способ включает стадии получения раствора дикетопиперазина с ограниченной растворимостью при низком значении рН, добавления полисорбата 80 к раствору и осаждения микрочастиц дикетопиперазина на стадии добавления кислоты к раствору. Изобретение также относится к способу нанесения покрытия на предварительно сформированную указанную микрочастицу. Способ включает получение суспензии, содержащей предварительно сформированную кристаллическую микрочастицу, активный агент и растворитель, изменение свойств суспензии для регулирования энергетического взаимодействия между указанным активным агентом и предварительно сформированной кристаллической микрочастицей и адсорбирование активного агента на поверхности микрочастицы для обеспечения нанесения покрытия. При этом стадия изменения свойств и стадия адсорбирования протекают без удаления растворителя из суспензии. Изобретение обеспечивает получение стабильных частиц, к которым активный агент имеет более высокое сродство, чем к раствору, в котором он находится. 3 н. и 12 з.п. ф-лы, 8 ил., 4 табл.
Реферат
Перекрестная ссылка на родственные заявки
По настоящей заявке испрашивается приоритет в соответствии с предварительной заявкой США №60/717524, поданной 14 сентября 2005, согласно 35 U.S.C. §119(е); и приоритет в соответствии с предварительной заявкой США №60/744882, поданной 14 апреля 2006, все содержание которых приведено здесь в качестве ссылки в полном объеме.
Область техники, к которой относится изобретение
Это изобретение в основном относится к области лекарственных композиций, в частности относится к способам нанесения активных агентов на поверхность кристаллических микрочастиц.
Уровень техники, к которой относится изобретение
Доставка терапевтических агентов представляет значительную проблему. Пероральный способ введения является одним из наиболее распространенных и предпочтительных путей доставки вследствие легкости введения, комплаентности пациента и невысокой стоимости. Однако к неудобствам этого пути относятся низкая или неустойчивая активность и неэффективная адсорбция лекарственного средства. Это особенно заметно, когда соединение, которое необходимо доставить, является нестабильным в условиях желудочно-кишечного тракта. В области техники разработано множество покрытий и способов инкапсуляции, но только немногие из них эффективны в отношении этой проблемы. Тем не менее, существуют терапевтические соединения, которые обычно менее активны в условиях желудочно-кишечного тракта и должны назначаться в более высоких дозировках, чтобы адсорбироваться в кровоток в эффективном количестве.
Разработан широкий ряд систем лекарственных композиций, которые направлены на достижение оптимальной доставки лекарственного средства и основаны на включении лекарственного средства в матрицу, которая играет роль носителя. К факторам, учитываемым в лекарственной композиции, относятся следующие требования: система должна быть нетоксичной, не взаимодействовать с лекарственным средством, которое необходимо доставить, экономичной в производстве, сформированной из легко доступных компонентов и должна соответствовать требованиям в отношении окончательной композиции и физических характеристик, включая стабильность и скорость высвобождения. Также предпочтительно, чтобы система доставки лекарственного средства была сформирована из материалов, легко выводимых из организма в результате нормальных физиологических процессов.
Лекарственные композиции на основе микрочастиц можно применять с помощью различных путей введения, но, в частности, хорошо подходят для доставки через легкие. К преимуществам легких для доставки агентов, оказывающих системные эффекты, относятся: большая площадь поверхности и легкость поглощения поверхностью слизистой оболочки. В патенте США №6071497, приведенном здесь в качестве ссылки, описывается система доставки лекарственного средства через легкие, основанная на формировании микрочастиц дикетопиперазина, а также микрочастиц на основе полимера.
Сущность изобретения
Предоставляются способы формирования покрытия из активного агента на кристаллических микрочастицах. В основном, микрочастицы покрывают активным агентом с помощью изменения поверхностных свойств микрочастиц таким образом, что активный агент имеет более высокое сродство к поверхности микрочастицы, чем к раствору, в котором он находится.
В настоящем изобретении рассматриваются улучшенные способы покрытия кристаллических частиц, таких как микрочастицы фумарилдикетопиперазина (FDKP), активными агентами, такими как белки, с использованием электростатических, гидрофобных ассоциаций или ассоциаций, полученных на основе водородных связей. В настоящем изобретении жидкость можно не обязательно удалять (для восстановления микрочастиц, покрытых активным агентом) с помощью фильтрации или сушки или вытеснять с помощью замены на другую среду растворителя. В любом случае, удаление жидкой среды не является обязательным шагом в формировании активного комплекса микрочастица-агент. В настоящем изобретении раскрыт способ нанесения покрытия на микрочастицы, основанный на изменении поверхностных свойств кристаллических микрочастиц, для достижения адсорбции активного агента к микрочастице.
В специфических вариантах осуществления настоящего изобретения применяется способ покрытия активным агентом предварительно сформированной кристаллической микрочастицы в суспензии, включающий: а) регулирование энергетического взаимодействия между активным агентом и кристаллической микрочастицей, независимо от удаления растворителя; б) обеспечение времени для адсорбции активного агента на поверхности микрочастицы. В некоторых вариантах осуществления изобретения, способ покрытия активным агентом предварительно сформированной кристаллической микрочастицы в суспензии может далее включать шаг удаления или замены растворителя без существенного влияния на взаимодействие между активным агентом и микрочастицей.
В других специфических вариантах осуществления настоящего изобретения, способ покрытия микрочастиц активным агентом осуществляется с помощью изменения поверхностных свойств микрочастицы. Изменение поверхностных свойств микрочастицы достигается с помощью изменения условий растворения. Эти условия, не ограничиваясь ими, включают изменение pH среды. В других вариантах осуществления поверхностные свойства микрочастицы изменяют с помощью: 1) изменения полярности раствора; 2) присоединения моновалентных или поливалентных ионов и 3) химического преобразования микрочастицы.
В еще одном варианте осуществления настоящее изобретение включает шаг растворения активного агента в жидкой фазе суспензии микрочастиц и последующего изменения pH среды. Такой шаг растворения активного агента в жидкой фазе относится к растворению твердого вещества. Кроме того, такой шаг растворения активного агента относится к добавлению более концентрированного раствора активного агента в дополнение к добавлению твердого вещества.
В еще одном варианте осуществления изменяют условия pH суспензии микрочастиц для улучшения взаимодействия между активным агентом и микрочастицей до или после добавления активного агента.
В других вариантах осуществления активный агент имеет более одного типа энергетически благоприятного взаимодействия с поверхностью микрочастицы.
В другом специфическом варианте осуществления настоящего изобретения, активным агентом является инсулин или его аналог.
В других специфических вариантах осуществления настоящего изобретения поверхностные свойства, которые создают благоприятное взаимодействие между активным агентом и микрочастицей, выбраны из группы, включающей электростатические свойства, гидрофобные свойства и свойства водородных связей.
В другом варианте осуществления настоящего изобретения, микрочастица является пористой и имеет внутренние поверхности, доступные для основной жидкой части раствора. В этом варианте осуществления микрочастица включает дикетопиперазин, такой как фумарилдикетопиперазин, но не ограничиваясь им.
В вариантах осуществления настоящего изобретения с помощью способа нанесения покрытия создается монослой активного агента на поверхности микрочастицы. В одних вариантах осуществления настоящего изобретения монослой является постоянным. В других вариантах осуществления настоящего изобретения активный агент в монослое может иметь предпочтительную ориентацию.
В еще одном варианте осуществления предоставляется способ покрытия инсулином предварительно сформированной кристаллической микрочастицы в суспензии; этот способ включает регулирование энергетического взаимодействия между активным агентом и кристаллической микрочастицей, независимо от удаления растворителя, и абсорбцию инсулина на поверхности микрочастиц.
Применяемый здесь термин растворитель относится к жидкой среде, в которой "плавают" активный агент и микрочастица. Это не следует толковать как необходимость присутствия в растворе всех компонентов. В действительности, во многих случаях термин может применяться в отношении жидкой среды, в которой взвешены микрочастицы.
Краткое описание чертежей
Следующие чертежи являются частью данного описания и включены для дальнейшей демонстрации определенных аспектов раскрытых здесь примеров. Изобретение может лучше пониматься с помощью ссылки на один или более этих чертежей в комбинации с подробным описанием представленных здесь специфических вариантов осуществления.
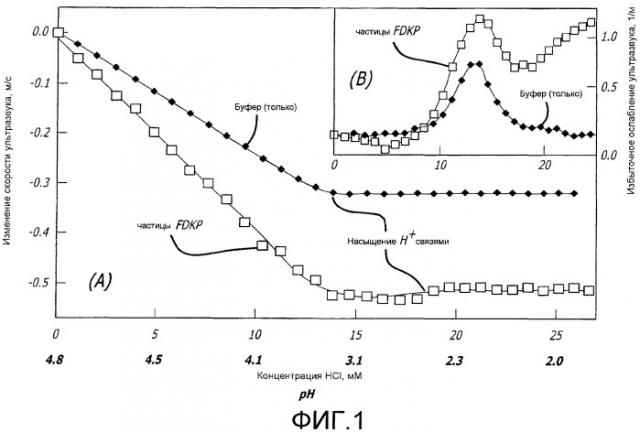
На фиг.1 представлены профили ультразвукового титрования HCl для отдельных компонентов суспензии фумарилдикетопиперазина (FDKP), частиц FDKP и буфера, согласно изложению настоящего изобретения. Величина изменений профиля титрования скорости ультразвука (Фиг.1; панель A) отражает гидратационные изменения, вызываемые протонированием ионизируемых карбоксилатных групп компонентов образца. Дополнительные пики ослабления ультразвука (Фиг.1; панель B) являются следствием быстрой релаксации в реакции протонного обмена в точке насыщения. Частота (F) равна 15 МГц, температура равна 25°С.
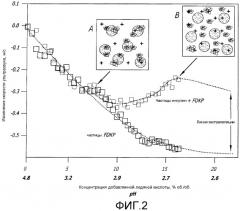
На фиг.2 представлены профили ультразвукового титрования ледяной уксусной кислотой частиц FDKP + инсулина и частиц FDKP в отдельности, согласно изложению настоящего изобретения. Профиль скорости ультразвука был рассчитан с помощью вычитания вклада инсулина; частота равна 8 МГц, температура равна 25°C. Также показано дополнительное ослабление ультразвука в зависимости от концентрации добавленной ледяной уксусной кислоты. Две стадии индуцированного окисления ледяной уксусной кислоты подобны наблюдаемой при титровании HCl. На панели вставки слева (панель A) представлено ассоциирование активного агента с микрочастицей FDKP при pH более приблизительно 2,9. На панели вставки справа (панель B) представлено ослабление взаимодействия между активным агентом и микрочастицей при pH менее приблизительно 2,9.
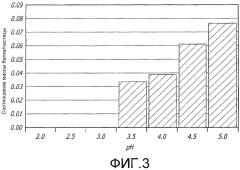
На фиг.3 представлена адсорбция белка на поверхности ионизируемых микрочастиц согласно изложению настоящего изобретения. Белок добавили в суспензию микрочастиц после регулирования pH, не связавшийся белок отфильтровали, а микрочастицы растворили для высвобождения связанного белка.
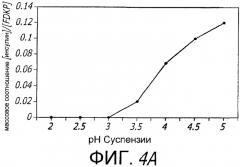
На фиг.4 показано влияние pH на адсорбцию активных агентов на поверхности микрочастиц FDKP согласно изложению настоящего изобретения. На фиг.4A показана адсорбция инсулина; на фиг.4B показана адсорбция моноклонального антитела anti-SSX-241-49; на фиг.4C показана адсорбция гормона паращитовидной железы (PTH), и на фиг.4D показана адсорбция грелина.
На фиг.5 показано влияние pH на адсорбцию инсулина на поверхности микрочастиц FDKP с ограничением концентрации инсулина согласно изложению настоящего изобретения.
На фиг.6 показано изменение скорости ультразвука в суспензии микрочастиц FDKP (11 мг/мл) при поэтапном титровании микрочастиц FDKP с белком (10 мг/мл) согласно изложению настоящего изобретения. Вклад свободного белка и эффект растворения микрочастиц FDKP не учитывали. Температура составляла 25°C.
На фиг.7 показаны кривые насыщения для адсорбции активного агента на поверхности микрочастиц FDKP, согласно изложению настоящего изобретения. Для микрочастиц активный агент/FDKP показаны кривые загрузки в зависимости от концентрации активного агента при pH 5,0. На фиг.7A показана адсорбция глюкагоноподобного пептида 1 (GLP-1); на фиг.7B показана адсорбция PTH; на фиг.7C показана адсорбция моноклонального антитела anti-SSX241-49, а на фиг.7D показана адсорбция моноклонального антитела anti-MOPC-21.
На фиг.8 показана адсорбция активных агентов на поверхности микрочастиц при pH 5,0 под влиянием повышения концентрации соли, согласно изложению настоящего изобретения. Активный агент добавили в суспензию микрочастиц после регулирования pH, не связавшийся агент отфильтровали, а микрочастицы растворили для высвобождения связанного агента. На фиг.8A показана адсорбция инсулина, на фиг.8B показана адсорбция моноклонального антитела anti-SSX-241-49, на фиг.8C показана адсорбция PTH, а на фиг.8D показана адсорбция грелина.
Подробное описание изобретения
Агенты, которые необходимо доставить
Вещество для нанесения на кристаллическую микрочастицу называется здесь активным агентом. К примерам классов активных агентов относятся фармацевтические композиции, синтетические соединения и органические макромолекулы, которые имеют терапевтическую, профилактическую и/или диагностическую полезность.
В основном, любая форма активного агента может быть нанесена на поверхность кристаллической микрочастицы. Эти материалы могут быть органическими макромолекулами, включая нуклеиновые кислоты, синтетическими органическими соединениями, полипептидами, пептидами, белками, полисахаридами и другими сахарами, и липидами. Пептиды, белки и полипептиды представляют собой цепи аминокислот, связанных пептидными связями. В основном считают, что пептиды состоят из менее 30 аминокислотных остатков, но могут состоять из большего числа. Белки являются полимерами, которые могут содержать более чем 30 аминокислотных остатков. Известный в области техники и применяемый здесь термин полипептид может относиться к пептиду, белку или любой другой цепи аминокислот любой длины, имеющей многочисленные пептидные связи, даже состоящей из, по крайней мере, 10 аминокислот. Активные агенты, применяемые в композиции покрытия, могут относиться к различным классам по биологической активности, таким как, например, вазоактивные агенты, нейроактивные агенты, гормоны, антикоагулянты, иммуномодулирующие агенты, цитотоксические агенты, антибиотики, противовирусные агенты, антигены и антитела. Конкретнее, к активным агентам могут относиться, не ограничиваясь ими, инсулин и его аналоги, гормон роста, гормон паращитовидной железы (PTH), грелин, гранулоцитарно-макрофагальный колониестимулирующий фактор (GM-CSF), глюкагоноподобный пептид 1 (GLP-1), техасский красный, алкины, циклоспорины, клопидогрель и PPACK (дифенилаланил-L-пролил-L-аргининхлорметилкетон), антитела и их фрагменты, включая, но не ограничиваясь ими, человеческие антитела или искусственные антитела; F(ab), F(ab)2 или одноцепочечное антитело в отдельности либо слитое с другими полипептидами; терапевтические или диагностические моноклональные антитела к раковым антигенам, цитокинам, инфекционным агентам, медиаторам воспаления, гормонам и поверхностным клеточным антигенам. К неограничивающим примерам антител к опухолевым антигенам относятся anti-SSX-241-49 (синовиальная саркома, X инициация реаранжировки 2), anti-NY-ESO-1 (ассоциированный с опухолью пищевода антиген), anti-PRAME (предпочтительно экспрессируемый антиген меланомы), anti-PSMA (простатоспецифический мембранный антиген), anti-Melan-A (опухолеассоциированный антиген меланомы), антитирозиназа (опухолеассоциированный антиген меланомы) и anti-MOPC-21 (плазмоклеточный белок миеломы).
Система доставки - кристаллические микрочастицы
В основном, термин "микрочастица" относится к частице с диаметром приблизительно 0,5-1000 мкм, независимо от точно определенной внешней или внутренней структуры. В пределах широкой категории микрочастиц, "микросферы" относятся к микрочастицам с однородной сферической формой. Применяемый здесь термин «кристаллические микрочастицы» относится к микрочастицам, имеющим внутреннюю структуру, но не обязательно внешнюю форму кристалла, и имеющим правильное расположение атомов в пространственной решетке, термин «ионизируемые кристаллические поверхности» относится к кристаллическим микрочастицам, которые имеют дополнительную емкость, чтобы нести электрический заряд.
Предпочтительно, химическое вещество, составляющее кристаллическую микрочастицу, способно обратимо взаимодействовать с активным агентом, который необходимо доставить, а также является нетоксичным и не подвергается метаболизму, по крайней мере, у грызунов и людей. Кроме того, кристаллическая структура предпочтительных микрочастиц существенно не разрушается в процессе нанесения активного агента. Композиция кристаллической микрочастицы определяет, на какие виды химических взаимодействий можно воздействовать, чтобы управлять адсорбцией активного агента на поверхности микрочастицы.
Для формирования кристаллических микрочастиц можно применять многие вещества. Собственно микрочастицы имеют внешнюю поверхность, на свойства которой можно воздействовать в процессе нанесения покрытия. К характерным материалам, из которых можно сформировать кристаллические микрочастицы, относятся, но не ограничиваясь ими: ароматические аминокислоты, соли с ограниченной растворимостью в определенном диапазоне pH, такие как дикетопиперазины и сульфаты морфолина.
В патентах США 5352461 и 5503852, приведенных здесь в качестве ссылки в полном объеме, описана система доставки лекарственного средства, основанная на формировании микрочастиц дикетопиперазина (DKP) из производных дикетопиперазина, таких как 3,6-бис-N-фумарил-N-(н-бутил)амино (также называемый фумарилдикетопиперазин или FDKP; также называемый (E)-3,6-бис-[4-(N-карбокси-2-пропенил)амидобутил]-2,5-дикетопиперазин), которые являются устойчивыми при низком pH и распадаются при pH крови или тонкой кишки. Как раскрыто в вышеупомянутых патентах, лекарственное средство, которое необходимо доставить, комбинируется или загружается частицами дикетопиперазина с помощью формирования микрочастиц DKP в присутствии лекарственного средства (полезная загрузка). Система, основанная на структурных элементах дикетопиперазина или одном из его замещенных производных, включая, но не ограничиваясь ими, дикетоморфолины и дикетодиоксаны, формирует микрочастицы с желательным распределением по размеру и диапазонам pH, а также с хорошей толерантностью к полезной загрузке. Широкий диапазон устойчивых, воспроизводимых характеристик может быть получен с помощью соответствующих манипуляций замещающих групп.
К другим дикетопиперазинам, которые могут рассматриваться в настоящем изобретении, относятся 3,6-ди(4-аминобутил)-2,5-дикетопиперазин; 3,6-ди(сукцинил-4-аминобутил)-2,5-дикетопиперазин (сукцинилдикетопиперазин или SDKP); 3,6-ди(малеил-4-аминобутил)-2,5-дикетопиперазин; 3,6-ди(цитраконил-4-аминобутил)-2,5-дикетопиперазин; 3,6-ди(глутарил-4-аминобутил)-2,5-дикетопиперазин; 3,6-ди(малонил-4-аминобутил)-2,5-дикетопиперазин; 3,6-ди(оксалил-4-аминобутил)-2,5-дикетопиперазин и их производные. В настоящем изобретении могут применяться также соли дикетопиперазина, и они могут включать, например, фармацевтически приемлемую соль, такую как соль Na, K, Li, Mg, Ca, аммония или моно-, ди- или триалкиламмония (полученную из триэтиламина, бутиламина, диэтаноламина, триэтаноламина или пиридинов и т.п.). Соль может быть моно-, ди- или смешанной солью. Соли более высокого порядка также предусмотрены для дикетопиперазинов, в которых R-группы содержат более одной кислотной группы. В других аспектах изобретения, основная форма агента может быть смешана с дикетопиперазином для формирования соли лекарственного средства с дикетопиперазином, такой, что лекарственное средство является противоположным катионом дикетопиперазина.
В патентах США 6444226 и 6652885, каждый из которых приведен здесь в качестве ссылки в полном объеме, описано получение и предоставление микрочастиц DKP в водной суспензии, в которую добавляют раствор активного агента, а затем проводят решающий шаг лиофилизации суспензии, для получения микрочастиц, имеющих оболочку из активного агента. Основным для этой композиции является то, что нанесение покрытия, содержащего активный агент, на микрочастицу управляется с помощью удаления жидкой среды с помощью лиофилизации (см. также патент США 6440463, приведенный здесь в качестве ссылки в полном объеме). В отличие от описаний предшествующего уровня техники, настоящее изобретение предоставляет средства регулирования связывания активного агента с микрочастицей до удаления растворителя. Таким образом, удаление жидкой среды с помощью насыпных физических методов (например, фильтрации или седиментации) или методов испарения (например, лиофилизации или распылительной сушки) может приводить к сопоставимой загрузке.
Контролируемое нанесение покрытия на кристаллические микрочастицы
Контролируемое нанесение покрытия относится к направленному процессу адсорбции активного агента на поверхности кристаллической микрочастицы. Процесс нанесения покрытия включает изменение поверхностных свойств кристаллических микрочастиц в жидкой суспензии либо с помощью изменения условий растворения (таких как pH фактор, температура, полярность, ионная сила и ко-растворители), либо с помощью образования комплексов с моно- или мультивалентными ионами, или с помощью химического преобразования. Изменение поверхностных свойств микрочастицы или до, или после добавления активного агента изменяет ее химические взаимодействия с активным агентом, что приводит к адсорбции активного агента на кристаллической микрочастице. Химическое взаимодействие между микрочастицей и активным агентом управляет адсорбцией и приводит к образованию монослоя активного агента на поверхности микрочастицы. Как только молекула активного агента адсорбируется, эта часть поверхности микрочастицы становится недоступной для дальнейшего взаимодействия и адсорбции дополнительного активного агента в той конкретной точке поверхности. Получающийся монослой может быть или сплошным (нет промежутков между адсорбированными молекулами активного агента на доступной поверхности), или несплошным (промежутки непокрытой поверхности микрочастицы между адсорбированными молекулами активного агента).
Адсорбция активного агента на микрочастицах
Как обсуждалось выше, адсорбция активного агента на микрочастице приводит к нанесению активного агента на микрочастицу в виде монослоя. Тем не менее, существует более одного механизма адсорбции активного агента, такого как, например, инсулин, на кристаллические микрочастицы.
Получение монослоя активного агента, такого как инсулин, который покрывает микрочастицу, является одной стадией процесса загрузки инсулина на микрочастицу, но не обязательно конечной, приводящей к процессу загрузки, при котором могут быть сформированы как мономерные, так и мультимерные слои, основываясь на энергетических свойствах системы.
В условиях необязательной растворимости, таких как низкая концентрация инсулина и/или низкий pH (в основном ниже pH 5,0), силы притяжения между инсулином и поверхностью частицы FDKP намного больше, чем самоассоциативные силы инсулина. Таким образом, нанесение инсулина на микрочастицу происходит в виде монослоя, и насыщенность покрытия достигается без необходимости концентрации инсулина или создания его мультислоя на поверхности микрочастицы (см. пример 6). Если растворимость приближается к насыщению, вследствие высокой концентрации инсулина и/или значения pH, близкого к 5,0 (минимум растворимости для природного инсулина), самоассоциирование инсулина становится более энергетически выгодным. Таким образом, процесс нанесения покрытия может пойти далее точки создания насыщенного монослоя, и на частицу могут быть добавлены дополнительные слои инсулина. Можно выделить две формы самоассоциирования: мультимеризацию и агрегацию. Мультимеризация характеризуется специфическими межмолекулярными взаимодействиями и постоянной стехиометрией. Агрегация характеризуется неспецифическими межмолекулярными взаимодействиями и непостоянной стехиометрией. В общих чертах, мультимерные активные агенты могут адсорбироваться в мультимерном состоянии или в разъединенном на мономеры или на мультимеры низшего порядка и адсорбироваться на поверхности в таком состоянии. В любом случае агрегация может опосредовать нанесение активного агента на микрочастицу. В соответствии с настоящими представлениями изобретателей, при общих условиях, используемых в примерах настоящего раскрытия (таких как растворение инсулина в уксусной кислоте), осаждение дополнительных слоев инсулина происходит в виде агрегации негексамерного инсулина.
Способ нанесения покрытия на микрочастицы
Процесс нанесения покрытия, содержащего активные агенты, на кристаллические микрочастицы, такие как предварительно сформированные кристаллические микрочастицы, описывается, в основном, следующим образом: кристаллические микрочастицы, предварительно сформированные с помощью осаждения или другого способа, суспендируются в жидкой среде, такой как вода; и среда регулируется для изменения поверхности частиц либо до, либо после добавления активного агента. В этой точке активный агент будет адсорбироваться на поверхности микрочастицы и через определенный период времени (например, <1, 1, 2, 3, 4, 5, 6, 7, 8, 9 или 10 минут; предпочтительно от <1 до 5 минут), процесс нанесения покрытия завершается. Жидкая среда может быть удалена с помощью любого способа, включая фильтрацию, центрифугирование, лиофилизацию или распылительную сушку, или заменена с помощью обмена на другую среду. Адсорбция может быть подтверждена с помощью любого из двух экспериментальных способов: 1) демонстрации отсутствия значительных количеств активного агента в фильтрате или в супернатанте и/или 2) демонстрации присутствия активного агента в твердой фазе, одновременно показывающего, что активный агент не осаждается, когда тот же самый процесс проходит в отсутствие микрочастиц.
Воздействие на поверхностные свойства микрочастиц
Как здесь было раскрыто ранее, на поверхностные свойства микрочастиц можно воздействовать с помощью различных способов. Поверхностные свойства микрочастиц, на которые можно воздействовать, включают, но не ограничиваясь ими, электростатические, гидрофобные свойства и способность к образованию водородных связей. В различных вариантах осуществления эти воздействия осуществляют в отсутствии или присутствии активного агента либо до, либо после смешивания микрочастиц и активного агента. Когда воздействие осуществляют в присутствии активного агента, например, с помощью изменения условий растворения, также можно оказать воздействия на активный агент, которые изменяют его сродство к поверхности. Таким образом, в некоторых вариантах осуществления настоящего изобретения, процесс нанесения покрытия на микрочастицы может включать воздействие на поверхностные свойства и изменение свойств активного агента. Способы, подобные последним, раскрыты в со-заявке в стадии рассмотрения на патент США № __/_ (Attorney Docket No. 51300-00035), называемой «Способ получения лекарственной композиции, основанный на усилении сродства активных агентов к поверхности кристаллической микрочастицы», поданной в одну и ту же дату с настоящей заявкой и приведенной здесь в качестве ссылки в полном объеме.
К электростатическим взаимодействиям относятся притяжения между противоположными зарядами или отталкивания между одинаковыми зарядами, которые становятся сильнее при приближении зарядов друг к другу. Электростатические взаимодействия являются ключевым компонентом в понимании взаимодействий между заряженными телами в ионных растворах. Например, стабильность коллоидных частиц, рассеянных в растворителе, можно объяснить с помощью рассмотрения конкуренции между отталкивающими электростатическими взаимодействиями и притягивающими взаимодействиями Ван-дер-Ваальса. Кроме того, химические функциональные группы (например, но не ограничиваясь ими, COOH, NH и др.) на поверхности микрочастицы могут использоваться как противоионы по отношению к ионизированному активному агенту так, что смесь активный агент/частица включает соль. Электростатические взаимодействия также важны, когда рассматриваются взаимодействие и адгезия между частицами.
Изменение pH системы окружающего раствора может изменять электростатические свойства ионизируемых кристаллических микрочастиц в суспензии. Как показано в примере 3, изменение pH раствора в свою очередь изменяет ионизацию микрочастицы так, что активный агент адсорбируется на поверхности микрочастицы. В частности, в примере 4 показано, что микрочастицы, состоящие из FDKP (3,6-бис[N-фумарил-N-(н-бутил)амино]2,5-дикетопиперазина), ионизируются. Микрочастицы нерастворимы в воде при pH ниже 3,5, но быстрое повышение растворимости при pH от 3,5 до 5,0, по-видимому, происходит вследствие ионизации карбоксильных групп. Микрочастица FDKP частично ионизирована при pH 5 и полностью растворяется при более высоком pH, что может быть опосредованно обнаружено с помощью ультразвуковой спектроскопии. В примере 5 показано контролируемое нанесение покрытия, содержащего белок, на поверхность микрочастицы FDKP. В одном варианте осуществления, микрочастицы дикетопиперазина суспендируют в кислом растворе, к суспензии добавляют активный агент, и pH раствора повышается после того, как активный агент и микрочастицы смешивают вместе. Повышенный pH изменяет поверхностные свойства микрочастиц и создает среду, в которой активный агент имеет более высокое сродство к микрочастице, чем к растворителю.
В альтернативном варианте, pH суспензии микрочастиц может быть повышен непосредственно перед добавлением активного агента в раствор. Свойства поверхностного заряда микрочастицы изменяют с помощью изменения pH так, что активный агент имеет более высокое сродство к микрочастице, чем к сохранению в растворе, и адсорбируется к поверхности микрочастицы после добавления.
В примерах 6 и 7 показано нанесение инсулина на частицы FDKP с помощью воздействия на условия pH. Наконец, насыщение микрочастиц с помощью адсорбции белка и формирование монослоя описаны в примере 6.
Другие способы воздействия на поверхность микрочастиц
В дополнение к электростатическим свойствам, для воздействия на адсорбцию активного агента могут использоваться другие свойства поверхности микрочастицы. Для изменения поверхностных свойств можно воздействовать на микрочастицы, содержащие соединения с имидазолом, пиридином, основаниями Шиффа, кетоном, биоизостерами карбоновых кислот, амидами или другими функциональными группами, которые могут существовать в сложных структурах.
Гидрофобные взаимодействия являются ассоциациями неполярных групп друг с другом в водных растворах вследствие их нерастворимости в воде. Гидрофобные взаимодействия могут влиять на многие молекулярные процессы, включая, но не ограничиваясь ими, структурную стабилизацию (будь это одиночные молекулы, комплексы из двух или трех молекул или более крупные образования) и динамику, и важным образом способствовать процессам связывания белок-белок и белок-лиганд. Также известно, что эти взаимодействия играют роль при ранней стадии укладки структуры белка и вовлечены в комплексообразование и феномен самосборки (например, формирование мембран).
На гидрофобные взаимодействия можно воздействовать с помощью изменения протонирования микрочастиц, состоящих из гистидина. Присоединение протона к гистидину уменьшает нуклеофильность кристаллических микрочастиц и придает положительный заряд.
Водородные связи являются особо сильными диполь-дипольными силами между молекулами; атом водорода в полярной связи (например, H-F, H-O или H-N) может подвергаться воздействию силы притяжения соседней отрицательно заряженной молекулы или иона, который имеет неподеленную пару электронов (обычно атом F, O или N в другой молекуле). Водородные связи отвечают за уникальные свойства воды и очень важны в организации биологических молекул, особенно при влиянии на структуру белков и ДНК.
В настоящем изобретении, свойства водородных связей поверхности микрочастицы можно контролировать с помощью химического преобразования. Для изменения поверхности микрочастицы могут быть химически добавлены доноры/акцепторы водородных связей. Например, водород в связи N-H может подвергаться воздействию водородной связи кислорода в связи C=O. Если N-H заменяется на N-CH3, то это специфическое взаимодействие водородной связи пропадает. Аналогично, замена группы C=O на группу C=C также устраняет это специфическое взаимодействие связей.
Микрочастицы с поверхностями, содержащими ионизируемые ароматические группы, полярны в состоянии ионизации, но гидрофобны в неионизированном состоянии. Начиная с протонирования поверхностей и воздействия на условия растворения для уменьшения ионизации поверхности частицы, гидрофобные или ароматические активные агенты покрывают поверхность микрочастицы.
На микрочастицы с кетонными поверхностными группами можно было бы воздействовать с помощью изменения полярности раствора. С помощью уменьшения полярности раствора (с помощью добавления низкополярных органических растворителей к водному раствору) енольная форма становится преобладающим видом на поверхности частицы. Такая енольная форма является донором водородной связи, тогда как кетоформа является акцептором водородной связи. Адсорбция нитросодержащих лекарственных средств на поверхности микрочастицы активизируется таким же образом.
Микрочастицы с поверхностными группами, которые подвергаются pH- или температурно-индуцированной изомеризации, могут также быть индуцированы для адсорбции молекул лекарственного средства с помощью воздействия на условия растворения. В случае с этими поверхностями, введение нелинейных участков в линейную поверхностную группу, вследствие изомеризации, увеличивает подвижность (текучесть) групп на поверхности микрочастицы. Это позволяет поверхности формировать больше контактов с активным агентом, чем это возможно при упорядоченной поверхности. Если дополнительные взаимодействия с активным агентом благоприятны в каждом случае, то благоприятной становится общая энергия взаимодействия, и лекарственное средство адсорбируется на поверхности микрочастицы.
Способы удаления жидкой среды
Удаление растворителя после контролируемого покрытия кристаллических поверхностей активным агентом может быть достигнуто с помощью способов, включающих, но не ограничиваясь ими, седиментацию, фильтрацию или сушку. Способы сушки включают, но не ограничиваясь ими, лиофилизацию и распылительную сушку. Эти способы известны специалистам, знакомым с уровнем техники. В одном варианте осуществления настоящего изобретения растворитель удаляют с помощью распылительной сушки. Способы распылительной сушки микрочастиц дикетопиперазина описаны, например, в предварительной заявке на патент США №60/776605, поданной 22 февраля 2006, приведенной здесь в качестве ссылки в полном объеме, в которой рассматривается распылительная сушка микрочастиц дикетопиперазина.
Анализ изменений поверхностных свойств
В настоящем изобретении применяется способ ультразвуковой спектроскопии, чтобы анализировать изменения поверхностных свойств кристаллических микрочастиц в жидкой суспензии, которые способствуют или улучшают адсорбцию активного агента на кристаллической микрочастице. Как здесь было раскрыто, к таким изменениям относятся изменения условий растворения (таких как pH, температура, полярность, ионная сила и ко-растворители) с помощью комплексообразования с моно- или мультивалентными ионами или с помощью химических преобразований с целью изменения поверхностных свойств микрочастицы до или после добавления активного агента.
Ультразвуковая спектроскопия относится к аналитическим способам, известным специалистам в области техники. Вкратце, в ультразвуковой спектроскопии применяются звуковые волны. В частности, в ультразвуковой спектроскопии применяется высокочастотная акустическая волна, которая исследует межмолекулярные силы в образцах/материалах. Вибрационная компрессия (и декомпрессия) ультразвуковой волны вызывает колебание молекулярных структур в образце, что вызывает межмолекулярное притяжение или отталкивание.
Проходя через образцы, ультразвуковая волна теряет свою энергию (уменьшение амплитуды) и изменяет свою скорость. Уменьшение амплитуды и изменение скорости анализируются как характеристики образца. Следовательно, распространение ультразвуковых волн зависит от скорости и ослабления ультразвука.
Скорость ультразвука зависит от