Фармацевтические композиции и способы лечения сухих кератитов
Иллюстрации
Показать всеГруппа изобретений относится к медицине, а именно к офтальмологии, и может быть использована для лечения сухости глаз и восстановления нормальной секреции слезной жидкости у млекопитающего. Для этого млекопитающему вводят композицию, содержащую фармацевтически эффективное количество ингибитора янус-киназы-3, имеющего структуру: 3-{(3R,4R)-4-метил-3-[метил-(7Н-пирроло[2,3-d]пиримидин-4-ил)амино]пиперидин-1-ил}-3-оксопропионитрил. Ведение ингибитора янус-киназы-3 позволяет значительно увеличить объем секретируемой слезной жидкости. 3 н. и 8 з.п. ф-лы, 2 табл., 6 пр., 8 ил.
Реферат
По настоящей заявке испрашивается приоритет согласно предварительной заявке США №60/949216, поданной 11 июля 2007 г., и предварительной заявке США №61/060032, поданной 9 июня 2008 г., содержание которых вводится в настоящее изобретение полностью с помощью ссылки.
Уровень техники
Сухость глаз, также известная в общем как сухой кератоконъюнктивит, является широко распространенным офтальмологическим расстройством, от которого страдают миллионы американцев каждый год. Сухость глаз является многофакторным заболеванием, связанным с секрецией слезной жидкости и поверхностью глаз, которое вызывает симптомы дискомфорта, нарушения зрения и нестабильности слезной пленки с возможным повреждением поверхности глаза. Оно сопровождается повышенной осмолярностью слезной пленки и воспалением поверхности глаза.
Сухость глаз может поражать индивидуумов с разной степенью тяжести. Сухость глаз, в частности, широко распространена у женщин после менопаузы в результате гормональных изменений после потери способности к деторождению. В легких формах заболевания пациент может испытывать жжение, чувство сухости и постоянное раздражение, подобное тому, которое вызвано маленькими частицами, попадающими между глазным веком и поверхностью глаза. В тяжелых случаях зрение может быть повреждено значительно. Другие заболевания, такие как болезнь Шегрена и рубцующийся пемфигоид, проявляют осложнения с сухостью глаз.
Этиопатогенная классификация сухости глаз была впервые разработана в 1995 г. National Eye Institute/Industry Dry Eye Workshop и затем дополнена в январе 2007 г. определениями. The Ocular Surface, vol.5, no. 2, 75-92 (2007). Основные классы сухости глаз включают сухость глаз при недостатке водной компоненты слезной жидкости и сухость глаз в результате испарения. Сухость глаз при недостатке водной компоненты слезной жидкости включает два основных подкласса, сухость глаз при синдроме Шегрена и сухость глаз, не связанная с синдромом Шегрена (первичные и вторичные дефекты слезной железы, обструкция каналов слезных желез, рефлекторная гипосекреция, блокировка двигательных рефлексов). Сухость глаз в результате испарения, являющаяся результатом избыточной потери воды с подвергаемой внешним воздействиям поверхности глаза при нормальной секреции слезной жидкости, включает подклассы по внутренним причинам (дисфункция мейбомиевой железы, заболевания отверстия века и заболевания века/глазного яблока, низкая частота моргания) и внешним причинам (расстройства и заболевания поверхности глаза, ношение контактных линз, аллергические конъюнктивиты, такие как весенние кератоконъюнктивиты).
Хотя кажется, что сухость глаз может возникать в результате ряда несвязанных патогенных причин, все проявления осложнения обладают общим эффектом, а именно нарушением глазной слезной пленки, что приводит к обезвоживанию подвергаемой внешним воздействиям внешней поверхности и многим симптомам, изложенным выше (Lemp, Report of the national Eye Institute/Industry workshop on Clinical Trials in Dry Eyes, the CLAO Journal, vol.21, no. 4, p.221-231 (1995)).
Практикующие врачи применяют несколько подходов для лечения сухости глаз. Один общий подход заключается в том, что нужно восполнять и стабилизировать глазную слезную пленку, применяя так называемую искусственную слезную жидкость, закапываемую в течение дня. Другие подходы включают применение глазных вставок, которые имитируют глазную жидкость или стимулируют эндогенную секрецию слезной жидкости.
Примеры подхода с применением заменителя слезной жидкости включают применение буферных, изотонических солевых растворов, водных растворов, содержащих растворимые в воде полимеры, которые придают раствору большую вязкость и, таким образом, менее легко стекают с глаз. Слезную пленку также пытаются восстановить добавлением одного или более компонентов слезной пленки, таких как фосфолипиды и масла. Показано, что фосфолипидные композиции являются пригодными для лечения сухости глаз; смотри, например, McCulley and Shine, Tear film structure and dry eye, Contactologio, vol.20(4), p.145-9 (1998). Также известны системы доставки фосфолипидных лекарственных средств, содержащих фосфолипиды, пропелленты и активное вещество, смотри патент США №5174988.
Другой подход включает применение смазочных веществ вместо искусственных слез. Например, в патенте США №4818537 (Guo) описывают применение смазочных композиций на основе липосом и в патенте США №5800807 (Hu et al.) описывают композиции, содержащие глицерин и пропиленгликоль, для лечения сухости глаз.
Хотя при применении данных подходов достигается некоторый успех, проблемы при лечении сухости глаз, тем не менее, остаются. Применение заменителей слезной жидкости, хотя временно и эффективно, обычно требует повторного применения в часы бодрствования пациента. Нередко пациент вынужден применять раствор искусственной слезной жидкости 10-20 раз в течение дня. Данный процесс является не только утомительным и требующим много времени, но он также является потенциально очень дорогим. Сообщают, что временные симптомы сухости глаз, связанные с рефрактивной хирургией, проявляются в некоторых случаях в течение промежутка времени от шести недель до шести месяцев или более после хирургической операции.
Помимо исследований, направленных непосредственно на облегчение симптомов, связанных с сухостью глаз, также ведутся поиски способов и композиций, направленных на лечение состояния, при котором наблюдается сухость глаз. Например, в патенте США №5041434 (Lubkin) описывают применение половых стероидов, таких как конъюгированные эстрогены, для лечения состояний с сухостью глаз у женщин после менопаузы; в патенте США №5290572 (MacKeen) описывают применение мелкоизмельченной композиции, содержащей ионы кальция, для того чтобы стимулировать генерирование слезной пленки передней поверхности глаз; и в патенте США №4966773 (Gressel et al.) описывают применение микрочастиц одного или более ретиноидов для нормализации глазных тканей.
В некоторых печатных сообщениях предполагают, что пациенты, страдающие от синдрома сухости глаз, несоразмерно проявляют отличительные признаки чрезмерного воспаления в соответствующих глазных тканях, таких как слезная и мейбомиевая железа. Описывают применение различных соединений для лечения пациентов с сухостью глаз, таких как стероиды, например, в патенте США №5968912; Marsh, et al., Topical nonpreserved methylprednisolone therapty for keratoconjunctivities sicca in Sjogren syndrome, Ophthalmology, 106(5): 881-816 (1999); Plugfelder et al, в патенте США №6153607; ингибиторы высвобождения цитоксинов (Yanni, J. M.; et al WO0003705 A1), циклоспорин A [Tauber, J. Adv. Exp. Med. Biol. 1998, 438, (Lacrimal Gland, Tear Fiom and Dry Eye Syndromes 2), 969] и 15-HETE (Yanni et al., U.S. Pat. №5696166).
В добавление к сухости глаз, Jak3 ингибиторы могут быть полезны для лечения других глазных заболеваний, связанных с воспалением, включая, но не ограничиваясь, глаукому, увеит, диабетическую ретинопатию и возрастную дегенерацию желтого пятна. При финансируемых CNIB исследованиях было обнаружено, что пациенты, имеющие биомаркер воспаления, антикардиолипин, были в четыре раза более склонны к развитию глаукомы. Ранее Jak3 ингибиторы рекомендовали для лечения диабета, хотя, по-видимому, их не рассматривали в качестве лекарственных средств, в частности, для лечения диабетической ретинопатии. Cetkovic-Cvrle, M. and Uckun, F. M., Arch Immunol Ther Exp (Warsz), 52(2), 69-82 (2004). Rodrigues обнаружил, что выделение иммуноглобулинов, белков системы комплемента, цитокинов и активированной микроглии в клетках пигментного эпителия сетчатки (RPE) и друзах свидетельствует о роли воспаления в возрастной дегенерации желтого пятна с сухостью глаз. Rodrigues E.B., Ophthalmologica, 221(3):143-52 (2007).
Сущность изобретения
Настоящее изобретение относится к способу лечения сухости глаз, который включает введение млекопитающему композиции, содержащей фармацевтически приемлемый носитель и фармацевтически эффективное количество ингибитора янус-киназы-3 ("Jak3"). В одном аспекте Jak3 ингибиторы являются соединением формулы I:
,
где
R1 представляет собой группу формулы
,
в которой y равен 0, 1 или 2;
R4 выбирают из группы, состоящей из водорода, (С1-C6)алкила, (C1-C6)алкилсульфонила, (C2-C6)алкенила, (C2-C6)алкинила, в которых алкильная, алкенильная и алкинильная группы необязательно замещены дейтерием, гидрокси, амино, трифторметилом, (C1-C4)алкокси, (C1-C6)ацилокси, (C1-C6)алкиламино, ((C1-C6)алкил)2амино, циано, нитро, (C2-C6)алкенилом, (C2-C6)алкинилом или (C1-C6)ациламино; или R4 представляет собой (C3-C10)циклоалкил, в котором циклоалкильную группа необязательно замещена дейтерием, гидрокси, амино, трифторметилом, (C1-C6)ацилокси, (C1-C6)ациламино, (C1-C6)алкиламино, ((C1-C6)алкил)2амино, циано, циано(C1-C6)алкилом, трифторметил(C1-C6)алкилом, нитро, нитро(C1-C6)алкилом или (C1-C6)ациламино;
R5 представляет собой (C2-C9)гетероциклоалкил, в котором гетероциклоалкильные группы должны быть замещены 1-5 карбокси, циано, амино, дейтериями, гидрокси, (C1-C6)алкилами, (C1-C6)алкокси, галогенами, (C1-C6)ацилами, (C1-C6)алкиламино, амино(C1-C6)алкилами, (C1-C6)алкокси-CO-NH, (C1-C6)алкиламино-CO-, (C2-C6)алкенилами, (C2-C6)алкинилами, (C1-C6)алкиламино, амино(C1-C6)алкилами, гидрокси(C1-C6)алкилами, (C1-C6)алкокси(C1-C6)алкилами, (C1-C6)ацилокси(C1-C6)алкилами, нитро, циано(C1-C6)алкилами, галоген(C1-C6)алкилами, нитро(C1-C6)алкилами, трифторметилами, трифторметил(C1-C6)алкилами, (C1-C6)ациламино, (C1-C6)ациламино(C1-C6)алкилами, (C1-C6)алкокси(C1-C6)ациламино, амино(C1-C6)ацилами, амино(C1-C6)ацил(C1-C6)алкилами, (C1-C6)алкиламино(C1-C6)ацилами, ((C1-C6)алкил)2амино(C1-C6)ацилами, R15R16N-CO-O-, R15R16N-CO-(C1-C6)алкилами, (C1-C6)алкил-S(O)m, R15R16NS(O)m, R15R16NS(O)m, (C1-C6)алкилами, R15S(O)mR16N, R15S(O)mR16N(C1-C6)алкилами, где m равно 0, 1 или 2 и каждый из R15 и R16 независимо выбирают из водорода или (C1-C6)алкила; или группу формулы
,
где a равно 0, 1, 2, 3 или 4; каждый b, c, e, f и g независимо равен 0 или 1; d равно 0, 1, 2 или 3;
X представляет собой S(O)n, где n равно 0, 1 или 2; кислород, карбонил или -C(=N-циано);
Y представляет собой S(O)n, где n равно 0, 1 или 2; или карбонил; и Z представляет собой карбонил, C(O)O-, C(O)NR- или S(O)n, где n равно 0, 1 или 2;
каждый R6, R7, R8, R9, R10 и R11 независимо выбирают из группы, состоящей из водорода или (C1-C6)алкила, необязательно замещенного дейтерием, гидрокси, амино, трифторметилом, (C1-C6)ацилокси, (C1-C6)ациламино, (C1-C6)алкиламино, ((C1-C6)алкил)2амино, циано, циано(C1-C6)алкилом, трифторметил(C1-C6)алкилом, нитро, нитро(C1-C6)алкилом или (C1-C6)ациламино;
R12 представляет собой карбокси, циано, амино, оксо, дейтерий, гидрокси, трифторметил, (C1-C6)алкил, трифторметил(C1-C6)алкил, (C1-C6)алкокси, галоген, (C1-C6)ацил, (C1-C6)алкиламино, ((C1-C6)алкил)2амино, амино(C1-C6)алкил, (C1-C6)алкокси-CO-NH, (C1-C6)алкиламино-CO-, (C2-C6)алкенил, (C2-C6)алкинил, (C1-C6)алкиламино, гидрокси(C1-C6)алкил, (C1-C6)алкокси(C1-C6)алкил, (C1-C6)ацилокси(C1-C6)алкил, нитро, циано(C1-C6)алкил, галоген(C1-C6)алкил, нитро(C1-C6)алкил, трифторметил, трифторметил(C1-C6)алкил, (C1-C6)ациламино, (C1-C6)ациламино(C1-C6)алкил, (C1-C6)алкокси(C1-C6)ациламино, амино(C1-C6)ацил, амино(C1-C6)ацил(C1-C6)алкил, (C1-C6)алкиламино(C1-C6)ацил, ((C1-C6)алкил)2амино(C1-C6)ацил, R15R16N-CO-O-, R15R16N-CO-(C1-C6)алкил, R15C(O)NH, R15OC(O)NH, R15NHC(O)NH, (C1-C6)алкил-S(O)m, (C1-C6)алкил-S(O)m-(C1-C6)алкил, R15R16NS(O)m, R15R16NS(O)m (C1-C6)алкил, R15S(O)mR16N, R15S(O)mR16N(C1-C6)алкил, где m равно 0, 1 или 2 и каждый R15 и R16 независимо выбирают из водорода или (C1-C6)алкила;
каждый R2 и R3 независимо выбирают из группы, состоящей из водорода, дейтерия, амино, галогена, гидрокси, нитро, карбокси, (C2-C6)алкенила, (C2-C6)алкинила, трифторметила, трифторметокси, (CrC6)алкила, (C1-C6)алкокси, (C1-C10)циклоалкила, в которых алкильную, алкокси или циклоалкильную группу необязательно замещают 1-3 группами, выбранными из галогена, гидрокси, карбокси, амино(C1-C6)алкилтио, (C1-C6)алкиламино, ((C1-C6)алкил)2амино, (C5-C9)гетероарила, (C2-C9)гетероциклоалкила, (C3-C9)циклоалкила или (C1-C10)арила; или каждый R2 и R3 независимо представляет (C1-C10)циклоалкил, (C1-C10)циклоалкокси, (C1-C6)алкиламино, ((C1-C6)алкил)2амино, (C1-C10)ариламино, (C1-C6)алкилтио, (C1-C10)арилтио, (C1-C6)алкилсульфинил, (C6-C10)арилсульфинил, (C1-C6)алкилсульфонил, (C6-C10)арилсульфонил, (C1-C6)ацил, (C1-C6)алкокси-CO-NH-, (C1-C6)алкиламино-CO-, (C5-C9)гетероарил, (C2-C9)гетероциклоалкил или (C6-C10)арил, в которых гетероарильную, гетероциклоалкильную и арильную группы необязательно замещают 1-3 галогенами, (C1-C6)алкилами, (C1-C6)алкил-CO-NH-, (C1-C6)алкокси-CO-NH-, (C1-C6)алкил-CO-NH-(C1-C6)алкилами, (C1-C6)алкокси-CO-NH-(C1-C6)алкилами, (C1-C6)алкокси-CO-NH-(C1-C6)алкокси, карбокси, карбокси(C1-C6)алкилами, карбокси(C1-C6)алкокси, бензилоксикарбонил(C1-C6)алкокси, (C1-C6)алкоксикарбонил(C1-C6)алкокси, (C1-C10)арилами, амино, амино(C1-C6)алкилами, (C1-C6)алкоксикарбониламино, (C1-C10)арил(C1-C6)алкоксикарбониламино, (C1-C6)алкиламино, ((C1-C6)алкил)2амино, (C1-C6)алкиламино(C1-C6)алкилами, ((C1-C6)алкил)2амино(C1-C6)алкилами, гидрокси, (C1-C6)алкокси, карбокси, карбокси(C1-C6)алкилами, (C1-C6)алкоксикарбонилами, (C1-C6)алкоксикарбонил(C1-C6)алкилами, (C1-C6)алкокси-CO-NH-, (C1-C6)алкил-CO-NH-, циано, (C5-C9)гетероциклоалкилами, амино-CO-NH-, (C1-C6)алкиламино-CO-NH, ((C1-C6)алкил)2амино-CO-NH-, (C6-C10)ариламино-CO-NH-, (C1-C6)гетероариламино-CO-NH-, (C1-C6)алкиламино-CO-NH-(C1-C6)алкилами, ((C1-C6)алкил)2амино-CO-NH-(C1-C6)алкилами, (C6-C10)ариламино-CO-NH-(C1-C6)алкилами, (C5-C9)гетероариламино-CO-NH-(C1-C6)алкилами, (C1-C6)алкилсульфонилами, (C1-C6)алкилсульфониламино, (C1-C6)алкилсульфониламино(C1-C6)алкилами, (C6-C10)арилсульфонилами, (C6-C10)арилсульфониламино, (C6-C10)арилсульфониламино(C1-C6)алкилами, (C1-C6)алкилсульфониламино, (C1-C6)алкилсульфониламино(C1-C6)алкилами, (C5-C9)гетероарилами или (C2-C9)гетероциклоалкилами, или их фармацевтически приемлемыми солями.
Настоящее изобретение также относится к способу лечения глаукомы, увеита, диабетической ретинопатии и возрастной дегенерации желтого пятна, включающему введение млекопитающему композиции, содержащей фармацевтически эффективное количество Jak3 ингибитора, являющегося соединением формулы I.
Конкретные соединения формулы I включают соединения, где указанное соединение выбирают из группы, состоящей из:
метил[4-метил-1-(пропан-1-сульфонил)пиперидин-3-ил]-(7H-пирроло[2,3-d]пиримидин-4-ил)амина;
метилового эфира 4-метил-3-[метил-(7H-пирроло[2,3-d]пиримидин-4-ил)амино]пиперидин-1-карбоновой кислоты;
3,3,3-трифтор-1-{4-метил-3-[метил-(7H-пирроло[2,3-d]пиримидин-4-ил)амино]пиперидин-1-ил}пропан-1-она;
диметиламида 4-метил-3-[метил-(7H-пирроло[2,3-d]пиримидин-4-ил)амино]пиперидин-1-карбоновой кислоты;
этилового эфира ({4-Метил-3-[метил-(7H-пирроло[2,3-d]пиримидин-4-ил)амино]пиперидин-1-карбонил}амино)уксусной кислоты;
3-{4-метил-3-[метил-(7H-пирроло[2,3-d]пиримидин-4-ил)амино]пиперидин-1-ил}-3-оксопропионитрила;
3,3,3-трифтор-1-{4-метил-3-[метил-(5-метил-7H-пирроло[2,3-d]пиримидин-4-ил)амино]пиперидин-1-ил}пропан-1-она;
1-{4-метил-3-[метил-(7H-пирроло[2,3-d]пиримидин-4-ил)амино]пиперидин-1-ил}-бут-3-ин-1-она;
1-{3-[(5-хлор-7H-пирроло[2,3-d]пиримидин-4-ил)метиламино]-4-метилпиперидин-1-ил}пропан-1-она;
1-{3-[(5-фтор-7H-пирроло[2,3-d]пиримидин-4-ил)метиламино]-4-метилпиперидин-1-ил}-пропан-1-она;
N-циано-4-метил-3-[метил-(7H-пирроло[2,3-d]пиримидин-4-ил)-амино]-N'-пропилпиперидин-1-карбоксамидина и
N-циано-4,N',N'-триметил-3-[метил-(7H-пирроло[2,3-d]пиримидин-4-ил)амино]пиперидин-1-карбоксамидина.
В конкретном варианте осуществления Jak3 ингибитор представляет собой 3-{(3R,4R)-4-метил-3-[метил-(7H-пирроло[2,3-d]пиримидин-4-ил)амино]пиперидин-1-ил}-3-оксопропионитрил (CP0690550), который имеет структуру:
В одном аспекте настоящего изобретения введение Jak3 ингибитора значительно увеличивает объем секретируемой слезной жидкости по сравнению с объемом секретируемой слезной жидкости без обработки в течение двух дней. В следующем аспекте настоящего изобретения введение Jak3 ингибитора увеличивает объем секретируемой слезной жидкости, по меньшей мере, на 30% по сравнению с первоначальным объемом слезной жидкости в течение первых двух дней введения. В следующем аспекте введение Jak3 ингибитора увеличивает объем секретируемой слезной жидкости, по меньшей мере, на 50% по сравнению с первоначальным объемом слезной жидкости в течение первых двух дней введения. В следующем аспекте настоящего изобретения введение Jak3 ингибитора увеличивает объем секретируемой слезной жидкости, по меньшей мере, на 100% по сравнению с первоначальным объемом слезной жидкости в течение первых двух дней введения. В другом варианте осуществления Jak3 ингибитор увеличивает объем секретируемой слезной жидкости до уровня, сравнимого с уровнем при нормальной секреции слезной жидкости. В следующем аспекте настоящего варианта осуществления Jak3 ингибитор увеличивает объем секретируемой слезной жидкости до уровня, сравнимого с уровнем при нормальной секреции слезной жидкости в течение 8 дней первоначальной обработки.
В альтернативном варианте осуществления настоящее изобретение включает восстановление нормальной секреции слезной жидкости у млекопитающего, включающее введение млекопитающему композиции, содержащей фармацевтически приемлемый носитель и фармацевтически эффективное количество ингибитора янус-киназы-3 ("Jak3"). В одном аспекте данного варианта осуществления JAK3 ингибитор представляет собой 3-{(3R,4R)-4-метил-3-[метил-(7H-пирроло[2,3-d]пиримидин-4-ил)амино]пиперидин-1-ил}-3-оксопропионитрил (СР0690550).
В другом аспекте настоящего изобретения, Jak3 ингибитор вводят не более чем дважды в день (BID). В следующем аспекте Jak3 ингибитор вводят один раз в день (QD).
В следующем аспекте настоящего изобретения композицию вводят местно на поверхность глаз.
В другом аспекте настоящего изобретения фармацевтически эффективное количество Jak3 ингибитора составляет от 0,0001% до меньше чем 1,0 мас.%. В следующем аспекте количество Jak3 ингибитора составляет от 0,0003% до меньше чем 0,1 мас.%. В другом аспекте настоящего изобретения количество Jak3 ингибитора составляет от 0,0003 до 0,03 мас.%. В еще другом аспекте количество Jak3 ингибитора составляет от 0,003 до 0,005 мас.%. В еще другом аспекте количество Jak3 ингибитора составляет от 0,01 до 0,03 мас.%. В еще следующем варианте осуществления количество Jak3 ингибитора составляет приблизительно 0,003 мас.%, 0,005 мас.%, 0,01 мас.% или 0,03 мас.%.
В другом аспекте настоящего изобретения офтальмологическая композиция для местного применения, кроме того, содержит агент, регулирующий тоничность, и буфер. В еще следующем аспекте настоящего изобретения агент, регулирующий тоничность, представляет собой или простой сахар, или сахарный спирт. В еще другом аспекте настоящего изобретения буфер выбирают из фосфата или цитрата.
В еще другом аспекте настоящего изобретения композиция, кроме того, содержит поверхностно-активное вещество. В предпочтительном варианте осуществления настоящего изобретения поверхностно-активное вещество выбирают из TritonX114 и тилоксапола. В следующем аспекте данного варианта осуществления композиция, кроме того, содержит стабилизирующий полимер. В еще следующем аспекте настоящего изобретения стабилизирующий полимер представляет собой карбомер 974 p.
Краткое описание чертежей
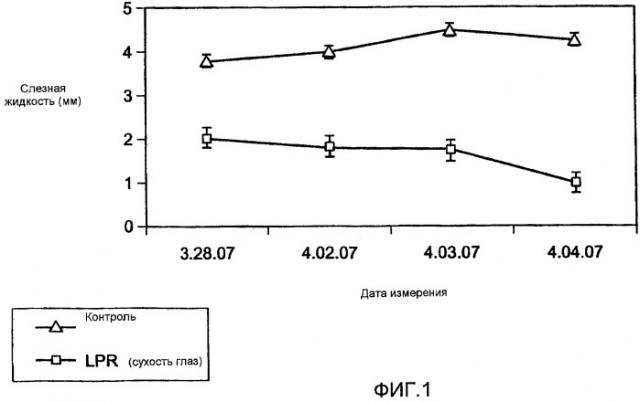
На фигуре 1 показана секреция слезной жидкости у MRL/lpr мыши ("мышь с сухостью глаз") относительно контрольной C57 мыши, как обсуждается в примере 1 ниже.
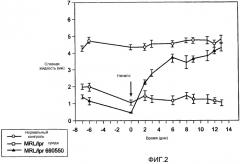
На фигуре 2 показана секреция слезной жидкости у мыши с сухостью глаз относительно C57 мыши при введении Jak3 ингибитора, 3-{(3R,4R)-4-метил-3-[метил-(7H-пирроло[2,3-d]пиримидин-4-ил)амино]пиперидин-1-ил}-3-оксопропионитрила (CP0690550).
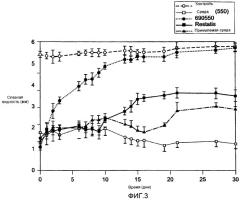
На фигуре 3 показана секреция слезной жидкости при введении Jak3 ингибитора CP0690550 по сравнению с Restasis®, являющимся лидирующим на рынке лекарственным средством для лечения сухости глаз.
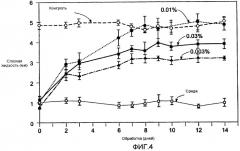
На фигуре 4 показаны дозозависимые эффекты СР690550 при концентрациях 0,003 мас.%, 0,01 мас.% и 0,03 мас.% в среде композиции 1, по сравнению с контрольными группами с нормальной секрецией слезной жидкости и с сухостью глаз.
На фигуре 5 показаны дозозависимые эффекты СР690550 при концентрациях 0,001 мас.% и 0,003 мас.% в среде композиции 3, по сравнению с контрольными группами с нормальной секрецией слезной жидкости и с сухостью глаз.
На фигуре 6 показаны дозозависимые эффекты СР690550 при концентрациях 0,001 мас.%, 0,003 мас.% и 0,01 мас.% в среде композиции 4, по сравнению с контрольными группами с нормальной секрецией слезной жидкости и с сухостью глаз.
На фигуре 7 показаны дозозависимые эффекты СР690550 при концентрациях 0,003 мас.% и 0,01 мас.% в среде композиции 3 в модели мыши с искусственно вызванной сухостью глаз, по сравнению с контрольной группой с нормальной секрецией слезной жидкости и с группой применения среды.
На фигуре 8 показаны дозозависимые эффекты СР690550 при концентрациях 0,003 мас.% и 0,005 мас.% в среде композиции 5 в модели мыши с искусственно вызванной сухостью глаз, по сравнению с контрольной группой с нормальной секрецией слезной жидкости и с группой применения среды.
Подробное описание настоящего изобретения
Согласно настоящему изобретению ингибиторы янус-киназы-3 (Jak3) вводят млекопитающему, страдающему от сухости глаз, и в частности, человеку, страдающему от сухости глаз. В одном аспекте Jak3 селективные ингибиторы настоящего изобретение обладают селективностью при ингибировании Jak3 по сравнению с другими протеинтирозинкиназами, в частности, с близкородственным членом семейства, Jak2. Причина состоит в том, что Jak2 контролирует передачу сигнала посредством рецепторов эритропоэтина (EPO), колониестимулирующего фактора макрофагов (M-CSF), колониестимулирующего фактора гранулоцитов-макрофагов (GM)-CSF и тромбопоэтина (TPO). Более того, недостаток Jak2 является летальным для зародыша в результате нарушенного эритропоэза. Можно было бы ожидать, что значительное фармакологическое ингибирование Jak2 in vivo приводило бы в результате к анемии, тромбоцитопении и лейкемии. Pesu et al., Immunological Reviews 203, 127-142 (2005). При ферментных концентрациях Jak3 ингибиторы настоящего изобретения являются, по меньшей мере, в 10 раз более эффективными относительно Jak3 по сравнению с Jak2 и являются в 3000 раз более специфичными по сравнению с другими киназами.
Настоящее изобретение относится к способу лечения сухости глаз, включающему введение млекопитающему композиции, содержащей фармацевтически приемлемый носитель и фармацевтически эффективное количество ингибитора янус-киназы-3 ("Jak3"), имеющего формулу I и/или конкретных вариантов осуществления, как описано выше. Jak3 ингибиторы описывают в патентах США №6627754 и 7091208, содержание которых вводится в настоящее изобретение с помощью ссылки. Конкретный вариант осуществления настоящего изобретения включает введение пациенту фармацевтически эффективного количества 3-{(3R,4R)-4-метил-3-[метил-(7H-пирроло[2,3-d]пиримидин-4-ил)амино]пиперидин-1-ил}-3-оксопропионитрила.
Термин "алкил", как применяют в настоящем изобретении, если не указано особо, включает насыщенные одновалентные углеводородные радикалы, содержащие прямые или разветвленные фрагменты или их комбинации.
Термин "алкокси", как применяют в настоящем изобретении, включает O-алкильные группы, в которых "алкил" определен выше.
Термин "галоген", как применяют в настоящем изобретении, если не указано особо, включает фтор, хлор, бром или йод.
Соединения настоящего изобретения могут содержать двойные связи. При наличии двойных связей соединения настоящего изобретения существуют в цис и транс конфигурациях и в виде их смесей.
Если не указано особо, алкильная и алкенильная группы, относящиеся к настоящему изобретению, также как алкильные фрагменты других групп, относящихся к настоящему изобретению (например, алкокси), могут быть линейными или разветвленными, и они могут также быть циклическими (например, циклопропил, циклобутил, циклопентил, циклогексил или циклогептил) или быть линейными или разветвленными и содержать циклические фрагменты. Если не указано особо, галоген включает фторид, хлорид, бромид и йодид.
(C2-C9)Гетероциклоалкил, при применении в настоящем изобретении, относится к пирролидинилу, тетрагидрофуранилу, дигидрофуранилу, тетрагидропиранилу, пиранилу, тиопиранилу, азиридинилу, оксиранилу, метилендиоксилу, хроменилу, изоксалидинилу, 1,3-оксазолидин-3-илу, изотиазолидинилу, 1,3-тиазолидин-3-илу, 1,2-пиразолидин-2-илу, 1,3-пиразолидин-1-илу, пиперидинилу, тиоморфолинилу, 1,2-тетрагидротиазин-2-илу, 1,3-тетрагидротиазин-3-илу, тетрагидротиадиазинилу, морфолинилу, 1,2-тетрагидродиазин-2-илу, 1,3-тетрагидродиазин-1-илу, тетрагидроазепинилу, пиперазинилу, хроманилу и т.д. Специалисту в данной области техники ясно, что связь указанных (C2-C9)гетероциклоалкильных колец осуществляется через атом углерода или гетероатом азота с sp3 гибридизацией.
(C2-C9)Гетероарил, при применении в настоящем изобретении, относится к фурилу, тиенилу, тиазолилу, пиразолилу, изотиазолилу, оксазолилу, изоксазолилу, пирролилу, триазолилу, тетразолилу, имидазолилу, 1,3,5-оксадиазолилу, 1,2,4-оксадиазолилу, 1,2,3-оксадиазолилу, 1,3,5-тиадиазолилу, 1,2,3-тиадиазолилу, 1,2,4-тиадиазолилу, пиридилу, пиримидилу, пиразинилу, пиридазинилу, 1,2,4-триазинилу, 1,2,3-триазинилу, 1,3,5-триазинилу, пиразоло[3,4-b]пиридинилу, циннолинилу, птеридинилу, пуринилу, 6,7-дигидро-5H-[1]пиридинилу, бензо[b]тиофенилу, 5,6,7,8-тетрагидрохинолин-3-илу, бензоксазолилу, бензотиазолилу, бензизотиазолилу, бензизоксазоилу, бензимидазолилу, тианафтенилу, изотианафтенилу, бензофуранилу, изобензофуранилу, изоиндолилу, индолилу, индолизинилу, индазолилу, изохинолилу, хинолил, фталазинилу, хиноксалинилу, хиназолинилу, бензоксазинилу и т.д. Специалисту в данной области техники ясно, что связь указанных (C2-C9)гетероциклоалкильных колец осуществляется через атом углерода или гетероатом азота с sp3 гибридизацией.
(C6-C10)Арил, при применении в настоящем изобретении, относится к фенилу или нафтилу.
Предпочтительные соединения формулы I включают соединения, где a равно 0; b равно 1; X представляет собой карбонил; c равно 0; d равно 0; e равно 0; f равно 0; и g равно 0.
Дополнительные предпочтительные соединения формулы I включают соединения, где a равно 0; b равно 1; X представляет собой карбонил; c равно 0; d равно 1; e равно 0; f равно 0; и g равно 0.
Дополнительные предпочтительные соединения формулы I включают соединения, где a равно 0; b равно 1 ; X представляет собой карбонил; c равно 1; d равно 0; e равно 0; f равно 0; и g равно 0.
Дополнительные предпочтительные соединения формулы I включают соединения, где a равно 0; b равно 1; X представляет -C(=N=циано)-; c равно 1; d равно 0; e равно 0; f равно 0; и g равно 0.
Дополнительные предпочтительные соединения формулы I включают соединения, где a равно 0; b равно 0; c равно 0; d равно 0; e равно 0; f равно 0; g равно 1; и Z представляет собой -C(O)-O-.
Дополнительные предпочтительные соединения формулы I включают соединения, где a равно 0; b равно 1; X представляет собой S(O)n; n равно 2; c равно 0; d равно 0; e равно 0; f равно 0; и g равно 0.
Дополнительные предпочтительные соединения формулы I включают соединения, где a равно 0; b равно 1; X представляет собой S(O)n; n равно 2; c равно 0; d равно 2; e равно 0; f равно 1; g равно 1; и Z представляет собой карбонил.
Дополнительные предпочтительные соединения формулы I включают соединения, где a равно 0; b равно 1; X представляет собой S(O)n; n равно 2; c равно 0; d равно 2; e равно 0; f равно 1; и g равно 0.
Дополнительные предпочтительные соединения формулы I включают соединения, где a равно 0; b равно 1; X представляет собой карбонил; c равно 1; d равно 0; e равно 1; Y представляет собой S(O)n; n равно 2; f равно 0; и g равно 0.
Дополнительные предпочтительные соединения формулы I включают соединения, где a равно 0; b равно 1; X представляет собой S(O)n; n равно 2; c равно 1; d равно 0; e равно 0; f равно 0; и g равно 0.
Дополнительные предпочтительные соединения формулы I включают соединения, где a равно 1; b равно 1; X представляет собой карбонил; c равно 1; d равно 0; e равно 0; f равно 0; и g равно 0.
Дополнительные предпочтительные соединения формулы I включают соединения, где a равно 0; b равно 1; X представляет собой S(O)n; c равно 0; d равно 1; e равно 1; Y представляет собой S(O)n; n равно 2; f равно 0; и g равно 0.
Дополнительные предпочтительные соединения формулы I включают соединения, где a равно 0; b равно 1; X представляет собой S(O)n; c равно 0; d равно 1; e равно 1; Y равно S(O)n; n равно 2; f равно 1; и g равно 0.
Дополнительные предпочтительные соединения формулы I включают соединения, где a равно 0; b равно 1; X представляет собой кислород; c равно 0; d равно 1; e равно 1; Y представляет собой S(O)n; n равно 2; f равно 1; и g равно 0.
Дополнительные предпочтительные соединения формулы I включают соединения, где a равно 0; b равно 1; X представляет собой кислород; c равно 0; d равно 1; e равно 1; Y представляет собой S(O)n; n равно 2; f равно 0; и g равно 0.
Дополнительные предпочтительные соединения формулы I включают соединения, где a равно 0; b равно 1; X представляет собой карбонил; c равно 1; d равно 1; e равно 1; Y представляет собой S(O)n; f равно 0; и g равно 0.
Дополнительные предпочтительные соединения формулы I включают соединения, где a равно 0; b равно 1; X представляет собой карбонил; c равно 1; d равно 1; e равно 1; Y представляет собой S(O)n; n равно 2; f равно 1; и g равно 0.
Дополнительные предпочтительные соединения формулы I включают соединения, где R12 представляет собой циано, трифторметил, (С1-C6)алкил, трифторметил(С1-C6)алкил, (С1-C6)алкиламино, ((С1-C6)алкил)2амино, (C2-C6)алкинил, циано(С1-C6)алкил, (С1-C6)алкил-S(O)m, где m равно 0, 1 или 2.
Композиции, вводимые согласно настоящему изобретению, содержат фармацевтически эффективное количество одного или более из указанных Jak3 ингибиторов. Как применяют в настоящем изобретении, "фармацевтически эффективное количество" является количеством, которое является достаточным для того, чтобы ослабить или устранить признаки симптомов сухости глаз или других расстройств, требующих увлажнения глаз. Эффективную дозу можно вводить одним или более введениями.
Как ясно из клинического контекста, введение эффективного количества лекарственного средства, соединения или фармацевтической композиции можно осуществлять отдельно или совместно с другим лекарственным средством, соединением или фармацевтической композицией. Таким образом, "эффективное количество" или "эффективную дозу" можно рассматривать в контексте введения одного или более терапевтических агентов, и отдельный агент можно рассматривать в качестве вводимого в эффективном количестве, если совместно с одним или более другими агентами можно достичь или достигается требуемый результат.
Как применяют в настоящем изобретении, "лечение" является подходом для получения лечебного или требуемого результатов, включая клинические результаты. Для целей настоящего изобретения лечебный или требуемый клинические результаты включают, но не ограничиваются, ослабление и/или устранение признаков симптомов сухости глаз или других расстройств, требующих увлажнения глаз.
Большинство практикующих врачей диагностируют и лечат синдром сухости глаз на основании одних симптомов (JAMA 2001; 286:2114-9). Ответы на анкету для диагностирования сухости глаз McMonnies & HO можно применять в качестве средства для определения симптомов сухости глаз (значение большее, чем 14,5 соответствует диагнозу о наличии сухости глаз). Тем не менее, лаборатория по сухости глаз национального института глазных болезней определяет 'симптомы дискомфорта глаз' в качестве только одного аспекта 'сухости глаз'. Анализ наблюдаемого недостатка слезной жидкости или возможности избыточного испарения слезной жидкости и повреждения подвергаемой внешнему воздействию поверхности глаз может давать подтверждение диагноза 'сухости глаз'.
Как применяют в настоящем изобретении, "значительно увеличивает секрецию слезной жидкости" обозначает статистически значимое (т.е. p<0,05) увеличение секреции слезной жидкости, как измерено стандартными офтальмологическими способами, такими как тест Ширмера или фенольный тест с применением красной нити, тест на время разрыва слезной пленки с флуоресцеином, или любой из тестов, описанный ниже.
Самыми распространенными тестами на сухость глаз являются тесты на время разрыва слезной пленки, тест Ширмера и окрашивание флуоресцеином, хотя данные тесты не являются исчерпывающими. Ниже приведены известные тесты на определение сухости глаз и предельные значения, отражающие возможность применения данных тестов для диагностирования сухости глаз:
| Таблица 1 | |
| Тест | Аномальные предельные значения для диагностирования сухости глаз |
| Тест Ширмера I | Меньше чем или равно 5 мм смачиванию в течение 5 минут |
| Фенольный тест с применением красной нити | Меньше чем 9 мм |
| Тест на время разрыва слезной пленки | Меньше чем или равно 10 секундам |
| Тест на окрашивание флуоресцеином | Больше чем 3, но меньше 15 |
| Тест на окрашивание бенгальским розовым | Больше чем 3, но меньше 18 |
| Тест на осмолярность слезной пленки | Меньше чем или равно 312 мОсм/л |
| Метод импрессионной цитологии | Больше чем 1 |
| Метод цитологии с применением специальной щеточки | Больше чем 1 |
| Тест на лактоферрин в слезной жидкости | Меньше чем 1 или равно 0,9 мкг/мл |
Тест Ширмера I
В тесте Ширмера I измеряют количество слез, которое секретировано глазом: слезы собирают в течение приблизительно 5 минут или около того, что позволяет офтальмологу определить является ли секретированное количество достаточным для поддержания глаза в здоровом состоянии или нет. Если секретировано небольшое количество слезной жидкости, можно диагностировать сухость глаз в результате недостатка слезной жидкости. Если секретировано достаточное количество слезной жидкости, но у пациента все еще сохраняются симптомы дискомфорта глаз, затем можно диагностировать сухость глаз в результате испарения.
В тес