Применение bifidobacterium longum в производстве лекарственного средства или терапевтической питательной композиции для лечения воспалительного заболевания кишечника у млекопитающего и для ослабления воспаления кишечника, связанного с пищевыми аллергенами, у млекопитающего
Иллюстрации
Показать всеИзобретение касается применения Bifidobacterium longum ATCC BAA-999 в производстве лекарственного средства или терапевтической питательной композиции для лечения воспалительного заболевания кишечника у млекопитающего и в производстве лекарственного средства или терапевтической питательной композиции для ослабления воспаления кишечника у млекопитающего. Терапевтическая питательная композиция представляет собой детскую смесь и корм для домашних животных и содержит от 104 до 1012 КОЕ/г Bifidobacterium longum ATCC BAA-999 к массе сухой основы. Изобретение обеспечивает проявление высокой противовоспалительной активности выше обозначенного пробиотического штамма бифидобактерий. 2 н. и 10 з.п. ф-лы, 5 ил., 3 табл., 4 пр.
Реферат
Это изобретение имеет отношение к способу предупреждения и лечения воспаления.
В недавнем прошлом определенные штаммы бактерий привлекли к себе большое внимание, поскольку было обнаружено, что они обладают ценными свойствами для человека, если принимать их внутрь. В частности, было найдено, что определенные штаммы родов Lactobacillus и Bifidobacterium способны адаптироваться к существованию в кишечном тракте и временно поселяться в кишечнике, снижая адгезию патогенных бактерий на эпителии кишечника, обладая иммуномодулирующим эффектом и способствуя поддержанию здоровья. Такие бактерии обычно называют пробиотиками.
Для идентификации новых пробиотических штаммов были проведены всесторонние исследования. Например, патенты ЕР 0199535, ЕР 0768375, WO 97/00078, EP 0577903 и WO 00/53200 раскрывают особые штаммы молочнокислых бактерий и бифидобактерии и их благоприятные эффекты.
Воспаление представляет собой сложную реакцию врожденной иммунной системы, которая включает накопление и активацию лейкоцитов и белка плазмы крови в местах инфекции, воздействие токсинов или повреждение клеток. Несмотря на то что воспаление служит в качестве защитной функции при контролировании инфекций и стимулирует восстановление ткани, оно также может вызывать повреждение и заболевание ткани. Желудочно-кишечные заболевания, такие как воспалительное заболевание кишечника (например, Болезнь Крона, неспецифический язвенный колит и резервуарный илеит), пищевые аллергии и атопический дерматит, возникающий в результате пищевых аллергий, всегда сопровождаются аберрантными воспалительными ответами кишечника на разных уровнях. Смягчение этого кишечного воспаления путем изменения баланса между провоспалительными и противовоспалительными цитокинами или введения регуляторных цитокинов было предложено в качестве возможного лечения для этих хронических заболеваний. Существует множество таких цитокинов, среди которых такие, например, как IFN-γ, IL1, IL8, IL12 и TNF-α, считаются провоспалительными, а такие, например, как IL10 и TGF-β, считаются противовоспалительными.
Макрофаги представляют собой расположенные в ткани фагоцитарные клетки, которые происходят из моноцитов, играющих важную роль во врожденном иммунном ответе. Они активируются микробными компонентами и, будучи проактивированными, могут сами секретировать как провоспалительные и противовоспалительные цитокины. В работе "Stimulation of the Secretion of Pro-Inflammatory Cytokines by Bifidobacterium Strains" (Microbiol. Immunol., 46 (11), 781-785, 2002) He et al исследовали способность различных штаммов бифидобактерии влиять на продукцию происходящих из макрофагов цитокинов. Они обнаружили, что «взрослый тип» бифидобактерии, такой как Bifidobacterium adolescentis и Bifidobacterium longum, индуцирует значительно большую секрецию провоспалительного цитокина, чем это делает «детский тип» бифидобактерии, такой как Bifidobacterium bifidum, Bifidobacterium breve и Bifidobacterium infantis. Дополнительно, они заметили, что, в частности, В. adolescentis не стимулирует продукцию противовоспалительного цитокина IL-10. Они заключили, что бифидобактерии взрослого типа могут быть более эффективны для усиления воспалительного ответа, но менее способны для понижающей регуляции воспалительного ответа.
Совсем недавно усилия по идентификации наиболее многообещающих пробиотических штаммов для применения у людей привели к пониманию того, что обобщения, сделанные Не и соавт., вероятно, ненадежно подтверждены, поскольку в настоящее время показано, что свойства определенного штамма - например, его противовоспалительные свойства - не могут быть точно предсказаны путем отсылки к его таксономической классификации.
Раскрытие изобретения
Авторы настоящего изобретения неожиданно обнаружили, что определенный пробиотический штамм В. longum, называемый Bifidobacterium longum АТСС ВАА-999, обладает исключительными противовоспалительными свойствами.
Следовательно, настоящее изобретение обеспечивает применение Bifidobacterium longum ATCC ВАА-999 в производстве лекарственного средства или терапевтической питательной композиции для предупреждения или ослабления воспаления у млекопитающего.
Изобретение дополнительно распространяется на способ предупреждения или ослабления воспаления у нуждающегося в этом пациента-млекопитающего, который включает введение пациенту терапевтического количества Bifidobacterium longum ATCC ВАА-999.
Настоящее изобретение может быть применено в обстоятельствах, где оно требуется для предотвращения или ослабления кишечного воспаления независимо от условий, которые могут представлять собой, например, реакцию на пищевой аллерген, хроническое или острое воспаление кишечника, вызванное заболеванием желудочно-кишечного тракта, такого как воспалительное заболевание кишечника или колит, постинфекционное воспаление или хроническое субклиническое воспаление у пожилых людей, а также в обстоятельствах, при которых требуется предотвратить воспаление в смысле профилактики, то есть там, где нет условий, которые могут привести к воспалению.
Преимущество настоящего изобретения заключается в том, что оно может быть применено для снижения или предупреждения воспаление у млекопитающего путем перорального введения терапевтической питательной композиции или лекарственного средства, содержащего в себе пробиотик. Следует понимать, что такое пероральное введение более приемлемо и удобно для пациента, чем композиция, требующая внутривенного или подкожного введения, которая требует не только специально обученного персонала, но также не настолько безопасна или удобна.
Осуществление изобретения
В настоящем описании изобретения следующим словам даны определения, которые должны быть приняты во внимание при чтении и интерпретации описания, примеров и формулы изобретения.
«Младенец»: ребенок в возрасте менее чем 12 месяцев;
«Детская смесь»: продукт питания, предназначенный для полноценного питания младенцев в течение первых четырех-шести месяцев жизни и в качестве дополнения к другим продуктам питания для возраста вплоть до 12 месяцев.
«Пробиотик»: препараты микробных клеток или компоненты микробных клеток с благоприятным влиянием на здоровье или общее состояние хозяина. (Salminen S, Ouwehand A. Benno Y. et al "Probiotics: how should they be defined" Trend Food Sci. Technol. 1999: 10 107-10).
Млекопитающее может быть человеком или животным-компаньоном, таким как собака или кошка.
Bifidobacterium longum ATCC BAA-999 («BL999») может быть введен сам по себе, например, будучи заключен в капсулы, каждая из которых содержит, например, 108 колониеобразующих единиц (КОЕ), или включен в питательную композицию, такую как полная питательная формула (например, детская смесь или диетический питательный продукт), молочный продукт, порошок для получения напитков, сухой суповой концентрат, диетическую добавку, заменитель пищи, питательный батончик, сухой завтрак, кондитерское изделие или сухой корм для домашних животных. Если BL999 включен в пищевую композицию, то он может присутствовать в композиции в количестве, равном от 104 до 1012 КОЕ/г (сухой вес). Эти выражения количества учитывают вероятность того, что бактерии живы, инактивированы или мертвы или даже присутствуют в виде таких фрагментов, как ДНК, или материалы клеточной стенки или как метаболиты. Другими словами, количества бактерий выражают в терминах колониеформирующей способности такого количества бактерий, как если все бактерии были живы независимо от того, живы они или нет, фактически, живые, инактивированные или мертвые, фрагментированные или смесь любых или всех этих состояний. Предпочтительно, BL999 присутствуют в количестве, равном от 105 до 1010, более предпочтительно от 107 до 1010 КОЕ/г сухой композиции.
BL999 может быть получен из Morinaga Milk Industry Co. Ltd. of Japan под торговой маркой ВВ536. Он может быть культивирован в соответствии с любым подходящим способом и подготовлен для включения в капсулу или для добавления к питательной композиции, например, путем сушки замораживанием или сушки распылением. Альтернативно, он может быть приобретен уже в подходящей форме, подготовленной для добавления к продуктам питания.
Полная питательная смесь для применения в настоящем изобретении может включать источник белка, предпочтительно, пищевой белок, такой как животный белок (например, белок молока, мяса или яйца), растительный белок (например, белок соевых бобов, пшеницы, риса или гороха); смеси свободных аминокислот; или их комбинации. Белки молока, такие как казеин, и белки сыворотки, и белки соевых бобов особенно предпочтительны. Композиция может также содержать источник углеводов и источник жиров.
Если композиция включает источник жиров, то она предпочтительно обеспечивает от 5% до 55% энергии композиции; например, от 20% до 50% энергии. Липиды, образующие источник жиров, могут быть любым подходящим жиром или смесью жиров. Особенно подходят растительные жиры, такие как соевое масло, пальмовое масло, кокосовое масло, сафлоровое масло, подсолнечное масло, кукурузное масло, масло канолы и лецитины. Животные жиры, такие как жир молока, могут быть также добавлены, если требуется.
Если композиция включает источник углеводов, то он предпочтительно обеспечивает от 40% до 80% энергии композиции. Может быть применен любой подходящий углевод, например сахароза, лактоза, глюкоза, фруктоза, сухая кукурузная патока, мальтодекстрины и их смеси. Может быть также добавлено диетическое волокно, если требуется. Диетическое волокно может быть из любого подходящего источника, включая, например, соевые бобы, горох, овес, пектин, гуаровую камедь, гуммиарабик, фруктоолигосахариды, галактоолигосахариды, сиалил-лактозу и олигосахариды, полученные из молока животных.
Подходящие витамины и минералы могут быть включены в питательную композицию в количестве, удовлетворяющем соответствующим методическим рекомендациям.
Если требуется, то в питательную композицию могут быть включены один или несколько пригодных для употребления в пищу эмульгаторов; например, моно- и диглицериновые эфиры диацетилвинной кислоты, лецитин и моно- и диглицериды. Подобным образом могут быть включены подходящие соли и стабилизаторы.
Полная питательная композиция может быть получена любым подходящим способом. Например, источник белка, источник углевода и источник жира могут быть перемешаны в подходящих соотношениях. Если применяют эмульгатор, то он может быть включен в смесь. Витамины и минералы могут быть добавлены на этом этапе, обычно их добавляют позднее для того, чтобы избежать тепловой деградации. Любые липофильные витамины, эмульгаторы и им подобные могут быть растворены в источнике жира перед смешиванием. Затем для образования жидкой смеси могла быть примешена вода, предпочтительно вода, которая подвергалась обратному осмосу.
Затем жидкая смесь могла быть подвергнута термообработке для снижения бактериальных нагрузок. Например, жидкая смесь могла быть быстро нагрета до температуры в диапазоне от примерно 80°С до примерно 110°С в течение от примерно 5 секунд до примерно 5 минут. Эту операцию можно проводить с помощью инжекции пара или с помощью теплообменника; например, пластинчатого теплообменника.
Затем жидкая смесь может быть охлаждена до температуры в диапазоне от примерно 60°С до примерно 85°С; например, с помощью мгновенного охлаждения. Затем жидкая смесь может быть гомогенизирована; например, в две стадии, от примерно 10 МРа до примерно 30 МРа на первой стадии и от примерно 2 МРа до примерно 10 МРа на второй стадии. Затем гомогенизированная смесь может быть дополнительно охлаждена, для того чтобы можно было добавить любые чувствительные к нагреванию компоненты; такие как витамины и минералы. pH и содержание сухих веществ гомогенизированной смеси удобно стандартизировать на этом этапе.
Затем гомогенизированная смесь может быть перенесена в подходящее устройство для сушки, такое как распылительная сушка или сублимационная сушка, и превращена в порошок. Порошок должен содержать влагу в количестве менее чем примерно 5% по массе. BL999 может быть добавлен к порошку в требуемом количестве путем сухого смешивания.
Сухой корм для домашних животных для применения в настоящем изобретении может включать любой источник углевода, один или несколько, источник белка и источник липидов.
Может быть применен любой подходящий источник углевода. Предпочтительно источник углевода обеспечивают в виде круп, муки или крахмалов. Например, источник углевода может представлять собой рисовую, ячменную, сорговую, просяную, овсяную, кукурузную муку грубого помола или пшеничную муку. Могут быть также применены простые сахара, такие как сахароза, глюкоза и кукурузные сиропы. Количество углевода, обеспечиваемое источником углевода, может быть выбрано по желанию. Например, корм для домашних животных может содержать вплоть до примерно 60% по массе углевода.
Подходящие источники белка могут быть выбраны из любого подходящего источника белка животного или растительного происхождения; например мышечное или скелетное мясо, мясная и костная мука, мука из домашней птицы, рыбная мука, молочные белки, кукурузная клейковина, пшеничная клейковина, мука из соевых бобов, концентраты соевых белков, вещества, выделенные из соевых белков, белки яиц, сыворотка, казеин, глютен и им подобные. Для пожилых животных предпочтителен источник белка, содержащий высококачественный животный белок. Количество белка, обеспечиваемое источником белка, может быть выбрано по желанию. Например, корм для домашних животных может содержать от примерно 12% до примерно 70% по массе белка к сухой основе.
Корм для домашних животных может содержать источник жира. Может быть применен любой подходящий источник жира. Предпочтительно источник жира представляет собой животный источник жира, такой как твердый жир (сало). Могут быть также применены растительные масла, такие как кукурузное масло, подсолнечное масло, сафлоровое масло, рапсовое масло, соевое масло, оливковое масло и другие масла, богатые мононенасыщенными и полиненасыщенными жирными кислотами. В дополнении к основным жирным кислотам (линолевой и альфа-линолевой кислоте) источник жира может включать длинноцепочечные жирные кислоты. Подходящие длинноцепочечные жирные кислоты включают гамма-линолевую кислоту, стеаридоновую кислоту, арахидоновую кислоту, эйкозапентаеновую кислоту и докозагексаеновую кислоту. Рыбьи жиры представляют собой подходящий источник эйкозапентаеновой кислоты и докозагексаеновой кислоты. Масло бурачника, масло семян черной смородины и масло энотеры представляют собой подходящие источники гамма-линолевой кислоты. Рапсовое масло, соевое масло, льняное масло и масло грецкого ореха представляют собой подходящие источники альфа-линоленовой кислоты. Сафлоровые масла, подсолнечные масла, кукурузные масла и соевые масла представляют собой подходящие источники линолевой кислоты. Оливковое масло, рапсовое масло (канола), подсолнечное масло с высоким содержанием олеиновой кислоты, сафлоровое масло, арахисовое масло и масло из рисовых отрубей представляют собой подходящие источники мононенасыщенных жирных кислот. Количество жиров, обеспечиваемое источником жира, может быть выбрано по желанию. Например, корм для домашних животных может содержать от примерно 5% до примерно 40% по массе жиров к сухой основе. Предпочтительно, корм для домашних животных имеет сравнительно сниженное количество жиров.
Выбор углевода, белка и источника липидов не важен, и они могут быть выбраны на основе питательных потребностей животного, вкусовых предпочтений и типа получаемого изделия. Дополнительно разнообразные иные ингредиенты, например сахар, соль, специи, приправы, витамины, минералы, вкусоароматические добавки, камеди и пробиотические микроорганизмы, по желанию также могут быть включены в корм для домашних животных.
Для пожилых домашних животных корм для домашних животных предпочтительно содержит пропорционально меньше жира, чем корма для домашних животных, предназначенные для молодых домашних животных. Дополнительно, источники крахмала могут включать один или несколько из таких источников, как ячмень, рис, ячмень, пшеница и кукуруза.
Корм для домашних животных может быть получен с помощью варочной экструзии, также может быть применена выпечка и другие подходящие способы. При применении варочной экструзии корм для домашних животных обычно получают в виде гранулированного корма. BL999 предпочтительно наносят на поверхность или закладывают внутрь сухого корма для домашних животных. Подходящий способ описан в патентной заявке European Patent Application No 0862863.
Теперь изобретение будет дополнительно описано путем отсылок к следующим примерам.
Описание фигур
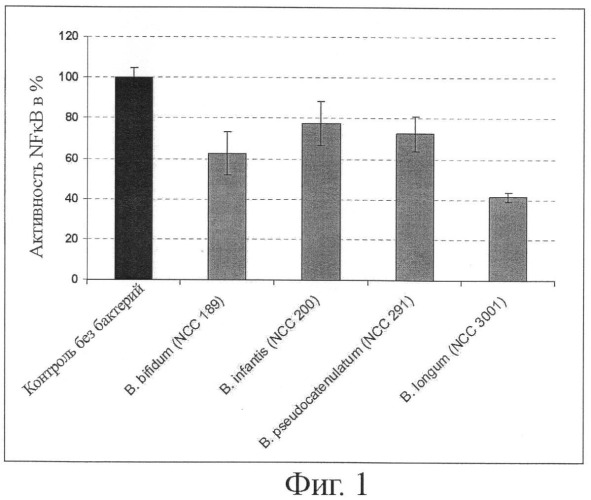
На фигуре 1 приведено сравнение активности NFκB в процентах после стимуляции клеток кишечника in vitro с помощью LPS в присутствии четырех различных бифидобактерий (клеточные, основанные на гене-репортере NFκB исследования);
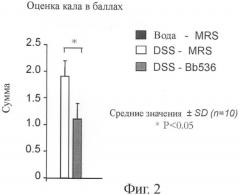
На фигуре 2 приведено сравнение оценок кала в баллах, наблюдаемых в модели колита у мышей, имитирующей патологии IBD (DSS-индуцированный колит) с включением и без включения BL999;
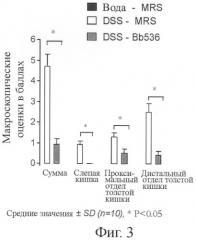
На фигуре 3 приведено сравнение показателей макроскопического воспаления, полученных для модели колита у мышей, имитирующей патологии IBD (DSS-индуцированный колит) с включением и без включения BL999;
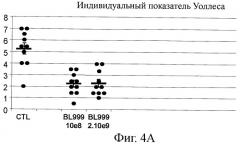
На фигурах от 4А до Е приведено сравнение индивидуальных показателей Уоллеса (А), среднее значение показателей Уоллеса (В), процент защиты (С), миелопероксидазная активность (D) и двухдневная потеря веса (Е), полученные в модели TNBS-индуцированного колита, в которой двум группам вводили BL999 в различных дозах и контрольная группа не получала бактерий; и
На фигуре 5 приведено сравнение защитной способности BL999 в той же модели колита у мышей по сравнению с защитной способностью В. longum NCC2705, L.rhamnosus АТСС 53103, L.johnsonii CNCM I-1225, L.plantarum NCIMB8826, L.lactis NZ9000 и MG1363; и с защитным эффектом лекарственного средства преднизолона.
Примеры
Пример 1
Ниже приведен пример композиции детской смеси для применения в настоящем изобретении. Эта композиция приведена только с целью иллюстрации.
| Нутриент | на 100 ккал | на литр |
| Энергия (ккал) | 100 | 670 |
| Белок (г) | 1,83 | 12,3 |
| Жир (г) | 5,3 | 35,7 |
| Линолевая кислота (г) | 0,79 | 5,3 |
| α-Линоленовая кислота (мг) | 101 | 675 |
| Лактоза (г) | 11,2 | 74,7 |
| Минералы (г) | 0,37 | 2,5 |
| Na (мг) | 23 | 150 |
| К (мг) | 89 | 590 |
| Cl (мг) | 64 | 430 |
| Са (мг) | 62 | 410 |
| Р (мг) | 31 | 210 |
| Mg (мг) | 7 | 50 |
| Mn (мкг) | 8 | 50 |
| Se (мкг) | 2 | 13 |
| Витамин А (мкг RE) | 105 | 700 |
| Витамин D (мкг) | 1,5 | 10 |
| Витамин Е (мг ТЕ) | 0,8 | 5,4 |
| Витамин К1 (мкг) | 8 | 54 |
| Витамин С (мг) | 10 | 67 |
| Витамин В1 (мг) | 0,07 | 0,47 |
| Витамин В2 (мг) | 0,15 | 1,0 |
| Ниацин (мг) | 1 | 6,7 |
| Витамин В6 (мг) | 0,075 | 0,50 |
| Фолевая кислота (мкг) | 9 | 60 |
| Пантотеновая кислота (мг) | 0,45 | 3 |
| Витамин В12 (мкг) | 0,3 | 2 |
| Биотин (мкг) | 2,2 | 15 |
| Холин (мг) | 10 | 67 |
| Fe (мг) | 1,2 | 8 |
| I (мкг) | 15 | 100 |
| Cu (мг) | 0,06 | 0,4 |
| Zn (мг) | 0,75 | 5 |
| В.longum BB 536 | 108 КОЕ/г порошка, живые бактерии |
Пример 2
В этом примере приведено сравнение ингибирующей активности BL999 с ингибирующими эффектами других пробиотических бактериальных штаммов в клеточных исследованиях с геном-репортером ядерного фактора каппа В (NFκB).
Было опубликовано множество работ, касающихся центральной роли, которую играет транскрипционный фактор NFκВ в индукции и сохранении хода событий при воспалении. NFκB активируется в ответ на энтероинвазивные патогенные бактерии и другие воспалительные стимулы, приводящие к продукции воспалительных молекул, таких как фактор-α некроза опухоли (TNF-α), интерлейкин-8 (IL-8), молекула межклеточной адгезии типа 1 (ICAM-1) и индуцируемая циклооксигеназа (СОХ-2).
В этом исследовании применяют линию эпителиальных человеческих кишечных клеток (НТ29 NFκB), стабильно экспрессирующих конструкцию гена-репортера (секретируемая щелочная фосфатаза) под контролем эндогенного промотора NFκB (Blum S и соавт.; Riedel С.и соавт.. World J Gastroenterol. 2006, в печати). Измеряют способность четырех штаммов бифидобактерий ингибировать индуцированную липополисахаридом (LPS) активность NFκB в этих клетках. Клетки инкубируют со свежеприготовленными В.bifidum (NCC 189, CNCM I-2333), В.infantis (NCC 200, CNCM 1-2334), В.pseudocatenulatum (NCC 291) и В.longum (NCC 3001, ATCC BAA-999) в соотношении клетка к бактериям 1:100. После преинкубации клеток с бактериями в течение 1 часа добавляют LPS в концентрации 10 нг/мл и инкубируют дополнительно 4 часа, отработавшие культуральные супернатанты собирают для измерения NFκB-опосредуемой активности репортера. Измерения проводят в двойном повторе и повторяют, по меньшей мере, 3 раза при каждом повторении, нормализуя на стимуляцию LPS без бактерий бактерии, контроль без бактерий. Данные приведены на фигуре 1 как средний процент LPS-стимулированной активности NFκB ± SEM.
Можно видеть, что клетки, обработанные LPS, имеют 10-кратную индукцию в активности NFκB после 4-часовой инкубации. Все четыре штамма бифидобактерий снижали активность NFκB, однако BL999 обладал наивысшей ингибирующей активностью в этом исследовании. В заключении BL999 представляет собой отличный штамм-кандидат для применения там, где очень важно ингибировать воспалительную активность.
Пример 3
Этот пример демонстрирует способность BL999 и его метаболитов предупреждать воспаление в модели IBD на мышах.
В этом эксперименте применяли модель индуцированного натриевой солью декстран-сульфата (DSS) колита у мышей, признанной в качестве подходящей модели для патологий IBD (Blumberg RS и соавт., Current Opin. Immunol. 1999; 11(6): 648-56). Введение DSS индуцировало гистопатологическое нарушения в толстой кишке, аналогичные тем, что наблюдают у пациентов с неспецифическим язвенным колитом. Обработка DSS была проведена для того, чтобы индуцировать острое кишечного воспаление.
Экспериментальные группы и диеты:
- «Контроль-MRS»: мыши получали контрольную диету (Таблица 1) ad libitum, со свободным доступом к водопроводной воде в течение всего эксперимента, и ежедневно получали MRS путем внутрижелудочного кормления через зонд от дня 1 до дня 14
- «DSS-MRS»: мыши получали контрольную диету ad libitum в течение всего эксперимента, со свободным доступом к водопроводной воде, содержавшей 1%-ный DSS от дня 7 до дня 14, и ежедневно получали MRS путем внутрижелудочного кормления через зонд от дня 1 до дня 14
- «DSS-BL»: мыши получали контрольную диету в течение всего эксперимента, от дня 1 до дня 14, со свободным доступом к водопроводной воде, содержавшей 1% DSS от дня 7 до дня 14, и ежедневно получали BL999 (NCC3001) (109 cfu/мышь/день) путем внутрижелудочного кормления через зонд от дня 1 до дня 14
| Таблица 1 | |
| Контрольная диета | |
| Компоненты | Процент от всей диеты (% по массе) |
| Резистентный крахмал (Cerestar SF 12018) | 40,0 |
| Растворимый казеин | 20,0 |
| Сахароза | 27,3 |
| DL-метионин | 0,3 |
| Кукурузное масло | 5,0 |
| Целлюлоза | 2,0 |
| Минеральный премикс AIN 93 | 4,4 |
| Витаминный премикс AIN 93 | 1,0 |
Эксперимент с животными проводили, как описано ниже. Самцов мышей BALBc/J (8-недельные, Janvier, France) случайным образом распределяли по 4-м экспериментальным группам (n=10 мышей на группу). В течение 7-дневного периода акклиматизации мыши имели свободный доступ к водопроводной воде и получали контрольную диету. Затем мыши в группе DSS-BL ежедневно получали BL999 (109 КОЕ/мышь/день) с культуральным супернатантом путем внутрижелудочного кормления с помощью зонда в течение 14 дней, в то же время мыши в других двух группах ежедневно получали MRS путем внутрижелудочного кормления с помощью зонда. Дополнительно от дня 7 до дня 14 мыши в обеих группах, DSS-MRS и DSS-BL, получали 1%-ный DSS со своей питьевой водой, тогда как контрольная группа получала нормальную водопроводную воду.
Каждые 2 дня в течение этого эксперимента исследовали образцы кала, отобранные у каждой мыши, и регистрировали консистенцию и присутствие или отсутствие крови (Hemoccult II, SKD, Roissy, France). Рассчитывали оценку кала в баллах, как показано в таблице 2, и результаты приведены на фигуре 2.
| Таблица 2 | |
| Шкала для расчета клинических симптомов у мыши | |
| Величина баллов | Наблюдения |
| Оценка стула в баллах | |
| 0 | Нормальный, твердый |
| 1 | Мягкий, хорошо сформированный, вязкий |
| 2 | Не сформированный |
| 3 | Жидкий, диарея |
По окончанию 14-дневного периода мышей забивали путем смещения шейного отдела позвоночника. Сегменты слепой и толстой кишки быстро извлекали из животного, мягко промывали физиологическим солевым буфером и подсчитывали баллы для макроскопических воспалительных признаков с последующим переводом по шкале, ранее опубликованной Appleyard и Wallace (Appleyard C.B and Wallace J.L. "Reactivation of hapten-induced colitis and its prevention by anti-inflammatory drugs" Am J. Physiol 269, G119-125) (Таблица 3). Результаты приведены на фигуре 3.
| Таблица 3 | ||
| Критерии для подсчета макроскопических повреждений слепой и толстой кишки (Appleyard и Wallace) | ||
| Балл | Проявление | |
| Уплотнение | ||
| 0 | Нормальная слизистая оболочка | |
| 1 | Умеренное уплотнение | |
| 2 | Сильное уплотнение | |
| Изъязвление | ||
| 0 | Нет | |
| 1 | Покраснение | |
| 2 | Легкое изъязвление | |
| 3 | Сильное изъязвление | |
| Содержимое слепой | ||
| и толстой кишок | ||
| 0 | Нет крови | |
| 1 | Следы крови | |
| 2 | Сильное выделение крови |
Из фигур 2 и 3 можно видеть, что BL999 эффективно нормализует характеристики стула и значительно снижает воспаление в слепой кишке и в проксимальном и дистальном отделах толстой кишки по сравнению с теми же характеристиками, наблюдаемыми в группе DSS-MRS. Таким образом, можно видеть, что BL999 представляет собой эффективное средство для предупреждения DSS-индуцированного воспаления, так как мыши в группе DSS-BL получали бактерии как перед началом, так и в течение периода введения DSS.
Пример 4
В этом примере на модели острого колита мышей, индуцированного TNBS, было проведено исследование противовоспалительного потенциала бактерий BL999 и было проведено сравнение с другими штаммами молочнокислых бактерий, а также с преднизолоном, обычно применяемым противовоспалительным лекарственным средством.
Исследовали следующие бактериальные штаммы:
| NCC No | Штамм | Официальный номер в банке данных |
| NCC 3001 | Bifidobacterium longum | АТСС ВАА-999 |
| NCC 2705 | Bifidobacterium longum | CNCM I-2618 |
| NCC 3003 | Lactobacillus rhamnosus | АТСС 53103 |
| NCC 533 | Lactobacillus johnsonii | CNCM I-1225 |
| Lactobacillus plantarum | NCIMB8826 | |
| Lactococcus lactis | NZ9000 | |
| Lactococcus lactis | MG1363 |
Штаммы молочнокислых бактерий растили аэробно при 37°С в среде MRS (Difco). Бифидобактерии растили анаэробно при 37°С в MRS, дополненной 0,05% L-цистеин гидрохлоридом (Sigma). Lactococcus lactis MG1363 и Lactococcus lactis NZ9000 растили при 30°С в среде M17, дополненной 0,5% глюкозой. Число бактерий (КОЕ) подсчитывали на стационарной фазе роста, измеряя поглощение при 600 нм (A600), с помощью соответствующей калибровочной кривой для каждого штамма. Для рутинных экспериментов in vivo бактерии растили в течение 18 часов, дважды промывали в стерильном PBS pH 7,2 и ресуспендировали в концентрации 108 и 2·109 КОЕ/мл в 0,2 М NaHCO3-буфере, содержавшем 2% глюкозы.
Взрослые самки мышей BALB/C в возрасте от 7 до 8 недель были приобретены в Charles River. Мыши были случайным образом разделены на экспериментальные группы по 10 мышей на группу. Мыши жили группами (от 8 до 10 на клетку) и имели свободный доступ к воде и стандартный корм для грызунов. Они проходили, по меньшей мере, 1-недельную акклиматизацию перед каким-либо вмешательством. Мыши в группах, обработанных бактериями, получали с помощью внутрижелудочного кормления через зонд бактериальные суспензии (в количестве 108 КОЕ/мышь/день) в 0,2 М NaHCO3-буфере при pH 8,5 с 2% глюкозы с четвертого дня перед индукцией колита до дня, когда колит был индуцирован. Мыши в группе, обработанной преднизолоном, получали преднизолоном в количестве 10 мг/кг массы тела/день. Мыши в контрольной группе не получали ни бактерий, ни преднизолона. Дополнительно, исследовали влияние величины дозы, вводя одной группе BL999 в количестве 2·109 КОЕ/мышь/день.
Перед индукцией колита, все мыши были анестезированы с помощью внутрибрюшинной инъекции 3 мг кетамина (Imalgene 1000, Merial, Lyon, France), 46,7 мкг диазепама (Valium, Roche Diagnostics, France) и 15 мкг атропина (Aguettant Laboratory, Lyon, France), растворенных в 0,9%-ном хлориде натрия. Затем индуцировали колит путем ректального введения 50 мкл тринитробензолсульфоновой кислоты (TNBS, Fluka, France), растворенной в 0,9% NaCl/этанол (50/50 объем/объем) в дозе 100-120 мг/кг массы тела. Коэффициент смертности и показатели воспаления определяли через 48 часов после введения TNBS. Мышей взвешивали перед введением TNBS и при забое, который проводили с помощью смещения шейных позвонков.
Толстую кишку извлекали, освобождали от жиров и брыжейки, осторожно открывали и очищали с помощью PBS. Повреждение и воспаление толстой кишки оценивали по критериям Уоллеса (Wallace J.L. et al. Inhibition of leukotriene synthesis markedly accelerates healing in a rat model of inflammatory bowel disease" Gastroenterology 96: 29-36, 1989). Эти критерии для макроскопического подсчета баллов хорошо разработаны для исследований на мышах и отражают интенсивность воспаления, уплотнение слизистой оболочки толстой кишки и степень изъязвления. Повреждение и воспаление толстой кишки были оценены в баллах двумя независимыми экспериментаторами.
Дополнительно определяли активность миелопероксидазы (МРО), маркера первичных гранул полиморфоноядерных нейтрофилов по модифицированному методу Bradley и соавт.(«Measurement of cutaneous inflammation: estimation of neutrophil content with an enzyme marker» J Invest Dermatol. 60(3):618-22). Концентрацию белка определяли по методу Лоури, и активность МРО выражали как единицы U МРО/см кишки.
Активность МРО определяли в ткани проксимального отдела толстой кишки сразу после забоя. Образец толстой кишки (длиной в 1 см) брали на расстоянии 3-х см от места соединения слепой и толстой кишки, суспендировали в калий-фосфатном буфере (50 ммоль/л, pH 6,0) и гомогенизировали на льду с помощью политрона. Проводили три цикла замораживания и оттаивания, суспензии центрифугировали при 10000 g в течение 15 мин при 4°С. Супернатанты отбрасывали, а осадки ресуспендировали в буфере с детергентом гексадецилтриметиламмоний бромидом (НТАВ 0,5%, масса/объем, в 50 ммоль/л калий-фосфатном буфере, pH 6,0), индуцируя выход МРО из первичных гранул полиморфноядерных нейтрофилов. Полученные суспензии подвергали ультразвуковой обработке на льду и снова центрифугировали в течение 15 мин при 4°С. Супернатанты разводили в калий-фосфатном буфере (pH 6,0), содержавшем 0,167 мг/мл 0-дианизидин дигидрохлорида и 0,0005% перекиси водорода (Н2О2). МРО нейтрофилов человека (0,1 Ед./100 мл, Sigma) применяли в качестве стандарта. Регистрировали изменения в поглощении при 450 нм, через 5 и 10 мин с помощью спектрофотометра для микропланшетов (ELX808, Bio-Tek Instrument, CA). Одна единица активности МРО была определена как количество МРО, необходимое для разрушения 1 ммоля перекиси водорода/мин/мл при 25°С.
Результаты анализировали с помощью непараметрического однонаправленного анализа, U-теста Манна-Уитни. Разницы признавались статистически значимыми в случае, когда p-значение <0,05.
Результаты приведены на фигурах от 4, А до Е и на фигуре 5. На фигурах 4А и В приведено сравнение индивидуальных критериев Уоллеса и среднего значения критерия Уоллеса для мыши, обработанной BL999, взятыми в двух дозах, 108 КОЕ/мышь/день и 2-10 КОЕ/мышь/день, с контрольной группой, не получавшей бактерий. Можно видеть, что мыши из обеих групп, получавших BL999, имеют существенно сниженные показатели Уоллеса по сравнению с мышами контрольной группы.
Фигура 4С показывает защиту, обеспечиваемую BL999, в процентах. Это соответствует снижению среднего значения макроскопического воспаления у обработанных бактериями мышей (n=10) по сравнению со средней оценкой в баллах контрольных мышей, обработанных TNBS (мыши, обработанные буфером NaOHCO3, n=10).
На фигуре 4D приведено сравнение среднего значения активности МРО мышей, обработанных BL999, взятыми в двух дозах, с контрольной группой. Можно видеть, что мыши из обеих группы, получавшие BL999, имеют существенно сниженную активность МРО по сравнению с мышами контрольной группы.
На фигуре 4Е приведено сравнение 2-х дневной потери веса у мышей, обработанных BL999, взятыми в двух дозах, с контрольной группой. Можно видеть, что мыши из обеих группы, получавшие BL999, имеют существенно сниженные показатели потери веса, по сравнению с мышами контрольной группы.
На фигуре 5 приведено сравнение в процентах защиты, обеспечиваемой различными протестированными штаммами молочнокислых бактерий и обеспечиваемой в результате введения преднизолона. Можно видеть, что BL999 обеспечивает заметно более высокую степень защиты, чем другие протестированные бактериальные штаммы и сравнимый с лекарственным средством уровень защиты.
1. Применение Bifidobacterium longum ATCC BAA-999 в производстве лекарственного средства или терапевтической питательной композиции для лечения воспалительного заболевания кишечника у млекопитающего.
2. Применение по п.1, где терапевтическая питательная композиция представляет собой детскую смесь.
3. Применение по п.1, где терапевтическая питательная композиция представляет собой корм для домашних животных.
4. Применение по любому из пп.1-3, где терапевтическая питательная композиция содержит от 104 до 1012 КОЕ/г Bifidobacterium longum ATCC ВАА-999 к массе сухой основы.
5. Применение по п.4, в котором терапевтическая питательная композиция содержит от 105 до 1010 КОЕ/г Bifidobacterium longum ATCC ВАА-999 к массе сухой основы.
6. Применение по п.5, в котором терапевтическая питательная композиция содержит от 107 до 1010 КОЕ/г Bifidobacterium longum ATCC ВАА-999 к массе сухой основы.
7. Применение Bifidobacterium longum ATCC ВАА-999 в производстве лекарственного средства или терапевтической питательной композиции для ослабления воспаления кишечника, связанного с пищевыми аллергенами, у млекопитающего.
8. Применение по п.7, где терапевтическая питательная композиция представляет собой детскую смесь.
9. Применение по п.7, где терапевтическая питательная композиция представляет собой корм для домашних животных.
10. Применение по любому из пп.7-9, где терапевтическая питательная композиция содержит от 104 до 1012 КОЕ/г Bifidobacterium longum АТСС ВАА-999 к массе сухой основы.
11. Применение по п.10, в котором терапевтическая питательная композиция содержит от 105 до 1010 КОЕ/г Bifidobacterium longum ATCC ВАА-999 к массе сухой основы.
12. Применение по п.11, в котором терапевтическая питательная композиция содержит от 107 до 1010 КОЕ/г Bifidobacterium longum ATCC ВАА-999 к массе сухой основы.