Способ получения n-фенил(бензил)-1,5,3-дитиазепинан-3-аминов и 2,4-диметил-n-фенил(бензил)-1,5,3-дитиазепинан-3-аминов
Иллюстрации
Показать всеИзобретение относится к способу получения N-фенил(бензил)-1,5,3-дитиазепинан-3-аминов и 2,4-диметил-N-фенил(бензил)-1,5,3-дитиазепинан-3-аминов общей формулы (I):
R=Ph, Bz; R'=H, Me, который заключается в предварительном перемешивании формальдегида или ацетальдегида с 1,2-этандитиолом с последующим добавлением фенилгидразина (бензилгидразина) при мольном соотношении исходных реагентов альдегид: 1,2-этандитиол: фенилгидразин (бензилгидразин) = 20:10:10 и перемешиванием при температуре 0°C и атмосферном давлении в течение 2-4 ч. Технический результат - разработан способ получения новых соединений, которые могут найти применение в качестве антибактериальных, антигрибковых и антивирусных агентов, в качестве биологически активных комплексообразователей, селективных сорбентов и экстрагентов драгоценных металлов, специальных реагентов для подавления жизнедеятельности бактерий в различных технических средах. 1 табл., 1 пр.
Реферат
Предлагаемое изобретение относится к области органической химии, в частности к способу получения N-фенил(бензил)-1,5,3-дитиазепинан-3-аминов и 2,4-диметил-N-фенил(бензил)-1,5,3-дитиазепинан-3-аминов общей формулы (1) на основе фенил(бензил)гидразина, альдегидов R'CHO (R'=H, Me) и 1,2-этандитиола:
R=Ph, Bz; R'=H, Me
Азот и серусодержащие гетероциклы известны как антибактериальные, антигрибковые и антивирусные агенты (Stillings M.R., Welbourn A.P., Walter D.J. Substituted 1,3,4-thiadiazoles with anticonvulsant activity // Med. Chem. 1986. 29. P.2280-2284. Kidwai M., Negi N., Chaudhary S.R. Cyclothiomethylation of arge hydrazines with formaldehyde // Acta Pharma. 1995. 45. P.511. Тюкавкина H.A., Зурабян С.Э., Белобородов В.Л. и др. Органическая химия. M.: Дрофа, 2008. с.66-67). Они перспективны в качестве катализаторов, биологически активных комплексообразователей, селективных сорбентов и экстрагентов драгоценных металлов [Deutsche Gold- und Silber-Scheideanstalt vormals Roessler. F.P. 1,341,792/1963 (Chem. Abs., 1964, 60, 5528d)], специальных реагентов для подавления жизнедеятельности бактерий в различных технических средах (от легкой промышленности до нефти) (Джемилев У.М., Алеев Р.С., Дальнова Ю.С., Кунакова Р.В., Хафизова С.Р., Ковтуненко С.В., Калимуллин А.А., Андрианов В.М., Исмагилов Ф.Р., Гафиатуллин P.P. Средство для подавления роста сульфатвосстанавливающих бактерий. Патент РФ №2160233, 2000; Джемилев У.М., Алеев Р.С., Дальнова Ю.С., Кунакова Р.В., Хафизова С.Р. Средство для подавления роста сульфатвосстанавливающих бактерий. Патент РФ №2206726, 2003).
Известен способ (В.Р.Ахметова, Г.Р.Надыргулова, С.Р.Хафизова и др. Журнал органической химии, 2006, 1, с.151) получения 3-фенил-1,3,4-тиадиазолидина формулы (3) взаимодействием солянокислого фенилгидразина с CH2O и H3S в соотношении 1:3:2 (pH 0.45-0.5) при 0°C с выходом 35% по схеме:
Известным способом не могут быть получены N-фенил(бензил)-1,5,3-дитиазепинан-3-амины и 2,4-диметил-N-фенил(бензил)-1,5,3-дитиазепинан-3-амины общей формулы (1).
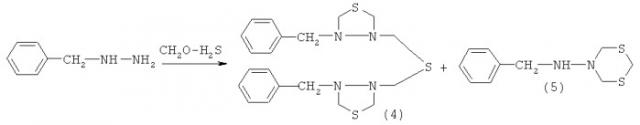
Известен способ (В.Р.Ахметова, Г.Р.Надыргулова, С.Р.Хафизова и др. Журнал органической химии, 2006, 1, с.151) совместного получения производных 1,3,4-тиадиазолидинового (4) и 1,3,5-дитиазинанового (5) ряда циклотиометилированием бензилгидразина с помощью CH2O и H2S в нейтральной среде (соотношение исходных реагентов соответственно 1:3:2, температура ~20°C).
Известный способ не позволяет получать N-фенил(бензил)-1,5,3-дитиазепинан-3-амины и 2,4-диметил-N-фенил(бензил)-1,5,3-дитиазепинан-3-амины общей формулы (1).
Таким образом, в литературе отсутствуют сведения по получению N-фенил(бензил)-1,5,3-дитиазепинан-3-аминов и 2,4-диметил-N-фенил(бензил)-1,5,3-дитиазепинан-3-аминов общей формулы (1).
Предлагается новый способ получения N-фенил(бензил)-1,5,3-дитиазепинан-3-аминов и 2,4-диметил-N-фенил(бензил)-1,5,3-дитиазепинан-3-аминов общей формулы (1).
Сущность способа заключается в предварительном перемешивании формальдегида или ацетальдегида с 1,2-этандитиолом при температуре 0°C в течение 30 мин с последующим добавлением фенилгидразина (бензилгидразина), взятых в мольном соотношении альдегид: 1,2-этандитиол: фенилгидразин (бензилгидразин) = 20:10:10. Смесь перемешивают 2-4 ч при температуре 0°C и атмосферном давлении, выделяют N-фенил(бензил)-1,5,3-дитиазепинан-3-амины и 2,4-диметил-N-фенил(бензил)-1,5,3-дитиазепинан-3-амины общей формулы (1) с выходом 61-79%. Реакция протекает по схеме:
N-фенил(бензил)-1,5,3-дитиазепинан-3-амины и 2,4-диметил-N-фенил(бензил)-1,5,3-дитиазепинан-3-амины общей формулы (1) образуются только лишь с участием формальдегида или ацетальдегида, сероводорода и фенилгидразина (бензилгидразина), взятых в мольном соотношении 20:10:10. При другом соотношении исходных реагентов снижается селективность реакции. В присутствии других альдегидов (например, арилзамещенные альдегиды), других серусодержащих соединений (например, алкил-, арилтиолы) или других замещенных гидразинов (например, диалкилгидразины, диарилгидразины, алкиларилгидразины) целевые продукты (1) не образуются.
Реакции проводили при температуре 0°C. При температуре выше 0°C (например, 40°C) снижается селективность реакции и увеличиваются энергозатраты, а при температуре ниже 0°C (например, -10°C) снижается скорость реакции.
Существенные отличия предлагаемого способа
В известном способе реакция идет с участием в качестве исходных соединений фенил- или бензилгидразина, формальдегида и H2S c выходом целевых продуктов не более 35%. Известный способ не позволяет получать N-фенил(бензил)-1,5,3-дитиазепинан-3-амины и 2,4-диметил-N-фенил(бензил)-1,5,3-дитиазепинан-3-амины общей формулы (1).
В предлагаемом способе в качестве исходных реагентов применяются формальдегид или ацетальдегид, 1,2-этандитиол и фенилгидразин (бензилгидразин), которые приводят в разработанном способе к целевым продуктам с выходом более 60%. В отличие от известных способов предлагаемый способ позволяет получать индивидуальные N-фенил(бензил)-1,5,3-дитиазепинан-3-амины и 2,4-диметил-N-фенил(бензил)-1,5,3-дитиазепинан-3-амины общей формулы (1).
Способ поясняется следующими примерами
ПРИМЕР 1. В стеклянный реактор, снабженный механической мешалкой, капельной воронкой, при температуре 0°C помещают 20 ммоль формальдегида, 1,2-этандитиола (10 ммоль) перемешивают в течение 30 мин, затем добавляют 10 ммоль фенилгидразина. Реакционную смесь перемешивают при температуре ~0°C в течение 3 ч, экстрагируют хлороформом, выделяют N-фенил-1,5,3-дитиазепинан-3-амин с выходом 48-65%.
Другие примеры, подтверждающие способ, приведены в табл.1.
| Таблица 1 | ||||
| № п/п | Исходный альдегид | Исходный гидразин | Время реакции, час | Выход (1), % |
| 1 | формальдегид | фенилгидразин | 3 | 65 |
| 2 | - | - | 4 | 72 |
| 3 | - | - | 2 | 48 |
| 4 | ацетальдегид | - | 3 | 68 |
| 8 | формальдегид | бензилгидразин | 3 | 61 |
| 9 | ацтальдегид | - | 3 | 75 |
Все опыты проводили при температуре (~0°C) в мольном соотношении альдегид: 1,2-этандитиол: фенил(бензил)гидразин = 20:10:10.
Спектральные характеристики N-фенил(бензил)-1,4,6-дитиазипинан-6-аминов и N-фенил(бензил)-5,7-диметил-1,4,6-дитиазипинан-6-аминов общей формулы (1):
| N-фенил-1,5,3-дитиазепинан-3-амин: | |
| Спектр ЯМР 1Н (δ, м.д., J, Гц, 20°C): 3.08 (с, 4H, CH2 (2,3)); 4.31 (с, 4H, CH2 (5,7)); 6.18 (с, Н, NH (8)); 6.96 (д, 4H, CH2 (10,14) J=8 Гц); 6.88 (т, 2Н, CH2 (12) J1=7.6 Гц, J2=7.2 Гц); 7.26 (т, 4H, CH2 (9, 11, 13) J1=7.6 Гц, J2=8 Гц). Спектр ЯМР 13C (δ, м.д.): 35.46 (C-2,3); 61.19 (C-7,5); 114.51 (C-10,14); 120.15 (C-12); 129.35 (C-11,13); 146.02 (C-9). | |
| N-фенил-5,7-диметил-1,5,3-дитиазепинан-3-амин: | |
| Спектр ЯМР 1Н (δ, м.д., J, Гц, 20°C): 1.45 (д, 6Н, СН3 (8,16) J=6.8 Гц); 3.1 (м, 4H, CH2 (2,3)); 4.51 (к, 2Н, СН (5,7) J2=6.8 Гц); 6.03 (с, Н, NH (9)); 6.75-7.30 (м, 5Н, СН(11-15)). Спектр ЯМР 13C (δ, м.д.): 21.59 (C-8,16); 34.47 (C-2,3); 72.26 (C-7,5); 112.33 (C-11,15); 118.22 (C-13); 129.13 (C-12,14); 148.32 (C-10). |
| N-бензил-1,5,3-дитиазепинан-3-амин: | |
| Спектр ЯМР 1H (δ, м.д., J, Гц, 20°C): 2.45 (с, 4H, CH2 (2,3)); 3.73 (с, 1Н, CH2 (9));4.23 (с, 4H, CH2 (5,7)); 6.10 (с, Н, NH(8)); 6.45 (д, 4H, CH2(11,15) J=8 Гц); 6.67 (т, 2Н, CH2 (13) J1=7.6 Гц, J2=7.2 Гц); 7.16 (т, 4H, CH2 (10,12,14) J1=7.6 Гц, J2=8 Гц). Спектр ЯМР 13C (δ, м.д.): 34. 64 (C-2,3); 59.14 (C-7,5); 53.19 (C-9); 113.49 (C-11,15); 121.15 (C-13); 127.35 (C-12,14); 146.00 (C-10). | |
| 2,4-диметил-N-бензил-1,5,3-дитиазепинан-3-амин: | |
| Спектр ЯМР 1Н (δ, м.д., J, Гц, 20°C): 1.32 (д, 6Н, CH3 (8,16) J=6.8 Гц); 3.1 (м, 4H, CH2 (2,3)); 3.5 (с, 2Н, CH2 (10)); 4.34 (к, 2H, CH (5,7) 2J=6.8 Гц); 6.00 (с, H, NH (9)); 6.72-7.38 (м, 5H, CH (11-16)). Спектр ЯМР 13C (δ, м.д.): 20.43 (C-8,16); 32.74 (C-2,3); 53.67 (C-10); 69.26 (C-7,5); 112.31 (C-12,16); 117.34 (C-14); 128.12 (C-13,15); 148.32 (C-11). |
Способ получения N-фенил(бензил)-1,5,3-дитиазепинан-3-аминов и 2,4-диметил-N-фенил(бензил)-1,5,3-дитиазепинан-3-аминов общей формулы (I) R - Ph, Bz; R' - H, Meотличающийся тем, что смесь формальдегида или ацетальдегида с 1,2-этандитиолом подвергают взаимодействию с фенилгидразином (бензилгидразином) при мольном соотношении исходных реагентов альдегид:1,2-этандитиол:фенилгидразин (бензилгидразин) = 20:10:10 при температуре 0°C и атмосферном давлении в течение 2-4 ч.