Способ получения 4-(4-бром-2-фторанилино)-6-метокси-7(1-метилпиперидин-4-илметокси)хиназолина(zd6474) и способы получения промежуточных соединений для его получения
Иллюстрации
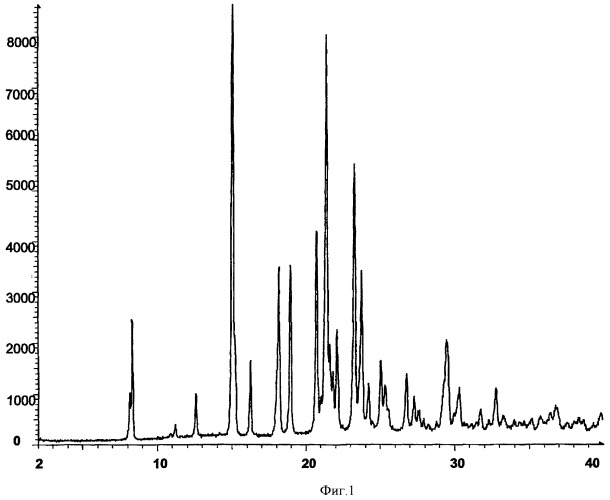
Показать всеНастоящее изобретения относится к способу получения 4-(4-бром-2-фторанилино)-6-метокси-7(1-метилпиперидин-4-илметокси)хиназолина (ZD6474), имеющего формулу, приведенную ниже, и его солей из соединения формулы X. Изобретение также относится к способу получения промежуточного соединения формулы Х и его солей, а также к способам получения других определенных промежуточных соединений, которые пригодны для получения (ZD6474). 6 н. и 21 з.п. ф-лы, 1 фиг., 2 таб., 19 пр.
Реферат
Настоящее изобретение относится к химическим способам приготовления определенных производных хиназолина или их фармацевтически приемлемых солей. Изобретение также относится к способам приготовления определенных промежуточных соединений, пригодных для приготовления производных хиназолина, и к способам приготовления производных хиназолина, используя указанные промежуточные соединения.
В частности, настоящее изобретение относится к химическим способам и промежуточным соединениям, пригодным для приготовления соединения 4-(4-бром-2-фторанилино)-6-метокси-7-(1-метилпиперидин-4-илметокси)хиназолин. Это соединение подпадает под широкое раскрытие в WO 98/13354 и в качестве примеров приведено в WO 01/32651, в примерах 2а, 2b и 2с.
Соединение 4-(4-бром-2-фторанилино)-6-метокси-7-(1-метилпиперидин-4-илметокси)хиназолин описывается в настоящей заявке с помощью формулы I:
и как ZD6474, кодовый номер, под которым известно соединение. Соединение ZD6474 также известно как Vandetanib и как Zactima™.
Нормальный ангиогенез играет важную роль в разнообразных процессах, включая эмбриональное развитие, заживление ран и некоторых составляющих женской репродуктивной функции. Нежелательный или патологический ангиогенез связан с болезненными состояниями, включая диабетическую ретинопатию, псориаз, злокачественные новообразования, ревматоидный артрит, атерому, саркому Капоши и гемангиому (Fan и др., 1995, Trends Pharmacol. Sci. 16:57-66; Folkman, 1995, Nature Medicine 1:27-31). Полагают, что изменение проницаемости сосудов играет важную роль как в нормальных, так и в патологических физиологических процессах (Cullinan-Bove и др., 1993, Endocrinology 133:829-837; Senger и др., 1993, Cancer and Metastasis Reviews, 12:303-324). Были идентифицированы определенные полипептиды, которые в условиях in vitro обладают стимулирующим действием на рост эндотелиальных клеток, включая кислые и щелочные факторы роста фибробластов (aFGF и bFGF) и фактор роста эндотелия сосудов (VEGF). Активность фактора роста VEGF посредством ограниченной экспрессии его рецепторов в отличие от таковой у FGF является относительно специфичной по отношению к клеткам эндотелия. Исследования, проведенные в последнее время, убедительно свидетельствуют о том, что VEGF является существенным стимулятором как нормального, так и патологического ангиогенеза (Jakeman и др., 1993, Endocrinology, 133:848-859; Kolch и др., 1995, Breast Cancer Research and Treatment, 36: 139-155) и проницаемости сосудов (Connolly и др., 1989, J.Biol.Chem. 264:20017-20024). Антагонистическое действие по отношению к VEGF путем блокирования VEGF при помощи антитела может приводить к ингибированию роста опухолей (Kim и др., 1993, Nature 362:841-844).
Рецепторные тирозинкиназы (RTK) занимают важное место в передаче биохимических сигналов через плазматическую мембрану клеток. Как правило, эти трансмембранные молекулы включают внеклеточный лиганд-связывающий домен, связанный при помощи сегмента в плазматической мембране с внутриклеточным доменом тирозинкиназы. Связывание лиганда с рецептором приводит к стимулированию связанной с рецептором активности тирозинкиназы, что приводит к фосфорилированию остатков тирозина как в рецепторе, так и в других внутриклеточных молекулах. Эти изменения в фосфорилировании тирозина инициируют каскадный путь передачи сигналов, что приводит ко многим ответным реакциям клеток. К настоящему времени было идентифицировано по крайней мере девятнадцать различных подсемейств RTK на основании гомологии аминокислотных последовательностей. Одно из этих подсемейств в настоящее время состоит из fms-подобного рецептора тирозинкиназы Flt-1 (также называется VEGFR-1), рецептора KDR, содержащего домен со вставкой киназы (который также называется VEGFR-2 или Flk-1), и другого fms-подобного рецептора тирозинкиназы, Flt-4. Было показано, что две эти родственные RTK, Fit-1 и KDR связывают VEGF с высоким сродством (De Vries и др., 1992, Science 255:989-991; Terman и др., 1992, Biochem Biophys. Res. Comm. 1992, 187:1579-1586). Связывание VEGF с этими рецепторами, которые экспрессируются в гетерологичных клетках, ассоциировано с изменениями уровня фосфорилирования тирозина белков клетки и потоками кальция.
VEGF является ключевым стимулятором васкулогенеза и ангиогенеза. Этот цитокин вызывает фенотипическое образование отростков сосудов путем стимулирования пролиферации эндотелиальных клеток, экспрессии протеазы и миграции с последующей организацией этих клеток с образованием капилляра (Keck, P.J., Hauser, S.D., Krivi, G., Sanzo, K., Warren, Т., Feder, J. и Connolly, D.T., Science (Washington DC), 246:1309-1312, 1989; Lamoreaux, W.J., Fitzgerald, M.E., Reiner, A., Hasty, K.A. и Charles, S.T., Microvasc. Res., 55:29-42, 1998; Pepper, M.S., Montesano, R., Mandroita, S.J., Orci, L. и Vassalli, J.D., Enzyme Protein, 49:138-162, 1996.). Кроме того, VEGF вызывает значительное повышение проницаемости сосудов (Dvorak, H.F., Detmar, M., Claffey, K.P., Nagy, J.A., van de Water, L., и Senger, D.R., (Int. Arch. Allergy Immunol, 107; 233-235, 1995; Bates, D.O., Heald, R.I., Curry, F.E. и Williams, B.J. Physiol. (Lond.), 533:263-272, 2001), стимулируя формирование сверхпроницаемости недоразвитой сосудистой сети, что является характерной особенностью патологического ангиогенеза.
Было показано, что активирование только KDR достаточно для активизации всех основных фенотипических ответных реакций на VEGF, включая пролиферацию эндотелиальных клеток, миграцию и выживание и индуцирование проницаемости сосудов (Меуеr, М., Clauss, M., Lepple-Wienhues, A., Waltenberger, J., Augustin, H.G., Ziche, M., Lanz, G, Büttner, M., Rziha, H-J. и Dehio, C, EMBO J., 18: 363-374, 1999; Zeng, H., Sanyal, S. и Mukhopadhyay, D., J. Biol. Chem, 276; 32714-32719, 2001; Gille, H., Kowalski, J., Li, B., LeCouter, J., Moffat, B, Zioncheck, T.F., Pelletier, N. и Ferrara, N., J. Biol. Chem, 276:3222-3230, 2001).
ZD6474 является эффективным ингибитором VEGF RTK, а также имеет незначительную активность по отношению к фактору роста эпидермиса (EGF) RTK. ZD6474 ингибирует действия VEGF и представляет интерес в связи с его антиангиогенными действиями и/или действиями на проницаемость сосудов. Ангиогенез и/или повышенная проницаемость сосудов присутствует при многих различных болезненных состояниях, включая злокачественное новообразование (включая лейкоз, множественную миелому и лимфому), диабет, псориаз, ревматоидный артрит, саркому Капоши, гемангиому, острую и хроническую нефропатии, атерому, артериальный рестеноз, аутоиммунные заболевания, острое воспаление, чрезмерное образование рубцов и спаек, лимфатический отек, эндометриоз, дисфункциональное маточное кровотечение и заболевания глаз с пролиферацией сосудов сетчатки, включая дегенерацию желтого пятна, связанную со старением. Было показано, что ZD6474 обладает широким спектром противоопухолевого действия в диапазоне моделей после перорального введения один раз в сутки (Wedge S.R., Ogilvie D.J., Dukes M. и др., Proc. Am. Assoc. Cane. Res. 2001; 42: реферат 3126).
В WO 98/13354 описаны определенные возможные пути для приготовления соединений 4-анилинохиназолина. Однако в документе WO 98/13354 отдельно не описан способ получения соединения формулы I.
В WO 98/10767 также описано несколько возможных путей для приготовления 4-анилинохиназолина. Однако в документе WO 98/10767 отдельно не описан способ получения соединения формулы I.
В WO 01/32651 описаны несколько альтернативных путей получения соединения формулы I.
Путь, который описан в примере 2а заявки WO 01/32651, предусматривает реакцию соединения 4-(4-бром-2-фторанилино)-6-метокси-7-(пиперидин-4-илметокси)хиназолина с водным формальдегидом, затем с цианоборогидридом натрия в смеси растворителей тетрагидрофуран и метанол. Продукт очищали с помощью хроматографии и выделяли в виде свободного основания. После этого свободное основание превращали в гидрохлоридную соль путем реакции с хлористым водородом в смеси растворителей метиленхлорид и метанол.
Путь, который описан в примере 2b заявки WO 01/32651, предусматривает реакцию соединения 4-(4-бром-2-фторанилино)-6-метокси-7-(1-(трет-бутоксикарбонил)пиперидин-4-илметокси)хиназолина с водным формальдегидом в муравьиной кислоте с последующим взаимодействием с гидроксидом натрия в воде и экстрагированием продукта этилацетатом. Продукт находится в виде свободного основания.
Путь, который описан в примере 2 с заявки WO 01/32651, предусматривает реакцию соединения 4-хлор-6-метокси-7-(1-метилпиперидин-4-илметокси)хиназолина с 4-бром-2-фторанилином и хлористым водородом в изопропаноле. После этого продукт выделяли в виде гидрохлоридной соли. В ЯМР-исследовании гидрохлоридную соль растворяли в диметилсульфоксиде и превращали в свободное основание путем добавления твердого карбоната калия. Затем свободное основание превращали в трифторацетатную соль путем добавления трифторуксусной кислоты. В другом опыте гидрохлоридную соль суспендировали в метиленхлориде и промывали насыщенным гидрокарбонатом натрия для получения свободного основания.
В WO 01/32651 также описаны пути приготовления исходных веществ, которые используются в примерах 2а, 2b и 2с, таких как соединения 4-(4-бром-2-фторанилино)-6-метокси-7-(пиперидин-4-илметокси)хиназолин, 4-(4-бром-2-фторанилино)-6-метокси-7-(1-(трет-бутоксикарбонил)пиперидин-4-илметокси)хиназолин и 4-хлор-6-метокси-7-(1-метилпиперидин-4-илметокси)хиназолин. Некоторые из этих путей более подробно обсуждаются ниже.
Пути, описанные в WO 01/32651 для получения ZD6474 (в виде гидрохлоридной соли или свободного основания), также описаны и/или на них ссылаются в публикациях, относящихся к комбинированным лечениям, включающим ZD6474, таких как WO 03/039551, WO 2004/014383, WO 2004/014426, WO 2004/032937, WO 2004/071397 и WO 2005/004870.
Существующие пути для получения соединения формулы I достаточны для синтеза относительно небольших количеств соединения. Тем не менее, для путей, предусматривающих линейный вместо конвергентного синтеза, необходимо использование множественных стадий очистки и выделения большого количества промежуточных соединений. По существу, суммарный выход синтеза не является высоким. Следовательно, существует потребность в более эффективном синтезе соединения формулы I, пригодном для применения для получения больших количеств этого соединения. Также существует потребность в более эффективных синтезах промежуточных соединений, пригодных для синтеза соединения формулы I для применения для получения больших количеств этих промежуточных соединений.
Предпочтительно, новые синтезы должны минимизировать количество промежуточных соединений, которые необходимо выделять, и не должны использовать дорогие и трудоемкие методики очистки. Дополнительно, новые синтезы должны образовывать постоянно высококачественные соединения, в частности, для того, чтобы образовать высококачественное соединение формулы I для соответствия требованиям высокой чистоты для фармацевтического продукта. Новые синтезы также должны использовать методики и реагенты, которые могут безопасно использоваться на производственном предприятии и которые отвечают рекомендациям по охране окружающей среды.
В соответствии с настоящим изобретением сейчас мы обеспечили улучшенные способы приготовления ZD6474, соединения формулы I.
В соответствии с настоящим изобретением обеспечиваются также способы приготовления ключевых промежуточных соединений, которые могут использоваться для приготовления ZD6474.
Новые способы являются благоприятными, поскольку они позволяют получить соединения с высокой чистотой и высоким выходом в большом количестве. Способы позволяют существенно уменьшить количество промежуточных соединений, которые следует выделить, и, в целом, являются более конвергентными, чем предыдущие пути. Такие изменения обеспечивают существенные преимущества относительно времени и затрат.
Для избегания неопределенности термин "ZD6474", как используется в настоящем изобретении, относится к свободному основанию ZD6474, если специально не указано иначе.
Ключевым промежуточным соединением, которое может использоваться для получения ZD6474, является соединение формулы IIа
где R представляет собой подходящий сложный сульфонатный эфир, такой как мезилат, эзилат, безилат или тозилат.
В дальнейшем варианте осуществления соединение формулы IIа представляет собой 1-(трет-бутоксикарбонил)-4-(4-метилфенилсульфонилоксиметил)пиперидин, соединение формулы II:
В примере 2 заявки WO 01/32651 описан путь получения соединения формулы II. Этот путь предусматривает реакцию этил 4-пиперидинкарбоксилата с ди-трет-бутилдикарбонатом в этилацетатном растворителе, получая этил 4-(1-(трет-бутоксикарбонил)пиперидин)карбоксилат, который выделяют. После этого этил 4-(1-(трет-бутоксикарбонил)пиперидин)карбоксилат подвергают реакции с литийалюминийгидридом в тетрагидрофуране, получая 1-(трет-бутоксикарбонил)-4-гидроксиметилпиперидин, который выделяют. Затем 1-(трет-бутоксикарбонил)-4-гидроксиметилпиперидин повергают реакции с 1,4-диазабицикло[2,2,2]октаном и толуолсульфбнилхлоридом в трет-бутилметиловом простом эфирном растворителе, получая соединение формулы II.
В заявке ЕР-А-0317997 описан путь получения соединения формулы II. Этот путь предусматривает реакцию 4-карбоксипиперидина (также известного как изонипекотиновая кислота) с карбонатом натрия и да-трет-бутилдикарбонатом в водном растворителе, получая сложный трет-бутиловый эфир 4-карбокси-пиперидин-1-карбоновой кислоты, который выделяют. После этого сложный трет-бутиловый эфир 4-карбокси-пиперидин-1-карбоновой кислоты подвергают реакции с бораном в тетрагидрофурановом растворителе, получая соединение формулы II.
В заявке WO 94/27965 описан путь получения соединения формулы II. Этот путь предусматривает реакцию 4-гидроксиметилпиперидина с ди-трет-бутилдикарбонатом в тетрагидрофурановом расторителе, получая трет-бутил 4-(гидроксиметил)пиперидин-1-карбоксилат, который выделяют в виде масла. После этого 1-(трет-бутоксикарбонил)-4-гидроксиметилпиперидин подвергают реакции с толуолсульфонилхлоридом и пиридином, получая соединение формулы II.
Пути, описанные в документах предшествующего уровня техники, для получения соединения формулы II достаточны для синтеза относительно небольших количеств соединения. Тем не менее, они все требуют выделения каждого из промежуточных соединений, и следовательно, предусматривают много стадий выделения и/или очистки. Это приводит к удовлетворительному суммарному выходу соединения формулы II, используемого в небольшом масштабе. Однако пути, описанные в документах предшествующего уровня техники, неприемлемы для применения в промышленном масштабе, поскольку они предусматривают много стадий выделения и/или очистки, которые не могут быть эффективно осуществлены в промышленном масштабе. В частности, пути, описанные в документах предшествующего уровня техники, непригодны для применения для приготовления фармацевтического продукта с высокой чистотой.
Следовательно, существует потребность в более эффективном синтезе соединения формулы II, подходящего для применения для получения больших количеств этого соединения. Предпочтительно, новые синтезы не должны предусматривать дорогостоящие и трудоемкие выделения и/или очистки. Таким образом, в новом синтезе должно быть уменьшено количество необходимых методик выделения и/или очистки, посредством этого уменьшена стоимость и время производства. Предпочтительно, в новом синтезе должно быть минимизировано количество растворителей, используемых при осуществлении метода, что улучшает экологические показатели и предоставляет возможность для восстановления растворителя. Предпочтительно, новый синтез также должен обеспечивать устойчивый и надежный способ выделения соединения формулы II и равным образом обеспечивать высокое качество соединения формулы II, например, для того, чтобы соответствовать нормативным требования для внедрения исходных веществ в получение фармацевтических продуктов.
В соответствии с первым аспектом осуществления настоящего изобретения обеспечивается способ получения соединения формулы IIа из (С1-С6)алкил-4-пиперидинкарбоксилатного соединения формулы III:
где способ включает стадии:
(а) взаимодействие (С1-С6)алкил-4-пиперидинкарбоксилатного соединения формулы III с ди-трет-бутилдикарбонатом в присутствии толуола или ксилола с образованием первой смеси, содержащей толуол или ксилол, трет-бутанол и соединение формулы IV:
(б) практически полное удаление трет-бутанола из первой смеси;
(в) взаимодействие соединения формулы IV с подходящим восстановителем in situ в присутствии толуола или ксилола с образованием второй смеси, содержащей толуол, восстановленные побочные продукты, включая спиртовые побочные продукты, и соединение формулы V:
(г) практически полное удаление спиртовых побочных продуктов из второй смеси; и
(д) взаимодействие соединения формулы V с подходящим сульфирующим реагентом in situ с образованием сложного сульфонатного эфира в присутствии подходящего основания и толуола, получая соединение формулы IIа.
где R представляет собой подходящий сложный сульфонатный эфир, такой как мезилат, эзилат, безилат или тозилат. В одном варианте осуществления изобретения сульфирующий реагент представляет собой тозилхлорид.
Для избежания неопределенности термин 'in situ' обозначает, что взаимодействие осуществляют без выделения реагентов с предыдущей стадии способа.
Способ первого аспекта настоящего изобретения является благоприятным, так как он обеспечивает возможность получения соединения формулы IIа с высокой чистотой и высоким выходом в промышленном масштабе. Обычно каждая из стадий способа первого аспекта настоящего изобретения осуществляется с выходом больше 95%.
Все стадии первого аспекта настоящего изобретения осуществляются в толуоле или ксилоле в качестве растворителя. В другом варианте осуществления все стадии первого аспекта настоящего изобретения осуществляются в толуоле. Это позволяет осуществлять способ в виде непрерывного процесса без выделения и/или очистки промежуточных соединений формул IV и V. Это существенно уменьшает время и стоимость производства формулы IIа в промышленном масштабе. Использование единственного растворителя, такого как толуол или ксилол, также может предоставить возможность повторного использования растворителя, что повышает эффективность способа и обеспечивает преимущества использования для окружающей природной среды. Применение толуола или ксилола в качестве растворителя также позволяет эффективно и удобно удалить реакционно-способные побочные продукты (такие как спирты), например, путем перегонки. Присутствие таких реакционно-способных побочных продуктов может привести к загрязнению соединения формулы IIа, если их своевременно не удалить.
Дополнительно, использование толуола или ксилола в качестве растворителя в способе первого аспекта настоящего изобретения позволяет удобно выделить соединение формулы IIа путем кристаллизации. Соединение формулы IIа, например, может быть выделено с чистотой больше чем 99,5% путем кристаллизации непосредственно из реакционной смеси без необходимости дальнейшей очистки. Это является благоприятным, например, если соединение формулы IIа вводят на поздней стадии в получение фармацевтического продукта, например соединения формулы I, поскольку это минимизирует риск введения загрязнений в фармацевтический продукт.
На стадии (а) способа используют (С1-С6)алкил-4-пиперидинкарбоксилатное соединение формулы III, предпочтительно (С1-С4)алкил-4-пиперидинкарбоксилатное соединение формулы III. В частности, подходящим (С1-С6)алкил-4-пиперидинкарбоксилатным соединением формулы III, которое может применяться на стадии (а), может быть, например, этил 4-пиперидинкарбоксилат. Другим названием для этил 4-пиперидинкарбоксилата является этилизонипекотат.
Взаимодействие на стадии (а) осуществляют при температуре в интервале, например, от 0 до 45°С, подходяще в интервале от 15 до 35°С, более подходяще в интервале от 25 до 30°С.
Исходные вещества (С1-С6)алкил-4-пиперидинкарбоксилатные соединения формулы III и ди-трет-бутилдикарбонат, используемые на стадии (а) способа, являются коммерчески доступными или могут быть получены с помощью общепринятых методов. Например, (С1-С6)алкил-4-пиперидинкарбоксилатные соединения формулы III могут быть получены, как описано в заявке на патент Японии JP 03002162 А2.
Трет-бутанол, который образуется на стадии (а), представляет собой побочный продукт реакции между (С1-С6)алкил-4-пиперидинкарбоксилатным соединением формулы III и ди-трет-бутилдикарбонатом. В процессе согласно настоящему изобретению этот побочный продукт легко и удобно практически полностью удаляется из реакционной смеси, например, путем дистилляции на стадии (б).
Является благоприятным практически полностью удалять трет-бутанольный побочный продукт из реакционной смеси, например, путем дистилляции на стадии (б), поскольку любой трет-бутанольный побочный продукт, который не удаляется, вероятно, реагирует с восстановителем на стадии (в), в связи с этим уменьшается количество восстановителя, доступное для осуществления желательной реакции с соединением формулы IV. Таким образом, удаление трет-бутанольного побочного продукта на стадии (б) предусматривает правильную стехиометрию реагентов на стадии (в) способа и, следовательно, более эффективное осуществление реакции на этой стадии. Это, в свою очередь, обеспечивает высокий выход и чистоту соединения формулы V на стадии (в).
Под термином "практически полностью удаляется" мы подразумеваем, что по меньшей мере 85% побочного трет-бутанола, который образуется на стадии (а), удаляется, например, путем дистилляции. Обычно дистилляцию осуществляют до тех пор, пока внутренняя температура не достигает интервала от 102 до 112°С. Дистилляцию на стадии (б) подходяще осуществляют или при атмосферном или частично пониженном давлении.
Подходящими восстановителями для применения на стадии (в) являются натрий бис(2-метоксиэтокси)алюминийгидрид, литийалюминийгидрид и диизобутилалюминийгидрид. Более предпочтительно, восстановителем, используемым на стадии (в), является натрий бис(2-метоксиэтокси)алюминийгидрид.
Взаимодействие на стадии (в) осуществляют при температуре в интервале, например, от 20 до 55°С, подходяще в интервале от 30 до 50°С, более подходяще в интервале от 35 до 45°С.
Специалист в данной области техники примет во внимание, что реакция стадии (в) обычно обеспечивает восстановленные побочные продукты дополнительно к желательному соединению формулы V. Восстановленные побочные продукты включают спиртовые побочные продукты. Спиртовые побочные продукты имеют происхождение из -O-(С1-С6)алкильной части сложноэфирной группы в соединении формулы IV и также могут иметь происхождение из восстановителя. Например, если соединение формулы IV представляет собой этил 4-(1-трет-бутоксикарбонил)пиперидин)карбоксилат и восстановителем, используемым на стадии (в), является натрий бис(2-метоксиэтокси)алюминийгидрид, то типичные восстановленные побочные продукты включают соли алюминия и спиртовые побочные продукты, такие как этанол и 2-метоксиэтанол. Спиртовые побочные продукты легко и подходяще практически полностью удаляются из реакционной смеси, например, путем дистилляции на стадии (г).
Благоприятным является практически полное удаление спиртовых побочных продуктов на стадии (г), поскольку любые такие побочные продукты, которые не удалены, вероятно, взаимодействуют с сульфирующим реагентом на стадии (д), вследствие этого повышается количество примесей, которые могут загрязнять желательный продукт и уменьшать количество сульфирующего реагента, доступного для желательной реакции с соединением формулы V. Таким образом, удаление спиртовых побочных продуктов позволяет соблюсти правильную стехиометрию реагентов на стадии (д) способа и, следовательно, более эффективно осуществить реакцию на этой стадии. Это, в свою очередь, обеспечивает высокий выход и чистоту соединения формулы II на стадии (д).
Под термином "практически полное удаление" мы подразумеваем, что по меньшей мере 98% спиртовых побочных продуктов, которые образуются на стадии (в), удаляются, например, путем дистилляции. Обычно дистилляцию осуществляют до тех пор, пока внутренняя температура не достигает интервала от 102°С до 112°С. Дистилляцию на стадии (г) подходяще осуществляют или при атмосферном, или частично пониженном давлении.
Дистилляция на стадии (г) также обычно практически полностью удаляет любую присутствующую воду. Это также позволяет соблюсти правильную стехиометрию реагентов на стадии (д) способа, поскольку любая вода, которая не удалена, вероятно, взаимодействует с сульфирующим реагентом на стадии (д), вследствие этого снижается количество сульфирующего реагента, доступного для желательной реакции с соединением формулы V. Под термином "практически полное удаление" мы подразумеваем, что меньше чем 20 мол.% воды остается после дистилляции.
Специалист в данной области техники примет во внимание, что обычно необходимо закаливать реакционную смесь на стадии (в) для удаления любого непрореагировавшего присутствующего восстановителя перед осуществлением реакции на стадии (д). Обычно на стадии закаливания также удаляются некоторые из восстановленных побочных продуктов, перечисленных выше, например соли алюминия и некоторые, но не все, спиртовые побочные продукты. Подходящие гасящие добавки в большинстве случаев могут быть выбраны из любого средства, которое описано в литературе и/или известно специалисту в данной области техники. Например, если восстановитель, используемый на стадии (в), представляет собой натрий бис(2-метоксиэтокси)алюминий гидрид, то гасящая добавка обычно может представлять собой водный раствор виннокислого калия-натрия (также известен как сегнетова соль). Обычно полученную в результате водную фазу (содержащую гасящий восстановитель) затем удаляют путем отделения. Стадию закаливания осуществляют перед дистилляцией на стадии (г).
Подходящим основанием для применения на стадии (д) является третичное аминовое основание, например триэтилендиамин.
Реакцию стадии (д) осуществляют при температуре в интервале, например, от 15 до 45°С, более подходяще в интервале от 25 до 35°С.
Специалист в данной области техники примет во внимание, что типично необходимо закаливать реакционную смесь на стадии (д) для удаления любого непрореагировавшего присутствующего сульфирующего реагента. Подходящие гасящие добавки в большинстве случаев могут быть выбраны из любого средства, которое описано в литературе и/или известно специалисту в данной области техники. Например, подходящей гасящей добавкой может быть основание, такое как гидроксид натрия или карбонат калия.
В одном аспекте способ получения соединения формулы II дополнительно может включать стадию (е) выделения и/или очистки соединения формулы II. Стадия (е) может включать любые подходящие стадии или методики выделения желательного продукта, которые описаны в литературе и/или известны специалисту в данной области техники. Предпочтительные стадии, которые могут применяться, будут обеспечивать высокое качество и высокую чистоту продукта.
Например, стадия (е) может включать стадии промывания соединения формулы II водой и/или разведенной лимонной кислотой. Стадия (е) также, например, может включать кристаллизацию с использованием подходящей системы растворителей. Примером подходящей системы растворителей является система растворителей, содержащая толуол и изогексан, что обеспечивает получение соединения формулы II с высокой чистотой, обычно с чистотой больше чем 98%, подходяще, больше чем 99,5%, и с высоким выходом, обычно с выходом больше чем 80%, подходяще, больше чем 85%. Специалист в данной области техники примет во внимание, что стадия (е) также может включать стадию циклического воздействия температуры (также называемое как "созревание Освальда") соединения формулы II, улучшая таким образом физическую форму продукта, если это является необходимым.
Другим ключевым промежуточным соединением, которое может применяться для получения ZD6474, является защищенное производное 7-гидрокси-4-(4-бром-2-фторанилино)-6-метоксихиназолина, соединение формулы VI:
где R1 представляет собой кислотолабильную защитную группу, такую как бензил, замещенный бензил, трет-бутил, аллил или метоксиэтоксиметил.
В примере 2 заявки WO 01/32651 и примере 24 заявки WO 97/32856 описан путь получения гидрохлоридной соли соединения формулы VI, где R' представляет собой бензил. Путь предусматривает реакцию гидрохлоридной соли 7-бензилокси-4-хлор-6-метоксихиназолина с 4-бром-2-фторанилином в 2-пропанольном растворителе с получением гидрохлоридной соли соединения формулы VI, которую выделяют. В примере 2 заявки WO 01/32651 указывается, что гидрохлоридную соль 7-бензилокси-4-хлор-6-метоксихиназолина получают в соответствии с примером 1 заявки WO 97/22596.
В примере 1 заявки WO 97/22596 гидрохлоридную соль 7-бензилокси-4-хлор-6-метоксихиназолина получают путем реакции 7-бензилокси-6-метокси-3,4-дигидрохиназолин-4-она с тионилхлоридом в N,N-диметилформамидном растворителе. Аналогичный процесс получения гидрохлоридной соли 7-бензилокси-4-хлор-6-метоксихиназолина описан в примере 4 заявки WO 97/32856.
В заявке WO 98/10767 описан путь получения 6,7-дизамещенных 4-анилинохиназолиновых соединений. Путь предусматривает реакцию 6,7-дизамещенного хиназолинонового соединения с хлорирующим реагентом и катализатором при отсутствии растворителя или с хлорирующим реагентом в присутствии улавливающего средства, получая 6,7-дизамещенное 4-хлорхиназолиновое соединение. Затем 6,7-дизамещенное 4-хлорхиназолиновое соединение подвергают реакции с замещенным анилиновым соединением, необязательно в присутствии подходящего основания, получая гидрохлоридную соль 6,7-дизамещенного 4-анилинохиназолинового соединения, которую затем можно превратить в свободное основание. В заявке WO 98/10767 не описан 7-бензилокси-4-(4-бром-2-фторанилино)-6-метоксихиназолин, также не описан способ его получения.
Пути, описанные в документах предшествующего уровня техники, для получения соединения формулы VI достаточны для синтеза относительно небольших количеств соединения. Однако для всех их необходимо выделение и/или очистка промежуточных соединений. Это приводит к удовлетворительному, но не высокому суммарному выходу соединения формулы VI.
Следовательно, существует потребность в более эффективном синтезе соединения формулы VI, подходящем для получения больших количеств этого соединения. Предпочтительно, в новом синтезе не должны применяться дорогие и трудоемкие методики выделения и/или очистки. Следовательно, в новом синтезе должно быть уменьшено количество необходимых методик выделения и/или очистки, уменьшая таким образом стоимость и время приготовления. Новый способ также должен обеспечивать эффективное выделение соединения формулы VI в кристаллической форме с высокой чистотой и выходом, где кристаллическая форма будет иметь хорошие фильтрационные характеристики.
В соответствии со вторым аспектом настоящего изобретения обеспечивается способ получения соединения формулы VI:
где R1 представляет собой кислотолабильную защитную группу;
из соединения формулы VII:
где способ включает стадии:
(ж) взаимодействие соединения формулы VII с подходящим хлорирующим реагентом в присутствии подходящего основания и подходящего растворителя, где реакцию осуществляют путем:
(ж-1) добавления смеси соединения формулы VII и основания в растворителе к смеси хлорирующего реагента в растворителе при температуре в диапазоне от 60 до 110°С, подходяще от 60 до 80°С в течение приблизительно 60 минут; или
(ж-2) добавления хлорирующего реагента к смеси соединения формулы VII и основания в растворителе при температуре окружающей среды в течение приблизительно 15 минут и после этого нагревания реакционной смеси в течение приблизительно 90 минут до температуры в диапазоне от 70 до 90°С и перемешивания реакционной смеси при этой температуре приблизительно в течение 1 часа; или
(ж-3) добавления хлорирующего реагента к смеси соединения формулы VII и основания в растворителе при температуре в диапазоне от 60 до 110°С, подходяще от 70 до 90°С в течение приблизительно 15 минут, получая соединение формулы VIII:
и
(з) взаимодействие соединения формулы VIII с 4-бром-2-фторанилином in situ в присутствии растворителя, который используют на стадии (ж), получая гидрохлоридную соль соединения формулы VI;
и после этого соединение формулы VI, полученное в виде гидрохлоридной соли, может быть превращено в свободное основание или в форму альтернативной соли, если это является необходимым.
Термин "кислотолабильная защитная группа" относится к группам, которые легко удаляются в кислых условиях. Подходящими методами защиты являются методы, известные специалисту в данной области техники. Могут применяться общепринятые защитные группы в соответствии со стандартной практикой (для иллюстрации см. T.W.Green, Protective Groups in Organic Synthesis, John Wiley и Sons, 1991). Подходящими защитными группами для R1 являются бензил, замещенный бензил (например, С1-4алкоксибензил и C1-4алкибензил), трет-бутил, 1,1-диметил-1-этилметил, аллил, замещенный аллил (такой как С1-4алкилаллил) или метоксиэтоксиметил. В другом варианте осуществления R1 представляет собой бензил.
Способ второго аспекта изобретения является благоприятным, поскольку он обеспечивает получение соединение формулы VI с высокой чистотой и высоким выходом в большом масштабе. Обычно каждая из стадий способа второго аспекта настоящего изобретения обеспечивает выход больше чем 90%.
Подходящий растворитель для стадии (ж) выбирают из группы, включающей простой арилалкиловый эфир, такой как анизол, простой диалкиловый эфир, такой как простой 1,2-диметиловый эфир, бензол, замещенный галогеном, такой как хлорбензол или трифтортолуол, или бензол, замещенный алкилом, такой как ксилол, этилбензол или толуол. В одном варианте осуществления изобретения растворитель на стадии (ж) представляет собой анизол или толуол. В другом варианте осуществления изобретения растворитель на стадии (ж) представляет собой толуол.
Обе стадии (ж) и (з) осуществляют в идентичном растворителе, где растворитель выбирают из подходящего растворителя, как описано выше. Это позволяет осуществить способ в виде непрерывного способа без выделения и/или очистки промежуточного соединения формулы VIII. Это существенно уменьшает время и стоимость получения соединения формулы VI в большом масштабе. Дополнительно, применение единственного растворителя может предоставить возможность повторного использования растворителя, что повышает эффективность способа и обеспечивает преимущества использования для окружающей природной среды. Применение толуола или анизола в качестве растворителя реакции является благоприятным, поскольку эти растворители сводят к минимуму образование побочных продуктов, которые могут образовываться вследствие димеризации соединения формулы VII, как обсуждалось выше. Выбор растворителя также позволяет осуществить легкое и удобное выделение соединения формулы VI. Например, если реакционную смесь охлаждают до температуры окружающей среды, то соединение формулы VI обычно образует твердое вещество, где твердое вещество затем может быть собрано с помощью любого общепринятого метода.
Режим добавления реагентов на стадии (ж) (то есть, как описано на стадиях (ж-1), (ж-2) и (ж-3)) является благоприятным, так как это сводит к минимуму образование побочных продуктов/примесей на этой стадии. Обычно любые такие побочные продукты/примеси преимущественно образуются путем димеризации соединения формулы VII. Уменьшение образования побочных продуктов/примесей предоставляет возможность использовать промежуточное соединение формулы VIII, полученное на стадии (ж), на стадии (з) без выделения и/или очистки. Уменьшение образования побочных продуктов/примесей на стадии (ж) также предоставляет возможность правильной стехиометрии для реагентов на стадии (з) способа и, следовательно, более эффективное осуществление реакции на этой стадии.