Способ получения 4-деметилдаунорубицина
Иллюстрации
Показать всеИзобретение относится к способу получения антрациклина карминомицина, представленного формулой (1),
из антрациклина даунорубицина. Способ включает взаимодействие даунорубицина, представленного формулой (2), или N-защищенного даунорубицина, представленного формулой (3):
со слабой кислотой Льюиса, выбранной из группы, включающей TiHal4, BHal3, MgHal2, где Hal=F, Cl, Вr, I, для деметилирования 4-метокси группы даунорубицина, представленного формулой 2, или N-защищенного даунорубицина, представленного формулой 3. Изобретение позволяет получить карминомицин способом, не приводящим к деструкции С-7 гликозидной связи и уменьшающим количество стадий синтеза. 5 з.п. ф-лы, 1 пр.
Реферат
Заявки, имеющие отношение к данному изобретению
В соответствии с разделом 119(е) Кодекса законов США (35 U.S.C.) и другими применимыми законами данная заявка включает преимущества предварительной заявки США№60/749,464, поданной 13 декабря 2005. Таким образом, предварительная заявка США №60/749,464 во всей своей полноте включена в данную заявку в виде ссылки.
Область техники
В целом, область техники, к которой относится данное изобретение, связана с химическими способами, используемыми для получения антрациклинов, соединений, используемых в качестве лекарства при противораковой химиотерапии. Более конкретно, данное изобретение относится к способам получения цитостатического антрациклинового антибиотика 4-деметилдаунорубицина (обычно называемого "карминомицин") в форме, соответствующей Формуле (1) (где An- является анионом любой сильной кислоты, например, в случае 4'-эпирубицина An- включает Cl-).
Уровень техники
Антрациклины образуют одну из крупнейших групп (семейств) природных биологически активных соединений. Было показано, что несколько членов этого семейства обладают терапевтической (клинической) эффективностью в качестве противоопухолевых агентов. Эти соединения включают, например, даунорубицин, доксорубицин, идарубицин, эпирубицин, пирарубицин, зорубицин, акларубицин и карминомицин. Было показано, в частности, что эти соединения полезны при лечении карциномы молочной железы, острого лимфолейкоза и нелимфоцитарной лейкемии (non-lymphocytic leukemia), хронического лимфолейкоза, лимфомы, не являющейся лимфомой Ходжкина (non-Hodgkin's lymphoma), и других солидных злокачественных опухолей.
Карминомицин (в форме, соответствующей Формуле (1)) является хорошо известным антрациклиновым антибиотиком, используемым как в определенной клинической практике, так и в качестве исходного материала при синтезе множества 4-модифицированных антрациклинов, в частности идарубицина (см., например, патент США №7,053,191, включенный в данное изобретение в виде ссылки).
Микробиологический способ получения карминомицина осложнен чрезвычайно низкой продуктивностью известных штаммов микроорганизмов, находящейся на уровне 0.1-0.3 г/л. Вплоть до настоящего времени синтетические способы получения карминомицина были очень длинными (включали 10-12 химических стадий) и дорогими. Согласно описанным ранее способам субстратом деметилирования 4-метокси группы был даунорубицинон, т.к. не были известны способы деметилирования 4-метокси группы без разрушения С-7 гликозидной связи. Наиболее общепринятый способ деметилирования 4-метокси группы включает обработку даунорубицинона сильной кислотой Льюиса, AlCl3, в инертных растворителях, таких как хлорированные углеводороды (например, дихлорметан) при температуре кипения. При попытке провести аналогичный синтез с даунорубицином даунозоамин-гликозидная связь оказалась разорванной и антрациклиновое ядро - разрушенным.
Раскрытие изобретения
Данное изобретение направлено на создание новаторского способа получения карминомицина с использованием нового способа деметилирования 4-метокси группы легко доступного исходного соединения даунорубицина, способа, не приводящего к деструкции С-7 гликозидной связи и уменьшающего количество стадий синтеза с 10-12 до 1-3.
Деметилирование осуществляют путем обработки даунорубицина или N-защищенного даунорубицина (Формула 2 и Формула 3 соответственно) слабыми кислотами Льюиса, такими как TiHal4, ВНаl3, MgHal2, где Hal=F, Cl, Br, I, в безводных растворителях, таких как алканы, циклоалканы, арены, галогеноалканы, простые эфиры, CS2, все из которых являются устойчивыми в кислотах Льюиса при температурах 10-80°С.
Экстракцию карминомицина или N-защищенного карминомицина осуществляют путем обработки реакционной массы водным раствором сильных органических или неорганических кислот. После разрушения реакционного комплекса карминомицина с кислотами Льюиса реакционную массу (в случае использования водорастворимых простых эфиров) экстрагируют нерастворимыми в воде (гидрофобными) органическими растворителями, такими как галогеноалканы, циклоалканы, арены, С4-С6 спирты и их смеси. Карминомицин экстрагируется в виде основания.
Детальное раскрытие изобретения
Согласно данному изобретению способ получения карминомицина с использованием в качестве исходного соединения даунорубицина включает следующие стадии.
I. Деметилирование даунорубицина или N-защищенного даунорубицина
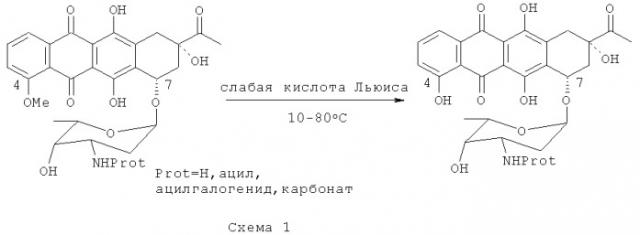
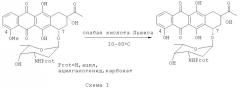
Реакцию деметилирования осуществляют путем обработки даунорубицина или N-защищенного даунорубицина (Формула 2 и Формула 3 соответственно) слабыми (мягкими) кислотами Льюиса, такими как TiHal4, ВHаl3, MgHal2, где Hal=F, Cl, Br, I, в безводных растворителях, таких как алканы, циклоалканы, арены, галогеноалканы, простые эфиры, CS2, все из которых являются устойчивыми в кислотах Льюиса при температурах в интервале примерно 10-80°С (как показано на Схеме 1).
При использовании N-защищенного даунорубицина реакция завершается с меньшим количеством побочных продуктов (примесей) и с большим выходом.
Количество кислоты Льюиса, используемой в реакции, составляет 1-5 моль на 1 моль даунорубицина, предпочтительно 1.5-3 моля.
Температура проведения реакции зависит от силы кислоты Льюиса и должна обеспечивать максимальную региоселективность процесса, включающего расщепление связи 4-ОМе при сохранении связи 7-О-даунозоамин, и предпочтительно составляет 40-60°С.
Растворители, подходящие для проведения реакции, выбирают исходя из тех же принципов, что и при выборе температуры. Предпочтение отдается галогеноалканам, простым эфирам и CS2.
Экстракцию карминомицина или N-защищенного карминомицина осуществляют путем обработки реакционной массы водным раствором сильных органических кислот, таких как щавелевая кислота, трифторуксусная кислота, или тиках минеральных кислот, как серная кислота или соляная кислота, рН 2.5±1. После разрушения реакционного комплекса карминомицина с кислотами Льюиса реакционную массу (в случае использования растворимых в воде простых эфиров) экстрагируют нерастворимыми в воде (гидрофобными) органическими растворителями, такими как галогеноалканы, циклоалканы, арены, С4-С6 спирты и их смеси. Карминомицин может быть экстрагирован в виде основания.
3'N-защитную группу (3'N-Prot-rpynny) в случае использования N-защищенного даунорубицина удаляют сразу после завершения синтеза или после дальнейшей модификации 4-R заместителя в зависимости от целей синтеза.
Пример
6.25 грамм N-трифторацетилдаунорубицина растворяют в 150 мл тетрагидрофурана и медленно добавляют 2.9 грамм безводного хлорида магния в условиях, исключающих контакт с влагой атмосферы. Полученную смесь инкубируют при 40°С в течение 1.5 часов, затем выливают в ледяную воду, титруют до рН 2.5 трифторуксусной кислотой и затем экстрагируют дихлорметаном (2 раза аликвотами по 50 мл). Органический слой отделяют и сушат безводным MgSO4. Затем растворитель упаривают при давлении ниже атмосферного. В результате получают 4.8 грамма N-TFA-карминомицина с чистотой порядка 65-80% (подтверждено жидкостной хроматографией высокого давления, HPLC).
N-TFA-карминомицин, полученный описанным выше способом, затем суспендируют в 200 мл дистиллированной воды при температуре 30°С и добавляют 15 мл 1.0 N раствора NaOH. Смесь инкубируют в течение 30 минут, а затем нейтрализуют до рН 7 раствором соляной кислоты, после чего подвергают препаративной хроматографии. После упаривания элюата получают 3.0-3.8 грамм карминомицина с чистотой около 96% (подтверждено HPLC).
1. Способ получения антрациклина карминомицина, представленного формулой (1): из антрациклина даунорубицина, включающий следующие стадии:взаимодействие даунорубицина, представленного формулой (2), или N-защищенного даунорубицина, представленного формулой (3): со слабой кислотой Льюиса, выбранной из группы, включающей TiHal4, BHal3, MgHal2, где Hal - F, Cl, Вr, I, для деметилирования 4-метокси группы даунорубицина, представленного формулой 2, или N-защищенного даунорубицина, представленного формулой 3, с получением реакционной массы.
2. Способ по п.1, отличающийся тем, что реакцию проводят используя растворитель, выбранный из группы, включающей безводные алканы, циклоалканы, арены, галогеноалканы, простые эфиры и CS2.
3. Способ по п.1, отличающийся тем, что реакцию проводят при температуре от примерно 10 до примерно 80°С в течение от 1 до 10 ч.
4. Способ по п.1, дополнительно включающий стадии:обработку реакционной массы водным раствором сильной органической или неорганической кислоты; иэкстракцию карминомицина в виде основания из обработанной реакционной массы с помощью не растворимого в воде органического растворителя.
5. Способ по п.4, отличающийся тем, что одна из сильных органических кислот или неорганических кислот выбрана из группы, включающей серную кислоту или соляную кислоту.
6. Способ по п.4, отличающийся тем, что не растворимый в воде органический растворитель включает один из галогеноалканов, циклоалканов, аренов, C4-C6 спиртов или их смесь.