Способ получения 2-(3-феноксифенилзамещенных)бензимидазолов
Иллюстрации
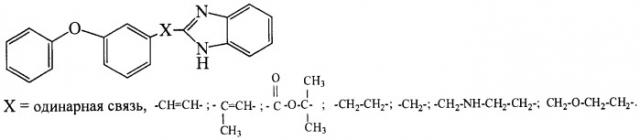
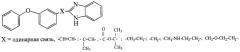
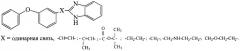
Показать всеНастоящее изобретение относится к органической химии, а именно к способу получения производных бензимидазолов формулы
который заключается во взаимодействии нитрилов, выбранных из ряда: 3-феноксибензонитрила, 3-феноксифенилацетонитрила, 3-(3-феноксифенил)акрилонитрила, 3-(3-феноксифенил)-2-бутенонитрила, 3-(3-феноксифенил)пропионитрила, 3-(3-феноксибензиламино)пропионитрила, 2-метил-2-(3-феноксибензоат)пропионитрила, 3-феноксифенилметоксипропионитрила с гидрохлоридом орто-фенилендиамина в запаянной стеклянной ампуле. При этом процесс проводят при мольном соотношении нитрила и гидрохлорида о-фенилендиамина, равном 1:1,2, при температуре 190-200°С. Технический результат: разработан новый способ получения 2-(3-феноксифенилзамещенных)бензимидазолов с хорошим выходом, высокой степенью чистоты. 1 з.п. ф-лы.
Реферат
Предлагаемое изобретение относится к химии производных бензимидазолов, в частности к способу получения 2-(3-феноксифенилзамещенных)бензимидазолов общей формулы
которые являются новыми по структуре 3-феноксифенилсодержащими соединениями и могут представлять интерес в качестве полупродуктов в синтезе биологически активных веществ. Анализ литературных источников и работа с патентными базами показали, что гетероциклические соединения, молекулы которых содержат дифенилоксидный фрагмент, являются перспективными биологически активными веществами и проявляют ряд фармакологических свойств.
Так перметрин [(3-феноксифенил)метиловый эфир 3-(2,2-дихлорэтенил)-2,2-диметилциклопропанкарбоновой кислоты; смесь цис- и транс-изомеров (3:1)] и фенотрин [2,2-диметил-3-(2-метил-1-пропенил)циклопропан-карбоновой кислоты (3-феноксифенил)метиловый эфир] используются как лекарственные препараты, обладающие противопаразитарным, противопедикулезным, инсектицидным, овоцидным фармакологическим действием. Имеются примеры использования феноксифенилацетиленов, полученных на основе 1-(2-метил-4-феноксифенил)этанона и 1-(3-феноксифенил)этанона, в качестве противотромботических, противовоспалительных, жаропонижающих агентов и анальгетиков [Химическая энциклопедия: В 5 т.: Т.5 / Ред. кол.: Кнунянц И.Л. и др. - М.: Большая Российская энцикл., 1992. - 639 с.].
Интересен класс бензимидазолов, сам бензимидазол обладает аналитическим действием, причем превышает по силе действия фармпрепарат анальгин [Т.В.Гамма, И.И.Коренюк // Ученые записки Таврического национального университета им. В.И.Вернадского, серия «Биология, химия». Том 23 (62). 2010. №2. С.66-71].
Производные бензимидазола обладают фунгицидной активностью, например препарат «Фундазол» [B.C.Пилюгин, С.Л.Кузнецова // Журнал общей химии. Том 78. 2008. №3. С.461-466].
Бензимидазолы являются хорошо известным классом противогельминтных агентов, которые широко используют для борьбы с эндопаразитами, особенно с нематодами, у домашних и сельскохозяйственных животных. Альбендазол показан для использования применительно к людям [Пат. РФ №2121837, А61К 31/415, А61К 31/34, A01N 43/30, A01N 43/90, 20.11.1998].
Известен способ получения производных бензимидазола, заключающийся во взаимодействии аминопроизводных, например 4-гидрокси-5-амино-фталонитрила с карбоновыми кислотами и их ангидридами [М.Н.Воронько, С.В.Воронов // Известия высших учебных заведений. Химия и химическая технология. 2008, №4. Т.51. С.54-55].
Недостатком данного метода является использование большого избытка кислоты (1:25), что в нашем случае невозможно из-за высокой себестоимости соединений, содержащих 3-феноксифенильный фрагмент.
Данный метод не приводит к получению вещества заявляемой структурной формулы.
Известен также способ получения бензимидазолов конденсацией нитрилов с орто-фенилендиаминами в присутствии кислот [Edward L. Holljes, Jr. and E.C.Wagner / J. Org. Chem., 1944, 09 (1), p.31-49].
Данный метод также не приводит к получению вещества заявляемой структурной формулы.
Задачей предлагаемого изобретения является разработка технологичного малостадийного метода синтеза 2-(3-феноксифенилзамещенных)бензимидазолов с хорошим выходом и высокой степенью чистоты.
Техническим результатом является расширение ассортимента химических соединений, в частности получение новых 2-(3-феноксифенилзамещенных)бензимидазолов с хорошими выходами, высокой степенью чистоты.
Поставленный технический результат достигается в способе получения 2-(3-феноксифенилзамещенных)бензимидазолов общей формулы
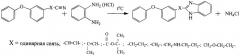
заключающийся во взаимодействии нитрилов, выбранных из ряда: 3-феноксибензонитрила, 3-феноксифенилацетонитрила, 3-(3-феноксифенил)акрилонитрила, 3-(3-феноксифенил)-2-бутенонитрила, 3-(3-феноксифенил)пропионитрила, 3-(3-феноксибензиламино)пропионитрила, 2-метил-2-(3-феноксибензоат)пропионитрила, 3-феноксифенилметоксипропионитрила с гидрохлоридом орто-фенилендиамина в запаянной стеклянной ампуле. При этом процесс проводят при мольном соотношении нитрила и гидрохлорида орто-фенилендиамина, равном 1:1,2, при температуре 190-200°С.
Сущностью метода является реакция взаимодействия гидрохлорида орто-фенилендиамина с нитрилами, выбранными из ряда: 3-феноксибензонитрила, 3-феноксифенилацетонитрила, 3-феноксифенилакрилонитрила, 3-(3-феноксифенил)-2-бутенонитрила, 3-(3-феноксифенил)пропионитрила, 3-(3-феноксибензиламино)пропионитрила, 2-метил-2-(3-феноксибензоат)пропионитрила, 3-феноксифенилметоксипропионитрила.
Способ осуществляется следующим образом.
Смесь гидрохлорида орто-фенилендиамина и нитрила, содержащего 3-феноксифенильный фрагмент, нагревают в запаянной стеклянной ампуле в течение 5-7 часов при температуре 190-200°С.
Реакционную массу растирают в ступке и нагревают в круглодонной колбе с 5% раствором соляной кислоты в течение 1 часа. Раствор фильтруют, в фильтрат добавляют аммиачную воду, при этом раствор меняет цвет с синего на фиолетовый и выпадает осадок. Далее смесь фильтруют на фильтре Шотта и сушат. 2-(3-Феноксифенилзамещенные)бензимидазолы перекристаллизовывают из абсолютного этанола.
Выход данных продуктов после выделения 52-68%.
Как показали проведенные исследования, оптимальным и технологичным условием проведения реакции является ее осуществление в массе исходных реагентов при мольном соотношении нитрил: гидрохлорид орто-фенилендиамина 1:1,2. Меньший избыток гидрохлорида орто-фенилендиамина приводил к некоторому снижению выхода целевого продукта за счет неполной конверсии нитрильного соединения. Дальнейшее увеличение избытка гидрохлорида орто-фенилендиамина не влияло на выход 2-(3-феноксифенилзамещенных)бензимидазолов и являлось нецелесообразным.
Оптимальной температурой реакции является 190-200°С. Снижение температуры до комнатной приводит к сильному увеличению продолжительности данного взаимодействия и снижению выхода целевого продукта.
Пример 1. 2-(3-феноксифенил)бензимидазол.
Смесь 4,5 г (0,03 моль) гидрохлорида орто-фенилендиамина и 5 г (0,026 моль) 3-феноксибензонитрила нагревают в запаянной стеклянной ампуле в течение 5-7 часов при температуре 190-200°С.
Реакционную массу растирают в ступке и нагревают в круглодонной колбе с 5% раствором соляной кислоты в течение 1 часа. Раствор фильтруют, в фильтрат добавляют аммиачную воду, при этом раствор меняет цвет с синего на фиолетовый и выпадает осадок. Далее смесь фильтруют на фильтре Шотта и сушат и перекристаллизовывают из абсолютного этанола.
Выход - 5,01 г (0,018 моль, 68%). Т. пл. 170-173°С. Спектр ЯМР 1Н, δ, м.д.: 7,17-7,74 м (13Н, С6Н5ОС6Н4, CH4), 4,65 (1Н, NH). Найдено, %: С 79.72; N 9.83; Н 4.89. C19H14N2O. Вычислено, %: С 79.70; N 9.80; Н 4.90.
Пример 2. 2-(3-феноксифенилацето)бензимидазол.
Смесь 4,2 г (0,03 моль) гидрохлорида орто-фенилендиамина и 5 г (0,024 моль) 3-феноксифенилацетонитрила нагревают в запаянной стеклянной ампуле в течение 5-7 часов при температуре 190-200°С.
Реакционную массу растирают в ступке и нагревают в круглодонной колбе с 5% раствором соляной кислоты в течение 1 часа. Раствор фильтруют, в фильтрат добавляют аммиачную воду, при этом раствор меняет цвет с синего на фиолетовый и выпадает осадок. Далее смесь фильтруют на фильтре Шотта и сушат и перекристаллизовывают из абсолютного этанола.
Выход - 4,46 г (0,015 моль, 62%). Т. пл. 177-180°С. Спектр ЯМР 1Н, δ, м.д.: 7,17-7,74 м (13Н, С6Н5ОС6Н4, С6Н4,), 3,81 с (-СН2-), 4,68 (1Н, NH).
Найдено, %: С 80.04; N 9.29; Н 5.35. C2OH16N2O. Вычислено, %: С 80.00; N 9.33; Н 5.33.
Пример 3. 2-(3-феноксифенилакрило)бензимидазол.
Смесь 4 г (0,027 моль) гидрохлорида орто-фенилендиамина и 5 г (0,023 моль) 3-феноксифенилакрилонитрила нагревают в запаянной стеклянной ампуле в течение 5-7 часов при температуре 190-200°С.
Реакционную массу растирают в ступке и нагревают в круглодонной колбе с 5% раствором соляной кислоты в течение 1 часа. Раствор фильтруют, в фильтрат добавляют аммиачную воду, при этом раствор меняет цвет с синего на фиолетовый и выпадает осадок. Далее смесь фильтруют на фильтре Шотта и сушат и перекристаллизовывают из абсолютного этанола.
Выход - 4,74 г (0,015 моль, 66%). Т. пл. 190-192°С. Спектр ЯМР 1Н, δ, м.д.: 7,17-7,74 м (13Н, С6Н5ОС6Н4, С6Н4). 6,96-7,00 д (1Н, Ar-СН); 5,62-5,67 д (1Н, CH-CN), 4,75 (1H, NH). Найдено, %: С 80.78; N 9.01; Н 5.17. C21H16N2O. Вычислено, %: С 80.77; N 9.00; Н 5.13.
Пример 4. 2-(3-(3-феноксифенил)-2-бутенил)бензимидазол.
Смесь 3,7 г (0,0255 моль) гидрохлорида орто-фенилендиамина и 5 г (0,021 моль) 3-(3-феноксифенил)-2-бутенонитрила нагревают в запаянной стеклянной ампуле в течение 5-7 часов при температуре 190-200°С.
Реакционную массу растирают в ступке и нагревают в круглодонной колбе с 5% раствором соляной кислоты в течение 1 часа. Раствор фильтруют, в фильтрат добавляют аммиачную воду, при этом раствор меняет цвет с синего на фиолетовый и выпадает осадок. Далее смесь фильтруют на фильтре Шотта и сушат и перекристаллизовывают из абсолютного этанола.
Выход - 3,7 г (0,011 моль, 54%). Т. пл. 200-202°С. Спектр ЯМР 1Н, δ, м.д.: 7,17-7,74 м (13Н, С6Н5ОС6Н4, С6Н4), 6,62 с (1Н, CH-CN), 2,42 с (3Н, СН3), 4,28 (1Н, NH). Найдено, %: С 80.97; N 8.59; Н 5.51. C22H18N2O. Вычислено, %: С 80.98; N 8.59; Н 5.52.
Пример 5. 2-(3-(3-феноксифенил)пропио)бензимидазол.
Смесь 3,9 г (0,0275 моль) гидрохлорида орто-фенилендиамина и 5 г (0,0224 моль) 3-(3-феноксифенил)пропионитрила нагревают в запаянной стеклянной ампуле в течение 5-7 часов при температуре 190-200°С.
Реакционную массу растирают в ступке и нагревают в круглодонной колбе с 5% раствором соляной кислоты в течение 1 часа. Раствор фильтруют, в фильтрат добавляют аммиачную воду, при этом раствор меняет цвет с синего на фиолетовый и выпадает осадок. Далее смесь фильтруют на фильтре Шотта и сушат и перекристаллизовывают из абсолютного этанола.
Выход - 3,95 г (0,0125 моль, 56%). Т. пл. 195-197°С. Спектр ЯМР 1Н, δ, м.д.: 7,14-7,70 м (13Н, С6Н5ОС6Н4, С6Н4); 2,81-2,86 т (2Н, Ar-СН2); 3,42-3,49 т (2Н, CH2-CN), 4,88 (1Н, NH). Найдено, %: С 80.27; N 8.94; Н 5.71. C21H18N2O. Вычислено, %: С 80.25; N 8.92; Н 5.73.
Пример 6. 2-(3-(3-феноксибензиламино)пропио)бензимидазол.
Смесь 3,45 г (0,0238 моль) гидрохлорида орто-фенилендиамина и 5 г (0,02 моль) 3-(3-феноксибензиламино)пропионитрила нагревают в запаянной стеклянной ампуле в течение 5-7 часов при температуре 190-200°С.
Реакционную массу растирают в ступке и нагревают в круглодонной колбе с 5% раствором соляной кислоты в течение 1 часа. Раствор фильтруют, в фильтрат добавляют аммиачную воду, при этом раствор меняет цвет с синего на фиолетовый и выпадает осадок. Далее смесь фильтруют на фильтре Шотта и сушат и перекристаллизовывают из абсолютного этанола.
Выход - 4,1 г (0,012 моль, 60%). Т. пл. 207-210°С. Спектр ЯМР 1H, δ, м.д.: 6,89-7,70 м (13Н, С6Н5ОС6Н4, С6Н4) 8,2 с (N-H), 3,6 д (2Н, Ar-СН2-N) 2,2 т (2Н, СН2), 2,7 т (2Н, СН2), 4,93 (1Н, NH). Найдено, %: С 80.45; N 12.29; Н 6.09. C22H21N3O. Вычислено, %: С 80.47; N 12.24; Н 6.12.
Пример 7. 2-(3-феноксифенилметоксипропио)бензимидазол.
Смесь 3,45 г (0,0238 моль) гидрохлорида орто-фенилендиамина и 5 г (0,02 моль) 3-феноксифенилметоксипропионитрила нагревают в запаянной стеклянной ампуле в течение 5-7 часов при температуре 190-200°С.
Реакционную массу растирают в ступке и нагревают в круглодонной колбе с 5% раствором соляной кислоты в течение 1 часа. Раствор фильтруют, в фильтрат добавляют аммиачную воду, при этом раствор меняет цвет с синего на фиолетовый и выпадает осадок. Далее смесь фильтруют на фильтре Шотта и сушат и перекристаллизовывают из абсолютного этанола.
Выход - 3,47 г (0,01 моль, 52%). Т. пл. 193-195°С. Спектр ЯМР 1Н, δ, м.д.: 7,04-7,72 м (13Н, С6Н5ОС6Н4, С6Н4); 4,2 с (2Н, Ar-СН2-O), 3,32-3-36 т (2Н, СН2), 2,13-2,27 т (2Н, CH2-CN), 5,02 (1Н, NH). Найдено, %: С 80.22; N 8.16; Н 6.12. C22H21N2O2. Вычислено, %: С 80.23; N 8.14; Н 6.10.
Пример 8. 2-(2-метил-2-(3-феноксибензоат)пропио)бензимидазол.
Смесь 3,1 г (0,0216 моль) гидрохлорида орто-фенилендиамина и 5 г (0,018 моль) 2-метил-2-(3-феноксибензоат)пропионитрила нагревают в запаянной стеклянной ампуле в течение 5-7 часов при температуре 190-200°С.
Реакционную массу растирают в ступке и нагревают в круглодонной колбе с 5% раствором соляной кислоты в течение 1 часа. Раствор фильтруют, в фильтрат добавляют аммиачную воду, при этом раствор меняет цвет с синего на фиолетовый и выпадает осадок. Далее смесь фильтруют на фильтре Шотта и сушат и перекристаллизовывают из абсолютного этанола.
Выход - 3,48 г (0,009 моль, 52%). Т. пл. 233-234°С. Спектр ЯМР 1Н, δ, м.д.: 6,84-7,2 м (13Н, С6Н5ОС6Н4, С6Н4); 1,8 с (6Н, СН3), 4,98 (1Н, NH). Найдено, %: С 70.95; N 7.50; Н 5.38. C23H20N2O3. Вычислено, %: С 70.97; N 7.53; Н 5.38.
Выводы
Предлагаемый способ позволяет получить 2-(3-феноксифенилзамещенные)бензимидазолы в одну стадию с хорошими выходами. К его достоинствам можно отнести препаративную простоту синтеза и легкость выделения целевых продуктов с высокой степенью чистоты. Структура синтезированных соединений подтверждена масс-, ЯМР 1Н-спектроскопией и элементным анализом.
1. Способ получения 2-(3-феноксифенилзамещенных)бензимидазолов формулы заключающийся во взаимодействии нитрилов, выбранных из ряда: 3-феноксибензонитрила, 3-феноксифенилацетонитрила, 3-(3-феноксифенил)акрилонитрила, 3-(3-феноксифенил)-2-бутенонитрила, 3-(3-феноксифенил)пропионитрила, 3-(3-феноксибензиламино)пропионитрила, 2-метил-2-(3-феноксибензоат)пропионитрила, 3-феноксифенилметоксипропионитрила с гидрохлоридом орто-фенилендиамина в запаянной стеклянной ампуле.
2. Способ по п.1, отличающийся тем, что процесс проводят при мольном соотношении нитрила и гидрохлорида орто-фенилендиамина, равном 1:1,2, при температуре 190-200°С.