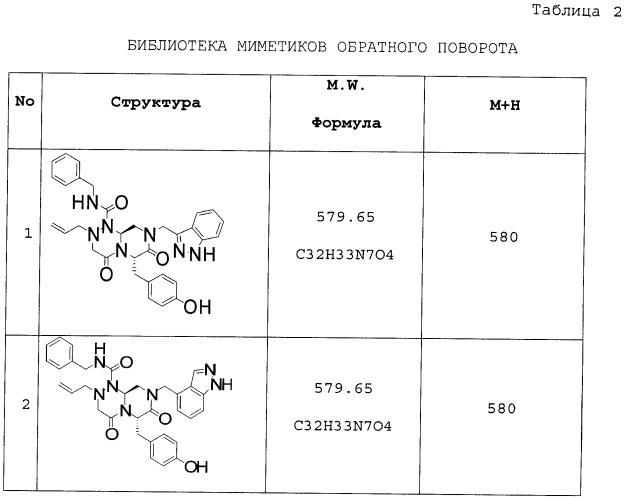
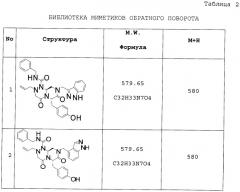
Новые соединения миметики обратного поворота и их применение
Иллюстрации
Показать всеОписываются новые соединения общей Формулы (I):
в виде отдельного стереоизомера или смеси стереоизомеров или в виде его фармацевтически приемлемой соли, где
R1 - индазолил или замещенный индазолил;
R6 - С6арил или С6-12арил, замещенный галогеном, гидрокси, циано и C1-6алкокси; или С6гетероциклил, содержащий 1-2 гетероатома, выбранных из азота или кислорода;
каждый из X2 и Х3 независимо означает водород, гидрокси или фосфат. Данные соединения могут быть использованы для получения лекарственного препарата для лечения или предотвращения рака, в частности острой миелоидной лейкемии. 5 з.п. ф-лы, 6 табл., 8 прим., 4 ил.
Реферат
Область техники
Настоящее изобретение в основном относится к новым соединениям миметикам обратного поворота и их применению в лечении медицинских патологических состояний, например раковых заболеваний, и фармацевтическим композициям, содержащим миметики.
Уровень техники
Многие годы проводился бессистемный скрининг молекул на предмет возможной активности в качестве терапевтических агентов и привел к открытию ряда важных лекарственных средств. Несмотря на то что достижения в молекулярной биологии и вычислительной химии породили повышенный интерес к тому, что было определено понятием «направленное проектирование лекарственных средств», подобные методики оказались не такими быстрыми и надежными, как первоначально ожидалось. Таким образом, в последние годы возобновился интерес к бессистемному скринингу лекарственных средств и к нему вернулись. В связи с этим были сделаны большие успехи в новых технологиях, основанных на разработке библиотек комбинаторной химии и скрининге подобных библиотек в поисках биологически активных членов.
Первоначально библиотеки комбинаторной химии были в основном ограничены членами пептидного или нуклеотидного происхождения.
Несмотря на то что комбинаторные библиотеки, содержащие члены пептидного и нуклеотидного происхождения, имеют огромное значение, все же на данном уровне техники остается необходимость в библиотеках, содержащих члены другого происхождения. Например, в классических пептидных библиотеках для получения членов библиотеки в основном просто варьируется аминокислотная последовательность. Хотя общепризнано, что вторичные структуры пептидов имеют большое значение с точки зрения биологической активности, подобные пептидные библиотеки не обеспечивают своим членам устойчивую вторичную структуру.
В связи с этим некоторые исследователи циклизовали пептиды при помощи дисульфидных мостиков в попытке обеспечить более устойчивую вторичную структуру (Tumelty et al., J. Chem. Soc. 1067-68, 1994; Eichler et al., Peptide Res. 7:300-306, 1994). Однако подобные циклизованные пептиды обычно все же остаются достаточно лабильными и в малой степени биодоступными и, таким образом, достигают лишь скромного успеха.
Совсем недавно были разработаны непептидные соединения, которые более подробно имитируют вторичную структуру обратных поворотов, обнаруженные в биологически активных белках или пептидах. Например, патент США № 5440013 автора Kahn и опубликованные заявки PCT № WO 94/03494, WO 01/00210A1 и WO 01/16135A2 автора Kahn, каждая, раскрывают конформационно устойчивые, непептидные соединения, которые имитируют трехмерную структуру обратных поворотов. Кроме того, патент США № 5929237 и его частичное продолжение патент США № 6013458, оба автора Kahn, раскрывают конформационно устойчивые соединения, которые имитируют вторичную структуру областей обратных поворотов биологически активных пептидов и белков. Синтез и определение конформационно устойчивых миметиков обратного поворота и их применение для лечения заболеваний подробно рассмотрены в Obrecht (Advances in Med. Chem., 4, 1-68, 1999).
Несмотря на то что в синтезе и определении конформационно устойчивых миметиков обратного поворота были сделаны значительные успехи, на данном уровне техники остается необходимость в небольших молекулах, которые имитируют вторичную структуру пептидов. Также на данном уровне техники существует необходимость в библиотеках, содержащих подобные члены, а также методиках синтеза и скрининга членов библиотеки, которые являются важными объектами, особенно биологическими объектами, для того чтобы идентифицировать биологически активные члены библиотеки.
Между тем, протоонкоген представляет собой нормальный ген, который может стать онкогеном в результате мутаций или повышенной экспрессии. c-Myc (MYC) известен как один из протоонкогенов, и дисрегуляцию c-Myc считают одним из серии онкогенных событий, необходимых для онкогенеза у млекопитающих (Pelengaris S., Khan M. The many faces of c-MYC. Arch Biochem Biophys. 2003; 416:129-136). Также было обнаружено, что дисрегуляция MYC, посредством многообразия механизмов, связана с миелоидной лейкемией (Hoffman B., Amanullah A., Shafarenko M., Liebermann D. A. The proto-oncogene c-Myc in hematopoietic development and leukemogenesis, Oncogene. 2002; 21:3414-3421). Кроме того, было обнаружено, что c-Myc быстро вызывает острую миелоидную лейкемию (Hui Luo et al. "c-Myc rapidly induces acute myeloid leukemia in mice without evidence of lymphoma-associated antiapoptotic mutations", Blood, 1 October 2005, volume 106, Number 7, p. 2452-2461).
Поскольку экспрессия c-Myc может быть активирована при острой миелоидной лейкемии, исследовали онкогенное действие c-Myc и изучили его точную роль в миелоидном лейкомогенезе. Совсем недавно некий ученый обнаружил, что Myc преимущественно стимулирует рост миелоидных клеток-предшественников в метилцеллюлозе, и показал, что Myc представляет собой критический нижележащий эффектор миелоидного лейкомогенеза (из того же источника).
Открытие того факта, что c-Myc играет критическую роль в миелоидном лейкомогенезе, означает, что посредством ингибирования активации белка c-Myc можно лечить или предотвращать острую миелоидную лейкемию.
С другой стороны, ферменты суперсемейства цитохрома P450 (CYP) являются основными определяющими факторами периода полувыведения и обеспечивают фармакологические эффекты многих терапевтических лекарственных средств. Подсемейство человеческого цитохрома P450 (CYP) 3A включает CYP3A4, который наиболее распространен в печени человека (~40%), и метаболизирует более 50% клинически применяемых лекарственных средств (Shimada et al. 1994; Rendic and Di Carlo, 1997). В связи с ключевой ролью CYP3A4 в метаболизме лекарственных средств значительная инактивация данного фермента могла бы привести к выраженным фармакокинетическим межлекарственным взаимодействиям. Ингибирование CYP3A4 может стать причиной сильной лекарственной токсичности из-за повышенного подвергания действию совместно вводимых лекарств (Dresser et al. 2000). Например, при совместном введении необратимых ингибиторов CYP3A4, таких как эритромицин или кларитромицин, с терфенадином, астемизолом или пимозидом у пациентов может начаться двунаправленная тахикардия (опасная для жизни желудочковая аритмия, связанная с удлинением интервала QT) (Spinler et al. 1995; Dresser et al. 2000). Пациенты с раковыми заболеваниями порой подвергаются множеству терапий, что увеличивает опасность межлекарственных взаимодействий, в результате которых появляются неблагоприятные побочные реакции.
Следовательно, при разработке терапевтических агентов, особенно когда их нужно водить в комбинации с другими лекарственными средствами, существует необходимость обеспечить соединения, имеющие слабую CYP3A4 ингибирующую активность.
Сущность изобретения
Целью настоящего изобретения является создание новых соединений, которые имитируют вторичную структуру областей обратных поворотов биологически активных пептидов и белков и имеют биологическую активность, такую как противораковый эффект.
Другой целью настоящего изобретения является обеспечение новых соединений, которые ингибируют Wnt передачу сигнала.
Еще одной целью настоящего изобретения является обеспечение новых соединений, которые можно применять в качестве лекарственных препаратов, в частности, имеющих слабую CYP3A4 ингибирующую активность (более высокий IC50).
Еще одной целью настоящего изобретения является обеспечение новых соединений для лечения или предотвращения острой миелоидной лейкемии посредством регуляции, уменьшающей экспрессию c-Myc.
Настоящее изобретение относится к новому типу конформационно устойчивых соединений и их производных, в том числе пролекарств, которые имитируют вторичную структуру областей обратных поворотов биологически активных пептидов и белков. Данное изобретение также раскрывает библиотеки, содержащие подобные соединения, а также их синтез и скрининг. Соединения по настоящему изобретению имеют следующую общую формулу (I):
,
в которой E представляет собой -ZR3- или -(C=O)-, при этом Z представляет собой CH или N; W представляет собой -(C=O)-, -(C=O)NH-, -(C=O)O-, -(C=O)S-, -S(O)2- или простую связь; а каждый из R1, R2, R3, R4 и R5 являются одинаковыми или различаются и независимо представляют собой функциональную группу аминокислотной боковой цепи или производное аминокислотной боковой цепи. Соединение, имитирующее обратный поворот, может находиться в виде отдельного стереоизомера, или смеси стереоизомеров, или в виде их фармацевтически приемлемой соли.
В некоторых вариантах осуществления R1 соединений формулы (I) представляет собой индазолил или замещенный индазолил.
Конкретные примеры R1, R2, R3, R4 и R5 приведены в нижеследующем подробном описании.
В варианте осуществления, в котором E представляет собой CHR3, соединения по данному изобретению имеют следующую формулу (II):
,
в которой W представляет собой группу, определенную выше, а R1, R2, R3, R4 и R5 определены в нижеследующем подробном описании.
В некоторых вариантах осуществления соединения по данному изобретению имеют следующую общую формулу (III):
,
в которой R1, R4, R6, X1, X2 и X3 определены в нижеследующем подробном описании.
Настоящее изобретение также относится к пролекарствам с применением библиотек, содержащих одно или более соединений формулы (I). Обычно пролекарство предназначено для высвобождения активного лекарственного средства в организме в процессе или после абсорбции посредством ферментативного и/или химического гидролиза. Пролекарственный подход представляет собой эффективное средство улучшения пероральной биодоступности или в.в. (внутривенного) введения лекарственных средств, которые плохо растворяются в воде, посредством химического получения производных более водорастворимых соединений. Самым широко распространенным пролекарственным подходом для повышения водорастворимости лекарственных средств, содержащих гидроксильную группу, является получение сложных эфиров, содержащих ионогенную группу; например фосфатную группу, карбоксилатную группу, алкиламиногруппу (Fleisher et al., Advanced Drug Delivery Reviews, 115-130, 1996; Davis et al., Cancer Res., 7247-7253, 2002, Golik et al., Bioorg. Med. Chem. Lett., 1837-1842, 1996).
Примеры функциональной группы, которая может высвобождаться в организме, могут включать фосфат,
но могут применяться и любые другие функциональные группы, которые обычно применяют в качестве ионогенной группы в пролекарстве.
В некоторых вариантах осуществления пролекарства по настоящему изобретению имеют следующую общую формулу (IV):
,
в которой (III) представляет собой формулу (III), как описано выше; один из R1, R4, R6, X1, X2 и X3 связан с R7 через Y; Y представляет собой кислород, серу или азот в R1, R4 или R6, или кислород в X1, X2 или X3; а R7 представляет собой гидроксиалкил, гликозил, фосфорилоксиметилоксикарбонил, замещенную или незамещенную пиперидин карбонилоксигруппу или его соль; или Y-R7 представляет собой аминокислотный остаток, комбинацию аминокислотных остатков, фосфат, гемималат, гемисукцинат, диметиламиноалкилкарбамат, диметиламиноацетат или его соль; и в случае когда не связаны с R7: R1, R4, R6, X1, X2 и X3 определяются в нижеследующем подробном описании.
В некоторых вариантах осуществления пролекарства по настоящему изобретению могут служить в качестве субстрата для фосфатазы, карбоксилазы или других ферментов и превращаться с их помощью в соединения, имеющие общую формулу (III). Настоящее изобретение также относится к библиотекам, содержащим одно или более соединений формулы (I), приведенной выше, а также способам синтеза подобных библиотек и способам их скрининга с целью идентификации биологически активных соединений. Кроме того, в одном сопутствующем аспекте настоящее изобретение обеспечивает новые соединения, которые имеют слабую CYP3A4 ингибирующую активность. Настоящее изобретение также обеспечивает новые соединения, которые имеют ингибирующую активность по отношению к передаче сигнала Wnt. Настоящее изобретение также обеспечивает новые соединения, которые можно применять для получения лекарственного средства для лечения или профилактики острой миелоидной лейкемии.
Настоящее изобретение обеспечивает новые соединения миметики обратного поворота. Соединения по настоящему изобретению проявляют более слабую CYP3A4 ингибирующую активность (более высокий IC50), что дает возможность применять данные соединения в качестве потенциальных фармацевтических средств, особенно в случае, когда необходимо вводить их в комбинации с другими лекарственными средствами. Соединения по настоящему изобретению показали сильную ингибирующую активность по отношению к передаче сигнала Wnt. Данные соединения ингибировали рост раковых клеток ОМЛ (острой миелоидной лейкемии), и это можно применять в лечении или предотвращении острой миелоидной лейкемии.
Краткое описание чертежей
Здесь подробно будет сделана ссылка на предпочтительный вариант осуществления настоящего изобретения, примеры которого проиллюстрированы на чертежах, прилагаемых к данному документу. Варианты осуществления описаны ниже таким образом, чтобы объяснить настоящее изобретение путем ссылок на фигуры.
Фигура 1 раскрывает общую схему синтеза для получения миметиков обратного поворота по настоящему изобретению.
Фигура 2 показывает эффект исследуемых соединений (Соединения A, B и C) на CYP3A4 активность. Данный график основан на измерении IC50 для соединений по настоящему изобретению при анализе ингибирования CYP3A4, при котором ингибирование активности CYP3A4 измеряли при различных концентрациях данного соединения с целью получения значения IC50. Подробные процедуры раскрыты в Примере 1.
Фигура 3 показывает результаты измерения IC50 соединения D для клеток SW480 в биоанализе гена-репортера TopFlash.
Фигура 4 показывает ингибирование роста раковых клеток ОМЛ при помощи исследуемых соединений в зависимости от концентрации исследуемых соединений (Соединения A и C).
Предпочтительный вариант осуществления изобретения
Как применяется в данном описании и прилагаемой формуле изобретения, если не оговорено иное, приведенные ниже понятия имеют определенное значение.
"Амино" относится к -NH2 радикалу.
"Амидино" относится к -C(=NH)-NH2 радикалу. Один или оба атома водорода аминной группы амидино могут быть замещены одной или двумя алкильными группами, как определено в контексте данного документа. Алкил-производные амидино радикалы также называются "алкиламидино" и "диалкиламидино" соответственно.
"Циано" относится к -CN радикалу.
"Карбокси" относится к -COOR радикалу, в котором R представляет собой водород или алкил, как определено в контексте данного документа.
"Ацил" относится к -COR радикалу, в котором R представляет собой алкил, арил, циклоалкил, гетероциклил, как определено в контексте данного документа. Например, R может быть метилом, бутенилом, циклопропилом и тому подобным. Алкил или арил могут быть необязательно замещены заместителями, которые описаны для алкильной или арильной группы соответственно. Примерные ацильные группы включают без ограничения фенилацил, бензилацил, C1-6ацил (например, ацетил) и тому подобное.
"Алкилсульфонат" относится к -S(O)2-OR радикалу, в котором R представляет собой алкил, как определено в контексте данного документа.
"Амидосульфонат" относится к радикалу -OS(O)2-NR2, при этом каждый R независимо представляет собой водород или алкил. Примерные амидосульфонаты включают -OS(O)2NH2, -OS(O)2NHMe.
"Аминокарбонил" относится к радикалу -C(O)NR2, при этом каждый R независимо представляет собой водород, алкил, амино, циклоалкилалкил, гетероциклил, алкоксиалкил, гидроксиалкил, гидроксил, алкокси, арилалкил, гетероциклилалкил, или два R вместе с атомом азота, к которому они прикреплены, образуют гетероциклил, как определено в контексте данного документа. Если один из R представляет собой водород, то другой R представляет собой C1-4алкил, аминокарбонил может быть представлен "C1-4алкилформамидилом".
"N-формамидил" относится к радикалу -NHC(O)H.
"Фенилсульфонил" относится к -S(O)2-R радикалу, в котором R представляет собой фенил, фенил может быть дополнительно замещенным алкилом или хлором.
"Фенилсульфонат" относится к -O-S(O)2-R радикалу, в котором R представляет собой фенил, фенил может быть дополнительно замещенным алкилом или хлором.
"Алкилсульфонил" относится к -S(O)2-R радикалу, в котором R представляет собой алкил, как определено в контексте данного документа. Примерные алкилсульфонильные радикалы включают метилсульфонил.
"Алкилтио" относится к -SR радикалу, в котором R представляет собой алкил, как определено в контексте данного документа.
"Арилтио" относится к -SR радикалу, в котором R представляет собой арил, как определено в контексте данного документа. Арильная группа арилтио может быть дополнительно замещенной алкилом или хлором.
"Арилокси" относится к -OR радикалу, в котором R представляет собой арил, как определено в контексте данного документа. Арильная группа может быть дополнительно замещенной алкилом, алкокси и тому подобным.
"Ацилоксиалкил" относится к -R'-OC(O)-R радикалу, в котором R представляет собой алкил, арил, циклоалкил, гетероциклил, как определено в контексте данного документа; а R' представляет собой алкил.
"Гуанидино" относится к -NH-C(=NH)-NH2 радикалу. Один или оба атома водорода аминной группы гуанидино могут быть замещены одной или двумя алкильными группами, как определено в контексте данного документа. Алкилированные гуанидиновые радикалы также называются "алкилгуанидино" и "диалкилгуанидино" соответственно.
"Нитро" относится к -NO2 радикалу.
"Алкил" относится к радикалу с линейной или разветвленной углеводородной цепью, состоящему только из атомов углерода и водорода. Алкил может быть насыщенным (содержащим атомы углерода, связанные между собой только ординарными связями) или ненасыщенным (содержащим атомы углерода, связанные между собой, по крайней мере, одной двойной связью или тройной связью). Алкил, содержащий от одного до двенадцати атомов углерода, также называется "низшей алкильной группой" и может быть представлен "C1-12алкилом". В других вариантах осуществления алкил может содержать от одного до четырех атомов углерода и быть представлен "C1-4алкилом". В других вариантах осуществления алкил может содержать от двух до пяти атомов углерода и быть представлен "C2-5алкилом". Алкил присоединяется к остальной молекуле посредством ординарной связи. Примеры насыщенных алкилов включают без ограничения метил, этил, н-пропил, 1-метилэтил (изопропил), н-бутил, н-пентил, 1,1-диметилэтил (трет-бутил), 3-метилгексил, 2-метилгексил и тому подобное. Примеры ненасыщенных алкилов включают, без ограничения, этенил (т.е. винил), проп-1-енил (т.е. аллил), бут-1-енил, пент-1-енил, пента-1,4-диенил, этинил (т.е. ацетиленил), проп-1-инил и тому подобное.
Алкил может также представлять собой моноциклический или бициклический углеводородный кольцевой радикал, который может включать конденсированные или мостиковые кольцевые системы. Циклический алкил также называется "циклоалкилом". В некоторых вариантах осуществления циклоалкил может содержать от трех до шести атомов углерода и быть представлен "C3-6циклоалкилом". Примеры моноциклических циклоалкильных радикалов включают, например, циклопропил, циклобутил, циклопентил, циклогексил, циклогептил и циклооктил. Ненасыщенный циклоалкил содержит внутреннюю двойную связь (т.е. двойную связь в кольце). Примеры ненасыщенных циклоалкилов включают циклогексенил. Примеры бициклических циклоалкильных радикалов включают, например, норборнил (т.е. бицикло[2.2.1]гептил), 7,7-диметил-бицикло[2.2.1]гептил и тому подобное.
Если не установлено иначе конкретно в данном описании, то подразумевается, что понятие "алкил" включает как алкил, так и "замещенный алкил", который относится к алкильному радикалу, в котором один или более атомов водорода замещены одним или более заместителями, независимо выбранными из ацила, амидино, алкиламидино, диалкиламидино, алкокси, арила, циано, циклоалкила, гуанидино, алкилгуанидино, диалкилгуанидино, галогено, гетероциклила, гидразинила, гидроксила, нитро, -OC(O)-R11, -N(R11)2, -C(O)OR11, -C(O)N(R11)2, -N(R11)C(O)OR11, -N(R11)C(O)R11, -N(R11)S(O)tR11 (где t представляет собой 1 или 2), -S(O)tOR11 (где t представляет собой 1 или 2), -S(O)pR11 (где p представляет собой 0, 1 или 2) и -S(O)tN(R11)2 (где t представляет собой 1 или 2), при этом каждый R11 независимо представляет собой водород, алкил, арил, арилалкил, гетероциклил или гетероциклилалкил, как определено в контексте данного документа.
"Алкокси" относится к радикалу, представленному формулой алкил-O-, в которой алкил определен в контексте данного документа. Алкильная часть может быть дополнительно замещена одним или более галогеном. Алкоксигруппа также может быть представлена количеством атомов углерода в алкильной группе, например C1-6алкокси или C1-3алкокси.
"Арил" относится к радикалу, полученному из ароматической моноциклической или бициклической кольцевой системы посредством удаления атома водорода от кольцевого атома углерода. Ароматическая моноциклическая или бициклическая углеводородная кольцевая система содержит от шести до двенадцати атомов углерода (т.е. C6-12арил), при этом, по крайней мере, одно из колец в кольцевой системе является полностью ненасыщенным, т.е. она содержит циклическую, делокализованную (4n+2) π-электронную систему в соответствии с теорией Хюккеля. Необязательно один или два кольцевых атома арила могут быть гетероатомами, выбранными из азота, кислорода или серы. Примеры арильных радикалов включают, но не ограничиваются, фенил и нафтил. Если не установлено иначе конкретно в данном описании, то подразумевается, что понятие "арил" включает в себя как арил, так и "замещенный арил", который относится к арильному радикалу, в котором один или более атомов водорода замещены одним или более заместителями, независимо выбранными из алкила, ацила, амидино, амидосульфоната, алкокси, арилокси, циано, гуанидино, алкилгуанидино, диалкилгуанидино, галогено, гидразинила, гидроксила, нитро, гетероциклила, -OC(O)-R11, -N(R11)2, -C(O)OR11, -C(O)N(R11)2, -N(R11)C(O)OR11, -N(R11)C(O)R11, -N(R11)S(O)tR11 (где t представляет собой 1 или 2), -S(O)tOR11 (где t представляет собой 1 или 2), -S(O)pR11 (где p представляет собой 0, 1 или 2) и -S(O)tN(R11)2 (где t представляет собой 1 или 2), при этом каждый R11 независимо представляет собой водород, алкил, арил, арилалкил, гетероциклил или гетероциклилалкил.
"Арилалкил" относится к алкильному радикалу, в котором один или более атомов водорода алкила замещены одной или более арильными группами, как определено в контексте данного документа. В различных вариантах осуществления арилалкилы включают от 7 до 15 атомов углерода и могут быть представлены C7-15арилалкилом. В некоторых вариантах осуществления арилалкил представляет собой арилC1-4алкил, в котором C1-4алкил является замещенным одним арилом или двумя арильными группами, причем последний также называется "диарилалкилом" или "бисарилалкилом". Примеры арилC1-4алкила включают, но не ограничиваются, арилметил, арилэтил, арилпропил, арилбутил, бисарилметил, бисарилэтил, бисарилпропил, бисарилбутил. Примерные арилалкильные радикалы включают без ограничения бензил, нафтилметил, дифенилметил, 3,3-бисфенилпропил и тому подобное. Если не установлено иначе конкретно в данном описании, то подразумевается, что понятие "арилалкил" включает как арилалкил, так и "замещенный арилалкил", в котором алкильная часть и/или арильная часть арилалкильного радикала может быть замещена, как описано в контексте данного документа для алкильного радикала и арильного радикала соответственно.
"Циклоалкилалкил" относится к алкильному радикалу, в котором один или более атомов водорода алкила замещены одной или более циклическими группами, как определено в контексте данного документа. В некоторых вариантах осуществления циклоалкилалкил представляет собой циклоалкилC1-2алкил, такой как циклоалкилметил, циклоалкилэтил и тому подобное. Примерные циклоалкилалкильные радикалы включают без ограничения циклогексилалкил (например, циклогексилметил и циклогексилэтил) и циклопентилалкил (например, циклопентилметил и циклопентилэтил) и тому подобное. Если не установлено иначе конкретно в данном описании, то подразумевается, что понятие "циклоалкилалкил" включает в себя как циклоалкилалкил, так и "замещенный циклоалкилалкил", в котором алкильная часть и/или циклоалкильная часть циклоалкилалкильного радикала могут быть замещены, как описано в контексте данного документа для алкильного радикала и циклоалкильного радикала соответственно.
"Гликозил" относится к радикалу, полученному посредством удаления полуацетальной гидроксильной группы из циклической формы моносахарида (например, глюкозы), дисахарида, олигосахарида (содержащего от трех до десяти моносахаридов) или полисахарида (содержащего более десяти моносахаридов).
"Галогено" или "галоген" относится к фторным, хлорным, бромным или йодным радикалам.
"Галогеналкил" относится к алкильному радикалу, как определено в контексте данного документа, который замещен одним или более галогеновыми радикалами, как определено в контексте данного документа. Примерные галогеналкилы включают без ограничения трифторметил, дифторметил, трихлорметил, 2,2,2-трифторэтил, 1-фторметил-2-фторэтил, 3-бром-2-фторпропил, 1-бромметил-2-бромэтил и тому подобное. Алкил, замещенный одним или более атомами фтора, также называется "перфторалкил", например "перфторC1-4алкил". Алкильная часть галогеналкильного радикала может быть необязательно замещена, как определено в контексте данного документа для алкильной группы.
"Гетероциклил" относится к устойчивому гетероциклическому кольцевому радикалу, который содержит от двух до одиннадцати атомов углерода и от одного до трех гетероатомов, выбранных из азота, кислорода и серы. В некоторых вариантах осуществления гетероциклил содержит один или два гетероатома. Если не установлено иначе конкретно в данном описании, то гетероциклильный радикал может быть моноциклической или бициклической кольцевой системой, которая может включать конденсированные или мостиковые кольцевые системы. В некоторых вариантах осуществления гетероциклил может быть 5-, 6- или 7-членным моноциклическим кольцом. В других вариантах осуществления гетероциклил может быть 8-, 9-, 10-, 11- или 12-членным конденсированным бициклическим кольцом. Гетероатомы в гетероциклильном радикале могут быть необязательно окисленными. Один или более атомов азота, если присутствуют, могут быть необязательно кватернизованы. Гетероциклильный радикал может быть неароматическим или ароматическим (т.е., по крайней мере, одно кольцо в гетероциклильном радикале имеет делокализованную (4n+2) π-электронную систему в соответствии с теорией Хюккеля). Гетероциклил может быть присоединен к остальной молекуле через любой атом кольца(ец). Примеры неароматических гетероциклильных радикалов включают, но не ограничиваются, диоксоланил, декагидроизохинолил, имидазолинил, имидазолидинил, изотиазолидинил, изоксазолидинил, морфолинил, октагидроиндолил, октагидроизоиндолил, 2-оксопиперазинил, 2-оксопиперидинил, 2-оксопирролидинил, оксазолидинил, пиперидинил (также называемый "пиперидил"), пиперазинил, 4-пиперидонил, 3-пирролинил, пирролидинил, пиразолидинил, хинуклидинил, тиазолидинил, тетрагидрофурил, тритианил, тетрагидропиранил, тиоморфолинил и тиаморфолинил. Примеры ароматических гетероциклильных радикалов включают, но не ограничиваются, азепинил, акридинил, бензимидазолил, бензиндолил, 1,3-бензодиоксолил, бензофуранил, бензооксазолил, бензоизоксазолил, бензо[d]тиазолил, бензотиадиазолил, бензо[b][1,4]диоксепинил, бензо[b][1,4]оксазинил, 1,4-бензодиоксанил, бензоксазолил, бензодиоксолил, бензодиоксинил, бензопиранил, бензопиразолил, бензофуранил, бензофуранонил, бензотиенил (бензотиофенил), бензотиено[3,2-d]пиримидинил, бензотриазолил, карбазолил, хромон, циннолинил, циклопента[d]пиримидинил, дибензофуранил, дибензотиофенил, фуранил, фуранонил, фуро[3,2-c]пиридинил, изотиазолил, имидазолил, индазолил, индолил, индазолил, изоиндолил, индолинил, изоиндолинил, изохинолил, индолизинил, изоксазолил, 5,8-метано-5,6,7,8-тетрагидрохиназолинил, нафтиридинил, 1,6-нафтиридинонил, оксадиазолил, 2-оксоазепинил, оксазолил, оксиранил, 5,6,6a,7,8,9,10,10a-октагидробензо[h]хиназолинил, феназинил, фенотиазинил, феноксазинил, фталазинил, птеридинил, пуринил, пирролил, пиразолил, пиразоло[3,4-d]пиримидинил, пиридинил (также называемый пиридил), пиридо[3,2-d]пиримидинил, пиридо[3,4-d]пиримидинил, пиразинил, пиримидинил, пиридазинил, пирролил, хиназолинил, хиноксалинил, хинолинил, изохинолинил, тетрагидрохинолинил, 1,2,3,4-тетрагидрокарбазолил, 5,6,7,8-тетрагидрохиназолинил, тиазолил, тиадиазолил, триазолил, тетразолил, триазин-2-ил, тиено[2,3-d]пиримидинил, тиено[3,2-d]пиримидинил, тиено[2,3-c]пиридинил и тиофенил (т.е. тиенил). Если не установлено иначе конкретно в данном описании, то подразумевается, что понятие "гетероциклил" включает в себя как гетероциклил, так и "замещенный гетероциклил", который относится к гетероциклильному радикалу, замещенному одним или более заместителями, выбранными из алкила, ацила, оксо (например, пиридинонила, пирролидонила), арила, арилалкила, ацилоксиалкила, амидино, алкокси, циано, гуанидино, алкилгуанидино, диалкилгуанидино, галогено, гидразинила, гидроксила, нитро, -OC(O)-R11, -N(R11)2, -C(O)OR11, -C(O)N(R11)2, -N(R11)C(O)OR11, -N(R11)C(O)R11, -N(R11)S(O)tR11 (где t представляет собой 1 или 2), -S(O)tOR11 (где t представляет собой 1 или 2), -S(O)pR11 (где p представляет собой 0, 1 или 2) и -S(O)tN(R11)2 (где t представляет собой 1 или 2), при этом каждый R11 независимо представляет собой водород, алкил, арил, арилалкил, гетероциклил или гетероциклилалкил.
"Гетероциклилалкил" относится к алкильному радикалу, в котором один или более атомов водорода алкила замещены одной или более гетероциклильными группами, как определено в контексте данного документа. Если гетероциклил представляет собой азот-содержащий гетероциклил, то такой гетероциклил может быть присоединен к алкильному радикалу при атоме азота. В некоторых вариантах осуществления алкильная часть гетероциклилалкила содержит 1-4 атома углерода и может быть представлена гетероциклилC1-4алкилом. Примеры гетероциклилалкильных радикалов включают без ограничения морфолинилалкил, такой как морфолинилметил, пиперидилалкил, такой как пиперидилметил, имидазолидинилалкил, такой как имидазолидинилметил и тому подобное. Дополнительные примеры гетероциклилалкильных радикалов, в которых гетероциклильная часть является ароматической, включают, но не ограничиваются, пиридилметил, пиридилэтил, пиридилпропил, пиридилбутил, хинолинилметил, хинолинилэтил, хинолинилпропил, хинолинилбутил, индазолилметил, индазолилэтил, индазолилпропил, индазолилбутил, бензпиразолилметил, бензпиразолилэтил, бензпиразолилпропил, бензпиразолилбутил, изохинолинилметил, изохинолинилэтил, изохинолинилпропил, изохинолинилбутил, бензотриазолилметил, бензотриазолилэтил, бензотриазолилпропил, бензотриазолилбутил и тому подобное. Если не установлено иначе конкретно в данном описании, то подразумевается, что понятие "гетероциклилалкил" включает в себя как гетероциклилалкил, так и "замещенный гетероциклилалкил", в котором алкильная часть и/или гетероциклильная часть гетероциклилалкильного радикала может быть замещена, как описано в контексте данного документа для алкильного радикала и гетероциклильного радикала соответственно.
Соединения или их фармацевтически приемлемые соли могут содержать один или более асимметрических центров и могут, таким образом, давать энантиомеры, диастереомеры и другие стереоизомерные формы, которые могут быть определены в рамках абсолютной стереохимии, как, например, (R)- или (S)- или как (D)- или (L)- для аминокислот. Когда соединения, описанные в контексте данного документа, содержат олефиновые двойные связи или другие центры геометрической асимметрии, и, если не установлено иное, предполагается, что данные соединения включают как E, так и Z геометрические изомеры (например, цис или транс). Аналогично предполагается, что также включены все возможные изомеры, а также их рацемические и оптически чистые формы и все таутомерные формы.
Подразумевается, что применяемое в контексте данного документа понятие "аминокислота" включает в себя природные α-аминокислоты и/или неприродные аминокислоты, такие как β-аминокислоты и гомоаминокислоты. Примеры аминокислот включают, но не ограничиваются, аланин, аргинин, аспарагин, аспарагиновую кислоту, цистеин, глутамин, глутаминовую кислоту, глицин, гистидин, изолейцин, лейцин, лизин, метионин, фенилаланин, пролин, серин, треонин, триптофан, тирозин, валин, фосфосерин, фосфотреонин, фосфотирозин, 4-гидроксипролин, гидроксилизин, десмозин, изодесмозин, гамма-карбоксиглутамат, гиппуровую кислоту, октагидроиндол-2-карбоновую кислоту, статин, 1,2,3,4-тетрагидроизохинолин-3-карбоновую кислоту, пеницилламин, орнитин, 3-метилгистидин, норвалин, бета-аланин, гамма-аминобутиловую кислоту, цитруллин, гомоцистеин, гомосерин, метилаланин, пара-бензоилфенилаланин, фенилглицин, пропаргилглицин, саркозин, метионинсульфон, трет-бутилглицин, 3,5-дибромтирозин и 3,5-дийодтирозин.
"Аминокислотный остаток" или "группа аминокислотной боковой цепи" относится к части аминокислоты, которая остается после высвобождения молекулы воды (или спирта) при конденсации аминокислоты с какой-либо молекулой. Обычно аминокислота конденсируется с какой-либо молекулой, в том числе с соединением любой из формул (I)-(IV), посредством образования пептидной связи. В некоторых вариантах осуществления аминная функциональная группа аминокислоты может конденсироваться с группой карбоновой кислоты или ее эквивалентом по реакционной способности (например, ангидридом карбоновой кислоты) в молекуле. В других вариантах осуществления функциональная группа карбоновой кислоты в аминокислоте может конденсироваться с аминогруппой молекулы. Обычно в процессе образования пептидной связи высвобождается молекула воды. Примеры "аминокислотных остатков" или "группы аминокислотной боковой цепи" включают, но не ограничиваются, остатки аланина, аргинина, аспарагина, аспарагиновой кислоты, цистеина, глутамина, глутаминовой кислоты, глицина, гистидина, изолейцина, лейцина, лизина, метионина, фенилаланина, пролина, серина, треонина, триптофана, тирозина, валина, фосфосерина, фосфотреонина, фосфотирозина, 4-гидроксипролина, гидроксилизина, десмозина, изодесмозина, гамма-карбоксиглутамата, гиппуровой кислоты, октагидроиндол-2-карбоновой кислоты, статина, 1,2,3,4-тетрагидроизохинолин-3-карбоновой кислоты, пеницилламина, орнитина, 3-метилгистидина, норвалина, бета-аланина, гамма-аминобутиловой кислоты, цитруллина, гомоцистеина, гомосерина, метил-аланина, пара-бензоилфенилаланина, фенилглицина, пропаргилглицина, саркозина, метионинсульфона, трет-бутилглицина, 3,5-дибромтирозина, 3,5-дийодтирозина, гликозилированного треонина, гликозилированного серина и гликозилированного аспарагина.
"Производное с аминокислотной боковой цепью" относится к производному любой группы аминокислотной боковой цепи, описанной в таблице 1. В некоторых вариантах осуществления производное с аминокислотной боковой цепью представляет собой алкил, ацил, алкокси, арил, арилалкил, гетероциклил и