Конъюгаты цитотоксических средств с пептидами
Иллюстрации
Показать всеНастоящее изобретение относится к цитотоксическим соединениям направленного действия и способам их терапевтического применения для лечения неоплазии и других заболеваний. 7 н. и 2 з.п. ф-лы, 12 табл., 31 пр.; 3 ил.
Реферат
Область техники, к которой относится изобретение
Настоящее изобретение относится к лекарственным композициям и их применению для лечения болезненных состояний. В частности, настоящее изобретение относится к соединениям и композициям, а также к способам лечения заболеваний и состояний, связанных с аберрантной или нежелательной пролиферацией, миграцией и/или физиологической активностью клеток.
Уровень техники
Большинство цитотоксических средств вызывают нежелательные токсические побочные эффекты из-за отсутствия избирательного воздействия на требующие лечения ткани или клетки. Были исследованы разные подходы для достижения избирательной доставки цитотоксических агентов к клетке-мишени.
Использование лигандов биологических рецепторов в качестве носителей лекарственных средств для направленной доставки указанных средств к представляющим интерес клеткам позволяет уменьшить токсические побочные эффекты и значительно улучшить эффективность доставки лекарственного средства. Например, в международной публикации патента №WO97/19954 описаны конъюгаты цитотоксического средства антрациклина, такого как доксорубицин, с пептидным гормоном, таким как LHRH, бомбезин или соматостатин. Указанный цитотоксический агент ковалентно связан с пептидом при помощи линкера формулы: -С(О)-(СН2)n-С(О), где n=0-7.
Аналогичным образом в заявке на европейский патент № ЕР 1118336 описаны конъюгаты аналогов соматостатина, например, остреотида, ланреотида и вапреотида, с цитотоксическим средством, таким как паклитаксель, доксорубицин или камптотецин, образованные при помощи спейсера, который также имеет формулу: -С(О)-(СН2)n-С(О)-, где n=0-7.
В публикации заявки на патент США №2002/0115596 описаны конъюгаты цитотоксических агентов с олигопептидами, в которых аминокислотные последовательности пептидов предпочтительно расщепляются свободным антигеном предстательной железы. Такие конъюгаты, как указано, являются подходящими для лечения рака предстательной железы и доброкачественной гиперплазии предстательной железы.
В публикации заявки на патент США №2003/0064984 описаны конъюгаты цитотоксических аналогов СС-1065 и дуокармицинов с расщепляемыми линкерами и агента, обеспечивающего направленную доставку лекарственного средства, такого как антитело или пептид. Указано, что цитотоксические аналоги высвобождаются в результате расщепления линкера.
В международной заявке на патент №WO02/34237 описаны конъюгаты активных агентов, ковалентно связанных при помощи прямой связи с полипептидом. Отмечено, что полипептид стабилизирует активный агент, например, в желудке, защищая его структуру.
В международной заявке на патент №WO04/093807 описаны цитотоксические соединения направленного действия, конъюгированные с лигандом биологической мишени.
Однако по-прежнему существует значительная потребность в цитотоксических средствах направленного действия, обладающих улучшенными свойствами в отношении специфичности направленного воздействия, системной токсичности и фармакокинетики.
Сущность изобретения
Настоящее изобретение относится к цитотоксическим соединениям направленного действия, включающим цитотоксическую часть, связанную с частью, обеспечивающей направленную доставку лекарственного средства. Часть, обеспечивающая направленную доставку, является, например, лигандом биологического рецептора. Определенные преимущества соединений по настоящему изобретению и их применения при лечении опухолей и рака включают, не ограничиваясь ими:
a) менее выраженные токсические побочные эффекты;
b) более высокую эффективность лечения благодаря возможности введения более высоких доз, более продолжительного лечения, более частого введения доз и/или локализации и увеличения концентрации лекарственного средства в клетках-мишенях; и/или
c) уменьшение осложнений вследствие множественной лекарственной устойчивости;
или любые комбинации вышеуказанных преимуществ. Целью применения цитотоксических соединений направленного действия является лечение ряда раковых заболеваний или состояний. Например, лечение опухолей или разных типов рака, сверхэкспрессирующих рецепторы соматостатина, предполагает направленную доставку лекарственного средства и лечение нативным соматостатином, то есть H-Ala-Gly-Cys-Lys-Asn-Phe-Phe-Trp-Lys-Thr-Phe-Thr-Ser-Cys-OH (SEQ ID N0:1), и/или его фрагментами или аналогами, образующими комплекс с определенными цитотоксическими частями. Такие типы рака включают, не ограничиваясь ими, нейроэндокринные опухоли (например, карциноидные опухоли, нейробластомы, ульцерогенные аденомы поджелудочной железы, инсулиномы, медуллярный рак щитовидной железы или рак клеток Меркеля), рак молочной железы, лимфомы (ходжкинская и неходжкинская лимфома), лейкоз, мелкоклеточный рак легкого (SCLC), гепатомы, меланомы и рак почки, которые, как известно, характеризуются повышенным содержанием рецептора соматостатина типа 2 (SSTR-2). Карциномы и саркомы предстательной железы являются типичными примерами рака, сверхэкспрессирующего рецептор соматостатина типа 1, SSTR-1; кроме того, известно, что разные типы рака предстательной железы характеризуются высоким содержанием рецептора соматостатина типа 4 (SSTR-4). Аденомы гипофиза характеризуются повышенным содержанием рецептора соматостатина типа 5 (SSTR-5). (См. публикации Reubi, J.C. et al., Eur. J. Nucl. Med. Mod. Imaging, 2002, 29(7):855-62; Schally, A.V. et al., Life Sci., 2003, 72(21):2305-20; Hansson, J. et al., Prostate, 2002, 53(1):50-9; Reubi, J.C. et al., Eur. J. Nucl. Med., 2001, 28(7):836-46). Дополнительные типы рака или опухолей, которые можно лечить, используя соединения или композиции по настоящему изобретению, включают, не ограничиваясь ими, медуллярные опухоли надпочечника (феохромацитому, нейробластому, ганглионеврому), опухоли желудка, кишечника и поджелудочной железы (GEP) (глюкагоному, вазоактивную полипептидсекретирующую опухоль кишечника (VIPoma), гормонально-неактивные опухоли GEP), параганглиому, аденому гипофиза, астроцитомы, доброкачественные и злокачественные опухоли кости, дифференцированную карциному щитовидной железы (папиллярную карциному, фолликулярную карциному, оксифильную карциному), менингиому и немелкоклеточный рак легкого (см. публикацию Society of Nuclear Medicine Procedure Guideline for Somatostatin Receptor Scintigraphy with In-111 Pentetreotid, Version 1.0, February 2001). Дополнительные состояния или заболевания, на которые соединения по настоящему изобретению оказывают благоприятное воздействие, включают, не ограничиваясь ими, аутоиммунные заболевания (болезнь Грейвса, офтальмопатия Грейвса), бактериальную пневмонию, инсульт, фиброзную дисплазию, гранулемы (туберкулез, саркоид) и лучевой пневмонит (см. публикацию Society of Nuclear Medicine Procedure Guideline for Somatostatin Receptor Scintigraphy with In-111 Pentetreotid, Version 1.0, February 2001). Таким образом, возможность направленно воздействовать на определенные типы SSTR при помощи определенных аналогов соматостатина, конъюгированных с цитотоксическими частями, позволяет лечить вышеуказанные раковые заболевания.
Аналогичным образом на опухоли, сверхэкспрессирующие рецепторы бомбезина, можно эффективно воздействовать при помощи цитотоксических соединений направленного действия, содержащих нативный бомбезин, то есть Tyr-Gln-Arg-Leu-Gly-Asn-Gln-Trp-Ala-Val-Gly-His-Leu-Met-NH2 (SEQ ID NO:2), и/или его фрагменты или аналоги. Такие типы рака включают, не ограничиваясь ими, рак молочной железы, рак предстательной железы, рак легкого, мелкоклеточный рак легкого, ульцерогенные аденомы поджелудочной железы и рак почки (см. публикацию Reubi, J.C. et al., Clin. Can. Res., 2002, 8(4):1139-46).
Настоящее изобретение относится также к конъюгатам цитотоксических средств с пептидами, предназначенным для лечения ангиогенных и/или пролиферативных заболеваний. Например, соединения по настоящему изобретению можно использовать для лечения заболеваний, ассоциированных с образованием новых кровеносных сосудов, экспрессирующих высокие уровни SSTR-2 (см. публикакацию van Hagen et al., Eur. J. Endocrinol., 2000, 143(Suppl.1):S43-51). Заболевания, ассоциированные с образованием новых кровеносных сосудов, являющихся мишенью для соединений по настоящему изобретению, включают, не ограничиваясь ими, ангиогенез, пролиферативную диабетическую ретинопатию, кистозную опухоль желтого пятна, ревматоидный артрит, эндометриоз, рестеноз и псориаз.
Первым объектом настоящего изобретения являются цитотоксическая часть и часть, обеспечивающая направленную доставку лекарственного средства, формулы IA:
А-В-С-Е
(IA)
где:
А означает камптотецин или его производное;
В означает rvAbu, rvAhp, rvAla, rvAnc, rvApn, rvArg, rvAsp, rvCha, rvDap(Z), rvGlu, rvGly, rvPhe, rvVal или отсутствует;
С означает D1-D2-D3-D4, где
D1 означает глутарил, сукцинил или отсутствует;
D2 означает (Doc)m, где m в каждом случае независимо означает 4, 5, 6 или [Peg]х, где х в каждом случае независимо означает 0-100;
D3 означает (Aepa)n, где n в каждом случае независимо означает 0 или 1; и
D4 означает D-Phe или Lys-D-Tyr-D-Tyr;
Е означает аналог соматостатина формулы
с(Cys-A2-A3-D-Trp-Lys-A6-Cys)-A8-R, где
А2 означает Phe или отсутствует;
А3 означает Phe, 3-(I)Tyr или Tyr;
A6 означает Abu, Thr или отсутствует;
А8 означает Thr или отсутствует; и
R означает NH2 или ОН;
или их фармацевтически приемлемая соль.
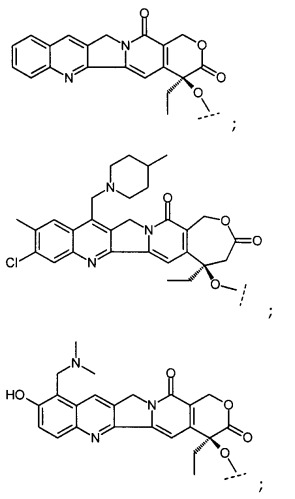
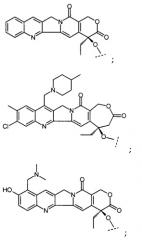
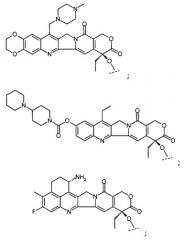
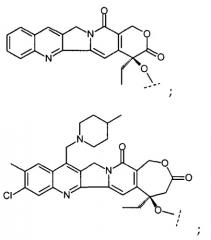
Первый вариант осуществления первого объекта настоящего изобретения относится к соединениям формулы (IA), содержащим часть камптотецина, выбираемую из группы, включающей:
где пунктирной линией “---” отмечена точка присоединения камптотецина ко второй части, например линкеру или пептиду.
Второй вариант осуществления первого объекта настоящего изобретения относится к соединениям формулы (IA), в которых часть, обеспечивающая направленную доставку лекарственного средства, является нативным соматостатином или его фрагментом и/или аналогом, соответствующим любой из нижеследующих формул:
H-Ala-Gly-Cys-Lys-Asn-Phe-Phe-Trp-Lys-Thr-Phe-Thr-Ser-Cys-OH (нативный SRIF) (SEQ ID NO:1);
c(Cys-3-(I)Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
c(Cys-Phe-Phe-D-Trp-Lys-Thr-Cys)-NH2 или
с(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2,
или к их фармацевтически приемлемым солям.
Третий вариант осуществления первого объекта настоящего изобретения относится к любому из нижеследующих соединений:
камптотецин-rvGly-Glut-(Doc)6-Lys-D-Tyr-D-Tyr-c(Cys-3-(I)Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
камптотецин-rvGly-Glut-(Doc)4-Lys-D-Tyr-D-Tyr-c(Cys-3-(I)Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
камптотецин-rvGly-Glut-(Doc)4-Lys-D-Tyr-D-Tyr-c(Cys-Phe-Phe-D-Trp-Lys-Thr-Cys)-NH2;
камптотецин-rvAsp-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
камптотецин-rvGlu-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
камптотецин-rvArg-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
камптотецин-rvDap(Z)-Sue-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
камптотецин-rvCha-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
камптотецин-rvPhe-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
камптотецин-rvApn-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
камптотецин-rvAbu-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
камптотецин-rvAla-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
камптотецин-rvVal-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
камптотецин-Glut-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
камптотецин-rvAnc-Suc-(Doc)4-Aepa-D-Phe-UHKno(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
камптотецин-rvAhp-Suc-(Doc)4-Aepa-D-Phe-UMKno(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
SN38-rvGly-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
или к его фармацевтически приемлемой соли.
Четвертый вариант осуществления первого объекта настоящего изобретения относится к любому из нижеследующих соединений:
камптотецин-rvAsp-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
камптотецин-rvGlu-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
камптотецин-rvCha-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
камптотецин-rvAbu-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
камптотецин-rvAla-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
камптотецин-rvVal-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
камптотецин-rvAnc-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
SN38-rvGly-Suc-(Doc)4-Aepa-D-Phe-c (Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
или к его фармацевтически приемлемой соли.
Пятый вариант осуществления первого объекта настоящего изобретения относится к любому из нижеследующих соединений:
камптотецин-rvAsp-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
камптотецин-rvGlu-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
камптотецин-rvCha-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
камптотецин-rvAbu-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
SN38-rvGly-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
или к его фармацевтически приемлемой соли.
Шестой вариант осуществления первого объекта настоящего изобретения относится к любому из нижеследующих соединений:
камптотецин-rvAsp-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
камптотецин-rvCha-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-cys)-Thr-NH2;
SN38-rvGly-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys) -Thr-NH2;
или к его фармацевтически приемлемой соли.
Седьмой вариант осуществления первого объекта настоящего изобретения относится к соединению:
камптотецин-rvAsp-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2
или к его фармацевтически приемлемой соли.
Восьмой вариант осуществления первого объекта настоящего изобретения относится к соединению:
камптотецин-rvCha-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2
или к его фармацевтически приемлемой соли.
Девятый вариант осуществления первого объекта настоящего изобретения относится к соединению:
SN38-rvGly-Suc- (Doc)4-Aepa-D-Phe-c (Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2
или к его фармацевтически приемлемой соли.
Вторым объектом настоящего изобретения являются цитотоксическая часть и часть, обеспечивающая направленную доставку лекарственного средства, формулы IB:
где:
А означает камптотецин или его производное;
В означает rvD-Abu, rvD-Ala, rvD-Arg, rvD-Asp, rvD-Cha, rvD-Dap(Z), rvD-Glu, rvD-Phe, rvD-Val или отсутствует;
С означает D1-D2-D3-D4, где
D1 означает глутарил, сукцинил или отсутствует;
D2 означает (Doc)m, где m в каждом случае независимо означает 4, 5, 6 или [Peg]x, где х в каждом случае независимо означает 0-100;
D3 означает (Aepa)n, где n в каждом случае независимо означает 0 или 1; и
D4 означает D-Phe или Lys-D-Tyr-D-Tyr;
Е означает аналог соматостатина формулы
с(Cys-A2-A3-D-Trp-Lys-A6-Cys)-A8-R, где
А2 означает Phe или отсутствует;
А3 означает Phe, 3-(I)Tyr или Tyr;
А6 означает Abu, Thr или отсутствует;
А8 означает Thr или отсутствует; и
R означает NH2 или ОН;
или их фармацевтически приемлемая соль.
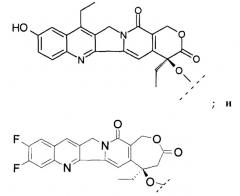
Первый вариант осуществления второго объекта настоящего изобретения относится к соединениям формулы (IB), содержащим часть камптотецина, выбираемую из группы, включающей:
где пунктирной линией “---” отмечена точка присоединения камптотецина ко второй части, например линкеру или пептиду.
Второй вариант осуществления второго объекта настоящего изобретения относится к соединениям формулы (IB), в которых часть, обеспечивающая направленную доставку лекарственного средства, является нативным соматостатином или его фрагментом и/или аналогом, соответствующим любой из нижеследующих формул:
H-Ala-Gly-Cys-Lys-Asn-Phe-Phe-Trp-Lys-Thr-Phe-Thr-Ser-Cys-OH (нативный SRIF) (SEQ ID NO:1);
с(Cys-3-(I)Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
с(Cys-Phe-Phe-D-Trp-Lys-Thr-Cys)-NH2 или
с(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2,
или к их фармацевтически приемлемым солям.
Третий вариант осуществления второго объекта настоящего изобретения относится к любому из нижеследующих соединений:
камптотецин-rvD-Asp-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
камптотецин-rvD-Glu-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
камптотецин-rvD-Arg-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
камптотецин-rvD-Dap(Z)-Sue-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
камптотецин-rvD-Cha-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
камптотецин-rvD-Phe-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
камптотецин-rvD-Abu-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
камптотецин-rvD-Val-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
камптотецин-rvD-Ala-Suc-(Doc)4-Aepa-D-Phe-c (Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
камптотецин-rvD-Asp-Suc-(Peg3)3-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
камптотецин-rvD-Asp-Suc-Pegn-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
камптотецин-rvD-Glu-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
или к его фармацевтически приемлемой соли.
Четвертый вариант осуществления второго объекта настоящего изобретения относится к любому из нижеследующих соединений:
камптотецин-rvD-Asp-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
камптотецин-rvD-Glu-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
камптотецин-rvD-Cha-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
камптотецин-rvD-Abu-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
камптотецин-rvD-Ala-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
камптотецин-rvD-Val-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
камптотецин-rvD-Asp-Suc-(Peg3)3-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
камптотецин-rvD-Asp-Suc-Pegn-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
камптотецин-rvD-Glu-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
или к его фармацевтически приемлемой соли.
Пятый вариант осуществления второго объекта настоящего изобретения относится к любому из нижеследующих соединений:
камптотецин-rvD-Asp-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
камптотецин-rvD-Glu-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
камптотецин-rvD-Cha-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
камптотецин-rvD-Abu-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
камптотецин-rvD-Asp-Suc-(Peg3)3-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
камптотецин-rvD-Asp-Suc-Pegn-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
камптотецин-rvD-Glu-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
или к его фармацевтически приемлемой соли.
Шестой вариант осуществления второго объекта настоящего изобретения относится к любому из нижеследующих соединений:
камптотецин-rvD-Asp-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
камптотецин-rvD-Cha-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
камптотецин-rvD-Asp-Suc-(Реg3)3-Aepa-D-Phe-c (Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
камптотецин-rvD-Asp-Suc-Pegu-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
камптотецин-rvD-Glu-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2;
или к его фармацевтически приемлемой соли.
Седьмой вариант осуществления второго объекта настоящего изобретения относится к соединению:
камптотецин-rvD-Asp-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2
или к его фармацевтически приемлемой соли.
Восьмой вариант осуществления второго объекта настоящего изобретения относится к соединению:
камптотецин-rvD-Cha-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2
или к его фармацевтически приемлемой соли.
Девятый вариант осуществления второго объекта настоящего изобретения относится к соединению:
камптотецин-rvD-Asp-Suc-(Реg3)3-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2
или к его фармацевтически приемлемой соли.
Десятый вариант осуществления второго объекта настоящего изобретения относится к соединению:
камптотецин-rvD-Asp-Suc-Pegu-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2
или к его фармацевтически приемлемой соли.
Одиннадцатый вариант осуществления второго объекта настоящего изобретения относится к соединению:
камптотецин-rvD-Glu-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2
или к его фармацевтически приемлемой соли.
Соединения формул IA и IB по настоящему изобретению являются по существу чистыми соединениями. По существу чистые соединения представляют собой соединения, которые содержат примерно 98% или более идентичных молекул формул IA или IB и примерно 2% или менее неидентичных молекул, то есть примесей, неполных молекул, промежуточных молекул или энантиомерных форм. По существу чистые соединения включают, конечно, соединения, содержащие примерно 99%, 99,5%, 99,8%, 99,9% или более идентичных молекул и примерно 1%, 0,5%, 0,2%, 0,1% или менее неидентичных молекул. По существу чистые соединения включают также соединения, содержащие 100% идентичных молекул.
Третьим объектом настоящего изобретения является смесь соединений формул IA и IB, в которых линкер аминокислоты, присоединенной в обратной ориентации, (rv) имеет D-форму (формула IB) в некоторых соединениях смеси или L-форму (формула IA) в некоторых соединениях смеси. Соединения находятся в смеси в массовом соотношении, равном примерно 2:98, примерно 5:95, примерно 10:90, примерно 15:85, примерно 20:80, примерно 25:75, примерно 30:70, примерно 35:65, примерно 40:60, примерно 45:50, примерно 50:50, примерно 55:45, примерно 60:40, примерно 65:35, примерно 70:30, примерно 75:25, примерно 80:20, примерно 85:15, примерно 90:10, примерно 95:5, примерно 97:3 или даже примерно 98:2, при этом линкер аминокислоты, присоединенной в обратной ориентации, имеет соответственно D-форму (формула IB) и L-форму (формула IA). Типичные смеси включают, не ограничиваясь ими, смеси соединений камптотецин-rvD-Asp-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2 и камптотецин-rvAsp-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2 или их фармацевтически приемлемых солей либо соединений камптотецин-rvD-Glu-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2 и камптотецин-rvGlu-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2 или их фармацевтически приемлемых солей.
Соединения формул IA и IB, относящиеся к третьему объекту настоящего изобретения, являются по существу чистыми соединениями в смеси. По существу чистые соединения представляют собой соединения, содержащие примерно 98% или более идентичных молекул формул IA или IB и примерно 2% или менее неидентичных молекул, то есть примесей, неполных молекул, промежуточных молекул или энантиомерных форм. По существу чистые соединения включают, конечно, соединения, содержащие примерно 99%, 99,5%, 99,8%, 99,9% или более идентичных молекул и примерно 1%, 0,5%, 0,2%, 0,1% или менее неидентичных молекул. По существу чистые соединения включают также соединения, содержащие 100% идентичных молекул.
В первом варианте осуществления третьего объекта настоящего изобретения смесь включает камптотецин-rvD-Asp-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2 и камптотецин-rvAsp-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2 или их фармацевтически приемлемые соли. В соответствии с одним отличительным признаком первого варианта осуществления третьего объекта настоящего изобретения смесь включает камптотецин-rvD-Asp-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2 и камптотецин-rvAsp-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2 или их фармацевтически приемлемые соли в процентном соотношении по массе, соответственно равном примерно 44:56, примерно 58:42, примерно 87:13, примерно 88:12, примерно 97:3 или примерно 98:2.
В соответствии с другим отличительным признаком смесь включает камптотецин-rvD-Asp-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2 и камптотецин-rvAsp-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2 или их фармацевтически приемлемые соли в массовом соотношении, соответственно равном примерно 44:56. В соответствии с другим отличительным признаком смесь включает камптотецин-rvD-Asp-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2 и камптотецин-rvAsp-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2 или их фармацевтически приемлемые соли в массовом соотношении, соответственно равном примерно 58:42. В соответствии с другим отличительным признаком смесь включает камптотецин-rvD-Asp-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2 и камптотецин-rvAsp-Suc- (Doc)4-Aepa-D-Phe-c (Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2 или их фармацевтически приемлемые соли в массовом соотношении, соответственно равном примерно 87:13. В соответствии с другим отличительным признаком смесь включает камптотецин-rvD-Asp-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2 и камптотецин-rvAsp-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2 или их фармацевтически приемлемые соли в массовом соотношении, соответственно равном примерно 88:12. В соответствии с другим отличительным признаком смесь включает камптотецин-rvD-Asp-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2 и камптотецин-rvAsp-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2 или их фармацевтически приемлемые соли в массовом соотношении, соответственно равном примерно 97:3. В соответствии с другим отличительным признаком смесь включает камптотецин-rvD-Asp-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2 и камптотецин-rvAsp-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2 или их фармацевтически приемлемые соли в массовом соотношении, соответственно равном примерно 98:2.
Во втором варианте осуществления третьего объекта настоящего изобретения смесь включает в массовом соотношении камптотецин-rvD-Glu-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2 и камптотецин-rvGlu-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2 или их фармацевтически приемлемые соли. В соответствии с другим отличительным признаком смесь включает камптотецин-rvD-Glu-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2 и камптотецин-rvGlu-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2 или их фармацевтически приемлемые соли в массовом соотношении, соответственно равном примерно 80:20, примерно 85:15, примерно 87:13, примерно 88:12, примерно 90:10, примерно 95:5, примерно 97:3 или примерно 98:2. В соответствии с другим отличительным признаком смесь включает камптотецин-rvD-Glu-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2 и камптотецин-rvGlu-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2 или их фармацевтически приемлемые соли в массовом соотношении, соответственно равном примерно 80:20. В соответствии с другим отличительным признаком смесь включает камптотецин-rvD-Glu-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2 и камптотецин-rvGlu-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2 или их фармацевтически приемлемые соли в массовом соотношении, соответственно равном примерно 85:15. В соответствии с другим отличительным признаком смесь включает камптотецин-rvD-Glu-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2 и камптотецин-rvGlu-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2 или их фармацевтически приемлемые соли в массовом соотношении, соответственно равном примерно 87:13. В соответствии с другим отличительным признаком смесь включает камптотецин-rvD-Glu-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2 и камптотецин-rvGlu-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2 или их фармацевтически приемлемые соли в массовом соотношении, соответственно равном примерно 88:12. В соответствии с другим отличительным признаком смесь включает камптотецин-rvD-Glu-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2 и камптотецин-rvGlu-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2 или их фармацевтически приемлемые соли в массовом соотношении, соответственно равном примерно 90:10. В соответствии с другим отличительным признаком смесь включает камптотецин-rvD-Glu-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2 и камптотецин-rvGlu-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2 или их фармацевтически приемлемые соли в массовом соотношении, соответственно равном примерно 95:5. В соответствии с другим отличительным признаком смесь включает камптотецин-rvD-Glu-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2 и камптотецин-rvGlu-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2 или их фармацевтически приемлемые соли в массовом соотношении, соответственно равном примерно 97:3. В соответствии с другим отличительным признаком смесь включает камптотецин-rvD-Glu-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2 и камптотецин-rvGlu-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2 или их фармацевтически приемлемые соли в массовом соотношении, соответственно равном примерно 98:2.
Четвертым объектом настоящего изобретения является фармацевтическая композиция, включающая терапевтически эффективное количество по существу чистого соединения формулы (IA), по существу чистого соединения формулы (IB) или смесь по существу чистых соединений формул (IA) и (IB) в соответствии с любым из вышеуказанных вариантов осуществления изобретения или их фармацевтически приемлемых солей и фармацевтически приемлемый носитель.
Пятым объектом настоящего изобретения является способ лечения заболевания или состояния у нуждающегося субъекта, который включает введение терапевтически эффективного количества по существу чистого соединения формулы (IA), по существу чистого соединения формулы (IB) или смеси по существу чистых соединений формул (IA) и (IB) в соответствии с любым из вышеуказанных вариантов осуществления изобретения, их фармацевтически приемлемых солей или вышеописанной фармацевтической композиции, при этом указанное заболевание или состояние характеризуется нежелательной пролиферацией клеток, экспрессирующих рецепторы соматостатина одного или нескольких типов. В другом варианте осуществления изобретения рецептор соматостатина является рецептором соматостатина типа 2.
Шестым объектом настоящего изобретения является способ уменьшения размера опухоли у нуждающегося субъекта, который включает введение терапевтически эффективного количества по существу чистого соединения формулы (IA), по существу чистого соединения формулы (IB) или смеси по существу чистых соединений формул (IA) и (IB) в соответствии с любым из вышеуказанных вариантов осуществления изобретения, их фармацевтически приемлемых солей или вышеописанной фармацевтической композиции, при этом терапевтически эффективное количество является таким количеством, которое уменьшает размер опухоли у субъекта.
Седьмым объектом настоящего изобретения является способ ингибирования нежелательной пролиферации опухолевых клеток у нуждающегося субъекта, который включает введение терапевтически эффективного количества по существу чистого соединения формулы (IA), по существу чистого соединения формулы (IB) или смеси по существу чистых соединений формул (IA) и (IB) в соответствии с любым из вышеуказанных вариантов осуществления изобретения, их фармацевтически приемлемых солей или вышеописанной фармацевтической композиции, при этом терапевтически эффективное количество является таким количеством, которое ингибирует нежелательную пролиферацию опухолевых клеток у субъекта.
Восьмым объектом настоящего изобретения является способ оказания агонистического воздействия на рецептор соматостатина у нуждающегося субъекта, который включает введение терапевтически эффективного количества по существу чистого соединения формулы (IA), по существу чистого соединения формулы (IB) или смеси по существу чистых соединений формул (IA) и (IB) в соответствии с любым из вышеуказанных вариантов осуществления изобретения, их фармацевтически приемлемых солей или вышеописанной фармацевтической композиции, при этом терапевтически эффективное количество является таким количеством, которое оказывает агонистическое воздействие на рецептор соматостатина.
Девятым объектом настоящего изобретения является способ оказания агонистического воздействия на рецептор соматостатина у нуждающегося субъекта, который включает введение терапевтически эффективного количества по существу чистого соединения формулы (IA), по существу чистого соединения формулы (IB) или смеси по существу чистых соединений формул (IA) и (IB) в соответствии с любым из вышеуказанных вариантов осуществления изобретения, их фармацевтически приемлемых солей или вышеописанной фармацевтической композиции, при этом рецептор является рецептором SSTR типа 2 и агонист является агонистом SSTR типа 2.
Десятым объектом настоящего изобретения является способ оказания агонистического воздействия на рецептор соматостатина у нуждающегося субъекта, который включает введение терапевтически эффективного количества по существу чистого соединения формулы (IA), по существу чистого соединения формулы (IB) или смеси по существу чистых соединений формул (IA) и (IB) в соответствии с любым из вышеуказанных вариантов осуществления изобретения, их фармацевтически приемлемых солей или вышеописанной фармацевтической композиции, при этом агонист является избирательно действующим агонистом SSTR типа 2.
Одиннадцатым объектом настоящего изобретения является способ оказания агонистического воздействия на рецептор соматостатина у нуждающегося субъекта, который включает введение терапевтически эффективного количества камптотецин-rvAsp-Suc-(Doc)4-Aepa-D-Phe-с(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2, его фармацевтически приемлемой соли или вышеописанной фармацевтической композиции.
Двенадцатым объектом настоящего изобретения является способ оказания агонистического воздействия на рецептор соматостатина у нуждающегося субъекта, который включает введение терапевтически эффективного количества камптотецин-rvCha-Suc-(Doc)4-Aepa-D-Phe-с(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2, его фармацевтически приемлемой соли или вышеописанной фармацевтической композиции.
Тринадцатым объектом настоящего изобретения является способ оказания агонистического воздействия на рецептор соматостатина у нуждающегося субъекта, который включает введение терапевтически эффективного количества SN38-rvGly-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2, его фармацевтически приемлемой соли или вышеописанной фармацевтической композиции.
Четырнадцатым объектом настоящего изобретения является способ оказания агонистического воздействия на рецептор соматостатина у нуждающегося субъекта, который включает введение терапевтически эффективного количества камптотецин-rvD-Asp-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2, его фармацевтически приемлемой соли или вышеописанной фармацевтической композиции.
Пятнадцатым объектом настоящего изобретения является способ оказания агонистического воздействия на рецептор соматостатина у нуждающегося субъекта, который включает введение терапевтически эффективного количества камптотеин-rvD-Cha-Suc-(Doc)4-Aepa-D-Phe-с(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2, его фармацевтически приемлемой соли или вышеописанной фармацевтической композиции.
Шестнадцатым объектом настоящего изобретения является способ оказания агонистического воздействия на рецептор соматостатина у нуждающегося субъекта, который включает введение терапевтически эффективного количества смеси, включающей камптотецин-rvD-Asp-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2 и камптотецин-rvAsp-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2, их фармацевтически приемлемых солей или вышеописанной фармацевтической композиции.
Семнадцатым объектом настоящего изобретения является способ оказания агонистического воздействия на рецептор соматостатина у нуждающегося субъекта, который включает введение терапевтически эффективного количества смеси, включающей камптотецин-rvD-Glu-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2 и камптотецин-rvGlu-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2, их фармацевтически приемлемых солей или вышеописанной фармацевтической композиции.
Восемнадцатым объектом настоящего изобретения является способ оказания агонистического воздействия на рецептор соматостатина у нуждающегося субъекта, который включает введение терапевтически эффективного количества камптотецин-rvD-Asp-Suc-(Реg3)3-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NHa, его фармацевтически приемлемой соли или вышеописанной фармацевтической композиции.
Девятнадцатым объектом настоящего изобретения является способ оказания агонистического воздействия на рецептор соматостатина у нуждающегося субъекта, который включает введение терапевтически эффективного количества камптотецин-rvD-Asp-Suc-Pegu-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2, его фармацевтически приемлемой соли или вышеописанной фармацевтической композиции.
Двадцатым объектом настоящего изобретения является способ оказания агонистического воздействия на рецептор соматостатина у нуждающегося субъекта, который включает введение терапевтически эффективного количества камптотецин-rvD-Glu-Suc-(Doc)4-Aepa-D-Phe-c(Cys-Tyr-D-Trp-Lys-Abu-Cys)-Thr-NH2, его фармацевтически приемлемой соли или вышеописанной фармацевтической композиции.
Двадцать первым объектом настоящего изобретения является способ лечения заболевания или состояния у нуждающегося субъекта, который включает введение терапевтически эффективного количества по существу чистого соединения фор