Производные, родственные лизину, как ингибиторы аспартилпротеазы вич
Иллюстрации
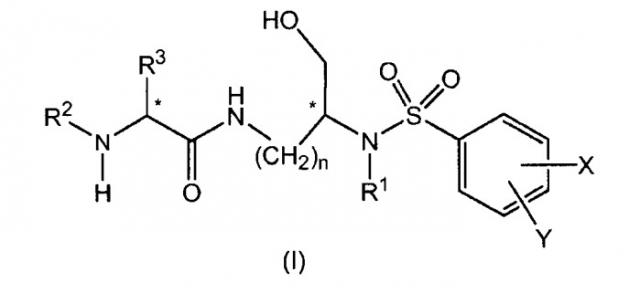
Показать всеНастоящее изобретение относится к новым производным, родственным лизину, формулы (II) и, когда соединение формулы (II) содержит аминогруппу, к его фармацевтически приемлемым солям аммония, обладающим способностью ингибировать ВИЧ-протеазу, к фармацевтической композиции на их основе и к их применению для изготовления лекарственного средства.
где n принимает значение 3 или 4, Х представляет собой Н, Y представляет собой прямую или разветвленную алкильную группу из 1-6 атомов углерода, замещенную -NH2, R1 выбран из группы, состоящей из разветвленной алкильной группы из 3-6 атомов углерода, R2 выбран из группы формулы R2A-CO-, при этом R2A выбирается из алкоксигруппы с 1-6 атомами углерода, R3 выбран из группы, состоящей из дифенилметильной группы формулы IV
где X' и Y' выбраны из Н. 3 н. и 5 з.п. ф-лы, 2 пр.
Реферат
Данное изобретение относится к производным, родственным лизину, их применению в качестве ингибиторов протеазы, в частности в качестве ингибиторов аспартилпротеазы ВИЧ, способам их получения, а также фармацевтическим композициям и диагностическим наборам, содержащим их. Данное изобретение также относится к комбинациям данных производных, родственных лизину, с другим антиретровирусным средством. Оно, кроме того, относится к их применению в анализах в качестве эталонных соединений или в качестве реагентов.
Вирус, вызывающий синдром приобретенного иммунодефицита (СПИД, AIDS), известен под различными названиями, включающими Т-лимфоцитный вирус III (HTLV-III) или вирус, связанный с лимфаденопатией (LAV), или вирус, связанный со СПИД (ARV), или вирус иммунодефицита человека (ВИЧ, HIV). К настоящему времени были идентифицированы два различных типа, т.е. ВИЧ-1 и ВИЧ-2. Далее в настоящей работе ВИЧ будет использоваться для обозначения в основном этих вирусов.
Один из важных этапов в жизненном цикле ретровируса состоит в процессинге полипротеиновых предшественников аспаратиновой протеазой. Например, ВИЧ вирусный gag-pol белок подвергается процессингу протеазой ВИЧ. Точный процессинг предшественников полипротеинов аспаратиновой протеазой требуется для сборки инфекционных вирионов, таким образом, аспаратиновая протеаза является перспективной мишенью для противовирусной терапии. В частности, для лечения ВИЧ ВИЧ-протеаза представляет собой перспективную мишень.
Ингибиторы протеазы ВИЧ (PI) обычно вводят пациентам со СПИДом в комбинации с другими анти-ВИЧ соединениями, такими как, например, нуклеозидные ингибиторы обратной транскриптазы (NRTI), ненуклеозидные ингибиторы обратной транскриптазы (NNRTI), ингибиторы слияния, такие как Т-20, или другие ингибиторы протеазы. Несмотря на то, что данные антиретровирусные средства являются очень полезными, они имеют общее ограничение, а именно: целевые ферменты в ВИЧ способны мутировать таким образом, что известные лекарственные средства становятся менее эффективными или даже неэффективными против данных мутантных ВИЧ-вирусов. Или, иначе говоря, ВИЧ создает все возрастающую устойчивость против доступных лекарственных средств.
Устойчивость ретровирусов, в частности ВИЧ, против ингибиторов представляет собой главную причину неблагоприятного исхода терапии. Например, половина пациентов, получающих комбинированное лечение против ВИЧ, полностью не реагируют на лечение, главным образом из-за устойчивости вируса к одному или нескольким из примененных лекарственных средств. Более того, было показано, что устойчивый вирус переносится на вновь инфицированные индивидуумы, приводя к строго ограниченным вариантам терапии для данных, не подвергающихся воздействию лекарственных средств пациентов. Поэтому существует потребность в данной области в новых соединениях для ретровирусной терапии, в большей степени для терапии СПИДа. Потребность в данной области особенно является острой по соединениям, которые активны не только в отношении ВИЧ дикого типа, но также в отношении ВИЧ с более общей возрастающей устойчивостью.
Известные антиретровирусные средства, часто вводимые по схеме комбинированной терапии, фактически будут вызывать устойчивость, изложенную выше. Это часто может вынуждать врача усилить уровни плазмы активных лекарственных средств, чтобы восстановить эффективность указанных антиретровирусных средств против мутированного ВИЧ. Следствием этого является очень нежелательное повышение в нагрузке пилюль. Увеличенные уровни плазмы могут также приводить к повышенному риску несогласованности с предписанной ранее терапией. Таким образом, не только важно иметь соединения, проявляющие активность для широкого спектра мутантов ВИЧ, но также важно, что существует незначительное или отсутствие различия в соотношении между активностью против мутантного ВИЧ-вируса и активностью против ВИЧ-вируса дикого типа (также определяемом как кратная устойчивость или FR) на широком спектре мутантных ВИЧ-штаммов. Как таковой пациент может оставаться на той же самой комбинированной схеме лечения в течение более долгого периода времени, так как шанс, что мутантный ВИЧ-вирус будет чувствительным к активным ингредиентам, будет возрастать.
Выявление соединений с высокой эффективностью в отношении дикого типа и на большом разнообразии мутантов также важно, так как нагрузка пилюль может быть снижена, если терапевтические уровни держатся на минимуме. Один способ снижения этой нагрузки пилюль представляет собой выявление анти-ВИЧ соединений с хорошей биодоступностью, т.е. с благоприятным фармакокинетическим и метаболическим профилем, таким, что суточная доза может быть снижена до минимума и, следовательно, также число таблеток, предназначенных для употребления.
Другая важная характеристика хорошего анти-ВИЧ соединения состоит в том, что плазменное белковое связывание ингибитора имеет минимальное влияние или даже не оказывает влияния на его эффективность.
В настоящее время на рынке существует или развиваются несколько ингибиторов протеазы, например ампренавир (APV), саквинавир (SQV), индинавир (IDV), ритонавир (RTV), нелфинавир (NFV), лопинавир (LPV) и дарунавир (TMC114).
Хотя данные ингибиторы протеазы имеют отличные свойства, существует постоянная высокая медицинская потребность в новых ингибиторах протеазы, которые способны уничтожать широкий спектр мутантов ВИЧ с незначительным изменением в кратной устойчивости, обладают хорошей биодоступностью и испытывают слабое влияние или не испытывают влияния на эффективность плазменного белкового связывания.
Удивительным образом было установлено, что соединение формулы (I) показало повышенную противовирусную активность при сравнении с, например, ампренавиром, лопинавиром, нелфинавиром или ритонавиром при тестировании на штамме мутанта ВИЧ.
Данное изобретение относится к соединению формулы (I)
и, когда соединение формулы (I) содержит аминогруппу, к его фармацевтически приемлемым солям аммония,
где n принимает значение 3 или 4,
где Х представляет собой Н, и Y представляет собой прямую или разветвленную алкильную группу из 1-6 атомов углерода, замещенную азотом,
или Х и Y являются одинаковыми и каждый представляет собой прямую или разветвленную алкильную группу из 1-6 атомов углерода, замещенную азотом,
где R1 выбран из группы, состоящей из прямой алкильной группы из 1-6 атомов углерода, разветвленной алкильной группы из 3-6 атомов углерода, циклоалкилалкильной группы, содержащей 3-6 атомов углерода в ее циклоалкильной части и 1-3 атома углерода в ее алкильной части,
где R2 выбран из группы, состоящей из Н, прямой алкильной группы из 1-6 атомов углерода, разветвленной алкильной группы из 3-6 атомов углерода, циклоалкильной группы из 3-6 атомов углерода, группы формулы R2A-CO-, при этом R2A выбирается из группы, состоящей из прямой или разветвленной алкильной группы из 1-6 атомов углерода, циклоалкильной группы, содержащей 3-6 атомов углерода, циклоалкилалкильной группы, содержащей 3-6 атомов углерода в ее циклоалкильной части и 1-3 атома углерода в ее алкильной части, алкоксигруппы из 1-6 атомов углерода, тетрагидро-3-фуранилокси, -CН2ОН, -CF3, -CH2CF3, -CH2CH2CF3, пирролидинильной пиперидинильной, 4-морфолинильной, СН3О2C-, СН3О2ССН2-, ацетил-ОСН2СН2-, НО2ССН2-, 3-гидроксифенильной, 4-гидроксифенильной, 4-СН3ОС6Н4СН2-, СН3NH-, (СН3)2N-, (CH3CH2)2N-, (CH3CH2CH2)2N-, HOCH2CH2NH-, CH3OCH2O-, CH3OCH2CH2O-, C6H5CH2O-, 2-пирролильной, 2-пиридильной, 3-пиридильной, 4-пиридильной, 2-пиразинильной, 2-хинолильной, 3-хинолильной, 4-хинолильной, 1-изохинолильной, 3-изохинолильной, 2-хиноксалинильной, фенильной группы формулы
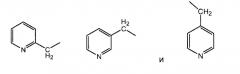
пиколильной группы, выбранной из группы, состоящей из
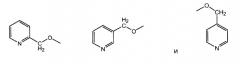
пиколилоксигруппы, выбранной из группы, состоящей из
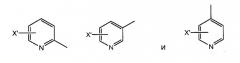
замещенной пиридильной группы, выбранной из группы, состоящей из
группы, выбранной из группы, состоящей из
где Х' и Y', одинаковые или различные, выбраны из группы, состоящей из Н, прямой алкильной группы из 1-6 атомов углерода, разветвленной алкильной группы из 3-6 атомов углерода, циклоалкильной группы из 3-6 атомов углерода, F, Cl, Br, I, -CF3, -NO2, -NR4R5, -NHCOR4, -OR4, -SR4, -COOR4, -COR4 и -CH2OH,
где R4 и R5, одинаковые или различные, выбраны из группы, состоящей из Н, прямой алкильной группы из 1-6 атомов углерода, разветвленной алкильной группы из 3-6 атомов углерода, циклоалкильной группы из 3-6 атомов углерода,
где R3 выбран из группы, состоящей из
дифенилметильной группы формулы IV
нафтил-1-СН2-группы формулы V
нафтил-2-СН2-группы формулы VI
бифенилметильной группы формулы VII
и (антрацен-9-ил)метильной группы формулы VIII
Предпочтительно соединения согласно изобретению имеют следующую стереоизомерную форму, изображенную формулой (II)
Предпочтительными являются соединения, в которых R1 представляет собой изо-бутил и n=4; более предпочтительными являются те соединения, в которых R2 представляет собой СН3О2C-, и даже более предпочтительными являются те соединения, в которых R3 представляет собой , хотя самыми предпочтительными соединениями являются те соединения, в которых Х означает Н и Y означает -CH2NH2.
Самое предпочтительное соединение представлено формулой (III)
Кроме того, данное изобретение относится к фармацевтическим препаратам, которые в качестве составных частей содержат эффективную дозу, по меньшей мере, одного из соединений формулы (I, II или III) кроме обычных фармацевтически безвредных наполнителей и вспомогательных добавок. Фармацевтические препараты обычно содержат от 0,1 до 90 мас.% соединения формулы (I, II или III). Фармацевтические препараты могут быть приготовлены способом, известным в чистом виде специалисту в данной области. С этой целью, по меньшей мере, одно из соединений формулы (I, II или III) вместе с одним или несколькими твердыми или жидкими фармацевтическими наполнителями и/или вспомогательными добавками и, если желательно, в комбинации с другими фармацевтическими активными соединениями вводят в подходящую форму для введения или лекарственную форму, которая затем может использоваться в качестве фармацевтического средства в медицине для человека или в ветеринарной медицине.
Фармацевтические средства, которые содержат соединение согласно изобретению, можно вводить перорально, например, включая суспензии, капсулы, таблетки, саше, растворы, эмульсии; парентерально, применяя, например, подкожную, внутривенную, внутримышечную, внутригрудинную инъекцию или методики инфузии; ректально, применяя, например, суппозитории; внутривагинально; ингаляцией или локальным образом. Предпочтительное введение зависит от индивидуальных случаев, например от определенного течения расстройства, предназначенного для лечения. Пероральное введение предпочтительно.
Специалист в данной области на основе своего практического опыта знаком со вспомогательными добавками, которые являются подходящими для требуемого фармацевтического препарата. Помимо растворителей, гелеобразующих средств, основ для суппозиториев, вспомогательных добавок для таблеток и другого активного соединения также применяются носители, антиоксиданты, диспергирующие средства, эмульгаторы, противовспениватели, вкусовые корригенты, консерванты, солюбилизаторы, средства для достижения эффекта депо, буферные вещества или красители.
Для формы, предназначенной для перорального введения, соединения данного изобретения смешивают с подходящими добавками, такими как наполнители, стабилизаторы или инертные разбавители, и вносят посредством обычных способов в подходящие формы для введения, такие как таблетки, таблетки с покрытием, твердые капсулы, водные, спиртовые или масляные растворы. Примеры подходящих инертных носителей представляют собой гуммиарабик, магнезию, карбонат магния, фосфат калия, лактозу, глюкозу или крахмал, в частности кукурузный крахмал. В данном случае препарат может быть выполнен как в сухих, так и во влажных гранулах. Подходящие масляные наполнители или растворители представляют собой растительные масла или животные жиры, такие как подсолнечное масло или жир из печени трески. Подходящие растворители для водных или спиртовых растворов представляют собой воду, этанол, растворы сахаров или их смеси.
Полиэтиленгликоли и полипропиленгликоли также применимы в качестве дополнительных вспомогательных добавок для других вводимых форм.
Для подкожного или внутривенного введения активные соединения, если желательно с обычно принятыми веществами, такими как солюбилизаторы, эмульгаторы или дополнительные добавки, вносят в раствор, суспензию или эмульсию. Соединения формулы (I), (II) или (III) можно также лиофилизировать и полученные лиофилизаты применять, например, для изготовления препаратов для инъекции или инфузии. Подходящие растворители для водных или спиртовых растворов представляют собой воду, физиологический раствор или спирты, например этанол, пропанол, глицерин, кроме этого также растворы сахаров, такие как растворы глюкозы или маннита, или, в альтернативном случае, смеси различных упомянутых растворителей.
Подходящие фармацевтические препараты для введения в форме аэрозолей или спреев представляют собой, например, растворы, суспензии или эмульсии соединений формулы (I), (II) или (III) или их физиологически допустимых солей в фармацевтически приемлемом растворителе, таком как этанол или вода, или смесь таких растворителей. Если требуется, то препарат может также дополнительно содержать другие фармацевтические добавки, такие как ПАВ, эмульгаторы и стабилизаторы, а также пропеллент. Такой препарат обычно содержит активное соединение в концентрации от приблизительно 0,1 до 50%, в особенности от приблизительно 0,3 до 3 мас.%.
Вследствие благоприятных фармакологических свойств, особенно их активности против протеазных ферментов ВИЧ, устойчивых ко многим лекарственным средствам, соединения данного изобретения применимы в лечении индивидуумов, инфицированных ВИЧ, и для профилактики данных индивидуумов.
Профилактическое лечение может быть полезным в случаях, где индивидуум был подвергнут высокому риску экспозиции вирусом, которая может иметь место, когда индивидуум был в контакте с инфицированным индивидуумом, где существует высокий риск передачи вируса. В качестве примера, профилактическое введение указанных соединений было бы полезно в ситуации, где медицинский работник был подвержен воздействию крови индивидуума, инфицированного ВИЧ, или в других ситуациях, где деятельность индивидуума связана с высоким риском, который потенциально подвергает индивидуума воздействию ВИЧ.
В целом, соединения данного изобретения могут быть применимы в лечении теплокровных животных, инфицированных вирусами, существование которых опосредовано протеазным ферментом или зависит от протеазного фермента. Состояния, которые можно предотвращать или лечить соединениями данного изобретения, включают, но не ограничиваясь только ими, лечение широкого диапазона состояний ВИЧ-инфекции: AIDS, ARC (относящийся к СПИДу комплекс), как симптомной так и бессимптомной, и фактической или потенциальной экспозиции ВИЧ. Соединения данного изобретения также применимы для лечения прогрессирующей генерализованной лимфаденопатии, синдрома Капоши, тромбоцитопенической пурпуры, неврологических состояний, связанных со СПИД, таких как комплекс деменции, множественный склероз, тропический паралич, анти-ВИЧ, антитело-положительные и ВИЧ-положительные состояния, включающие такие состояния у бессимптомных пациентов. Например, соединения данного изобретения применимы в лечении инфекции от ВИЧ после подозреваемой экспозиции ВИЧ в прошлом под действием, например, переливания крови, изменения общего содержания жидкости в организме, укусов, случайного прокола иглой, или воздействия на пациента крови в течение хирургического вмешательства. Термин «предотвращение» включает профилактику ВИЧ-инфекции и профилактику развития ВИЧ-инфекции до СПИДа.
Соединения данного изобретения или любые их производные поэтому могут быть применены как лекарственные средства против вышеупомянутых состояний. Указанное применение в качестве лекарственного средства или способ лечения включает системное введение субъектам, инфицированным ВИЧ, количества, эффективного для подавления состояния, связанного с ВИЧ и другими патогенными ретровирусами, особенно ВИЧ-1. Следовательно, соединения данного изобретения могут применяться в изготовлении лекарственного средства, предназначенного для лечения состояний, связанных с ВИЧ и другими патогенными ретровирусами, в частности лекарственных средств, предназначенных для лечения пациентов, инфицированных ВИЧ-вирусом, устойчивым ко многим лекарственным средствам.
В предпочтительном варианте осуществления изобретение относится к применению соединения формулы (I, II или III) или любого его производного в изготовлении лекарственного средства для лечения или уничтожения инфекции или заболевания у млекопитающего, связанного с инфекцией ретровирусов, устойчивых ко многим лекарственным средствам, в частности с ВИЧ-1 инфекцией. Таким образом, изобретение также относится к способу лечения ретровирусной инфекции или заболевания, связанного с инфекцией ретровирусов, устойчивых ко многим лекарственным средствам, включающему введение млекопитающему, нуждающемуся в этом, эффективного количества соединения формулы (I, II или III) или его производного.
В другом предпочтительном варианте осуществления данное изобретение относится к применению соединения формулы (I, II или III) или любого его производного в изготовлении лекарственного средства для ингибирования протеазы ретровируса, устойчивого ко многим лекарственным средствам, в млекопитающих, инфицированных указанным ретровирусом, в частности ВИЧ-1 ретровирусом.
В другом предпочтительном варианте осуществления данное изобретение относится к применению соединения формулы (I, II или III) или любого его производного в изготовлении лекарственного средства для ингибирования ретровирусной репликации, устойчивой ко многим лекарственным средствам, в частности ВИЧ-1 репликации.
Кроме того, комбинация антиретровирусного соединения и соединения данного изобретения может применяться в качестве лекарственного средства. Таким образом, данное изобретение также относится к продукту или композиции, содержащей (а) соединение данного изобретения (согласно формуле (I, II или III)) и (b) другое антиретровирусное соединение, как комбинированному препарату для одновременного, раздельного или последовательного применения в лечении ретровирусных инфекций, в частности в лечении инфекций с ретровирусами, устойчивыми ко многим лекарственным средствам. Таким образом, чтобы уничтожать или лечить ВИЧ-инфекции или инфекцию или заболевание, связанные с ВИЧ-инфекциями, такие как синдром приобретенного иммунодефицита (СПИД, AIDS) или относящийся к СПИДу комплекс (ARC), соединения данного изобретения могут быть введены совместно в комбинации с, например, ингибиторами присоединения.
Соединения данного изобретения могут быть также введены в комбинации с модуляторами метаболических превращений после применения лекарственного средства индивидуумом. Данные модуляторы включают соединения, которые вмешиваются в метаболические превращения при цитохромах, таких как цитохром Р450. Некоторые модуляторы ингибируют цитохром Р450. Известно, что существуют несколько изоферментов цитохрома Р450, один из которых представляет собой цитохром Р450 3А4. Ритонавир представляет собой пример модулятора метаболических превращений посредством цитохрома Р450. Представляющие интерес соединения, действующие на цитохром Р450, включают такие соединения, которые содержат группу тиазолила, имидазолила или пиридинила. Такая комбинированная терапия различными препаратами может быть применена одновременно, раздельно или последовательно. В альтернативном случае, такая комбинация может применяться как один препарат, где активные ингредиенты высвобождаются из препарата одновременно или раздельно.
Такой модулятор может быть введен в таком же или другом отношении как соединение данного изобретения. Предпочтительно массовое отношение такого модулятора по отношению к соединению данного изобретения (модулятор: соединение данного изобретения) равно 1:1 или менее, более предпочтительное отношение равно 1:3 или менее, в подходящем случае отношение равно 1:10 или менее, в более подходящем случае отношение равно 1:30 или менее.
Комбинация может давать синергический эффект, посредством которого инфективность вируса и связанные с ним симптомы могут быть предотвращены, существенно снижены или полностью устранены. Комбинации соединений формулы (I, II или III) с другим ингибитором протеазы ВИЧ, как ингибитором цитохрома Р450, могут действовать синергическим образом, аддитивно или антагонистически. Это можно оценить в экспериментальном плане, где измеряют эффективность различных соотношений ингибиторов ВИЧ-протеазы. Результаты можно представлять в виде графика изоболограммы согласно способу, описанному Chou и Talalay (Adv. Enzyme Regul. 22: 27-55, 1984). Синергизм между двумя ингибиторами означал бы более сильную комбинированную терапию, но без повышения нежелательных побочных эффектов.
Другой аспект данного изобретения относится к набору или контейнеру, содержащему соединение формулы (I, II или III) в количестве, эффективном для применения в качестве стандарта или реагента в тесте или анализе по определению способности потенциального фармацевтического средства ингибировать протеазу ВИЧ, рост ВИЧ или и то и другое. Данный аспект изобретения может найти свое применение в программах фармацевтических исследований.
Соединения данного изобретения могут применяться в анализах по мониторингу фенотипической устойчивости, таких как известные рекомбинантные анализы, в клиническом регулировании устойчивости, развивающей заболевания типа ВИЧ. Особенно применимая система мониторинга устойчивости представляет собой рекомбинантный анализ, известный как Antivirogram™. Antivirogram™ является высокоавтоматизированным, высокопроизводительным, второго поколения, рекомбинантным анализом, который может измерять чувствительность, особенно вирусную чувствительность, к соединениям данного изобретения (Hertogs K., de Bethune MP, Miller V. et al., Antimicrob. Agents Chemother., 1998; 42(2): 269-276).
Следует подразумевать, что термины “ВИЧ-протеаза” и “ВИЧ-аспаратиновая протеаза” применяются как взаимозаменяемые и включают аспаратиновую протеазу, кодированную посредством ВИЧ типа 1 или 2.
“Прямая алкильная группа, включающая 1-6 атомов углерода” включает, например, метил, этил, пропил, бутил, пентил, гексил.
“Разветвленная алкильная группа, включающая 1-6 атомов углерода” включает, например, изо-бутил, трет-бутил, 2-пентил, 3-пентил и т.д.
Следует подразумевать, что циклоалкильная группа, содержащая 3-6 атомов углерода” включает, например, циклопропил, циклобутил, циклопентил, циклогексил (т.е. С6Н11).
Всякий раз, когда применяется термин “замещенный” в определении соединений формулы (I, II или III), он предназначен для указания того, что один или несколько атомов водорода на указанном атоме при использовании выражения “замещенный” замещены выборкой из указанной группы при условии, что нормальная валентность указанных атомов не является превышающей и что замещение дает химически устойчивое соединение, т.е. соединение, которое является достаточно прочным, чтобы выдержать выделение из реакционной смеси до пригодной степени чистоты и рецептурирование в терапевтическое средство.
Соли соединений формулы (I), (II) или (III) представляют собой соли, в которых противоион является фармацевтически или физиологически приемлемым. Однако соли, имеющие фармацевтически неприемлемый противоион, также могут найти применение, например, в приготовлении или очистке фармацевтически приемлемого соединения формулы (I), (II) или (III). Все соли, независимо от того, фармацевтически приемлемые или нет, включены в объем данного изобретения.
Фармацевтически приемлемые или физиологически допустимые аддитивные солевые формы, которые соединения, применяемые в данном изобретении, способны образовать, можно готовить подходящим образом, применяя соответствующие кислоты, такие как, например, неорганические кислоты, а именно галогенводородные кислоты, такие как хлористоводородная или бромистоводородная кислота; серная; гемисерная, азотная; фосфорная и тому подобные кислоты; или органические кислоты, такие как, например, уксусная, аспарагиновая, додецилсерная, гептановая, гексановая, никотиновая, пропановая, гидроксиуксусная, молочная, пировиноградная, щавелевая, малоновая, янтарная, малеиновая, фумаровая, яблочная, винная, лимонная, метансульфоновая, этансульфоновая, бензолсульфоновая, п-толуолсульфоновая, цикламовая, салициловая, п-аминосалициловая, памовая и тому подобные кислоты.
Наоборот, названные кислотно-аддитивные солевые формы могут превращаться в форму свободного основания обработкой соответствующим основанием.
Соединения формулы (I), (II) или (III), содержащие кислотный протон, могут также превращаться в их нетоксичную металл- или аминоаддитивную солевую форму обработкой соответствующими органическими и неорганическими основаниями. Соответствующие основные солевые формы представляют собой, например, соли аммония, соли щелочных и щелочноземельных металлов, например лития, натрия, калия, магния, кальция и тому подобное, соли с органическими основаниями, например бензатининовые, N-метиловые, -D-глюкаминовые, гидрабаминовые соли, и соли с аминокислотами, такими как, например, аргинин, лизин и тому подобное.
Наоборот, названные основно-аддитивные солевые формы могут превращаться в форму свободного основания обработкой соответствующей кислотой.
Термин “соли” также включает гидраты и формы с присоединением растворителя, которые соединения данного изобретения способны образовывать. Примеры таких форм представляют собой, например, гидраты, алкоголяты и тому подобное.
Данное соединение, применяемое в настоящем изобретении, может также существовать в его стереохимически изомерной форме, определяющей все возможные соединения, составленные из тех же самых атомов, связанных той же последовательностью связей, но имеющие различные трехмерные структуры, которые не являются взаимозаменяемыми. Если не оговорено особо или не указано, химическое обозначение соединений охватывает смесь всех стереохимически возможных изомерных форм, которыми указанные соединения могли обладать.
Указанная смесь может содержать все диастереомеры и/или энантиомеры основной молекулярной структуры указанного соединения. Все стереохимически изомерные формы соединений, примененных в данном изобретении либо в чистом виде, либо в смеси друг с другом, включены в объем данного изобретения.
Чистые стереоизомерные формы соединений и промежуточных продуктов, упоминаемых в настоящем описании, определены как изомеры, в основном свободные от других энантиомерных или диастереомерных форм той же самой молекулярной структуры указанных соединений или промежуточных продуктов. В частности, термин “стереоизомерно чистый” относится к соединениям или промежуточным продуктам, имеющим стереоизомерный избыток, равный, по меньшей мере, 80% (т.е. минимум 90% одного изомера и максимум 10% других возможных изомеров) вплоть до стереоизомерного избытка, равного 100% (т.е. 100% одного изомера и отсутствие других), точнее к соединениям или промежуточным продуктам, имеющим стереоизомерный избыток от 90% вплоть до 100%, еще точнее имеющим стереоизомерный избыток от 94% вплоть до 100% и наиболее точно имеющим стереоизомерный избыток от 97% вплоть до 100%. Термины "энантиомерно чистый" и "диастереомерно чистый" следует понимать аналогично, но в таком случае относящиеся к энантиомерному избытку, соответственно, диастереомерному избытку рассматриваемой смеси.
Чистые стереоизомерные формы соединений и промежуточных продуктов, примененных в данном изобретении, можно получать использованием процедур, известных в данной области. Например, энантиомеры можно отделять друг от друга селективной кристаллизацией их диастереомерных солей с оптически активными кислотами или основаниями. Их примерами являются винная кислота, дибензоилвинная кислота, дитолуоилвинная кислота и камфосульфоновая кислота. В альтернативном случае энантиомеры можно разделять хроматографическими методиками с применением хиральных стационарных фаз. Указанные стереохимически чистые изомерные формы можно также получать из соответствующих стереохимически чистых изомерных форм соответствующих исходных продуктов при условии, что реакция протекает стереоспецифически. Предпочтительно, если желателен определенный стереоизомер, указанное соединение должно быть синтезировано стереоспецифическими способами приготовления. Данные способы будут преимущественно использовать энантиомерно чистые исходные продукты.
Диастереомерные рацематы формулы (I, II или III) можно получать раздельно обычными способами. Соответствующие физические способы разделения, которые преимущественно можно использовать, представляют собой, например, селективную кристаллизацию и хроматографию, например колоночную хроматографию.
Абсолютная конфигурация каждого асимметрического центра, который может присутствовать в соединениях формулы (I), может быть указана стереохимическими дескрипторами R и S, причем данные R и S символы соответствуют правилам, описанным в Pure Appl. Chem. 1976, 45, 11-30.
Примеры
1. Способ получения метилового эфира (S)-(S)-(1-{5-[(4-аминометилбензолсульфонил)изобутиламино]-6-гидроксигексилкарбамоил}-2,2-дифенилэтил)карбаминовой кислоты (8)
Синтез трет-бутилового эфира (S)-(5-бензилоксикарбониламино-6-гидроксигексил)карбаминовой кислоты (2)
Коммерчески доступную (S)-2-бензилоксикарбониламино-6-трет-бутоксикарбониламиногексановую кислоту (1) (14,89 г) растворяли в 120 мл сухого ТГФ. Данный раствор охлаждали до -10°С. Медленно добавляли ВН3 (80 мл, 1 М в ТГФ), полученный раствор перемешивали в течение 1 часа при температуре ниже -5°C позволяли ему нагреваться при комнатной температуре в продолжение ночи. Реакцию гасили с помощью МеОН, смесь упаривали досуха и применяли как таковую в следующей реакции.
Синтез трет-бутилового эфира (S)-(5-амино-6-гидроксигексил)карбаминовой кислоты (3)
Остаток из первой реакции растворяли в МеОН (150 мл). Добавляли Pd/C (3 г). Смесь помещали в атмосферу Н2 и гидрировали в течение ночи при комнатной температуре. Смесь фильтровали через слой дикалита, упаривали досуха. Сырое соединение очищали колоночной хроматографией, используя EtOAc-MeOH(NH3) 93-7 в качестве элюента. После упаривания получали общий выход в 75% (от двух стадий).
Синтез трет-бутилового эфира (S)-(6-гидрокси-5-изобутиламиногексил)карбаминовой кислоты (4)
трет-Бутиловый эфир (S)-(5-амино-6-гидроксигексил)карбаминовой кислоты (3) (6,85 г) растворяли в 200 мл CH2Cl2. Добавляли изобутиральдегид (2,67 мл) и данный раствор перемешивали в течение 2 часов. Добавляли триацетоксиборогидрид натрия (1,1 экв.) и раствор перемешивали в течение 2 часов при комнатной температуре. Раствор промывали насыщенным NaHCO3. Мутную органическую фазу отделяли и упаривали досуха. Остаток очищали колоночной хроматографией, используя 99:1 EtOAc (100%) до EtOAc-MeOH(NH3) 99-1 в качестве элюента. Фракции, содержащие продукт, упаривали, получая 2,60 г (31%) указанного в заголовке соединения.
Синтез трет-бутилового эфира (S)-{5-[(4-цианобензолсульфонил)изобутиламино]-6-гидроксигексил}карбаминовой кислоты (5)
трет-Бутиловый эфир (S)-(6-гидрокси-5-изобутиламиногексил)карбаминовой кислоты (4) (1,85 г) растворяли в 50 мл CH2Cl2. Добавляли триэтиламин (1,05 экв.) и 4-цианобензолсульфонилхлорид (1 экв.) и смесь перемешивали в течение ночи. Добавляли насыщенный NaHCO3 (50 мл) и смесь энергично встряхивали. Органический слой отделяли, сушили над MgSO4, фильтровали и упаривали. Сырое соединение очищали колоночной хроматографией, используя EtOAc-гептан (1-3) в качестве элюента. Фракции, содержащие продукт, упаривали, получая (1,06 г, 36%) твердое вещество.
Синтез (S)-N-(5-амино-1-гидроксиметилпентил)-4-циано-N-изобутилбензолсульфонамида (6)
трет-Бутиловый эфир (S)-{5-[(4-цианобензолсульфонил)изобутиламино]-6-гидроксигексил}карбаминовой кислоты (5) (1,06 г) растворяли в 50 мл МеОН. Добавляли HCl (5-6 Н в изо-PrOH, 30 мл) и смесь перемешивали в течение ночи при комнатной температуре. Смесь упаривали досуха и применяли как таковую в следующей реакции.
Синтез метилового эфира (S)-(S)-(1-{5-[(4-цианобензолсульфонил)изобутиламино]-6-гидроксигексилкарбамоил}-2,2-дифенилэтил)карбаминовой кислоты (7)
(S)-N-(5-Амино-1-гидроксиметилпентил)-4-циано-N-изобутилбензолсульфонамид (6), полученный по предыдущей реакции, растворяли в 50 мл CH2Cl2. Добавляли ВОР (2 экв.) и триэтиламин (5 экв.). Через 10 минут добавляли (S)-2-метоксикарбониламино-3,3-дифенилпропионовую кислоту (1 экв.) и смесь перемешивали в течение 3 часов при комнатной температуре. ЖХМС/LCMS показала завершение реакции. Реакционную смесь промывали насыщенным NaHCO3. Водную фазу промывали снова 100 мл CH2Cl2. Объединенные органические слои сушили над MgSO4, фильтровали через дикалит и упаривали досуха. Остаток очищали колоночной хроматографией, используя смесь CH2Cl2-MeOH(NH3) (97:3). Соответствующую фракцию упаривали досуха (1,31 г, 84% выход от 2 стадий).
Синтез метилового эфира (S)-(S)-(1-{5-[(4-аминометилбензолсульфонил)изобутиламино]-6-гидроксигексилкарбамоил}-2,2-дифенилэтил)карбаминовой кислоты (8)
Метиловый эфир (S)-(S)-(1-{5-[(4-цианобензолсульфонил)изобутиламино]-6-гидроксигексилкарбамоил}-2,2-дифенилэтил)карбаминовой кислоты (7) (1,31 г) суспендировали в МеОН, содержащем NH3 (7 H). Добавляли водную суспензию Ra/Ni. Смесь помещали в атмосферу Н2 и перемешивали при комнатной температуре. После завершения реакции смесь упаривали досуха и остаток очищали препаративной ВЭЖХ-МС/HPLC-MS. После упаривания получали 0,435 г (34%) не совсем белого твердого вещества. ЖХ-МС: m/z=639; 1H-ЯМР (CDCl3): 7,78 ч.м. (д, J=8,01, 2H); 7,45 ч.м. (д, J=7,56, 2H); 7,35-7,15 ч.м. (м, 10 Н); 6,61 ч.м. (ушир.с, 1Н, NH); 5,58 ч.м. (д, J=8,65, 1H, NH); 4,86 ч.м. (дд, J=9,74, J=9,66, 1H); 4,42 ч.м. (д, J=10,65, 1H); 4,04 ч.м. (д, J=15,42, 1H); 4,02 ч.м. (д, J=15,58, 1H); 3,58 ч.м. (с, 3Н); 3,57-3,52 (м, 4Н); 3,11-2,8 (м, 3Н); 2,45 (м, 1Н); 1,89 (септ., J=7,11, 1H); 1,34 ч.м. (м, 2Н); 1,1 (м, 1Н); 0,99-0,96 ч.м. (м, 6Н); 0,95-0,75 (м, 2Н).
2. Вирусологические свойства соединения настоящего изобретения
Соединение, имеющее структурную формулу III, оценивали в анализе на клетках, используя МЕ4-LTR-EGFP клетки, по противовирусной активности. Анализ показал, что соединение проявляет потенциальную активность против ВИЧ по отношению к лабораторному штамму ВИЧ дикого типа (WT IIIB-2-001).
Из-за возрастающего появления штаммов ВИЧ, устойчивых к лекарственным средствам, данное соединение также оценивали