3-(1-нафтилметил)-4,5,6,7-тетрагидроиндазола гидрохлорид, средство, обладающее противомикробными свойствами
Иллюстрации
Показать всеИзобретение относится к области органической химии, а именно к новому биологически активному соединению класса индазола - 3-(1-нафтилметил)-4,5,6,7-тетрагидроиндазола гидрохлориду формулы 1. Соединение 1 получают взаимодействием 2-(1-нафтилацетил)-циклогексанона с гидразингидратом в среде изопропанола при кипячении с последующим выделением целевого продукта известными приемами. Соединение 1 представляет собой бесцветное кристаллическое вещество, легко растворимое в ДМСО и ДМФА, трудно растворимое в воде, спирте, хлороформе. Изобретение также относится к средству, обладающему противомикробным действием. Технический результат - соединение 1 проявляет выраженное ингибирующее действие относительно штаммов золотистого стафилококка и тормозит их рост в концентрации 0,5 мкг/мл, проявляет бактерицидный эффект в концентрации 2,0 мкг/мл, а также тормозит рост грибка Candida albicans в концентрации 2 мкг/мл и вызывает гибель штамма в концентрации 62,5 мкг/мл. ЛД50 при пероральном введении составила более 1000,0 мг/кг. 2 н.п. ф-лы, 1 табл., 2 пр.
Реферат
Изобретение относится к области органической химии, а именно к новому биологически активному соединению класса индазола - 3-(1-нафтилметил)-4,5,6,7-тетрагидроиндазола гидрохлориду формулы 1:
провляющему антимикробную активность, что позволяет предположить его использование в медицине в качестве антимикробного средства.
В практической медицине известен препарат фенилсалицилат, аналогичный по фармакологическому (противомикробному) действию предлагаемому соединению (см. Машковский М.Д., Лекарственные средства. - Харьков: Торгсин, 1998, т.2, с.418). Данный препарат взят в качестве эталона сравнения для предлагаемого решения.
Близкими по структуре к предлагаемому соединению являются 1,3-диарилциклоалканопиразолы (индазолы), представляющие собой ингибиторы циклооксигеназы и противовоспалительные агенты (см. Ferro M., Sui Z., Wachter M. Preparation of 1,3 and 2,3-diarylcycloalkano and cycloalkeno pyrazoles as selective inhibitors of cyclooxygenase-2 and antiflammatory agents. Pat. US 6083969; Chem. Abstracts, 2000, Vol.133, №7, 89521f). Ближайший среди них аналог имеет следующую структуру:
Сведения об антимикробной активности аналогов отсутствуют.
Более близкими структурными аналогами к заявляемым соединениям, взятыми за поототип, являются основания обшей формулы:
где R=4-СН3, 4-NO2 - замещенные фенилы (см. Михайловский А.Г., Алиев З.Г., Базина Н.Г., Пантюхин А.А., Вахрин М.И. 2-Ароилциклогексаноны в синтезе азолов, ХГС, 2010, №6, с.905-911). Их основное отличие по структуре от заявляемых соединений в том, что они содержат другие радикалы в положении 3 индазольного цикла и являются основаниями, а не гидрохлоридами. Данных об антимикробной активности этих соединений в литературе не имеется.
Задачей изобретения является получение нового соединения, обладающего противомикробными свойствами, и создание на его основе противомикробного средства для практического здравоохранения.
Техническая задача решается посредством настоящего изобретения и состоит в синтезе гидрохлорида 3-(1-нафтилметил)-4,5,6,7-тетрагидроиндазола (1) формулы:
проявляющего антимикробную активность в отношении бактерий Staphylococcus aureus и грибка Candida albicans.
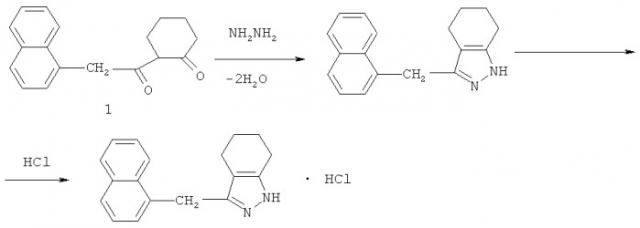
Соединение 1 получают взаимодействием 2-(2-нафтилацетил)-циклогексанона с гидразингидратом в среде изопропанола при кипячении в течение 1 часа с последующим выделением целевых продуктов известными приемами. Реакция идет по схеме, приведенной ниже.
Исходный дикетон (2-(1-нафтилацетил)-циклогексанон) получен по методике, использованной нами ранее для синтеза 2-ароилциклогексанонов (см. Михайловский А.Г., Алиев З.Г., Базина Н.Г., Пантюхин А.А., Вахрин М.И. 2-Ароилциклогексаноны в синтезе азолов, ХГС, 2010, №6, с.905-911) и использован в качестве промежуточного продукта без перекристаллизации.
Технический результат, получаемый при реализации изобретения, состоит в получении малотоксичного соединения с высоким выходом и высокой антимикробной активностью. Методика синтеза проста, исходные соединения легкодоступны.
Изобретение иллюстрируется нижеследующими примерами.
Пример 1. Синтез 3-(1-нафтилметил)-4,5,6,7-тетрагидроиндазола гидрохлорида.
К раствору 2,52 г (0,01 моль) 2-(1-нафтилацетил)-циклогексанона в 20,0 мл кипящего 2-пропанола прибавляли 0,7 мл (15,0 ммоль) кипящего (0,015 моль) 70% раствора гидразингидрата. Смесь кипятили 1 час, охлаждали до 20°C, разбавляли 100 мл ледяной воды, выпавший осадок растворяли в 150 мл этилацетата и пропусканием сухого газообразного НСl получали гидрохлорид соединения 1, который отфильтровывали, сушили и перекристаллизовывали из 2-пропанола. Выход 67%. Тпл. 205-206°C. Соединение 1 C18H18N2·HCl.
Найдено, %: C 72.27; H 6.22; N 9.26; Cl 11.75.
Вычислено, %: C 72.35; H 6.41; N9.37; Cl 11.86.
Соединение 1 представляет собой бесцветное кристаллическое вещество, легко растворимое в ДМСО и ДМФА, трудно растворимое в воде, спирте, хлороформе. Устойчиво при хранении в обычных условиях.
В ИК спектре основания соединения 1, снятого в пасте в вазелиновом масле, присутствуют полосы валентных колебаний групп NH индазольного цикла (3250 см-1). Получение основания вещества 1: водную суспензию обрабатывают избытком водного раствора аммиака, полученное основание отфильтровывают, тщательно промывая водой, и сушат.
Спектр ПМР гидрохлорида 1 снят в ДМСО-D6 (300 МГц), внутренний эталон - ГМДС. Спектр содержит (δ, м.д.): 1.61-1.78 мультиплет, 4Н, 5,6-(CH2)2; 2.49-2.63 мультиплет, 4Н, 4-CH2 и 7-CH2; 4.52 синглет (СН2-нафтил); 7.41-8.10, мультиплет (7Н, Ar); 10.02 синглет (NH+).
Пример 2. Антимикробная активность и токсичность.
Исследование биологической активности (токсичности и специфического действия) заявляемых соединений проводили на белых беспородных мышах массой 18-20 г и микроорганизмах Esherichia coli (1257) и Staphylococcus aureus (6538P, 906). Противогрибковое действие изучено на музейном штамме дрожжеподобного грибка Candida albicans, 264/624.
Определение средней летальной дозы (ЛД50) проводили по методу Г.Н.Першина путем однократного орального введения и наблюдения за поведением и гибелью животных в течение 7 суток. Противомикробное действие выявляли методом двукратных серийных разведений в соответствии с методикой изучения противомикробного действия препаратов (Першин Г.Н. Методы экспериментальной химиотерапии. - М.: Медицина, 1971, с.109). Для культивирования бактерий использовали рыбно-пептонный агар и бульон (pH 7,2-7,4); для культивирования дрожжеподобных грибков - бульон и агар Сабуро. Готовили исходные разведения микробных тел по оптическому стандарту мутности из суточной агаровой культуры. Для определения противомикробного (бактериостатического, бактерицидного и фунгицидного) действия микробную взвесь (микробная нагрузка равна 2,5×105 микробных тел в 1 мл питательной среды) вносили в приготовленные разведения препарата в питательной среде. Результаты опытов учитывали после 20-часового (ингибирующее) и 7-суточного (бактерицидное действие) термостатирования при 37°C - для бактерий, через 48 часов и 7 суток - для Candida albicans.
Противомикробную (фунгицидную) активность оценивали по минимально действующей концентрации. Максимально испытанная концентрация соединения составила 1000 мкг/мл. Эталоном сравнения служил известный в медицинской практике фенилсалицилат.
Проведенные исследования показали (см. таблицу), что соединение 1 проявляет выраженное ингибирующее действие относительно штаммов золотистого стафилококка и тормозит их рост в концентрации 0,5 мкг/мл, что активнее эталона (фенилсалицилата) в 1500 раз.
Концентрация 2,0 мкг/мл заявляемого соединения вызывает гибель испытанных штаммов золотистого стафилококка, т.е. соединение 1 проявляет бактерицидный эффект. В сравнении с бактерицидным действием эталона - фенилсалицилата - заявляемое соединения более активно в 1000 раз.
Кроме того, предлагаемое соединение тормозит рост грибка Candida albicans в концентрации 2,0 мкг/мл и вызывает гибель этого штамма в концентрации 62,5 мкг/мл. Препарат сравнения антигрибкового действия в отношении Candida albicans не проявляет.
Предлагаемое вещество не оказывает действия в отношении кишечной палочки (см. таблицу), что можно рассматривать как благоприятный фактор, способствующий сохранению микрофлоры кишечника.
| Таблица | ||||||
| Соединение | Противомикробная активность, мкг/мл | |||||
| Escherichia coli | Staphylococcus aureus | Candida albicans | ||||
| МИК* | МБК** | МИК* | МБК** | МИК* | МБК** | |
| 1 | - | - | 0,5 | 2,0 | 2,0 | 62,5 |
| фенилсалицилат | - | - | 750,0 | 2000,0 | - | - |
| контроль: ДМСО | рост | рост | рост | |||
| Примечание: препараты растворяли в диметилсульфоксиде (ДМСО); | ||||||
| «-» означает отсутствие противомикробного действия в испытанных концентрациях;*МИК - минимальная ингибирующая концентрация; | ||||||
| **МБК - минимальная бактерицидная концентрация. |
Острая токсичность определена перорально. Предлагаемое соединение является малотоксичным. При пероральном введении величина ЛД50 составила для него более 1000 мг/кг.
В связи с тем, что 3-(1-нафтилметил)-4,5,6,7-тетрагидроиндазола гидрохлорид обладает выраженным противомикробным действием в отношении бактерий Staphylococccus aureus и дрожжеподобного грибка Candida albicans, он может найти применение в практической медицине.
1. 3-(1-Нафтилметил)-4,5,6,7-тетрагидроиндазола гидрохлорид формулы 1:
2. Средство, обладающее противомикробными свойствами, представляющее собой 3-(1-Нафтилметил)-4,5,6,7-тетрагидроиндазола гидрохлорид формулы 1: