Агонистические антитела против notch3 и их применение для лечения notch3-ассоциированных заболеваний
Иллюстрации
Показать всеНастоящее изобретение относится к иммунологии и биотехнологии. Предложены: агонистическое антитело или его функционально активный фрагмен, которые специфически связываются с эпитопом, содержащим первый домен Lin12 Notch3, и активируют сигнальный путь Notch3. Описано меченое антитело и гуманизированное антитело на их основе. Предложены: кодирующая нуклеиновая кислота, клетка для получения антитела, содержащая указанную НК, а также вектор экспрессии. Описан способ получения антител путем культивирования клетки. Раскрыто применение антител для изготовления лекарственного средства для лечения Notch3-ассоциированных заболевания или нарушения. Описано применение антител для диагностики Notch3-ассоциированного заболевания или нарушения. Использование изобретения может найти применение в медицине в лечении и диагностике заболеваний CADASIL. 13 н. и 13 з.п. ф-лы, 11 ил., 6 табл., 11 пр.
Реферат
ПЕРЕКРЕСТНЫЕ ССЫЛКИ НА РОДСТВЕННЫЕ ЗАЯВКИ
Настоящая заявка заявляет приоритет на основании предварительной заявки США № 60/852861, поданной 19 октября 2006, и предварительной заявки США № 60/879218, поданной 6 января 2007, описания которых включены в данный документ в виде ссылки во всей полноте.
ОБЛАСТЬ ТЕХНИКИ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к агонистическим антителам против Notch3 и к их применению для улучшения, лечения или профилактики Notch3-ассоциированного заболевания или нарушения.
УРОВЕНЬ ТЕХНИКИ
Ген Notch впервые был описан в 1917 г., когда было обнаружено, что полотна крыльев штамма плодовой мушки Drosophila melanogaster имеют насечки (Morgan, Am Nat 51:513 (1917)). Спустя почти семьдесят лет ген клонировали и установили, что он кодирует клеточный поверхностный рецептор, играющий ключевую роль в развитии многих типов клеток и тканей Drosophila (Wharton et al., Cell 43:567 (1985)). Вскоре было обнаружено, что сигнальный путь Notch представляет собой механизм, опосредуемый контактированием клеток, и в эволюционном отношении является консервативным от дрозофилы до человека. Обнаружено, что рецепторы Notch участвуют во многих клеточных процессах, таких как дифференциация, решение о гибели клетки, поддержание стволовых клеток, двигательная активность клеток, пролиферация и апоптоз, в разных типах клеток в процессе развития и гомеостаза тканей (обзор можно найти в Artavanis-Tsakonas, et al., Science 268:225 (1995)).
У млекопитающих обнаружено четыре рецепторных белка Notch (обозначаемых Notch1-Notch4) и пять соответствующих лигандов (обозначаемых дельта-подобный лиганд-1 (DLL-1), дельта-подобный лиганд-3 (DLL-3), дельта-подобный лиганд-4 (DLL-4), Jagged-1 и Jagged-2). Гены рецептора Notch млекопитающих кодируют белки размером ~300 кДа, которые расщепляются при транспортировке к клеточной поверхности и существуют в виде гетеродимеров. Внеклеточный фрагмент рецептора Notch содержит тридцать четыре эпидермальных факторов роста (EGF)-подобных повторов и три повтора, обогащенных цистеином Notch/LIN12. Связь двух расщепляемых субъединиц осуществляется при участии последовательностей, находящихся непосредственно в N-концевой и C-концевой области участка расщепления, причем две указанные субъединицы составляют домены гетеродимеризации Notch (HD) (Wharton, et al., Cell 43:567 (1985); Kidd, et al., Mol Cell Biol 6:3431 (1986); Kopczynski, et al., Genes Dev 2:1723 (1988); Yochem, et al., Nature 335:547 (1988)).
В настоящее время пока не ясно, как сигнальный путь Notch регулируется разными рецепторами или как пять лигандов различаются по вкладу в передачу сигнала или регуляцию. Различия в передаче сигнала и/или регуляции могут определяться характером их экспрессии в разных тканях или разными условиями окружающей среды. Показано, что лигандные белки Notch, в том числе Jagged/Serrate и дельта/дельта-подобные, способны специфически связываться с участком повтора EGF и индуцировать рецептор-опосредованный сигнальный путь Notch (обзор опубликован Bray, Nature Rev Mol Cell Biol. 7:678 (2006), и Kadesch, Exp Cell Res. 260:1 (2000)). Из повторов EGF 10ый-12ый необходимы для связывания лиганда с рецептором Notch, а другие повторы EGF могут усиливать взаимодействие рецептора с лигандом (Xu, et al., J Biol Chem. 280:30158 (2005); Shimizu, et al., Biochem Biophys Res Comm. 276:385 (2000)). Хотя повторы LIN12 и домен димеризации не участвуют непосредственно в связывании лиганда, они играют важную роль в поддержании гетеродимерного белкового комплекса, предотвращая лиганд-независимое расщепление под действием протеазы и активацию рецептора (Sanche-Irizarry, et al., Mol Cell Biol. 24:9265 (2004); Vardar et al., Biochem. 42:7061 (2003)).
Самоподдержание и определение метаболического пути нормальных стволовых клеток из многих тканей, в том числе из ткани кишечника и нервной ткани, зависят от сигнального пути Notch (Fre, et al., Nature, 435: 964 (2005); van Es, et al., Nature, 435: 959 (2005); Androutsellis-Theotokis, et al., Nature, 442: 823 (2006)). Следовательно, агонистическое антитело Notch3 можно использовать для лечения дегенеративных заболеваний. CADASIL (церебральная аутосомно-доминантная артериопатия с подкорковыми инфарктами и лейкоэнцефалопатией) вызывает инсульт и деменцию, характерные признаки которых включают в себя подкорковые ишемические события и мультиинфарктную деменцию. Обнаружено, что CADASIL связана с локализацией мутантного гена в хромосоме 19 (Joutel, et al., Nature 383:707 (1996)). Joutel et al. идентифицировали у пациентов с CADASIL мутации, которые вызывают серьезное разрушение гена Notch 3, следовательно, пациенты с CADASIL могут иметь дефектный белок Notch3. К сожалению, данное заболевание, которое является в высокой степени инвалидизирующим и часто летальным, в основном остается недиагностированным, или диагностируется ошибочно как рассеянный склероз и болезнь Альцгеймера. Проводимые в настоящее время исследования имеют тенденцию демонстрировать, что данное состояние распространено гораздо шире, чем считалось вначале.
Другим примером Notch3-ассоциированного заболевания является семейная гемиплегическая мигрень (FHM), доминантно-аутосомная форма мигрени с предвестником эпилептического припадка, связанная с нарушением, расположенным в том же участке хромосомы 19, что и ген Notch3. Следует отметить, что более 30% пациентов, страдающих от CADASIL, также страдают от мигрени с предвестником эпилептического припадка. Однако последнее заболевание встречается приблизительно только у 5% населения, причем полученные результаты свидетельствуют о том, что ген Notch3 участвует в механизме данного состояния. Подобным образом, семейная парокситическая атаксия связана с геном, расположенным в том же участке хромосомы 19, и можно сделать вывод, что Notch3 участвует в развитии данного состояния. Другие состояния и заболевания, связанные с Notch3, включают в себя синдром Алагилля (Flynn, et al., J Pathol 204:55 (2004)).
В настоящее время проводят исследования, чтобы идентифицировать другие заболевания и состояния, связанные с недостаточностью экспрессии и/или сигнального пути Notch3. Поскольку существует большое число заболеваний человека, связанных с сигнальным путем Notch 3, важно определить новые способы профилактики и лечения данных заболеваний. Настоящее изобретение предлагает новые агонистические антитела против Notch3, которые можно использовать для удовлетворения данной потребности медицины.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение предлагает новые агонистические антитела и их фрагменты, которые специфически связываются с эпитопом человеческого рецептора Notch3 в домене LIN12. Другой аспект данного изобретения включает в себя эпитоп-связывающий участок и антитела, которые связывают такой же эпитоп, как и антитела настоящего изобретения. Антитела настоящего изобретения активируют Notch3-опосредованный сигнальный путь через рецептор Notch3 независимо от связывания лиганда.
Данное изобретение предлагает аминокислотные последовательности вариабельных участков тяжелых и легких цепей антител и соответствующие им нуклеотидные последовательности. Другое воплощение данного изобретения включает в себя последовательности CDR указанных антител.
Другое воплощение настоящего изобретения включает в себя клеточные линии и векторы, несущие последовательности антител настоящего изобретения.
Настоящее изобретение также включает в себя эпитоп, распознаваемый агонистическими антителами данного изобретения. Кроме того, настоящее изобретение включает в себя антитела, которые связывают данный эпитоп. Воплощения включают в себя эпитоп Notch3, содержащий домен Lin12, последовательность которого, по меньшей мере, на 80%, 85%, 90% или 95% идентична SEQ ID NO:10. Более конкретно, эпитоп Notch3 содержит SEQ ID NO:11. Настоящее изобретение включает в себя агонистические антитела, которые связывают данный эпитоп.
Другое воплощение настоящего изобретения относится к применению указанных антител в производстве лекарственного средства или композиции для лечения Notch3-ассоциированных заболеваний и нарушений, связанных, например, с инактивацией рецептора.
Другое воплощение настоящего изобретения относится к применению указанных антител для лечения Notch3-ассоциированных заболеваний или нарушений, связанных, например, с инактивацией рецептора, включающему в себя компенсацию указанных дефектов, например, путем активации сигнального пути Notch3 независимо от связывания лиганда. Notch3-ассоциированные нарушения могут включать в себя, без ограничения, CADASIL, семейную гемиплегическую мигрень (FHM), семейную парокситическую атаксию, синдром Алагилля и другие дегенеративные заболевания.
КРАТКОЕ ОПИСАНИЕ ФИГУР
На фиг.1 изображена аминокислотная последовательность Notch3. Участок повтора EGF простирается от аминокислотного остатка 43 до аминокислотного остатка 1383; домен LIN12 простирается от аминокислотного остатка 1384 до аминокислотного остатка 1503; и домен димеризации простирается от аминокислотного остатка 1504 до аминокислотного остатка 1640.
На фиг.2 (A-H) приведено сравнительное изображение аминокислотных последовательностей человеческих Notch1, Notch2, Notch3 и Notch4.
На фиг.3 показан процент идентичности Notch 1, Notch 2, Notch 3 и Notch 4.
На фиг.4A и 4B изображены последовательности вариабельных участков тяжелой и легкой цепи моноклонального антитела MAb 256A-13 против Notch3 (SEQ ID NO: 2), причем участки CDR подчеркнуты.
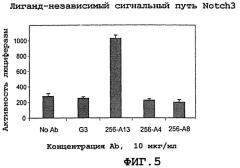
На фиг.5 приведены результаты люциферазного репортерного анализа примера 5, демонстрирующие активирующее действие MAb против Notch3 на рецептор Notch3.
На фиг.6 показано влияние агонистических антител Notch3 на металлопротеазное расщепление Notch3.
На фиг.7 изображено эпитопное картирование связывающего участка 256A-13 из конструкций гибридных белков Notch3-Fc.
На фиг.8 приведено сравнительное изображение полученной рекомбинантным методом последовательности, кодирующей лидерный пептид Notch3, и нативной последовательности, кодирующей лидерный пептид Notch3 (номер доступа в NCBI GenBank: NM_000435), демонстрирующее, что рекомбинантная последовательность, кодирующая лидерный пептид Notch, несет изменения в нуклеотидном составе (8A) и обуславливает изменения транслируемой аминокислотной последовательности (8B). На фиг.8C изображен домен LIN12, а на фиг.8D изображен эпитоп субдомена LIN12.
На фиг.9 изображено получение конструкции с переставленными доменами методом PCR-SOE. Прямоугольники со стрелками обозначают праймеры ПЦР. Незакрашенные прямоугольники относятся к последовательности Notch3. Закрашенные прямоугольники относятся к последовательности Notch1.
На фиг.10 изображены аминокислотные последовательности, используемые при эпитопном картировании домена LIN12 Notch3 из MAb 256A-13.
На фиг.11 изображены аланиновые сканирующие пептиды, используемые для линейного эпитопного картирования 256A-13.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Данное изобретение не ограничивается описанными здесь конкретными методами, схемами, клеточными линиями, векторами или реагентами, поскольку они могут варьировать. Кроме того, используемая в данном документе терминология предназначена только для описания конкретных воплощений и не ограничивает объем настоящего изобретения. В данном описании и в прилагающейся формуле изобретения, если контекст не указывает иначе, единственное число включает в себя множественное, например термин "клетка-хозяин" включает в себя совокупность таких клеток-хозяев. Если не указано иначе, все используемые здесь технические и научные термины, а также все сокращения имеют традиционные значения, известные рядовым специалистам в области данного изобретения. В данном описании приводятся примеры способов, устройств и материалов, однако при осуществлении настоящего изобретения можно использовать любые способы и материалы, подобные или эквивалентные описанным.
Все упомянутые здесь патенты и публикации включены в данное описание в виде ссылки в степени, допускаемой законом для описания и раскрытия указанных в них белков, ферментов, векторов, клеток-хозяев и методов, пригодных для применения в настоящем изобретении. Однако приведенную здесь информацию не следует рассматривать как допущение, что настоящее изобретение дает право расценивать эту информацию как уровень техники и противопоставлять ее предыдущему изобретению.
Определения
Термины, используемые по тексту данной заявки, следует интерпретировать в их традиционных значениях, известных рядовому специалисту в данной области. Однако нижеследующие термины авторы данной заявки предлагают использовать в конкретных, указанных ниже значениях.
Фраза "практически идентичный" в отношении последовательности полипептидной цепи антитела может означать, что последовательность антитела, по меньшей мере, на 70%, или 80%, или 90%, или 95%, идентична сравниваемой полипептидной последовательности. В отношении нуклеотидной последовательности данный термин может означать, что последовательность нуклеотидов, по меньшей мере, на 85%, или 90%, или 95%, или 97% идентична сравниваемой нуклеотидной последовательности.
Термин "идентичность" или "гомология" следует понимать, как процент аминокислотных остатков в последовательности-кандидате, идентичных остаткам последовательности, с которой сравнивают последовательность-кандидат, определяемый после выравнивания последовательности и введения пробелов, если это необходимо для достижения максимального процента идентичности всей последовательности, причем консервативные замены не рассматриваются как часть идентичности последовательности. N- или C-концевые удлинения или вставки не должны истолковываться как уменьшение идентичности или гомологии. Способы выравнивания и компьютерные программы для их осуществления хорошо известны в данной области. Идентичность последовательности можно определить с помощью программы для анализа последовательностей.
Термин "антитело" используется в самом широком смысле, а именно он охватывает моноклональные антитела (в том числе полноразмерные моноклональные антитела), поликлональные антитела, и полиспецифичные антитела (например, биспецифичные антитела), а также фрагменты антител, обладающие желательной биологической активностью. Антитела (Ab) и иммуноглобулины (Ig) представляют собой гликопротеины, имеющие одинаковые структурные особенности. Тогда как антитела обладают специфичностью связывания по отношению к конкретной мишени, иммуноглобулины включают в себя и антитела, и другие антитело-подобные молекулы, не обладающие специфичностью по отношению к мишени. Антитела данного изобретения могут относиться к любому типу (например, IgG, IgE, IgM, IgD, IgA и IgY), классу (например, IgG1, IgG2, IgG3, IgG4, IgA1 и IgA2) или подклассу. Нативные антитела и иммуноглобулины, как правило, представляют собой гетеротетрамерные гликопротеины размером приблизительно 150000 дальтон, которые состоят из двух идентичных легких (L) цепей и двух идентичных тяжелых (H) цепей. Каждая тяжелая цепь содержит на одном конце вариабельный домен (VH), за которым следует ряд константных доменов. Каждая легкая цепь содержит на одном конце вариабельный домен (VL), а на другом конце константный домен.
В данном описании термин "антитело против Notch3" относится к антителу, которое специфически связывается с человеческим Notch3, активируя сигнальный путь Notch 3 независимо от лиганда.
Термин "вариабельный" в применении к домену антитела означает, что последовательности некоторых участков вариабельных доменов сильно различаются у разных антител и отвечают за специфическое связывание конкретного антитела с конкретной мишенью. Однако на протяжении вариабельных доменов антител вариабельность распределяется не равномерно. Она концентрируется в трех сегментах, называемых участки, определяющие комплементарность (CDR; т.е. CDR1, CDR2 и CDR3), или гипервариабельные участки, которые присутствуют в вариабельных доменах как легкой, так и тяжелой цепей. Более консервативные фрагменты вариабельных доменов называют каркасными участками (FR). Все вариабельные домены нативных тяжелых и легких цепей содержат четыре участка FR, которые, как правило, имеют β-складчатую конфигурацию и соединяются тремя CDR, образующими петлеобразное соединение и, в некоторых случаях, часть β-складчатой структуры. CDR одной цепи удерживаются вместе в непосредственной близости участками FR и вместе с CDR другой цепи участвуют в формировании участка связывания антитела с мишенью (см. Kabat, et al. Sequences of Proteins of Immunological Interest, National Institute of Health, Bethesda, Md. (1987)). Если не указано иначе, в данном описании для нумерации аминокислотных остатков иммуноглобулинов используется система нумерации аминокислотных остатков иммуноглобулинов Kabat, et al.
Термин "фрагмент антитела" относится к фрагменту полноразмерного антитела, как правило, к участку, связывающему мишень, или к вариабельному участку. Примеры фрагментов антител включают в себя фрагменты F(ab), F(ab'), F(ab')2 и Fv. Фраза "функциональный фрагмент или аналог" антитела относится к соединению, обладающему количественной биологической активностью, подобной биологической активности полноразмерного антитела. Например, Функциональный фрагмент или аналог антитела против Notch3 способен связываться с рецептором Notch3, предотвращая или существенно снижая способность рецептора связываться с лигандами или инициировать передачу сигнала. В данном описании термин "функциональный фрагмент" в применении к антителам относится к фрагментам Fv, F(ab) и F(ab')2. Фрагмент "Fv" представляет собой димер, состоящий из вариабельного домена одной тяжелой и вариабельного домена одной легкой цепи, находящихся в тесной нековалентной связи (димер VH-VL). В данной конфигурации три CDR каждого вариабельного домена взаимодействуют, образуя участок связывания с мишенью на поверхности димера VH-VL. Вместе шесть CDR определяют способность антитела специфически связываться с мишенью. Однако даже один вариабельный домен (или половина Fv, содержащая только три CDR, специфичных к мишени) обладает способностью распознавать и связывать мишень, хотя и с более низким сродством, чем целый связывающий участок.
Фрагменты антител "одноцепочечный Fv" или "sFv" содержат VH и VL домены антитела, причем указанные домены находятся в одной полипептидной цепи. Как правило, полипептид Fv также содержит полипептидный линкер между доменами VH и VL, позволяющий sFv формировать структуру, необходимую для связывания мишени.
Термин "диатела" относится к маленьким фрагментам антител, содержащим два антиген-связывающих участка, причем указанные фрагменты в одной полипептидной цепи содержат вариабельный домен тяжелой цепи (VH), соединенный с вариабельным доменом легкой цепи (VL). Путем применения линкера, который является слишком коротким, чтобы позволить спариться двум доменам, расположенным на одной цепи, домены вынуждают спариваться с комплементарными доменами другой цепи с формированием двух антиген-связывающих участков.
Фрагмент F(ab) содержит константный домен легкой цепи и первый константный домен (CH1) тяжелой цепи. Фрагменты F(ab') отличаются от фрагментов F(ab) добавлением нескольких остатков по карбоксильному концу домена СН1 тяжелой цепи, в том числе одного или нескольких остатков цистеина в шарнирном участке антитела. Фрагменты F(ab') получают путем расщепления дисульфидной связи, образованной остатками цистеина шарнирного участка, в продукте расщепления пепсином F(ab')2. Специалистам в данной области известны и другие химические способы соединения фрагментов антител.
Термин "моноклональное антитело" в данном описании относится к антителу, полученному из популяции практически гомогенных антител, т.е. из популяции, отдельные антитела которой являются идентичными за исключением возможных природных мутаций, которые могут присутствовать в минорных количествах. Моноклональные антитела в соответствии с настоящим описанием включают в себя "химерные" антитела (иммуноглобулины), в которых часть тяжелой и/или легкой цепи идентична или гомологична соответствующей последовательности антитела, полученного от животного конкретного вида или принадлежащего к конкретному классу или подклассу антител, а остальная часть цепи (цепей) идентична или гомологична соответствующей последовательности антитела, полученного от животного другого вида или принадлежащего к другому классу или подклассу антител, а также фрагменты таких антител, обладающие желательной биологической активностью (патент США № 4816567; и Morrison, et al., Proc Natl Acad Sci USA 81:6851 (1984)). Моноклональные антитела обладают высокой специфичностью и направлены против одного участка мишени. Кроме того, в отличие от традиционных (поликлональных) препаратов антител, которые обычно состоят из разных антител, направленных против разных детерминант (эпитопов), каждое моноклональное антитело направлено против одной детерминанты мишени. Помимо специфичности преимуществом моноклональных антител является возможность их синтеза в гибридомной культуре, что позволяет избежать загрязнения другими иммуноглобулинами. Определение "моноклональный" указывает на то, что антитело получено из практически гомогенной популяции антитела, и не должно истолковываться как отнесение к какому-либо конкретному способу получения. Например, моноклональные антитела, пригодные для применения в настоящем изобретении, можно выделить из фаговых библиотек антител, используя хорошо известные методы. Исходные моноклональные антитела для применения в соответствии с настоящим изобретением можно получить с помощью гибридомного метода, впервые описанного Kohler, et al, Nature 256:495 (1975), или с помощью рекомбинантных методов.
"Гуманизированные" формы нечеловеческих (например, мышиных) антител представляют собой химерные иммуноглобулины, цепи иммуноглобулинов или их фрагменты (такие как Fv, Fab, Fab', F(ab')2 или другие мишень-связывающие субпоследовательности антител), которые содержат минимальную последовательность нечеловеческого иммуноглобулина. Как правило, практически все вариабельные домены гуманизированного антитела из, по меньшей мере, одного или, чаще всего, двух, содержат все или почти все участки CDR, соответствующие нечеловеческому иммуноглобулину, и все или почти все участки FR, соответствующие матричной последовательности человеческого иммуноглобулина. Гуманизированное антитело также может содержать, по меньшей мере, часть константного участка (Fc) иммуноглобулина, как правило, выбранного из человеческой матрицы иммуноглобулина.
Термины "клетка", "клеточная линия" и "клеточная культура" включают в себя потомство. Следует понимать, что не все потомство может быть полностью идентичным родительским клеткам по содержанию ДНК вследствие присутствия преднамеренных или непреднамеренных мутаций. В объем данного изобретения также входит вариантное потомство, обладающее такими же функциями или биологическими свойствами, как и исходная трансформированная клетка. "Клетки-хозяева", используемые в настоящем изобретении, обычно представляют собой прокариотические или эукариотические клетки.
"Трансформацию" клеточного организма, клетки или клеточной линии с помощью ДНК осуществляют путем введения ДНК в клетку-мишень либо в виде внехромосомного элемента, либо посредством встраивания в хромосому, с помощью способа, позволяющего сохранить способность ДНК к репликации. "Трансфекция" клетки или организма молекулой ДНК представляет собой поглощение ДНК, например, вектора экспрессии, клеткой или организмом независимо от того, экспрессируется ли фактически какая-либо кодирующая последовательность или нет. Термины "трансфицированная клетка-хозяин" и "трансформированная клетка-хозяин" относятся к клетке, в которую введена ДНК. Клетка, называемая "клетка-хозяин", может быть прокариотической или эукариотической. Типичные прокариотические клетки-хозяева включают в себя разные штаммы E. coli. Типичные эукариотические клетки-хозяева представляют собой клетки млекопитающих, такие как клетки яичника китайского хомячка или человеческие клетки. Вводимая последовательность ДНК может относиться к тому же виду, что и клетка-хозяин, или к другому виду, или она может представлять собой гибридную последовательность ДНК, содержащую несколько чужеродных и несколько гомологичных ДНК.
Термин "вектор" относится к конструкции ДНК, содержащей последовательность ДНК, функционально связанную с подходящей контрольной последовательностью, способной обеспечивать экспрессию ДНК в подходящем хозяине. Такие контрольные последовательности включают в себя промотор, обеспечивающий транскрипцию, необязательную последовательность оператора, контролирующую такую транскрипцию, последовательность, кодирующую подходящие участки связывания мРНК рибосомой, и последовательности, контролирующие терминацию транскрипции и трансляции. Вектор может представлять собой плазмиду, фаговую частицу или просто потенциальную геномную вставку. После трансформации в подходящего хозяина вектор может реплицироваться и функционировать независимо от генома хозяина, или в некоторых случаях, он может интегрироваться в геном как таковой. В настоящем описании термины "плазмида" и "вектор" иногда используются как взаимозаменяемые, поскольку плазмида представляет собой наиболее широко используемую форму вектора. Однако предполагается, что данное изобретение включает в себя и другие, известные в данной области, формы векторов, которые выполняют эквивалентную функцию.
"Млекопитающее", подлежащее лечению, может представлять собой любое животное, относящееся к классу млекопитающих, и включает в себя человека, ручных и сельскохозяйственных животных, отличных от человека приматов, а также диких животных, спортивных животных или домашних животных, таких как собаки, лошади, кошки, коровы и др.
Термин "маркер" в данном описании относится к детектируемому соединению или детектируемой композиции, которые могут быть конъюгированы непосредственно или через другие соединения с молекулой или белком, например антителом. Маркер сам может быть детектируемым (например, радиоизотопные метки или флуоресцентные метки) или, как в случае ферментного маркера, может катализировать детектируемое химическое изменение субстратного соединения или субстратной композиции.
В данном описании термин "твердая фаза" обозначает неводную основу, к которой может прилипать антитело настоящего изобретения. Примеры твердых фаз, входящих в объем данного изобретения, включают в себя фазы, полученные частично или полностью из стекла (например, стекло с контролируемым размером пор), полисахариды (например, агароза), полиакриламиды, полистирол, поливиниловый спирт и кремнийорганические соединения. В некоторых воплощениях, в зависимости от контекста, к твердой фазе может относиться лунка аналитического планшета; в других воплощениях твердая фаза может представлять собой колонку для очистки (например, колонку для аффинной хроматографии).
В данном описании термин "Notch3-опосредованое нарушение" относится к состоянию или заболеванию, которое характеризуется дефектной или пониженной экспрессией рецептора Notch3, а именно данный термин может включать в себя состояния, ассоциированные с дегенеративными заболеваниями, такие как CADASIL, FHM, семейная парокситическая атаксия, синдром Аллагиля и другие дегенеративные заболевания.
Рецептор NOTCH3 как иммуноген, вызывающий образование антител
Растворимые мишени или их фрагменты можно использовать в качестве иммуногенов для получения антител. Антитело направлено против представляющей интерес мишени. Предпочтительно, мишенью является биологически важный полипептид, и введение антитела млекопитающему, страдающему от заболевания или нарушения, может оказывать благоприятное терапевтическое действие на млекопитающего. В качестве иммуногена для получения антител можно использовать целые клетки. Иммуноген можно получить с помощью рекомбинантных или синтетических способов. Иммуноген также можно выделить из природного источника.
В случае трансмембранных молекул, таких как рецепторы, в качестве иммуногена можно использовать их фрагменты (например, внеклеточный домен рецептора). Альтернативно, в качестве иммуногена можно использовать клетки, экспрессирующие трансмембранные молекулы. Такие клетки можно получить из природного источника (например, из линии раковых клеток) или путем трансформации исходных клеток с использованием рекомбинантных методов, обеспечивающих повышенную экспрессию трансмембранной молекулы. Специалистам в данной области известны и другие формы иммуногенов, которые можно использовать для получения антител.
Альтернативно, ген или кДНК, кодирующую человеческий рецептор Notch3, можно клонировать в плазмиде или другом векторе экспрессии и экспрессировать в любой системе экспрессии с помощью способов, хорошо известных специалистам в данной области. Способы клонирования и экспрессии рецептора Notch3, а также кодирующей его нуклеотидной последовательности, описаны в литературе (см., например, патенты США №№ 5821332 и 5759546). Вследствие вырожденности генетического кода можно использовать большое число нуклеотидных последовательностей, кодирующих рецепторный белок или полипептиды Notch3. Нуклеотидную последовательность можно варьировать путем отбора сочетаний, исходя из возможных вариантов кодонов. Данные сочетания получают в соответствии с триплетным генетическим кодом, используемым в нуклеотидной последовательности, кодирующей природный рецептор Notch3, причем можно рассматривать все полученные вариации. Любой из указанных полипептидов можно использовать для иммунизации животного с целью получения антител, связывающих человеческий рецептор Notch3.
Вследствие высокой консервативности аминокислотной последовательности Notch3 в качестве иммуногенов для получения антител можно использовать также рекомбинантные белки Notch3 других видов. Сравнение человеческого и мышиного Notch3 показывает, что свыше 90% аминокислотных последовательностей двух видов являются идентичными.
Иммуногенный рецептор Notch3 при необходимости можно экспрессировать в виде гибридного белка, содержащего рецептор Notch3, соединенный с гибридизационным фрагментом. Гибридизационный фрагмент часто облегчает очистку белка, например позволяет выделить и очистить гибридный белок методом аффинной хроматографии, и, кроме того, его также можно использовать для повышения иммуногенности. Гибридные белки можно получить путем культивирования рекомбинантной клетки, трансформированной гибридной нуклеотидной последовательностью, кодирующей белок с присоединенным по карбоксильному или амино-концу гибридизационным фрагментом. Гибридизационные фрагменты могут включать в себя, без ограничения, участки Fc иммуноглобулинов, глутатион-S-трансферазу, β-галактозидазу, полигистидиновый фрагмент, способный связываться с двухвалентным ионом металла, и белок, связывающий мальтозу.
Рекомбинантный рецепторный белок Notch3, как описано в примере 1, используют для иммунизации мышей с целью получения гибридом, продуцирующих моноклональные антитела настоящего изобретения. Примеры полипептидов включают в себя полноразмерную последовательность SEQ ID NO:1 и ее фрагменты или их варианты.
Получение антител
Антитела настоящего изобретения можно получить с помощью любого подходящего способа, известного в данной области. Антитела настоящего изобретения могут включать в себя поликлональные антитела. Способы получения поликлональных антител известны опытным специалистам (Harlow, et al., Antibodies: a Laboratory Manual, Cold spring Harbor Laboratory Press, 2nd ed. (1988)), содержание данной публикации включено в настоящее описание в виде ссылки во всей полноте).
Например, как описано в примере 1, иммуноген можно вводить разным животным-хозяевам, включащим в себя, без ограничения, кроликов, мышей, крыс и др., индуцируя продукцию сыворотки, содержащей поликлональные антитела, специфичные к антигену. Введение иммуногена может включать в себя одну или несколько инъекций иммунизирующего средства и, при необходимости, адъюванта. Для усиления иммунологического ответа можно использовать разные адъюванты, которые зависят от вида хозяина и включают в себя, без ограничения, адъювант Фрейнда (полный и неполный), минеральные гели, такие как гидроксид алюминия, поверхностно-активные вещества, такие как лизолецитин, плюрониловые полиолы, полианионы, пептиды, масляные эмульсии, гемоцианин лимфы улитки, динитрофенол и потенциально полезные человеческие адъюванты, такие как BCG (бацилла Кальметта-Герена) и Corynebacterium parvum. Другие примеры пригодных для использования адъювантов включают в себя адъювант MPL-TDM (монофосфорил липида A, синтетический дикориномиколат трегалозы). Схемы иммунизации хорошо известны в данной области и могут проводиться любыми известными в данной области способами, которые вызывают иммунный ответ у выбранного животного-хозяина. Адъюванты также хорошо известны в данной области.
Как правило, иммуноген (вместе с адъювантом или без адъюванта) вводят млекопитающему путем нескольких подкожных или внутрибрюшинных инъекций, либо внутримышечно или внутривенно. Иммуноген может включать в себя полипептид Notch3, гибридный белок или их варианты. В зависимости от природы полипептида (т.е. от степени гидрофобности, степени гидрофильности, стабильности, суммарного заряда, изоэлектрической точки и др.), иногда полезно конъюгировать иммуноген с белком, который заведомо является иммуногенным для иммунизируемого млекопитающего. Такое конъюгирование проводят либо химическими способами путем дериватизации активных химических функциональных групп на подлежащих конъюгированию иммуногенах или иммуногенных белках с образованием ковалентной связи, либо с помощью способов получения гибридных белков, или других способов, известных специалистам в данной области. Примеры таких иммуногенных белков включают в себя, без ограничения, гемоцианин лимфы улитки, овальбумин, сывороточный альбумин, бычий тиреоглобулин, ингибитор соевого трипсина и различные пептиды T-хелперов. Как указано выше, для усиления иммунного ответа можно использовать разные адъюванты.
Антитела настоящего изобретения включают в себя моноклональные антитела. Моноклональные антитела представляют собой антитела, распознающие один антигенный участок. Их единообразная специфичность делает моноклональные антитела гораздо более полезными, чем поликлональные антитела, которые обычно содержат антитела, распознающие несколько разных антигенных участков. Моноклональные антитела можно получить с использованием гибридомной технологии, такой как описанная в Kohler, et al., Nature 256:495 (1975); Патент США № 4376110; Harlow, et al., Antibodies: A Laboratory Manual, Cold spring Harbor Laboratory Press, 2nd ed. (1988) и Hammerling, et al., Monoclonal Antibodies and T-Cell Hybridomas, Elsevier (1981), методов рекомбинантных ДНК или других методов, известных специалистам в данной области. Другие примеры методов, которые можно использовать для получения моноклональных антител, включают в себя, без ограничения, метод гибридом человеческих B-клеток (Kosbor, et al., Immunology Today 4:72 (1983); Cole, et al., Proc Natl Acad Sci USA 80:2026 (1983)), и метод EBV-гибридом (Cole, et al., Monoclonal Antibodies and Cancer Therapy, pp. 77-96, Alan R. Liss (1985)). Такие антитела могут относиться к любому классу иммуноглобулинов, в том числе IgG, IgM, IgE, IgA, IgD, а также к любому подклассу. Гибридомы, продуцирующие MAb данного изобретения, можно культивировать in vitro или in vivo.
В гибридомном методе хозяина, такого как мышь, гуманизированная мышь, мышь с человеческой иммунной системой, хомяк, кролик, верблюд или любого другого подходящего животного-хозяина иммунизируют, чтобы вызвать образование лимфоцитов, продуцирующих или способных продуцировать антитела, которые специфически связываются с белком, используемым для иммунизации. Альтернативно, лимфоциты можно иммунизировать in vitro. Затем лимфоциты гибридизуют с клетками миеломы, используя подходящий гибридизующий агент, такой как полиэтиленгликоль, и получают гибридомные клетки (Goding, Monoclonal Antibodies: Principles and Practice, Academic Press, pp.59-103 (1986)).
Как правило, для получения гибридом, продуцирующим антитела, используют либо лимфоциты периферической крови ("PBL"), если нужны человеческие клетки, либо клетки селезенки или лимфатического узла, если требуются клетки млекопитающего, отличного от человека. Затем лимфоциты гибридизуют с иммортализованной клеточной линией, используя подходящий гибридизующий агент, такой как полиэтиленгликоль, и получают гибридомные клетки (Goding, Monoclonal Antibodies: Principles and Practice, Academic Press, pp. 59-103 (1986)). Иммортализованные клеточные линии, как правило, представляют собой трансформированные