Лечение миодистрофии дюшена
Иллюстрации
Показать всеИзобретение относится к области органической химии и фармацевтики и касается нового производного бензоксазола - 5-(этилсульфонил)-2-(нафталин-2-ил)бензо[d]оксазола и фармацевтической композиции для лечения или профилактики миодистрофии Дюшена или миодистрофии Беккера. Изобретение обеспечивает высокую эффективность лечения. 3 н.п. ф-лы, 1 табл., 4 ил., 50 пр.
Реферат
Настоящее изобретение относится к способу лечения миодистрофии Дюшена.
Миодистрофия Дюшена (МДД) представляет собой общее, генетическое нейромышечное заболевание, связанное с прогрессирующей деградацией мышечной функции, впервые описанное более 150 лет назад французским неврологом Duchenne de Boulogne, именем которого названо это заболевание. МДД характеризуется как вызываемое мутацией в гене дистрофина X-сцепленное рецессивное нарушение, которым страдает 1 из 3500 мужчин. Ген является наибольшим в геноме человека, содержит 2,6 миллионов пар нуклеотидов ДНК и включает 79 экзонов. Приблизительно 60% мутаций дистрофина представляют собой большие вставки или делеции, которые приводят к ошибкам сдвига рамки считывания в нисходящем направлении, тогда как приблизительно 40% представляют собой точечные мутации или небольшие перестановки со сдвигом рамки считывания. У подавляющего большинства пациентов с МДД отсутствует белок дистрофина. Миодистрофия Беккера представляет собой намного более мягкую форму МДД, вызываемую уменьшением количества или изменением размера белка дистрофина. Высокая частота МДД (1 из 10000 сперматозоидов или яйцеклеток) означает, что генетический скрининг никогда не устранит заболевание, так что эффективная терапия крайне желательна.
Существует ряд природных и разработанных моделей МДД на животных, и они предоставляют основу для преклинических исследований (Allamand, V. & Campbell, K. P. Animal models for muscular dystrophy: valuable tools for the development of therapies. Hum. Mol. Genet. 9, 2459-2467 (2000)). Хотя во всех моделях на мышах, кошках и собаках существуют мутации в гене МДД, и эти модели характеризуются биохимической дистрофинопатией, сходной с дистрофинопатией, наблюдаемой у людей, они демонстрируют неожиданную и значительную вариабельность с точки зрения их фенотипа. Подобно людям, модели на собаках (миодистрофия золотых ретриверов и немецких короткошерстных легавых) обладают тяжелым фенотипом; эти собаки, как правило, умирают от сердечной недостаточности. Собаки являются лучшей фенокопией заболевания человека, и их рассматривают как лучший критерий для преклинических исследований. К сожалению, разведение этих животных является дорогостоящим и трудоемким, а клиническое течение может варьировать от потомства к потомству.
Наиболее широко используемой моделью являются мыши mdx ввиду их доступности, короткого периода вынашивания, времени до созревания и относительно низкой стоимости (Bulfield, G., Siller, W. G, Wight, P. A. & Moore, K. J. X chromosome-linked muscular dystrophy (max) in the mouse. Proc. Natl Acad. Sci. USA 81, 1189-1192 (1984)).
Со времени открытия гена МДД приблизительно 20 лет назад достигнуты различные степени успеха в лечении МДД в преклинических исследованиях на животных, некоторые из которых подтвердились и у людей. Существующие в настоящее время стратегии лечения можно грубо подразделить на три группы: первая - подходы генной терапии; вторая - клеточная терапия; и последняя - фармакологическая терапия. Основанные на генах и клетках способы лечения предоставляют фундаментальное преимущество, устраняя необходимость в отдельной коррекции вторичных дефектов/патологии (например, контрактур), особенно если лечение начато на начальных стадиях течения заболевания. К сожалению, эти подходы сталкиваются с рядом технических препятствий. Сообщалось об иммунологическом ответе на вирусные векторы, миобласты и вновь синтезированный дистрофин, а также токсичности, отсутствии стабильной экспрессии и сложности доставки.
Фармакологические подходы к лечению миодистрофии отличаются от основанных на генах и клетках подходов тем, что они не предназначены для доставки недостающего гена и/или белка. В основном, в фармакологических стратегиях в попытке улучшить фенотип используют лекарственные средства/молекулы такими способами, как снижение воспаления, улучшение гомеостаза кальция и улучшение пролиферации или коммитирования мышечных предшественников. Эти стратегии предоставляют то преимущество, что они обеспечивают легкую системную доставку и могут обходить многие иммунологические и/или токсикологические проблемы, которые связаны со способами лечения на основе векторов или клеток. Хотя исследования с кортикостероидами и кромогликатом натрия для уменьшения воспаления, дантроленом для поддержания гомеостаза кальция и кленбутеролом для увеличения мышечной силы дали многообещающие результаты, ни один из этих потенциальных способов лечения еще не продемонстрировал эффективности при лечении МДД.
Альтернативным фармакологическим подходом является активирующая терапия. Активирующая терапия основана на увеличении экспрессии альтернативных генов для замены дефектного гена, и она особенно эффективна, когда на ранее отсутствующий белок развивается иммунный ответ. В качестве потенциальной терапии МДД предложено повышение экспрессии утрофина, аутосомного паралога дистрофина (Perkins & Davies, Neuromuscul Disord, S1: S78-S89 (2002), Khurana & Davies, Nat Rev Drug Discov 2:379-390 (2003)). Когда у трансгенных мышей mdx сверхэкспрессирован утрофин, он локализуется у сарколеммы мышечных клеток и восстанавливает компоненты ассоциированного с дистрофином белкового комплекса (DAPC), предотвращающего развитие дистрофии и, в свою очередь, приводящего к функциональному улучшению скелетной мускулатуры. Показано, что аденовирусная доставка утрофина собакам предотвращает патологию. Стимуляция повышенной экспрессии вскоре после рождения в модели на мышах может являться эффективной, и при повсеместной экспрессии утрофина не наблюдается токсичности, что является обещающим для переноса этого способа лечения людям. Повышения экспрессии эндогенного утрофина до достаточных уровней для снижения патологии можно достигать посредством доставки способных к диффузии низкомолекулярных соединений.
Авторы заявки при прогностических скринингах нашли группу соединений, которые повышают экспрессию эндогенного утрофина и, таким образом, могут быть полезными для лечения МДД.
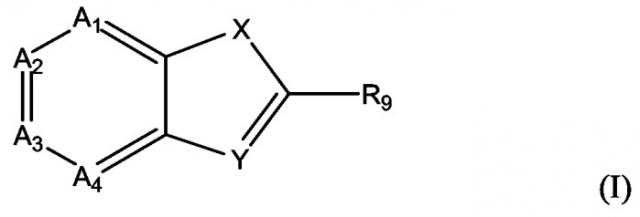
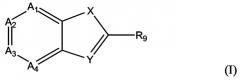
В соответствии с изобретением авторы предлагают применение соединения формулы (I)
в которой
A1, A2, A3 и A4, которые могут быть одинаковыми или различными, представляют собой N или CR1,
X представляет собой дивалентную группу, выбранную из O, S(O)n, C=W, NR4, NC(=O)R5 и CR6R7,
W представляет собой O, S, NR20,
Y представляет собой N или CR8,
один из R4, R5, R6, R8, R9 и NR20 представляет собой - L-R3, в котором L представляет собой одинарную связь или линкерную группу,
дополнительно, R3 - R9, которые могут быть одинаковыми или различными, независимо представляют собой водород или заместитель и
R20 представляет собой водород, гидроксил, алкил, необязательно замещенный арилом, алкокси, необязательно замещенный арилом, арил, CN, необязательно замещенный алкокси, необязательно замещенный арилокси, необязательно замещенный алканоил, необязательно замещенный ароил, NO2, NR30R31, в котором R30 и R31, которые могут быть одинаковыми или различными, представляют собой водород, необязательно замещенный алкил или необязательно замещенный арил; дополнительно, один из R30 и R31 может представлять собой необязательно замещенный алканоил или необязательно замещенный ароил,
n представляет собой целое число от 0 до 2,
кроме того,
когда каждая из соседних пар A1 - A4 представляет собой CR1, тогда соседние атомы углерода, вместе с их заместителями могут образовывать кольцо B,
когда X представляет собой CR6R7, R6 и R7, вместе с атомом углерода, к которому они присоединены, могут образовывать кольцо C,
когда один из A1-A4 представляет собой CR1, и R1 представляет собой COR16, R16 предпочтительно представляет собой алкокси или NR10R11,
или их фармацевтически приемлемых солей,
для получения лекарственного средства для терапевтического и/или профилактического лечения миодистрофии Дюшена, миодистрофии Беккера или кахексии.
Соединения формулы I могут существовать в форме таутомеров, энантиомеров и диастереомеров, которые все включены в объем изобретения.
Некоторые соединения формулы I являются новыми. В соответствии с изобретением авторы изобретения также предлагают те соединения формулы I, которые являются новыми, вместе со способом их получения, содержащими их композициями, а также их применение в качестве фармацевтических средств.
Некоторые из соединений, попадающих в рамки формулы I, являются известными, как таковые, но не в качестве фармацевтических средств. В соответствии с изобретением авторы изобретения заявляют в качестве фармацевтических средств соединения, известные в данной области как таковые, но ранее не описанные для применения в качестве фармацевтических средств.
Все соединения формулы I можно получать традиционными способами. Способы получения гетероароматических кольцевых систем хорошо известны в данной области. В частности, методы синтеза обсуждаются в Comprehensive Heterocyclic Chemistry, Vol. 1 (Eds.: AR Katritzky, CW Rees), Pergamon Press, Oxford, 1984 и в Comprehensive Heterocyclic Chemistry II: A Review of the Literature 1982-1995. The Structure, Reactions, Synthesis, and Uses of Heterocyclic Compounds, Alan R. Katritzky (Editor), Charles W. Rees (Editor), E.F.V. Scriven (Editor), Pergamon Pr, June 1996. Другие общие ресурсы, которые могут помочь синтезу представляющих интерес соединений, включают March's Advanced Organic Chemistry: Reactions, Mechanisms, and Structure, Wiley-Interscience; 5th edition (15 января 2001 года). Особую значимость имеют способы синтеза, обсуждаемые в WO 2006/044503.
Некоторые общие способы синтеза являются такими, как изложено ниже.
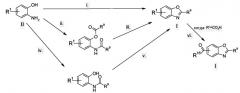
Бензоксазолы формулы I или их фармацевтически приемлемые соли можно получать из соединений формулы II.
Схема 1
Условия реакции:
i. R9CO2H (или R9COCl), PPA, нагревание; или R9COCl, диоксан, микроволны, затем NaOH
ii. R9COCl, пиридин, комн. темп.
iii. TsOH, ксилолы
iv. R9CO2H, HATU, пиридин, DMF
v. PPA, нагревание
vi. HATU, DMF, iPr2NEt, алкилNH2, комн. темп.
Получение бензоксазола I можно проводить различными способами, как проиллюстрировано выше.
Например, реакцией соединения формулы II с ацильным производным, таким как кислота или хлорангидрид, и нагреванием в подходящем растворителе и при подходящей температуре в присутствии кислотного катализатора, например полифосфорной кислоты. Это проиллюстрировано выше как стадия (i).
Реакцию можно проводить в апротонном растворителе, предпочтительно полярном апротонном растворителе, например тетрагидрофуране, и температуре от -10°C до +150°C. Как правило, реакцию можно проводить при температуре кипения растворителя с обратным холодильником при нормальном давлении.
Альтернативно, соединение формулы II можно сначала подвергать реакции с избытком ацильного производного R9COX (где X представляет собой, например, Cl) так, чтобы ацилирование проходило и по кислороду, и по азоту. Это можно осуществлять, например, посредством реакции в пиридине при комнатной температуре (стадия ii). Затем может происходить замыкание кольца с образованием соединения формулы II в последующей стадии замыкания кольца в которой, например, дважды ацилированный продукт нагревают в ксилолах в присутствии кислотного катализатора, такого как сульфоновая кислота (стадия iii).
Другой иллюстративный пример получения соединения формулы I показан посредством стадий iv и v. Сначала амин конденсируют с кислотой с применением пептидного конденсирующего реагента. Доступные конденсирующие реагенты хорошо известны специалистам в данной области и включают HBTU, TBTU и HATU. Получение амида в присутствии подходящего конденсирующего реагента происходит, например, в DMF в присутствии нуклеофильного катализатора, такого как пиридин.
Когда R1 = CO2H, эту кислоту можно конденсировать с амином, как показано на стадии (vi). Подходящие условия конденсации включают применение HATU в DMF в присутствии iPr2NEt, R16NH2 при комнатной температуре.
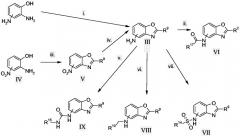
Соединения, в которых шестичленное кольцо замещено амидным производным, представляют особый интерес. Их можно получать из промежуточного аминного производного III.
Схема 2
Условия реакции:
i. Как для (i) схемы 1
ii. R17COCl, пиридин (или NEt3, DCM); или R9CO2H, HATU, пиридин, DMF
iii. Как для (i) схемы 1
iv. SnCl2, EtOH, нагревание; или Pd/C, H2, IMS; или Fe, NH4Cl, IMS/вода, нагревание
v. R9NCO, DCM, комн. темп.
vi. NaBH(OAc)3, R10CHO, DCE, комн. темп.
vii. R14SO2Cl, пиридин, DCM, комн. темп.
Промежуточный амин III можно синтезировать или с применением способа, описанного на схеме 1, стадии (i), где R1 = NH2, или альтернативно, в двухстадийном процессе, как определено стадиями (iii) и (iv) схемы 2. Нитрозамещенное производное бензоксазола V получают из нитрозамещенного фенильного производного IV, также способом, аналогичным способу, проиллюстрированному на схеме 1, стадии 1, а затем нитропроизводное бензоксазола V восстанавливают на последующей стадии с получением промежуточного амина III. Специалисту хорошо известны подходящие способы восстановления нитрогруппы с получением амина. Взятые в качестве примера способы восстановления NO2 до NH2 включают Sn/HCl или H2/Pd/C в подходящем растворителе, например этаноле, при температуре от 0° до 80°C или нагревании в присутствии железа, NH4Cl в промышленном метиловом спирте/воде.
Затем промежуточный амин III можно конденсировать в соответствии с необходимостью.
Конденсацией амина III с ацильным производным можно получать амидные производные формулы VI. Этого можно достигать, например, реакцией соответствующего хлорангидрида в пиридине или в CH2Cl2 (стадия ii).
Реакцией амина III с подходящим сульфонилхлоридом, например, в CH2Cl2 в присутствии пиридина при комнатной температуре можно получать сульфонамидные производные VII.
Применяя подходящую стратегию восстановительного аминирования, можно получать аминные производные VIII. Способы восстановительного аминирования хорошо известны в данной области. Например, они включают реакцию амина с подходящим альдегидом и триацетоксиборогидридом натрия в 1,2-дихлорэтане.
Производные мочевины формулы IX можно получать, например, реакцией амина III с подходящим изоцианатом, например, при комнатной температуре в CH2Cl2.
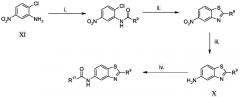
Бензотиазолы формулы X или их фармацевтически приемлемые соли можно получать из соединений формулы XI.
Схема 3
Условия реакции:
i. R9COCl, пиридин, комн. темп.
ii. Na2S, S8, IMS, нагревание
iii. Fe, NH4Cl, IMS, нагревание
iv. R17COCl, пиридин (или NEt3, DCM); или R17CO2H, HATU, пиридин, DMF
Соединения формулы XI можно преобразовывать в соответствующий амид, например, реакцией с соответствующим хлорангидридом в пиридине (стадия (i)) или посредством применения соответствующего пептидного конденсирующего реагента. Такие способы хорошо известны специалистам в области, как обсуждалось в данном документе выше.
Затем амид можно преобразовывать в нитробензотиазол формулы XII посредством способа в виде одной реакции, включающего реакции с Na2S, S8 при повышенной температуре в промышленном метиловом спирте. Нитропроизводное XII можно восстанавливать, как обсуждалось ранее, и полученный первичный амин преобразовывать способом, аналогичным первичному амину на схеме 2 стадиях (ii), (v), (vi) и (vii).
Схема 4
Условия реакции:
i. R9CO2H, PPA, нагревание; или R9COCl, пиридин; затем PPA, нагревание
ii. SnCl2, IMS, нагревание; или Pd/C, H2, IMS
iii. R17COCl, пиридин и т.д. (как для схемы 1)
iv. R4NH2, ДМСО, основание, нагревание
v. Дитионит натрия, THF/вода; также смотри (ii)
Бензимидазолы формулы XII можно получать в соответствии со схемой 4. Реакция диаминофенильного производного формулы XIII с ацильным производным, таким как кислота или хлорангидрид в подходящем растворителе и при подходящей температуре в присутствии кислотного катализатора, например полифосфорной кислоты, дает производное бензимидазола формулы XII. Это проиллюстрировано выше, как стадия (i). Затем нитрогруппу можно восстанавливать и преобразовывать с получением другой функциональности, как обсуждалось выше в настоящем документе.
Альтернативно, бензимидазолы можно получать реакцией динитросоединения формулы XIV, где X представляет собой уходящую группу, предпочтительно галоген, такой как хлор или фтор, с амином, например, в ДМСО при повышенной температуре в присутствии основания. Затем можно осуществлять последующее избирательное восстановление одной нитрогруппы с применением дитионита натрия в THF/воде с получением диамина формулы XV. Затем можно осуществлять замыкание кольца с образованием бензимидазолов и преобразование нитрогруппы, как проиллюстрировано и обсуждалось выше.
Схема 5
Условия реакции:
i. Na2S гидрат, MeOH, NH4Cl, вода; или Na2S2O4/EtOH; или SnCl2, EtOH
ii. Как для (i) схемы 1; или R9COCl, пиридин; затем PPA, нагревание
iii. SnCl2, EtOH, нагревание
iv. R1B(OH)2, Pd(PPh3)4, K2CO3, диоксан/вода, микроволны
v. R17COCl, пиридин, комн. темп.
vi. EtOC(S)SK, пиридин, нагревание
vii. SOCl2; или POCl3
viii. R3B(OH)2, Pd(PPh3)4, K2CO3, растворитель
ix. PPA, нагревание в R2CO2H
Бензоксазолы формулы XVI можно получать способами, аналогичными способам, описанным ранее. Например, способ, проиллюстрированный выше (ix), включает нагревание соединения формулы XVII в подходящем растворителе в присутствии кислотного катализатора и подходящего ацильного производного, например карбоновой кислоты.
Бензоксазолы формулы XVIII и XIX можно синтезировать из соответствующих нитросоединений формулы XX. Восстановление нитросоединения XX дает соответствующий аминоспирт XXI (например, с применением Sn/HCl, или любого из других подходящих способов, хорошо известных специалистам в данной области). Затем можно осуществлять получение бензоксазолов реакцией аминоспирта с соответствующим ацильным производным с применением любого из описанных выше в настоящем документе способов.
Затем, для получения дальнейших производных, для оксазолов формулы XXIII, в которой X = Br, можно применять реакцию сочетания Сузуки. Примером соответствующих условий, в которых образуется бензоксазол формулы XIX, является R1B(OH)2, Pd(PPh3)4, K2CO3, диоксан/вода, микроволны. Специалист в данной области хорошо знаком с реакциями сочетания Сузуки и может легко манипулировать условиями с получением широкого множества соединений.
Для оксазолов, получаемых на стадии (ii), у которых X = NO2, нитрогруппу можно восстанавливать до соответствующего амина с применением любого из обсуждаемых в настоящем документе способов, хорошо известных специалистам в данной области. Затем амин можно преобразовывать, например, с применением любого из способов, обсуждаемых для схемы 2 выше, с получением, например, соединения формулы XVIII.
Альтернативно, бензоксазолы формулы XVIII также можно получать из соединения формулы XX через тиокарбамат XXII, который получают нагреванием соединения формулы XX с EtOC(S)SK в пиридине. Соединение формулы XXII можно преобразовывать в хлорид формулы XXIII, например, с применением хорошо известных реагентов, таких как SOCl2 или POCl3. Сочетание Сузуки, например, с применением условий, проиллюстрированных для стадии viii выше, дает бензоксазол формулы XVIII.
В указанных выше способах может являться необходимым защищать любые функциональные группы, например гидрокси- или аминогруппы, присутствующие в исходных веществах, таким образом, для получения соединения формулы I может являться необходимым удалять одну или несколько защитных групп.
Подходящие защитные группы и способы их удаления представляют собой группы, описанные, например, в "Protective Groups in Organic Synthesis" by T. Greene and P.G.M. Wutts, John Wiley and Sons Inc, 1991. Например, гидроксигруппы можно защищать арилметильными группами, такими как фенилметил, дифенилметил или трифенилметил; ацильными группами, такими как ацетил, трихлорацетил или трифторацетил; или в качестве тетрагидропиранильных производных. Подходящие защитные группы для аминогрупп включают арилметильные группы, такие как бензил, (R,S)-α-фенилэтил, дифенилметил или трифенилметил, и ацильные группы, такие как ацетил, трихлорацетил или трифторацетил. Можно использовать общепринятые способы снятия защиты, включая гидрогенолиз, кислотный или основный гидролиз или фотолиз. Например, арилметильные группы можно удалять посредством гидрогенолиза в присутствии металлического катализатора, например палладия на активированном угле. Тетрагидропиранильные группы можно расщеплять гидролизом в кислых условиях. Ацильные группы можно удалять гидролизом основанием, таким как гидроксид натрия или карбонат калия, или группу, такую как трихлорацетил, можно удалять восстановлением, например, цинком и уксусной кислотой.
Соединения формулы I и их соли можно выделять из их реакционных смесей с применением общепринятых способов.
Соли соединений формулы I можно получать реакцией свободной кислотой или ее соли, или свободного основания или его соли, или производного с одним или несколькими эквивалентами подходящего основания или кислоты. Реакцию можно проводить в растворителе или среде, в которой соль нерастворима, или в растворителе, в котором соль растворима, например этаноле, тетрагидрофуране или диэтиловом эфире, который можно удалить под вакуумом или посредством лиофильной сушки. Реакция также может представлять собой обменный процесс, или ее можно проводить на ионообменной смоле.
Фармацевтически приемлемые соли соединений формулы I включают соли щелочных металлов, например натриевые и калиевые соли; соли щелочноземельных металлов, например соли кальция и магния; соли элементов группы III, например соли алюминия; и аммонийные соли. Соли с подходящими органическими основаниями, например соли с гидроксиламином; низшими алкиламинами, например метиламином или этиламином; с замещенными низшими алкиламинами, например с гидроксизамещенными алкиламинами; или с моноциклическими гетероциклическими соединениями с азотом, например с пиперидином или морфолином; и соли с аминокислотами, например с аргинином, лизином и т.д, или их N-алкильными производными; или с аминосахаром, например с N-метил-D-глюкамином или глюкозамином. Предпочтительны нетоксические физиологически приемлемые соли, хотя также пригодны другие соли, например, для выделения или очистки продукта.
Диастереоизомеры можно разделять общепринятыми способами, например хроматографией или фракционной кристаллизацией. Различные оптические изомеры можно выделять разделением рацемической или другой смеси соединений общепринятыми способами, например фракционной кристаллизацией или ВЭЖХ. Альтернативно желаемые оптические изомеры можно получать реакцией соответствующих оптически активных исходных веществ в условиях, которые не вызывают рацемизации.
Заместители, которые может представлять алкил, включают метил, этил, бутил, например втор-бутил.
Галоген может представлять собой F, Cl, Br и I, особенно Cl.
Примеры заместителей, которые в соединении формулы 1 может представлять R3, включают алкил, алкокси или арил, каждый, необязательно замещенный одним или несколькими, предпочтительно от одного до трех, заместителями R2, которые могут быть одинаковыми или различными.
Кроме того, когда L представляет собой одинарную связь, R3 может представлять собой тиоалкил, необязательно замещенный алкилом или необязательно замещенный арилом,
тиоарил, в котором арил необязательно замещен,
необязательно замещенный арил,
гидроксил,
NO2,
CN,
NR10R11,
галоген,
SO2R12,
NR13SO2R14,
C(=W)R16,
OC(=W)NR10R11,
NR15C(=W)R17,
P(=O)OR40R41,
где R10, R11, R12, R13, R14, R15, R16, R17, R40 и R41, которые могут быть одинаковыми или которые могут быть одинаковыми или различными, представляют водород, алкил, необязательно замещенный необязательно замещенным арилом, необязательно замещенный арил,
кроме того,
NR10R11 вместе с азотом, к которому они присоединены, могут образовывать кольцо,
R12 может иметь то же значение, что и NR10R11,
когда R17 представляет собой NR10R11, тогда R10 и R11, которые могут быть одинаковыми или различными, могут представлять собой водород, CO-алкил и необязательно замещенный CO арил,
R16 и R17, которые могут быть одинаковыми или различными, каждый могут представлять собой
алкил, замещенный одним или несколькими из галогена, необязательно замещенным арилом алкокси или необязательно замещенным арилом,
необязательно замещенный арилокси,
арил или NR10R11,
и когда R16 или R17 представляют собой NR10R11, один из R10 и R11 может дополнительно представлять собой необязательно замещенный CO-алкил или необязательно замещенный CO-арил,
и в дополнение к определениям, общим с R17, R16 может представлять собой гидрокси.
Примеры заместителей, которые могут представлять собой R1 и R2, которые могут быть одинаковыми или различными, включают:
алкил, необязательно замещенный одним или нескольким галогенами, алкокси или необязательно замещенными арилами, тиоарилами или арилокси,
алкокси, необязательно замещенный необязательно замещенным алкилом или необязательно замещенным арилом,
гидроксил,
OC(=W)NR10R11,
необязательно замещенный арил,
тиоалкил, необязательно замещенный алкилом или необязательно замещенным арилом,
тиоарил, в котором арил является необязательно замещенным,
NO2,
CN,
NR10R11,
галоген,
SO2R12,
NR13SO2R14,
C(=W)R16,
NR15C(=W)R17,
где R10, R11, R12, R13, R14, R15, R16 и R17, которые могут быть одинаковыми или различными, представляют собой водород, алкил, необязательно замещенный необязательно замещенным арилом, необязательно замещенный арил,
кроме того,
NR10R11 вместе с азотом, к которому они присоединены, могут образовывать кольцо,
R12 может иметь то же значение, что и NR10R11,
когда R17 представляет собой NR10R11, тогда R10 и R11, которые могут быть одинаковыми или различными, могут представлять собой водород, CO-алкил и необязательно замещенный CO арил,
R16 может представлять собой гидрокси, алкокси или NR10R11,
R17 может представлять собой алкил, замещенный одним или несколькими из галогена, алкокси, необязательно замещенный арил или NR10R11,
и когда R17 представляет собой NR10R11, тогда NR10R11 может представлять собой водород, CO-алкил и необязательно замещенный CO арил.
Когда L представляет собой линкерную группу, примеры линкерных групп, которые может представлять собой L, включают:
O, S, (CO)nNR18,
алкилен, алкенилен, алкинилен, каждый из которых может необязательно прерываться одним или несколькими из O, S, NR18 или одной или несколькими одинарными, двойными или тройными C-C-связями,
одинарную или двойную связь -N-N-,
R18 представляет собой водород, алкил, COR16.
Когда L представляет собой (CO)nNR18, n может представлять собой 0, 1 или 2, когда n представляет собой 1 или 2, R18 предпочтительно представляет собой водород.
Хотя область изменения R4, R5, R6, R7 и R8 является большой, предпочтительно R4, R5, R6, R7 и R8 представляют собой водород, алкил или необязательно замещенный арил.
Y предпочтительно представляет собой N, а X представляет собой O, S или NR4. Т.е. предпочтительно соединения формулы I представляют собой бензоксазол, бензтиазол или бензимидазол.
Хотя любой из R4, R6, R8 или R9 может представлять собой -L-R3-, в предпочтительных соединениях -L-R3 представляет собой R9.
Алкил может представлять собой любую алкильную цепь. Алкил включает неразветвленный и разветвленный, насыщенный и ненасыщенный алкил, а также циклический алкил, такой как циклопропил, циклобутил, циклопентил, циклогексил и циклогептил. Однако предпочтительно, когда какой-либо из заместителей представляет собой алкил, алкил является насыщенным, линейным или разветвленным и содержит от 1 до 10 атомов углерода, предпочтительно от 1 до 8 атомов углерода и более предпочтительно - от 1 до 6 атомов углерода. Когда какой-либо из заместителей представляет собой алкил, особенно предпочтительной группой является циклоалкил, например циклопропил, циклобутил, циклопентил, циклогексил и циклогептил.
Арил может представлять любую ароматическую систему. Предпочтительно в соединениях формулы I, арил представляет собой ароматический углеводород или 5-10-членный ароматический гетероцикл, содержащий в качестве составляющих кольца кроме углерода от 1 до 4 атомов, выбранных из атома кислорода, атома серы и атома азота. Авторы изобретения предпочитают гетероциклы, содержащие один или два гетероатома. Ароматические гетероциклы, которые можно указать, включают фуран, тиофен, пиррол, пиридин.
Особенно предпочтительно, когда арил представляет собой ароматический углеводород, арил представляет собой 6-10-членную моноциклическую или бициклическую систему, например фенил или нафталин.
Насыщенные и ненасыщенные гетероциклы, которые можно указать, включают циклы, содержащие от 4 до 7 кольцевых атомов, предпочтительно 5 или 6 кольцевых атомов, предпочтительно содержащие от одного до двух гетероатомов, выбранных из N, S и O. Гетероциклы, которые можно указать, включают пирролидин, пиперидин, тетрагидрофуран, пиперазин и морфолин. Особенно предпочтительны N-содержащие гетероциклы, например, когда NR10R11 образует гетероциклическое кольцо.
Как подробно описано выше, когда каждая из соседних пар A1 - A4 представляет собой CR1, соседние атомы углерода, вместе с их заместителями могут образовывать кольцо B. Также, когда X представляет собой CR6R7, R6 и R7, вместе с углеродом, к которому они присоединены, могут образовывать кольцо C. Предпочтительно кольцо B и/или кольцо C представляет собой насыщенное или ненасыщенное 3-10-членное карбоциклическое или гетероциклическое кольцо.
Особенно предпочтительное кольцо B представляет собой бензольное кольцо.
Особенно предпочтительное кольцо C представляет собой 3-10-членное насыщенное или ненасыщенное карбоциклическое кольцо.
Авторы изобретения особенно предпочитают соединения, в которых, по меньшей мере, один R1 представляет собой NR15C(=W)R17, более конкретно - группу NR15COR17.
Авторы изобретения также предпочитают соединения, в которых, по меньшей мере, один R1 представляет собой CONR10R11.
Для одной группы из особенно предпочтительных соединений, по меньшей мере, один R1 представляет собой амидную группу NHCOR17; где R17 выбран из:
C1-C6-алкила,
C1-C6-алкила, замещенного фенилом,
C1-C6-алкила, замещенного C1-C6-алкокси,
C1-C6-галогеналкила,
C1-C6-перфторалкила,
фенила, необязательно замещенного одним или несколькими из галогена, C1-C6-алкила, C1-C6-алкокси, амино, (C1-C6-алкил)амино, ди(C1-C6-алкил)амино или фенила,
CH:CH фенила,
нафтила, пиридинила, тиофенила и фуранила.
Авторы изобретения предпочитают соединения, в которых один или оба из R1 и R2 отличаются от -COOH.
Для другой группы особенно предпочтительных соединений, по меньшей мере, один R1 представляет собой группу NR15CONR10R11, в которой R10 и R11, которые могут быть одинаковыми или различными, выбраны из необязательно замещенного арила, алкила и необязательно замещенного CO-арила. Особенно предпочтительная группа, которую может представлять, по меньшей мере, один из R1, представляет собой NHCONHR15, и R15 выбран из фенила, алкила от C1 до C6 и CO-фенила, необязательно замещенного одним или несколькими галогенами.
Для другой группы особенно предпочтительных соединений, по меньшей мере, один R1 представляет собой алкил от C1 до C6, необязательно замещенный фенилом или 5- или 6-членный насыщенный или ненасыщенный гетероцикл, содержащий от одного до двух гетероатомов, выбранных из N, S и O.
Для другой группы особенно предпочтительных соединений, по меньшей мере, один R1 представляет собой COR16, и R16 представляет собой C1-C6-алкокси, амино, (C1-C6-алкил)амино или ди(C1-C6-алкил)амино.
Для другой группы особенно предпочтительных соединений, по меньшей мере, один R1 представляет собой:
NO2,
галоген,
амино или (C1-C6-алкил)амино или ди(C1-C6-алкил)амино, в котором алкил от C1 до C6 представляет собой необязательно замещенный фенил или 5- или 6-членный насыщенный или ненасыщенный гетероцикл,
NHSO2(C1-C6)-алкил, NHSO2фенил,
SO2(C1-C6)-алкил,
фенил, необязательно замещенный от C1 до C6 (C1-C6)-алкокси,
5-10-членный, насыщенный или ненасыщенный, моно- или бициклический гетероцикл, содержащий от 1 до 3 гетероатомов, выбранных из N, S и O.
Для группы R3 также существует широкая область изменения. Предпочтительно R3 представляет собой арил и необязательно замещен заместителями R2 в количестве от одного до трех, которые могут быть одинаковыми или различными.
Особенно предпочтительно, R3 представляет собой 5-10-членную ароматическую моно- или бициклическую систему, особенно углеводородную 5-10-членную ароматическую моно- или бициклическую систему, например бензол или нафталин.
Альтернативно 5-10-членная ароматическая моно- или бициклическая система может представлять собой гетероциклическую систему, содержащую до трех гетероатомов, выбранных из N, O и S, например тиофен, фуран, пиридин или пиррол.
Предпочтительно заместитель(и) R2 выбран из:
C1-C6-алкила, необязательно замещенного тиофенилом или фенокси, каждый, необязательно замещенный галогеном,
C1-C6-алкокси,
фенила,
C1-C6-тиоалкила,
тиофенила, необязательно замещенного галогеном,
NO2,
CN,
NR10R11, в котором R10 и R11, которые могут быть одинаковыми или различными, представляют собой водород, C1-C6-алкил, или вместе с азотом, к которому они присоединены, формируют 5-7-членное кольцо, которое может содержать один или несколько дополнительных гетероатомов, выбранных из N, O и S,
галогена,
SO2R12, в котором R12 представляет собой 5-7-членное кольцо, которое может содержать один или несколько дополнительных гетероатомов, выбранных из N, O и S,
NHCOR17, в котором R17 представляет собой
C1-C6-алкил, необязательно замещенный:
фенилом или галогеном, или
фенилом, необязательно замещенным C1-C6-алкокси, карбокси или галогеном,
или 5- или 6-членным насыщенным или ненасыщенным гетероциклом;
фенил или 5- или 6-членный насыщенный или ненасыщенный гетероцикл, необязательно замещенный галогеном, алкокси от C1 до C6, карбокси или группой SO2NR10R11.
Особенно предпочтительно, когда R2 представляет собой NR10R11, где NR10R11 представляет собой N-пиррол, N-пиперидин, N'(C1-C6)-алкил-N-пиперазин или N-морфолин.
Предпочтительно линкерная группа L представляет собой:
-NH.NH-
-CH=CH
-NCOR16, в котором R16 предста