Получение гликопротеинов
Иллюстрации
Показать всеИзобретение относится к области биотехнологии, конкретно к получению гликопротеинов, и может быть использовано для крупномасштабного получения фактора свертывания крови IX в культуре клеток. Способ включает культивирование клеток млекопитающего, содержащих ген, кодирующий фактор свертывания крови IX, в среде для культивирования клеток, которая содержит приблизительно от 10 нМ до 600 нМ марганца при условиях и в течение времени, достаточного для осуществления экспрессии фактора свертывания крови IX. Изобретение позволяет получить экспрессированный фактор свертывания крови IX с повышенной степенью гликозилирования по сравнению со степенью гликозилирования, наблюдаемой при использовании таких же условий и такой же среды, но в отсутствие марганца. 2 н. и 23 з.п. ф-лы, 8 ил., 4 табл., 5 пр.
Реферат
Настоящее изобретение относится к способу получения гликопротеинов в среде для культивирования клеток, которая содержит марганец, и к среде для культивирования клеток для применения согласно такому способу.
ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
Настоящая заявка находится одновременно на рассмотрении, имеет по меньшей мере одного общего автора и испрашивает приоритет в соответствии с предварительной заявкой на патент США №60/830,658, поданной 13 июля 2006 года, содержание которой включено в данную заявку посредством ссылки в полном объеме.
ПРЕДПОСЫЛКИ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Белки и полипептиды становятся все более важными терапевтическими агентами. В большинстве случаев такие белки и полипептиды получают в культуре клеток из клеток, продуцирующих необычно высокое количество конкретного представляющего интерес белка или полипептида, что достигают с помощью генной инженерии и/или селекции. Контроль и оптимизация условий культивирования клеток важны для успешного коммерческого производства белков и полипептидов.
Многие белки и полипептиды, полученные в культуре клеток, представляют собой гликопротеины, содержащие ковалентно присоединенные углеводородные структуры, включающие олигосахаридные цепи. Такие олигосахаридные цепи присоединяются к белку в эндоплазматическом ретикулуме и аппарате Гольджи посредством присоединения по атому азота или кислорода (N-присоединение или О-присоединение соответственно). Олигосахаридные цепи могут составлять значительную часть массы гликопротеина. Считают, что олигосахаридные цепи играют ключевую роль в функционировании гликопротеина, в том числе облегчают правильную укладку гликопротеина, опосредуют белок-белковые взаимодействия, сообщают стабильность, фармакодинамические и/или фармакокинетические свойства, ингибируют протеолитическое расщепление, направляют гликопротеин на соответствующий секреторный путь и способствуют попаданию гликопротеина в конкретный орган или органы.
Обычно N-присоединенные олигосахаридные цепи присоединяются к образующемуся транслоцируемому белку в просвете эндоплазматического ретикулума (см. Molecular Biology of the Cell, Alberts et al., 1994, включенную в данную заявку посредством ссылки). Олигосахариды присоединяются к аминогруппе на боковой цепи остатка аспарагина, находящегося в составе консенсусной последовательности-мишени Asn-X-Ser/Thr, где X может представлять собой любую аминокислоту, кроме пролина. Исходная олигосахаридная цепь обычно укорачивается специфическими ферментами гликозидазами в эндоплазматическом ретикулуме, в результате чего образуется короткий разветвленный коровый олигосахарид из двух остатков N-ацетилглюкозамина и трех остатков маннозы.
После начальных этапов процессинга в эндоплазматическом ретикулуме гликопротеин транспортируется через малые везикулы в аппарат Гольджи, где олигосахаридная цепь подвергается дальнейшему процессингу перед секрецией на поверхность клетки. Указанная укороченная N-присоединенная олигосахаридная цепь может быть модифицирована добавлением нескольких остатков маннозы, в результате чего образуется олигосахарид с высоким содержанием маннозы. Кроме того, к коровым субъединицам маннозы может быть присоединен один или более мономер моносахарида N-ацетилглюкозамина с образованием сложных полисахаридов. К субъединицам N-ацетилглюкозамина может быть присоединена галактоза, а к субъединицам галактозы могут быть присоединены субъединицы сиаловой кислоты с образованием цепей, содержащих на конце либо сиаловую кислоту, либо галактозу, либо N-ацетилглюкозамин. Кроме того, к остатку N-ацетилглюкозамина корового олигосахарида может быть присоединен остаток фукозы. Каждая такая реакция присоединения катализируется специфичной гликозилтрансферазой.
Помимо модификации путем N-гликозилирования, гликопротеины могут также быть модифицированы путем присоединения О-присоединенных олигосахаридных цепей к конкретным остаткам серина или треонина в ходе процессинга в аппарате Гольджи. Присоединение остатков О-присоединенного олигосахарида происходит поочередно, при этом присоединение каждого остатка катализируется специфическим ферментом. В отличие от N-гликозилирования консенсусная последовательность аминокислот для О-гликозилирования является менее определенной.
На конечный рисунок и степень гликозилирования белка могут оказывать существенное влияние условия культивирования клеток. Например, при стандартном периодическом культивировании и культивировании с подпиткой обращают основное внимание на конечный уровень продуцируемого пептида, но при этом часто образующийся гликопротеин характеризуется меньшей степенью гликозилирования и/или характером гликозилирования, при котором остатки сахара олигосахаридов слабо соответствуют остаткам сахаров, присутствующим в природной форме гликопротеина. Повышение степени гликозилирования и/или изменение состава сахарных остатков для более точного соответствия уровню и составу гликозилирования, которые присутствуют в природной форме гликопротеина, могло бы потенциально способствовать получению терапевтического агента на основе гликопротеинов с большей активностью, улучшенными фармакодинамическими и/или фармокинетическими свойствами и меньшими побочными эффектами. Хотя были предприняты некоторые попытки улучшения качественных и количественных показателей гликозилирования гликопротеинов, полученных в культуре клеток, остается потребность в дополнительных усовершенствованиях. В частности, существует потребность в разработке систем для получения гликопротеинов с улучшенными характером гликозилирования в культуре клеток в среде определенным составом.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Способы и композиции согласно настоящему изобретению обеспечивают улучшенную систему для крупномасштабного получения гликопротеинов с улучшенными характеристиками гликозилирования в культуре клеток. Например, в конкретных вариантах реализации настоящее изобретение обеспечивает способы культивирования в промышленных масштабах (например, 500 л или более), в которых применяют среду, содержащую суммарную молярную концентрацию марганца приблизительно 10-600 нМ. В конкретных вариантах реализации суммарная молярная концентрация глутамина в среде составляет менее чем приблизительно 8 мМ. В некоторых вариантах реализации настоящего изобретения суммарная молярная концентрация глутамина в среде составляет менее чем приблизительно 4 мМ. Следует понимать, что термин «суммарный» при использовании в данной заявке относится к общему количеству конкретного компонента или компонентов, добавленных в процессе культивирования клеток, включая компоненты, добавленные в начале культивирования, и компоненты, добавляемые впоследствии. В конкретных вариантах реализации изобретения желательно минимизировать «подпитку» культуры с течением времени, при этом желательно максимально увеличить содержание питательных веществ в начале культивирования. Очевидно, компоненты в среде метаболизируются в процессе культивирования таким образом, что в клеточных культурах с одинаковым суммарным количеством данных компонентов будут наблюдаться различные абсолютные уровни, если указанные компоненты добавляют в различные моменты времени (например, все компоненты присутствуют на начальном этапе или же некоторые компоненты добавляют при подпитке).
Согласно настоящему изобретению применение такой питательной среды позволяет получать гликопротеины с желательным характером гликозилирования. В некоторых вариантах реализации настоящего изобретения гликопротеины могут иметь большую степень гликозилирования и/или могут иметь распределение олигосахаридных цепей, которое в большей степени соответствует распределению олигосахаридных цепей, присоединенных к гликопротеину, в природной клетке-хозяине. В некоторых вариантах реализации результатом применения системы согласно настоящему изобретению может быть продукция гликопротеина, который имеет характер гликозилирования, схожий или идентичный характеру гликозилирования, который наблюдался бы при экспрессии указанного гликопротеина эндогенной клеткой человека.
Как очевидно специалисту в данной области, состав среды согласно настоящему изобретению охватывает как среды с определенным составом, так и сложные среды. В конкретных вариантах реализации настоящего изобретения культуральная среда представляет собой среду с определенным составом, состав которой известен и контролируется.
В некоторых вариантах реализации клетки выращивают при одном или более варианте условий, описанных в предварительной заявке на патент США №60/605,097, включенной в данную заявку посредством ссылки. В некоторых вариантах реализации клетки выращивают при одном или более варианте условий, описанных в предварительной заявке на патент США №11/213,308, включенной в данную заявку посредством ссылки.
В культуры клеток согласно настоящему изобретению можно добавлять питательные вещества и/или другие компоненты среды, в том числе гормоны и/или другие факторы роста, определенные ионы (например, натрий, хлорид, кальций, магний, и фосфат), буферы, витамины, нуклеозиды или нуклеотиды, микроэлементы (неорганические соединения, обычно присутствующие в очень низкой конечной концентрации), аминокислоты, липиды или глюкоза или другие источники энергии. В конкретных вариантах реализации настоящего изобретения может потребоваться добавление в среду химических индукторов, таких как гексаметиленбис(ацетамид) ("НМВА") и бутират натрия ("NaB"). Такие вещества можно добавлять в начале культивирования или можно добавлять на последующих этапах для пополнения истощенных запасов питательных веществ или для другой цели. В целом, желательно выбрать исходный состав среды таким образом, чтобы минимизировать добавление веществ в ходе культивирования в соответствии с настоящим изобретением.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
На Фигуре 1 показано исследование гликозидазной активности в ретентате ультрафильтрации/диафильтрации (УФ/ДФ). Для каждого эксперимента приведены данные для различных вариантов К4 и К4', столбцы слева направо: К4 (Fuc-GlcNAc-Gal-SA), К4′ (Fuc-GlcNAc-Gal), К4′ (Fuc-GlcNAc) и К4′ (Fuc).
На Фигуре 2 показано распределение вариантов К4 в rFIX, полученных в культурах, выращенных в колбах со встряхиванием. Для каждого эксперимента приведены данные для различных вариантов К4 и К4′, столбцы слева направо: К4 (Fuc-GlcNAc-Gal-SA), К4′ (Fuc-GlcNAc-Gal), К4′ (Fuc-GlcNAc) и К4′ (Fuc).
На Фигуре 3 показано распределение вариантов К4 из культур, выращенных в колбах со встряхиванием с добавление различных компонентов в среду. Для каждого эксперимента приведены данные для различных вариантов К4 и К4′, столбцы слева направо: К4 (Fuc-GlcNAc-Gal-SA), К4′ (Fuc-GlcNAc-Gal), К4' (Fuc-GlcNAc) и К4′ (Fuc).
На Фигуре 4 показано распределение вариантов К4 из культур, выращенных в колбах со встряхиванием в среде с добавками. Для каждого эксперимента приведены данные для различных вариантов К4 и К4′, столбцы слева направо: К4 (Fuc-GlcNAc-Gal-SA), К4′ (Fuc-GlcNAc-Gal), К4′ (Fuc-GlcNAc) и К4′ (Fuc).
На Фигуре 5 показано распределение образцов К4 из культур, выращенных в колбах со встряхиванием с добавлением различных компонентов в среду. Для каждого эксперимента приведены данные для различных вариантов К4 и К4′, столбцы слева направо: К4 (Fuc-GlcNAc-Gal-SA), К4′ (Fuc-GlcNAc-Gal), К4′ (Fuc-GlcNAc) и К4′ (Fuc).
На Фигуре 6 показано распределение вариантов К4 из культур, выращенных в колбах со встряхиванием с различным содержанием марганца. Для каждого эксперимента приведены данные для различных вариантов К4 и К4′, столбцы слева направо: К4 (Fuc-GlcNAc-Gal-SA), К4′ (Fuc-GlcNAc-Gal), К4′ (Fuc-GlcNAc) и К4′ (Fuc).
На Фигуре 7 представлено графическое сравнение процента общей площади пиков для G0, G1 и G2, определенных методом HPAEC-PED. Для каждого эксперимента приведены данные для сложных N-присоединенных разветвленных (biantennary) гликанов, столбцы слева направо: G0, G1 и G2.
На Фигуре 8 представлено графическое сравнение процента общей площади пиков для G0, G1 и G2, определенных методом HPAEC-PED. Для каждого эксперимента приведены данные для сложных N-присоединенных разветвленных гликанов, столбцы слева направо: G0, G1 и G2.
ОПРЕДЕЛЕНИЯ
«Аминокислота»: термин «аминокислота» при использовании в данной заявке относится к любой из двадцати природных аминокислот, которые в норме используются при образовании полипептидов, или аналогам или производным таких аминокислот, или любым неприродным аминокислотам. Аминокислоты согласно настоящему изобретению содержатся в среде для культивирования клеток. Аминокислоты, содержащиеся в среде, могут быть представлены в виде солей или в форме гидратов.
«Антитело»: термин «антитело» при использовании в данной заявке относится к молекуле иммуноглобулина или иммунологически активной части молекулы иммуноглобулина, т.е. молекуле, содержащей антигенсвязывающий сайт, специфично связывающийся с антигеном, например, Fab- или F(ab′)2 фрагменту. В некоторых вариантах реализации настоящего изобретения антитело представляет собой типичное природное антитело, известное специалистам в данной области, например гликопротеин, включающий четыре полипептидные цепи: две тяжелые цепи и две легкие цепи. В конкретных вариантах реализации антитело представляет собой одноцепочечное антитело. Например, в некоторых вариантах реализации настоящего изобретения одноцепочечное антитело включает вариант типичного природного антитела, в котором два или более компонента тяжелой и/или легкой цепей ковалентно связаны, например, посредством пептидной связи. В конкретных вариантах реализации одноцепочечное антитело представляет собой белок, имеющий структуру из двух полипептидных цепей, состоящую из тяжелой и легкой цепи, которые стабилизированы, например, внутрицепочечным линкерным пептидом, при этом такой белок обладает способностью специфично связываться с антигеном. В конкретных вариантах реализации настоящего изобретения антитело представляет собой антитело, которое содержит только тяжелые цепи, например, встречающиеся у представителей семейства Camelidae, включающего лам и верблюдов (см., например, патенты США №№6,765,087, Casterman et al., 6,015,695 Casterman et al., и 6,005,079 Casterman et al., включенные в данное описание посредством ссылки в полном объеме). Термины «моноклональные антитела» и «композиции моноклональных антител» при использовании в данной заявке обозначают популяцию молекул антител, которые содержат только один вид антигенсвязывающего сайта и, таким образом, обычно взаимодействуют только с отдельным эпитопом или конкретным антигеном. Композиции моноклональных антител, таким образом, демонстрируют одинаковую аффинность к конкретному эпитопу, с которым они связываются. Термины «поликлональные антитела» и «композиции поликлональных антител» относятся к популяциям молекул антитела, содержащим различные виды антигенсвязывающих сайтов, которые взаимодействуют с конкретным антигеном.
«Периодическое культивирование»: термин «периодическое культивирование» (butch culture) при использовании в данной заявке относится к способу культивирования клеток, при котором все компоненты, которые в конечном счете будут использованы при культивировании клеток, включая среду (см. определение «среды» ниже), а также сами клетки, обеспечивают в начале процесса культивирования. Периодическое культивирование, как правило, прекращают в некоторый момент времени и собирают клетки и/или компоненты в среде, после чего их могут подвергать очистке.
«Биореактор»: термин «биореактор» при использовании в данной заявке относится к любому сосуду, используемому для выращивания культуры клеток млекопитающего. Биореактор может быть любого размера, при условии, что его можно применять для культивирования клеток млекопитающего. Обычно такой биореактор имеет объем по меньшей мере 1 литр и может иметь объем 10, 100, 250, 500, 1000, 2500, 5000, 8000, 10000, 12000 литров или более или любой объем между данными значениями. Внутренние условия биореактора, включающие, но не ограниченные указанными параметрами: рН, растворенный кислород и температуру, обычно регулируют в ходе культивирования. Биореактор может быть изготовлен из любого материала, подходящего для содержания культуры клеток млекопитающего, ресуспендированных в среде при условиях культивирования согласно настоящему изобретению, в том числе из стекла, пластмассы или металла. Термин «промышленный биореактор» при использовании в данной заявке относится к окончательному варианту биореактора, используемого при производстве интересующего гликопротеина. Объем промышленного биореактора обычно составляет по меньшей мере 500 литров и может составлять 1000, 2500, 5000, 8000, 10000, 12000 литров или более или может равняться любому значению между указанными. Специалисту в данной области известны, и он способен выбрать подходящие биореакторы для применения при реализации настоящего изобретения на практике.
«Плотность клеток»: термин «плотность клеток» при использовании в данной заявке относится к количеству клеток, присутствующих в данном объеме в среде.
«Жизнеспособность клеток»: термин «жизнеспособность клеток» при использовании в данной заявке относится к способности клеток в культуре выживать при данных условиях культивирования или вариантах эксперимента. Данный термин при использовании в данной заявке также относится к доле клеток, жизнеспособных в конкретный момент времени относительно общего числа клеток, живых и мертвых, присутствующих в культуре в конкретный момент времени.
«Сложная среда»: термин «сложная среда» при использовании в данной заявке относится к среде, содержащей по меньшей мере один компонент, природа которого или количество либо не известно, либо не контролируется.
«Культура», «культура клеток»: данные термины при использовании в данной заявке относятся к популяции клеток, ресуспендированных в среде (см. определение «среды» ниже) при условиях, подходящих для выживания и/или роста популяции клеток. Как очевидно специалистам в данной области, в конкретных вариантах реализации данные термины при использовании в данной заявке относятся к совокупности популяции клеток и среды, в которой ресуспендирована популяция клеток. В конкретных вариантах реализации клетки в составе популяции клеток включают клетки млекопитающего.
«Среда с определенным составом»: термин «среда с определенным составом» при использовании в данной заявке относится к среде, состав которой известен и контролируется.
«Культура с подпиткой»: термин «культура с подпиткой» при использовании в данной заявке относится к способу культивирования клеток, при котором дополнительные компоненты добавляют в культуру в один или несколько моментов времени или после начала процесса культивирования. Такие дополнительные компоненты обычно включают питательные компоненты для клеток, истощенные в процессе культивирования. В качестве дополнения или альтернативы, такие дополнительные компоненты могут включать вспомогательные компоненты (см. определение «вспомогательных компонентов» ниже). В конкретных вариантах реализации дополнительные компоненты добавляют в питательную среду (см. определение «питательной среды» ниже). Культивирование с подпиткой обычно прекращают в некоторый момент времени и собирают клетки и/или компоненты в среде, после чего их можно подвергнуть очистке.
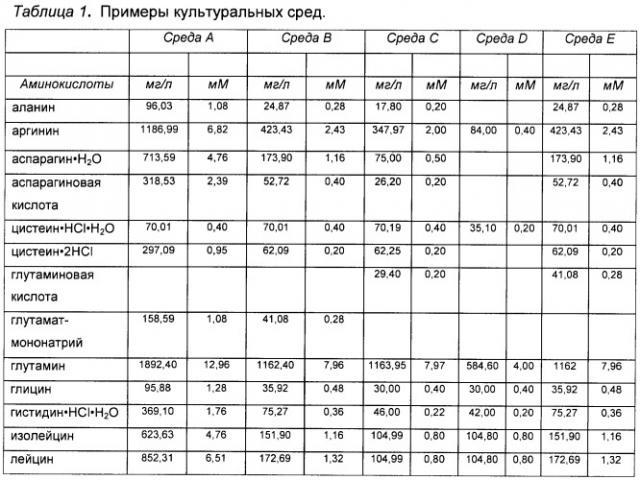
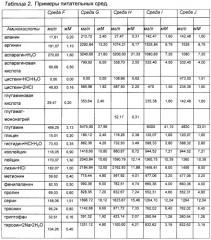
«Питательная среда»: термин «питательная среда» при использовании в данной заявке относится к раствору, содержащему питательные вещества, которые питают растущие клетки млекопитающего, который добавляют после начала культивирования клеток. Питательная среда может содержать компоненты, идентичные компонентам, содержащимся в исходной среде для культивирования клеток. Кроме того, питательная среда может содержать один или более дополнительный компонент, помимо компонентов, содержащихся в исходной среде для культивирования клеток. Кроме того или в качестве альтернативы, в питательной среде может отсутствовать один или более компонент, содержащийся в исходной среде для культивирования клеток. В некоторых вариантах реализации один или более компонент питательной среды присутствует в той же или схожей концентрации или на том же или схожем уровне, что и в исходной питательной среде. В некоторых вариантах реализации настоящего изобретения один или более компонент питательной среды присутствует в концентрации или на уровне, отличающемся от концентрации или уровня данного компонента в исходной среде для культивирования клеток. Примеры питательных сред приведены в Таблице 2, хотя настоящее изобретение не ограничивается применением данных сред. Специалисту в данной области очевидно, что можно использовать альтернативные питательные среды и/или что состав питательных сред, приведенных в качестве примеров в Таблице 2, можно варьировать. В конкретных вариантах реализации питательная среда содержит вспомогательные компоненты (см. определение «вспомогательных компонентов» ниже).
«Фрагмент»: термин «фрагмент» при использовании в данной заявке относится к полипептиду, определяемому как любая дискретная часть данного полипептида, которая является уникальной или характерной для данного полипептида. Например, данный термин при использовании в данной заявке относится к любой части данного полипептида, которая включает по меньшей мере часть с установленной последовательностью, имеющуюся в составе полноразмерного полипептида. Для определенных фрагментов указанная часть последовательности составляет по меньшей мере 4-5, 10, 15, 20, 25, 30, 35, 40, 45, 50 или более аминокислот полноразмерного полипептида. Кроме того или в качестве альтернативы, указанный термин при использовании в данной заявке относится к любой дискретной части данного полипептида, которая сохраняет по меньшей мере часть по меньшей мере одной активности полноразмерного полипептида. В конкретных вариантах реализации доля сохраняющейся активности составляет по меньшей мере 10% от активности полноразмерного полипептида. В конкретных вариантах реализации доля сохраняющейся активности составляет по меньшей мере 20%, 30%, 40%, 50%, 60%, 70%, 80% или 90% от активности полноразмерного полипептида. В конкретных вариантах реализации доля сохраняющейся активности составляет по меньшей мере 95%, 96%, 97%, 98% или 99% от активности полноразмерного полипептида. В конкретных вариантах реализации настоящего изобретения фрагмент сохраняет 100% активности полноразмерного полипептида. В конкретных вариантах реализации фрагмент согласно настоящему изобретению содержит последовательность пептида, которая служит в качестве сайта гликозилирования. В некоторых вариантах реализации фрагмент согласно настоящему изобретению содержит часть сайта гликозилирования, таким образом, что, когда он соединяется с другим фрагментом, содержащим другую часть сайта гликозилирования, происходит восстановление функционального сайта гликозилирования.
«Ген»: термин «ген» при использовании в данной заявке относится к любой нуклеотидной последовательности, ДНК или РНК, по меньшей мере некоторая часть которой кодирует дискретный конечный продукт, который, как правило, представляет собой, но не ограничивается им, полипептид, функционирующий в некотором аспекте метаболизма или развития клетки. Ген может включать не только кодирующую последовательность, которая кодирует полипептид или другой дискретный конечный продукт, но также включает области, предшествующие кодирующей последовательности и/или следующие за ней, которые модулируют базовый уровень экспрессии (см. определение «генетического контролирующего элемента» ниже), и/или промежуточные последовательности («интроны»), расположенные между отдельными кодирующими сегментами («экзонами»).
«Генетический контролирующий элемент»: термин «генетический контролирующий элемент» при использовании в данной заявке относится к любой последовательности элемента, который модулирует экспрессию гена, с которым он связан с сохранением функциональности. Генетические контролирующие элементы могут функционировать либо увеличивая, либо снижая уровень экспрессии и могут располагаться перед, в пределах или после кодирующей последовательности. Генетические контролирующие элементы могут функционировать на любом этапе экспрессии гена, регулируя, например, инициацию, элонгацию или терминацию транскрипции, сплайсинг мРНК, редактирование мРНК, стабильность мРНК, внутриклеточную локализацию мРНК, инициацию, элонгацию или терминацию трансляции или любой другой этап экспрессии гена. Генетические контролирующие элементы могут функционировать в отдельности или в комбинации друг с другом.
«Гликопротеин»: термин «гликопротеин» при использовании в данной заявке относится к белку или полипептиду, который содержит одну или более ковалентно присоединенную цепь олигосахарида. Олигосахаридные цепи могут быть образованы из одного остатка сахара, одиночной неразветвленной цепи остатков сахара или могут быть образованы цепью остатков сахара с одним или более разветвлением. В некоторых вариантах реализации олигосахаридные цепи являются N-присоединенными. В некоторых вариантах реализации цепи являются О-присоединенными.
«Характер/степень гликозилирования»: термин «характер/степень гликозилирования» относится к наблюдаемому характеру гликозилирования данного гликопротеина или гликопротеинов. Говорят, что гликопротеин с большим числом ковалентно присоединенных остатков сахара в олигосахаридной цепи имеет повышенное гликозилирование или повышенную степень гликозилирования. И наоборот, говорят, что гликопротеин с меньшим числом ковалентно присоединенных сахарных остатков в олигосахаридной цепи имеет пониженное гликозилирование или меньшую степень гликозилирования. Термин «характер/степень гликозилирования» при использовании в данной заявке также относится к характерному распределению нескольких различных вариантов гликозилирования на конкретных гликопротеинах, экспрессируемых согласно настоящему изобретению. В этом значении увеличение степени гликозилирования означает усиление характерных вариантов гликозилирования экспрессируемых гликопротеинов.
«Клетка-хозяин»: термин «клетка-хозяин» при использовании в данной заявке относится к клетке, которой манипулируют согласно настоящему изобретению с получением гликопротеина с желаемым характером гликозилирования, как описано выше. В некоторых вариантах реализации клетка-хозяин представляет собой клетку млекопитающего.
«Гибридома»: термин «гибридома» при использовании в данной заявке относится к клетке или потомству клетки, образованной слиянием иммортализованной клетки с клеткой, продуцирующей антитела. Образующаяся в результате этого гибридома представляет собой иммортализованную клетку, продуцирующую антитела. Отдельные клетки, используемые для создания гибридомы, могут быть получены от любого млекопитающего, включая без ограничений крысу, свинью, кролика, овцу, козу и человека. В конкретных вариантах реализации гибридома представляет собой триомную линию клеток, образующуюся при слиянии клеток-потомков гетерогибридной миеломы, являющихся в свою очередь продуктом слияния клеток человека и линии клеток миеломы мыши, с плазматической клеткой. В конкретных вариантах реализации настоящего изобретения гибридома представляет собой любую иммортализованную гибридную линию клеток, продуцирующую антитела, такую как квадрома (см., например, Milstein et al., Nature, 537:3053, 1983).
«Среда», «среда для культивирования клеток», «культуральная среда»: эти термины при использовании в данной заявке относятся к раствору, содержащему питательные вещества, питающие растущие клетки млекопитающего. Обычно такие растворы обеспечивают незаменимые и заменимые аминокислоты, витамины, источники энергии, липиды и микроэлементы, требующиеся клетке для минимального роста и/или жизнеспособности. Такой раствор может также содержать вспомогательные компоненты (см. определение «вспомогательных компонентов» ниже), которые усиливают рост и/или жизнеспособность, делая их выше минимальных показателей, включающие - но не ограниченные перечисленными - гормоны и/или другие факторы роста, конкретные ионы (такие как натрий, хлорид, кальций, магний и фосфат), буферы, витамины, нуклеозиды или нуклеотиды, микроэлементы (неорганические соединения, обычно присутствующие в очень низкой конечной концентрации), аминокислоты, липиды и/или глюкозу или другой источник энергии. В конкретных вариантах реализации среда преимущественно имеет рН и концентрацию солей, оптимальные для жизнеспособности и пролиферации клеток. Примеры культуральных сред представлены в Таблице 1, хотя настоящее изобретение не ограничено применением указанных сред. Как понятно специалисту в данной области, можно применять альтернативные культуральные среды, и/или могут быть сделаны некоторые изменения в составе культуральных сред, приведенных в качестве примеров в Таблице 1. В конкретных вариантах реализации среда представляет собой среду для подпитки, которую добавляют после начала культивирования клеток (см. определение «среды для подпитки», выше).
«Полипептид»: термин «полипептид» при использовании в данной заявке обозначает цепь последовательных аминокислот, соединенных вместе посредством пептидных связей. Термин используется для обозначения цепи из аминокислот любой длины, но, как очевидно специалисту в данной области, термин не ограничивается протяженными цепями и может относиться к минимальной цепи, включающей две аминокислоты, связанные вместе посредством пептидной связи. Как известно специалистам в данной области, полипептиды могут подвергаться процессингу и модификациям. Например, полипептид может быть гликозилирован (см. определение «гликопротеина» выше).
«Белок»: термин «белок» при использовании в данной заявке относится к одному или более полипептиду, который функционирует в виде дискретной единицы. Если отдельный полипептид представляет собой дискретную функционирующую единицу и не требует постоянной или временной физической ассоциации с другими полипептидами для формирования дискретной функционирующей единицы, термины «полипептид» и «белок» могут использоваться равнозначно. Если дискретная функциональная единица включает более одного полипептида, физически соединенных друг с другом, термин «белок» относится к совокупности полипептидов, которые физически связаны и функционируют вместе в виде дискретной единицы.
«Рекомбинантно экспрессируемый гликопротеин» и «рекомбинантный гликопротеин»: эти термины при использовании в данной заявке относятся к гликопротеину, экспрессируемому в клетке-хозяине, с которой провели манипуляции таким образом, чтобы указанная клетка экспрессировала данный гликопротеин. В конкретных вариантах реализации настоящего изобретения клетка-хозяин представляет собой клетку млекопитающего. В конкретных вариантах реализации такого рода манипуляции включают одну или более генетическую модификацию. Например, клетки-хозяева млекопитающего могут быть генетически модифицированы введением одного или более гетерологичного гена, кодирующего гликопротеин, экспрессию которого осуществляют. Гетерологичный рекомбинатно экспрессируемый гликопротеин может быть идентичным или схожим с гликопротеином, который в норме экспрессируется в клетке-хозяине млекопитающего. Гетерологичный рекомбинантно экспрессируемый гликопротеин может также быть чужеродным для указанной клетки-хозяина, то есть гетерологичным по отношению к гликопротеинам, в норме экспрессируемым указанным клеткой-хозяином млекопитающего. В конкретных вариантах реализации гетерологичный рекомбинантно экспрессируемый гликопротеин является химерным в том отношении, что он содержит последовательности аминокислот, идентичные или схожие с последовательностями гликопротеинов, в норме экспрессирующихся в клетке-хозяине млекопитающего, тогда как другие участки указанного гликопротеина являются чужеродными по отношению к клетке-хозяину. Кроме того, клетка-хозяин млекопитающего может быть генетически модифицирована путем активации или увеличения экспрессии одного или более эндогенных генов.
«Вспомогательные компоненты»: термин «вспомогательные компоненты» при использовании в данной заявке относится к компонентам, которые усиливают рост и/или жизнеспособность клеток, делая их выше минимального уровня, включающим - но не ограниченным перечисленными - гормоны и/или другие факторы роста, конкретные ионы (например, натрий, хлорид, кальций, магний и фосфат), буферы, витамины, нуклеозиды или нуклеотиды, микроэлементы (неорганические соединения, как правило, присутствующие в очень низкой конечной концентрации), аминокислоты, липиды и/или глюкозу или другой источник энергии. В некоторых вариантах реализации вспомогательные компоненты могут быть добавлены к начальной культуре клеток. В некоторых вариантах реализации вспомогательные компоненты могут быть добавлены после начала культивирования клеток.
«Титр»: термин «титр» при использовании в данной заявке относится к общему количеству рекомбинантно экспрессируемого гликопротеина, продуцируемого культурой клеток млекопитающего в данном объеме среды. Обычно титр выражают в единицах миллиграмм гликопротеина на миллилитр среды.
ПОДРОБНОЕ ОПИСАНИЕ НЕКОТОРЫХ ВАРИАНТОВ РЕАЛИЗАЦИИ ИЗОБРЕТЕНИЯ
Настоящее изобретение обеспечивает улучшенные системы для получения гликопротеинов в культуре клеток. В частности, предусмотрены системы, обеспечивающие продукцию гликопротеина с желаемым характером гликозилирования. Например, гликопротеин может иметь более высокую степень гликозилирования и/или может иметь распределение олигосахаридных цепей, имеющее большую степень сходства с распределением олигосахаридных цепей, присоединенных к гликопротеину в природной клетке-хозяине. В некоторых вариантах реализации применение системы согласно настоящему изобретению может обеспечивать производство гликопротеина с характером гликозилирования, схожим или идентичным характеру гликозилирования, наблюдаемому при экспрессии гликопротеина в эндогенной клетке-хозяине. Некоторые варианты реализации настоящего изобретения рассмотрены подробно ниже. Однако, как ясно специалисту в данной области, возможны различные модификации указанных вариантов реализации в пределах объема прилагаемой формулы. Именно формула и эквиваленты определяют область настоящего изобретения, которая не ограничена и которую не следует ограничивать настоящим описанием отдельных вариантов реализации.
СОСТАВ СРЕД
В соответствии с настоящим изобретением можно применять широкий спектр сред для роста клеток млекопитающего. В конкретных вариантах реализации клетки можно выращивать в одной из ряда сред с известным определенным составом {defined media), при котором компоненты среды известны и контролируемы. В конкретных вариантах реализации клетки можно выращивать в сложной среде, в которой не все компоненты известны и/или контролируемы.
В течение последних десятилетий были разработаны и широко описаны в литературе среды для роста культур клеток млекопитающего с определенным химическим составом. Все компоненты среды с определенным составом хорошо охарактеризованы, и такие среды не содержат сложных добавок, например сыворотку или гидролизаты. Ранее состав сред разрабатывали таким образом, чтобы они обеспечивали рост клеток и поддерживали их жизнеспособность, при этом лишь незначительное внимание уделяли продукции белка или вообще ее не учитывали. В последнее время были разработаны среды, предназначенные специально для поддержания клеточных культур с высоким уровнем продукции рекомбинантного белка и/или гликопротеина.
Среда с определенным составом обычно включает около пятидесяти химических соединений в известной концентрации, растворенных в воде. Большинство из них также содержат один или более из известных белков, например инсулин, IGF-1, трансферрин или БСА, но другие среды не требуют белковых компонентов, и