Производное хиназолина и фармацевтический препарат
Иллюстрации
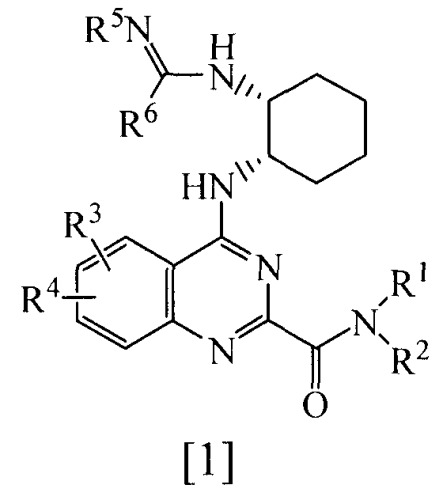
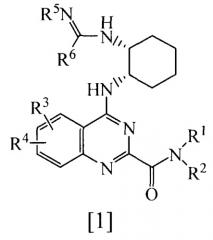
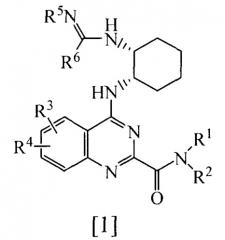
Показать всеНастоящее изобретение относится к производному хиназолина, представленному общей формулой [1], или его фармацевтически приемлемой соли
, где R1-R6 имеют значения, представленные в п.1 формулы, за исключением соединения, в котором R5 представляет собой водород, и R6 представляет собой -NH2. Изобретение также относится к фармацевтической композиции, обладающей активностью противозудного средства, содержащей в качестве активного ингредиента указанное выше производное хиназолина или его фармацевтически приемлемую соль. Технический результат - получение нового производного хиназолина с меньшим раздражающим действием на кожу и превосходным действием существенного подавления поведения расчесывания, а также противозудного средства, содержащего такое производное хиназолина в качестве активного ингредиента. 2 н. и 7 з.п. ф-лы, 250 пр., 7 табл.
Реферат
Область техники
Настоящее изобретение относится к производному хиназолина, применимому в качестве фармацевтического препарата, в частности противозудного средства, и его фармацевтически приемлемой соли, и фармацевтической композиции, содержащей любое из указанных соединений в качестве активного ингредиента.
Уровень техники
Зуд является ощущением, т.е., ощущением зуда, которое имеет место в поверхностном слое кожи и слизистых оболочек. Ощущение зуда является ощущением вследствие восприятия паразита или раздражения в поверхностном слое кожи и желания удаления проникающего вещества или раздражителя царапанием или иным способом. Зуд можно легко представить как ощущение, вызывающее побуждение чесаться, но его механизм пока полностью не выяснен.
Заболевания, сопровождаемые зудом, условно делят на зудящие дерматозы, сопровождаемые повреждением кожи (например, атопический дерматит, крапивница, псориаз, ксеродермия и дерматофития), и кожный зуд, который не сопровождается повреждением кожи, но вызывается вследствие гемодиализа и висцеральных заболеваний [например, диабета, болезней крови, холестатического повреждения печени (первичный биллиарный цирроз печени) и болезней почек], гипертиреоидизма, рассеянного склероза или подобных заболеваний. Кроме того, в качестве примеров заболеваний, сопровождающихся сильным зудом, можно назвать болезни роговицы и конъюнктивы, такие как аллергический конъюнктивит. Недавно любое из таких заболеваний быстро перерастало в большую проблему с точки зрения QOL (качества жизни). Общим для большинства сопровождающихся зудом болезней является факт, что патологический цикл вызывается расчесыванием кожи. Гистамин известен как типичное вызывающее зуд вещество, и он вызывает зуд в случае, когда добавляется извне и высвобождается в организме из мастоцитов.
Антигистаминные средства, противоаллергические средства, стероидные наружные препараты и т.п. применяют для лечения зудящего дерматоза. Однако не имеется лекарственного средства, которое является удовлетворительным для лечения зуда вследствие зудящего дерматоза. Также недавно появилось сообщение, что факторы, иные, чем гистамин, участвуют в появлении ощущения зуда при атопическом дерматите. Действительно, также во многих клинических случаях антигистаминное средство или противоаллергическое средство не оказывает заметного действия на зуд при атопическом дерматите. При лечении кожного зуда в некоторых случаях прописывают антигистаминное средство или стероидный наружный препарат. Однако эффект почти не заметен, и, таким образом, в настоящее время эффективного лечения не существует. Как описано выше, не имеется удовлетворительного лекарственного средства для болезней, сопровождаемых зудом, и лекарственное средство, которое эффективно подавляет зуд независимо от этиологии, остро необходимо с клинической точки зрения.
Для того чтобы решить указанную проблему, в качестве соединения, применимого для противозудного средства, в литературе описываются производное хиназолина (см., например, патентный документ 1), ингибитор нейронной синтазы оксида азота (см., например, патентный документ 2), агонист каннабиноидного рецептора (см., например, патентный документ 3), ингибитор глутаматного рецептора (см., например, патентный документ 4), производное пиперидина (см., например, патентный документ 5), производное простагландина (см., например, патентный документ 6) и т.п. Среди указанных средств производное хиназолина, описанное в патентном документе 1, сильно подавляет поведение расчесывания, спонтанно возникающее на мышиной модели с разрушением барьера рогового слоя, и применимо в качестве лекарственного средства для эффективного подавления зуда независимо от этиологии.
В коже при заболеваниях, сопровождающихся зудом, в особенности, при атопическом дерматите и подобном заболевании, сопровождаемом повреждением кожи, развивается разрушение барьера рогового слоя или гиперчувствительность чувствительных нервов по сравнению со здоровой кожей, и кожа признается чувствительной к раздражению. Когда при таких заболеваниях, сопровождающихся зудом, применяют наружный препарат, необходимо, чтобы такой препарат оказывал исключительно слабое раздражение кожи. Однако, когда в качестве наружного препарата для больного атопическим дерматитом применяют производные хиназолина, описанные в патентном документе 1, которые содержат гуанидиногруппу в боковой цепи в положении 4 хиназолинового скелета, существует вероятность появления раздражения кожи.
Патентный документ 1: WO 03/091224.
Патентный документ 2: JP-A-2002-138052.
Патентный документ 3: JP-A-2003-201250.
Патентный документ 4: JP-A-2004-107209.
Патентный документ 5: JP-A-2005-047909.
Патентный документ 6: JP-A-2005-139194.
Непатентный документ 1: J. Am. Chem. Soc., 1975, 97, 2512.
Непатентный документ 2: J. Am. Chem. Soc., 1942, 64, 1827.
Непатентный документ 3: J. Org. Chem., 1942, 432.
Непатентный документ 4: J. Chem. Soc. Perkin Trans 2, 2000, 1435.
Непатентный документ 5: J. Med. Chem., 1997, 40, 2363.
РАСКРЫТИЕ ИЗОБРЕТЕНИЯ
Задачи, решаемые изобретением
Целью настоящего изобретения является, главным образом, новое производное хиназолина с меньшим раздражающим действием на кожу и превосходным действием сильного подавления поведения расчесывания и противозудное средство, содержащее такое производное хиназолина в качестве активного ингредиента.
Способы решения указанных задач
Авторы изобретения провели интенсивные исследования и в результате обнаружили, что описанное далее производное хиназолина, которое является новым соединением, и его фармацевтически приемлемая соль могут соответствовать указанной выше цели, и таким образом было осуществлено настоящее изобретение.
Настоящее изобретение относится к производному хиназолина, представленному приведенной далее общей формулой [1], или его фармацевтически приемлемой соли (называемым далее “соединением по изобретению”).
Химическая часть 2
R1 представляет водород или алкил;
R2 представляет водород, алкокси, тетрагидропиранил, фенил, циклоалкил, (циклоалкил)алкил или алкил. Алкокси, тетрагидропиранил, фенил, циклоалкил, (циклоалкил)алкил и алкил могут быть замещены одной-тремя группами, выбранными из группы, состоящей из (1) алкокси, (2) галогена, (3) алкоксиалкила, (4) гидрокси, (5) алкилтио, (6) 5-10-членной ароматической гетероциклической группы, содержащей один-три гетероатома, выбранных из группы, состоящей из атома азота, атома кислорода и атома серы, (7) 5-7-членной насыщенной алифатической гетероциклической группы, которая может быть замещена ацилом и содержит один-три атома азота, и (8) фенила, который может быть замещен галогеном или алкокси;
R3 и R4 являются одинаковыми или различными, и каждый представляет собой водород, алкил, алкокси или галоген.
R5 объединяют с R6, что представляет алкилен, или R5 представляет собой водород, гидрокси, алкил, фенил или алкокси. Алкилен может быть замещен гидрокси или оксо и может конденсироваться с бензольным циклом. Алкил, фенил и алкокси, представленные R5, могут быть замещены одной-тремя группами, выбранными из группы, состоящей из алкокси, алкилтио и галогена;
R6 представляет собой (1) алкил, (2) циклоалкил, (3) фенил, (4) 5-10-членную ароматическую гетероциклическую группу, содержащую один-три гетероатома, выбранных из группы, состоящей из атома азота, атома кислорода и атома серы, или (5) -N(R61)(R62). Алкил, циклоалкил, фенил и ароматическая гетероциклическая группа могут быть замещены одной-тремя группами, выбранными из группы, состоящей из (1) алкокси, (2) гидрокси, (3) фенила, (4) пиридила, (5) фурила, (6) галогена и (7) N,N-диалкиламино. R61 объединяют с R62, что представляет -О-(СН2)n-, или R61 представляет собой водород или алкил. R62 представляет собой водород или алкокси, который может быть замещен одной-тремя группами, выбранными из группы, состоящей из алкокси, алкилтио и галогена. В данном случае n равен целому числу от 3 до 5.
Исключением является соединение, в котором R5 представляет собой водород, и R6 представляет собой -NH2.
Предпочтительными соединениями в настоящем изобретении могут быть, как примеры, перечисленные далее производные хиназолина (1)-(29) и их фармацевтически приемлемые соли.
(1) 4-{[(1S,2R)-2-(Этанимидоиламино)циклогексил]амино}-N-(2-метоксиэтил)-6-метилхиназолин-2-карбоксамид,
(2) N-(2,2-Диметилпропил)-4-({(1S,2R)-2-[(2-метокси-2-метилпропанимидоил)амино]циклогексил]амино}-6-метилхиназолин-2-карбоксамид,
(3) 4-({(1S,2R)-2-[(3-Метоксипропанимидоил)амино]циклогексил}амино)-N-(3-метоксипропил)-6-метилхиназолин-2-карбоксамид,
(4) 4-({(1S,2R)-2-[(3-Гидроксипропанимидоил)амино]циклогексил}амино)-N-изопропил-6-метилхиназолин-2-карбоксамид,
(5) 4-({(1S,2R)-2-[(3-Гидроксипропанимидоил)амино]циклогексил}амино)-N-(3-метоксипропил)-6-метилхиназолин-2-карбоксамид,
(6) 4-({(1S,2R)-2-[(2-Гидрокси-2-метилпропанимидоил)амино]циклогексил}амино)-N-изобутил-6-метилхиназолин-2-карбоксамид,
(7) N-(2-Этоксиэтил)-4-({(1S,2R)-2-[(3-гидроксипропанимидоил)амино]циклогексил}амино)-6-метилхиназолин-2-карбоксамид,
(8) 4-({(1S,2R)-2-[(2-Гидрокси-2-метилпропанимидоил)амино]циклогексил}амино)-N-изопропил-6-метилхиназолин-2-карбоксамид,
(9) 4-({(1S,2R)-2-[(2-Гидрокси-2-метилпропанимидоил)амино]циклогексил}амино)-N-(2-метоксиэтил)-6-метилхиназолин-2-карбоксамид,
(10) 4-({(1S,2R)-2-[(2-Метоксиэтанимидоил)амино]циклогексил}амино)-N-(2-метоксиэтил)-6-метилхиназолин-2-карбоксамид,
(11) 4-{[(1S,2R)-2-(Этанимидоиламино)циклогексил]амино}-N-(3-метоксипропил)-6-метилхиназолин-2-карбоксамид,
(12) 4-({(1S,2R)-2-[(2-Метоксиэтанимидоил)амино]циклогексил}амино)-N-(3-метоксипропил)-6-метилхиназолин-2-карбоксамид,
(13) 4-{[(1S,2R)-2-(Этанимидоиламино)циклогексил]амино}-N-(2-этоксиэтил)-6-метилхиназолин-2-карбоксамид,
(14) N-(2-Этоксиэтил)-4-({(1S,2R)-2-[(2-метоксиэтанимидоил)амино]циклогексил}амино)-6-метилхиназолин-2-карбоксамид,
(15) 4-{[(1S,2R)-2-(Этанимидоиламино)циклогексил]амино}-N-изопропил-6-метилхиназолин-2-карбоксамид,
(16) 4-[((1S,2R)-2-{[Амино(метоксиимино)метил]амино}циклогексил)амино]-N-(2-метоксиэтил)-6-метилхиназолин-2-карбоксамид,
(17) 4-[((1S,2R)-2-{[Амино(метоксиимино)метил]амино}циклогексил)амино]-N-изобутил-6-метилхиназолин-2-карбоксамид,
(18) 4-[((1S,2R)-2-{[Амино(гидроксиимино)метил]амино}циклогексил)амино]-N-изобутил-6-метилхиназолин-2-карбоксамид,
(19) 4-[((1S,2R)-2-{[Амино(метоксиимино)метил]амино}циклогексил)амино]-N-(циклопропилметил)-6-метилхиназолин-2-карбоксамид,
(20) 4-[((1S,2R)-2-{[Амино(метоксиимино)метил]амино}циклогексил)амино]-N-изопропил-6-метилхиназолин-2-карбоксамид,
(21) 4-{[(1S,2R)-2-({Имино[метокси(метил)амино]метил}амино)циклогексил]амино}-N-изобутил-6-метилхиназолин-2-карбоксамид,
(22) 4-[((1S,2R)-2-{[Амино(метоксиимино)метил]амино}циклогексил)амино)-N-(3-метоксипропил)-6-метилхиназолин-2-карбоксамид,
(23) 4-[((1S,2R)-2-{[Амино(гидроксиимино)метил]амино}циклогексил)амино]-N-(3-метоксипропил)-6-метилхиназолин-2-карбоксамид,
(24) 4-[((1S,2R)-2-{[Амино(метоксиимино)метил]амино}циклогексил)амино]-N-(2-этоксиэтил)-6-метилхиназолин-2-карбоксамид,
(25) 4-[((1S,2R)-2-{[Амино(этоксиимино)метил]амино}циклогексил)амино]-N-(2-метоксиэтил)-6-метилхиназолин-2-карбоксамид,
(26) 4-{[(1S,2R)-2-({Амино[(2-метоксиэтокси)имино]метил}амино)циклогексил]амино}-N-(2-метоксиэтил)-6-метилхиназолин-2-карбоксамид,
(27) 4-{[(1S,2R)-2-({Амино[(2-фторэтокси)имино]метил}амино)циклогексил]амино}-N-(2-метоксиэтил)-6-метилхиназолин-2-карбоксамид,
(28) 4-({(1S,2R)-2-[(Амино{[2-(метилтио)этокси]имино}метил)амино)циклогексил}амино)-N-(2-метоксиэтил)-6-метилхиназолин-2-карбоксамид,
(29) 4-[((1S,2R)-2-{[Амино(метоксиимино)метил]амино}циклогексил)амино]-N-(2-метоксиэтил)-6-метилхиназолин-2-карбоксамид.
Кроме того, настоящее изобретение также относится к фармацевтической композиции, содержащей соединение по изобретению в качестве активного ингредиента, например фармацевтической композиции для подавления зуда, содержащей соединение по изобретению в качестве активного ингредиента.
Далее настоящее изобретение будет описываться подробнее.
Примеры “алкила” могут включать линейный или разветвленный алкил с 1-10 атомами углерода, и его конкретные примеры могут включать метил, этил, н-пропил, изопропил, н-бутил, изобутил, втор-бутил, трет-бутил, н-пентил, изопентил, н-гексил, изогексил, н-гептил, изогептил, н-октил, н-нонил и н-децил. Предпочтителен алкил с 1-8 атомами углерода, и более предпочтителен алкил с 1-6 атомами углерода.
Примеры алкильной группы в “алкокси”, “(циклоалкил)алкиле”, “алкоксиалкиле”, “алкилтио” и “N,N-диалкиламино” могут включать такой же алкил, примеры которого описаны выше.
Примеры “тетрагидропиранила” могут включать 2-тетрагидропиранил, 3-тетрагидропиранил и 4-тетрагидропиранил.
Примеры “циклоалкила” могут включать циклический алкил с 3-10 атомами углерода, который является моноциклическим-трициклическим, и его конкретные примеры могут включать циклопропил, циклобутил, циклопентил, циклогексил, циклогептил, циклооктил, циклононил, циклодеканил, адамантил (1-адамантил, 2-адамантил и т.п.), 2-бицикло[3.1.1]гептил и 2-бицикло[2.2.1]гептил. Предпочтительным является циклический алкил с 4-9 атомами углерода, и более предпочтительным является циклический алкил с 5-8 атомами углерода.
Примеры циклоалкильной группы в “(циклоалкил)алкиле” могут включать такой же циклоалкил, примеры которого описаны выше.
Примеры “галогена” могут включать фтор, хлор, бром и иод.
Примеры “ароматической гетероциклической группы” могут включать 5-10-членную ароматическую гетероциклическую группу, содержащую один-три гетероатома, выбранных из группы, состоящей из атома азота, атома кислорода и атома серы, и ее конкретные примеры могут включать пиридил (2-пиридил, 3-пиридил, 4-пиридил), пиримидинил (2-пиримидинил, 4-пиримидинил, 5-пиримидинил), пиразинил (2-пиразинил и т.п.), пиридазинил (3-пиридазинил, 4-пиридазинолил), пирролил (2-пирролил и т.п.), фурил (2-фурил, 3-фурил), тиенил (2-тиенил, 3-тиенил), имидазолил (1-имидазолил, 4-имидазолил и т.п.), пиразолил (3-пиразолил, 5-пиразолил и т.п), оксазолил (4-оксазолил, 5-оксазолил и т.п.), тиазолил (1,3-тиазол-2-ил, 1,3-тиазол-5-ил и т.п.), изоксазолил (изоксазол-4-ил, изоксазол-5-ил и т.п.) и 1,3,4-тиадиазол-2-ил.
Примеры “ацила” могут включать ацил с 1-11 атомами углерода, и его конкретные примеры могут включать формил, ацетил, пропионил, бутирил, изобутирил, бензоил, 1-нафтоил и 2-нафтоил.
Примеры “насыщенной алифатической гетероциклической группы” могут включать 5-7-членную насыщенную алифатическую гетероциклическую группу, содержащую один-три атома азота, и ее конкретные примеры могут включать пирролидинил (1-пирролидинил, 2-пирролидинил, 3-пирролидинил), пиперидинил (1-пиперидинил, 2-пиперидинил, 3-пиперидинил, 4-пиперидинил), пиперазинил (1-пиперазинил, 2-пиперазинил), гомопиперазинил (1-гомопиперазинил, 2-гомопиперазинил, 3-гомопиперазинил, 6-гомопиперазинил), морфолинил (2-морфолинил, 3-морфолинил, 4-морфолинил) и тиоморфолинил (2-тиоморфолинил, 3-тиоморфолинил, 4-тиоморфолинил).
Примеры “пиридила” могут включать 2-пиридил, 3-пиридил и 4-пиридил.
Примеры “фурила” могут включать 2-фурил и 3-фурил.
Примеры “алкилена” могут включать линейный или разветвленный алкилен с 1-6 атомами углерода, и его конкретные примеры могут включать метилен, этилен, триметилен, тетраметилен, пентаметилен и гексаметилен. Среди них предпочтительным является алкилен с 2-5 атомами углерода, и более предпочтительным является алкилен с 3-5 атомами углерода.
Примеры “зуда” могут включать зуд, сопровождающий атопический дерматит, крапивницу, псориаз, ксеродермию, дерматофитию, витилиго, локальный кожный зуд, вызванный экскрецией или секрецией насекомого, узловатым пруриго, гемодиализом, диабетом, болезнями крови, холестатическим повреждением печени (первичным биллиарным циррозом печени), болезнями печени, болезнями почек, эндокринными расстройствами и расстройствами обмена веществ, висцеральной злокачественностью, гипертиреоидизмом, аутоиммунными заболеваниями, рассеянным склерозом, неврологическими заболеваниями, психоневрозом, аллергическим конъюнктивитом, весенним катаром, атопическим кератоконъюнктивитом или избыточным применением некоторых продуктов или лекарственных средств.
Наилучший способ осуществления изобретения
Химическая часть 3
Соединение по изобретению [1] можно получить согласно, например, описанному далее способу из известного соединения или промежуточного соединения, которое можно легко синтезировать. При получении соединения по изобретению [1] в случае, когда исходное вещество содержит заместитель, который оказывает влияние на взаимодействие, общим положением является то, что взаимодействие осуществляют после того, как в исходное вещество введут подходящую защитную группу способом, известным в технике. Понятно, что после взаимодействия защитную группу удаляют известным способом.
Способ получения 1
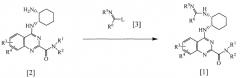
Соединение по изобретению [1] можно получить согласно, например, следующей схеме взаимодействия.
Химическая часть 4
В приведенных формулах R1-R6 имеют значения, указанные выше. L представляет удаляемую группу (например, алкокси, галоген, пиразол-1-ил или метилтио).
Соединение по изобретению [1] можно получить взаимодействием соединения [2] с одним эквивалентом или избыточным количеством соединения [3] в растворителе, например растворителе на основе спирта, такого как метанол или этанол, растворителе на основе углеводорода, такого как бензол или толуол, растворителе на основе простого эфира, такого как диоксан или тетрагидрофуран, галогенсодержащем растворителе, таком как хлороформ или 1,2-дихлорэтан, диметилформамиде или подобном растворителе, в присутствии основания, такого как триэтиламин или N,N-диизопропилэтиламин, или без него, при температуре от 0ºС до температуры кипения используемого растворителя в течение от нескольких часов до нескольких суток. Предпочтительно, чтобы взаимодействие осуществлялось в присутствии триэтиламина с использованием этоксигруппы как удаляемой группы L соединения [3] и этанола в качестве растворителя при 80ºС в течение 1-48 часов.
Соединение [2], которое является исходным соединением, можно получить известным способом (см., например, патентный документ 1).
Соединение [3], которое является исходным соединением, коммерчески доступно, но его также можно получить известным способом (см., например, непатентные документы 1 и 2).
Способ получения 2
Соединение по изобретению [1а], в котором R5 представляет собой алкокси, R6 представляет собой -N(R61)(R62), и R61 и R62 оба представляют собой водород, также можно получить согласно схеме взаимодействия, приведенной далее.
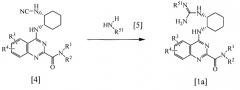
Химическая часть 5
В приведенных формулах R1 - R4 имеют значения, указанные выше. R51 представляет алкокси, который может быть замещен одной-тремя группами, выбранными из группы, состоящей из алкокси, алкилтио и галогена.
Способ получения 3
Соединение по изобретению [1b], в котором R5 представляет собой водород, и R6 представляет собой -N(R61)(R62), также можно получить согласно схеме взаимодействия, приведенной далее.
Химическая часть 6
В приведенных формулах R1 - R4, R61 и R62 имеют значения, указанные выше.
Соединение по изобретению [1а] или [1b] можно получить взаимодействием соединения [4] с одним эквивалентом или избыточным количеством соединения [5] или [6] в растворителе, например растворителе на основе спирта, такого как метанол или этанол, растворителе на основе углеводорода, такого как бензол или толуол, растворителе на основе простого эфира, такого как диоксан или тетрагидрофуран, галогенсодержащем растворителе, таком как хлороформ или 1,2-дихлорэтан, диметилформамиде или подобном растворителе, в присутствии неорганического основания, такого как карбонат натрия или карбонат калия, или органического основания, такого как триэтиламин или N,N-диизопропилэтиламин, или без него, при температуре от 0ºС до температуры кипения используемого растворителя в течение от нескольких часов до нескольких суток. Предпочтительно, чтобы взаимодействие осуществлялось в присутствии карбоната натрия с использованием этанола или диоксана в качестве растворителя при 50ºС-80ºС в течение 1-24 часов.
Соединение [4], которое является исходным соединением, можно получить согласно схеме взаимодействия, приведенной далее.
Химическая часть 7
В приведенных формулах R1 - R4 имеют значения, указанные выше.
Соединение [4] можно получить взаимодействием соединения [2] с одним эквивалентом или избыточным количеством BrCN в растворителе, например растворителе на основе углеводорода, такого как бензол или толуол, растворителе на основе простого эфира, такого как диоксан или тетрагидрофуран, галогенсодержащем растворителе, таком как хлороформ или 1,2-дихлорэтан, диметилформамиде или подобном растворителе, в присутствии неорганического основания, такого как карбонат натрия или карбонат калия, или органического основания, такого как триэтиламин или N,N-диизопропилэтиламин, при температуре от -78ºС до температуры кипения используемого растворителя в течение от нескольких минут до нескольких суток. Предпочтительно, чтобы взаимодействие осуществлялось в присутствии триэтиламина с использованием тетрагидрофурана в качестве растворителя при -50ºС-0ºС в течение 10 минут - 1 часа.
Кроме того, соединение [4], которое является исходным соединением, также можно получить согласно схеме взаимодействия, приведенной далее.
Химическая часть 8
Соединение [7] можно получить взаимодействием соединения [2] с одним эквивалентом или избыточным количеством цианата калия в растворителе, например воде, растворителе на основе спирта, такого как метанол или этанол, или подобном растворителе, в присутствии кислоты, такой как хлороводородная кислота или серная кислота, или без нее или основания, такого как триэтиламин, N,N-диизопропилэтиламин, гидроксид натрия или гидроксид калия, при температуре от 0ºС до температуры кипения используемого растворителя в течение от нескольких часов до нескольких суток. Предпочтительно, чтобы взаимодействие осуществлялось в присутствии триэтиламина с использованием водного этанола в качестве растворителя при 50ºС-100ºС в течение 1 часа - 5 часов. Соединение [4] можно получить взаимодействием соединения [7] с метансульфонилхлоридом в пиридине при при -10ºС-50ºС в течение 30 минут - 5 часов.
Соединения [5] и [6], которые являются исходными соединениями, коммерчески доступны, но их также можно получить известным способом (см., например, непатентные документы 3-5).
Производное хиназолина по настоящему изобретению можно использовать в качестве фармацевтического средства в форме самого свободного основания или можно использовать, превратив в форму фармацевтически приемлемой соли известным способом. Примеры таких солей включают соли с неорганическими кислотами, такими как хлороводородная кислота, бромоводородная кислота, серная кислота или фосфорная кислота, и соли с органическими кислотами, такими как уксусная кислота, лимонная кислота, винная кислота, малеиновая кислота, янтарная кислота, фумаровая кислота, п-толуолсульфоновая кислота, бензолсульфоновая кислота или метансульфоновая кислота и т.п.
Например, соль гидрохлорид производного хиназолина по настоящему изобретению можно получить, растворяя производное хиназолина по настоящему изобретению в подходящем растворителе и добавляя к нему спиртовой раствор, раствор в этилацетате или в эфире хлороводорода, с последующим концентрированием досуха.
Некоторые соединения из числа соединений по изобретению [1] могут содержать асимметричный атом углерода, и все оптические изомеры и их смеси таких соединений также входят в объем настоящего изобретения. Такие оптические изомеры можно получить, например, исходя из рацемата, полученного так, как описано выше, используя его основность, и с использованием оптически активной кислоты (винной кислоты, дибензоилвинной кислоты, миндальной кислоты, 10-камфорсульфоновой кислоты или подобной кислоты), известным способом оптического расщепления, или с использованием предварительно полученного оптически активного соединения в качестве исходного вещества. Кроме того, оптические изомеры также можно получить оптическим расщеплением или асимметричным синтезом с использованием хиральной колонки.
Кроме того, среди соединений по изобретению [1] также имеются соединения, которые могут существовать в цис-форме, транс-форме, Z-форме или Е-форме, и каждый такой изомер и их смеси также входят в объем настоящего изобретения.
Когда соединение по изобретению вводят как фармацевтический препарат, соединение по изобретению вводят млекопитающим, в том числе, людям, в том виде, в каком оно есть, или в фармацевтически приемлемом нетоксичном инертном носителе, например, в виде фармацевтической композиции, содержащей соединение по изобретению в количестве 0,001%-99,5%, предпочтительно, 0,1%-90%.
В качестве носителя можно использовать один или несколько типов вспомогательных средств для композиции, таких как твердые, полутвердые или жидкие разбавители, наполнители и другие вспомогательные средства для лекарственного препарата. Предпочтительно, чтобы фармацевтическую композицию по настоящему изобретению вводили в стандартной лекарственной форме. Введение фармацевтической композиции можно осуществлять введением в ткани, пероральным введением, внутривенным введением, местным введением (трансдермальное введение, инстилляция или подобное) или ректальным введением. Понятно, что используют лекарственную форму, подходящую для соответствующего пути из таких путей введения. Например, предпочтительно пероральное введение или местное введение (трансдермальное введение или инстилляция).
Хотя предпочтительно, чтобы доза в виде противозудного средства подбиралась в зависимости от состояния пациента, такого как возраст, масса тела, характер и степень развития заболевания, а также способа введения, суточная доза соединения по изобретению как активного ингредиента для взрослого, как правило, находится в интервале 0,1 мг - 5 г на взрослого, предпочтительно, от 1 мг до 500 мг на взрослого, в случае перорального введения. В случае трансдермального введения доза находится в интервале 0,001%-5%, предпочтительно, от 0,01% до 0,1%. В случае инстилляции доза находится в интервале от 0,0001% до 0,5%, предпочтительно, от 0,001% до 0,01%. В некоторых случаях достаточной может быть меньшая доза, или может потребоваться более высокая доза. Как правило, дозу дают один раз в сутки, или ее можно давать внутривенно и периодически в течение 1-24 часов в сутки.
Пероральное введение можно осуществлять в твердой или жидкой лекарственной форме, такой как объемный порошок, порошок, таблетка, препарат с сахарным покрытием, капсула, гранула, суспензия, жидкость, сироп, капли, подъязычная таблетка, суппозиторий, или в других лекарственных формах. Объемный порошок получают измельчением активного ингредиента до подходящего размера. Порошок получают измельчением активного ингредиента до подходящего размера с последующим смешиванием с фармацевтическим носителем, таким как съедобный углевод, в том числе, крахмал или маннит, который измельчен подобным образом до подходящего размера. При необходимости, в порошок можно подмешивать корригент, консервант, диспергирующий агент, краситель, отдушку или другую добавку.
Капсулу получают, заполняя объемным порошком или порошком, который предварительно получен так, как описано выше, или гранулами, полученными так, как описано в разделе “Таблетка”, например, капсульную оболочку, такую как желатиновая капсула. Также возможно осуществить такую операцию заполнения после смешивания смазывающего вещества, флюидизирующего агента, такого как коллоидный диоксид кремния, тальк, стеарат магния, стеарат кальция или твердый полиэтиленгликоль, с материалом в форме порошка. Если добавляют вещество, способствующее рассыпанию, или солюбилизатор, такой как карбоксиметилцеллюлоза, кальцийкарбоксиметилцеллюлоза, гидроксипропилцеллюлоза с низкой степенью замещения, натрийкросскармелоза, натрийкарбоксикрахмал, карбонат кальция или карбонат натрия, эффективность фармацевтического препарата, заключенного в капсулу, может возрасти.
Тонкоизмельченный порошок соединения по изобретению можно суспендировать и диспергировать в растительном масле, полиэтиленгликоле, глицерине или поверхностно-активном веществе и затем инкапсулировать в желатиновую оболочку, причем посредством этого получают мягкую капсулу. Таблетки получают, обрабатывая порошкообразную смесь, превращая ее в гранулы или комки, добавляя к ним вещество, способствующее рассыпанию, или смазывающее вещество и затем прессуя смесь в таблетки. Порошкообразную смесь получают, смешивая соответствующим образом измельченный материал с разбавителем или основой, описанной выше, и, при необходимости, смесь также можно смешать со связующим веществом (например, натрийкарбоксиметилцеллюлозой, гидроксипропилцеллюлозой, метилцеллюлозой, гидроксипропилметилцеллюлозой, желатином, поливинилпирролидоном, поливиниловым спиртом или подобным веществом), замедлителем растворения (например, парафином, воском, гидрированным касторовым маслом или подобным веществом), промотором всасывания (например, четвертичной солью) или адсорбентом (например, бентонитом, каолином, дифосфатом кальция или подобным веществом). Порошкообразную смесь можно гранулировать, смачивая ее связующим веществом, таким как сироп, крахмальный клей, аравийская камедь, раствор целлюлозы или раствор полимера, и затем принудительно пропуская смесь через сито. Вместо гранулирования порошок, описанный выше, можно подвергнуть сначала таблетированию на таблетировочной машине и получить не полностью оформленный комок, который затем измельчают и получают гранулы. Можно предотвратить слипание полученных таким образом гранул, добавляя смазывающее вещество, такое как стеариновая кислота, стеарат, тальк или минеральное масло или подобное. Затем смесь, смазанную таким образом, прессуют в таблетки. На плоские таблетки, полученные таким образом, можно нанести пленочное покрытие или сахарное покрытие.
Кроме того, соединение по изобретению также можно прессовать в таблетки непосредственно после смешивания его с флюидизированным инертным носителем, не подвергая процессу грануляции или комкования, описанным выше. Также можно использовать прозрачную или полупрозрачную защитную пленку, полученную из шеллака, пленку, полученную из сахара или полимерного материала, и глянцевитую пленку, полученную из воска.
Другие пероральные лекарственные формы, такие как раствор, сироп и эликсир, также можно получить в стандартной лекарственной форме, такой чтобы определенное количество препарата содержало определенное количество соединения по изобретению. Сироп получают растворением соединения по изобретению в подходящем водном растворе с добавлением корригента, в то время как эликсир получают, используя нетоксичный спиртовой носитель. Суспензию получают, диспергируя соединения по изобретению в нетоксичном носителе. При необходимости также можно добавить солюбилизатор, эмульгатор (например, этоксилированный изостеариловый спирт или сложный эфир полиоксиэтиленсорбита), консервант, корригент (например, масло перечной мяты или сахарин) или любую другую добавку.
Стандартная лекарственная форма для перорального введения при необходимости также может представлять микрокапсулу. Такая форма может быть покрыта или заключена в полимер, воск или подобный материал, для того чтобы достичь пролонгированного действия или отсроченного высвобождения.
Ректальное введение можно осуществить с использованием суппозиториев, полученных смешиванием соединения по изобретению с водорастворимым или нерастворимым в воде твердым веществом с низкой температурой плавления, таким как полиэтиленгликоль, масло какао, эфиры высших кислот (например, миристилпальмитат) и их смесь.
Введение в ткани можно осуществить с использованием жидкой стандартной лекарственной формы, например формы раствора или суспензии, как препарата для подкожного, внутримышечного введения, введения в мочевой пузырь или внутривенной инъекции. Любой из таких препаратов можно получить суспендированием или растворением определенного количества соединения по изобретению в нетоксичном жидком носителе, подходящем для целей инъекции, таком как водная или масляная среда, с последующей стерилизацией полученных суспензии или раствора. С другой стороны, определенное количество соединения по изобретению можно поместить во флакон, который затем стерилизуют вместе с его содержимым и затем герметично закрывают. Вспомогательный флакон и носитель можно предоставить в сочетании с порошкообразным или лиофилизованным активным ингредиентом для цели растворения или смешивания непосредственно перед введением. Можно добавить нетоксичную соль или раствор соли для цели придания изотоничности раствору для инъекции. Также возможно использование стабилизатора, консерванта, эмульгатора или подобного вещества в сочетании.
Трансдермальное введение можно осуществить твердой или жидкой стандартной лекарственной формой, такой как аэрозоль, жидкость, суспензия, эмульсия, адгезивный препарат, мазь, припарка, линимент, лосьон, или другой лекарственной формой.
Мазь получают, например, смешивая и растирая определенное количество соединения по изобретению с фармацевтически приемлемой твердой основой, подходящей для мази, например водорастворимой основой или липидорастворимой основой, описанными в фармакопее Японии. Также возможно использование добавки, такой как стабилизатор, консервант, эмульгатор или суспендирующее вещество.
Инстилляцию можно осуществить жидкой стандартной лекарственной формой, например формой раствора или суспензии. Любой из таких препаратов можно получить, суспендируя или растворяя определенное количество соединения по изобретению в нетоксичном жидком носителе, подходящем для инстилляции, таком как водная или масляная среда, с последующей стерилизацией полученных суспензии или раствора. С другой стороны, определенное количество соединения по изобретению можно поместить во флакон, который затем стерилизуют вместе с его содержимым и затем герметично закрывают. Вспомогательный флакон и носитель можно предоставить в сочетании с порошкообразным или лиофилизованным активным ингредиентом для цели растворения или смешивания непосредственно перед введением. Можно добавить фармацевтически приемлемую соль или раствор соли для цели придания изотоничности глазным каплям. Также возможно использование стабилизатора, консерванта, эмульгатора или подобного вещества в сочетании.
ПРИМЕРЫ
Далее настоящее изобретение будет описываться подробнее со ссылкой на ссылочные примеры, примеры, примеры испытаний и примеры препаратов. Однако изобретение не ограничивается только приведенными примерами.
Ссылочный пример 1
4-{[(1S,2R)-2-Аминоциклогексил]амино}-N-(2-метоксиэтил)-6-метилхиназолин-2-карбоксамид
Стадия 1. трет-Бутил-{(1S,2R)-2-[(2-{[(2-метоксиэтил)амино]карбонил}-6-метилхиназолин-4-ил)амино]циклогексил}карбамат
К суспензии 15,0 г этил-4-({(1S,2R)-2-[(трет-бутоксикарбонил)амино]циклогексил}амино)-6-метилхиназолин-2-карбоксилата в 15 мл метанола добавляют 7,89 г 2-метоксиэтиламина и смесь перемешивают при 50ºС в течение 15 часов. После охлаждения реакционного раствора до комнатной температуры к нему добавляют 45 мл диизопропилового эфира и смесь перемешивают при 0ºС в течение 30 минут. Выпавшее в осадок кристаллическое вещество собирают фильтрацией, промывают диизопропиловым эфиром и сушат при пониженном давлении, посредство