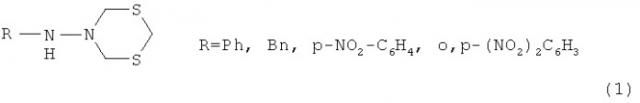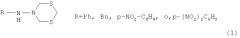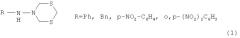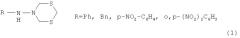Способ получения n-арил(бензил)-(1,3,5-дитиазиан-5-ил)аминов
Иллюстрации
Показать всеИзобретение относится к области органической химии, в частности к способу получения N-арил(бензил)-(1,3,5-дитиазин-5-ил)аминов общей формулы (1):
который заключается в том, что N-арил(бензил)-гидразины (фенилгидразин, бензилгидразин, n-нитрофенилгидразин, o-,n-динитрофенилгидразин) подвергают взаимодействию с 1,3,5-тритианом в присутствии катализатора Cp2TiCl2 при мольном соотношении N-арил(бензил)-гидразин: 1,3,5-тритиан: Cp2TiCl2=10:(10-12):(0.3-0.7), предпочтительно 10:11:0.5, при комнатной температуре (20°C) и атмосферном давлении в течение 3-5 ч. Технический результат - разработан новый способ получения N-арил(бензил)-(1,3,5-дитиазин-5-ил)аминов, которые могут найти применение в качестве веществ, модифицирующих и интенсифицирующих вкус и ароматы кондитерских изделий, а также в качестве селективных сорбентов и экстрагентов драгоценных металлов, специальных реагентов для подавления жизнедеятельности бактерий в различных средах. 1 табл., 1 пр.
Реферат
Предлагаемое изобретение относится к области органической химии, конкретно, к способу получения N-арил(бензил)-(1,3,5-дитиазинан-5-ил)аминов общей формулы (1):
Замещенные 1,3,5-дитиазинаны применяются в качестве добавок, модифицирующих и интенсифицирующих вкус и ароматы бекона, жареного мяса, тертого орехового ядра, ракообразных, кондитерских изделий, карамели, продуктов переработки плодов и овощей [Пат. 4228278 США; Р.Ж.Хим., 11, 11Р268П (1981), Пат. 4235938 США; Р.Ж.Хим., 23, 23Р282 (1981), Пат. 4200741 США; Р.Ж.Хим., 2, 2Р248 (1981)]. Производные 1,3,5-дитиазинана перспективны в качестве комплексообразователей [C.J.Galvez-Ruiz, C.Guadarrama-Perez, H.Nöth, A.Flores-Parra. Eur.J.Inorg. Chem., 601 (2004); Inorg. Chem., 23, 7569 (2003)], селективных сорбентов и экстрагентов драгоценных металлов [Deutsche Gold- und Silber-Scheideanstalt vormals Roessler. F.P. 1341792/1963 (Chem. Abs., 1964, 60, 5528d)], специальных реагентов для подавления жизнедеятельности бактерий в различных средах от легкой промышленности до нефтеперерабатывающей (Джемилев У.М., Алеев Р.С., Дальнова Ю.С., Кунакова Р.В., Хафизова С.Р., Ковтуненко С.В., Калимуллин А.А., Андрианов В.М., Исмагилов Ф.Р., Гафиатуллин P.P. Средство для подавления роста сульфатвосстанавливающих бактерий. Пат. РФ №2160233, 2000; Джемилев У.М., Алеев Р.С., Дальнова Ю.С., Кунакова Р.В., Хафизова С.Р. Средство для подавления роста сульфатвосстанавливающих бактерий. Пат. РФ №2206726, 2003).
Известен способ [Пат. 4228278 США; Р.Ж.Хим., 11, 11Р268П (1981), Пат. 4235938 США; Р.Ж.Хим., 23, 23Р282 (1981), Пат. 4200741 США; Р.Ж.Хим., 2, 2Р248 (1981)] получения производных 1,3,5-дитиазинана, в частности 2,4,6-триизобутил-1,3,5-дитиазинана формулы (2), взаимодействием аммиака с сероводородом и изовалериановым альдегидом при 20°C по схеме:
Известный способ не позволяет получать N-арил(бензил)-(1,3,5-дитиазинан-5-ил)амины общей формулы (1).
Известен способ [Deutsche Gold- und Silber-Scheideanstalt vormals Roessler. F.P. 1341792/1963 (Chem. Abs., 1964, 60, 5528d)] получения производных, 1,3,5-дитиазинана, в частности 5-[2-(1,3,5-дитиазинан-5-ил)этил]-1,3,5-дитиазинана формулы (3), с выходом 91% взаимодействием этилендиамина с гидросульфидом натрия и формальдегидом при 20°C по схеме:
Известным способом не могут быть получены N-арил(бензил)-(1,3,5-дитиазинан-5-ил)амины общей формулы (1).
Известен способ (В.Р.Ахметова, Г.Р.Надыргулова, С.Р.Хафизова и др., ЖОрХ, 2006, 1, 151) получения производных 1,3,5-дитиазинана, в частности N-метилен-(1,3,5-дитиазинан-5-ил)амина формулы (4), взаимодействием гидразина с формальдегидом и сероводородом (CH2O-H2S-NH2NH2=4:2:1) в присутствии промотора n-BuONa с выходом 56% по схеме:
Известный способ не позволяет получать N-фенил(бензил)-(1,3,5-дитиазинан-5-ил)амины общей формулы (1).
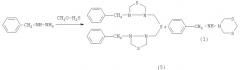
Известен способ (В.Р.Ахметова, Г.Р.Надыргулова, С.Р.Хафизова и др., Журн. орган химии, 2006, 1, с.151) получения N-бензил-(1,3,5-дитиазинан-5-ил)амина общей формулы (1) в смеси с соединением 1,3,4-тиадиазолидинового ряда (5) циклотиометилированием бензилгидразина с помощью CH2O и H2S в нейтральной среде (соотношение исходных реагентов соответственно 1:3:2, температура ~20°C).
Известный способ не селективный и позволяет получать лишь N-бензил-(1,3,5-дитиазинан-5-ил)амин общей формулы (1) в смеси с соединением 1,3,4-тиадиазолидинового ряда (5). Известным способом не могут быть получены N-арил-(1,3,5-дитиазинан-5-ил)амины общей формулы (1).
Таким образом, в литературе отсутствуют сведения о селективном получении N-бензил-(1,3,5-дитиазинан-5-ил)амина, отсутствуют сведения о получении N-арил-(1,3,5-дитиазинан-5-ил)аминов формулы (1).
Предлагается новый способ селективного получения N-арил(бензил)-(1,3,5-дитиазинан-5-ил)аминов общей формулы (1).
Сущность способа заключается во взаимодействии N-арил(бензил)-гидразинов (фенилгидразин, бензилгидразин, n-нитрофенилгидразин, o-,n-динитрофенилгидразин) с 1,3,5-тритианом в присутствии катализатора Cp2TiCl2, взятыми в мольном соотношении N-арил(бензил)-гидразин: 1,3,5-тритиан: Cp2TiCl2=10:(10-12):(0.3-0.7), предпочтительно 10:11:0.5, при комнатной температуре (20°C) и атмосферном давлении в ацетонитриле в качестве растворителя в течение 3-5 ч. Выход N-арил(бензил)-(1,3,5-дитиазинан-5-ил)аминов (1) составляет 64-76%. Реакция протекает по схеме:
N-арил(бензил)-(1,3,5-дитиазинан-5-ил)амины (1) образуются только лишь с участием N-арил(бензил)-гидразинов (фенилгидразин, бензилгидразин, n-нитрофенилгидразин, o-,n-динитрофенилгидразин) и 1,3,5-тритиана. В присутствии других соединений гидразина (например, алкилгидразины, диарилгидразины, алкиларилгидразины) целевые продукты (1) не образуются. Без катализатора реакция идет с выходом, не превышающим 15%.
Проведение указанной реакции в присутствии катализатора Cp2TiCl2 больше 0.7 ммолей не приводит к существенному увеличению выхода целевого продукта (1). Использование катализатора Cp2TiCl2 менее 0.3 ммолей снижает выход (1), что связано, возможно, со снижением каталитически активных центров в реакционной массе. Реакции проводили при температуре 20°C. При температуре выше 20°C (например, 60°C) снижается селективность реакции и увеличиваются энергозатраты, а при температуре ниже 20°C (например, -10°C) снижается скорость реакции. Опыты проводили в ацетонитриле, т.к. в нем хорошо растворяется 1,3,5-тритиан.
Существенные отличия предлагаемого способа.
В известном способе реакция идет с участием в качестве исходного соединения бензилгидразина, формальдегида и токсичного газообразного сероводорода в присутствии промотора n-BuONa. Способ не селективный и позволяет получать N-бензил-(1,3,5-дитиазин-5-ил)амин (1) в смеси с соединением 1,3,4-тиадиазолидинового ряда (5).
В предлагаемом способе в качестве исходных реагентов применяются арил(бензил)гидразины и 1,3,5-тритиан, a Cp2TiCl2 применяется в каталитических количествах. В отличие от известных способов предлагаемый способ позволяет синтезировать индивидуальные N-арил(бензил)-(1,3,5-дитиазинан-5-ил)амины (1).
Способ поясняется следующими примерами.
ПРИМЕР 1. В сосуд Шленка, установленный на магнитной мешалке, в атмосфере аргона помещают 5 мл ацетонитрила, 0.5 ммоль Cp2TiCl2, 10 ммоль фенилгидразина, 11 ммоль 1,3,5-тритиана. Реакционную смесь перемешивают при комнатной температуре (-20°C) в течение 4 ч. Из реакционной массы выделяют N-фенил-(1,3,5-дитиазинан-5-ил)амин с выходом 69%.
Другие примеры, подтверждающие способ, приведены в табл.1.
| Таблица 1 | ||||
| № п/п | Исходный арил-(бензил)гидразин | Соотношение арил(бензил)-гидразин: 1,3,5-тритиан: Cp2TiCl2, ммоль | Время реакции, час | Выход (1), % |
| 1 | фенилгидразин | 10:11:0.5 | 4 | 69 |
| 2 | -«- | 10:12:0.5 | 4 | 71 |
| 3 | -«- | 10:10:0.5 | 4 | 66 |
| 4 | -«- | 10:11:0.7 | 4 | 73 |
| 5 | -«- | 10:11:0.3 | 4 | 64 |
| 6 | -«- | 10:11:0.5 | 5 | 70 |
| 7 | -«- | 10:11:0.5 | 3 | 65 |
| 8 | бензилгидразин | 10:11:0.5 | 4 | 67 |
| 9 | n-нитрофенил-гидразин | 10:11:0.5 | 4 | 76 |
| 10 | o-,n-динитро-фенилгидразин | 10: 11:0.5 | 4 | 74 |
Все опыты проводили в ацетонитриле при комнатной температуре (~20°C).
Спектральные характеристики N-фенил-(1,3,5-дитиазинан-5-ил)-амина: Спектр ЯМР 1H (δ, м.д., CDCl3, J/Гц): 4.79 (c, 2H, H2C (2)); 5.20 (c, 4H, H2C (4,6)); 7.37-8.13 (м, 5H, H2C (8-13)). Спектр ЯМР 13C (δ, м.д., J/Гц): 32.19 (т, C (2)); 58.64 (т, C (4,6)); 114.45 (д, C (9,13)), 120.28 (д, C (10,12)), 129.13 (д, C (11)), 145.87 (c, C (8)).
Спектральные характеристики N-бензил-(1,3,5-дитиазинан-5-ил)-амина: Спектр ЯМР 1H (δ, м.д., CDCl3, J/Гц): 4.25 (c, 2H, H2C (2)); 4.63 (c, 2H, H2C(8)); 4.72 (c, 4H, H2C (4,6); 7.87-8.05 (уш.с, 5H, H2C (9-14)). Спектр ЯМР 13C (δ, м.д., J/Гц): 31.74 (т, C (2)); 58.17 (т, C (4,6)); 59.03 (т, C (8)), 127.34 (д, C (12)), 128.42 (д, C (11, 13)), 129.04 (д, C (10, 14)); 138.15 (c, С (9)).
Спектральные характеристики N-(4-нитрофенил)-1,3,5-дитиазинан-5-ил)амина:
Спектр ЯМР 1H (δ, м.д., J, Гц, 20°C): 3,6 (с, 1H, NH (7)); 3.55 (с, 2H, CH2 (2)); 4.24 (с, 4H, CH2 (4,6)); 7.22 (с, 2H, CH (10,12)); 8.13 (с, 2H, CH (9,13)). Спектр ЯМР 13C (CDCl3, δ, м.д.): 31.67 (т, С (2)); 56.33 (т, С (6,4)); 112,13 (д, С (13,9)); 122,68 (д, С (12,10)); 141,55 (с, С (11)); 152,36 (с, С (8)).
Спектральные характеристики N-(2,4-динитрофенил)-1,3,5-дитиазинан-5-ил)амина: Спектр ЯМР 1Н (δ, м.д., J, Гц, 20°C): 3,22 (с, 1H, NH (7)); 4.31 (с, 2H, CH2 (2)); 4.98 (с, 4 H, CH2 (4,6)); 7.64 (д, H, CH (13)); 8.25 (д, H, CH (12)); 9.01 (с, Н, СН (10)). Спектр ЯМР 13С (CDCl3, 5, м.д.): 34.79 (т, С (2)); 58.12 (т, С (6,4)); 114,20 (д, С (13)); 121,36 (д, С (12)); 127,41 (с, С (9)); 130,88 (с, С (12)); 139,45 (с, С (11)); 153,11 (с, С (8)).
Способ получения N-арил(бензил)-(1,3,5-дитиазинан-5-ил)аминов общей формулы (1): отличающийся тем, что N-арил(бензил)-гидразины (фенилгидразин, бензилгидразин, n-нитрофенилгидразин, o-, n-динитрофенилгидразин) подвергают взаимодействию с 1,3,5-тритианом в присутствии катализатора Cp2TiCl2 при мольном соотношении N-арил(бензил)-гидразин:1,3,5-тритиан:Cp2TiCl2=10:(10-12):(0,3-0,7), предпочтительно 10:11:0,5 при комнатной температуре (20°C) и атмосферном давлении в течение 3-5 ч.