Твердое лекарственное средство с контролируемым высвобождением
Иллюстрации
Показать всеИзобретение относится к медицине и фармацевтической промышленности и касается средства с контролируемым высвобождением, превосходящее по стабильности активного ингредиента. Средство может проявлять фармакологические эффекты стабильно и быстро после введения и демонстрирует продолжительный фармакологический эффект в течение длительного промежутка времени. Твердое лекарственное средство с контролируемым высвобождением содержит комбинацию (1) антацида, (2) части немедленного высвобождения, содержащей соединение, неустойчивое к кислоте и основанию, и (3) части замедленного высвобождения, содержащей соединение, неустойчивое к кислоте и основанию и имеющее пленку, которая растворяется при рН 6,5 или выше. 13 з.п. ф-лы, 8 табл., 12 прим.
Реферат
Область техники, к которой относится изобретение
Настоящее изобретение относится к твердому лекарственному средству. В частности, настоящее изобретение относится к твердому лекарственному средству с контролируемым высвобождением, которое является превосходным по стабильности активного ингредиента, может проявлять фармакологические эффекты устойчиво и быстро после введения и демонстрирует устойчивый фармакологический эффект в течение длительного периода времени.
Уровень техники
Так как ингибиторы протонового насоса (в дальнейшем иногда называемые как PPI (ИПН)), такие как соединения бензимидазола (например, лансопразол, омепразол, рабепразол, пантопразол, илапразол и подобные), обладают ингибирующим действием на секрецию желудочной кислоты, защитным действием на слизистую оболочку желудка и тому подобное, они широко использовались в качестве терапевтических агентов для язвенной болезни.
Однако эти соединения обладают низкой стабильностью и неустойчивы к влажности, температуре, свету, кислоте и тому подобное. Эти соединения особенно неустойчивы к кислоте и становятся чрезвычайно неустойчивыми, когда pH водного раствора или его суспензии становится низким. При пероральном введении, поэтому, эти соединения, возможно, не будут проявлять достаточную активность, так как они разрушаются желудочной кислотой и т.п.
Стабильность этих соединений в лекарственных формах, таких как таблетка, порошок, мелкодисперсные гранулы, капсулы и тому подобное, может стать ниже, чем стабильность соединений самих по себе, за счет сильных взаимодействий с другими ингредиентами компонентов в лекарственном средстве. В результате изменение цвета и разрушение можно наблюдать в течение получения и хранения.
Различные попытки были сделаны в фармацевтических лекарственных средствах, содержащих эти соединения в качестве активных ингредиентов, чтобы преодолеть нестабильность соединений. Например, были раскрыты таблетка, гранулы или мелкодисперсные гранулы, содержащие частицы ядра, содержащие ИПН или его соль, или его оптически активную форму в качестве активного ингредиента, и, в частности, pH-зависимо растворимая контролирующая высвобождение пленка (кишечнорастворимая пленка) (ссылка на патент 1). Благодаря кишечнорастворимой пленке эти лекарственные средства могут подавлять разрушение активного ингредиента желудочной кислотой и т.п. Однако так как для растворения кишечнорастворимой пленки в желудочно-кишечном тракте и абсорбции лекарственного средства требуется некоторое время, быстрое проявление фармакологического эффекта на ранней стадии введения вряд ли ожидается.
В то же время раскрыто разрушающееся в желудке твердое лекарственное средство, свободное от кишечнорастворимой пленки, которое содержит активный ингредиент, неустойчивый к кислоте, и по меньшей мере один вид компонента, выбранный из оксидов металлов и гидроксидов металлов (ссылка на патент 2). Кроме того, раскрыта жевательная таблетка, свободная от кишечнорастворимой пленки, которая содержит активный ингредиент, неустойчивый к кислоте, и по меньшей мере один вид компонента, выбранный из карбонатов щелочноземельного металла, оксидов металлов и гидроксидов металлов (ссылка на патент 3). Эти лекарственные средства могут подавлять разрушение активного ингредиента желудочной кислотой и т.п. после введения и являются подходящими для быстрого проявления фармакологических эффектов после введения. Однако сохранение фармакологического эффекта в течение длительного периода времени затруднительно для этих лекарственных средств.
Кроме того, раскрыто применение основной неорганической соли для стабилизации активного ингредиента при получении (ссылки на патент 4-6, ссылка на не-патент 1).
Кроме того, раскрыты различные лекарственные средства, обладающие множественными различными системами контроля высвобождения в комбинации для быстрого проявления фармакологического эффекта после введения и сохранения фармакологического эффекта в течение длительного периода времени (ссылка на патент 7-11).
ссылка на патент 1: JP-A-2004-292427
ссылка на патент 2: JP-A-2003-327533
ссылка на патент 3: JP-A-2005-154431
ссылка на патент 4: JP-A-62-277322
ссылка на патент 5: JP-A-2000-281564
ссылка на патент 6: JP-A-2000-103731
ссылка на патент 7: JP-A-2004-292442
ссылка на патент 8: JP-A-2004-300149
ссылка на патент 9: патент США №6610323
ссылка на патент 10: WO 01/51050
ссылка на патент 11: WO 03/61584
ссылка на не-патент 1: «DRUG DEVELOPMENT AND INDUSTRIAL PHARMACY», 18 (13), 1437-1447 (1992)
Раскрытие изобретения
Проблемы, которые решаются в изобретении
Существует требование для усовершенствования твердого лекарственного средства, включающего активный ингредиент, обладающий высокой стабильностью, в котором активный ингредиент устойчиво и быстро проявляет его фармакологический эффект после введения, и фармакологический эффект сохраняется в течение длительного периода времени.
Авторы настоящего изобретения провели интенсивные исследования и обнаружили, что твердое лекарственное средство, включающее (1) антацид, (2) часть немедленного высвобождения, содержащую соединение, неустойчивое к кислоте, и основание, и (3) часть замедленного высвобождения, содержащую соединение, неустойчивое к кислоте, и основание, и имеющую пленку, которая растворяется при рН 6,5 или выше в комбинации, демонстрирует высокую стабильность активного ингредиента, проявляет фармакологический эффект активного ингредиента устойчиво и быстро после введения и сохраняет фармакологический эффект в течение длительного периода времени, который привел к завершению настоящего изобретения.
Способы решения проблем
Соответственно, настоящее изобретение обеспечивает [1] твердое лекарственное средство с контролируемым высвобождением, включающее (1) антацид, (2) часть немедленного высвобождения, содержащую соединение, неустойчивое к кислоте, и основание, и (3) часть замедленного высвобождения, содержащую соединение, неустойчивое к кислоте, и основание, и имеющую пленку, которая растворяется при рН 6,5 или выше в комбинации;
[2] лекарственное средство вышеупомянутого [1], в котором пленка, которая растворяется при рН 6,5 или выше, содержит один вид или смесь двух или более видов, выбранных из группы, состоящей из фталата гидроксипропилметилцеллюлозы, фталата ацетата целлюлозы, карбоксиметилэтилцеллюлозы, сополимера метилметакрилат-метакриловая кислота, сополимера метакриловая кислота-этилакрилат, сополимера метакриловая кислота-метилакрилат-метилметакрилат, сукцината ацетата гидроксипропилметилцеллюлозы, фталата поливинилацетата и шеллака;
[3] лекарственное средство вышеупомянутого [1], в котором часть замедленного высвобождения включает частицу ядра, содержащую соединение, неустойчивое к кислоте, и основание, промежуточный слой, образованный на поверхности частицы ядра, и пленку, которая растворяется при рН 6,5 или выше, которая образована через промежуточный слой;
[4] лекарственное средство вышеупомянутого [1], в котором соединение, неустойчивое к кислоте, представляет собой ингибитор протонового насоса (ИПН);
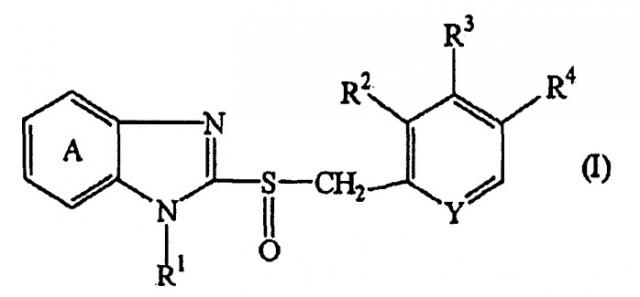
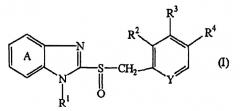
[5] лекарственное средство вышеупомянутого [4], в котором ИПН представляет собой соединение, представленное формулой (I):
где кольцо А представляет собой бензольное кольцо, необязательно имеющее заместитель(и), R1 представляет собой атом водорода, аралкильную группу, необязательно имеющую заместитель(и), ацильную группу или ацилоксигруппу, R2, R3 и R4 являются одинаковыми или различными и каждый представляет собой атом водорода, алкильную группу, необязательно имеющую заместитель(и), алкоксигруппу, необязательно имеющую заместитель(и), или аминогруппу, необязательно имеющую заместитель(и), и Y представляет собой атом азота или СН, или его оптически активную форму или его соль;
[6] лекарственное средство вышеупомянутого [4], в котором ИПН представляет собой лансопразол, омепразол, рабепразол, пантопразол, илапразол или его оптически активную форму или его соль;
[7] лекарственное средство вышеупомянутого [1], в котором антацид представляет собой по меньшей мере один компонент, выбранный из оксида металла, гидроксида металла и карбоната щелочноземельного металла;
[8] лекарственное средство вышеупомянутого [1], в котором 1% водный раствор или 1% водная суспензия антацида имеет pH менее чем 8,0;
[9] лекарственное средство вышеупомянутого [7], в котором оксид металла представляет собой по меньшей мере один вид, выбранный из группы, состоящей из оксида магния, силиката магния, сухого геля гидроксида алюминия и алюмометасиликата магния;
[10] лекарственное средство вышеупомянутого [7], в котором гидроксид металла представляет собой по меньшей мере один вид, выбранный из группы, состоящей из гидроксида магния, гидроксида алюминия, синтетического гидроталькита, совместного осадка гидроксида алюминия и гидроксида магния, совместного осадка гидроксида алюминия, карбоната магния и карбоната кальция и совместного осадка гидроксида алюминия и бикарбоната натрия;
[11] лекарственное средство вышеупомянутого [7], в котором карбонат щелочноземельного металла представляет собой карбонат кальция или карбонат магния;
[12] лекарственное средство вышеупомянутого [1], в котором содержание антацида составляет 5 мэкв - 50 мэкв;
[13] лекарственное средство вышеупомянутого [1], в котором весовое отношение содержания соединения, неустойчивого к кислоте, в части немедленного высвобождения и части замедленного высвобождения составляет 10:1-1:10;
[14] лекарственное средство вышеупомянутого [1], которое демонстрирует увеличение внутрижелудочного среднего pH до 4 или выше через 0,5 часа после перорального введения млекопитающему и время сохранения pH 4 или выше не менее чем 14 часов в сутки; и
[15] твердое лекарственное средство, демонстрирующее увеличение внутрижелудочного среднего рН до 4 или выше через 0,5 часа после перорального введения млекопитающему и время сохранения рН 4 или выше не менее чем 14 часов в сутки.
Настоящее изобретение объясняется подробно в следующем.
Твердое лекарственное средство с контролируемым высвобождением по настоящему изобретению включает (1) антацид, (2) часть немедленного высвобождения, содержащую соединение, неустойчивое к кислоте, и основание, и (3) часть замедленного высвобождения, содержащую соединение, неустойчивое к кислоте, и основание, и имеющую пленку, которая растворяется при рН 6,5 или выше в комбинации.
В настоящем описании термины «твердое лекарственное средство с контролируемым высвобождением по настоящему изобретению» и «твердое лекарственное средство по настоящему изобретению» используются взаимозаменяемо, если не определено иначе.
(1) Антацид
Твердое лекарственное средство по настоящему изобретению содержит антацид. Антацид нейтрализует внутрижелудочный рН до высвобождения соединения, неустойчивого к кислоте, которое представляет собой активный ингредиент в желудке, посредством чего остаточное отношение соединения увеличивается и устойчивый и быстрый фармакологический эффект соединения может быть проявлен. В качестве антацида, который используют в настоящем изобретении, по меньшей мере один вид компонента, выбранный из группы, состоящей из оксида металла, гидроксида металла и карбоната щелочноземельного металла, является предпочтительным.
В качестве вышеупомянутого оксида металла предпочтительно используют по меньшей мере один вид, выбранный из группы, состоящей из оксида магния, силиката магния (2MgO·3SiO2·xH2O), сухого геля гидроксида алюминия (Al2O3·xH2O) и алюмометасиликата магния (Al2O3·MgO·2SiO2·xH2O), все для фармацевтических агентов.
Из них оксид магния является более предпочтительным. Оксид магния для медицинского применения, который является превосходящим по кислотной реактивности и имеет нейтрализующую способность, является предпочтительным. Так же, как оксид магния, можно применять полученный общим способом производства и коммерчески доступный продукт. Что называют легко обожженным оксидом магния, который получают прокаливанием при низкой температуре, является предпочтительным. Оксид магния, полученный прокаливанием при температуре примерно 500°C - примерно 1000°C, является обычно предпочтительным, а из аспекта нейтрализующей способности оксид магния, полученный прокаливанием при температуре примерно 600°C - примерно 900°C, является наиболее предпочтительным, и оксид магния, полученный прокаливанием примерно при 800°C, является самым предпочтительным. Из таких оксидов магния оксид магния, имеющий удельную площадь поверхности по методу ВЕТ обычно 10-50 м2/г, предпочтительно 20-50 м2/г, является самым предпочтительным.
В настоящем описании удельная площадь поверхности по методу ВЕТ представляет собой удельную площадь поверхности, измеренную методом адсорбции газообразного азота, где удельную площадь поверхности измеряют, основываясь на количестве газообразного азота, адсорбируемого определенным количеством поверхности оксида магния и мелкодисперсных пор, в которые поступает газообразный азот.
Примеры оксида магния включают коммерчески доступный тяжелый оксид магния (производства Kyowa chemical Industries Ltd.), тяжелый оксид магния (производства Tomita Pharmaceutical Co., Ltd.), тяжелый N-оксид магния (производства Kyowa chemical Industries Ltd.), легкий оксид магния (производства Kyowa chemical Industries Ltd.) и подобные. В частности, тяжелый N-оксид магния (производства Kyowa chemical Industries Ltd.) и т.п. является предпочтительным.
В качестве гидроксида металла по меньшей мере один вид, выбранный из группы, состоящей из гидроксида магния, гидроксида алюминия, синтетического гидроталькита (Mg6Al2(OH)16CO3 ·4H2O), совместного осадка гидроксида алюминия и гидроксида магния, совместного осадка гидроксида алюминия, карбоната магния и карбоната кальция и совместного осадка гидроксида алюминия и бикарбоната натрия, все для фармацевтических агентов, является предпочтительным. Из них гидроксид магния является предпочтительным ввиду свойства дезинтеграции лекарственного средства, свойства растворимости соединения, неустойчивого к кислоте, и т.п.
В качестве вышеупомянутого карбоната щелочноземельного металла можно использовать карбонат кальция и карбонат магния для фармацевтических агентов и т.п.
Вышеупомянутый оксид металла, гидроксид металла и карбонат щелочноземельного металла могут быть использованы отдельно или два или более их видов могут быть объединены.
Некоторые из оксидов металлов и гидроксидов металлов полируют поверхность аппарата для получения составов в процессе производства с получением таблеток, имеющих полностью или частично темную поверхность или темную область, линию или плоскость, или прилипают к прессу для таблетирования.
Эти свойства заметно уменьшают производительность. Таким образом, было обнаружено, что, когда должен быть выбран оксид металла или гидроксид металла, обладающий свойством истираемости и прилипания к прессу, то оксид металла и гидроксид металла, свободные от таких свойств, можно использовать в комбинации, или они могут быть подвергнуты влажному или сухому гранулированию вместе с добавкой, пригодной для фармацевтических продуктов (например, с эксципиентом, связывающим веществом, дезинтегрантом и подобными, описанными в нижеупомянутом (4)), посредством чего полирующее действие и свойство прилипания к прессу могут быть подавлены.
Вышеупомянутый антацид предпочтительно имеет pH не менее чем 8,0, более предпочтительно в пределах диапазона 8,0-12,0, когда он приготовлен в 1% водном растворе или 1% водной суспензии.
Вышеупомянутый антацид добавляют в количестве, позволяющем быстрое растворение антацида для нейтрализации желудочной кислоты, вместе с внутрижелудочной дезинтеграцией твердого лекарственного средства и предпочтительно до растворения соединения, неустойчивого к кислоте, чтобы предотвратить разрушение неустойчивого к кислоте соединения в результате воздействия желудочной кислоты. Хотя количество изменяется в зависимости от способности каждого антацида нейтрализовать желудочную кислоту, в твердом лекарственном средстве по настоящему изобретению оно предпочтительно составляет 5 мэкв - 50 мэкв, более предпочтительно 10 мэкв - 50 мэкв.
2) Часть немедленного высвобождения
Часть немедленного высвобождения твердого лекарственного средства по настоящему изобретению содержит соединение, неустойчивое к кислоте и основанию.
В части немедленного высвобождения свойство высвобождения соединения, неустойчивого к кислоте, которое представляет собой активный ингредиент, является немедленным высвобождением. В данном описании немедленное высвобождение означает отношение извлечения активного ингредиента за 30 минут после начала теста не менее чем 85%, когда Japanese Pharmacopoeia Dissolution Test Method 2 (Paddle Method) выполняют, используя подходящий испытуемый раствор (500 мл или 900 мл) при условиях вращения мешалки 100 оборотов в минуту. В качестве испытуемого раствора соединения, неустойчивого к кислоте, в части немедленного высвобождения используют, например, испытуемый раствор, имеющий концентрацию активного ингредиента не более чем 1/3 предела растворимости соединения, неустойчивого к кислоте, после его 100% растворения в испытуемом растворе. Предпочтительно используют 2-ую жидкость Japanese Pharmacopoeia Dissolution Test Method или воду.
(2-1) Соединение, неустойчивое к кислоте
Вышеупомянутое соединение, неустойчивое к кислоте, особенно не ограничивается и может быть любым соединением, которое становится неустойчивым в результате воздействия желудочной кислоты. В качестве такого соединения, неустойчивого к кислоте, могут быть использованы, например, противовоспалительные ферментные агенты, такие как ИПН, эритромициновые антибактериальные соединения, серрапептаза, полущелочная протеиназа и тому подобное, ИПН является предпочтительным.
В качестве ИПН, например, соединение, представленное следующей формулой (I) [в дальнейшем иногда называется просто как соединение (I)], является предпочтительным.
Примеры соединения (I) включают соединение, представленное формулой (I):
где кольцо A представляет собой бензольное кольцо, необязательно имеющее заместитель(и), R1 представляет собой атом водорода, аралкильную группу, необязательно имеющую заместитель(и), ацильную группу или ацилоксигруппу, R2, R3 и R4 являются одинаковыми или различными и каждый представляет собой атом водорода, алкильную группу, необязательно имеющую заместитель(и), алкоксигруппу, необязательно имеющую заместитель(и), или аминогруппу, необязательно имеющую заместитель(и), и Y представляет собой атом азота или CH, или его оптически активную форму или его соль.
В вышеупомянутом соединении (I) примеры «заместителя» «бензольного кольца, необязательно имеющего заместитель(и)» для кольца A, включают атом галогена, цианогруппу, нитрогруппу, алкильную группу, необязательно имеющую заместитель(и), гидроксигруппу, алкоксигруппу, необязательно имеющую заместитель(и), арильную группу, арилоксигруппу, карбоксигруппу, ацильную группу, ацилоксигруппу, 5-10-членную гетероциклическую группу и тому подобное. Бензольное кольцо может быть замещено примерно 1-3 из этих заместителей. Когда число заместителей представляет собой два или более, каждый заместитель может быть одинаковым или различным. Из этих заместителей атом галогена, алкильная группа, необязательно имеющая заместитель(и), алкоксигруппа, необязательно имеющая заместитель(и), и подобные являются предпочтительными.
Примеры атома галогена включают атом фтора, хлора, брома и тому подобное. Из них атом фтора является предпочтительным.
Примеры «алкильной группы» «алкильной группы, необязательно имеющей заместитель(и)», включают C1-7 алкильную группу (например, метильная, этильная, пропильная, изопропильная, бутильная, изобутильная, втор-бутильная, трет-бутильная, пентильная, гексильная, гептильная группа и т.д.) и подобные. Примеры «заместителя» «алкильной группы, необязательно имеющей заместитель(и)», включают атом галогена, гидроксигруппу, C1-6 алкоксигруппу (например, метокси, этокси, пропокси, бутокси и т.д.), C1-6 алкоксикарбонильную группу (например, метоксикарбонильная, этоксикарбонильная, пропоксикарбонильная и т.д.), карбамоильную группу и подобные, и число этих заместителей может быть примерно 1-3. Когда число заместителей представляет собой два или более, каждый заместитель может быть одинаковым или различным.
Примеры «алкоксигруппы» «алкоксигруппы, необязательно имеющей заместитель(и)», включают C1-6 алкоксигруппу (например, метокси, этокси, пропокси, изопропокси, бутокси, изобутокси, пентокси и т.д.) и подобные. Примеры «заместителя» «алкоксигруппы, необязательно имеющей заместитель(и)», включают заместитель, подобный «заместителю» вышеупомянутой «алкильной группы, необязательно имеющей заместитель(и)», и число заместителей является таким же.
Примеры «арильной группы» включают C6-14 арильную группу (например, фенил, 1-нафтил, 2-нафтил, бифенил, 2-антрил и т.д.) и подобные.
Примеры «арилоксигруппы» включают C6-14 арилоксигруппу (например, фенилокси, 1-нафтилокси, 2-нафтилокси и т.д.) и подобные.
Примеры «ацильной группы» включают формил, алкилкарбонил, алкоксикарбонил, карбамоил, алкилкарбамоил, алкилсульфинил, алкилсульфонил и подобные.
Примеры «алкилкарбонильной группы» включают C1-6 алкилкарбонильную группу (например, ацетил, пропионил и т.д.) и подобные.
Примеры «алкоксикарбонильной группы» включают C1-6 алкоксикарбонильную группу (например, метоксикарбонил, этоксикарбонил, пропоксикарбонил, бутоксикарбонил и т.д.) и подобные.
Примеры «алкилкарбамоильной группы» включают N-C1-6 алкилкарбамоильную группу (например, метилкарбамоильная, этилкарбамоильная группа и т.д.), N,N-ди-C1-6алкилкарбамоильную группу (например, N,N-диметилкарбамоил, N,N-диэтилкарбамоил и т.д.) и подобные.
Примеры «алкилсульфинильной группы» включают C1-7 алкилсульфинильную группу (например, метилсульфинил, этилсульфинил, пропилсульфинил, изопропилсульфинил и т.д.) и подобные.
Примеры «алкилсульфонильной группы» включают C1-7 алкилсульфонильную группу (например, метилсульфонил, этилсульфонил, пропилсульфонил, изопропилсульфонил и т.д.) и подобные.
Примеры «ацилоксигруппы» включают алкилкарбонилокси, алкоксикарбонилокси, карбамоилокси, алкилкарбамоилокси, алкилсульфинилокси, алкилсульфонилокси и подобные.
Примеры «алкилкарбонилоксигруппы» включают C1-6 алкилкарбонилоксигруппу (например, ацетилокси, пропионилокси и т.д.) и подобные.
Примеры «алкоксикарбонилоксигруппы» включают C1-6 алкоксикарбонилоксигруппу (например, метоксикарбонилокси, этоксикарбонилокси, пропоксикарбонилокси, бутоксикарбонилокси и т.д.) и подобные.
Примеры «алкилкарбамоилоксигруппы» включают C1-6 алкилкарбамоилоксигруппу (например, метилкарбамоилокси, этилкарбамоилокси и т.д.) и подобные.
Примеры «алкилсульфинилоксигруппы» включают C1-7 алкилсульфинилоксигруппу (например, метилсульфинилокси, этилсульфинилокси, пропилсульфинилокси, изопропилсульфинилокси и т.д.) и подобные.
Примеры «алкилсульфонилоксигруппы» включают C1-7 алкилсульфонилоксигруппу (например, метилсульфонилокси, этилсульфонилокси, пропилсульфонилокси, изопропилсульфонилокси и т.д.) и подобные.
Примеры «5-10-членной гетероциклической группы» включают 5-10-членную (предпочтительно 5- или 6-членную) гетероциклическую группу, содержащую, кроме атома углерода, один или несколько (например, 1-3) гетероатомов, выбранных из атома азота, атома серы и атома кислорода и тому подобное. Определенные примеры включают 2- или 3-тиенильную группу, 2-, 3- или 4-пиридильную группу, 2- или 3-фурильную группу, 1-, 2- или 3-пирролильную группу, 2-, 3-, 4-, 5- или 8-хинолильную группу, 1-, 3-, 4- или 5-изохинолильную группу, 1-, 2- или 3-индолильную группу и подобные. Из них предпочтительной является 5- или 6-членная гетероциклическая группа, такая как 1-, 2- или 3-пирролильная группа и подобные.
Предпочтительно, кольцо A представляет собой бензольное кольцо, необязательно имеющее 1 или 2 заместителя, выбранных из атома галогена, необязательно галогенированной C1-4 алкильной группы, необязательно галогенированной C1-4 алкоксигруппы и 5- или 6-членной гетероциклической группы.
Примеры «аралкильной группы» «аралкильной группы, необязательно имеющей заместитель(и)» для R1, включают C7-16 аралкильную группу (например, C6-10арилC1-6алкильная группа, такая как бензил, фенетил и т.д. и т.п.) и подобные. Примеры «заместителя» «аралкильной группы, необязательно имеющей заместитель(и)», включают заместители, подобные «заместителю» вышеупомянутой «алкильной группы, необязательно имеющей заместитель(и)», и число заместителей представляет собой примерно 1-4. Когда число заместителей представляет собой два или более, каждый заместитель может быть одинаковым или различным.
Примеры «ацильной группы» для R1 включают «ацильную группу», описанную в качестве заместителя для вышеупомянутого кольца A, и т.п.
Примеры «ацилоксигруппы» для R1 включают «ацилоксигруппу», описанную в качестве заместителя для вышеупомянутого кольца A, и т.п.
Предпочтительный R1 представляет собой атом водорода.
Примеры «алкильной группы, необязательно имеющей заместитель(и)» для R2, R3 или R4, включают «алкильную группу, необязательно имеющую заместитель(и)», описанную в качестве заместителя для вышеупомянутого кольца A, и т.п.
Примеры «алкоксигруппы, необязательно имеющей заместитель(и)» для R2, R3 или R4, включают «алкоксигруппу, необязательно имеющую заместитель(и)», описанную в качестве заместителя для вышеупомянутого кольца A, и т.п.
Примеры «аминогруппы, необязательно имеющей заместитель(и)» для R2, R3 или R4, включают аминогруппу, моно-C1-6алкиламиногруппу (например, метиламино, этиламино и т.д.), моно-C6-14ариламиногруппу (например, фениламино, 1-нафтиламино, 2-нафтиламино и т.д.), ди-C1-6алкиламиногруппу (например, диметиламино, диэтиламино и т.д.), ди-C6-14ариламиногруппу (например, дифениламино и т.д.) и подобные.
Предпочтительный R2 представляет собой C1-6 алкильную группу, C1-6 алкоксигруппу, C1-6алкокси-C1-6алкоксигруппу или ди-C1-6алкиламиногруппу. Более предпочтительный R2 представляет собой C1-3 алкильную группу или C1-3 алкоксигруппу.
Предпочтительный R3 представляет собой атом водорода, C1-6алкокси-C1-6алкоксигруппу или необязательно галогенированную C1-6 алкоксигруппу. Более предпочтительный R3 представляет собой C1-3 алкоксигруппу, которая является необязательно галогенированной или замещенной C1-3 алкоксигруппой.
Предпочтительный R4 представляет собой атом водорода или C1-6 алкильную группу. Более предпочтительный R4 представляет собой атом водорода или C1-3 алкильную группу (в частности, атом водорода).
Предпочтительный Y представляет собой атом азота.
Предпочтительное соединение формулы (I) представляет собой соединение, в котором кольцо A представляет собой бензольное кольцо, необязательно имеющее заместитель(и), выбранный из атома галогена, необязательно галогенированной C1-4 алкильной группы, необязательно галогенированной C1-4 алкоксигруппы и 5- или 6-членной гетероциклической группы, R1 представляет собой атом водорода, R2 представляет собой C1-6 алкильную группу, C1-6 алкоксигруппу, C1-6алкокси-C1-6алкоксигруппу или ди-C1-6алкиламиногруппу, R3 представляет собой атом водорода, C1-6алкокси-C1-6алкоксигруппу или необязательно галогенированную C1-6 алкоксигруппу, R4 представляет собой атом водорода или C1-6 алкильную группу, и Y представляет собой атом азота.
Из соединения (I), соединение, представленное формулой (Ia):
где R1 представляет собой атом водорода, R2 представляет собой C1-3 алкильную группу или C1-3 алкоксигруппу, R3 является C1-3 алкоксигруппой, необязательно галогенированной или замещенной C1-3 алкоксигруппой, R4 представляет собой атом водорода или C1-3 алкильную группу, и R5 представляет собой атом водорода, необязательно галогенированную C1-3 алкоксигруппу или пирролильную группу (например, 1-, 2- или 3-пирролильную группу).
В формуле (Ia) соединение, где R1 представляет собой атом водорода, R2 представляет собой C1-3 алкильную группу, R3 представляет собой необязательно галогенированную C1-3 алкоксигруппу, R4 представляет собой атом водорода, и R5 представляет собой атом водорода или необязательно галогенированную C1-3 алкоксигруппу, является более предпочтительным.
Определенные примеры соединения (I) включают следующие соединения:
2-[[[3-метил-4-(2,2,2-трифторэтокси)-2-пиридинил]метил]сульфинил]-1H-бензимидазол, 2-[[(3,5-диметил-4-метокси-2-пиридинил)метил]сульфинил]-5-метокси-1H-бензимидазол, 2-[[[4-(3-метоксипропокси)-3-метил-2-пиридинил]метил]сульфинил]-1H-бензимидазола натриевая соль, 5-дифторметокси-2-[[(3,4-диметокси-2-пиридинил)метил]сульфинил]-1H-бензимидазол и подобные.
Из этих соединений 2-[[[3-метил-4-(2,2,2-трифторэтокси)-2-пиридинил]метил]сульфинил]-1H-бензимидазол (лансопразол) является предпочтительным.
Соединение (I) может быть рацематом или оптически активной формой, такой как R-форма, S-форма и подобные. Например, соединение (I) может быть оптически активной формой, такой как (R)-2-[[[3-метил-4-(2,2,2-трифторэтокси)-2-пиридинил]метил]сульфинил]-1H-бензимидазол (который иногда упоминается как лансопразол R форма) и тому подобное. Кроме того, оптически активная форма является предпочтительной.
В качестве соли соединения (I) или его оптически активной формы фармацевтически приемлемая соль является предпочтительной. Например, могут быть упомянуты соли соединения (I) или его оптически активной формы с неорганическим основанием, органическим основанием и основной аминокислотой, и т.п.
Предпочтительные примеры соли с неорганическим основанием включают соли щелочного металла, такие как натриевая соль, калиевая соль и подобные; соли щелочноземельного металла, такие как кальциевая соль, магниевая соль и подобные; аммониевая соль и подобные.
Предпочтительные примеры соли с органическим основанием включают соли с алкиламином (триметиламином, триэтиламином и т.д.), гетероциклическим амином (пиридином, пиколином и т.д.), алканоламином (этаноламином, диэтаноламином, триэтаноламином и т.д.), дициклогексиламином, N,N'-дибензилэтилендиамином и тому подобное.
Предпочтительные примеры соли с основной аминокислотой включают соли с аргинином, лизином, орнитином и тому подобное.
Из них предпочтительной является соль щелочного металла или соль щелочноземельного металла. Особенно натриевая соль является предпочтительной.
Соединение (I) может быть получено способом, известным по существу, например, способом, описанным в JP-A-61-50978, US-B-4628098, JP-A-10-195068, WO98/21201 и тому подобное, или способом, аналогичным этому.
Оптически активная форма соединения (I) может быть получена способом, таким как способ оптического разрешения (фракционная перекристаллизация, метод хиральной колонки, диастереомерный метод, метод с использованием микроорганизма или фермента и т.д.), асимметричное окисление и тому подобное. Например, лансопразол R форма может быть получен согласно способам, описанным в WO00/78745, WO01/83473, WO01/87874 и WO02/44167.
ИПН, который используют в настоящем изобретении, предпочтительно выбирают из соединений бензимидазола, обладающих противоязвенной активностью, таких как лансопразол, омепразол, рабепразол, пантопразол и илапразол, и их оптически активных форм и их фармацевтически приемлемых солей. Наиболее предпочтительными являются лансопразол, омепразол, рабепразол или пантопразол.
(2-2) Основание
В настоящем изобретении основание добавляют к части немедленного высвобождения для стабилизации вышеупомянутого соединения, неустойчивого к кислоте, в лекарственном средстве.
Примеры вышеупомянутого основания включают карбонаты щелочноземельного металла (например, карбонат кальция, карбонат магния для фармацевтического агента и т.д.), трометамол, сукцинат динатрия, вторичный кислый фосфат натрия, ортофосфат натрия, вторичный кислый фосфат калия, L-аргинин и тому подобное. Предпочтительным является карбонат щелочноземельного металла, и более предпочтительным является карбонат кальция. Эти основания могут быть использованы отдельно, или два или более их видов могут быть использованы в комбинации.
Количество основания, которое будет добавлено, особенно не ограничивают, до тех пор, пока оно достаточно для стабилизации вышеупомянутого вещества, неустойчивого к кислоте. Оно обычно составляет 1,0 масс.% - 60 масс.%, предпочтительно 3,0 масс.% - 50 масс.% относительно общего количества части немедленного высвобождения.
Вышеупомянутое основание следует отличать от антацида, описанного в вышеупомянутом (1). Например, вещество, используемое в качестве вышеупомянутого основания, может быть также использовано в качестве антацида вышеупомянутого (1) (например, вышеупомянутый «карбонат щелочноземельного металла»). Когда такое вещество используют в качестве антацида, оно нейтрализует внутрижелудочный pH. С другой стороны, когда его добавляют к части немедленного высвобождения в качестве основания, оно стабилизирует соединение, неустойчивое к кислоте, в лекарственном средстве.
Форма вышеупомянутой части немедленного высвобождения может быть любой. Чтобы достичь немедленного высвобождения, гранулы, мелкодисперсные гранулы и тому подобное являются предпочтительными.
Вышеупомянутая часть немедленного высвобождения может быть получена способом, известным по существу. Например, она может быть получена путем комбинирования достаточных количеств соединения, неустойчивого к кислоте и основанию, и, где необходимо, добавки, такой как эксципиент, связывающее вещество, дезинтегрирующее вещество, лубрикант, модификатор лекарственных веществ, краситель, ароматизатор и тому подобное, и гранулирования смеси.
Вышеупомянутое гранулирование предпочтительно осуществляют способом влажного гранулирования. Способ влажного гранулирования включает диспергирование или растворение смеси активного ингредиента и других компонентов, таких как эксципиент и подобные, в воде, связывающем веществе или растворителе, гранулирование дисперсии или раствора и сушку того же самого с получением продукта гранулирования, такого как гранулы, мелкодисперсные гранулы и тому подобное. Способ влажного гранулирования может быть осуществлен согласно способу, известному в фармацевтической области. В качестве механизма гранулирования могут быть использованы, например, известные методы, такие как экструдирование, ожижение, обработка в барабане, центрифугирование, размешивание, распыление и подобные.
(3) Часть замедленного высвобождения
Часть замедленного высвобождения в твердом лекарственном средстве по настоящему изобретению содержит соединение, неустойчивое к кислоте, и основание, и имеет пленку, которая растворяется при рН 6,5 или выше.
В части замедленного высвобождения свойство высвобождения соединения, неустойчивого к кислоте, которое является активным ингредиентом, является замедленным высвобождением. Замедленное высвобождение означает отношение извлечения активного ингредиента за 30 минут после начала теста не менее чем 85%, когда Japanese Pharmacopoeia Dissolution Test Method 2 (Paddle Method) выполняют, используя подходящий испытуемый раствор (500 мл или 900 мл) при условиях вращения мешалки 100 оборотов в минуту. В качестве испытуемого раствора в данном описании может быть использован раствор, подобный приведенному в объяснении вышеупомянутой (2) части немедленного высв