Производное пиперидина
Иллюстрации
Показать всеИзобретение относится к соединениям формулы (I) или его фармацевтически приемлемым солям:
где R1, R2 и R3, которые являются одинаковыми или различными, означают Н, низший алкил; R4, R5, R6, R7 и R8, которые являются одинаковыми или различными, означают Н, низший алкил, галоген, нитро, -X-OR0, -X-NR10R11, -X-NR0C(O)R10, -Х-О-галоген низший алкил, -Х-О-Х-фенил; или R6 и R7 объединены с образованием -0-низший алкилен-О-; R0, который является одинаковым или различным, означает Н, низший алкил; R10, R11, которые являются одинаковыми или различными, означают Н, низший алкил; X, который является одинаковым или различным, означает связь, низший алкилен. Соединения проявляют ингибирующую активность в отношении 17βHSD типа 5, что позволяет использовать их для получения фармацевтической композиции и в способе ингибирования 17βHSD типа 5. 8 н. и 7 з.п. ф-лы, 11 табл., 32 пр.
Реферат
Область техники, к которой относится изобретение
Данное изобретение относится к производному пиперидина, обладающему фармакологической активностью, и/или к его соли. Кроме того, данное изобретение относится к лекарственному средству или фармацевтической композиции, содержащей производное пиперидина и/или его соль, описанные выше, в качестве активного ингредиента.
Уровень техники
Доброкачественная гиперплазия простаты (ВРН) представляет собой заболевание, возникающее в основном у мужчин в возрасте старше 50 лет или более и сопровождающееся мочевыми расстройствами, и степень ее распространенности повышается с возрастом. Число пациентов с ВРН в Японии постоянно увеличивалось в последние годы с ростом старения населения. ВРН значительно ухудшает качество жизни пожилых мужчин из-за мочевых расстройств и является серьезной проблемой в плане медицинской экономики, так как представляет собой наиболее часто диагностируемое и подвергаемое лечению заболевание в области урологии.
Было установлено, что два фактора, а именно непосредственное уретральное сдавление из-за гипертрофии простаты (механическая непроходимость) и подъем интрауретрального давления из-за повышенного сокращения гладкой мышцы простаты через симпатический нерв (функциональная непроходимость), одновременно включены в мочевые расстройства, сопровождающие ВРН. Лекарственная терапия может применяться в отношении обоих данных механизмов, при этом в случае механической непроходимости главным образом используются ингибиторы 5α-редуктазы и в случае функциональной непроходимости главным образом используются α1-симпатолитические средства (α1-блокаторы). Ингибиторы 5α-редуктазы вызывают регрессию простаты из-за их антиандрогенного эффекта, основанного на подавлении превращения тестостерона в 5α-дегидротестостерон (DHT), который представляет собой более сильнодействующий андроген, производимый 5α-редуктазой. Регрессирует только эпителий простаты, однако требуется длительный период времени (от нескольких недель до нескольких месяцев), чтобы эффективность лекарственного средства становилась очевидной. C другой стороны, так как α1-блокаторы проявляют свою эффективность как лекарственные средства очень быстро после введения и являются исключительными по безопасности, α1-блокаторы в настоящее время являются первоочередным средством для лечения ВРН. Однако в результате долговременных клинических изучений было установлено, что ингибитор 5α-редуктазы значительно замедлял переход к инвазивной терапии по сравнению с одним применением α1-блокатора и др. (“The New England Journal of Medicine”, 2003, Vol. 349, p. 2387-2398), поэтому применение ингибиторов 5α-редуктазы недавно было рассмотрено снова.
Считалось, что DHT в простате получается под действием 5α-редуктазы из тестостерона, который образуется в яичках и выделяется эндокринологически в простате. Недавно, однако, было опубликовано, что примерно половина DHT и его предшественник, тестостерон, в простате синтезируются из дегидроэпиандростерона (DHEA) - стероида, получаемого из надпочечника, в клетках простаты (“Frontier in Neuroendocrinology”, 2001, Vol. 22, p. 185-212). Данный тип системы продуцирования полового гормона в клетках целевых органов половых гормонов называется интракринологией.
Для ингибиторов 5α-редуктазы трудно ингибировать локальный синтез тестостерона (интракринный синтез тестостерона) в простате. Например, было опубликовано, что концентрация DHT в простате пациентов с BHP была снижена после введения финастерида, ингибитора 5α-редуктазы, приблизительно до 20% концентрации перед введением, в то время как концентрация тестостерона, предшественника, в простате была обратимо повышена в 4 раза (“The Journal of Urology”, 1999, Vol. 161, p. 332-337). Это означает, что хотя ингибитор 5α-редуктазы обладает эффектом по снижению концентрации DHT в простате, он не обладает эффектом по снижению концентрации тестостерона в простате и взамен повышает концентрацию. Так как тестостерон обладает активностью по связыванию андрогенного рецептора, равной примерно половине таковой у DHT, данное локальное повышение концентраций тестостерона в простате, как считают, должно быть частично ответственно за недостаточную лекарственную эффективность финастерида для BPH.
Антиандрогенные терапии с использованием хирургической кастрации и агонистов гонадотропин-высвобождающего гормона также применяются против рака простаты. Сообщается, что антиандрогенные терапии влияют на недостаточный эффект снижения концентраций тестостерона в простате. Например, у пациентов с раком простаты, которые получают антиандрогенную терапию, концентрация тестостерона в крови снижалась до 10% концентрации перед введением, в то время как концентрация DHT в простате оставалась равной примерно 50% (“The Journal of Clinical Endocrinology and Metabolism”, 1995, Vol. 80, p. 1066-1071). Это говорит о том, что концентрация тестостерона в простате также недостаточно снижена. Кроме того, андрогенные рецепторы локализовались в ядрах клеток также при раке простаты, рецидивирующем после антиандрогенной терапии (гормонально-резистентный рак простаты), и не наблюдалось значительной разницы между концентрацией тестостерона в тканях реккурентного рака простаты и концентрацией в нормальной простате (“Clinical Cancer Research”, 2004, Vol. 10, p. 440-448). Данные публикации наводят на мысль, что эффект снижения концентраций тестостерона в простате в существующих терапевтических методах является совершенно недостаточным для лечения реккурентного рака простаты и что подавление механизма синтеза тестостерона в простате, то есть интракринного синтеза тестостерона в простате, может представлять собой новую мишень для терапии рака простаты.
C учетом вышеописанных известных данных, поскольку ингибиторы интракринного синтеза тестостерона в простате обладают эффектом по снижению концентраций тестостерона в простате и не обладают эффектом по снижению концентраций тестостерона в крови, ожидают, что данные ингибиторы будут очень привлекательным средством для лечения ВРН и/или средством для лечения рака простаты, (1) которое может снижать не только концентрацию тестостерона, но также концентрацию DHT в простате и (2) которое может быть лишено вредных эффектов из-за подавления концентрации тестостерона, получаемого из яичек, в крови.
17β-гидроксистероид-дегидрогеназа (17βHSD) является важной для биосинтеза тестостерона. Существует несколько подтипов 17βHSD. 17βHSD типа 5 широко представлен в простате человека и, как было опубликовано, повышает проявление рака простаты и реккурентного рака простаты (“Steroids”, 2004, Vol. 69, p. 795-801; и “Cancer Research”, 2006, Vol. 66, p. 2815-2825). С другой стороны, почти весь тестостерон в крови производится с помощью 17βHSD типа 3 в яичках и экспрессия 17βHSD типа 3 редко наблюдается в других тканях, включая простату (“Nature Genetics”, 1994, Vol. 7, p. 34-39). Таким образом полагают, что 17βHSD типа 5 является ответственным за интракринный синтез тестостерона в простате и селективные ингибиторы 17βHSD типа 5 предполагаются для селективного подавления интракринного синтеза тестостерона в простате. Кроме того, так как вклад 17βHSD типа 5 отмечен также в эстрогензависимых тканях, таких как молочная железа и тому подобное, селективные ингибиторы, как ожидают, будут эффективны для эстрогензависимых заболеваний, таких как рак молочной железы и тому подобное (“Endocrine Reviews”, 2003, Vol. 24, p. 152-182). Кроме того, опубликовано, что AKR1C3 (другое название для 17βHSD типа 5), которая представляет собой подтип альдокеторедуктазы (AKR), метаболизирует полициклический ароматический углеводород (РАН) с образованием реакционноспособных кислородных соединений (ROS) (“The Journal of Biological Chemistry”, 2002, Vol. 277, No. 27, p. 24799-24808), и что единичный нуклеотидный полиморфизм (SNP) AKR1C3 гена, связанного с окислительным стрессом, коррелирует с риском рака легкого (“Carcinogenesis”, 2004, Vol. 25, No. 11, p. 2177-2181). То есть предполагается, что активность AKR1C3 в легких повышает риск рака легкого посредством генерирования ROS от PAH и ожидается, что селективные ингибиторы 17βHSD типа 5 будут эффективны для лечения рака легкого.
В качестве ингибиторов 17βHSD типа 5 известны стероидные производные (патентный документ 1) и NSAID (нестероидные противовоспалительные лекарственные средства), такие как флуфенаминовая кислота, индометацин и тому подобное (непатентный документ 1), производные коричной кислоты (непатентный документ 2) и тому подобное. Хотя механизм действия различный, производное индазола, представляющее собой соединение формулы (А), как известно, эффективно для ВРН (патентный документ 2).
[Хим. 1]
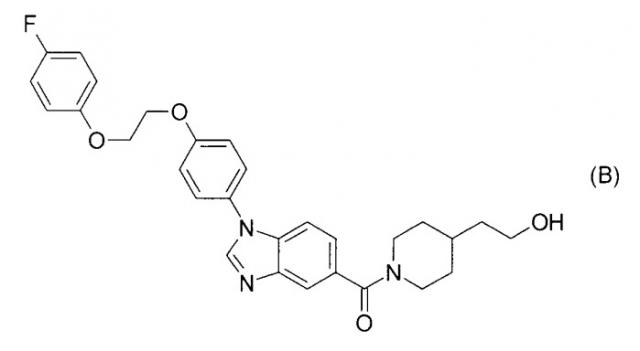
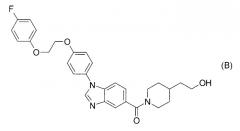
Согласно патентному документу 3 N-замещенные бензимидазоловые производные, включающие соединение формулы (В), обладают ингибирующим действием в отношении c-Kit онкогена и применимы для лечения рака простаты или тому подобного. Однако нет описания индолильной группы и также нет описания ингибирующего действия в отношении 17βHSD типа 5.
[Хим. 2]
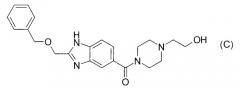
Согласно патентному документу 4 производные бензимидазола, включающие соединение формулы (С), обладают регулирующим действием на тирозинкиназу и применимы для лечения рака простаты или тому подобного. Однако не описана индолильная группа и также нет описания ингибирующего действия в отношении 17βHSD типа 5.
[Хим. 3]
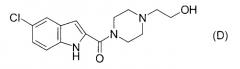
Согласно патентному документу 5 производные индола, включающие соединение формулы (D), обладают гистамин Н4 антагонистическим действием и применимы для лечения воспаления. Однако не описана неосновная (пиперидильная)алканольная структура и также нет описания ингибирующего действия в отношении 17βHSD типа 5 и эффективности в отношении BPH, рака простаты и тому подобного.
[Хим. 4]
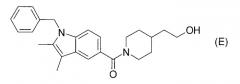
Согласно патентному документу 6 производные индола, включающие соединение формулы (Е), обладают регулирующим действием в отношении каннабиноидного рецептора и применимы для лечения цереброваскулярных нарушений и тому подобного. Однако также нет описания ингибирующего действия в отношении 17βHSD
типа 5 и эффективности в отношении BPH, рака простаты и тому подобного.
[Хим. 5]
[Патентный документ 1] Проспект международной публикации № WO99/046279
[Патентный документ 2] Проспект международной публикации № WO2004/064735
[Патентный документ 3] Проспект международной публикации № WO2005/021531
[Патентный документ 4] Проспект международной публикации № WO2007/056155
[Патентный документ 5] Проспект международной публикации № WO2002/072548
[Патентный документ 6] JP-A-2005-162657
[Непатентный документ 1] Cancer Research, 2004, Vol. 64, p. 1802-1810
[Непатентный документ 2] Molecular and Cellular Endocrinology, 2006, Vol. 248, p. 233-235
РАСКРЫТИЕ ИЗОБРЕТЕНИЯ
ПРОБЛЕМА, КОТОРУЮ ИЗОБРЕТЕНИЕ ПРЕДЛАГАЕТ ДЛЯ РЕШЕНИЯ
Задача данного изобретения состоит в том, чтобы предложить соединение, применимое в качестве лекарственного средства, обладающего селективной ингибирующей активностью в отношении 17βHSD типа 5, в частности в качестве средства для лечения доброкачественной гиперплазии простаты и/или рака простаты.
СПОСОБЫ ДЛЯ РЕШЕНИЯ ПРОБЛЕМЫ
В результате интенсивных изучений соединений, обладающих селективной ингибирующей активностью в отношении 17βHSD типа 5, авторы настоящего изобретения установили, что {1-[(индол-2-ил)карбонил]пиперидил}алканол-производное обладает потенциальной селективной ингибирующей активностью в отношении 17βHSD типа 5 и может быть средством для лечения и/или средством для предупреждения заболевания, связанного с 17βHSD типа 5, такого как доброкачественная гиперплазия простаты и рак простаты без сопутствующих вредных эффектов из-за снижения уровня тестостерона. Указанные результаты исследований были положены в основу настоящего изобретения.
То есть данное изобретение относится к соединению формулы (I) или его соли и к фармацевтической композиции, содержащей соединение формулы (I) или его соль и наполнитель.
[Хим. 6]
в формуле (I), R1, R2 и R3, которые являются одинаковыми или различными, представляют собой Н или низший алкил;
R4, R5, R6, R7 и R8, которые являются одинаковыми или различными, представляют собой Н, низший алкил, галоген, галоген-низший алкил, нитро, -Х-циклоалкил, который может быть замещенным, -Х-арил, который может быть замещенным, -Х-гетероциклическую группу, которая может быть замещенной, -Х-COOR0, -X-CONR10R11, -X-CN, -X-OR0, -X-SR0, -X-S(O)-низший алкил, -X-S(O)2-низший алкил, -Х-NR10R11, -X-NR0C(O)R10, -X-NR0C(O)OR10, -X-NR0C(O)NR10R11, -X-NR0S(O)2R10, -X-O-галоген-низший алкил, -Х-О-Х-циклоалкил, который может быть замещенным, -Х-О-Х-арил, который может быть замещенным, -Х-О-Х-гетероциклическую группу, которая может быть замещенной, или -Х-О-низший алкилен-OR0; или
R6 и R7 объединены с образованием -О-низший алкилен-О-;
R0, который является одинаковым или различным, представляет собой Н или низший алкил;
R10 и R11, которые являются одинаковыми или различными, представляют собой Н, низший алкил, галоген-низший алкил, -Х-циклоалкил, -Х-арил, или -Х-гетероциклическую группу; или
R10 и R11 вместе с N, к которому они присоединены, образуют насыщенную гетероциклическую группу, которая может быть замещенной; и
Х, который является одинаковым или различным, представляет собой связь или низший алкилен.
В данном описании символы, указанные выше, использованы для того, чтобы, если не оговорено особо, изображать одинаковые значения.
Кроме того, данное изобретение относится к фармацевтической композиции для лечения и/или предупреждения заболевания, связанного с 17βHSD типа 5, причем композиция содержит соединение формулы (I) или его соль, а именно средство для предупреждения и/или средство для лечения заболевания, связанного с 17βHSD типа 5, содержащее соединение формулы (I) или его соль.
Кроме того, данное изобретение относится к применению соединения формулы (I) или его соли для изготовления фармацевтической композиции для лечения и/или предупреждения заболевания, связанного с 17βHSD типа 5.
Кроме того, данное изобретение относится к способу лечения и/или предупреждения заболевания, связанного с 17βHSD типа 5, причем способ включает введение пациенту эффективного количества соединения формулы (I) или его соли.
Кроме того, данное изобретение относится к ингибитору 17βHSD типа 5, содержащему соединение формулы (I) или его соль.
Кроме того, данное изобретение относится к способу приготовления фармацевтической композиции для предупреждения или лечения заболевания, связанного с 17βHSD типа 5, причем способ включает смешивание соединения формулы (I) или его соли и фармацевтически приемлемого носителя, растворителя или эксципиента.
Кроме того, данное изобретение относится к упаковке для продажи, включающей фармацевтическую композицию, содержащую соединение формулы (I) или его соль; и инструкцию, в соответствии с которой соединение формулы (I) или его соль могут быть использованы или должны использоваться для лечения и/или предупреждения заболевания, связанного с 17βHSD типа 5.
ЭФФЕКТ ИЗОБРЕТЕНИЯ
Соединение формулы (I) селективно ингибирует 17βHSD типа 5. В соответствии с этим соединение формулы (I) может быть использовано как средство для предупреждения и/или лечения заболевания, связанного с 17βHSD типа 5. Например, оно может быть использовано как средство для предупреждения и/или лечения заболевания, связанного с андрогеном, так как синтез андрогена подавлен ингибированием 17βHSD типа 5.
НАИЛУЧШИЙ СПОСОБ ОСУЩЕСТВЛЕНИЯ ИЗОБРЕТЕНИЯ
Ниже в настоящем документе данное изобретение будет описано более подробно.
В определениях данного описания “алкил” и “алкилен” обозначают линейную или разветвленную углеводородную цепь, если, в частности, не оговорено особо.
“Низший алкил” обозначает алкил, содержащий 1-6 атомов углерода (ниже в настоящем описании обозначенный как “С1-6”), и его примеры включают метильную, этильную, н-пропильную, изопропильную, н-бутильную, изобутильную, втор-бутильную, трет-бутильную, н-пентильную, н-гексильную группу и тому подобное. В другом варианте осуществления он представляет собой С1-4алкил. В еще другом варианте осуществления он представляет собой метил, этил, н-пропил, изопропил или трет-бутил.
“Низший алкилен” обозначает С1-6алкилен, и его примеры включают метиленовую, этиленовую, триметиленовую, тетраметиленовую, пентаметиленовую, гексаметиленовую, пропиленовую, метилметиленовую, этилэтиленовую, 1,2-диметилэтиленовую, 1,1,2,2-тетраметилэтиленовую группу, и тому подобное. В другом варианте осуществления он представляет собой С1-5алкилен. В еще другом варианте осуществления он представляет собой метилен, этилен, триметилен, тетраметилен или пентаметилен.
“Галоген” обозначает F, Cl, Br или I.
“Галоген-низший алкил” обозначает низший алкил, замещенный одним или несколькими галогенами. В другом варианте осуществления он представляет собой низший алкил, замещенный 1-5 атомами галогена. В еще другом варианте осуществления он представляет собой трифторметил.
“Циклоалкил” представляет собой С3-10 насыщенную углеводородную циклическую группу, в которой может быть мостик. Примеры его включают циклопропильную, циклобутильную, циклопентильную, циклогексильную, циклогептильную, циклооктильную, бицикло[2.2.1]гептильную, адамантильную группу и тому подобное. В другом варианте осуществления он представляет собой С3-8циклоалкил. В еще другом варианте осуществления он представляет собой циклопропил, циклобутил, циклопентил или циклогексил.
“Арил” представляет собой С6-14 от моноциклической до трициклической ароматическую углеводородную циклическую группу, которая содержит циклическую группу, конденсированную с С5-8 циклоалкеном на его участке с двойной связью. Его примеры включают фенильную, нафтильную, тетрагидронафталенильную, инденильную, флуоренильную группу и тому подобное. В другом варианте осуществления он представляет собой фенил или нафтил. В еще другом варианте осуществления он представляет собой фенил.
“Гетероциклическая” группа обозначает циклическую группу, выбираемую из i) 3-8-членной моноциклической, и в другом варианте осуществления из 5-7-членного моноциклического гетероцикла, содержащего 1-4 гетероатома, выбираемого из О, S и N, и из ii) от бициклического до трициклического гетероцикла, содержащего 1-5 гетероатомов, выбираемых из О, S и N, который образован циклической конденсацией моноциклического гетероцикла с одним или двумя циклами, выбираемыми из группы, состоящей из моноциклического гетероцикла, бензольного кольца, С5-8циклоалкана и С5-8циклоалкена. Кольцевой атом, S или N, может быть окислен для образования оксида или диоксида. Кроме того, он может быть соединен мостиком или может образовать спироцикл.
Примеры “гетероциклической” группы включают азиридинил, азетидил, пирролидинил, пиперидил, азепанил, пиперазинил, гомопиперазинил, оксиранил, оксетанил, тетрагидрофуранил, тетрагидропиранил, тетрагидротиопиранил, морфолинил, гомоморфолинил, тиоморфолинил, пирролил, индолил, имидазолил, пиразолил, пиридил, пиримидинил, пиразинил, триазолил, тетразолил, фурил, тиенил, оксазолил, изоксазолил, оксадиазолил, тиазолил, тиадиазолил, бензимидазолил, хинолил, хиназолил, хиноксалинил, бензофуранил, бензотиофенил, бензоксазолил, бензтиазолил, карбазолил, индолинил, тетрагидрохинолинил, тетрагидроизохинолинил, хинуклидинил, дибензофуранилгруппу, и тому подобное.
В другом варианте осуществления она представляет собой моноциклическую или бициклическую 5-10-членную гетероциклическую группу.
В еще другом варианте осуществления она представляет собой пирролидинил, пиперидил, азепанил, пиперазинил, гомопиперазинил, оксиранил, оксетанил, тетрагидрофуранил, тетрагидропиранил, тетрагидротиопиранил, морфолинил, гомоморфолинил, тиоморфолинил, индолил, имидазолил, пиридил, пиримидинил, пиразинил, триазолил, тетразолил, фурил, тиенил, оксазолил, изооксазолил, тиадиазолил, бензимидазолил, тетрагидрохинолинил, тетрагидроизохинолинил или дибензофуранил.
“Насыщенная гетероциклическая” группа обозначает, среди вышеприведенной “гетероциклической” группы, группу, в которой все циклобразующие связи представляют собой одинарные связи.
Примеры “насыщенной гетероциклической” группы включают пирролидинил, пиперидил, азепанил, пиперазинил, гомопиперазинил, оксиранил, оксетанил, тетрагидрофуранил, тетрагидропиранил, тетрагидротиопиранил, морфолинил, гомоморфолинил, тиоморфолинилгруппу и тому подобное.
Выражение “который может быть замещенным” в данном описании обозначает незамещенный или замещенный 1-5 заместителями. Кроме того, если имеются многочисленные заместители, то заместители могут быть одинаковыми или различными.
Заместители для “циклоалкила, который может быть замещенным”, “арила, который может быть замещенным”, или “гетероциклической группы, которая может быть замещенной”, в R4, R5, R6, R7 и R8 включают, например, низший алкил, галоген, галоген-низший алкил, нитро, -X-CN, -X-OR0, -X-SR0, -X-S(O)-низший алкил, -X-S(O)2-низший алкил, -Х-NR10R11, -X-NR0C(O)R10, -X-NR0C(O)OR10, -X-NR0C(O)NR10R11, -X-NR0S(O)2R10, -X-O-галоген-низший алкил или -Х-О-низший алкилен-OR0. В другом варианте осуществления их примеры включают группы, выбираемые из низшего алкила, галогена, галоген-низшего алкила, -CN, и OR0. В еще другом варианте осуществления их примеры включают группы, выбираемые из метила, этила, F, Cl, трифторметила и метокси.
Хотя “циклоалкил”, “фенил”, “циклогексил” и тому подобное описаны как моновалентные группы в данном описании для удобства, они могут представлять собой поливалентные группы, дивалентные или более высокой валентности согласно их структурам. Данное изобретение охватывает эти структуры. Определенные варианты осуществления дивалентных групп соответствуют группам, имеющим суффиксы вышеприведенных кольцевых групп, превращенных в диил в соответствии с номенклатурой органической химии. Например, дивалентная группа, соответствующая фенильной группе, которая является моновалентной группой, представляет собой фенилен.
“Селективный ингибитор 17βHSD типа 5” обозначает ингибитор, в котором ингибирующая активность в отношении 17βHSD типа 3 проявляется 3-кратной или более, предпочтительно 10-кратной или более и более предпочтительно 100-кратной или более величиной относительно ингибирующей активности в отношении человеческого 17βHSD типа 5 (AKK1C3) исходя из величины IC50.
Вариант осуществления соединения формулы (I) данного изобретения будет описан ниже.
(1) Соединение формулы (Ia)
[Хим.7]
(2) Соединение, в котором R1 означает Н.
(3) Соединение, в котором R1 означает низший алкил.
(4) Соединение, в котором R1 означает метил.
(5) Соединение, в котором R2 означает Н.
(6) Соединение, в котором R2 означает низший алкил.
(7) Соединение, в котором R2 означает метил.
(8) Соединение, в котором R3 означает Н.
(9) Соединение, в котором R3 означает низший алкил.
(10) Соединение, в котором R4 означает Н, низший алкил, галоген или -О-низший алкил.
(11) Соединение, в котором R4 означает Н.
(12) Соединение, в котором R4 означает низший алкил.
(13) Соединение, в котором R4 означает галоген.
(14) Соединение, в котором R4 означает -О-низший алкил.
(15) Соединение, в котором R5 означает Н, низший алкил, галоген или -О-низший алкил.
(16) Соединение, в котором R5 означает Н.
(17) Соединение, в котором R5 означает низший алкил.
(18) Соединение, в котором R5 означает галоген.
(19) Соединение, в котором R5 означает -О-низший алкил.
(20) Соединение, в котором R6 означает Н, низший алкил, галоген, галоген-низший алкил, нитро, циклоалкил, ОН или -О-низший алкил.
(21) Соединение, в котором R6 означает низший алкил, галоген или -О-низший алкил.
(22) Соединение, в котором R6 означает Н.
(23) Соединение, в котором R6 означает низший алкил.
(24) Соединение, в котором R6 означает галоген.
(25) Соединение, в котором R6 означает галоген-низший алкил.
(26) Соединение, в котором R6 означает нитро.
(27) Соединение, в котором R6 означает циклоалкил.
(28) Соединение, в котором R6 означает ОН.
(29) Соединение, в котором R6 означает -О-низший алкил.
(30) Соединение, в котором R7 означает Н, низший алкил, галоген или -О-низший алкил.
(31) Соединение, в котором R7 означает Н.
(32) Соединение, в котором R7 означает низший алкил.
(33) Соединение, в котором R7 означает галоген.
(34) Соединение, в котором R7 означает -О-низший алкил.
(35) Соединение, в котором R8 означает Н, низший алкил, галоген или -О-низший алкил.
(36) Соединение, в котором R8 означает Н.
(37) Соединение, в котором R8 означает низший алкил.
(38) Соединение, в котором R8 означает галоген.
(39) Соединение, в котором R8 означает -О-низший алкил.
(40) Соединение, которое представляет собой комбинацию любых двух или более групп, описанных в вышеприведенных пунктах (1)-(39).
Конкретные примеры соединения вышеприведенного пункта (40) включают следующие соединения.
(41) Соединение, описанное в (1), в котором R1 и R3 означают Н.
(42) Соединение, описанное в (41), где R4, R5, R7 и R8, которые являются одинаковыми или различными, означают Н, низший алкил, галоген или -О-низший алкил, R6 означает Н, низший алкил, галоген, галоген-низший алкил, нитро, циклоалкил, ОН или -О-низший алкил.
(43) Соединение, описанное в (1), в котором R1 и R2 означают низший алкил, и R3 означает Н.
(44) Соединение, описанное в (43), где R4, R5, R7 и R8, которые являются одинаковыми или различными, означают Н, низший алкил, галоген или -О-низший алкил.
(45) Соединение, описанное в (43) или (44), где R6 означает Н, низший алкил, галоген, галоген-низший алкил, нитро, циклоалкил, ОН или -О-низший алкил.
(46) Соединение, описанное в (43)-(45), где R6 означает низший алкил, галоген или -О-низший алкил.
Другой вариант осуществления соединения формулы (I) данного изобретения будет описан ниже.
(47) Соединение, описанное в (1), где R1, R2, R3 и R4, которые являются одинаковыми или различными, означают Н или низший алкил, R5 означает Н, низший алкил, галоген или -О-низший алкил, R6 означает Н, низший алкил, галоген, ОН, -О-низший алкил, -О-низший алкиленфенил, -О-галоген-низший алкил, нитро, амино, -амино-С(О)-низший алкил или пирролил, R7 означает Н, галоген, ОН, или -О-низший алкил, или R6 и R7 объединены, чтобы образовать -О-низший алкилен-О-, и R8 означает Н или галоген.
(48) Соединение, описанное в (47), в котором R1 означает низший алкил.
(49) Соединение, описанное в (48), в котором R1 означает метил.
(50) Соединение, описанное в (47), в котором R2 означает низший алкил.
(51) Соединение, описанное в (50), в котором R2 означает метил.
(52) Соединение, описанное в (47), в котором R3 означает Н.
(53) Соединение, описанное в (47), в котором R4 означает Н.
(54) Соединение, описанное в (47), в котором R5 означает Н, Cl или метил.
(55) Соединение, описанное в (47), в котором R6 означает Н, Cl, метил, метокси или нитро.
(56) Соединение, описанное в (47), в котором R7 означает Н.
(57) Соединение, описанное в (47), в котором R8 означает Н или Cl.
(58) Соединение, которое представляет собой комбинацию из двух или более групп, описанных в вышеприведенных (48)-(57).
Конкретные соединения, охваченные данным изобретением, включают следующие соединения.
2-{1-[(5-метил-1Н-индол-2-ил)карбонил]пиперидин-4-ил}этанол,
1-[1-(1Н-индол-2-илкарбонил)пиперидин-4-ил]пропан-2-ол,
1-[1-(1Н-индол-2-илкарбонил)пиперидин-4-ил]-2-метилпропан-2-ол,
2-метил-1-{1-[(4-метил-1Н-индол-2-ил)карбонил]пиперидин-4-ил}пропан-2-ол,
2-метил-1-{1-[(5-метил-1Н-индол-2-ил)карбонил]пиперидин-4-ил}пропан-2-ол,
1-{1-[(3,5-диметил-1Н-индол-2-ил)карбонил]пиперидин-4-ил}-2-метилпропан-2-ол,
1-{1-[(5-трет-бутил-1Н-индол-2-ил)карбонил]пиперидин-4-ил}-2-метилпропан-2-ол,
1-{1-[(4-фтор-1Н-индол-2-ил)карбонил]пиперидин-4-ил}-2-метилпропан-2-ол,
1-{1-[(5-фтор-1Н-индол-2-ил)карбонил]пиперидин-4-ил}-2-метилпропан-2-ол,
1-{1-[(4-хлор-1Н-индол-2-ил)карбонил]пиперидин-4-ил}-2-метилпропан-2-ол,
1-{1-[(5-хлор-1Н-индол-2-ил)карбонил]пиперидин-4-ил}-2-метилпропан-2-ол,
1-{1-[(5-бром-1Н-индол-2-ил)карбонил]пиперидин-4-ил}-2-метилпропан-2-ол,
1-{1-[(7-хлор-5-фтор-1Н-индол-2-ил)карбонил]пиперидин-4-ил}-2-метилпропан-2-ол,
2-{[4-(2-гидрокси-2-метилпропил)пиперидин-1-ил]карбонил}-1Н-индол-5-ол,
1-{1-[(4-метокси-1Н-индол-2-ил)карбонил]пиперидин-4-ил}-2-метилпропан-2-ол,
1-{1-[(5-метокси-1Н-индол-2-ил)карбонил]пиперидин-4-ил}-2-метилпропан-2-ол,
1-{1-[(6-метокси-1Н-индол-2-ил)карбонил]пиперидин-4-ил}-2-метилпропан-2-ол,
2-метил-1-(1-{[(5-(трифторметокси)-1Н-индол-2-ил]карбонил}пиперидин-4-ил)пропан-2-ол, и
2-метил-1-{1-[(5-нитро-1Н-индол-2-ил)карбонил]пиперидин-4-ил}пропан-2-ол.
Соединение формулы (I) в некоторых случаях может существовать в форме таутомеров или геометрических изомеров в зависимости от вида заместителей. В настоящем описании соединение формулы (I) может быть представлено только в одной форме изомеров, но данное изобретение включает другие изомеры, а также выделенные формы или их смеси.
Кроме того, соединение формулы (I) может иметь асимметрические атомы углерода или аксиальные асимметрии в некоторых случаях и, соответственно, оно может существовать в форме оптических изомеров. Данное изобретение также включает изоляты или смеси оптических изомеров соединения формулы (I).
Кроме того, данное изобретение включает фармацевтически приемлемое пролекарство соединения формулы (I). Фармацевтически приемлемое пролекарство представляет собой соединение, содержащее группу, которую можно превратить в аминогруппу, гидроксильную группу, карбоксильную группу или тому подобное сольволизом или при физиологическом состоянии. Примеры группы, которая образует пролекарство, включает группы, описанные, например, в Prog. Med., 5, 2157-2161 (1985)
или “Pharmaceutical Research and Development” (Hirokawa Publishing Company, 1990), Vol. 7, “Drug Design”, pp. 163-198.
Кроме того, соль соединения формулы (I) представляет собой фармацевтически приемлемую соль соединения формулы (I) и может образовать кислотно-аддитивную соль или соль с основанием в зависимости от типа заместителей. В частности, их примеры включают кислотно-аддитивные соли с неорганическими кислотами, такими как хлористоводородная кислота, бромистоводородная кислота, йодистоводородная кислота, серная кислота, азотная кислота и фосфорная кислота, или с органическими кислотами, такими как муравьиная кислота, уксусная кислота, пропионовая кислота, щавелевая кислота, малоновая кислота, янтарная кислота, фумаровая кислота, малеиновая кислота, молочная кислота, яблочная кислота, миндальная кислота, винная кислота, дибензоилвинная кислота, дитолуоилвинная кислота, лимонная кислота, метансульфоновая кислота, этансульфоновая кислота, бензолсульфоновая кислота, пара-толуолсульфоновая кислота, аспарагиновая кислота и глутаминовая кислота, соли с неорганическими основаниями, такие как соли натрия, калия, магния, кальция и алюминия, или с органическими основаниями, такими как соли с метиламином, этиламином, этаноламином, лизином и орнитином, соли с различными аминокислотами и производными аминокислот, такими как соли ацетиллейцина, аммония, и тому подобные.
Кроме того, данное изобретение также включает различные гидраты или сольваты и полиморфные кристаллические вещества соединения формулы (I) и их соли. Кроме того, данное изобретение также включает соединения, меченные различными радиоактивными или нерадиоактивными изотопами.
СПОСОБЫ ПОЛУЧЕНИЯ
Соединение формулы (I) и его соль могут быть получены за счет использования свойств, основанных на типах его основного скелета или заместителей, и применением различных известных синтетических методов. В настоящее время в некоторых случаях исходя из методик получения эффективным является замена функциональной группы соответствующей защитной группой (группой, которая легко может быть превращена в функциональную группу) на стадии исходного продукта до промежуточного в зависимости от типа функциональной группы в процессе получения. Примеры таких функциональных групп включают аминогруппу, гидроксильную группу, карбоксильную группу и тому подобное, и примеры таких защитных групп включают защитные группы, описанные, например, в “Protective Groups in Organic Synthesis (the third edition, 1999)” edited by Greene and Wuts и тому подобном, которые могут быть соответствующим образом выбраны и использованы в зависимости от условий реакции. В данных методах требуемое соединение может быть получено введением защитной группы и выполнением реакции и затем удалением защитной группы, если желательно.
Кроме того, пролекарство соединения формулы (I) может быть получено тем же способом, как и в случае защитных групп, выполнением реакции после введения определенной группы на стадии от исходных продуктов до промежуточных продуктов или применением полученного соединения формулы (I). Реакция может быть осуществлена применением методов, известных специалистам в данной области, таких как этерификация, амидирование, дегидратация и тому подобное.
Далее в настоящем описании будут представлены наглядные способы получения соединения формулы (I). Каждый из способов получения может быть также выполнен с отнесением к ссылкам, прилагаемым к настоящему описанию. Кроме того, способы получения данного изобретения не ограничены примерами, показанными ниже.
[Хим. 8]
Соединение формулы (I) может быть получено взаимодействием соединения (II) c соединением (III).
Реакцию можно проводить, используя соединение (II) и соединение (III) в эквивалентных количествах или также их в избыточном количестве в присутствии конденсирующего агента в условиях от охлаждения до нагревания, предпочтительно от -20°С до 60°С, обычно с перемешиванием в течение от 0,1 часа до 5 суток, в растворителе, который является инертным для реакции.
В данном случае выбор растворителя не особенно ограничен, но его примеры включают ароматические углеводороды, такие как бензол, толуол и ксилол; галогенированные углеводороды, такие как дихлорметан, 1,2-дихлорэтан и хлороформ; простые эфиры, такие как диэтиловый эфир, тетрагидрофуран, диоксан и диметоксиэтан; N,N-диметилформамид, диметилсульфоксид, этилацетат, ацетонитрил, вода или их смесь.
Примеры конденсирующего агента включают 1-этил-3-(3-диметиламинопропил)карбодиимид или его гидрохлорид, дициклогексилкарбодиимид, 1,1'-карбонилдиимидазол, дифенилфосфорилазид, оксихлорид фосфора и тому подобное, но не ограничены только ими. В некоторых случаях для реакции может быть полезно, например, использовать добавку (например, 1-гидроксибензотриазол или тому подобное). В некоторых случаях может быть полезно для равномерного протекания реакции проводитьреакцию в присутствии органического основания, такого как триэтиламин, N,N-диизопропилэтиламин или N-метилморфолин, или неорганического основания, такого как карбонат калия, карбонат натрия или гидроксид калия.
Кроме того, может быть также использован метод, в котором соединение карбоновой кислоты (II) превращают в его реакционноспособное производное и затем подвергают взаимодействию с соединением (III). Примеры реакционноспособного производного карбоновой кислоты включают галогенангидрид, полученный взаимодействием с галогенирующим агентом, таким как оксихлорид фосфора или тионилхлорид, смешанный ангидрид кислоты, полученный взаимодействием с изобутилхлорформиатом, или тому подобное, и активный сложный эфир, полученный конденсацией с 1-гидроксибензотриазолом, или тому подобное. Реакция между данными реакционно