Сульфонамидные производные как ингибиторы химазы
Иллюстрации
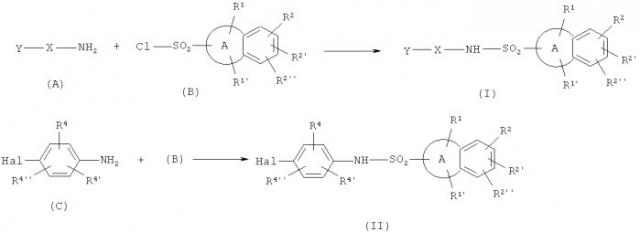
Показать всеИзобретение относится к новым сульфонамидным производным формулы (I), где X представляет собой фенилен, необязательно замещенный одним, двумя или тремя заместителями, независимо выбранными из группы, состоящей из галогена, C1-6-алкила, C1-6-алкокси, галоген-C1-6-алкила, галоген-C1-6-алкокси, C1-6-алкилсульфонила, C1-6-алкилсульфинила, C1-6-алкилтиогруппы, C1-6-алкилсульфонил-C1-6-алкила, C1-6 -алкилсульфинил-C1-6-алкила, C1-6-алкилтио-C1-6-алкила и C1-6-алкоксикарбонила; Y представляет собой пиридил, пиримидинил или пиперидил, которые необязательно могут быть замещены одним или двумя заместителями, независимо выбранными из группы, содержащей галоген, C1-6-алкокси и C1-6-алкоксикарбонил; и его фармацевтически приемлемым солям. Сульфонамидные производные формулы (I) представляют собой ингибиторы химазы и применяются для получения фармацевтической композиции. Технический результат - сульфонамидные производные формулы (I) в качестве ингибитора химазы. 2 н. и 6 з.п. ф-лы, 36 пр.
где фрагмент представляет собой
Реферат
Изобретение касается новых сульфонамидных производных формулы (I),
где
А представляет собой фенильное кольцо, либо гетероарильное кольцо, которое представляет собой моноциклическое ароматическое кольцо из 5 или 6 атомов, содержащее один или два гетероатома, выбранных из N, О и S, а остальные атомы кольца представляют собой С, или гетероциклическое кольцо, которое представляет собой неароматическое моноциклическое кольцо из 5 или 6 атомов, содержащее один или два гетероатома, выбранных из N и S(O)n (где n представляет собой целое число от 0 до 2), а остальные атомы кольца представляют собой С, причем один из углеродных атомов гетероциклического кольца необязательно может быть заменен карбонильной группой;
R1 и R1' независимо представляют собой водород, галогенную, нитро, циано, амино, C1-6 алкильную, гетероалкильную, С3-7 циклоалкильную, С2-6 алкенильную, С2-6 алкинильную, гидроксильную, C1-6 алкоксильную группы, -NR'R'', -(С0-6 алкилен)-NR'R'' группы, где R' и R'' независимо выбраны из группы, состоящей из водорода, C1-6 алкильной, гетероалкильной, формильной, С1-6 алкилкарбонильной, необязательно замещенной С3-7 циклоалкилкарбонильной, необязательно замещенной арилкарбонильной, необязательно замещенной гетероарилкарбонильной, необязательно замещенной гетероциклокарбонильной, C1-6 алкилсульфонильной, необязательно замещенной С3-7 циклоалкилсульфонильной, необязательно замещенной арилсульфонильной, необязательно замещенной гетероарилсульфонильной и необязательно замещенной гетероциклосульфонильной групп, или -(С0-6 алкилен)-OR', где R' представляет собой водород, C1-6 алкильную, гетероалкильную, формильную или C1-6 алкилкарбонильную группы, или R1' не присутствует, а присутствует только R1;
R2, R2' и R2'' независимо представляют собой водород, галоген, циано, нитро, амино-, моно- и ди-С1-6 алкил замещенные амино, C1-6 алкильные, С2-6 алкенильные, С2-6 алкинильные, гетероалкильные, гидрокси или C1-6 алкокси группы;
Х представляет собой фенилен, необязательно замещенный одним, двумя или тремя заместителями, независимо выбранными из группы, состоящей из галогена, циано, нитро, амино-, моно- и ди-С1-6 алкил замещенных амино, C1-6 алкильной, С2-6 алкенильной, С2-6 алкинильной, гетероалкильной, гидрокси, C1-6 алкокси, галоген-С1-6 алкильной, галоген C1-6 алкокси, гетероалкилокси, C1-6 алкилсульфонильной, C1-6 алкилсульфинильной, C1-6 алкилтио, C1-6 алкилсульфонил-С1-6 алкильной, C1-6 алкилсульфинил-С1-6 алкильной, C1-6 алкилтио-С1-6 алкильной, ацильной, формильной, C1-6 алкоксикарбонильной, гало С1-6 алкоксикарбонильной, гетероалкилоксикарбонильной и гетероалкилкарбонильной групп;
Y представляет собой необязательно замещенный гетероарил, где гетероарил представляет собой моноциклический ароматический радикал, содержащий 6 атомов в кольце, содержащий в кольце один или два гетероатома, выбранных из N(O)n (где n равно 0 или 1), О и S, а остальные атомы кольца представляют собой С, или
необязательно замещенный гетероциклил, где гетероциклил представляет собой неароматический моноциклический радикал, содержащий шесть атомов в кольце, содержащий в кольце один или два гетероатома, выбранных из N, О, или S(O)n (где n представляет собой целое число от 0 до 2), а остальные атомы кольца представляют собой С;
а также пролекарств и их фармацевтически приемлемых солей.
Кроме того, изобретение касается способа и интермедиатов для получения указанных выше соединений, фармацевтических препаратов, которые содержат такие соединения, применения этих соединений для производства фармацевтических препаратов, а также способа получения интермедиатов.
Соединения формулы (I) ингибируют химазу. Химаза представляет собой сериновую протеиназу с паттерном экспрессии, строго ограниченным субпопуляцией тучных клеток (МСТ тучные клетки). Химаза активируется только при активации и дегрануляции тучных клеток, что ограничивает активность фермента только МСТ положительными тканями. Химаза специфически расщепляет ряд патологически значимых субстратов (Raymond, W.W., S.W.Ruggles и др.; JBC 2003 278(36): 34517-34524), посредством чего данный фермент может активировать ангиотензин II, эндотелин, ТФР-b, ИЛ1, SCF (фактор стволовых клеток), коллагеназу и вызывать деградацию таких белков как тромбин, FN (фибронектин), АРО А1,2 (аполипротеин). Этот паттерн делает химазу привлекательной мишенью при аллергических, воспалительных и фиброзных заболеваниях. Действительно, ряд успешных исследований на животных с ингибиторами химазы продемонстрировали эффективность на животных с аллергией, при травмах сосудов и атеросклерозе (Doggrell SA, Wanstall JC Can J Physiol Pharmacol. Февраль 2005; 83(2): 123-30; Lindstedt KA, Kovanen PT. Curr Opin Lipidol. Октябрь 2004; 15(5):567-73; Reed CE, Kita H.J Allergy Clin Immunol. Ноябрь 2004; 114(5):997-1008; Takai S, et al,. Eur J Pharmacol, октябрь 2004 6; 501(1-3): 1-8; Takai S, et al, Trends Pharmacol Sci. октябрь 2004; 25(10):518-22; Takai S, Miyazaki M. Curr Vasc Pharmacol. Июнь 2003; l(2):217-24).
Таким образом, ингибирование химазы представляет собой полезный механизм при аллергии, астме, окклюзивных заболеваниях периферических артерий, критической ишемии конечностей (CLI), лечении пациентов с уязвимыми атеросклеротическими бляшками, нестабильной стенокардии, застойной сердечной недостаточности, гипертрофии левого желудочка, ишемической реперфузионной травме, кардиомиопатии, рестенозе, ревматоидном артрите, диабетической нефропатии, синдроме раздраженной толстой кишки, болезни Крона, заживлении ран (ожогов/язв у больных сахарным диабетом/CLI).
Настоящее изобретение предусматривает новые соединения формулы (I) в качестве ингибиторов химазы.
Если не указано иное, следующие определения приведены для иллюстрации и определения смысла и широты значения различных терминов, используемых для описания изобретения в настоящем документе.
Термин "галоген" или "гало" представляет собой фтор, хлор, бром и йод, причем предпочтительно фтор, хлор.
Термин "C1-6 алкил", отдельно или в комбинации с другими группами, представляет собой неразветвленный или разветвленный моновалентный алкильный радикал, включающий от одного до шести атомов углерода. Этот термин также можно проиллюстрировать такими радикалами, как метил, этил, н-пропил, изопропил, н-бутил, втор-бутил, трет-бутил. C1-4 алкил является более предпочтительным.
Термин "галоген C1-6 алкил", отдельно или в комбинации с другими группами, представляет собой C1-6 алкил, в котором один или несколько атомов водорода заменены одинаковыми или различными галогенами, такой как -СН2Сl, -CH2CF3, трифторметил. В качестве галогенов, хлор, бром или фтор являются предпочтительными, и хлор или фтор являются более предпочтительными.
Термин "галоген C1-6 алкокси", отдельно или в комбинации с другими группами, представляет собой C1-6 алкокси группу, в которой один или несколько атомов водорода заменены одинаковыми или различными галогенами. В качестве галогенов предпочтительными являются хлор, бром или фтор, и хлор или фтор являются более предпочтительными.
Термин "ацил", отдельно или в комбинации с другими группами, представляет собой -CO-C1-6 алкил.
Термин "гетероалкил" представляет собой C1-6 алкил, замещенный одним или несколькими заместителями, независимо выбранными из группы, состоящей из нитро, гидрокси, галогенной, циано, C1-6 алкоксильной, формильной, C1-6 алкилкарбонильной, карбоксильной, C1-6 алкилтио, C1-6 алкилсульфинильной, C1-6 алкилсульфонильной, амино-, и моно-, и ди-С1-6 алкил замещенных амино групп. Этот термин можно также проиллюстрировать такими радикалами, как 2-гидроксиэтил, перфторметил.
Термин "С3-7 циклоалкил", отдельно или в комбинации с другими группами, представляет собой насыщенный моновалентный циклический углеводородный радикал, содержащий от трех до семи атомов углерода в кольце, например циклопропил, циклобутил, циклогексил.
Термин "C1-6 алкокси", отдельно или в комбинации с другими группами, представляет собой группу R'-O-, где R' представляет собой C1-6 алкил.
Термин "С2-6 алкенил", отдельно или в комбинации с другими группами, представляет собой неразветвленный или разветвленный углеводородный остаток, содержащий двойную связь, включающий от двух до шести атомов углерода, такой как, например, этенил, 2-пропенил.
Термин "С2-6-алкинил", отдельно или в комбинации с другими группами, представляет собой неразветвленный или разветвленный углеводородный остаток, содержащий тройную связь, включающий от двух до шести атомов углерода, такой как, например, этинил, 2-пропинил.
Термин "С0-6 алкилен" представляет собой связь, или неразветвленную, или разветвленную двухвалентную насыщенную алифатическую углеводородную группу, включающую от 1 до 6 атомов углерода. С0 алкилен представляет собой связь.
Термин "арил", отдельно или в комбинации с другими группами, представляет собой фенильную или нафтильную группы, предпочтительно фенильную группу.
Термин "гетероциклил", отдельно или в комбинации с другими группами, представляет собой неароматический моно- или бициклический радикал, включающий от трех до восьми атомов в кольце, где один или два атома кольца представляют собой гетероатомы, выбранные из N, О, или S(O)n (где n представляет собой целое число от 0 до 2), а остальные атомы кольца представляют собой С.
Термин "гетероарил" представляет собой моноциклический, либо бициклический радикал, включающий от 5 до 12 атомов в кольце, содержащий, по крайней мере, одно ароматическое кольцо, содержащий один, два или три гетероатома в кольце, выбранных из N, О и S, а остальные атомы кольца представляют собой С. Предпочтительно, гетероарильный радикал присоединен к соединению по ароматическому кольцу.
Термины "необязательно замещенных арил", "необязательно замещенный гетероарил", "необязательно замещенный гетероциклил" и "необязательно замещенный С3-7 циклоалкил" представляют собой, соответственно, арил, гетероарил, гетероциклил и С3-7 циклоалкил, необязательно замещенные одним или несколькими заместителями, независимо выбранными из группы, состоящей из галогена, нитро, циано, амино, C1-6 алкильной, С2-6 алкенильной, С2-6 алкинильной, гидрокси, C1-6 алкокси, гетероалкилокси, моно- и ди-С1-6 алкил замещенных амино, ацильной, формильной, гетероалкилкарбонильной, C1-6 алкоксикарбонильной, гетероалкилоксикарбонильной и гетероалкильной групп.
Предпочтительные радикалы для химических групп, определенных выше, приведены в примерах.
Соединения формулы (I) могут образовывать фармацевтически приемлемые соли присоединения (с кислотой). Примерами таких фармацевтически приемлемых солей являются соли соединений формулы (I) с физиологически совместимыми минеральными кислотами, такими как соляная кислота, серная кислота, сернистая кислота и фосфорная кислота, или с органическими кислотами, такими как метансульфоновая кислота, п-толуолсульфоновая кислота, уксусная кислота, молочная кислота, трифторуксусная кислота, лимонная кислота, фумаровая кислота, малеиновая кислота, винная кислота, янтарная кислота или салициловая кислота. Термин "фармацевтически приемлемая соль" относится к таким солям. Соединения формулы (I), в которых присутствует СООН группа, могут также образовывать соли с основаниями. Примерами таких солей являются соли щелочных, щелочноземельных металлов и соли аммония, такие как, например, Na-, K-, Са- и триметиламмонийная соли. Термин "фармацевтически приемлемая соль" также относится к таким солям. Соли присоединения кислоты, как описано выше, являются предпочтительными.
Термины "необязательный" или "необязательно" означают, что последующее описанное явление или обстоятельство может, однако, не обязательно, иметь место, и что описание включает случаи, когда явление или обстоятельство имеет место, и случаи, когда этого не происходит. Например, термин "арильная группа, необязательно замещенная алкильной группой" означает, что алкильная группа может, однако, не обязательно, присутствовать, и данное описание включает в себя ситуацию, когда арильная группа замещена алкильной группой, и ситуацию, когда арильная группа не замещена алкильной группой.
"Фармацевтически приемлемое вспомогательное вещество" представляет собой вспомогательное вещество, которое полезно при изготовлении фармацевтической композиции, которое полностью безопасно, нетоксично и не является нежелательным ни с биологической, ни с какой-либо другой точки зрения, и включает вспомогательные вещества, которые являются приемлемыми для ветеринарного применения, а также для фармацевтического применения для людей. Термин "фармацевтически приемлемое вспомогательное вещество", используемый в описании и формуле изобретения, включает как одно, так и несколько таких вспомогательных веществ.
Соединения, которые имеют одинаковую молекулярную формулу, но различаются по природе или последовательности связей их атомов, или расположению атомов в пространстве называются "изомеры". Изомеры, которые отличаются расположением атомов в пространстве, называются "стереоизомеры". Стереоизомеры, которые не являются зеркальными изображениями друг друга, называются "диастереомеры", и стереоизомеры, которые представляют собой несуперпозиционные зеркальные изображения друг друга, называются "энантиомеры". Если соединение имеет асимметрический центр, например, если атом углерода связан с четырьмя различными группами, возможно образование пары энантиомеров. Энантиомеры могут характеризоваться абсолютной конфигурацией их асимметрического центра, описываться с помощью R- и S- номенклатуры Кана, Ингольда и Прелога или характеризоваться тем, каким образом молекулы вращают плоскость поляризованного света, и обозначаться как правовращающие или левовращающие (т.е. как (+)- или (-)-изомеры соответственно). Хиральные соединения могут существовать в виде отдельных энантиомеров или в виде смесей. Смесь, содержащая энантиомеры в равных пропорциях, называется "рацемической смесью".
Соединения формулы (I) могут обладать одним или несколькими асимметрическими центрами. Если не указано иное, описание или название конкретного соединения в описании и формуле изобретения включают как оба индивидуальных энантиомера, так и их смеси, как рацемические, так и нет, а также отдельные эпимеры и их смеси. Методы для определения стереохимии и разделения стереоизомеров хорошо известны в уровне техники.
Хотя определения A, R1-R2'', Х и Y в широком смысле даны ранее, некоторые радикалы являются предпочтительными.
I) В соединении формулы (I), А предпочтительно представляет собой фенильное кольцо или гетероарильное кольцо. Гетероарильное кольцо А также предпочтительно представляет собой пятичленное кольцо.
II) В соединении формулы (I),
предпочтительно представляет собой,
, или
более предпочтительно
представляет собой
, или
в которых R1 и R1' независимо представляют собой водород или C1-6 алкил,
еще более предпочтительно
представляет собой
, или
в которых R2, R2' и R2'' независимо представляют собой водород или галоген.
особенно предпочтительно представляет собой
III) В соединении формулы (I), Y предпочтительно находится в пара-положении в фениленовой группе в качестве X, по отношению к -NH-SO2-группе.
IV) В соединении формулы (I), X предпочтительно представляет собой фенилен, необязательно замещенный одним, двумя или тремя заместителями, независимо выбранными из группы, состоящей из галогена, C1-6 алкильной, C1-6 алкокси, гало С1-6 алкильной, гало C1-6 алкокси, C1-6 алкилсульфонильной, C1-6 алкилсульфинильной, C1-6 алкилтио, C1-6 алкилсульфонил-С1-6 алкильной, C1-6 алкилсульфинил-С1-6 алкильной, C1-6 алкилтио- C1-6 алкильной и C1-6 алкоксикарбонильной групп; более предпочтительно Х представляет собой фенилен, замененный гало С1-6, алкильной или C1-6 алкилсульфонильной группами в орто-положении по отношению к -NH-SO2- группе, еще более предпочтительно Х представляет собой фенилен, замещенный трифторметильной или метилсульфонильной группами в орто-положении относительно -NH-SO2-группы.
V) В соединении формулы (I), Y предпочтительно представляет собой необязательно замещенный гетероарил, где гетероарил представляет собой моноциклический ароматический радикал, содержащий 6 атомов в кольце, содержащий один или два атома азота в кольце, а остальные атомы кольца представляют собой С, или необязательно замещенный гетероциклил, где гетероциклил представляет собой неароматический циклический монорадикал, содержащий 6 атомов в кольце, содержащий один или два атома азота в кольце, а остальные атомы кольца представляют собой С.
Более предпочтительно, Y представляет собой пиридил, пиримидинил или пиперидил, необязательно замещенные одним или двумя заместителями, независимо выбранными из группы, состоящей из галогена, C1-6 алкоксильной и C1-6 алкоксикарбонильной групп.
VI) Предпочтительно, соединение изобретения представляет собой соединение формулы (I), которое представляет собой (4-пиридин-4-ил-2-трифторметил-фенил)-амид 5-фтор-3-метил-бензо[b]тиофен-2-сульфокислоты.
Соединения настоящего изобретения могут быть получены, например, с помощью общих методов синтеза, описанных ниже.
Общие методы синтеза
Схема 1
В схеме 1 A, R1-R2'', X, Y и Hal определены ранее. R4, R4' и R4'' независимо представляют собой водород, галоген, циано, нитро, амино-, моно- и ди- C1-6 алкил замещенные амино группы, C1-6 алкильную, С2-6 алкенильную, С2-6 алкинильную, гетероалкильную, гидрокси, C1-6 алкокси, гало C1-6 алкильную, гало С1-6 алкокси, гетероалкилокси, C1-6 алкилсульфонильную, C1-6 алкилсульфинильную, C1-6 алкилтио, C1-6 алкилсульфонил-С1-6 алкильную, C1-6-алкилсульфинил C1-6 алкильную, C1-6 алкилтио C1-6 алкильную, ацильную, формильную, C1-6 алкоксикарбонильную, гало C1-6 алкоксикарбонильную, гетероалкилоксикарбонильную или гетероалкилкарбонильную группы.
Соединения формул (I) и (II) преимущественно получали по реакции сульфонилхлорида (В) с амином (А) или с анилином (С) в присутствии основания. Основание предпочтительно представляет собой гидрид натрия или амин, выбранный из группы, состоящей из пиридина, пиколина, триэтиламина, диэтиламина, диизопропилэтиламина 4-N-диметиламинопиридина. Наиболее предпочтительными аминами являются пиридин и N,N-диметиламинопиридин (DMAP). Предпочтительными являются апротонные растворители, предпочтительно, выбранные из ацетонитрила, диоксана, метиленхлорида, тетрагидрофурана, толуола, диметоксиэтана, N,N-диметилацетамида, диметилсульфоксида, диметилформамида, и их комбинации. Предпочтительно, чтобы температура была в диапазоне от 0°С до 100°С.
С использованием соединения (II) в качестве интермедиата, соединения формулы (I) могут быть получены с помощью реакций образования С-С связи, таких как реакция Сузуки, в которой галогенид реагирует с соответствующим образом замещенным производным бороновой кислоты в присутствии основания и палладиевого катализатора.
Сульфонилхлориды (В) либо коммерчески доступны, либо могут быть синтезированы с использованием современных методов из нафталина, или бициклических гетероароматических соединений, или их производных. В частности, сульфонилхлоридная группа может быть введена с использованием реакции арил литиевой соли с диоксидом серы и последующего окисления/хлорирования с применением, например, сульфурилхлорида или N-хлорсукцинимида. Альтернативно, активированное положение ароматического кольца может прореагировать с хлорсульфоновой кислотой или с комплексом триоксида серы, таким как SO3·ДМФА или SO3·пиридин, с последующим хлорированием, например, с помощью тионилхлорида.
Анилины (А) либо представляют собой коммерчески доступные соединения, либо могут быть синтезированы с применением современных методов. Один из вариантов заключается в том, чтобы вводить галоидированные соединения (С) в реакции образования С-С связи, такие как реакция Сузуки, в которой галогенид реагирует с соответствующим образом замещенным производным бороновой кислоты в присутствии основания и палладиевого катализатора. Галоидированные производные анилина (С) либо коммерчески доступны, либо могут быть синтезированы с применением современных методов.
Как описано выше, соединения формулы (I) являются активными соединениями и ингибируют химазу. Следовательно, данные соединения препятствуют активации ангиотензина II, эндотелина, TGFb, IL1, SCF, коллагеназы и вызывают деградацию таких белков, как тромбин, FN, АРО А1,2. Поэтому они могут быть использованы для лечения и/или профилактики аллергических, воспалительных и/или фиброзных заболеваний, таких как аллергия, астма, окклюзивное заболевание периферических артерий, критическая ишемия конечностей (CLI), пациенты с уязвимыми атеросклеротическими бляшками, нестабильная стенокардия, застойная сердечная недостаточность, гипертрофия левого желудочка, ишемическая реперфузионная травма, удар, кардиомиопатия, рестеноз, ревматоидный артрит, диабетическая нефропатия, синдром раздраженной толстой кишки, болезнь Крона, атеротромбоз и/или ожоги/язвы у больных сахарным диабетом/CLI.
Предупреждение и/или лечение аллергических, воспалительных или фиброзных заболеваний, особенно атеротромбоза или астмы, представляют собой предпочтительное применение.
Изобретение также относится к фармацевтической композиции, включающей описанное выше соединение, а также фармацевтически приемлемое вспомогательное вещество.
Изобретение также охватывает соединения, как описано выше, для применения в качестве терапевтически активных веществ, особенно в качестве терапевтически активных веществ для лечения и/или профилактики аллергических, воспалительных и/или фиброзных заболеваний, таких как аллергия, астма, окклюзивное заболевание периферических артерий, критическая ишемия конечностей (CLI), пациенты с уязвимыми атеросклеротическими бляшками, нестабильная стенокардия, застойная сердечная недостаточность, гипертрофия левого желудочка, ишемическая реперфузионная травма, удар, кардиомиопатия, рестеноз, ревматоидный артрит, диабетическая нефропатия, синдром раздраженной толстой кишки, болезнь Крона, атеротромбоз и/или ожоги/язвы у больных сахарным диабетом/CLI.
Изобретение также относится к применению описанных выше соединений для получения лекарственных средств, предназначенных для терапевтического и/или профилактического лечения аллергических, воспалительных и/или фиброзных заболеваний, прежде всего для терапевтического и/или профилактического лечения аллергии, астмы, окклюзивного заболевания периферических артерий, критической ишемии конечностей (CLI), пациентов с уязвимыми атеросклеротическими бляшками, нестабильной стенокардией, застойной сердечной недостаточности, гипертрофии левого желудочка, ишемической реперфузионной травмы, удара, кардиомиопатии, рестеноза, ревматоидного артрита, диабетической нефропатии, синдрома раздраженной толстой кишки, болезни Крона, атеротромбоза и/или ожогов/язв у больных сахарным диабетом/CLI. Такие лекарственные средства включают соединения, как описано выше.
Изобретение также относится к способу получения и интермедиатам для получения соединений формулы (I), а также способу получения интермедиатов.
Ингибирование химазы соединениями настоящего изобретения может быть продемонстрировано с использованием пептидного субстрата, как описано в настоящем документе ниже.
Для химазы был выбран субстрат, содержащий пептид из 4 аминокислот AAPF, как стандартный субстрат для химотрипсиноподобного соединения (сукцинил-Аlа-Аlа-Рrо-Рhе-[7-амино-4-метилкумарин]; см. Lockhart BE, и др., "Recombinant human mast-cell chymase: an improved procedure for expression in Pichia pastoris and purification of the highly active enzyme." Biotechnol Appl Biochem., опубликованную в качестве немедленной публикации 26 мая 2004 года в виде рукописи ВА 20040074). Пептид был синтезирован с чистотой 95% (Bachem, Bubendorf, Switzerland). Химазу очищали из тучных клеток кожи человека, полученных из Calbiochem (Merck Biosciences, San Diego, California, USA). В тесте использовали 0,15 M NaCl, 0,05, трис-HCl, 0,05% CHAPS (3 -[(3-[холамидопропил)-диметиламмоний]-1-пропансульфонат) буфер, 0,1 мг/мл раствор гепарина (Гепарин натрий, Sigma, из слизистой оболочки кишечника свиней), 0,02 мМ раствор AAPF-субстрата, 1 нМ раствор химазы при рН 7,4. Анализ проводили в 96-ячеечных планшетах (Optiplate Packard), в объеме 0,05 мл при комнатной температуре. Активность химазы определяли по первоначальному темпу роста флуоресценции при 340/440 нм (возбуждение/излучение) свободного 7-амино-4-метилкумарина, отщепленного от субстрата. Ингибирование активности фермента ингибирующими соединениями измеряли после 30 минут преинкубации с химазой при комнатной температуре в буфере без AAPF-субстрата. Затем тест начинали добавлением указанной концентрации AAPF-субстрата.
Значения IC50 (полуингибирующая концентрация) активных соединений настоящего изобретения, предпочтительно составляют примерно от 1000 до 1 нМ, особенно предпочтительно, от 30 до 1 нМ.
| Пример | IC50 (нМ) |
| Пример 2 | 35 |
| Пример 16 | 106 |
| Пример 21 | 3 |
Соединения формулы (I) и/или их фармацевтически приемлемые соли могут быть использованы в качестве лекарственных средств, например, в виде фармацевтических препаратов для энтерального, парентерального или местного введения. Они могут использоваться, например, перорально, например в виде таблеток, покрытых таблеток, драже, твердых и мягких желатиновых капсул, растворов, эмульсий или суспензий, ректально, например в форме суппозиториев, парентерально, например в виде растворов для инъекций, или суспензий, или инфузионных растворов, либо местно, например в форме мазей, кремов и масел. Оральное введение является предпочтительным.
Производство фармацевтических препаратов может быть осуществлено, как известно специалистам в данной области техники, путем введения описанных соединений формулы (I) и/или их фармацевтически приемлемых солей, необязательно в сочетании с другими терапевтически ценными веществами, в галеновую форму вместе с подходящими, нетоксичными, инертными, терапевтически совместимыми твердыми или жидкими материалами-носителями и, при необходимости, с обычными фармацевтическими адъювантами.
Подходящие материалы-носители представляют собой не только неорганические материалы-носители, но также и органические материалы-носители. Так, например, в качестве материалов-носителей для таблеток, покрытых таблеток, драже и твердых желатиновых капсул могут быть использованы лактоза, кукурузный крахмал или их производные, тальк, стеариновая кислота и ее соли. Подходящие материалы-носители для мягких желатиновых капсул представляют собой, например, растительные масла, воски, жиры и полутвердые и жидкие полиолы (в случае мягких желатиновых капсул как формы введения, в зависимости от природы активного ингредиента, носители могут, однако, не потребоваться). Подходящие материалы-носители для производства сиропов и растворов представляют собой, например, воду, полиолы, сахарозу, инвертный сахар. Подходящие материалы-носители для инъекционных растворов представляют собой, например, воду, спирты, полиолы, глицерин и растительные масла. Подходящие материалы-носители для суппозиториев представляют собой, например, природные или отвердевшие масла (гидрированные), воски, жиры и полужидкие или жидкие полиолы. Подходящие материалы-носители для получения лекарственных форм для местного введения представляют собой глицериды, полусинтетические и синтетические глицериды, гидрогенизированные масла, жидкие воски, жидкие парафины, жидкие жирные спирты, стерины, полиэтиленгликоли и производные целлюлозы.
В качестве фармацевтических адъювантов можно использовать обычные стабилизаторы, консерванты, увлажняющие и эмульгирующие агенты, улучшающие консистенцию агенты, ароматизаторы, соли для изменения осмотического давления, буферные вещества, солюбилизаторы, красители, маскирующие агенты и антиоксиданты.
Дозировка соединений формулы (I) может варьироваться в широких пределах в зависимости от заболеваний, которые будут подвергаться лечению, возраста, индивидуального состояния пациента, режима введения, и, разумеется, должна быть определена индивидуально в каждом конкретном случае. Для взрослых пациентов ежедневная доза составляет от 1 до 1000 мг, особенно, приблизительно от 1 до 300 мг. В зависимости от тяжести заболевания и точного фармакокинетического профиля, соединение может быть введено в одной или нескольких дневных единичных дозированных формах, например в от 1 до 3 дневных единичных дозированных формах.
В лекарственных формах может содержаться около 1-500 мг, предпочтительно 1-100 мг, соединения формулы (I).
Примеры
Приведенные ниже примеры служат для более подробного иллюстрирования настоящего изобретения. Они, однако, никоим образом не ограничивают его.
Пример 1
(4-бром-2-трифторметил-фенил)-амид 5-фтор-3-метил-бензо[b]тиофен-2-сульфокислоты
К охлаждаемому льдом раствору 4-бром-2-(трифторметил)бензамина (CAS 445-02-3, 18 г) в пиридине (25 мл) добавили 5-фтор-3-метилбензо[b]тиофен-2-сульфонилхлорид (CAS:404964-34-7, 2,0 г). Реакционную смесь перемешивали при комнатной температуре в течение 72 часов, сконцентрировали в вакууме, и остаток хроматографировали на силикагеле с использованием смеси гептан/хлороформ в качестве элюента с получением (4-бром-2-трифторметил-фенил)-амида 5-фтор-3-метил-бензо[b]тиофен-2-сульфокислоты (2,35 г) в виде твердого бесцветного вещества. MS (ISN): 465,9, 468,0 (М-Н)-
Пример 2
(4-Пиридин-4-ил-2-трифторметил-фенил)-амид 5-фтор-3-метил-бензо[b]тиофен-2-сульфокислоты
Суспензию (4-бром-2-трифторметил-фенил)-амида 5-фтор-3-метил-бензо[b] тиофен-2-сульфокислоты (0,5 г) и 4-пиридинбороновой кислоты (0,197 г) в 1,2-диметоксиэтане (6 мл), этаноле (2 мл) и 2 М водном растворе карбоната натрия (4,0 мл) дегазировали 3-4 раза для удаления кислорода, а затем к суспензии добавили тетракис(трифенилфосфин)палладий (0,065 г). Реакционную смесь перемешивали при 80°С в течение 3 часов, быстро разбавили смесью лед/вода и экстрагировали этилацетатом. Органические слои промыли, высушили и сконцентрировали. Остаток хроматографировали на силикагеле, используя смесь гептан/этилацетат в качестве элюента, с получением указанного соединения (0,35 г) в виде твердого желтоватого вещества. MS (ISP): 467,3 (М+Н)+
Пример 3
[4-(2,6-дифтор-пиридин-4-ил)-2-трифторметил-фенил]-амид 5-фтор-3-метил-бензо[b]тиофен-2-сульфокислоты
Данное соединение было получено по аналогии с Примером 2 из (4-бром-2-трифторметил-фенил)-амида 5-фтор-3-метил-бензо[b]тиофен-2-сульфокислоты (0,12 г) и 2,6-дифторпиридин-4-бороновой кислоты (0,063 г) в 1,2-диметоксиэтане (1,5 мл), этиловом спирте (0,32 мл) и 2М водном растворе карбоната натрия (1,0 мл) с тетракис(трифенилфосфин)палладием (0,055 г). Указанное соединение было получено (0,055 г) в виде твердого коричневатого вещества. MS (ISP): 520,2 (M+NH4)+
Пример 4
[4-(3-фтор-пиридин-4-ил)-2-трифторметил-фенил]-амид 5-фтор-3-метил-бензо[b]тиофена-2-сульфокислоты
Данное соединение было получено по аналогии с Примером 2 из (4-бром-2-трифторметил-фенил)-амида 5-фтор-3-метил-бензо[b]тиофен-2-сульфокислоты (0,12 г) и гидрата 3-фторпиридин-4-бороновой кислоты (0,061 г) в 1,2-диметоксиэтане (1,5 мл), этиловом спирте (0,32 мл) и 2М водном растворе карбоната натрия (1,0 мл) с тетракис(трифенилфосфин)палладием (0,050 г). Указанное соединение было получено (0,025 г) в виде желтоватой пены. MS (ISP): 485,3 (М+H)+
Пример 5
[4-(2-фтор-пиридин-4-ил)-2-трифторметил-фенил]-амид 5-фтор-3-метил-бензо[b]тиофен-2-сульфокислоты
Данное соединение было получено по аналогии с Примером 2 из (4-бром-2-трифторметил-фенил)-амида 5-фтор-3-метил-бензо[b]тиофен-2-сульфокислоты (0,12 г) и 2-фторпиридин-4-бороновой кислоты (0,072 г) в 1,2-диметоксиэтане (1,5 мл), этиловом спирте (0,32 мл) и 2М водном растворе карбоната натрия (1,0 мл) с тетракис(трифенилфосфин)палладием (0,065 г). Указанное соединение было получено (0,085 г) в виде бесцветной пены. MS (ISN): 483,4 (М-Н)-
Пример 6
(4-пиридин-3-ил-2-трифторметил-фенил)-амид 5-фтор-3-метил-бензо[b]тиофен-2-сульфокислоты
Данное соединение было получено по аналогии с Примером 2 из (4-бром-2-трифторметил-фенил)-амида 5-фтор-3-метил-бензо[b]тиофен-2-сульфокислоты (0,10 г) и 3-пиридинбороновой кислоты (0,052 г) в 1,2-диметоксиэтане (1,5 мл), этиловом спирте (0,32 мл) и 2М водном растворе карбоната натрия (0,8 мл) с тетракис(трифенилфосфин)палладием (0,050 г). Указанное соединение было получено (0,086 г) в виде бесцветного твердого вещества. MS (ISP): 467,0 (М+Н)+
Пример 7
[4-(6-метокси-пиридин-3-ил)-2-трифторметил-фенил]-амид 5-фтор-3-метил-бензо[b]тиофен-2-сульфокислоты
Данное соединение было получено по аналогии с Примером 2 из (4-бром-2-трифторметил-фенил)-амида 5-фтор-3-метил-бензо[b]тиофен-2-сульфокислоты (0,10 г) и 2-метокси-5-пиридинбороновой кислоты (0,065 г) в 1,2-диметоксиэтане (1,5 мл), этиловом спирте (0,32 мл) и 2М водном растворе карбоната натрия (0,8 мл) с тетракис(трифенилфосфин)палладием (0,012 г). Указанное соединение было получено (0,081 г) в виде твердого бесцветного вещества. MS (ISP): 497,3 (М+Н)+
Пример 8
(4-пиримидин-5-ил-2-трифторметил-фенил)-амид 5-фтор-3-метил-бензо[b]тиофен-2-сульфокислоты
Данное соединение было получено по аналогии с Примером 2 из(4-бром-2-трифторметил-фенил)-амида 5-фтор-3-метил-бензо[b]тиофен-2-сульфокислоты (0,10 г) и пиримидин-5-бороновой кислоты (0,053 г) в 1,2-диметоксиэтане (1,5 мл), этиловом спирте (0,32 мл) и 2М водном растворе карбоната натрия (0,8 мл) с тетракис(трифенилфосфин)палладием (0,012 г). Указанное соединение было получено (0,045 г) в виде твердого бесцветного вещества. MS (ISN): 466,1 (М-Н)-
Пример 9
[4-(2-метокси-пиримидин-5-ил)-2-трифторметил-фенил]-амид 5-фтор-3-метил-бензо[b]тиофен-2-сульфокислоты
Данное соединение было получено по аналогии с Примером 2 из (4-бром-2-трифторметил-фенил)-амида 5-фтор-3-метил-бензо[b]тиофен-2-сульфокислоты (0,10 г) и 2-метокси-5-пиримидинбороновой кислоты (0,066 г) в 1,2-диметоксиэтане (1,5 мл), этиловом спирте (0,32 мл) и 2М водном растворе карбоната натрия (1,0 мл) с тетракис(трифенилфосфин)палладием (0,012 г). Указанное соединение было получено (0,064 г) в виде твердого бесцветного вещества. MS (ISP): 498,4 (М+Н)+
Пример 10
[4-(5-фтор-пиридин-3-ил)-2-трифторметил-фенил]-амид 5-фтор-3-метил-бензо[b]тиофен-2-сульфокислоты
Данное соединение было получено по аналогии с Примером 2 из (4-бром-2-трифторметил-фенил)-амида 5-фтор-3-метил-бензо[b]тиофе