Способы лечения псориаза
Иллюстрации
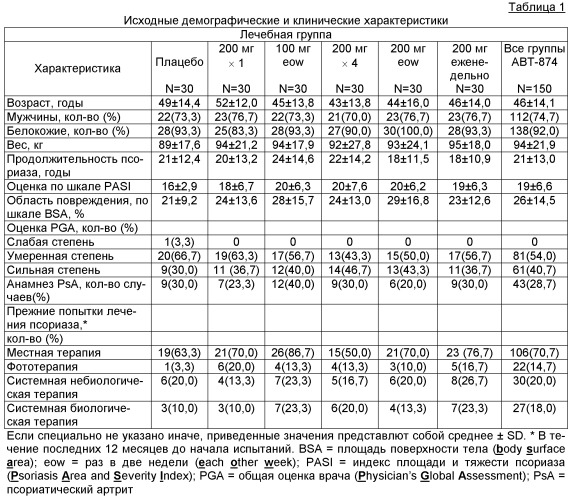
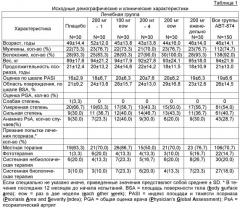
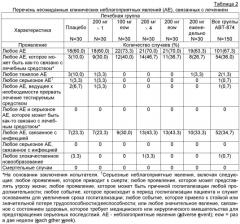
Показать всеГруппа изобретений относится к способу лечения пятнистого псориаза у субъекта путем введения субъекту антитела, способного связываться с р40-субъединицей IL-12 и/или IL-23. Указанное антитело или его антигенсвязывающая часть вводится субъекту от приблизительно 100 мг до приблизительно 200 мг, тем самым достигается лечение пятнистого псориаза. Группа изобретений позволяет осуществить эффективное лечение пятнистого псориаза. 13 н. и 54 з.п. ф-лы, 7 ил., 4 табл., 5 пр.
Реферат
РОДСТВЕННЫЕ ЗАЯВКИ
По настоящей заявке испрашивается приоритет по предварительной заявке США No. 60/880767, поданной 16 января 2007; предварительной заявке США No. 60/904022, поданной 27 февраля 2007; предварительной заявке США No. 60/925960, поданной 24 апреля 2007; предварительной заявке США No. 60/961764, поданной 24 июля 2007; и предварительной заявке США No. 60/997012, поданной 28 сентября 2007, полное содержание каждой из которых включено в настоящее описание в виде ссылки.
ОСНОВЫ СОЗДАНИЯ ИЗОБРЕТЕНИЯ
Псориаз представляет собой опосредованное T-клетками воспалительное заболевание, которое считается одним из наиболее распространенных аутоиммунных заболеваний, поражающих приблизительно от 2% до 3% взрослых, но при этом распространенность его в той или иной части мира сильно варьирует (Stern R.S., et al., J. Investig. Dermatol. Symp. Proc. 2004, 9: 136-39; Davidson A. and Diamond B.N. Engl. J. Med. 2001, 345: 340-50; Langley R.G.B., et al., Ann. Rheum. Dis. 2005, 64(Suppl. II): ii18-23). Псориаз существенно влияет на качество жизни (de Korte J, et al., J. Investig. Dermatol. Symp. Proc. 2004, 9: 140-7; Krueger G, et al., Arch. Dermatol. 2001, 137: 280-4; Finlay AY and Coles EC, Br. J. Dermatol. 1995, 132: 236-44) и ассоциирован с целым рядом психологических и психо-социальных проблем (Kimball AB, et al., Am. J.Clin. Dermatol. 2005, 6: 383-92; Russo PA, et al., Australas J. Dermatol. 2004, 45: 155-9). Многочисленные традиционные варианты терапии псориаза оказывают побочное токсическое воздействие; следовательно, их длительное применение имеет ограничения (Lebwohl M. and Ali S., J. Am. Acad. Dermatol. 2001, 45: 487-98; Lebwohl M. and Ali S., J. Am. Acad. Dermatol. 2001, 45: 649-61). Кроме того, многие пациенты с псориазом не удовлетворены традиционной терапией (Stern RS, et al, J. Investig. Dermatol. Symp. Proc. 2004, 9: 136-39; Finlay AY and Ortonne JP, J. Cutan. Med. Surg. 2004, 8: 310-20); таким образом, существует очевидная потребность в таких терапевтических подходах, которые являются более безопасными и более легкими для применения и которые могут быть прописаны на долговременной основе.
Интерлейкин-12 (IL-12) и родственный ему цитокин IL-23 являются членами суперсемейства цитокинов IL-12, которые имеют общую субъединицу p40 (Anderson EJR, et al., Springer Semin. Immunopathol. 2006, 27: 425-42). Оба цитокина вносят свой вклад в развитие иммунного ответа хелперных клеток типа 1T (Th1) при псориазе, но каждый из них играет особую роль (Rosmarin D and Strober BE, J. Drugs. Dermatol. 2005, 4: 318-25; Hong K, et al., J. Immunol. 1999, 162: 7480-91; Yawalkar N, et al., J. Invest. Dermatol. 1998, 111: 1053-57). IL-12, прежде всего, стимулирует дифференцировку Th1-клеток и последующую секрецию гамма-интерферона, тогда как IL-23 предпочтительно стимулирует дифференцировку наивных [или интактных] T-клеток в T-хелперные клетки-эффекторы (Th17), которые секретируют IL-17, провоспалительный медиатор. Rosmarin D and Strober BE, J. Drugs Dermatol. 2005, 4: 318-25; Harrington Le, et al., Nature Immunol 2005, 6: 1123-32; Park H, et al. Nature Immunol. 2005, 6: 1132-41). Сверхэкспрессия субъединицы p40 матричной РНК интерлейкина IL-12 и интерлейкина IL-23 при кожных поражениях при псориазе свидетельствует о том, что ингибирование IL-12 и IL-23 нейтрализующим антителом против белка субъединицы p40 IL-12/23 может оказаться эффективным терапевтическим подходом к лечению псориаза (Yawalkar N, et al., J. Invest. Dermatol. 1998, 111: 1053-57; Lee E, et al., J. Exp. Med. 2004, 199: 125-30; Shaker OG, et al., Clin. Biochem. 2006, 39:119-25; Piskin G, et al., J. Immunol. 2006, 176: 1908-15). Такие терапевтические подходы к лечению псориаза крайне необходимы в данной области.
КРАТКОЕ СОДЕРЖАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к способам и композициям для лечения псориаза, например хронического псориаза, с использованием антитела или его антиген-связывающей части, которое связывается с человеческим IL-12 и/или с человеческим IL-23.
В одном аспекте изобретение обеспечивает способ лечения псориаза у субъекта, включающий введение субъекту один раз в две недели, еженедельное введение или введение однократной дозы антитела или его антиген-связывающей части, направленного против человеческого IL-12 и/или человеческого IL-23.
В одном варианте осуществления ответ на введение один раз в две недели, еженедельное введение или введение однократной дозы антитела или его антиген-связывающей части поддерживается у субъекта в течение длительного периода времени, например, по меньшей мере приблизительно в течение 12 недель или по меньшей мере приблизительно 24 недели.
В другом варианте осуществления у субъекта поддерживается ответ на уровне по меньшей мере PASI-75 (Индекс площади и тяжести псориаза) в течение длительного периода времени после введения указанному субъекту один раз в две недели, еженедельного введения или введения однократной дозы антитела или его антиген-связывающей части, направленного против человеческого IL-12 и человеческого IL-23. В еще одном варианте осуществления по меньшей мере ответ PASI-90 поддерживается у субъекта в течение длительного периода времени после введения указанному субъекту один раз в две недели, еженедельного введения или введения однократной дозы антитела или его антиген-связывающей части, направленного против человеческого IL-12 и человеческого IL-23. В следующем варианте осуществления по меньшей мере ответ PASI-100 поддерживается у субъекта в течение длительного периода времени после введения указанному субъекту один раз в две недели, еженедельного введения или введения однократной дозы антитела или его антиген-связывающей части, направленного против человеческого IL-12 и человеческого IL-23. В одном варианте осуществления доза антитела, направленного против человеческого IL-12 и/или человеческого IL-23, составляет приблизительно 200 мг или приблизительно 100 мг.
В одном варианте осуществления псориаз представляет собой пятнистый псориаз, например хронический пятнистый псориаз. В другом варианте осуществления псориаз представляет собой хронический псориаз, например хронический пятнистый псориаз. Еще в одном варианте осуществления псориаз проявляется в формах от умеренной до тяжелой, например, от умеренной до тяжелой формы пятнистого псориаза, от умеренной до тяжелой формы хронического псориаза или от умеренной до тяжелой формы хронического пятнистого псориаза.
В одном варианте осуществления антитело или его антиген-связывающую часть вводят путем подкожного введения.
В другом аспекте изобретение относится к способу лечения псориаза у субъекта, включающему следующие стадии: (i) выбор субъекта, который страдает хроническим псориазом; и (ii) введение субъекту антитела или его антиген-связывающей части, которое способно связываться с эпитопом p40-субъединицы IL-12 и/или IL-23; тем самым достигается лечение псориаза у субъекта.
В одном варианте осуществления субъекту поставлен клинический диагноз псориаз по меньшей мере 6 месяцев назад. В другом варианте осуществления субъект имеет пятнистый псориаз на протяжении по меньшей мере 2 месяцев.
Еще в одном из аспектов изобретение обеспечивает способ лечения псориаза у субъекта, предусматривающий следующие стадии: (i) выбор субъекта, у которого ранее не было отмечено состояние, выбранное из группы, состоящей из проведения в прошлом системной или биологической анти-IL-12-терапии; наличия не-пятнистого псориаза; невозможности прервать местную терапию псориаза по меньшей мере за 2 недели до лечения; проведения ультрафиолетовой В-лучевой фототерапии по меньшей мере за 2 недели до лечения; проведения фототерапии псораленом-ультрафиолетовым облучением по меньшей мере за 4 недели до лечения; системной терапии по меньшей мере за 4 недели до лечения; биологической терапии по меньшей мере за 12 недель до лечения; необходимости потребления пероральных или инъецируемых кортикостероидов в процессе лечения; обострения астмы, требующего госпитализации в течение 10-летнего периода до скрининга; инфекции или факторов риска развития тяжелой инфекции; наличия в анамнезе злокачественных заболеваний, кроме успешно излеченной базально-клеточной карциномы, например плоскоклеточной карциномы или карциномы шейки матки in situ; и наличия в анамнезе проявления значительной иммунной реакции, например сывороточной болезни или анафилактоидной реакции, реакции на иммуноглобулин G-содержащее средство, например внутривенный гамма-глобулин, слитый белок или моноклональное антитело; и (ii) введение субъекту антитела или его антиген-связывающей части, которое способно связываться с эпитопом p40-субъединицы IL-12 и/или IL-23; тем самым достигается лечение псориаза у субъекта.
Еще в одном из аспектов изобретение обеспечивает способ лечения псориаза у субъекта, включающий следующие стадии: (i) выбор субъекта, которому в течение 1 месяца не производилась вакцинация средством, содержащим жизнеспособный вирус; и (ii) введение субъекту антитела или его антиген-связывающей части, которое способно связываться с эпитопом p40-субъединицы IL-12 и/или IL-23.
Еще в одном из дальнейших аспектов изобретение обеспечивает способ лечения псориаза у субъекта, включающий следующие стадии: (i) введение субъекту антитела или его антиген-связывающей части, которое способно связываться с эпитопом p40-субъединицы IL-12 и/или IL-23; (ii) мониторинг субъекта на предмет обнаружения клинически значимого аномального результата лабораторных анализов, выбранного из группы, состоящей из уровней аспартаттрансаминазы или аланинтрансаминазы, более чем в 5 раз превышающих верхнюю границу нормы; уровня общего сывороточного билирубина, более чем в 3 раза превышающего верхнюю границу нормы; уровня сывороточного креатинина, более чем в 3 раза превышающего верхнюю границу нормы; уровня креатинфосфокиназы, более чем в 5 раз превышающего верхнюю границу нормы; уровня гемоглобина, составляющего менее 8 г/дл; клеток белой крови, количество которых составляет менее 2×109/л; и тромбоцитов, насчитывающих менее 75×109/л; и (iii) прекращение введения антитела или его антиген-связывающей части субъекту, у которого обнаружен клинически значимый аномальный результат лабораторных анализов; тем самым достигается лечение псориаза у субъекта.
В одном из вариантов осуществления антитело или его антиген-связывающую часть вводят один раз в две недели. В другом варианте осуществления антитело или его антиген-связывающую часть вводят еженедельно или в однократной дозировке.
В другом варианте осуществления антитело или его антиген-связывающую часть вводят в дозе приблизительно 100 мг, 110 мг, 120 мг, 130 мг, 140 мг, 150 мг, 160 мг, 170 мг, 180 мг, 190 мг, 200 мг, 210 мг или 220 мг.
В одном из вариантов осуществлений антитело или его антиген-связывающая часть способно связываться с эпитопом p40-субъединицы, когда p40-субъединица связана с p35-субъединицей IL-12. В другом варианте осуществления антитело или его антиген-связывающая часть способно связываться с эпитопом p40-субъединицы, когда p40-субъединица связана с p19-субъединицей IL-23. В другом варианте осуществления антитело или его антиген-связывающая часть способно связываться с эпитопом p40-субъединицы, когда p40-субъединица связана с p35-субъединицей IL-12 и когда p40-субъединица связана с p19-субъединицей IL-23.
В одном из вариантов осуществлений псориаз представляет собой хронический псориаз, например хронический пятнистый псориаз, например, от умеренной до тяжелой форм хронического пятнистого псориаза.
В другом аспекте изобретение обеспечивает способ лечения псориаза у субъекта, включающий введение субъекту антитела или его антиген-связывающей части, которое способно связываться с эпитопом p40-субъединицы IL-12 и/или IL-23, при этом у субъекта поддерживается ответ на уровне по меньшей мере PASI-90 в течение длительного периода времени после первоначального введения антитела или его антиген-связывающей части, тем самым достигается лечение псориаза у субъекта.
В одном из вариантов осуществлений длительный период времении составляет по меньшей мере приблизительно 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23 или 24 недели.
В одном из вариантов осуществлений антитело или его антиген-связывающую часть вводят один раз в две недели. В другом варианте осуществления антитело или его антиген-связывающую часть вводят еженедельно. Еще в одном из вариантов осуществления антитело или его антиген-связывающую часть вводят в однократной дозировке.
В одном из вариантов осуществлений антитело или его антиген-связывающую часть вводят в дозе приблизительно 100 мг, 110 мг, 120 мг, 130 мг, 140 мг, 150 мг, 160 мг, 170 мг, 180 мг, 190 мг, 200 мг, 210 мг или 220 мг.
В одном из вариантов осуществлений псориаз представляет собой хронический псориаз, например хронический пятнистый псориаз, например, от умеренной до тяжелой форм хронического пятнистого псориаза.
В другом аспекте изобретение обеспечивает способ лечения псориаза у субъекта, включающий введение субъекту антитела или его антиген-связывающей части, которое способно связываться с эпитопом p40-субъединицы IL-12 и/или IL-23, при этом у субъекта поддерживается нулевой или минимальный уровень PGA (общей оценки пациента) в течение длительного периода времени после первоначального введения антитела или его антиген-связывающей части, тем самым достигается лечение псориаза у субъекта.
В одном из вариантов осуществления длительный период времени составляет по меньшей мере приблизительно 12, 13, 14, 15, 16, 17, 18, 19, 20, 21, 22, 23 или 24 недели.
В одном из вариантов осуществления антитело или его антиген-связывающую часть вводят один раз в две недели. В другом варианте осуществления антитело или его антиген-связывающую часть вводят еженедельно. Еще в одном из вариантов осуществления антитело вводят в однократной дозировке.
В одном из вариантов осуществления антитело или его антиген-связывающую часть вводят в дозе приблизительно 100 мг, 110 мг, 120 мг, 130 мг, 140 мг, 150 мг, 160 мг, 170 мг, 180 мг, 190 мг, 200 мг, 210 мг или 220 мг.
В одном из вариантов осуществления псориаз представляет собой хронический псориаз, например хронический пятнистый псориаз, например, от умеренной до тяжелой форм хронического пятнистого псориаза.
Еще в одном из вариантов осуществления изобретение обеспечивает способ лечения псориаза у субъекта, включающий введение субъекту антитела или его антиген-связывающей части, которое способно связываться с эпитопом p40-субъединицы IL-12 и/или IL-23, при этом у субъекта проявляется улучшенный индекс PASI приблизительно на 8 неделе после первоначального введения антитела или его антиген-связывающей части, тем самым достигается лечение псориаза у субъекта.
В одном из вариантов осуществления у субъекта проявляются улучшенные индексы PASI приблизительно через 7 недель, приблизительно через 6 недель, приблизительно через 5 недель, приблизительно через 4 недели, приблизительно через 3 недели, приблизительно через 2 недели, приблизительно через 1 неделю после первоначального введения антитела или его антиген-связывающей части.
В одном из вариантов осуществления антитело или его антиген-связывающую часть вводят один раз в две недели. В другом варианте осуществления антитело или его антиген-связывающую часть вводят еженедельно. Еще в одном из вариантов осуществления антитело вводят в однократной дозировке.
В одном из вариантов осуществления антитело или его антиген-связывающую часть вводят в дозе приблизительно 100 мг, 110 мг, 120 мг, 130 мг, 140 мг, 150 мг, 160 мг, 170 мг, 180 мг, 190 мг, 200 мг, 210 мг или 220 мг.
В одном из вариантов осуществления псориаз представляет собой хронический псориаз, например хронический пятнистый псориаз, например, от умеренной до тяжелой форм хронического пятнистого псориаза.
В другом варианте осуществления изобретение относится к способу лечения псориаза у субъекта, включающему введение субъекту антитела или его антиген-связывающей части, которое способно связываться с эпитопом p40-субъединицы IL-12 и/или IL-23, при этом у субъекта поддерживается по меньшей мере ответ PASI-50 в течение длительного периода времени после прекращения введения антитела или его антиген-связывающей части, тем самым достигается лечение псориаза у субъекта.
В близком к указанному выше аспекте изобретение обеспечивает способ лечения псориаза у субъекта, предусматривающий введение субъекту антитела или его антиген-связывающей части, которое способно связываться с эпитопом p40-субъединицы IL-12 и/или IL-23, при этом у субъекта поддерживается по меньшей мере ответ PASI-75 в течение длительного периода времени после прекращения введения антитела или его антиген-связывающей части, тем самым достигается лечение псориаза у субъекта.
Еще в одном близком аспекте изобретение обеспечивает способ лечения псориаза у субъекта, предусматривающий введение субъекту антитела или его антиген-связывающей части, которое способно связываться с эпитопом p40-субъединицы IL-12 и/или IL-23, при этом у субъекта поддерживается по меньшей мере ответ PASI-90 в течение длительного периода времени после прекращения введения антитела или его антиген-связывающей части, тем самым достигается лечение псориаза у субъекта.
В одном из вариантов осуществления длительный период времени после прекращения введения антитела составляет по меньшей мере приблизительно 12 недель.
В одном из вариантов осуществления антитело вводят в течение по меньшей мере приблизительно 12 недель.
В одном из вариантов осуществления антитело или его антиген-связывающую часть вводят один раз в две недели. В другом варианте осуществления антитело или его антиген-связывающую часть вводят еженедельно. Еще в одном варианте осуществления антитело или его антиген-связывающую часть вводят в однократной дозировке.
В одном из вариантов осуществления антитело или его антиген-связывающую часть вводят в дозе приблизительно 100 мг, 110 мг, 120 мг, 130 мг, 140 мг, 150 мг, 160 мг, 170 мг, 180 мг, 190 мг, 200 мг, 210 мг или 220 мг.
В одном из вариантов осуществления псориаз представляет собой хронический псориаз, например хронический пятнистый псориаз, например, от умеренной до тяжелой форм хронического пятнистого псориаза.
В одном варианте осуществления антитело или его антиген-связывающая часть, используемое в способах согласно изобретению, способно связываться с эпитопом p40-субъединицы IL-12.
В одном варианте осуществления антитело или его антиген-связывающая часть способно связываться с эпитопом p40-субъединицы, когда р40-субъединица связана с р35-субъединицей IL-12. В другом варианте осуществления аонтитело или его антиген-связывающая часть способно связываться с эпитопом р40-субъединицы, когда р40-субъединица связана с р19-субъединицей. В одном варианте осуществления антитело или его антигенсвязывающая часть способно связываться с эпитопом р40-субъединицы, когда р40-субъединица связана с р35-субъединицей IL-12 и когда р40-субъединица связана с р19-субъединицей.
В одном варианте осуществления антитело или его антиген-связывающая часть связывается с эпитопом p40-субъединицы IL-12, с которым связывается антитело, выбранное из группы, состоящей из Y61 и J695.
В другом варианте осуществления антитело дополнительно способно связываться с первым гетеродимером, а также способно связываться со вторым гетеродимером, где первый гетеродимер содержит p40-субъединицу IL-12 и p35-субъединицу IL-12 и где второй гетеродимер содержит p40-субъединицу IL-12 и p19-субъединицу.
В следующем варианте осуществления антитело нейтрализует активность первого гетеродимера. В другом варианте осуществления антитело нейтрализует активность второго гетеродимера. Еще в одном варианте осуществления антитело нейтрализует активность первого гетеродимера и второго гетеродимера.
В следующем варианте осуществления антитело или его антиген-связывающая часть, используемое в способах согласно изобретению, ингибируют фитогемагглютининовую бласт-пролиферацию в ФГА-анализе in vitro с IC50, составляющей 1×10-9 M или менее, или ингибируют продуцирование IFNγ с IC50, составляющей 1×10-10 M или менее.
В одном варианте осуществления антитело или его антиген-связывающая часть, используемое в способах согласно изобретению, диссоциирует из комплекса с p40-субъединицей IL-12 с Kd, составляющей 1×10-10 M или менее, или с константой скорости koff, составляющей 1×10-3 сек-1 или менее, как было определено методом резонансного возбуждения поверхностных плазмонов.
В одном из вариантов осуществления выделенное антитело или его антиген-связывающая часть, используемое в способах согласно изобретению, представляет собой химерное антитело, гуманизированное антитело или человеческое антитело.
В другом варианте осуществления антитело или его антиген-связывающая часть, используемое в способах согласно изобретению, имеет CDR3 тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO: 25, и CDR3 легкой цепи, содержащую аминокислотную последовательность SEQ ID NO: 26.
Еще в одном варианте осуществления антитело или его антиген-связывающая часть, используемое в способах согласно изобретению, имеет CDR2 тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO: 27, и CDR2 легкой цепи, содержащую аминокислотную последовательность SEQ ID NO: 28.
В одном варианте осуществления антитело или его антиген-связывающая часть, используемое в способах согласно изобретению, имеет CDR1 тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO: 29, и CDR1 легкой цепи, содержащую аминокислотную последовательность SEQ ID NO: 30.
В другом варианте осуществления антитело или его антиген-связывающая часть, используемое в способах согласно изобретению, способно связываться с интерлейкином, содержащим p40-субъединицу. В одном из вариантов осуществления интерлейкин содержит p40-субъединицу и p35-субъединицу, например, интерлейкин представляет собой IL-12. В другом варианте осуществления интерлейкин содержит p40-субъединицу и p19-субъединицу. Еще в одном варианте осуществления антитело или его антиген-связывающая часть нейтрализует активность интерлейкина.
В одном варианте осуществления антитело или его антиген-связывающая часть связывается с эпитопом p40-субъединицы.
В одном варианте осуществления антитело или его антиген-связывающую часть вводят субъекту в составе фармацевтической композиции, содержащей антитело или его антиген-связывающую часть и фармацевтически приемлемый носитель. Фармацевтическая композиция может содержать также и дополнительное средство, такое как терапевтическое средство, например, буденозид, эпидермальный фактор роста, кортикостероиды, циклоспорин, сульфазалазин, аминосалицилаты, 6-меркаптопурин, азатиоприн, метронидазол, ингибиторы липоксигеназы, мезаламин, олзалацин, балзалазид, антиоксиданты, ингибиторы тромбоксана, антагонисты рецептора IL-1, моноклональные антитела против IL-1β, моноклональные антитела против IL-6, факторы роста, ингибиторы эластазы, соединения пиридинил-имидазола, антитела или агонисты TNF, LT, IL-1, IL-2, IL-6, IL-7, IL-8, IL-15, IL-16, IL-18, EMAP-II, GM-CSF, FGF и PDGF, антитела против CD2, CD3, CD4, CD8, CD25, CD28, CD30, CD40, CD45, CD69, CD90 или их лиганды, метотрексат, циклоспорин, FK506, рапамицин, микофенолята мофетил, лефлуномид, NSAID, ибупрофен, кортикостероиды, преднизолон, ингибиторы фосфодиэстеразы, агонисты аденозина, антитромботические средства, ингибиторы комплемента, адренергические средства, IRAK, NIK, IKK, p38, ингибиторы MAP-киназы, ингибиторы IL-1β-превращающего фермента, ингибиторы TNFα-превращающего фермента, ингибиторы T-клеточных сигналов, ингибиторы металлопротеиназ, сульфазалазин, азатиоприн, 6-меркаптопурины, ингибиторы ангиотензинпревращающего фермента, растворимые рецепторы цитокинов, растворимый рецептор p55 TNF, растворимый рецептор p75 TNF, sIL-1RI, sIL-1RII, sIL-6R, противовоспалительные цитокины, IL-4, IL-10, IL-11, IL-13 и TGFβ.
В другом варианте осуществления терапевтическое средство в составе фармацевтической композиции, вводимой субъекту, может быть выбрано из группы, состоящей из анти-TNF-антител и их фрагментов, конструкций TNFR-Ig, ингибиторов TACE, ингибиторов PDE4, кортикостероидов, буденозида, дексаметазона, сульфазалазина, 5-аминосалициловой кислоты, олзалацина, ингибиторов IL-1β-превращающего фермента, IL-1ra, ингибиторов тирозинкиназы, 6-меркаптопуринов и IL-11.
В другом варианте осуществления указанное терапевтическое средство может быть выбрано из группы, состоящей из кортикостероидов, преднизолона, метилпреднизолона, азатиоприна, циклофосфамида, циклоспорина, метотрексата, 4-аминопиридина, тизанидина, интерферона-β1a, интерферона-β1b, сополимера 1, гипербарического кислорода, внутривенного иммуноглобулина, клабрибина, антител или агонистов TNF, LT, IL-1, IL-2, IL-6, IL-7, IL-8, IL-15, IL-16, IL-18, EMAP-II, GM-CSF, FGF, PDGF, антител против CD2, CD3, CD4, CD8, CD25, CD28, CD30, CD40, CD45, CD69, CD80, CD86, CD90 или лигандов, метотрексата, циклоспорина, FK506, рапамицина, микофенолята мофетила, лефлуномида, NSAID, ибупрофена, кортикостероидов, преднизолона, ингибиторов фосфодиэстеразы, агонистов аденозина, антитромботических средств, ингибиторов комплемента, адренергических средств, IRAK, NIK, IKK, p38 или ингибиторов MAP-киназы, ингибиторов IL-1β-превращающего фермента, ингибиторов TACE, ингибиторов T-клеточных сигналов, киназных ингибиторов, ингибиторов металлопротеиназ, сульфазалазина, азатиоприна, 6-меркаптопуринов, ингибиторов ангиотензин-превращающего фермента, растворимых рецепторов цитокинов, растворимого рецептора p55 TNF, растворимого рецептора p75 TNF, sIL-1RI, sIL-1RII, sIL-6R, SIL-13R, анти-P7, p-селектиновый гликопротеиновый лиганд (PSGL), противовоспалительных цитокинов, IL-4, IL-10, IL-13 и TGFβ.
В одном из вариантов осуществления антитело или его антиген-связывающая часть, используемое в способах согласно изобретению, связывается с человеческим IL-12 и/или человеческим IL-23 и диссоциирует из комплекса с человеческим IL-12 и/или человеческим IL-23, соответственно, с Kd, составляющей 1×10-10 M или менее, и с константой скорости koff, составляющей 1×10-3 сек-1 или менее, как было определено методом резонансного возбуждения поверхностных плазмонов. В одном варианте осуществления антитело или его антиген-связывающая часть диссоциирует из комплекса с человеческим IL-12 и/или человеческим IL-23 с константой скорости koff, составляющей 1×10-4 сек-1 или менее. В другом варианте осуществления антитело или его антиген-связывающая часть диссоциирует из комплекса с человеческим IL-12 и/или человеческим IL-23 с константой скорости koff, составляющей 1×10-5 сек-1 или менее.
В другом варианте осуществления антитело или его антиген-связывающая часть связывается с человеческим IL-12 и/или человеческим IL-23 и диссоциирует из комплекса с человеческим IL-12 и/или человеческим IL-23 с константой скорости koff, составляющей 1×10-2 сек-1 или менее, как было определено методом резонансного возбуждения поверхностных плазмонов. В другом варианте осуществления антитело или его антиген-связывающая часть диссоциирует из комплекса с человеческим IL-12 и/или человеческим IL-23 с константой скорости koff, составляющей 1×10-3 сек-1 или менее. Еще в одном варианте осуществления антитело или его антиген-связывающая часть диссоциирует из комплекса с человеческим IL-12 и/или человеческим IL-23 с константой скорости koff, составляющей 1×10-4 сек-1 или менее. В другом варианте осуществления антитело или его антиген-связывающая часть диссоциирует из комплекса с человеческим IL-12 и/или человеческим IL-23 с константой скорости koff, составляющей 1×10-5 сек-1 или менее.
Еще в одном варианте осуществления антитело или его антиген-связывающая часть связывается с человеческим IL-12 и/или человеческим IL-23 и диссоциирует из комплекса с человеческим IL-12 и/или человеческим IL-23, соответственно, с Kd, составляющей 1,34×10-10 M или менее. В другом варианте осуществления антитело или его антиген-связывающая часть связывается с человеческим IL-12 и/или человеческим IL-23 и диссоциирует из комплекса с человеческим IL-12 и/или человеческим IL-23, соответственно, с Kd, составляющей 9,74×10-11 M или менее. В одном из вариантов осуществления антитело или его антиген-связывающая часть представляет собой рекомбинантное антитело или его антиген-связывающую часть.
В одном варианте осуществления антитело или его антиген-связывающая часть, используемое в способах согласно изобретению, является нейтрализующим антителом, которое, например, нейтрализует активность человеческого IL-12 и/или человеческого IL-23. В одном из вариантов осуществления нейтрализующее антитело или его антиген-связывающая часть ингибирует фитогемагглютининовую бласт-пролиферацию в ФГА-анализе in vitro с IC50, составляющей 1×10-9 M или менее. В другом варианте осуществления нейтрализующее антитело или его антиген-связывающая часть ингибирует фитогемагглютининовую бласт-пролиферацию в ФГА-анализе in vitro с IC50, составляющей 1×10-10 M или менее. Еще в одном варианте осуществления нейтрализующее антитело или его антиген-связывающая часть ингибирует фитогемагглютининовую бласт-пролиферацию в ФГА-анализе in vitro с IC50, составляющей 1×10-11 M или менее. Еще в одном варианте осуществления нейтрализующее антитело или его антиген-связывающая часть ингибирует фитогемагглютининовую бласт-пролиферацию в фитогемагглютининовом анализе на бласт-пролиферацию (ФГА-анализ) in vitro с IC50, составляющей 1×10-7 M или менее. Еще в одном варианте осуществления нейтрализующее антитело или его антиген-связывающая часть ингибирует фитогемагглютининовую бласт-пролиферацию в ФГА-анализе in vitro с IC50, составляющей 1×10-8 M или менее. Еще в одном варианте осуществления нейтрализующее антитело или его антиген-связывающая часть ингибирует продуцирование человеческого IFNγ с IC50, составляющей 1×10-10 M или менее. Еще в одном варианте осуществления нейтрализующее антитело или его антиген-связывающая часть ингибирует продуцирование человеческого IFNγ с IC50, составляющей 1×10-11 M или менее. Еще в одном варианте осуществления нейтрализующее антитело или его антиген-связывающая часть ингибирует продуцирование человеческого IFNγ с IC50, составляющей 1×10-12 M или менее.
В одном варианте осуществления антитело или его антиген-связывающая часть, используемое в способах согласно изобретению,
a) ингибирует фитогемагглютининовую бласт-пролиферацию в ФГА-анализе in vitro с IC50, составляющей 1×10-9 M или менее;
b) имеет CDR3 тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO: 25; и
c) имеет CDR3 легкой цепи, содержащую аминокислотную последовательность SEQ ID NO: 26.
В одном варианте осуществления антитело дополнительно имеет CDR2 тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO: 27; и CDR2 легкой цепи, содержащую аминокислотную последовательность SEQ ID NO: 28.
Еще в одном варианте осуществления антитело или его антиген-связывающая часть дополнительно имеет CDR1 тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO: 29; и CDR1 легкой цепи, содержащую аминокислотную последовательность SEQ ID NO: 30. Еще в одном варианте осуществления антитело или его антиген-связывающая часть дополнительно ингибирует фитогемагглютининовую бласт-пролиферацию в ФГА-анализе in vitro с IC50, составляющей 1×10-10 M или менее. Еще в одном варианте осуществления антитело или его антиген-связывающая часть дополнительно ингибирует фитогемагглютининовую бласт-пролиферацию в ФГА-анализе in vitro с IC50, составляющей 1×10-11 M или менее.
В одном варианте осуществления антитело или его антиген-связывающая часть, используемое в способах согласно изобретению, имеет вариабельную область тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO: 31, и вариабельную область легкой цепи, содержащую аминокислотную последовательность SEQ ID NO: 32.
В одном варианте осуществления антитело или его антиген-связывающая часть, используемое в способах согласно изобретению, содержит константную область тяжелой цепи, выбранную из группы, состоящей из константных областей IgG1, IgG2, IgG3, IgG4, IgM, IgA и IgE. В одном из вариантов осуществления константная область тяжелой цепи антитела представляет собой IgG1. В другом варианте осуществления антитело представляет собой Fab-фрагмент, F(ab')2-фрагмент или одноцепочечный Fv-фрагмент.
В одном варианте осуществления антитело или его антиген-связывающая часть, используемое в способах согласно изобретению, диссоциирует из комплекса с человеческим IL-12 и/или человеческим IL-23 с Kd, составляющей 1×10-10 M или менее, и связывается с эпитопом на p40-субъединице человеческого IL-12 и/или человеческого IL-23.
В одном варианте осуществления антитело или его антиген-связывающая часть, используемое в способах согласно изобретению, представляет собой человеческое антитело или его антиген-связывающую часть, которое
a) диссоциирует из комплекса с человеческим IL-12 с константой скорости koff, составляющей 1×10-3 сек-1 или менее, как было определено методом резонансного возбуждения поверхностных плазмонов;
b) имеет CDR3 тяжелой цепи, содержащую аминокислотную последовательность SEQ ID NO: 25; и
c) имеет CDR3 легкой цепи, содержащую аминокислотную последовательность SEQ ID NO: 26.
В другом варианте осуществления антитело или его антиген-связывающая часть, используемое в способах согласно изобретению, диссоциирует из комплекса с человеческим IL-12 с константой скорости koff, составляющей 1×10-4 сек-1 или менее. Еще в одном варианте осуществления антитело человека или его антиген-связывающая часть диссоциирует из комплекса с человеческим IL-12 с константой скорости koff, составляющей 1×10-5 сек-1 или менее.
В одном из вариантов осуществления антитело или его антиген-связывающая часть, используемое в способах согласно изобретению, представляет собой человеческое антитело или его антиген-связывающую часть, которое связывается с человеческим IL-12 и содержит
CDR3-домен легкой цепи, содержащий аминокислотную последовательность SEQ ID NO: 26; и
CDR3-домен тяжелой цепи, содержащий аминокислотную последовательность SEQ ID NO: 25.
В одном варианте осуществления антитело или его антиген-связывающая часть имеет вариабельную область легкой цепи (LCVR), имеющую CDR3-домен, содержащий аминокислотную последовательность SEQ ID NO: 26, и имеет вариабельную область тяжелой цепи (HCVR), имеющую CDR3-домен, содержащий аминокислотную последовательность SEQ ID NO: 25. В другом варианте осуществления антитело или его антиген-связывающая часть содержит LCVR, дополнительно имеющую CDR2-домен, содержащий аминокислотную последовательность SEQ ID NO: 28, и HCVR, дополнительно имеющую CDR2-домен, содержащий аминокислотную последовательность SEQ ID NO: 27. Еще в одном варианте осуществления LCVR дополнительно имеет CDR1-домен, содержащий аминокислотную последовательность SEQ ID NO: 30, и HCVR имеет CDR1-домен, содержащий аминокислотную последовательность SEQ ID NO: 29.
В одном варианте осуществления антитело или его антиген-связывающая часть связывается с человеческим IL-12 и/или человеческим IL-23 и представляет собой антитело J695 (также обозначаемое ABT-874) или его антиген-связывающую часть.
В одном варианте осуществления антитело или его антиген-связывающая часть связывается с человеческим IL-12 и/или человеческим IL-23 и диссоциирует из комплекса с человеческим IL-12 с Kd, составляющей 1,34×10-10 M или менее, и нейтрализует человеческий IL-12 и/или человеческий IL-23. В одном варианте осуществления антитело или его антиген-связывающая часть диссоциирует из комплекса с человеческим IL-12 и/или с человеческим IL-23 с Kd, составляющей 9,74×10-11 M или менее. В одном варианте осуществления антитело или его антиген-связывающая часть ингибирует фитогемагглютининовую бласт-пролиферацию в ФГА-анализе in vitro с IC50, составляющей 1×10-7 M или менее. В одном варианте осуществления антитело или его антиген-связывающая часть ингибирует фитогемагглютининовую бласт-пролиферацию в ФГА-анализе in vitro с IC50, составляющей 1×10-8 M или менее. В одном варианте осуществления антитело или его антиген-связывающая часть ингибирует фитогемагглютининовую бласт-пролиферацию в ФГА-анализе in vitro с IC50, составляющей 1×10-9 M или менее. В одном варианте осуществления антитело или его антиген-связывающая часть ингибирует фитогемагглютининовую бласт-пролиферацию в ФГА-анализе in vitro с IC50, составляющей 1×10-10 M или менее. В одном варианте осуществления антитело или его антиген-связывающая часть ингибирует фитогемагглютининовую бласт-пролиферацию в ФГА-анализе in vitro с IC50, составляющей 1×10-11 M или менее. В одном из вариантов осуществления антитело или его антиген-связывающая часть ингибирует продуцирование человеческого IFNγ с IC50, составляющей 1×10-10 M или менее. В одном варианте осуществления антитело или его антиген-связывающая часть ингибирует продуцирование челове