Изолят белка канолы, способ его получения и применение
Иллюстрации
Показать всеИзобретение относится к пищевой промышленности. Получают водный раствор белков канолы 2S и 7S, состоящий преимущественно из белка 2S. Осуществляют изоэлектрическое осаждение белков канолы 7S из водного раствора путем добавления соли в водный раствор до электропроводимости, по меньшей мере, примерно 0,3 миллисименс (мСм). Доводят pH подсоленного водного раствора до значения от 2,0 до 4,0. Удаляют осажденный белок 7S из водного раствора. Выделяют изолят белка канолы, имеющего содержание белка, по меньшей мере, примерно 90% масс. (N×6,25) в пересчете на сухую массу (d.b.) и содержащего повышенную долю белка канолы 2S по сравнению с водным раствором белков 2S и 7S. Изобретение позволяет получить продукт, обладающий растворимостью, прозрачностью, термостойкостью и аминокислотным профилем. 11 з.п. ф-лы, 2 ил., 19 табл., 14 пр.
Реферат
Область техники, к которой относится изобретение
Настоящая заявка является частичным продолжением патентной заявки США №12/213499, поданной 20 июня 2009 г.
Настоящее изобретение относится к производству изолята белка канолы и его применению в водных растворах, включающих безалкогольные напитки и напитки для спортсменов.
Предшествующий уровень техники
Изоляты белка канолы, имеющие содержание белка, по меньшей мере, 100% масс. (N×6,25), могут быть получены из муки из масличных семян способом, описанным в совместно рассматриваемой патентной заявке США №10/137391, поданной 3 мая 2002 г. (публикация патентной заявки США №2003-0125526 и WO 02/089597), и в патентной заявке США №10/476230, поданной 9 июня 2004 г. (публикация патентной заявки США №2004-0254353), правопреемником по которым является автор настоящей заявки и содержание которых включено в настоящую заявку в виде ссылки. Способ представляет собой многостадийный процесс, включающий экстракцию муки из масличных семян канолы водным раствором соли; отделение полученного водного белкового раствора от остаточной муки из масличных семян; повышение концентрации белка в водном растворе, по меньшей мере, примерно до 200 г/л при одновременном поддержании ионной силы раствора, в основном, постоянной с применением селективной мембранной технологии; разбавление полученного концентрированного белкового раствора охлажденной водой с тем, чтобы вызвать образование белковых мицелл; осаждение белковых мицелл отстаиванием с получением аморфной, клейкой, студнеобразной, подобной клейковине белковой мицеллярной массы (РММ) и извлечение белковой мицеллярной массы из супернатанта, имеющего содержание белка, по меньшей мере, около 100% масс. (N×6,25). В контексте описания содержание белка указано в пересчете на сухую массу. Извлеченная РММ может подвергаться сушке.
В одном варианте воплощения способа супернатант от стадии отстаивания РММ подвергается обработке с целью извлечения из него изолята белка канолы. Эта процедура может осуществляться путем начального концентрирования супернатанта с применением ультрафильтрационной мембраны и последующей сушки концентрата. Полученный изолят белка канолы имеет содержание белка, по меньшей мере, около 90% масс., предпочтительно, по меньшей мере, примерно 100% масс. (N×6,25).
Способы, описанные в патентных заявках США №10/137391 и №10/476230, являются, по сути, периодическими способами. В совместно рассматриваемой патентной заявке США №10/298678, поданной 19 ноября 2002 г. (публикация патентной заявки США №2004-0039174 и WO 03/043439), правопреемником по которой является автор настоящей заявки и содержание которой включено в настоящую заявку в виде ссылки, описан непрерывный способ получения изолятов белка канолы. В соответствии с этим способом мука из масличных семян канолы непрерывно смешивается с водным раствором соли; смесь транспортируется по трубопроводу при одновременном экстрагировании белка из муки из масличных семян канолы с образованием водного белкового раствора; водный белковый раствор непрерывно пропускается через селективную мембрану с целью увеличения содержания белка в водном белковом растворе, по меньшей мере, примерно до 50 г/л при одновременном поддержании ионной силы раствора, в основном, постоянной; полученный концентрированный белковый раствор непрерывно смешивается с охлажденной водой с тем, чтобы инициировать образование белковых мицелл, и белковые мицеллы непрерывно осаждаются отстаиванием, в то время как супернатант непрерывно сливается с осадка до тех пор, пока в резервуаре-отстойнике не накопится желательное количество РММ. Эта РММ извлекается из резервуара-отстойника и может подвергаться сушке. РММ имеет содержание белка, по меньшей мере, около 90% масс. (N×6,25), предпочтительно, по меньшей мере, примерно 100% масс. Супернатант, слитый с осадка, может подвергаться обработке с целью извлечения из него изолята белка канолы, как описано выше.
Известно, что семена канолы содержат примерно от 10% до 30% масс. белков, и было идентифицировано несколько различных белковых компонентов. Эти белки включают глобулин 12S, известный как круциферин; белок 7S и запасной белок 2S, известный как напин. Как указывается в совместно рассматриваемой патентной заявке США №10/413371, поданной 15 апреля 2003 г. (публикация патентной заявки США №2004-0034200 и WO 03/088760), и в патентной заявке США №10/510766, поданной 29 апреля 2005 г. (публикация патентной заявки США №2005-0249828), правопреемником по которым является автор настоящей заявки и содержание которых включено в настоящую заявку в виде ссылки, описанные выше способы, включающие разбавление концентрированного водного белкового раствора для образования РММ и обработку супернатанта для извлечения дополнительного белка, приводят к получению изолятов различного белкового профиля.
Так, полученный из РММ изолят белка канолы имеет следующее содержание белковых компонентов: примерно от 60% до 98% масс. белка 7S; примерно от 1% до 15% масс. белка 12S и от 0 до примерно 25% масс. белка 2S. Полученный из супернатанта изолят белка канолы имеет следующее содержание белковых компонентов: примерно от 60% до 95% масс. белка 2S; примерно от 5% до 40% масс. белка 7S и от 0 до примерно 5% масс. белка 12S. Таким образом, в полученном из РММ изоляте белка канолы преобладает белок 7S, а в полученном из супернатанта изоляте белка канолы доминирует белок 2S. Как указывается в вышеупомянутых патентных заявках США №10/413371 и №10/510766, белок 2S имеет молекулярную массу около 14000 дальтон, белок 7S имеет молекулярную массу около 145000 дальтон, а белок 12S имеет молекулярную массу примерно 290000 дальтон.
Krzyzaniak et al. в Nahrung (42) 1998, Nr. 3/4, p.201-204, описал очистку до гомогенности запасного белка 2S (напин) из семян рапса и дал характеристику его вторичной структуры и стабильности конформации. Он выделял напин из семян рапса методом экстракции буфером А (50 мМ NaH2PO4, pH 7,0, 1 мМ ЭДТУ) с последующим осаждением с помощью (NH4)2SO4, растворением образовавшегося осадка в буфере А, диализом против этого же буфера и обессоливанием гель-хроматографией на колонке с Сефадекс G-50. Фракции, содержащие экстракт напина, собирались и повторно осаждались с помощью (NH4)2SO4. Полученный сырой напин растворялся в буфере В (буфер А при pH 7,4), подвергался диализу против этого же буфера, затем загружался на колонку с СМ-Сефадекс С-50 и элюировался градиентом от 0,15 до 0,35 М NaCl в буфере В. Фракции, содержащие напин, объединялись в одну, осаждались с помощью (NH4)2SO4, повторно растворялись в буфере А и подвергались диализу. Далее напин очищался катионообменной HPLC (высокоэффективная жидкостная хроматография) с использованием в качестве градиента до 1 М NaCl при pH 5,0. Фракции с λmax=280 нм собирались, концентрировались и подвергались анализу.
Заявители использовали следующие дополнительные литературные источники в части подготовки в лабораторных условиях образцов белка канолы 2S, очищенного до гомогенности:
Berot, S., Compoint, J.P., Larre, С., Malabat, С. and Gueguen, J. 2005. Large scale purification of rapeseed proteins (Brassica napus L) [Крупномасштабная очистка белков рапса]. J. Chromatography В, 818: 35-42.
Bhatty, R.S., McKenzie, S.L. and Finlayson, A.J. 1968. The proteins of rapeseed (Brassica napus L) soluble in salt solutions [Белки рапса, растворимые в солевых растворах]. Can. J. Biochem., 46: 1191-1197.
Gehrig, P.M., Krzyzaniak, A., Barciszewski, J. and Biemann, K. 1996. Mass spectrometric amino acid sequencing of a mixture of seed storage proteins (napin) from Brassica napus, products of a multigene family [Масс-спектрометрическое определение аминокислотной последовательности в смеси запасных белков (напин) из семян рапса, продуктов мультигенного семейства]. Proc. Natl. Acad. Sci. U.S.A., 93: 3647-3652.
Monsalve, R.I. and Rodriguez, R. 1990. Purification and characterization of proteins from the 2S fraction from seeds of the Brassicaceae family [Очистка и характеристика белков из 2S-фракции из семян семейства крестоцветных]. J. Exper. Bot., 41 (222): 89-94.
Muren. E., Ek, В., Bjork, I. and Rask, L. 1996. Structural comparison of the precursor and the mature form of napin, the 2S storage protein in Brassica napus. [Сравнительная оценка структуры предшественника и зрелой формы напина - запасного белка 2S рапса]. Eur. J. Biochem., 242: 214-219.
Изоляты белка канолы настоящего изобретения отличаются от известных в предшествующем уровне техники тем, что обеспечиваемые изобретением изоляты белка канолы, в которых преобладает белок 2S, содержат также и небольшое количество белка 7S.
Канола известна также как рапсовое семя или масличный рапс.
Краткое изложение сущности изобретения
Неожиданно было установлено, что изолят белка канолы, имеющий повышенную долю белка 2S, предпочтительно содержащий, по меньшей мере, около 85% масс. белка 2S и имеющий пониженную долю белка 7S, проявляет отличные свойства в водном растворе по сравнению с изолятом белка канолы, полученным из супернатанта согласно способу, описанному в вышеупомянутых патентных заявках США №10/137391 и 10/476230.
В дополнение к такой же или улучшенной растворимости в широком диапазоне значений pH изолят белка канолы, предлагаемый настоящим изобретением, способен обеспечить повышенную прозрачность в растворе с безалкогольными напитками и напитками для спортсменов, что позволяет получить прозрачные, обогащенные белком напитки. Кроме того, изолят белка канолы показывает более высокую растворимость при pH~3,5 в 0,1 М растворе хлорида натрия, чем полученный из супернатанта изолят белка канолы.
В одном аспекте настоящего изобретения обеспечивается изолят белка канолы, состоящий преимущественно из белка канолы 2S, имеющий содержание белка, по меньшей мере, около 90% масс. (N×6,25), предпочтительно, по меньшей мере, примерно 100% масс. в пересчете на сухую массу (d.b.) и содержащий повышенную долю белка канолы 2S и пониженную долю белка канолы 7S в сравнении с изолятами белка канолы, состоящими преимущественно из белка канолы 2S и полученными из водного супернатанта от образования и осаждения белковых мицелл канолы. Изолят белка канолы получают изоэлектрическим осаждением белка 7S из супернатанта.
Изолят белка канолы и композиция настоящего изобретения обладают рядом уникальных свойств, отличающихся от свойств изолятов белка канолы, полученных из супернатанта, и включающих растворимость, прозрачность, термостойкость, способность к поглощению света при 280 нм, поверхностную гидрофобность и аминокислотный профиль. Эти свойства описаны ниже, а данные, подтверждающие указанные свойства, представлены в нижеприведенных примерах.
Растворимость
Изолят белка канолы показывает такую же или улучшенную растворимость в воде и в газированных и негазированных безалкогольных напитках и напитках для спортсменов по сравнению с изолятом белка канолы, полученным из супернатанта, в широком диапазоне pH и при концентрации белка около 1% масс./об.
В дополнение к этому, изолят белка канолы показывает такую же или улучшенную растворимость в воде в широком диапазоне pH и при концентрации белка примерно 1% масс./об., причем после образования растворов или дисперсий образцы центрифугируются для осаждения нерастворимого материала с получением прозрачного супернатанта.
Кроме того, изолят белка канолы показывает более высокую растворимость в 0,1 М растворе хлорида натрия при pH 3,5, чем изолят белка канолы, полученный из супернатанта.
Прозрачность
Изолят белка канолы может вводиться в большое число напитков, таких как газированные и негазированные безалкогольные напитки, а также соки, пунши и коктейли, с целью обогащения этих напитков белком. Такие напитки имеют широкий диапазон значений pH - примерно от 2,5 до 5,0 - и зачастую разливаются в упаковки в количестве 12 жидких унций (0,355 л). Изолят белка канолы может добавляться в любом подходящем количестве для обогащения напитка белком, например в количестве, по меньшей мере, около 5 г изолята белка канолы из расчета на 12 жидких унций (0,355 л).
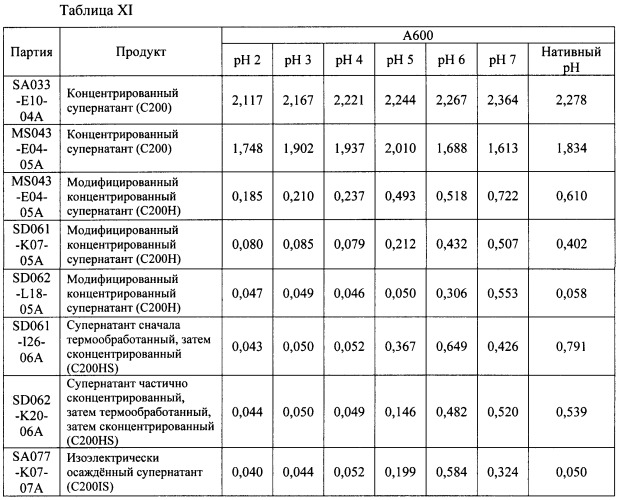
Добавленный изолят белка канолы растворяется в напитке и не ухудшает прозрачности напитка. В прозрачном напитке при концентрации белка 2% масс. прозрачность составляет менее примерно 0,5 при определении ее путем измерения поглощения видимого света при 600 нм. В воде при концентрации белка 1% масс. прозрачность составляет менее примерно 1,0 в диапазоне pH примерно от 2 до 7 при определении ее путем измерения поглощения видимого света при 600 нм.
Термостойкость
В сравнении с изолятом белка канолы, полученным из супернатанта, изолят белка канолы настоящего изобретения показывает улучшенную термостойкость как при pH 6, так и при pH 7. После изоэлектрического осаждения белка 7S из супернатанта, что более подробно описывается ниже, термообработанный супернатант оказался устойчивым к последующему осаждению белка при нагреве.
Способность к поглощению света при 280 нм
Изолят белка канолы настоящего изобретения обладает более низкой способностью к поглощению света при 280 нм, чем полученный из супернатанта изолят белка канолы. Этот результат указывает на то, что изолят белка канолы настоящего изобретения содержит меньше тирозина и триптофана, поглощающих много света при 280 нм, чем белок канолы, полученный из супернатанта.
Поверхностная гидрофобность
Изолят белка канолы настоящего изобретения показывает более низкую поверхностную гидрофобность, чем полученный из супернатанта изолят белка канолы, что, по всей вероятности, можно объяснить пониженным содержанием глобулинов в новом изоляте белка канолы по сравнению с полученным из супернатанта изолятом белка канолы.
Поверхностная гидрофобность изолята белка канолы в большинстве случаев составляет ниже примерно 25, предпочтительно - ниже примерно 20.
Изолят белка канолы настоящего изобретения получают изоэлектрическим осаждением белка 7S из концентрированного супернатанта из способа патентных заявок США №10/137391 и №10/476230 с тем, чтобы снизить долю белка 7S в концентрированном супернатанте и, следовательно, увеличить долю белка 2S. Альтернативно, подобную обработку можно проводить на супернатанте перед его концентрированном или после его частичного концентрирования. Таким образом, в другом аспекте настоящего изобретения обеспечивается способ получения изолята белка канолы, имеющего повышенную долю белка канолы 2S, который включает (а) обеспечение водного раствора белков 2S и 7S, состоящего преимущественно из белка 2S; (b) изоэлектрическое осаждение белка канолы 7S из водного раствора; (с) удаление осажденного белка 7S из водного раствора и (d) извлечение изолята белка канолы, имеющего содержание белка, по меньшей мере, около 90% масс. (N×6,25) в пересчете на сухую массу (d.b.) и содержащего повышенную долю белка канолы 2S по сравнению с водным раствором белков 2S и 7S.
Краткое описание фигур
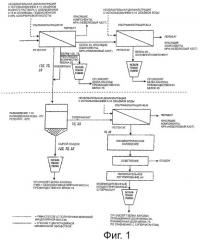
На фиг.1 схематически показан способ получения белкового изолята.
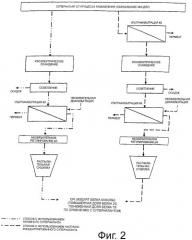
На фиг.2 схематически показан способ, который применяется для получения изолята белка канолы настоящего изобретения из супернатанта от процесса образования РРМ, представленного на фиг.1.
Подробное описание изобретения
Изолят белка канолы, обеспечиваемый настоящим изобретением, имеет содержание белка, по меньшей мере, около 90% масс. (N×6,25), предпочтительно, по меньшей мере, примерно 100% масс. и может выделяться из муки из масличных семян канолы периодическим способом или непрерывным способом либо полунепрерывным способом.
Изолят белка канолы, обеспечиваемый настоящим изобретением, состоит преимущественно из белка 2S и содержит повышенную долю белка канолы 2S и пониженную долю белка канолы 7S в сравнении с изолятами белка канолы, состоящими преимущественно из белка 2S и полученными из супернатанта от образования и осаждения белковых мицелл канолы при таких же экспериментальных условиях. Как утверждалось выше, в изолятах белка канолы настоящего изобретения наряду с пониженной долей белка 7S и повышенной долей белка 2S обычно присутствует небольшое остаточное количество белка 7S. Изолят белка канолы получают изоэлектрическим осаждением белка 7S из супернатанта.
Изоляты белка канолы содержат, по меньшей мере, около 85% масс. белка канолы 2S и менее примерно 15% масс. белка канолы 7S; предпочтительно, по меньшей мере, около 90% масс. белка канолы 2S и менее примерно 10% масс. белка канолы 7S; более предпочтительно - максимально возможную долю белка 2S. Как отмечалось выше, такие изоляты белка канолы можно получить обработкой супернатанта, частично концентрированного супернатанта и концентрированного супернатанта, что более подробно описано ниже. Обработка супернатанта, частично концентрированного супернатанта и концентрированного супернатанта приводит к осаждению белка 7S, который может удаляться из обработанного супернатанта любым удобным способом, таким как центрифугирование или фильтрация. На белок 2S указанная обработка не оказывает влияния, и, следовательно, эта обработка повышает долю присутствующего белка 2S за счет снижения доли белка 7S.
Изолят белка канолы растворяется в водном растворе в широком диапазоне значений pH, в большинстве случаев при pH примерно от 2 до 7,5, предпочтительно - примерно от 2 до 4; в большинстве случаев он показывает растворимость, равную или превышающую растворимость изолята белка канолы, состоящего преимущественно из белка 2S и полученного из супернатанта от образования и осаждения белковых мицелл канолы при таких же экспериментальных условиях. К тому же, водные растворы изолята белка канолы в безалкогольных напитках, включая как газированные, так и негазированные безалкогольные напитки, и в напитках для спортсменов, включая как газированные, так и негазированные энергетические напитки для спортсменов, например напитки промышленного производства, показывают более высокую прозрачность, чем такие же водные растворы изолята белка канолы, состоящего преимущественно из белка 2S и полученного из супернатанта от образования и осаждения белковых мицелл канолы при одинаковых условиях получения.
Концентрация изолята белка канолы в водном растворе, включая раствор в безалкогольных напитках и напитках для спортсменов, может варьировать в зависимости от предполагаемого использования раствора. В большинстве случаев концентрация белка может варьировать примерно от 0,1% до 30% масс., предпочтительно - примерно от 1% до 5% масс.
Таким образом, настоящее изобретение включает водные растворы обеспечиваемого им изолята белка канолы, к которым относятся не только вышеупомянутые растворы, но и другие напитки, такие как соки, алкогольные напитки, напитки на кофейной основе и напитки на молочной основе.
Начальная стадия способа получения изолятов белка канолы включает солюбилизацию белкового материала из муки из масличных семян канолы. Белковый материал, выделенный из муки из семян канолы, может быть нативным белком, присутствующим в семенах канолы, или белковый материал может представлять собой белок, модифицированный генетической манипуляцией, но обладающий характерными для нативного белка гидрофобными и полярными свойствами. Мука канолы может быть любой мукой канолы, полученной от удаления масла канолы из масличных семян канолы, с варьирующим уровнем неденатурированного белка, например, полученной от экстракции горячим гексаном или холодной экструзии масла. Удаление масла канолы из масличных семян канолы обычно осуществляется как отдельная операция описываемого здесь способа получения изолята белка.
Солюбилизация белка наиболее эффективно осуществляется при использовании раствора пищевой соли, поскольку присутствие соли облегчает удаление растворимого белка из муки из масличных семян. Если изолят белка канолы предназначается для непищевых целей, то можно использовать химические реагенты непищевого качества. Соль обычно является хлоридом натрия, хотя могут использоваться и другие соли, такие как хлорид калия. Раствор соли имеет ионную силу, по меньшей мере, примерно 0,05, предпочтительно, по меньшей мере, примерно 0,10, что позволяет достигать солюбилизации значительных количеств белка. С повышением ионной силы солевого раствора степень солюбилизации белка в муке из масличных семян начинает увеличиваться до тех пор, пока не достигнет максимального значения. Любое последующее повышение ионной силы раствора не приводит к увеличению общего количества солюбилизированного белка. Ионная сила раствора пищевой соли, которая инициирует максимальную солюбилизацию белка, варьирует в зависимости от используемой соли и выбранной муки из масличных семян.
С учетом повышенной степени разбавления, требуемой для осаждения белка при увеличении ионной силы, обычно предпочитается использовать значение ионной силы, ниже примерно 0,8, более предпочтительно - примерно от 0,1 до 0,15.
В периодическом способе солюбилизация белка солью осуществляется при температуре примерно от 5°C до 75°C и предпочтительно сопровождается перемешиванием для сокращения времени солюбилизации, которое обычно составляет примерно от 10 до 60 минут. Предпочтительно проводить солюбилизацию таким образом, чтобы экстрагировать максимально достижимое на практике количество белка из муки из масличных семян с тем, чтобы обеспечить высокий общий выход продукта.
В качестве нижнего температурного предела выбрана температура примерно 5°C, поскольку при температуре, ниже указанной, солюбилизация замедляется, что делает ее неэкономичной, в то время как в качестве верхнего предпочтительного температурного предела выбрана температура примерно 75°C, которая учитывает температуру денатурации некоторых из присутствующих белков.
В непрерывном способе экстрагирование белка из муки из масличных семян канолы проводится любым способом, обеспечивающим эффективное непрерывное экстрагирование белка из муки из масличных семян канолы. В одном варианте воплощения способа мука из масличных семян канолы непрерывно смешивается с раствором пищевой соли и смесь транспортируется по трубопроводу, длина которого и скорость потока в котором обеспечивают время нахождения смеси в трубопроводе, достаточное для достижения требуемого экстрагирования в соответствии с указанными здесь параметрами. В таком непрерывном способе стадия солюбилизации солью осуществляется быстро - за время примерно до 10 минут; предпочтительно проводить солюбилизацию таким образом, чтобы экстрагировать максимально достижимое на практике количество белка из муки из масличных семян канолы. Солюбилизация в непрерывном способе проводится при температурах примерно от 5°C до 75°C, предпочтительно - примерно от 15°C до 35°C.
Водный раствор пищевой соли в большинстве случаев имеет pH примерно от 5 до 6,8, предпочтительно - примерно от 5,3 до 6,2; pH раствора соли может устанавливаться на любом желательном для стадии экстракции уровне в диапазоне pH примерно от 5 до 6,8 с использованием подходящей кислоты, обычно соляной кислоты, или щелочи, обычно гидроксида натрия.
Концентрация муки из масличных семян в растворе пищевой соли на стадии солюбилизации может варьировать в широких пределах. Типичные значения концентрации составляют примерно от 5% до 15% масс./об.
Стадия экстрагирования белка водным раствором соли сопровождается дополнительным эффектом солюбилизации жиров, которые могут присутствовать в муке канолы, что впоследствии приводит к присутствию жиров в водной фазе.
Белковый раствор, полученный на стадии экстракции, в большинстве случаев имеет концентрацию белка примерно от 5 до 40 г/л, предпочтительно - примерно от 10 до 30 г/л.
Водный раствор соли может содержать антиоксидант. Антиоксидант может быть любым пригодным для данной цели антиоксидантом, таким как сульфит натрия или аскорбиновая кислота. Количество используемого антиоксиданта может варьировать примерно от 0,01% до 1% масс. раствора, предпочтительно - примерно 0,05% масс. Антиоксидант служит для ингибирования окисления фенольных соединений в белковом растворе.
Водная фаза от стадии экстракции может затем отделяться от остаточной муки канолы любым удобным способом, например с использованием декантирующей центрифуги с последующей обработкой в тарельчатой центрифуге и/или фильтрацией для удаления остаточной муки. Отделенная остаточная мука может подвергаться сушке для последующего использования.
Цвет готового изолята белка канолы можно улучшить с приданием ему более светлой окраски и менее интенсивного желтого оттенка путем смешивания активированного угля в порошке или другого адсорбента пигментов с отделенным водным белковым раствором и последующего удаления адсорбента (обычно фильтрацией) с получением белкового раствора. Для удаления пигментов может применяться также диафильтрация.
Указанная стадия удаления пигментов может проводиться в любых удобных для этого условиях, в большинстве случаев при комнатной температуре отделенного водного белкового раствора с использованием любого подходящего адсорбента пигментов. В случае использования активированного угля в порошке его количество составляет примерно от 0,025% до 5% масс./об., предпочтительно - примерно от 0,05% до 2% масс./об.
Если мука из семян канолы содержит значительные количества жира, как указывается в патентах США №№5844086 и 6005076, правопреемником по которым является автор настоящей заявки и содержание которых включено в настоящую заявку в виде ссылок, то описанные в этих патентах стадии обезжиривания могут проводиться на отделенном водном белковом растворе и на концентрированном водном белковом растворе, обсуждаемых ниже. Если предусматривается стадия улучшения цвета, то эта стадия может проводиться после первой стадии обезжиривания.
В качестве альтернативы экстракции муки из масличных семян водным раствором соли такая экстракция может проводиться с использованием только одной воды, хотя использование только воды приводит к экстрагированию меньшего количества белка из муки из масличных семян, чем при использовании водного раствора соли. В случае использования такого альтернативного способа соль в концентрациях, указанных выше, может добавляться к белковому раствору после отделения его от остаточной муки из масличных семян с целью удержания белка в растворе в ходе стадии концентрирования, описанной ниже. Если удаление жира проводится в одну стадию, то соль обычно добавляется по завершении этой операции.
Другим альтернативным способом является экстракция муки из масличных семян раствором пищевой соли при относительно высоком значении pH - выше примерно 6,8, в большинстве случаев - примерно до pH 9,9. Значение pH раствора пищевой соли может устанавливаться на требуемом уровне в щелочной области pH с использованием любой пригодной пищевой щелочи, такой как водный раствор гидроксида натрия. Альтернативно, экстракция муки из масличных семян раствором соли может проводиться при относительно низком pH - ниже примерно pH 5, в большинстве случаев - ниже примерно pH 3. При применении этого альтернативного способа водная фаза от стадии экстракции муки из масличных семян отделяется затем от остаточной муки канолы любым пригодным способом, таким как декантирующее центрифугирование с тарельчатым центрифугированием и/или фильтрацией для удаления остаточной муки. Отделенная остаточная мука может подвергаться сушке для последующего использования.
pH водного белкового раствора от стадии экстракции при высоком или низком pH устанавливается затем в диапазоне pH примерно от 5 до 6,8, предпочтительно - примерно от 5,3 до 6,2, как описано выше, перед последующей обработкой, которая обсуждается ниже. Такое регулирование pH может проводиться с использованием любой пригодной для этого кислоты, такой как соляная кислота, или щелочи, такой как гидроксид натрия, в зависимости от потребности.
Водный белковый раствор концентрируется для увеличения концентрации белка в нем при одновременном поддержании ионной силы раствора, в основном постоянной. Такое концентрированно в большинстве случаев проводится для получения концентрированного белкового раствора, имеющего концентрацию белка, по меньшей мере, около 50 г/л, предпочтительно, по меньшей мере, около 200 г/л, более предпочтительно, по меньшей мере, около 250 г/л.
Стадия концентрирования может проводиться любым удобным путем, совместимым с периодическим или непрерывным способом, например с применением любой удобной селективной мембранной технологии, такой как ультрафильтрация или диафильтрация, с использованием мембран, таких как мембраны из полых волокон или мембраны, свернутые в спирали, с соответствующей проницаемостью по молекулярной массе, например, примерно от 3000 до 100000 дальтон, предпочтительно - примерно от 5000 до 10000 дальтон, в зависимости от различных материалов, из которых изготовлены мембраны, и конфигурации мембран, а в случае непрерывного способа - в зависимости от размеров мембран, обеспечивающих требуемую степень концентрирования водного белкового раствора, пропускаемого через мембраны.
Как хорошо известно, ультрафильтрация и аналогичные селективные мембранные технологии обеспечивают прохождение низкомолекулярных веществ через мембрану с одновременным удерживанием веществ с более высокой молекулярной массой на мембране. Низкомолекулярные соединения включают не только ионные виды пищевой соли, но и низкомолекулярные материалы, экстрагированные из исходного материала, такие как углеводы, пигменты и антипитательные факторы, а также любые низкомолекулярные формы белка. Обычно выбирается мембрана с такой проницаемостью по молекулярной массе, которая обеспечивает удерживание значительной доли белка в растворе при одновременном прохождении загрязняющих веществ через мембрану, что зависит от различных материалов, из которых изготовлены мембраны, и конфигурации мембран.
Концентрированный белковый раствор может затем подвергаться стадии диафильтрации с использованием водного раствора соли такой же молярности и с таким же pH, какие имеет экстракционный раствор. Указанная диафильтрация может осуществляться с использованием примерно от 2 до 20 объемов диафильтрационного раствора, предпочтительно - примерно от 5 до 10 объемов диафильтрационного раствора. В ходе диафильтрации из водного белкового раствора удаляются дополнительные количества загрязняющих веществ, которые проходят через мембрану в пермеат. Операция диафильтрации может проводиться до тех пор, пока в пермеат не перейдут значительные дополнительные количества загрязняющих веществ и красящих веществ с заметной окраской. Указанная диафильтрация может осуществляться с применением той же мембраны, какая использовалась на стадии концентрирования. Однако при необходимости стадия диафильтрации может проводиться с применением отдельной мембраны с разной молекулярной проницаемостью, например мембраны с проницаемостью по молекулярной массе примерно от 3000 до 100000 дальтон, предпочтительно - примерно от 5000 до 10000 дальтон, в зависимости от материала, из которого изготовлена мембрана, и конфигурации мембраны.
В диафильтрационной среде может присутствовать антиоксидант, по меньшей мере, на каком-то этапе стадии диафильтрации. Антиоксидант может представлять собой любой пригодный для данной цели антиоксидант, такой как сульфит натрия или аскорбиновая кислота. Количество антиоксиданта, используемое в диафильтрационной среде, зависит от применяемых материалов и может варьировать примерно от 0,01% до 1% масс., предпочтительно составляя около 0,05% масс. Антиоксидант служит для ингибирования окисления фенольных соединений, присутствующих в концентрированном растворе изолята белка канолы.
Стадия концентрирования и стадия диафильтрации могут проводиться при любой удобной температуре, в большинстве случаев при температуре примерно от 20°C до 60°C, предпочтительно - примерно от 20°C до 30°C, в течение периода времени, достаточного для достижения требуемой степени концентрирования. Применяемые температурные и другие режимы зависят до некоторой степени от мембранного оборудования, используемого для проведения концентрирования, и от требуемой концентрации белка в растворе.
Концентрированный и необязательно диафильтрованный белковый раствор может подвергаться, при необходимости, последующей операции обезжиривания, как описано в патентах США №5844086 и 6005076.
Концентрированный и необязательно диафильтрованный белковый раствор может подвергаться операции удаления красящих веществ, альтернативной описанной выше операции удаления красящих веществ. Для этой цели может использоваться активированный уголь в порошке, а также гранулированный активированный уголь (GAC). Другим материалом, который может применяться в качестве адсорбента красящих веществ, является поливинилпирролидон.
Стадия обработки адсорбентом красящих веществ может проводиться при любых удобных условиях, в большинстве случаев при комнатной температуре раствора белка канолы. В случае применения активированного угля в порошке его количество может составлять примерно от 0,025% до 5% масс./об., предпочтительно - примерно от 0,05% до 2% масс./об. Если в качестве адсорбента красящих веществ используется поливинилпирролидон, то его количество может составлять примерно от 0,5% до 5% масс./об., предпочтительно - примерно от 2% до 3% масс./об. Адсорбент красящих веществ может удаляться из раствора белка канолы любым пригодным для этого способом, например фильтрацией.
Концентрированный и необязательно диафильтрованный раствор от необязательной стадии удаления красящих веществ может подвергаться пастеризации с целью уничтожения любых бактерий, которые могут присутствовать в муке-сырье как следствие ее хранения или других факторов и экстрагироваться из муки в раствор изолята белка канолы на стадии экстракции. Такая пастеризация может осуществляться при любых требуемых режимах пастеризации. В большинстве случаев концентрированный и необязательно диафильтрованный белковый раствор пастеризуется при температуре примерно от 55°C до 70°C, предпочтительно - примерно от 60°C до 65°C, в течение примерно от 10 до 15 минут, предпочтительно - в течение примерно 10 минут. Затем пастеризованный концентрированный белковый раствор может охлаждаться для последующей обработки, как описывается ниже, предпочтительно до температуры примерно от 25°C до 40°C.
В зависимости от температуры, применяемой на стадии концентрирования и необязательной стадии диафильтрации, и от того, проводится стадия пастеризации или нет, концентрированный белковый раствор может подогреваться до температуры, по меньшей мере, примерно от 20°C до 60°C, предпочтительно - примерно от 25°C до 40°C, для снижения вязкости концентрированного белкового раствора и облегчения, тем самым, выполнения последующей стадии разбавления и образования мицелл. Концентрированный белковый раствор не должен нагреваться до температуры, выше которой не происходит образования мицелл при разбавлении охлажденной водой.
Затем концентрированный белковый раствор от стадии концентрирования и необязательной стадии диафильтрации, необязательной стадии удаления красящих веществ, необязательной стадии пастеризации и необязательной стадии обезжиривания разбавляется с тем, чтобы инициировать образование мицелл при смешивании концентрированного белкового раствора с охлажденной водой, берущейся в объеме, требуемом для достижения желательной степени разбавления. Степень разбавления концентрированного белкового раствора может варьировать в зависимости от той доли белка канолы, которую желательно получить мицеллярным путем, и от той доли белка канолы, которая извлекается из супернатанта. В большинстве случаев при пониженных уровнях разбавления значительно больше белка канолы остается в водной фазе.
В том случае, если желательно получить максимальную долю белка мицеллярным путем, концентрированный белковый раствор разбавляется примерно в 5-25 раз, предпочтительно - примерно в 10-20 раз.
Охлажденная вода, с которой смешивается концентрированный белковый раствор, имеет температуру ниже примерно 15°C, в большинстве случаев - примерно от 1°C до 15°C, предпочтительно - ниже примерно 10°C, поскольку повышенный выход белкового изолята в форме белковой мицеллярной массы обеспечивается именно этими более низкими температурами при используемых коэффициентах разбавления.
В периодическом способе партия концентрированного белкового раствора добавляется в статическую толщу охлажденной воды, взятой в требуемом объеме, как обсуждалось выше. Разбавление концентрированного белкового раствора и, как следствие этого, понижение ионной силы раствора инициирует об