Антитела против nrr notch1 и способы их применения
Иллюстрации
Показать всеИзобретение относится к области иммунологии. Предложены варианты антител, специфически связывающихся с аминокислотными остатками 1446-1725 Notch1 мыши или 1446-1735 Notch1 человека. Раскрыт кодирующий полинуклеотид, вектор экспрессии на основе полинуклеотида, клетка-хозяин для экспрессии антитела. Описан способ получения антитела с использованием вектора, а также применение антител как лекарственного средства или в способе лечения против нарушений, связанных с повышенной передачей сигналов или повышенной экспрессией Notch1. Использование изобретения обеспечивает антитела, которые понижают передачу сигналов Notch1, что может найти применение в медицине для лечения нарушений, связанных с повышенной экспрессией Notch1. 10 н. и 32 з.п. ф-лы, 17 ил., 5 табл., 10 пр.
Реферат
ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
В настоящей заявке испрашивается приоритет по дате подачи предварительной заявки на выдачу патента США с регистрационным № 60/933072, поданной 4 июня 2007 г., и предварительной заявки на выдачу патента США с регистрационным № 60/994646, поданной 20 сентября 2007 г., описания которых включены в настоящее описание в виде ссылки.
ОБЛАСТЬ ТЕХНИКИ, К КОТОРОЙ ОТНОСИТСЯ ИЗОБРЕТЕНИЕ
Настоящее изобретение относится главным образом к области молекулярной биологии. Более конкретно, изобретение относится к антителам против области негативной регуляции (NRR) Notch1 и применениям таких антител.
УРОВЕНЬ ТЕХНИКИ
Семейство рецепторов Notch представляет собой класс эволюционно консервативных трансмембранных рецепторов, которые передают сигналы, влияющие на развитие самых разных организмов, от морских ежей до человека. И рецепторы Notch, и семейство их лигандов Delta и Serrate (известные как Jagged у млекопитающих) являются трансмембранными белками с большими внеклеточными доменами, которые содержат повторы, подобные эпидермальному фактору роста (EGF). Количество паралогов Notch отличаются у разных видов. Например, существует четыре рецептора Notch у млекопитающих (Notch1-Notch4), два у Caenorhabditis elegans (LIN-12 и GLP-1) и один у Drosophila melanogaster (Notch). Рецепторы Notch протеолитически процессируются во время транспорта к клеточной поверхности фурин-подобной протеазой на участке S1, расположенном с внешней стороны от трансмембранного домена, высвобождая внеклеточную субъединицу Notch (ECN) и трансмембранную субъединицу Notch (NTM). Две указанные субъединицы остаются нековалентно ассоциированными и составляют зрелый гетеродимерный рецептор клеточной поверхности. Субъединицы ECN Notch1 содержат 36 N-концевых EGF-подобных повторов, за которыми следуют три тандемно повторяющихся модуля Lin 12/Notch-повторов (LNR), которые предшествуют участку S1. Каждый модуль LNR содержит три дисульфидные связи и группу консервативных кислых и полярных остатков, которые предположительно координируют ион кальция. В области EGF-повтора находятся участки связывания активирующих лигандов. Модули LNR, которые содержат уникальный домен рецепторов Notch, принимают участие в поддержании Notch в конформации, соответствующей состоянию покоя, перед индуцируемой лигандом активацией. NTM Notch1 содержит внеклеточную область (которая включает сайт расщепления S2), трансмембранный фрагмент (который несет сайт расщепления S3) и большую внутриклеточную часть, которая включает домен RAM, повторы анкирина, домен трансактивации и последовательность PEST на карбоксильном конце. Стабильная ассоциация субъединиц ECN и NTM зависит от домена гетеродимеризации (HD), содержащего карбоксильный конец ECN (называемый HD-C) и внеклеточный амино-конец NTM (называемый HD-N). Связывание лиганда Notch с субъединицей ECN инициирует два следующих друг за другом протеолитических расщепления, которые происходят вследствие регулируемого внутримембранного протеолиза. Первое расщепление металлопротеазой в сайте S2 делает трансмембранную субъединицу Notch чувствительной ко второму расщеплению в сайте S3, расположенном вблизи внутреннего листка плазматической мембраны. Расщепление в сайте S3, которое катализируется мультибелковым комплексом, содержащим пресенилин и никастрин, высвобождает внутриклеточную часть трансмембранной субъединицы Notch, обеспечивая возможность ее транслокации в ядро и активации транскрипции генов-мишеней.
У человека идентифицировано пять лигандов Notch класса Jagged и Delta-подобного класса (Jagged 1 (также называемый Serrate 1), Jagged 2 (также называемый Serrate 2), Delta-подобный 1 (также называемый DLL1), Delta-подобный 3 (также называемый DLL3) и Delta-подобный 4 (также называемый DLL4)). Каждый из лигандов является однопроходным трансмембранным белком с консервативным N-концевым мотивом Delta, Serrate, LAG-2 (DSL), необходимым для связывания Notch. Серия EGF-подобных модулей, C-концевых по отношению к мотиву DSL, предшествует фрагменту, пронизывающему мембрану. В отличие от рецепторов Notch лиганды имеют короткие цитоплазматические хвосты из 70-215 аминокислот на C-конце. Кроме того, сообщалось о других типах лигандов (например, DNER, NB3 и F3/контактин).
Путь Notch функционирует в ходе различных процессов развития и физиологических процессов, включая влияние на нейрогенез у двукрылых и позвоночных. В общем, передача сигналов Notch вовлечена в латеральное торможение, принятие решений о выборе линии клеток и создание границ между группами клеток (смотри, например, Bray, Molecular Cell Biology 7: 678-679, 2006). Показано, что множество заболеваний человека, включая злокачественные опухоли и нейродегенеративные нарушения, являются результатом мутаций в генах, кодирующих рецепторы Notch или их лиганды (смотри, например, Nam et al., Curr. Opin. Chem. Biol. 6: 501-509, 2002). Связь между неограниченной передачей сигналов Notch и злокачественностью впервые была выявлена, когда идентифицировали рекуррентную хромосомную транслокацию t(7;9)(q34;q34.3), которая создает укороченный, конститутивно активный вариант Notch1 человека, в подгруппе пациентов с острым лимфобластным лейкозом (T-ALL). В мышиных моделях показано, что передача сигналов Notch1 необходима для развития T-клеток, и что опосредованные Notch1 сигналы стимулируют развитие T-клеток за счет развития B-клеток. Также в мышиных моделях избыточная передача сигналов Notch во время развития приводит к неоплазии T-клеток.
Кроме того, рецепторы Notch экспрессируются в большом числе злокачественных опухолей человека и полученных из опухолей клеточных линиях и стимулируют путь развития клеток нервной системы из эмбриональных стволовых клеток человека. Например, Notch экспрессируется на высоком уровне при неопластических поражениях шейки матки человека и в клетках почечноклеточной карциномы человека. Принимая во внимание участие пути передачи сигналов Notch в широком множестве заболеваний человека, ясно, что сохраняется потребность в средствах, которые регулируют передачу сигналов Notch, имеющих клинические характеристики, которые являются оптимальными для разработки терапевтических средств. Изобретение, описанное в настоящем документе, удовлетворяет такую потребность и обеспечивает другие преимущества.
Все публикации, упоминаемые в настоящем описании, включая заявки на выдачу патентов и публикации патентов, включены в виде ссылки в полном объеме.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Изобретение отчасти основано на идентификации множества агентов, связывающих область негативной регуляции (NRR) Notch1 (таких как антитела и их фрагменты). NRR Notch1 представляет собой важную и полезную терапевтическую мишень, и изобретение относится к композициям и способам, основанным на связывании NRR Notch1. Средства, связывающие NRR Notch1 согласно изобретению, которые описаны в настоящем документе, представляют собой ценные терапевтические и диагностические средства для применения в случае целенаправленного воздействия на патологические состояния, ассоциированные с экспрессией и/или активностью путей передачи сигналов Notch1. Соответственно, изобретение относится к способам, композициям, наборам и изделиям, имеющим отношение к связыванию NRR Notch1.
Настоящее изобретение относится к антителам, которые связываются с NRR Notch1. В одном аспекте отличительным признаком изобретения является изолированное антитело, которое связывает NRR Notch1. В конкретном аспекте в изобретении охарактеризовано изолированное антитело против NRR Notch1, которое связывает NRR Notch1 с Kd 1×10-7 или сильнее. В предпочтительных вариантах антитело против NRR Notch1 связывает NRR Notch1 с Kd 1×10-8 или сильнее или с Kd 1×10-9 или сильнее. В другом аспекте изобретение относится к изолированному анти-NRR Notch1-антителу, где полноразмерная IgG-форма антитела связывает NRR Notch1 человека и мыши с Kd 1×10-7 или сильнее. Как хорошо установлено в данной области, аффинность связывания лиганда с его рецептором может быть определена с использованием любого из множества анализов и выражена разными количественными показателями. Соответственно, в одном варианте аффинность связывания выражают в виде значений Kd, которые отражают действительную аффинность связывания (например, с минимизированными эффектами авидности). Обычно и предпочтительно аффинность связывания измеряют in vitro, либо в бесклеточных системах, либо в ассоциированных с клетками системах. Можно использовать любой из множества анализов, известных в данной области, включая анализы, описанные в настоящем документе, для проведения измерений аффинности связывания, включая, например, Biacore, радиоиммуноанализ (РИА) и ELISA.
В одном аспекте отличительным признаком изобретения является изолированное анти-NRR Notch1-антитело, содержащее:
(a) по меньшей мере, одну, две, три, четыре или пять последовательностей гипервариабельных областей (HVR), выбранных из:
(i) HVR-L1, содержащей последовательность A1-A11, где A1-A11 представляет собой RASQDVSTAVA (SEQ ID NO: 7),
(ii) HVR-L2, содержащей последовательность B1-B7, где B1-B7 представляет собой SASFLYS (SEQ ID NO: 8),
(iii) HVR-L3, содержащей последовательность C1-C9, где C1-C9 представляет собой QQSYTTPPT (SEQ ID NO: 9),
(iv) HVR-H1, содержащей последовательность D1-D10, где D1-D10 представляет собой GFTFSSYWIH (SEQ ID NO: 1),
(v) HVR-H2, содержащей последовательность E1-E18, где E1-E18 представляет собой ARINPSNGSTNYADSVKG (SEQ ID NO: 2), и
(vi) HVR-H3, содержащей последовательность F1-F14, где F1-F14 представляет собой ARGSGFRWVMDY (SEQ ID NO: 6); и
(b) по меньшей мере, один вариант HVR, где последовательность варианта HVR содержит модификацию, по меньшей мере, одного остатка в последовательности, указанной в SEQ ID NO: 1-12. Модификация по необходимости представляет собой замену, инсерцию или делецию.
В желательных вариантах осуществления изобретения вариант HVR-L3 содержит 1-4 (1, 2, 3 или 4) замены в любом сочетании следующих положений: C3 (S или F), C4 (Y или F), C5 (T или S) и C8 (P или A или S). В другом желательном варианте осуществления изобретения вариант HVR-H2 содержит 1-4 (1, 2, 3 или 4) замены в любом сочетании следующих положений: E6 (S или P или A); E8 (G или R); E10 (T или A или N); и E11 (N или H или Q или R).
В другом аспекте отличительным признаком изобретения является изолированное анти-NRR Notch1-антитело, которое содержит одну, две, три, четыре, пять или шесть HVR, где каждая HVR содержит, состоит или по существу состоит из последовательности, выбранной из последовательностей SEQ ID NO: 1-12, и где последовательность SEQ ID NO: 7 соответствует HVR-L1, последовательность SEQ ID NO: 8 соответствует HVR-L2, последовательность SEQ ID NO: 9, 10, 11 или 12 соответствует HVR-L3, последовательность SEQ ID NO: 1 соответствует HVR-H1, последовательность SEQ ID NO: 2, 3, 4 или 5 соответствует HVR-H2, и последовательность SEQ ID NO: 6 соответствует HVR-H3.
В одном аспекте изобретения предлагается антитело, содержащее область HVR-H1, включающую последовательность SEQ ID NO: 1. В одном аспекте в изобретении предлагается антитело, содержащее область HVR-H2, включающую последовательность SEQ ID NO: 2, 3, 4 или 5. В одном аспекте в изобретении предлагается антитело, содержащее область HVR-H3, включающую последовательность SEQ ID NO: 6. В одном аспекте в изобретении предлагается антитело, содержащее HVR-L3, включающую последовательность SEQ ID NO: 10, 11 или 12.
В одном аспекте в изобретении предлагается антитело, содержащее по меньшей мере одну, по меньшей мере две, по меньшей мере три или все четыре из следующих последовательностей:
(i) последовательность HVR-H1, содержащую последовательность SEQ ID NO: 1;
(ii) последовательность HVR-H2, содержащую последовательность SEQ ID NO:2, 3, 4 или 5;
последовательность HVR-H3, содержащую последовательность SEQ ID NO: 6;
последовательность HVR-L3, содержащую последовательность SEQ ID NO: 10, 11 или 12.
В предпочтительном варианте антитело содержит области HVR-L1, HVR-L2, HVR-L3, HVR-H1, HVR-H2 и HVR-H3, где каждая по порядку содержит последовательность SEQ ID NO: 7, 8, 9, 1, 2, 6. В другом предпочтительном варианте антитело содержит области HVR-L1, HVR-L2, HVR-L3, HVR-H1, HVR-H2 и HVR-H3, где каждая по порядку содержит последовательность SEQ ID NO: 7, 8, 10, 1, 3, 6. В следующем предпочтительном варианте антитело содержит области HVR-L1, HVR-L2, HVR-L3, HVR-H1, HVR-H2 и HVR-H3, где каждая по порядку содержит последовательность SEQ ID NO: 7, 8, 11, 1, 4, 6. В следующем предпочтительном варианте антитело содержит области HVR-L1, HVR-L2, HVR-L3, HVR-H1, HVR-H2 и HVR-H3, где каждая по порядку содержит последовательность SEQ ID NO: 7, 8, 12, 1, 5, 6.
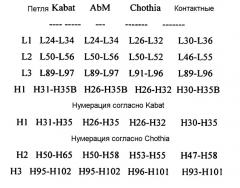
Аминокислотные последовательности SEQ ID NO: 1-12 пронумерованы в соответствии с отдельными HVR (т.е. H1, H2 или H3), которые указаны на фигуре 1, при этом нумерация соответствует системе нумерации Кабата, которая описана ниже.
В одном конкретном аспекте в изобретении предлагается изолированное анти-NRR Notch1-антитело, которое ингибирует, снижает и/или блокирует передачу сигналов Notch1. Некоторые варианты антител согласно изобретению содержат вариабельный домен легкой цепи гуманизированного антитела 4D5 (huMAb4D5-8) (HERCEPTIN®, Genentech, Inc., South San Francisco, Calif., USA) (также упоминаемого в патенте США № 6407213 и в публикации Lee et al., J. Mol. Biol. (2004), 340(5): 1073-1093), который изображен в виде последовательности SEQ ID NO: 53 ниже.
В одном варианте последовательность вариабельного домена легкой цепи huMAb4D5-8 модифицирована в одном или нескольких положениях 30, 66 и 91 (Asn, Arg и His, которые указаны жирным шрифтом/курсивом выше, соответственно). В конкретном варианте модифицированная последовательность huMAb4D5-8 содержит Ser в положении 30, Gly в положении 66 и/или Ser в положении 91. Соответственно, в одном варианте антитело согласно изобретению содержит вариабельный домен легкой цепи, содержащий последовательность, изображенную в SEQ ID NO: 54 ниже:
Замененные остатки относительно huMAb4D5-8 показаны жирным шрифтом/курсивом.
Антитела согласно изобретению могут содержать любую последовательность вариабельного домена каркаса, при условии, что активность связывания с NRR Notch1 по существу сохраняется. Например, в некоторых вариантах антитела согласно изобретению содержат консенсусную последовательность каркаса тяжелой цепи подгруппы III человека. В одном варианте таких антител, каркасная консенсусная последовательность содержит замену в положении 71, 73 и/или 78. В некоторых вариантах таких антител положение 71 представлено A, 73 представлено T и/или 78 представлено A. В одном варианте такие антитела содержат каркасные последовательности вариабельного домена тяжелой цепи huMAb4D5-8 (HERCEPTIN®, Genentech, Inc., South San Francisco, Calif., USA) (также описано в патентах США №№ 6407213 и 5821337 и в Lee et al., J. Mol. Biol. (2004), 340(5): 1073-1093). В одном варианте такие антитела дополнительно содержат консенсусную каркасную последовательность легкой цепи κI человека. В конкретном варианте такие антитела содержат последовательности HVR легкой цепи huMAb4D5-8, которое описано в патентах США №№ 6407213 и 5821337. В одном варианте такие антитела содержат последовательности вариабельного домена легкой цепи huMAb4D5-8 (HERCEPTIN®, Genentech, Inc., South San Francisco, Calif., USA) (также описанного в патента США №№ 6407213 и 5821337 и в Lee et al., J. Mol. Biol. (2004), 340(5): 1073-1093).
В одном варианте антитело согласно изобретению содержит вариабельный домен тяжелой цепи, в котором каркасная последовательность содержит последовательность SEQ ID NO: 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36 и/или 37, и последовательности HVR H1, H2 и H3 представляют собой последовательности SEQ ID NO: 1, 2 и/или 6, соответственно. В другом варианте каркасная последовательность содержит последовательность SEQ ID NO: 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36 и/или 37, и последовательности HVR H1, H2 и H3 представляют собой последовательности SEQ ID NO: 1, 3 и/или 6, соответственно. В еще одном варианте каркасная последовательность содержит последовательность SEQ ID NO: 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36 и/или 37, и последовательности HVR H1, H2 и H3 представляют собой последовательности SEQ ID NO: 1, 4 и/или 6, соответственно. В следующем варианте каркасная последовательность содержит последовательность SEQ ID NO: 19, 20, 21, 22, 23, 24, 25, 26, 27, 28, 29, 30, 31, 32, 33, 34, 35, 36 и/или 37, и последовательности HVR H1, H2 и H3 представляют собой последовательности SEQ ID NO: 1, 5 и/или 6, соответственно.
В конкретном варианте антитело согласно изобретению содержит вариабельный домен легкой цепи, в котором каркасная последовательность содержит последовательность SEQ ID NO: 38, 39, 40 и/или 41, и последовательности HVR L1, L2 и L3 представляют собой последовательности SEQ ID NO: 7, 8 и/или 9, соответственно. В другом варианте антитело согласно изобретению содержит вариабельный домен легкой цепи, в котором каркасная последовательность содержит последовательность SEQ ID NO: 38, 39, 40 и/или 41, и последовательности HVR L1, L2 и L3 представляют собой последовательности SEQ ID NO: 7, 8 и/или 10, соответственно. В дополнительном варианте антитело согласно изобретению содержит вариабельный домен легкой цепи, в котором каркасная последовательность содержит последовательность SEQ ID NO: 38, 39, 40 и/или 41, и последовательности HVR L1, L2 и L3 представляют собой последовательности SEQ ID NO: 7, 8 и/или 11, соответственно. В еще одном варианте антитело согласно изобретению содержит вариабельный домен легкой цепи, в котором каркасная последовательность содержит последовательность SEQ ID NO: 38, 39, 40 и/или 41, и последовательности HVR L1, L2 и L3 представляют собой последовательности SEQ ID NO: 7, 8 и/или 12, соответственно.
В другом варианте антитело согласно изобретению содержит вариабельный домен тяжелой цепи, в котором каркасная последовательность содержит последовательность SEQ ID NO: 42, 43, 44 и/или 45, и последовательности HVR H1, H2 и H3 представляют собой последовательности SEQ ID NO: 1, 2 и/или 6, соответственно. В дополнительном варианте антитело согласно изобретению содержит вариабельный домен тяжелой цепи, в котором каркасная последовательность содержит последовательность SEQ ID NO: 42, 43, 44 и/или 45, и последовательности HVR H1, H2 и H3 представляют собой последовательности SEQ ID NO: 1, 3 и/или 6, соответственно. В следующем варианте антитело согласно изобретению содержит вариабельный домен тяжелой цепи, в котором каркасная последовательность содержит последовательность SEQ ID NO: 42, 43, 44 и/или 45, и последовательности HVR H1, H2 и H3 представляют собой последовательности SEQ ID NO: 1, 4 и/или 6, соответственно. В еще одном варианте антитело согласно изобретению содержит вариабельный домен тяжелой цепи, в котором каркасная последовательность содержит последовательность SEQ ID NO: 42, 43, 44 и/или 45, и последовательности HVR H1, H2 и H3 представляют собой последовательности SEQ ID NO: 1, 5 и/или 6, соответственно.
В одном варианте антитело согласно изобретению содержит вариабельный домен легкой цепи, в котором каркасная последовательность содержит последовательность SEQ ID NO: 15, 16, 17 и/или 18, и последовательности HVR L1, L2 и L3 представляют собой последовательности SEQ ID NO: 7, 8 и/или 9, соответственно. В другом варианте антитело согласно изобретению содержит вариабельный домен легкой цепи, в котором каркасная последовательность содержит последовательность SEQ ID NO: 15, 16, 17 и/или 18, и последовательности HVR L1, L2 и L3 представляют собой последовательности SEQ ID NO: 7, 8 и/или 10, соответственно. В еще одном варианте антитело согласно изобретению содержит вариабельный домен легкой цепи, в котором каркасная последовательность содержит последовательность SEQ ID NO: 15, 16, 17 и/или 18, и последовательности HVR L1, L2 и L3 представляют собой последовательности SEQ ID NO: 7, 8 и/или 11, соответственно. В следующем варианте антитело согласно изобретению содержит вариабельный домен легкой цепи, в котором каркасная последовательность содержит последовательность SEQ ID NO: 15, 16, 17 и/или 18, и последовательности HVR L1, L2 и L3 представляют собой последовательности SEQ ID NO: 7, 8 и/или 12, соответственно.
В одном варианте антитело согласно изобретению содержит вариабельный домен тяжелой цепи, в котором каркасная последовательность содержит последовательности SEQ ID NO: 42, 43, 47 и/или 45, и последовательности HVR H1, H2 и H3 представляют собой последовательности SEQ ID NO:1, 2 и/или 6, соответственно. В дополнительном варианте антитело согласно изобретению содержит вариабельный домен тяжелой цепи, в котором каркасная последовательность содержит последовательности SEQ ID NO: 42, 43, 47 и/или 45, и последовательности HVR H1, H2 и H3 представляют собой последовательности SEQ ID NO: 1, 3 и/или 6, соответственно. В другом варианте антитело согласно изобретению содержит вариабельный домен тяжелой цепи, в котором каркасная последовательность содержит последовательности SEQ ID NO: 42, 43, 47 и/или 45, и последовательности HVR H1, H2 и H3 представляют собой последовательности SEQ ID NO: 1, 4 и/или 6, соответственно. В следующем варианте антитело согласно изобретению содержит вариабельный домен тяжелой цепи, в котором каркасная последовательность содержит последовательности SEQ ID NO: 42, 43, 47 и/или 45, и последовательности HVR H1, H2 и H3 представляют собой последовательности SEQ ID NO: 1, 5 и/или 6, соответственно.
В одном варианте антитело согласно изобретению содержит вариабельный домен легкой цепи, в котором каркасная последовательность содержит последовательности SEQ ID NO: 15, 16, 47 и/или 18, и последовательности HVR L1, L2 и L3 представляют собой последовательности SEQ ID NO: 7, 8 и/или 9, соответственно. В другом варианте антитело согласно изобретению содержит вариабельный домен легкой цепи, в котором каркасная последовательность содержит последовательности SEQ ID NO: 15, 16, 47 и/или 18, и последовательности HVR L1, L2 и L3 представляют собой последовательности SEQ ID NO: 7, 8 и/или 10, соответственно. В еще одном варианте антитело согласно изобретению содержит вариабельный домен легкой цепи, в котором каркасная последовательность содержит последовательности SEQ ID NO: 15, 16, 47 и/или 18, и последовательности HVR L1, L2 и L3 представляют собой последовательности SEQ ID NO: 7, 8 и/или 11, соответственно. В следующем варианте антитело согласно изобретению содержит вариабельный домен легкой цепи, в котором каркасная последовательность содержит последовательности SEQ ID NO: 15, 16, 47 и/или 18, и последовательности HVR L1, L2 и L3 представляют собой последовательности SEQ ID NO: 7, 8 и/или 12, соответственно.
В еще одном варианте антитело согласно изобретению является антителом с созревшей аффинностью, чтобы получить требуемую аффинность связывания мишени. В одном примере антитело с созревшей аффинностью согласно изобретению содержит замену в одном или нескольких положениях аминокислот H53, H55, H57, H58, L91 и L96. В одном примере антитело с созревшей аффинностью согласно изобретению содержит одну или несколько из следующих замен: (a) в тяжелой цепи S53P, S53A, G55R, T57A, T57N, N58H, N58Q и N58R или (b) в легкой цепи S91F, P96A и P96S.
В другом аспекте антитело согласно изобретению содержит вариабельный домен тяжелой цепи, содержащий последовательность SEQ ID NO: 58. В одном варианте антитело согласно изобретению содержит вариабельный домен легкой цепи, содержащий последовательность SEQ ID NO: 59. В одном варианте антитело согласно изобретению содержит вариабельный домен тяжелой цепи, содержащий последовательность SEQ ID NO: 58, и вариабельный домен легкой цепи, содержащий последовательность SEQ ID NO: 59. В другом аспекте антитело согласно изобретению содержит вариабельный домен тяжелой цепи, содержащий последовательность SEQ ID NO: 60. В одном варианте антитело согласно изобретению содержит вариабельный домен легкой цепи, содержащий последовательность SEQ ID NO: 61. В одном варианте антитело согласно изобретению содержит вариабельный домен тяжелой цепи, содержащий последовательность SEQ ID NO: 60, и вариабельный домен легкой цепи, содержащий последовательность SEQ ID NO: 61. В другом аспекте антитело согласно изобретению содержит вариабельный домен тяжелой цепи, содержащий последовательность SEQ ID NO: 62. В одном варианте антитело согласно изобретению содержит вариабельный домен легкой цепи, содержащий последовательность SEQ ID NO: 63. В одном варианте антитело согласно изобретению содержит вариабельный домен тяжелой цепи, содержащий последовательность SEQ ID NO: 62, и вариабельный домен легкой цепи, содержащий последовательность SEQ ID NO: 63. В другом аспекте антитело согласно изобретению содержит вариабельный домен тяжелой цепи, содержащий последовательность SEQ ID NO: 64. В одном варианте антитело согласно изобретению содержит вариабельный домен легкой цепи, содержащий последовательность SEQ ID NO: 65. В одном варианте антитело согласно изобретению содержит вариабельный домен тяжелой цепи, содержащий последовательность SEQ ID NO: 64, и вариабельный домен легкой цепи, содержащий последовательность SEQ ID NO: 65.
В одном аспекте в изобретении предлагается антитело, которое конкурирует с любым из описанных выше антител за связывание с NRR Notch1. В одном аспекте в изобретении предлагается антитело, которое связывается с тем же самым или подобным эпитопом на NRR Notch1, что и любое из описанных выше антител.
Как известно в данной области и как описано более подробно ниже, положение аминокислот/определение границ гипервариабельной области антитела могут варьировать в зависимости от контекста и различных определений, известных в данной области (которые описаны ниже). Некоторые положения в вариабельном домене могут рассматриваться как гибридные гипервариабельные положения, так как такие положения можно считать находящимися в гипервариабельной области согласно одной группе критериев, а также считать находящимися вне гипервариабельной области согласно другой группе критериев. Одно или несколько таких положений также можно найти в расширенных гипервариабельных областях (которые дополнительно определены ниже).
В некоторых вариантах антитело является моноклональным антителом. В других вариантах антитело является поликлональным антителом. В некоторых вариантах антитело выбрано из группы, состоящей из химерного антитела, антитела с созревшей аффинностью, гуманизированного антитела и антитела человека. В некоторых вариантах антитело представляет собой фрагмент антитела. В некоторых вариантах антитело представляет собой Fab, Fab', Fab'-SH, F(ab')2 или scFv.
В одном варианте антитело является химерным антителом, например антителом, содержащим антигенсвязывающие последовательности донора, отличного от человека, к которым привита гетерологичная последовательность животного, отличного от человека, человека или гуманизированная последовательность (например, каркасные последовательности и/или последовательности константного домена). В одном варианте донором, отличным от человека, является мышь. В следующем варианте антигенсвязывающая последовательность является синтетической, например, получена с помощью мутагенеза (например, с использованием скрининга в фаговом дисплее, и т.д.). В конкретном варианте химерное антитело согласно изобретению имеет мышиные V-области и человеческую C-область. В одном варианте V-область легкой цепи мыши сливают с легкой цепью каппа человека. В другом варианте V-область тяжелой цепи мыши сливают с C-областью IgG1 человека.
Гуманизированные антитела согласно изобретению включают антитела, которые имеют аминокислотные замены в каркасной области (FR), и варианты по созреванию аффинности с изменениями в привитых CDR. Заменяемые аминокислоты в CDR или FR не ограничены аминокислотами, присутствующими в донорном или реципиентном антителе. В других вариантах антитела согласно изобретению дополнительно содержат изменения в аминокислотных остатках в Fc-области, которые приводят к улучшенной эффекторной функции, включая усиленную функцию CDC и/или ADCC и B-клеточный киллинг. Другие антитела согласно изобретению включают антитела, имеющие специфичные изменения, которые повышают стабильность. В других вариантах антитела согласно изобретению содержат изменения аминокислотных остатков в Fc-области, которые приводят к пониженной эффекторной функции, например пониженной функции CDC и/или ADCC и/или сниженному B-клеточному киллингу. В некоторых вариантах антитела согласно изобретению характеризуются пониженным связыванием (например, отсутствием связывания) с фактором комплемента C1q человека и/или Fc-рецептором человека на природных клетках-киллерах (NK). В некоторых вариантах антитела согласно изобретению характеризуются пониженным связыванием (например, отсутствием связывания) с FcγRI, FcγRIIA и/или FcγRIIIA. В некоторых вариантах антитела согласно изобретению относятся к классу IgG (например, IgG1 или IgG4) и содержат, по меньшей мере, одну мутацию в E233, L234, G236, D265, D270, N297, E318, K320, K322, A327, A330, P331 и/или P329 (нумерация согласно указателю EU). В некоторых вариантах антитела содержат мутации L234A/L235A или D265A/N297A.
В одном аспекте в изобретении предлагаются анти-NRR Notch1-полипептиды, содержащие любую из антигенсвязывающих последовательностей, предлагаемых в изобретении, при этом анти-NRR Notch1-полипептиды специфично связываются с NRR Notch1, например с NRR Notch1 человека или мыши.
Антитела согласно изобретению связывают (например, специфично связывают) NRR Notch1 и в некоторых вариантах могут модулировать один или несколько аспектов передачи сигнала Notch1 и/или нарушения любого биологически важного биологического пути Notch1 и/или лиганда Notch1, и/или лечение и/или профилактику опухоли, клеточного пролиферативного нарушения или злокачественной опухоли, и/или лечение или профилактику нарушения, ассоциированного с экспрессией и/или активностью Notch1 (такой как повышенная экспрессия и/или активность Notch1). В некоторых вариантах антитело против NRR Notch1 специфично связывается с полипептидом, состоящим или в основном состоящим из NRR Notch1 (например, NRR Notch1 человека или мыши). В некоторых вариантах антитело специфично связывает Notch1 с Kd 1×10-7 или сильнее. В некоторых вариантах антитело согласно изобретению уменьшает, ингибирует и/или блокирует активность Notch1 in vivo и/или in vitro.
В одном аспекте изобретение относится к применению антитела согласно изобретению для получения лекарственного средства для терапевтического и/или профилактического лечения нарушения, такого как злокачественная опухоль, опухоль и/или клеточное пролиферативное нарушение. В некоторых вариантах нарушение представляет собой невропатию или нейродегенеративное заболевание. В следующих предпочтительных вариантах нарушение представляет собой патологическое состояние, ассоциированное с ангиогенезом. В некоторых вариантах патологическим состоянием, ассоциированным с ангиогенезом, является опухоль, злокачественная опухоль и/или клеточное пролиферативное нарушение. В некоторых вариантах патологическим состоянием, ассоциированным с ангиогенезом, является внутриглазное неоваскулярное заболевание.
В одном аспекте в изобретении предлагаются композиции, содержащие одно или несколько антител согласно изобретению и носитель. В одном варианте носитель является фармацевтически приемлемым.
В другом аспекте в изобретении предлагаются нуклеиновые кислоты, кодирующие анти-NRR Notch1-антитело согласно изобретению.
В еще одном аспекте в изобретении предлагаются векторы, содержащие нуклеиновую кислоту согласно изобретению.
В следующем аспекте в изобретении предлагаются композиции, содержащие одну или несколько нуклеиновых кислот согласно изобретению и носитель. В одном варианте носитель является фармацевтически приемлемым.
В одном аспекте в изобретении предлагаются клетки-хозяева, содержащие нуклеиновую кислоту или вектор согласно изобретению. Вектор может быть любого типа, например рекомбинантный вектор, такой как экспрессирующий вектор. Можно использовать любые из множества клеток-хозяев. В одном варианте клеткой-хозяином является прокариотическая клетка, например, E. coli. В другом варианте клеткой-хозяином является эукариотическая клетка, например, клетка млекопитающего, такая как клетка яичника китайского хомячка (CHO).
В следующем аспекте в изобретении предлагаются способы получения антитела согласно изобретению. Например, в изобретении предлагаются способы получения анти-NRR Notch1-антитела (которое, как определено в настоящем описании, включает полноразмерное антитело и его фрагменты), где указанный способ включает экспрессию в подходящей клетке-хозяине рекомбинантного вектора согласно изобретению, кодирующего антитело (или его фрагмент), и извлечение антитела.
В одном аспекте в изобретении предлагается изделие, содержащее емкость и композицию, находящуюся в емкости, при этом композиция содержит одно или несколько анти-NRR Notch1-антител согласно изобретению. В одном варианте композиция содержит нуклеиновую кислоту согласно изобретению. В другом варианте композиция, содержащая антитело, дополнительно содержит носитель, который в некоторых вариантах является фармацевтически приемлемым. В одном варианте изделие согласно изобретению дополнительно включает инструкции по введению композиции (например, антитела) человеку (например, инструкции по применению любого из способов, описанных в настоящем документе).
В другом аспекте в изобретении предлагается набор, включающий первую емкость, содержащую композицию, которая содержит одно или несколько анти-NRR Notch1-антител согласно изобретению, и вторую емкость, содержащую буфер. В одном варианте буфер является фармацевтически приемлемым. В одном варианте композиция, содержащая антитело, дополнительно содержит носитель, который в некоторых вариантах является фармацевтически приемлемым. В другом варианте набор дополнительно содержит инструкции по введению композиции (например, антитела) человеку.
В следующем аспекте изобретение относится к применению анти-NRR Notch1-антитела согласно изобретению для получения лекарственного средства для терапевтического и/или профилактического лечения нарушения, такого как злокачественная опухоль, опухоль и/или клеточное пролиферативное нарушение. В некоторых вариантах нарушение представляет собой невропатию или нейродегенеративное заболевание. В следующих предпочтительных вариантах нарушением является патологическое состояние, ассоциированное с ангиогенезом. В некоторых вариантах патологическим состоянием, ассоциированным с ангиогенезом, является опухоль, злокачественная опухоль и/или клеточное пролиферативное нарушение. В некоторых вариантах патологическим состоянием, ассоциированным с ангиогенезом, является внутриглазное неоваскулярное заболевание.
В одном аспекте изобретение относится к применению нуклеиновой кислоты согласно изобретению для получения лекарственного средства для терапевтического и/или профилактического лечения нарушения, такого как злокачественная опухоль, опухоль и/или клеточное пролиферативное нарушение. В некоторых вариантах нарушение представляет собой невропатию или нейродегенеративное заболевание. В следующих предпочтительных вариантах нарушением является патологическое состояние, ассоциированное с ангиогенезом. В некоторых вариантах патологическим состоянием, ассоциированным с ангиогенезом, является опухоль, злокачественная опухоль и/или клеточное пролиферативное нарушение. В некоторых вариантах патологическим состоянием, ассоциированным с ангиогенезом, является внутриглазное неоваскулярное заболевание.
В другом аспекте изобретение относится к применению экспрессирующего вектора согласно изобретению для получения лекарственного средства для терапевтического и/или профилактического лечения нарушения, такого как злокачественная опухоль, опухоль и/или клеточное пролиферативное нарушение. В некоторых вариантах нарушение представляет собой невропатию или нейродегенеративное заболевание. В следующих предпочтительных вариантах нарушением является патологическое состояние, ассоциированное с ангиогенезом. В некоторых вариантах патологическим состоянием, ассоциированным с ангиогенезом, является опухоль, злокачественная опухоль и/или клеточное пролиферативное нарушение. В некоторых вариантах патологическим состоянием, ассоциированным с ангиогенезом, является внутриглазное неоваскулярное заболевание.
В следующем аспекте изобретение относится к применению клетки-хозяина согласно изобретению для получения лекарственного средства для терапевтического и/или профилактического лечения нарушения, такого как злокачественная опухоль, опухоль и/или клеточное пролиферативное нарушение. В некоторых вариантах нарушение представляет собой невропатию или нейродегенеративное заболевание. В следующих предпочтительных вариантах нарушением является патологическое состояние, ассоциированное с ангиогенезом. В некоторых вариантах патологическим состоянием, ассоциированным с ангиогенезом, является опухоль, злокачественная опухоль и/или клеточное пролиферативное нарушение. В некоторых вариантах патологическим состоянием, ассоциированным с ангиогенезом, является в