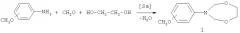Способ получения 3-(о-,м-,п-метоксифенил)-тетрагидро-2н-1,5,3-диоксазепинов
Иллюстрации
Показать всеИзобретение относится к области органической химии, в частности к способу получения 3-(о-, м-, п-метоксифенил)-тетрагидро-2Н-1,5,3-диоксазепинов, который заключается в том, что к предварительно полученной при 20°С в течение 30 мин смеси формальдегида с 1,2-этандиолом добавляют катализатор Sm(NO3)3·6H2O, о-(или м-, или п-)метоксианилин при мольном соотношении о-(или м-, или п-)метоксианилин: формальдегид:1,2-этандиол:Sm(NO3)3·6H2O=10:20:10:0.5, с последующим перемешиванием при комнатной (~20°С) температуре в течение 50-70 мин в хлороформе. Технический результат - разработан способ получения индивидуальных 3-(о-, м-, п-метоксифенил)-тетрагидро-2Н-1,5,3-диоксазепинов, которые могут найти применение в качестве антибактериальных, антигрибковых и антивирусных агентов, а также в тонком органическом синтезе. 1 табл., 1 пр.
Реферат
Предлагаемое изобретение относится к области органической химии, в частности к способу получения 3-(о-, м-, п-метоксифенил)-тетрагидро-2Н-1,5,3-диоксазепинов общей формулы (1):
Гетероциклические соединения известны как антибактериальные, антигрибковые и антивирусные агенты (Stillings M.R., Welbourn A.P., Walter D.J. Substituted 1,3,4-thiadiazoles with anticonvulsant activity // Med. Chem., 1986, 29, p.2280-2284; Kidwai M., Negi N., Chaudhary S.R. Cyclothiomethylation of arge hydrazines with formaldehyde // Acta Pharma., 1995, 45, p.511; Тюкавкина Н.А., Зурабян С.Э., Белобородов В.Л. и др. Органическая химия. M.: Дрофа, 2008, с.66-67), могут найти применение в тонком органическом синтезе.
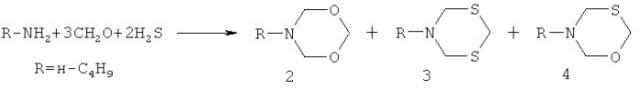
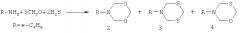
Известен способ (С.Р.Хафизова, В.Р.Ахметова, Л.Ф.Коржова, Т.В.Хакимова, Р.В.Кунакова, Э.А.Круглов, У.М.Джемилев. Многокомпонентная конденсация алифатических аминов с формальдегидом и сероводородом. Изв. АН. Сер. хим., 2005, №2, с.423-427) получения N,O-содержащих гетероциклов, а именно N-бутил-1,3,5-диоксазинана (2) с выходом 12% в смеси с N-бутил-1,3,5-дитиазинаном (3, 73%) и N-бутил-1,3,5-оксатиазинаном (4, 15%), взаимодействием бутиламина с формальдегидом (СН2О) и газообразным сероводородом по схеме:
В известном способе 1,3,5-диоксазинан (2) образуется с выходом 12% в смеси с N-бутил-1,3,5-дитиазинаном (3) и N-бутил-1,3,5-оксатиазинаном (4). Реакция идет с участием в качестве одного из исходных реагентов газообразного и токсичного сероводорода. По известному способу 3-(о-, м-, п-метоксифенил)-тетрагидро-2Н-1,5,3-диоксазепины общей формулы (1) не образуются.
Известен способ (H.Kapnang, G.Charles. Perhydro dioxazepines-1,5,3: methode generale de synthese. Tetrahedron Lett., 1980, 21, p.2949-2950) получения N,O-содержащих гетероциклов, а именно 3-алкил(циклоалкил)-1,3,5-пергидродиоксазепинов (5) с выходом 50-80%, взаимодействием первичных алкил(циклоалкил)аминов с 1,2-этандиолом и параформальдегидом в кипящем бензоле по схеме:
Известный способ не технологичен и пожароопасен, так как предполагает применение бензола (мутаген) в качестве растворителя при температуре его кипения. Кроме того, известным способом не могут быть получены 3-(о-, м-, п-метоксифенил)-тетрагидро-2Н-1,5,3-диоксазепины общей формулы (1).
Таким образом, в литературе отсутствуют сведения по получению 3-(о-, м-, п-метоксифенил)-тетрагидро-2Н-1,5,3-диоксазепинов общей формулы (1).
Предлагается новый способ получения 3-(о-, м-, п-метоксифенил)-тетрагидро-2Н-1,5,3-диоксазепинов общей формулы (1).
Сущность способа заключается в предварительном перемешивании водного раствора (37%) формальдегида с 1,2-этандиолом при комнатной (~20°С) температуре в течение 30 мин с последующим добавлением катализатора Sm(NO3)3·6H2O, хлороформа (CHCl3) в качестве растворителя и соответствующего о-, м-, п-метоксианилина, взятых в мольном соотношении формальдегид:1,2-этандиол:о-, м-, п-метоксианилин:Sm(NO3)3·6H2O=20:10:10:(0.3-0.7). Смесь перемешивают 50-70 минут при температуре ~20°С и атмосферном давлении, выделяют соответствующий 3-(о-, м-, п-метоксифенил)-тетрагидро-2Н-1,5,3-диоксазепин общей формулы (1) с выходом 60-86%. Реакция протекает по схеме:
3-(о-, м-, п-Метоксифенил)-тетрагидро-2Н-1,5,3-диоксазепины общей формулы (1) образуются только лишь с участием формальдегида, 1,2-этандиола и о-, м-, п-метоксианилина, взятых в мольном соотношении 20:10:10 (стехиометрические количества). При другом соотношении исходных реагентов снижается селективность реакции. В присутствии других альдегидов (например, алкил-, арилзамещенные альдегиды), других кислородсодержащих соединений (например, 1,3-пропандиол, 1,4-бутандиол) или других замещенных анилинов (например, алкил-, ариланилины) целевые продукты (1) не образуются. В этих условиях без катализатора реакция идет с выходом, не превышающим 10%.
Проведение указанной реакции в присутствии катализатора Sm(NO3)3·6H2O больше 7 мол.% не приводит к существенному увеличению выхода целевого продукта (1). Использование катализатора Sm(NO3)3·6H2O менее 3 мол.% снижает выход (1), что связано, возможно, со снижением каталитически активных центров в реакционной массе. Реакции проводили при температуре 20°С. При температуре выше 20°С (например, 60°С) снижается селективность реакции и увеличиваются энергозатраты, а при температуре ниже 20°С (например, -10°С) снижается скорость реакции. Опыты проводили в хлороформе, т.к. в нем хорошо растворяются исходные реагенты и целевые продукты.
Существенные отличия предлагаемого способа.
В известном способе реакция идет с участием в качестве исходного реагентов алкил(циклоалкил)аминов в кипящем бензоле с образованием 3-алкил(циклоалкил)-1,3,5-пергидродиоксазепинов (5). Известный способ не позволяет получать 3-(o-, м-, п-метоксифенил)-тетрагидро-2H-1,5,3-диоксазепины общей формулы (1).
В предлагаемом способе в качестве исходных реагентов применяются о-, м-, п-метоксианилины, реакция идет в хлороформе в качестве растворителя при комнатной температуре под действием каталитических количеств Sm(NO3)3·6H2O. В отличие от известных предлагаемый способ позволяет получать индивидуальные 3-(о-, м-, п-метоксифенил)-тетрагидро-2H-1,5,3-диоксазепины общей формулы (1).
Способ поясняется следующими примерами.
Пример 1. В сосуд Шленка, установленный на магнитной мешалке, в атмосфере аргона при температуре ~20°С помещают 20 ммоль водного раствора (37%) формальдегида и 10 ммоль 1,2-этандиола, перемешивают в течение 30 мин, затем добавляют 0.5 ммоль Sm(NO3)3·6H2O, 5 мл хлороформа и 10 ммоль м-мстоксианилина. Реакционную смесь перемешивают при температуре ~20°С в течение 60 минут, экстрагируют хлороформом, выделяют 3-(м-метоксифенил)-тстрагидро-2H-1,5,3-диоксазепин с выходом 81%.
Другие примеры, подтверждающие способ, приведены в табл.1.
| Таблица 1 | ||||
| №№ п/п | Исходный метоксианилин | Соотношение нитроанилин: формальдегид:1.2-этандиол:Sm(NO3)3·6H2O, ммоль | Время реакции, мин | Выход (1), % |
| 1 | м-метоксианилин | 10:20:10:0.5 | 60 | 81 |
| 2 | - «- | 10:20:10:0.3 | 60 | 77 |
| 3 | - «- | 10:20:10:0.7 | 60 | 86 |
| 4 | - «- | 10:20:10:0.5 | 50 | 74 |
| 5 | - «- | 10:20:10:0.5 | 70 | 84 |
| 6 | о-метоксианилин | 10:20:10:0.5 | 60 | 60 |
| 7 | n-метоксианилин | 10:20:10:0.5 | 60 | 75 |
Все опыты проводили в хлороформе при комнатной температуре (~20°С).
Спектральные характеристики 3-(м-метоксифеиил)-тетрагидро-2H-1,5,3-диоксазепина: спектр ЯМР 1Н (δ, м.д., CDCl3, J/Гц): 3.47-3.82 (м, 7Н, СН2, CH3 (6,7,15)); 4.87 (с, 4Н, CH2 (2,4)); 6.28-7.15 (м, 4H, CH (9,11,12,13)).
Спектр ЯМР 13С (δ, м.д., J/Гц): 55.14 (С-15); 69.40 (С-6,7); 80.66 (С-2,4); 102.18 (С-9); 105.46 (С-11); 108.33 (С-13); 129.78 (С-12); 147.80 (С-8); 158.26 (С-10).
Спектральные характеристики 3-(о-метоксифенил)-тетрагидро-2Н-1,5,3-диоксазепина: спектр ЯМР 1Н (δ, м.д., CDCl3, J/Гц): 3.53-3.79 (м, 7Н, СН2, CH3, (6,7,15)); 4.94 (с, 4H, CH2(2,4)); 6.37-7.23 (м, 4H, CH(10-13)).
Спектр ЯМР 13С (δ, м.д., J/Гц): 55.23 (С-15); 68.77 (С-6,7); 80.88 (С-2,4); 102.01 (С-10); 104.98 (C-13); 109.21 (С-12); 130.06 (C-11); 146.93 (С-8); 160.61 (C-9).
Спектральные характеристики 3-(п-метоксифенил)-тетрагидро-2H-1,5,3-диоксазепина: спектр ЯМР 1H (δ, м.д., CDCl3, J/Гц): 3.43-3.70 (м, 7H, СН2, CH3 (6,7,15)); 4.87 (с, 4Н, СН2 (2,4)); 6.40-7.28 (м, 4Н, CH (10-13)).
Спектр ЯМР 13С (δ, м.д., J/Гц): 59.89 (С-15); 73.83 (С-6,7); 81.07 (С-2,4); 112.66 (С-10,12); 129.92 (С-9,13); 146.74 (C-8); 160.69 (C-11).
Способ получения 3-(о-,м-,п-метоксифенил)-тетрагидро-2Н-1,5,3-диоксазепинов общей формулы (1) отличающийся тем, что к предварительно полученной при 20°С в течение 30 мин смеси формальдегида с 1,2-этандиолом добавляют катализатор Sm(NO3)3·6H2O, о-(или м-, или п-)метоксианилин при мольном соотношении о-(или м-, или п-)метоксианилин:формальдегид:1,2-этандиол:Sm(NO3)3·6H2O=10:20:10:0,5 с последующим перемешиванием при комнатной (~20°С) температуре в течение 50-70 мин в хлороформе.