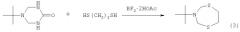Способ получения 2- и 4-(1,5,3-дитиазоцинан-3-ил)фенолов
Иллюстрации
Показать всеИзобретение относится к органической химии, конкретно к способу получения 2- и 4-(1,5,3-дитиазоцинан-3-ил)фенолов общей формулы (1): ,
который заключается в том, что формальдегид предварительно перемешивают с 1,3-пропандитиолом при комнатной (~20°С) температуре в течение 30 мин с последующим добавлением о-, n-аминофенола в EtOH в качестве растворителя в присутствии катализатора кристаллогидрата нитрата самария Sm(NO3)3·6H2O при мольном соотношении формальдегид: 1,3-пропандитиол: о-, n-аминофенол: Sm(NO3)3·6H2O = 20:10:10:(0.3-0.7) в атмосфере аргона при комнатной (~20°С) температуре и атмосферном давлении в течение 2.5-3.5 ч. Технический результат - разработан способ получения новых 2- и 4-(1,5,3-дитиазоцинан-3-ил)фенолов, которые могут найти применение в качестве биологически активных веществ, например, препаратов с антибактериальными, антигрибковыми, антивирусными свойствами, комплексообразователей, селективных сорбентов и экстрагентов драгоценных металлов, специальных реагентов для подавления жизнедеятельности бактерий в различных средах. 1 табл., 1 пр.
Реферат
Изобретение относится к органической химии, в частности к способу получения 2- и 4-(1,5,3-дитиазоцинан-3-ил)фенолов общей формулы (1):
Фенолы с гетеро(S,N)циклическим заместителем формулы (1) могут найти применение в качестве биологически активных веществ, например, лекарственных препаратов с антибактериальными, антигрибковыми, антивирусными свойствами, комплексообразователей, селективных сорбентов и экстрагентов драгоценных металлов, специальных реагентов для подавления жизнедеятельности бактерий в различных средах [Патент РФ 2160233. Бюл. №34 (2000); А.С.Заседателев, А.Л.Жузе, К.Циммер, С.Л.Гроховский, В.Г.Туманян, Г.В.Гурский, Б.П.Готтих. ДАН СССР, 1976, 4, с.1006; R.B.Pawar, V.V.Mulwad. ХГС, 2004, 2, с.2570; Ю.И.Муринов, В.Н.Майстренко, Н.Г.Афзалетдинова. Экстракция металлов S, N-органическими соединениями, Наука, М., 1993, с.192; А.В.Богатский, Н.Г.Лукьяненко, Ю.А.Попков, К.С.Захаров, В.М.Варавва. ЖОрХ, 1981, 5, с.1063].
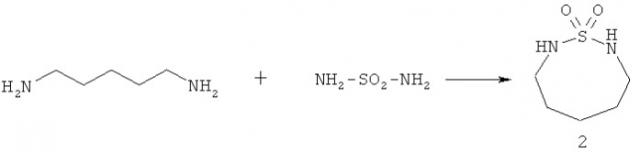
Известен способ (М. Preiss. 1,2,5-Thiadiazolidin-1,1-dioxid und Homologe. Chem. Ber, 1978, 111, p.1915-1921) получения соединений дитиазоцинанового ряда, а именно, 1,2,8-тиадиазоцин-1,1-диоксида (2) с выходом 23% взаимодействием пентаметилендиамина с сульфамидом в этаноле при комнатной температуре и перемешивании в течение 20 ч по схеме:
Известный способ не позволяет получать 2- и 4-(1,5,3-дитиазоцинан-3-ил)фенолы общей формулы (1).
Известен способ (U.Wellmar. Urea as Leaving Group in the Synthesis of 3-(tert-Butyl)perhydro-1,5,3-dithiazepine. J.Heterocyclic Chem., 1998, 35, p.1531) получения 3-(трет-бутил)пергидро-1,5,3-дитиазепина (3) с выходом 45% взаимодействием 5-(трет-бутил)-2-оксогексагидро-1,3,5-триазина с 1,2-этандитиолом в присутствии BF3·2HOAc при комнатной температуре за 2 ч по схеме:
Известным способом не могут быть получены 2- и 4-(1,5,3-дитиазоцинан-3-ил)фенолы общей формулы (1).
Таким образом, в литературе отсутствуют сведения о селективных способах получения 2- и 4-(1,5,3-дитиазоцинан-3-ил)фенолов общей формулы (1).
Предлагается новый способ получения 2- и 4-(1,5,3-дитиазоцинан-3-ил)фенолов общей формулы (1).
Сущность способа заключается в предварительном перемешивании формальдегида с 1,3-пропандитиолом при комнатной (~20°C) температуре в течение 30 мин с последующим добавлением о-, n-аминофенола в EtOH и катализатора Sm(NO3)3·6H2O, взятых в мольном соотношении формальдегид: 1,3-пропандитиол: о-, n-аминофенол: Sm(NO3)3·6H2O = 20:10:10:(0.3-0.7), предпочтительно 20:10:10:0.5. Смесь перемешивают 2.5-3.5 ч, предпочтительно 3 ч, при температуре ~20°C и атмосферном давлении в среде EtOH в качестве растворителя.
Выход 2- и 4-(1,5,3-Дитиазоцинан-3-ил)фенолов (1) составляет 60-72%.
Реакция протекает по схеме:
Целевые продукты (1) образуются только лишь с участием формальдегида, 1,3-пропандитиола и o-, n-аминофенолов, взятых в мольном соотношении 20:10:10 (стехиометрические количества). При другом соотношении исходных реагентов снижается селективность реакции. В присутствии других альдегидов (например, алкилзамещенные альдегиды), других дитиолов (например, 1,2-этандитиол, 1,4-бутандитиол) или других замещенных фенолов (например, алкилзамещенные фенолы) целевые продукты (1) не образуются. Без катализатора реакция идет с выходом, не превышающим 10%.
Проведение указанной реакции в присутствии катализатора Sm(NO3)3·6H2O больше 7 мол.% не приводит к существенному увеличению выхода целевого продукта (1). Использование катализатора Sm(NO3)3·6H2O менее 3 мол.% снижает выход (1), что связано, возможно, со снижением каталитически активных центров в реакционной массе. Реакции проводили при температуре 20°C. При температуре выше 20°C (например, 60°C) снижается селективность реакции и увеличиваются энергозатраты, а при температуре ниже 20°C (например, 0°C) снижается скорость реакции. Опыты проводили в среде EtOH, в котором хорошо растворяются исходные реагенты.
Существенные отличия предлагаемого способа:
В известном способе реакция идет с участием в качестве исходного реагента 5-(трет-бутил)-2-оксогексагидро-1,3,5-триазина в присутствии BF3·2HOAc с образованием 3-(трет-бутил)пергидро-1,5,3-дитиазепина (3). Известный способ не позволяет получать индивидуальные 2- и 4-(1,5,3-дитиазоцинан-3-ил)фенолы общей формулы (1).
В предлагаемом способе в качестве исходных реагентов применяются о-, n-аминофенолы, реакция идет под действием катализатора Sm(NO3)3·6H2O. В отличие от известных способов предлагаемый способ позволяет получать индивидуальные 2- и 4-(1,5,3-дитиазоцинан-3-ил)фенолы общей формулы (1).
Предлагаемый способ обладает следующими преимуществами:
Способ позволяет получать с высокой селективностью 2- и 4-(1,5,3-дитиазоцинан-3-ил)фенолы общей формулы (1) с использованием технологичных для практического применения исходных реагентов.
Способ поясняется примерами:
Пример 1. В сосуд Шленка, установленный на магнитной мешалке, в атмосфере аргона при температуре ~20°C помещают 20 ммолей водного раствора (37%) формальдегида и 10 ммолей 1,3-пропандитиола, перемешивают в течение 30 мин. Затем добавляют 10 ммолей n-аминофенола в 5 мл 95%-ного EtOH и 0.5 ммолей Sm(NO3)3·6H2O. Реакционную смесь перемешивают при температуре ~20°C в течение 3 ч. Из реакционной массы колоночной хроматографией на SiO2 выделяют 4-(1,5,3-дитиазоцинан-3-ил)фенол с выходом 68%. Другие примеры, подтверждающие способ, приведены в таблице.
| №№ п/п | Исходный аминофенол | Соотношение аминофенол: формальдегид: 1,3-пропандитиол: Sm(NO3)3·6H2O, ммоль | Время реакции, час | Выход (1), % |
| 1 | n-аминофенол | 10:20:10:0.5 | 3 | 68 |
| 2 | -//- | 10:20:10:0.7 | 3 | 72 |
| 3 | -//- | 10:20:10:0.3 | 3 | 60 |
| 4 | -//- | 10:20:10:0.5 | 3.5 | 70 |
| 5 | -//- | 10:20:10:0.5 | 2.5 | 63 |
| 6 | o-аминофенол | 10:20:10:0.5 | 3 | 61 |
Реакции проводили в среде EtOH в качестве растворителя при комнатной температуре (~20°C).
Спектральные характеристики 2-(1,5,3-дитиазоцинан-3-ил)фенола1:
(1Контроль реакции осуществляли методом ТСХ на пластинах Silufol W-254, проявляли парами I2. Для колоночной хроматографии использовали силикагель КСК (100-200 мкм). Одномерные спектры ЯМР (1Н, 13С), гомо- (COSY) и гетеро- (HSQC, НМВС) ядерные эксперименты ЯМР проводились на спектрометре Bruker Avance 400 (100.62 МГц для 13С и 400.13 МГц для 1H) по стандартным методикам фирмы Bruker, внутренний стандарт Me4Si, растворитель - CDCl3. Масс-спектры высокого разрешения получены на приборе MALDI TOF/TOF AUTOFLEX III фирмы Bruker.)
Элюент хлороформ:этилацетат:гексан (1:5:1), Rf 0.8. Спектр ЯМР 1H, δ, м.д.: 1.75 (м, 2Н, СН2 (7)); 2.57 (м, 4Н, СН2 (6,8)); 4.34 (м, 4Н, СН2 (2,4)); 6.42 (уш.с, 1H, OH (15)); 6.88 (т, J=6.2 Гц, 1Н, СН (11)); 6.96 (д, 1Н, J=6.4 Гц, CH (10)); 7.11 (д, J=64 Гц, 1H, CH (13)); 7.22 (т, J=8.8 Гц, 1H, CH (12)). Спектр ЯМР 13C, δ, м.д.: 29.43 (т, C-7), 30.78 (т, C-6, C-8), 55.93 (т, C-2, C-4), 115.07 (д, C-11), 120.37 (д, C-10), 125.25 (д, C-12), 127.43 (д, C-13), 135.40 (c, C-9), 151.39 (с, C-14). MALDI TOF, m/z: 242.362 [M+H]+. C11H15NOS2. M 241.374.
Спектральные характеристики 4-(1,5,3-дитиазоцинан-3-ил)фенола:
Элюент толуол:этилацетат:ацетон (4:1:1), Rf 0.85. Спектр ЯМР 1H, δ, м.д.: 1.80 (м, 2Н, СН2 (7)); 2.72 (т, J=5.8 Гц, 4Н, СН2 (6,8)); 4.50 (уш.с, 1Н, OH (15)); 4.76 (уш.с., 4Н, СН2 (2,4)); 6.83 (м, 4Н, СН (10, 11, 13, 14)). Спектр ЯМР 13С, δ, м.д.: 28.99 (т, С-6, С-8), 32.24 (т, C-7), 57.05 (т, C-2, C-4), 114.50 (д, C-10, C-14), 116.29 (д, C-11, C-13), 137.45 (с, С-9), 148.49 (с, C-12). MALDI TOF, m/z: 242.351 [M+H]+. C11H15NOS2. M 241.374.
Способ получения 2- и 4-(1,5,3-дитиазоцинан-3-ил)фенолов общей формулы (1): отличающийся тем, что формальдегид предварительно перемешивают с 1,3-пропандитиолом при комнатной (~20°С) температуре в течение 30 мин с последующим добавлением о-, п-аминофенола в EtOH в качестве растворителя в присутствии катализатора кристаллогидрата нитрата самария Sm(NO3)3·6H2O при мольном соотношении формальдегид:1,3-пропандитиол:о-, п-аминофенол: Sm(NO3)3·6H2O = 20:10:10:(0,3-0,7) в атмосфере аргона при комнатной (~20°С) температуре и атмосферном давлении в течение 2,5-3,5 ч.