Противоожоговый гель
Иллюстрации
Показать всеИзобретение относится к области фармацевтической промышленности, а именно к противоожоговому гелю. Противоожоговый гель для наружного применения, содержащий хитозан, салициловую кислоту, биорегулятор, выделенный из сыворотки крови крупного рогатого скота, представляющий собой фракцию кислых белков в интервале значений рН<3,0, и воду, взятые в определенном соотношении. Вышеописанный состав обладает выраженной заживляющей активностью. 7 ил., 9 пр.
Реферат
Изобретение относится к медицине и ветеринарии, а именно к эмульсионным лечебно-профилактическим средствам наружного применения при термических ожогах.
Актуальность разработки таких препаратов обусловлена тем, что в настоящее время частота термических поражений имеет тенденцию к росту, но при этом, несмотря на широкий спектр противоожоговых препаратов, не существует препаратов, которые бы смогли полностью восстановить структуру поврежденного участка кожи или другой ткани. По данным Всемирной организации здравоохранения, ожоги занимают третье место среди других травм. Во всем мире от ожогов ежедневно погибают около 60000 человек. Проблема борьбы с термическими поражениями крайне важна как для гражданской, так и для военно-полевой медицины. Развитие сложных промышленных производств, наличие на вооружении большинства армий зажигательных смесей, всевозрастающее количество природных катаклизмов и техногенных катастроф требует повышение эффективности терапии ожогов и ожоговой болезни при большей доступности и оперативности применения лекарственных препаратов.
Ожоги различной степени тяжести сопровождаются нарушением кислотно-щелочного равновесия и синтеза белков, совокупностью ферментных реакций распада сложных высокомолекулярных и биоорганических соединений, что приводит к некрозу тканей, экссудативным реакциям, образованию грануляционной ткани, бактериальной осемененности ожоговой поверхности.
В качестве противоожоговых препаратов в настоящее время используется большое количество лекарственных средств, среди которых особое место занимают препараты на основе неорганических и металлоорганических соединений, например следующие.
Известным противоожоговым препаратом является метилурацил, относящийся к классу пиримидинов и оказывающий влияние на восстановление разрушенных клеток и снижение воспалительных процессов. Для лечения применяется метилурациловая мазь на вазелино-ланолиновой основе [Патент РФ №2135180 (1999)]. Однако такая основа препятствует нормальному газообмену, что снижает ранозаживляюшую активность препарата, особенно при вялотекущих процессах, и может вызвать аллергическую реакцию.
Наиболее эффективными являются противоожоговые средства, имеющие эмульсионную или гелеобразную консистенцию, так как они легко наносятся и впитываются. Характер консистенции обеспечивается технологией получения лекарственного средства.
Наиболее близким по технической сущности к заявленному средству является средство для наружного применения "Полимед" [Патент РФ №2140264, кл. A61К 31/00 (1999)], которое выбрано нами в качестве прототипа.
Средство «Полимед» содержит фенол медицинский, резорцин, борную кислоту, дистиллированную воду, хитозан, диметилсульфоксид, йодистый калий, уксусную кислоту, глицерин и анестетик при следующем соотношении компонентов, мас.%:
| Хитозан | 3,0-3,1 |
| Фенол медицинский | 1,0-1,05 |
| Резорцин | 5,0-5,05 |
| Борная кислота | 1,0-1,05 |
| Диметилсульфоксид | 7,5-7,55 |
| Йодистый калий | 2,0-2,05 |
| Уксусная кислота ледяная | 4,8-5,0 |
| Глицерин | 3,0-3,5 |
| Анестетик | 0,5-10,0 |
| Дистиллированная вода | Остальное. |
При ожоговых поражениях препарат может использоваться как средство доврачебной помощи, так как на поверхности пораженной кожи образует пленку, служащую защитным покрытием. "Полимед" представляет собой устойчивый гель и может храниться при комнатной температуре в течение двух лет без потери фармакологической активности и физико-химических свойств.
К недостаткам прототипа следует отнести наличие в его составе токсических и канцерогенных веществ, таких как фенол, борная кислота, диметилсульфоксид, которые могут вызывать аллергические реакции со стороны организма при попадании на кожу, кроме этого некоторые компоненты средства обладают токсическим действием при попадании в кровь. Препарат недостаточно эффективен, поскольку он не содержит активного морфогенетического вещества.
Задача настоящего изобретения, заключается создание эффективного противоожогового средства для наружного применения, обладающего широким спектром противоожогового действия. В заявляемом препарате отсутствуют токсические компоненты, а присутствующий биорегулятор, выделенный из сыворотки крови крупного рогатого скота (КРС), стимулирует репаративные процессы, восстанавливая морфологически и биохимически нормальные структуры тканей. При этом данный биорегулятор добавляют в незначительном количестве, что сводит практически до нуля вероятность токсической или аллергической реакции на него со стороны организма.
Техническим результатом решения поставленной задачи является создание эффективного противоожогового средства, которое представляет собой гель для наружного применения, содержащий в качестве активных ингредиентов хитозан, салициловую кислоту и биорегулятор, выделенный из сыворотки крови крупного рогатого скота при следующем соотношении компонентов, (мас.%):
| Хитозан | 1,0-2,0 |
| Салициловая кислота | 0,3-0,4 |
| Биорегулятор | 10-9-10-11 |
| Вода | Остальное. |
Заявляемая композиция содержит следующие действующие компоненты:
Хитозан - катионный полимер, обычно получаемый из панцирей крабов, обладает бактериостатическими, ранозаживляющими и иммуностимулирующими свойствами, подавляет развитие фиброза, стимулирует макрофаги, способствует нормальному восстановлению кожного покрова. Образуя пленку на поверхности раны, он препятствует попаданию токсических компонентов, обладает хорошим осмотическим эффектом. Хитозан практически не токсичен для организма млекопитающих, его LD50 находится на уровне LD50 сахара и поваренной соли.
Салициловая кислота (о-оксибензойная кислота) - простейшая ароматическая оксикислота, представляющая собой бесцветные кристаллы, плохо растворимые в воде, хорошо растворимые в органических растворителях; широко распространена в природе, главным образом в виде гликозида ее метилового эфира (метилсалицилата). В промышленности ее обычно получают карбоксилированием фенола. Салициловая кислота обладает слабыми антисептическими, раздражающими и кератолитическими (в больших концентрациях) свойствами. Применяют наружно в мазях, пастах, присыпках и растворах при лечении кожных заболеваний; натриевую соль салициловой кислоты (салицилат натрия), ее амид (салициламид) и ацетилсалициловую кислоту (аспирин) используют как жаропонижающие, противоревматические, противовоспалительные и болеутоляющие средства; благодаря антисептическому действию ее употребляют при консервировании пищевых продуктов. Салициловая кислота токсична в больших дозах, для человека предполагаемая LD50 составляет 1.75 г/кг.
Биорегулятор выделяли из сыворотки крови крупного рогатого скота - стерильного, инактивированного коммерческого препарата, используемого в качестве добавки в ростовую среду клеточных культур, производства ФГУП «Предприятие по производству бактерийных и вирусных препаратов Института полиомиелита и вирусных энцефалитов им. М.П.Чумакова РАМН».
Выделение биорегулятора из сыворотки крови осуществляли путем высаливания в насыщенном растворе сернокислого аммония. Для этого к охлажденному раствору тканевого экстракта или сыворотки крови постепенно добавляли сухой сернокислый аммоний при постоянном перемешивании до образования насыщенного раствора соли (на 1000 мл раствора 780 г соли). Суспензию белков оставляли на 7 суток при температуре +4°С, после чего центрифугировали для осаждения примесных белков при 12000g в течение 30 минут с помощью центрифуги Т 32А Janetzki (Германия). Собирали фракцию супернатанта и осадка. Фракцию супернатанта диализовали против дистиллированной воды, а фракцию осадка - против физиологического раствора для удаления низкомолекулярных примесей и сульфата аммония в течение 14 дней. Присутствие в растворе ионов аммония определяли реакцией с реактивом Несслера. Полученные фракции супернатантов далее концентрировали, используя роторный вакуумный испаритель, при температуре +37°С. Фракции осадков хранили при температуре -70°С.
Изоэлектрофокусирование фракций супернатантов. Для проведения изоэлектрофокусирования (ИЭФ) приготавливали следующие растворы:
Тяжелый электродный раствор - 60% сахарозы, 1% H3PO4.
Легкий электродный раствор - 0,1% NaOH.
Тяжелый градиентный раствор - 75 г сахарозы, до 200 мл дистиллированной воды.
Легкий градиентный раствор - 15 г сахарозы, до 200 мл дистиллированной воды.
Фракции супернатантов сыворотки крови и экстракта костной ткани (общим объемом 100 мл каждая) разделяли с помощью метода ИЭФ в градиенте плотности сахарозы на колонке LKB-440 («LKB», Швеция), используя амфолины диапазона рН 3,5-10,0 (Serva, Германия) (Остерман, 1983). В колонку наслаивали растворы в следующем порядке: тяжелый электродный раствор, тяжелый и легкий градиентные растворы, которые подавали из градиентного смесителя, легкий электродный раствор. Исследуемую фракцию (не более 100 мг белка) в виде раствора вводили в тяжелый градиентный раствор. ИЭФ проводили при +4°С в течение 96 часов при напряжении 500-1500 В. Собирали фракции объемом 10 мл. Детекцию белков осуществляли на спектрофотометре Ultrospec 1100 pro (Biochrom Ltd., Великобритания) при 280 нм, для каждой фракции определяли значение рН с помощью рН-метра Oakton 2100 series (EUTECH Instruments, Сингапур). Согласно полученной картине разделения собирали фракцию кислых белков в интервале значений рН<3,0, которую далее длительно диализовали против дистиллированной воды и концентрировали. Данную фракцию далее разбавляли до соответствующей концентрации 10-8-10-10 мг белка/мл.
Существенным отличием заявляемого изобретения является то, что предлагаемое противоожоговое средство содержит биорегулятор, выделенный из сыворотки крови крупного рогатого скота (КРС) в низких концентрациях, который обладает выраженным репарирующим действием, что приводит к восстановлению морфологически и биохимически нормальной ткани кожи.
Для приготовления заявляемой гелевой композиции растворяют 10-20 г хитозана в 1 л воды в присутствии 3-4 г салициловой кислоты при 50°С. Раствор стерилизуют при 120°С в течение 5 мин, при этом образуется гель, который охлаждают и фильтруют, затем в полученный гель добавляют 10 мл водного раствора биорегулятора из сыворотки крови КРС в концентрации 10-8-10-10 мг/мл. Тщательно перемешивают в течение 15-30 мин, и получают готовый для использования гель. Указанные выше количества хитозана (от 10 до 20 г) выбраны потому, что при таком содержании хитозана образуется гель с определенным размером пор, через которые наиболее эффективно происходит высвобождение биорегулятора на раневую поверхность, что обеспечивает максимальную эффективность действия противоожогового средства.
При нанесении на ожоговую поверхность противоожогового геля тонким слоем образуется пленка, которая проницаема для воздуха, но при этом препятствует проникновению и размножению микроорганизмов на раневой поверхности за счет бактерицидного и бактериостатического действия салициловой кислоты и хитозана, соответственно. Кроме того, из образовавшейся пленки на раневую поверхность поступает вышеуказанный биорегулятор и оказывает регуляторное морфогенетическое действие, за счет этого достигается технический результат в виде эффективного противоожогового действия и восстановления повреждения. Было показано также, что существенно снижается болевой эффект немедленно после нанесения геля на ожоговую поверхность.
Изобретение иллюстрируется нижеследующими примерами получения и примерами конкретных составов заявляемого противоожогового геля, а также фигурами 1-7, демонстрирующими противоожоговое действие предлагаемых гелеобразных составов.
Краткое описание чертежей
Фиг.1. Заживление раны кожи крысы после ожога на 14 сутки: а) - контроль (рана не обрабатывалась); б) - обработка солкосерил-гелем; в) - обработка хитозановым гелем, не содержащим биорегулятор сыворотки крови; г) - обработка противоожоговым гелем, содержащим биорегулятор сыворотки крови. Цифрами обозначены: 1 - эпителий, 2 - дерма, 3 - волосяные фолликулы, 4 - струп, 5 - очаг воспаления.
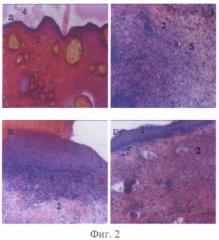
Фиг.2. Заживление раны кожи крысы после ожога на 25 сутки: а) - контроль (рана не обрабатывалась); б) - обработка солкосерил-гелем; в) - обработка хитозановым гелем, не содержащим биорегулятор сыворотки крови; г) - обработка противоожоговым гелем, содержащим биорегулятор сыворотки крови. Цифрами обозначены: 1 - эпителий, 2 - дерма, 3 - волосяные фолликулы, 4 - струп, 5 - очаг воспаления.
Фиг.3. Заживление раны кожи крысы после ожога и обработки противоожоговым гелем, содержащим биорегулятор сыворотки крови: а) - на 14 сутки; б) - на 25 сутки. Цифрами обозначены: 1 - эпителий, 2 - дерма, 3 - волосяные фолликулы, 4 - струп, 5 - очаг воспаления.
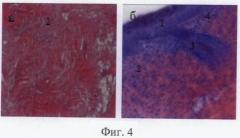
Фиг.4. Заживление раны кожи крысы после ожога и обработки противоожоговым гелем, содержащим биорегулятор сыворотки крови: а) - на 14 сутки; б) - на 25 сутки. Цифрами обозначены: 1 - эпителий, 2 - дерма, 3 - волосяные фолликулы, 4 - очаг воспаления.
Фиг.5. Состояние кожи крысы после ожога в контрольной группе (обработки раны не проводили): а, б - на 6 сутки; в - на 12 сутки; г, д - на 18 сутки.
а, в, г - макроскопическая картина; б, д - микроскопическая картина.
Фиг.6. Состояние кожи крысы после ожога в группе, где обработку раны проводили хитозановым гелем, не содержащим биорегулятор сыворотки крови: а, б - на 6 сутки; в, г - на 12 сутки; д - на 18 сутки.
а, в, д - макроскопическая картина; б, г - микроскопическая картина.
Фиг.7. Состояние кожи крысы после ожога в группе, где обработку раны проводили противоожоговым гелем, содержащим биорегулятор сыворотки крови: а, б - на 6 сутки; в, г - на 12 сутки; д, е - на 18 сутки.
а, в, д - макроскопическая картина; б, г, е - микроскопическая картина.
Пример 1.
Получение противоожогового геля.
Хитозан, салициловую кислоту и биорегулятор сыворотки крови (КРС) используют при следующем соотношении компонентов, (мас.%):
Хитозан - 1,0
Салициловая кислота - 0,3
Биорегулятор сыворотки крови крупного рогатого скота - 10-10
Вода - остальное (98,7).
Растворяют 10 г хитозана в 1 л воды в присутствии 3 г салициловой кислоты при 50°С. Раствор стерилизуют при 120°С в течение 5 мин, охлаждают, фильтруют и прибавляют 10 мл водного раствора биорегулятора из сыворотки крови КРС в концентрации 10-9 мг/мл.
Пример 2.
Хитозан, салициловую кислоту и биорегулятор сыворотки крови КРС используют при следующем соотношении компонентов, (мас.%):
Хитозан - 2,0
Салициловая кислота - 0,3
Биорегулятор сыворотки крови крупного рогатого скота - 10-11
Вода - остальное (97,7).
Растворяют 20 г хитозана в 1 л воды в присутствии и 3 г салициловой кислоты при 50°С. Раствор стерилизуют при 120°С в течение 5 мин, охлаждают, фильтруют и прибавляют 10 мл водного раствора биорегулятора из сыворотки крови КРС в концентрации 10-10 мг/мл.
Пример 3.
Хитозан, салициловую кислоту и биорегулятор из сыворотки крови КРС используют при следующем соотношении компонентов, (мас.%):
Хитозан - 1,0
Салициловая кислота - 0,4
Биорегулятор из сыворотки крови крупного рогатого скота - 10-9
Вода - остальное (98,6).
Растворяют 10 г хитозана в 1 л воды в присутствии 4 г салициловой кислоты при 50°С. Раствор стерилизуют при 120°С в течение 5 мин, охлаждают, фильтруют и добавляют 10 мл водного раствора биорегулятора из сыворотки крови КРС в концентрации 10-8 мг/мл.
Противоожоговое действие описываемой гелевой композиции было изучено на модели ожога кожи in vivo.
Исследование проводили на крысах (самцы F1 Cambell×Wistar) в течение 25 суток. Ожог вызывали на спине стеклянной пробиркой с кипящей водой (диаметр 2 см). Поврежденную поверхность кожи смазывали ежедневно:
1 группа - противоожоговый гель, содержащий биорегулятор из сыворотки крови КРС.
2 группа - препарат, содержащий хитозановый гель и все компоненты, кроме биорегулятора из сыворотки крови КРС.
3 группа - солкосерил-гель для глаз.
В контроле - ничем не смазывали.
Фрагменты кожи выделяли на 14-е и 25-е сутки, далее их фиксировали в растворе Буэна. Гистологические срезы толщиной 11 мкм окрашивали гематоксилином-эозином по стандартной методике.
В опытных и контрольной группах, после предварительного удаления шерсти на спинке, вызывали ожог кипятком. Получали термические поражения II-IIIA степени площадью около 4 см2. На следующий день крысам смазывали поверхность ожога соответствующим гелем, в контроле - ничем не смазывали.
Пример 4.
В качестве противоожогового геля использовали препарат, полученный по способу, аналогичному описанному в примере 1.
Состояние животных плохое, обожженная поверхность резко отечна. Кожа обожженной поверхности восковидная, горячая, гиперемирована, происходит выход экссудата. В контроле на следующие сутки отечность увеличивалась еще больше, появлялись изъязвления, заполненные некротическими массами. Во всех случаях в зоне раны отмечены признаки воспаления: расширение сосудов дермы под раневой поверхностью и ее клеточная инфильтрация, выраженные, однако не одинаково в различных группах. К концу 1-й недели у всех животных в контроле на поверхности ран формировался первичный струп, а в опыте гель застывал в виде плотной корки. На 12 день наблюдали в контроле влажную рану после ожога, которая плохо заживала. Картина заживления, после ожога под воздействием гелей проходила в случае без биорегулятора сыворотки крови незначительно. Наиболее благоприятную картину наблюдали в случае опыта в 1 и 3 группах. Лучшую картину наблюдали в случае противоожогового геля, содержащего биорегулятор сыворотки крови КРС. К 25 суткам ожоги почти у всех крыс зажили. На гистологических срезах наблюдали следующую картину заживления раны после ожога. В случае контроля на 14 сутки после ожога наблюдали практически полную реэпителизацию, струп прилегал неплотно к коже. Наблюдали незначительное воспаление в дерме и мышечном слое. Некроз волосяных фолликулов. В мышечном слое наблюдались полости между волокнами, образовавшиеся в результате воспаления. Под эпителием видны скопления нейтрофилов. Грануляционная ткань волокнисто-клеточная (Фиг.1а). К 25 суткам образовался соединительно-тканный рубец на месте ожога с незначительным присутствием нейтрофилов, наблюдали некроз волосяных фолликулов. Струп практически полностью отслоился (Фиг.2а).
В случае солкосерил-геля (3 группа) наблюдали на 14 сутки некроз волосяных фолликулов, практически полную реэпителизацию, струп прилегает к поверхности эпителия не плотно. В коже наблюдается сильное воспаление с инфильтрацией нейтрофилов сразу под эпителием, в мышечном слое наблюдаются полости между волокнами в результате воспаления. Грануляционная ткань больше клеточная, чем волокнистая (Фиг.1б).
На 25 сутки произошла полная реэпителизация с выраженным многоклеточным эпителием, практически полное отслоение струпа. В дерме наблюдается незначительное воспаление и гранулы гемосидерина. Образуется фиброзный рубец, коллагеновые волокна не рыхлые. Волосяных фолликулов в области повреждения не наблюдается (Фиг.2б).
В случае с хитозановым гелем, не содержащим биорегулятор сыворотки крови КРС (группа 2), наблюдали на 14 сутки практически на всей поверхности раны плотное прилегание струпа, реэпителизация была не полной, в области раны под эпителием наблюдали воспаление с инфильтрацией нейтрофилов. Формировалась рубцовая ткань. Также воспаление наблюдали и в прилежащем мышечном слое. Волосяных фолликулов в области раны не наблюдали. Грануляционная ткань была клеточно-волокнистая (Фиг.1в).
На 25 сутки наблюдали полную эпителизацию, но сильное воспаление осталось в дерме с инфильтрацией лейкоцитов. Происходит образование волокнистой рубцовой ткани. Струп отслоился не во всех местах и плотно прилегает в некоторых участках к эпителию (Фиг.2в). В случае применения противоожогового геля, содержащего биорегулятор сыворотки крови КРС (группа 1), на 14 сутки после ожога наблюдали практически полную реэпителизацию с хорошо развитым многослойным эпителием. Струп в некоторых местах отходит и прикреплен плотно лишь в месте неполной эпителизации. Эпителий, вновь образованный многослойный, хорошо развит, наблюдаются врастания тяжей в область дермы (предположительно формирование новых волосяных фолликулов). Воспаление в коже практически отсутствует, лишь незначительные участки инфильтрации нейтрофилов под эпителием. Мышечный слой хорошо развит и сохранен. Грануляционная ткань клеточно-волокнистая (Фиг.1г). На 25 сутки наблюдали практически полное отслоение струпа, полную эпителизацию. Незначительное воспаление в области дермы. Хорошо развита волокнистая и мышечная ткань. Видны скопления гемосидерина (Фиг.2г).
Пример 5.
В качестве противоожогового геля использовали препарат, полученный по способу, аналогичному описанному в примере 2. В случае применения противоожогового геля, содержащего биорегулятор сыворотки крови КРС (группа 1), на 14 сутки после ожога наблюдали практически полную реэпителизацию с хорошо развитым многослойным эпителием. Струп в некоторых местах отходит и прикреплен плотно лишь в месте неполной эпителизации. Эпителий, вновь образованный многослойный, хорошо развит, наблюдаются врастания тяжей в область дермы (предположительно формирование новых волосяных фолликулов). Воспаление в коже практически отсутствует, лишь незначительные участки инфильтрации нейтрофилов под эпителием. Мышечный слой хорошо развит и сохранен. Грануляционная ткань клеточно-волокнистая (Фиг.3а). На 25 сутки наблюдали практически полное отслоение струпа, полную эпителизацию. Незначительное воспаление в области дермы. Хорошо развита волокнистая и мышечная ткань. Видны скопления гемосидерина (Фиг.3б).
Пример 6.
В качестве противоожогового геля использовали препарат, полученный по способу, аналогичному описанному в примере 3.
В случае применения противоожогового геля, содержащего биорегулятор сыворотки крови КРС (группа 1), на 14 сутки после ожога наблюдали практически полную реэпителизацию с хорошо развитым многослойным эпителием. Эпителий, вновь образованный многослойный, хорошо развит, наблюдаются врастания тяжей в область дермы (предположительно формирование новых волосяных фолликулов). Воспаление в коже практически отсутствует, лишь незначительные участки инфильтрации нейтрофилов под эпителием. Мышечный слой хорошо развит и сохранен. Грануляционная ткань клеточно-волокнистая (Фиг.4а). На 25 сутки наблюдали практически полное отслоение струпа, полную эпителизацию. Незначительное воспаление в области дермы. Хорошо развита волокнистая и мышечная ткань. Видны скопления гемосидерина (Фиг.4б). По эффективности противоожогового действия изучаемый противоожоговый препарат, содержащий биорегулятор сыворотки крови КРС, превосходит примененные в качестве препарата сравнения Солкосерил-гель и действие препарата, не содержащего биорегулятор сыворотки крови КРС.
Кроме того, дополнительно было проведено исследование противоожоговой активности на модели, со значительно большей поверхностью повреждения.
Объектом исследования явились 3 группы лабораторных животных (белых крыс потомков семейства Вистар, массой 200-280 г, мужского пола), с забоем на 6, 12 и 18 сутки после ожога. Контрольная группа (1 группа) составила 5 животных, 2-3 группы составили по 15 животных, всего 35 животных.
Соответственно:
1 группа (контроль) 5 крыс - обработки раны не производилось,
2 группа 15 крыс - обработка препаратом, содержащим хитозановый гель и все компоненты кроме биорегулятора сыворотки крови КРС,
3 группа 15 крыс - обработка противоожоговым гелем, содержащим биорегулятор сыворотки крови КРС.
Всем животным наносилась стандартная ожоговая рана кожи и мягких тканей спины с предварительным удалением волосяного покрова. С использованием специального устройства достигался ожог II - III А степени общей площадью
10-12 см 2. В каждой группе моделировалась ожоговая травма на спинке крыс площадью 10% поверхности тела.
Во 2 и 3 группах в лечении ожоговой раны применялись гели, соответственно, не содержащий биорегулятор сыворотки крови КРС и содержащий последний в своем составе. Ожоговая рана оставалась открытой.
На 6-е, 12-е и 18-е сутки после нанесения ожога производился вывод животных из эксперимента (по 5 крыс из 2 и 3 групп и по 1-2 крысы из группы контроля) с одновременной визуальной оценкой раны (площадь, наличие грануляций, отека краев раны, степень эпителизации, наличие гнойных выделений) и забором материала из раны для гистологического исследования.
Из спины лабораторных животных вырезался плоскостной лоскут ткани площадью 15-17 см и немедленно фиксировался в 10-12% растворе нейтрального (забуференного) формальдегида. Ч/з 1-2 суток после фиксации проводилась «вырезка» стандартных кусочков ткани объемом 1 см3 из центра и периферических отделов раны. Кусочки проводились ч/з батарею спиртов и заливались в фиксатор «Гистомикс». Из залитых в гистомикс кусочков на санном микротоме МС-5 приготавливались гистологические срезы толщиной 7 мкм. Которые впоследствии окрашивались гематоксилином Эрлиха и пикрофуксиновой взвесью по методу Ван-Гизона. Гистологические срезы микроскопировались со стандартным и иммерсионным увеличением (объектив ×90). Выявленные гистологические изменения с помощью цифровой окулярной вставки регистрировались и заносились в память персонального компьютера (с возможностью последующей «распечатки»).
Пример 7. В качестве противоожогового геля использовали препарат, полученный, как описано в примере 1.
Морфологическое изучение влияния противоожогового геля, содержащего биорегулятор сыворотки крови КРС, на течение репаративных процессов при ожогах II-III А степени на 6, 12, 18 сутки по окончании эксперимента.
В 1-й контрольной группе выявлено:
На 6 сутки - отмечено формирование «четкого» темного серо-коричневого струпа, плотно спаянного с окружающими тканями. Под ними резко выраженные альтернативные изменения: некроз плоского эпителия, волосяных фолликулов, в ряде случаев окруженный зоной геморрагического пропитывания, резкий межуточный отек (Фиг.5а).
Выявлено начало формирования незрелой грануляционной ткани в краевых отделах плоскостной ожоговой раны. При этом в лимфо-плазмоклеточных инфильтратах определялись новообразованные сосуды, некротические фокусы выявлены в прилегающей к ране поперечнополосатой мускулатуре (Фиг.5б).
На 12 сутки - плотное прилегание струпа определялось не на всем протяжении ожоговой раны. Имелись единичные участки отторжения фибринозного струпа, фокусы образования одно- и многорядного эпителия в этих участках. Фокусы некроза заметно уменьшились в объеме (в плоском эпителии некроз отсутствовал вообще), единичные участки отмечены в поперечнополосатой мускулатуре. В инфильтратах заметно меньше определялось нейтрофильных лейкоцитов (гранулоцитов), плотность инфильтратов значительно уменьшилась (Фиг.5в).
На 18 сутки - отмечалось лишь «фрагментарное» прилегание струпа не на всем протяжении ожоговой раны. Имеющаяся под струпом грануляционная ткань приобретала характер волокнисто-клеточной. В ней все же имелись «целлюлярные» фокусы некроза и зоны геморрагической инфильтрации. Единичные участки некротических изменений отмечены и в поперечнополосатой мускулатуре. Краевые зоны раны содержали уже многорядный плоский эпителий (Фиг.5г, д).
Во 2 группе на 6 сутки макроскопически выявлено достаточно однородное, плотное прикрепление фибриново-лейкоцитарной пленки струпа к поверхности ожоговой раны (Фиг.6а). Гистологически определялся коагуляционный некроз как плоского эпителия, волосяных фолликулов, так и большой площади поперечнополосатой мускулатуры спины. В гистологических срезах определялась четкая демаркационная линия из лимфо-лейкоцитарных инфильтратов (Фиг.6б).
На 12 сутки после применения геля, не содержащего биорегулятор сыворотки крови КРС, в лечении ожоговой раны макроскопически струп был сохранен на значительных фрагментах плоскостной ожоговой раны.
Микроскопически определялись признаки выраженного некроза с воспалительной инфильтрацией межуточной ткани мышц. Густая воспалительная инфильтрация наблюдалась в области перимизия поверхностных слоях мышц (Фиг.6в, г).
На 18 сутки в ожоговой ране после применения геля, не содержащего биорегулятор сыворотки крови КРС, макроскопически выявлено, что струп сохраняется лишь на отдельных фрагментах плоскостной раны. Цвет струпа - темно-коричнево-серый.
Микроскопически определено, что плоский эпителий не полностью покрывает ожоговый дефект. «Наметившаяся» эпителизация слаба - лишь в краевых отделах ожоговой раны имеются одно-двурядные полоски плоского эпителия, под которым и в центральных отделах раны отмечено разрастание незрелой грануляционной ткани клеточно-волокнистого строения. В последней отмечены «целлюлярные» фокусы некроза, масса нейтрофилов и многочисленные макрофагальные клеточные элементы. Отмечены и признаки очагового миолиза (Фиг.6д).
В 3-й группе (с применением противоожогового геля, содержащего биорегулятор сыворотки крови КРС) на 6 сутки макроскопически отмечено плотное прилегание корки струпа к ожоговой раневой поверхности, струп был сохранен почти на всей площади ожоговой раны. Однако появлялись единичные «фестончатые» окна в корке струпа (Фиг.7а). Микроскопически определялись фокусы некроза поверхностных слоев плоского эпителия, мышечных волокон, единичных волосяных фолликулов. Отмечался также отек и разволокнение коллагеновых волокон в глубоких слоях дермы. Имелись признаки напряженности иммунитета - густые внутриэпителиальные инфильтраты (Фиг.7б).
На 12 сутки макроскопическая картина изменений заключалась в мозаичном плотном «прилегании» струпа с наличием «неполных» окон в фибриново-лейкоцитарной корке (Фиг.7в).
Гистологически выявлены мозаичные очаги некроза под пленкой струпа как в фиброзной основе дермы, волосяных фолликулов, так и в поверхностных слоях поперечнополосатой мышце (Фиг.7г). На 18 сутки в ожоговой ране после применения геля, содержащего биорегулятор сыворотки крови КРС, макроскопически отмечена множественная «фрагментация» в прилегании струпа к ожоговой поверхности. Очень многочисленны фестончатые окна (Фиг.7д).
Микроскопически некроза поверхностных и глубоких мышечных волокон нет. Отмечена эпителизация дефектов дермы и мышечной ткани за счет кератоакантотических тяжей плоского эпителия. Под слоем фибриново-лейкоцитарной пленки четко сформированная полоска (двух- трехрядного) плоского эпителия (Фиг.7е).
Т.е. можно сделать заключение, что в эти сроки происходит законченная и полная эпителизация плоскостной ожоговой раны, что показывает на преимущества геля, содержащего биорегулятор сыворотки крови КРС в ее лечении.
Пример 8.
В качестве противоожогового геля использовали препарат, полученный по способу аналогичному в примере 2.
В 3-й группе (с применением противоожогового геля, содержащего биорегулятор сыворотки крови КРС) на 6 сутки макроскопически отмечено плотное прилегание корки струпа к ожоговой раневой поверхности, струп был сохранен почти на всей площади ожоговой раны.
Микроскопически определялись фокусы некроза поверхностных слоев плоского эпителия, мышечных волокон, единичных волосяных фолликулов. Отмечался также отек коллагеновых волокон в глубоких слоях дермы. Имелись густые внутриэпителиальные инфильтраты.
На 12 сутки макроскопическая картина изменений заключалась в мозаичном плотном «прилегании» струпа.
Гистологически выявлены мозаичные очаги некроза под пленкой струпа как в фиброзной основе дермы, волосяных фолликулов, так и в поверхностных слоях поперечнополосатой мышце.
На 18 сутки в ожоговой ране после применения геля, содержащего биорегулятор сыворотки крови КРС, макроскопически отмечена множественная «фрагментация» в прилегании струпа к ожоговой поверхности.
Микроскопически некроза поверхностных и глубоких мышечных волокон нет. Отмечена эпителизация дефектов дермы и мышечной ткани за счет кератоакантотических тяжей плоского эпителия. Под слоем фибриново-лейкоцитарной пленки четко сформированная полоска (двух- трехрядного) плоского эпителия.
Т.е. можно сделать заключение, что в эти сроки происходит законченная и полная эпителизация плоскостной ожоговой раны, что показывает на преимущества геля, содержащего биорегулятор сыворотки крови КРС, в ее лечении.
Пример 9.
В качестве противоожогового геля использовали препарат, полученный по способу аналогичному в примере 3.
В 3-й группе (с применением противоожогового геля, содержащего биорегулятор сыворотки крови КРС) на 6 сутки макроскопически струп был сохранен почти на всей площади ожоговой раны. Однако появлялись единичные «фестончатые» окна в корке струпа.
Микроскопически определялись фокусы некроза плоского эпителия, мышечных волокон, волосяных фолликулов. Отмечалось также разволокнение коллагеновых волокон в глубоких слоях дермы.
На 12 сутки макроскопическая картина изменений заключалась в наличии «неполных» окон в фибриново-лейкоцитарной корке.
Гистологически выявлены очаги некроза как в дерме, волосяных фолликулах, так и в поверхностных слоях поперечнополосатой мышцы.
На 18 сутки в ожоговой ране после применения геля, содержащего биорегулятор сыворотки крови КРС макроскопически отмечена множественная «фрагментация» в прилегании струпа к ожоговой поверхности. Очень многочисленны фестончатые окна.
Микроскопически некроза поверхностных и глубоких мышечных волокон нет. Отмечена эпителизация дефектов дермы и мышечной ткани за счет кератоакантотических тяжей плоского эпителия. Под слоем фибриново-лейкоцитарной пленки четко сформированная полоска (двух- трехрядного) плоского эпителия.
Т.е. можно сделать заключение, что в эти сроки происходит законченная и полная эпителизация плоскостной ожоговой раны, что показывает на преимущества геля, содержащего биорегулятор сыворотки крови КРС, в ее лечении.
В результате проведенных исследований установлено, что заявляемая гелевая композиция обладает выраженным противоожоговым действием. На 12-е и особенно на 18-е сутки происходит законченная и полная эпителизация плоскостной ожоговой раны, полное созревание грануляционной ткани, отсутствие некротических изменений поперечнополосатой мускулатуры.
Противоожоговый гель для наружного применения, содержащий хитозан, отличающийся тем, что в качестве активных ингредиентов дополнительно содержит салициловую кислоту, биорегулятор, выделенный из сыворотки крови крупного рогатого скота, представляющий собой фракцию кислых белков в интервале значений рН<3,0, и воду при следующем соотношении компонентов, мас.%:
| Хитозан | 1,0-2,0 |
| Салициловая кислота | 0,3-0,4 |
| Биорегулятор | 10-9-10-11 |
| Вода | Остальное |